염료 감질 태양 전지
Overview
출처: 타마라 M. 파워스, 텍사스 A&M 대학교 화학학과
오늘날의 현대 세계는 많은 양의 에너지를 사용해야 합니다. 석탄과 석유와 같은 화석 연료의 에너지를 활용하지만, 이러한 원천은 재생 불가능한 공급이므로 공급이 제한됩니다. 글로벌 라이프스타일을 유지하기 위해 재생 가능한 에너지원에서 에너지를 추출해야 합니다. 가장 유망한 재생 가능 원천은 태양으로, 지구에 여러 번 연료를 공급하기에 충분한 태양 에너지를 제공합니다.
그렇다면 태양으로부터 에너지를 어떻게 추출할까요? 자연은 그것을 알아 낸 첫번째이었다: 광합성은 식물이 탄수화물과 산소로 물과 이산화탄소를 변환하는 과정입니다. 이 과정은 식물의 잎에서 발생하고 잎을 녹색으로 착색엽소 안료에 의존합니다. 햇빛으로부터 에너지를 흡수하는 것은 이 착색분자이며, 화학 반응을 유도하는 흡수에너지입니다.
1839년, 아버지의 실험실에서 실험하던 19세의 프랑스 물리학자 에드먼드 베케렐(Edmond Becquerel)이 최초의 태양광 세포를 만들었습니다. 그는 전압과 전류를 생성 백금 전극에 연결된 은 염화물의 산성 용액을 조명했다. 1 20세기 후반과 상반기에 많은 발견과 발전이 이루어졌으며, 1954년에만 벨 연구소에 의해 최초의 실용적인 태양전지가 지어졌습니다. 1950년대부터 태양전지는 우주에서 위성에 전력을 공급하는 데 사용되었습니다. 2
태양 전지는 전류를 만들기 위해 빛을 활용하는 전기 장치입니다. 이 비디오는 이러한 유형의 셀, 염료 민감성 태양 전지(DSSC)의 준비 및 테스트를 보여줍니다. 브라이언 오레건과 마이클 그레첼이 UC 버클리에서 처음 발명한 그레첼은 스위스의 에콜 폴리테크닉대학 페데랄 드 로잔에서 이 작품을 추구했으며, 1991년 최초의 고효율 DSSC에 절정을 이루었습니다. 3 식물과 같은 이 태양전지는 염료를 사용하여 태양으로부터 에너지를 활용합니다.
Procedure
1. TiO2 페이스트 준비
- 콜로이드 TiO2 분말 6 g을 질량으로 하여 박격포에 놓습니다.
- TiO2에2-3 mL의 식초를 조심스럽게 추가하고 균일 한 페이스트를 얻을 때까지 유봉으로 서스펜션을 연마하기 시작합니다. 연삭은 분말의 응집된 덩어리를 분해하는 역할을 합니다.
- 식초를 계속 첨가하고, ~ 1mL 단위로 연삭하면서 최대 ~ 9mL의 총 부피를 추가하십시오. 각 첨가하기 전에, 페이스트의 일관성은 균일하고 덩어리가 없어야합니다. 마지막 페이스트는 두껍지만 너무 두껍지 않아 서 드롭퍼 병에서 압착할 수 없습니다.
- 증류수 1mL에 접시 비누 1방울을 넣고 부드럽게 섞습니다.
- TiO2 서스펜션에 접시 비누 용액을 넣고 부드럽게 섞어 거품을 일으키지 않도록 주의하십시오.
- 서스펜션을 15분 동안 평형화할 수 있도록 허용합니다. 접시 비누는 계면 활
Results
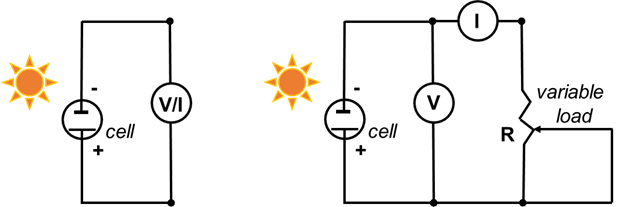
6.5.3-6.5.4 단계로 수집된 각 데이터 포인트에 대해 전류 밀도(mA/cm2)및 전력 밀도(mW/cm2)를계산합니다. 전류 밀도를 계산하려면 2.7단계에서 결정된 필름의 표면적으로 전류를 분할합니다. 전력 밀도를 계산하려면 전압을 전류 밀도별로 곱합니다. 6.3, 6.4 및 6.5.3-6.5.4 단계에서 수집된 데이터에 대해 전류(mA) 대 전압(mV)을 플롯합니다. 모든 데이터에 대해 현재 ?...
Application and Summary
References
- Williams, R. Becquerel Photovoltaic Effect in Binary Compounds. J Chem Phys, 32 (5), 1505-1514 (1960).
- Perlin (2005), Late 1950s - Saved by the Space Race", Solar Evolution - The history of Solar Energy. The Rahus Institute. Retrieved 28 June 2016.
- Regan, B., Gratzel, M. Nature, 353, 737-740 (1991).
- Miessler, G. L., Fischer, P. J., Tarr, D. A. Inorganic Chemistry, Pearson, 2014.
- Wikipedia page: Dye-sensitized solar cell,
- Smestad, G. P., Grätzel, M. Demonstrating Electron Transfer and Nanotechnology: A Natural Dye-Sensitized Nanocrystalline Energy Converter. J Chem Ed. 75 (6), 752 (1998).
- Burschka, J., Pellet, N., Moon, S.-J., Humphry-Baker, R., Nazeeruddin, M. K., Grätzel, M. Sequential deposition as a route to high-performance perovskite-sensitized solar cells. Nature, 499 (7458), 316-9 (2013).
Tags
건너뛰기...
이 컬렉션의 비디오:

Now Playing
염료 감질 태양 전지
Inorganic Chemistry
15.8K Views

슐렌크 라인 기술을 이용한 티(III) 메탈로센의 합성
Inorganic Chemistry
31.6K Views

글러브박스 및 불순물 센서
Inorganic Chemistry
18.6K Views

승화에 의한 페로센정화
Inorganic Chemistry
54.7K Views

에반스 방법
Inorganic Chemistry
68.7K Views

단일 결정 및 분말 X선 회절
Inorganic Chemistry
104.8K Views

전자 파라마그네틱 공명 (EPR) 분광법
Inorganic Chemistry
25.6K Views

뫼스바우어 분광법
Inorganic Chemistry
22.0K Views

루이스 산-베이스 상호 작용 Ph3P-BH3
Inorganic Chemistry
39.0K Views

페로센의 구조
Inorganic Chemistry
79.6K Views

IR 분광기에 그룹 이론의 적용
Inorganic Chemistry
45.6K Views

분자 궤도 (MO) 이론
Inorganic Chemistry
35.4K Views

네 배 금속 - 금속 본딩 패들 휠
Inorganic Chemistry
15.3K Views

산소 운반 코발트 (II) 복합체의 합성
Inorganic Chemistry
51.7K Views

급진적 중합 반응의 광화학 개시
Inorganic Chemistry
16.8K Views
Copyright © 2025 MyJoVE Corporation. 판권 소유