Method Article
Um modelo experimental para estudar a Tuberculose-Malária Coinfection sobre Transmissão Natural de Mycobacterium tuberculosis E Plasmodium berghei
Neste Artigo
Resumo
Tuberculose e malária são duas das infecções mais prevalentes em seres humanos e as principais causas de morbidade e mortalidade em populações empobrecidas nos trópicos. Nós estabelecemos um sistema de modelo experimental para estudar resultado de malária tuberculose co-infecção em camundongos após o desafio com ambos os patógenos através de sua rota natural de infecção.
Resumo
Co-infecções ocorrem naturalmente devido à sobreposição geográfica dos diferentes tipos de organismos patogênicos. Infecções simultâneas provavelmente modulam a respectiva resposta imune a cada único patógeno e afectar, assim, patogênese e evolução da doença. Pacientes co-infectados também podem responder diferencialmente a intervenções anti-infecciosos. A co-infecção entre a tuberculose como causada por micobactérias e do parasita da malária Plasmodium, sendo que ambos são coendemic em muitas partes da África Subsaariana, não foi estudada em detalhe. A fim de abordar o desafio, mas cientificamente e clinicamente questão de grande relevância como a imunidade do hospedeiro malária tuberculose coinfecção modular eo curso de cada doença, estabelecemos um modelo experimental do rato, que nos permite dissecar as respostas imunes desencadeados para ambos os patógenos no hospedeiro co-infectados . De notar que, a fim de a maioria das infecções humanas naturalmente adquiridos precisamente imitar, realizamos experimentalinfecções de camundongos com ambos os patógenos por suas rotas naturais de infecção, ou seja, aerosol e picada de mosquito, respectivamente.
Introdução
As populações humanas são raramente exposta a apenas um agente patogénico. Especialmente em regiões com alta incidência de infecções, como a África sub-saariana, co-infecções representam um problema de saúde pública principal, mas altamente subestimada. A tuberculose ea malária são as infecções bacterianas e parasitárias mais prevalentes em seres humanos, respectivamente, e continuam a ser as principais causas de morbidade e mortalidade em populações empobrecidas nos trópicos. Apesar da grande sobreposição geográfica entre a tuberculose ea malária e ao grande número de indivíduos em risco de co-infecção, muito pouco se sabe sobre as interações entre as diversas e, muitas vezes contrariando os reguladores do sistema imunológico e efetores desencadeados simultaneamente contra os parasitas da malária e bacilo da tuberculose em indivíduos co-infectados.
Modelos de roedores de infecções mistas permitem caracterizar reações imunes diferenciais contra patógenos diferentes em um host, lançando assim a luz na influência mútuaências modulando patologia e evolução clínica da doença individual, o que também ajudará a identificar novas recomendações para tratamento e prevenção. Nós estabelecemos um modelo experimental do rato que nos permite investigar as ramificações causadas pela infecção concomitante com Mycobacterium tuberculosis (MTB) e as espécies de Plasmodium roedor dentro do mesmo host 1. É importante ressaltar que para emular infecções humanas naturalmente adquiridos, tanto quanto possível, o nosso modelo implementa as rotas naturais de infecção utilizadas por ambos os patógenos. A tuberculose é uma infecção no ar, o que, por conseguinte, se manifesta principalmente nos pulmões. O agente causal, Mtb é transmitida por pessoas com doença ativa por via aerossol quando expelir gotículas de aerossóis infecciosos durante tossir ou espirrar. Assim, a infecção por aerossol é o método de escolha para imitar a infecção natural. Geração de partículas transportadas pelo ar que contêm M. tuberculosis pode ser alcançada através da utilizaçãode um sistema de exposição por inalação. Esta câmara de exposição do corpo inteiro permite expor animais experimentais para Mtb contendo gotículas de aerossóis infecciosos (Figura 1), que se inalada para os alvéolos dos pulmões onde a infecção é iniciada 2.
A malária, por outro lado é uma doença transmitida por vetor causada pelo protozoário, apicomplexan parasita Plasmodium, que é transmitido naturalmente pela picada de um mosquito Anofelíneos feminino. Durante a farinha de sangue, esporozoitos infecciosos são depositados sob a pele de acolhimento e subsequentemente atingir o fígado através da corrente sanguínea. Dentro de hepatócitos eles desenvolvem e se multiplicam rapidamente em esquizontes fígado em estágio. Eventualmente, esquizontes maduros rompem e libertam milhares de patogénicos merozóitos de primeira geração para a corrente sanguínea, onde eles iniciam um ciclo progressivo de invasão de glóbulos vermelhos, a replicação, a ruptura dos glóbulos vermelhos, e re-invasão 3. O ciclo de vida do Plasmodium continues como alguns merozoites evoluir para os estágios parasitários sexuais, os gametócitos masculinos e femininos, que podem ser ocupados por mosquitos durante as refeições de sangue. No mosquito, esporozoítos do Plasmodium desenvolver dentro de oocistos que residem no intestino médio do mosquito e, eventualmente, migram para as glândulas salivares para transmissão posterior em outro 3,4 host.
Enquanto em modelos animais experimentais da entrega de M. tuberculosis através do aerossol e rota assim mais relevante é muito comum, muitos estudos experimentais de infecção por Plasmodium de roedor, incluindo estudos sobre a malária-tuberculose coinfecção 5-7 foram efectuados através da infecção de ratinhos com eritrócitos parasitados, dando origem à infecção da malária do sangue em estágio, excluindo a fase de fígado em estágio clinicamente silenciosa. No entanto, a fase de fígado é um passo obrigatório durante a infecção e relevantes para a imunidade anti-plasmódio 8-11. Consideramos, portanto, importante para incluir o ph hepáticaase de transmissão e manutenção em estudos de ambos malária e malária tuberculose co-infecção, respectivamente malária. Além disso, tem sido demonstrado que os esporozoítos naturalmente transmissíveis são mais infeccioso do que os que foram transmitidos via infecções agulha 12, o que nos levou a estabelecer a infecção da malária pelo mosquito morder em vez de injetar isolado salivar das glândulas esporozoítos derivados. A única maneira de obter os mosquitos infecciosos para a transmissão natural de parasitas da malária é manter todo o ciclo de vida do parasita, tanto no hospedeiro vertebrado (aqui mouse) eo vetor mosquito. Assim, o acesso a um insetário para a manutenção do parasita é inevitável, a fim de realizar a transmissão natural, através da mordida.
Nosso protocolo aqui descrito foi desenvolvido para investigar como a co-infecção com Plasmodium esporozoítos impactos sobre a tuberculose crônica 1. Para fazê-lo, os ratinhos são infectados com M. aerossol tuberculose e 40 dias mais tarde, quando M. infecção por tuberculose atingiu a fase crônica, os ratos são expostos a mosquitos transmissores da malária infecciosa. O resultado de tanto da malária e da tuberculose nos animais co-infectados pode ser seguida monitorizando a parasitemia sanguínea e a carga bacteriana no tecido, respectivamente. Em nosso protocolo, vamos descrever em detalhes como para infectar ratos com ambos os patógenos através de sua rota de infecção natural e como confirmar transmissão de patógenos de sucesso. Em nossas mãos, a taxa de infecção comumente alcançada por ambas as infecções experimentais é 100%. Estes protocolos podem ser aplicados para estudar ambas as infecções separadamente ou, como fazemos, para modelar e estudar a co-infecção entre duas das doenças infecciosas humanas mais difíceis. Este modelo é aplicável a outras espécies de Mycobacterium e de roedores Plasmodium além dos descritos neste protocolo.
Protocolo
Medidas de segurança e Declaração de Ética
Os estudos aqui apresentados envolvem trabalho com o patógeno humano Mtb eo parasita de roedores malária Plasmodium berghei (P. berghei). Experimentos com Mtb (H37Rv) e P. berghei deve ser realizado sob as condições de biossegurança adequadas. Nível de Biossegurança (BSL) 2 laboratórios são necessários para os parasitas da malária de roedores, tais como P. berghei e BSL 3 para Mtb e, portanto, para todos os estudos co-infecção aqui descrito. NOTA: Ratos infectados com Mtb não espalhar a infecção para outros ratos dentro imediações (a nossa própria observação). Espalhe para o experimentador pode, portanto, ser excluído, roupas de proteção, porém, adequado tem que ser usado dentro do laboratório BSL 3 em todos os momentos. De acordo com nossas regras, os pesquisadores usam aventais cirúrgicos, redes de cabelo, respiradores descartáveis, e dois pares de luvas, dos quais o exterior é descartado sempre que umrms são retirados do gabinete. Os novos são colocados em antes de entrar no gabinete novamente. Dois recipientes, um com 2% Buraton (NOTA: outros desinfectantes aprovados para inativar Mtb podem ser usados na concentração aprovado) para o material de resíduos líquidos e infecciosa e uma para a descontaminação de superfícies, são preparados antes do experimento e colocado dentro do armário. Além disso, os sacos de plástico será utilizada para os resíduos sólidos não infecciosa. De acordo com a legislação alemã, todo o trabalho que envolve a manipulação e processamento de culturas Mtb ou tecidos derivados de Mtb camundongos infectados devem ser realizadas em uma cabine de segurança biológica de classe 2, dentro de um laboratório BSL3. Durante o manuseio de micobactérias, medidas têm que ser tomadas para evitar a geração de aerossóis em todos os momentos.
Fêmea C57BL / 6 (Charles River) com idades entre 6-8 semanas foram utilizados para todas as experiências de co-infecção e mantidas sob condições de barreira específicas em instalações BSL 3. Cuidados com os animais e experimentação foram performed de acordo com os protocolos aprovados pelo Comitê de Ética em Experimentação Animal do Ministério da Agricultura, Meio Ambiente e Meio Rural do Estado de Schleswig-Holstein
Para a obtenção de estágios do mosquito da malária, os camundongos NMRI foram adquiridos da Charles River Laboratory, Sulzfeld, Alemanha e mantidos em condições livres de patógenos específicos dentro do biotério da Universidade de Heidelberg (IBF). Todos os experimentos com animais foram realizados de acordo com os regulamentos europeus e aprovado pelas autoridades estaduais de Baden-Württemberg (Regierungspräsidium Karlsruhe).
1. Aerosol infecção de camundongos com Mtb usando um aerossol Câmara Glas-Col
A melhor maneira de padronizar infecção aerossol de animais experimentais com Mtb é usar micobactérias de estoques congelados com títulos UFC conhecidos. Para preparar culturas de cultura em caldo Middlebrook Mtb 7H9 suplementado com OADC (oleicoácido, Albumina, dextrose, catalase) enriquecimento médio e 0,05% Tween 80, uma fonte de carbono para micobactérias e medir a fim de evitar a aglutinação bacteriana, ao mesmo tempo. As culturas devem ter um ≤ OD 1 na altura da colheita. Na maior OD, aumenta aglomeração bacterianas e diminuições de viabilidade. Armazenar aliquotas de 1 mL a -80 ° C. Determinar o número de unidades formadoras de colônia viável (UFC) nos estoques congelados por chapeamento de uma série de diluições de 10 vezes de três frascos independentes sobre 7H11 placas de ágar, suplementado com 0,5% de glicerol, 1 g / L de asparagina, e OADC e enumerar colônias após 4 semana de incubação a 37 ° C. Realizar infecção por aerossol, tal como descrito abaixo.
- Estoques Thaw de BTT de título conhecido UFC e cuidadosamente misturar a suspensão de cinco vezes para dispersar aglomerados de bactérias usando uma seringa de 1 ml equipado com uma agulha G 27. Evitar a produção de aerossóis.
- Dependendo da dose de infecção desejada, transferir o volume necessário de estoque em micobactériasum tubo de 50 ml contendo PBS esterilizado. O volume final é de 6 ml. NOTA: Através da variação do número de microrganismos em suspensão, a percentagem de bactérias rolamento gotículas de aerossol é variada. Nós geralmente visam uma absorção de 100 bacilos viáveis por pulmão (infecção de baixa dose). Na nossa experiência, este requer cerca de 1-2 x 10 6 / ml de M. tuberculosis em um volume total de 6 ml de 5,5 ml que são nebulizadas (ver abaixo). Recomenda-se a fazer uma série de desafios em aerossol experimentais com diferentes concentrações de bactérias para encontrar as condições ideais para a sua infecção. Considerando que as infecções com altas doses de até 5.000 micobactérias pode ser feito para acelerar o processo infeccioso, tão poucos como cinco bactérias pode ser utilizado com êxito para infectar ratos por aerossol. A taxa de infecção é geralmente 100%.
- Retirar um volume suficiente (preparado em excesso de volume final obrigatório) para chapeamento para determinar o título de inóculo; normalmente remover 500 mL de placa triplicatas técnicas.
- Colocar animais emuma cesta compartimentado malha (um rato por cesta) dentro da câmara de aerossol circular e feche a tampa da câmara de aerossol. NOTA: Outros modelos estão equipados com uma cesta em forma de torta composta por cinco compartimentos individuais, cada uma com capacidade de 20 ratos.
- Fixe a unidade Venturi-nebulizador para as três articulações soquete de aço inoxidável.
- Retirar a suspensão de micobactérias a partir do tubo de 50 mL com uma seringa de 10 ml, equipado com uma agulha romba de 18 G, e transportar a seringa para a câmara de aerossol numa caixa de transporte fechado.
- Retire a tampa de rosca da unidade nebulizador e cuidadosamente injetar a suspensão micobactérias no nebulizador. Evite a geração de aerossóis. Descarte a seringa em um recipiente apropriado contendo 2% Buraton. Selar o nebulizador com a tampa de rosca.
- Ligue o interruptor de alimentação principal e da lâmpada UV. O visor do teclado de controle mostra "Glas-Col Aparelho Co".
- Ligue o interruptor de programa por diante. A vontade de exibiçãomostrar "é o nebulizador está pronto?" "É o cesto carregado?" Pressione Enter quando estiver pronto ". Pressione Enter.
- O visor mostra "Enter Pré-aqueça o Tempo 900", o que significa que o tempo de pré-aquecimento para o incinerador (que descontamina o ar escape) é de 900 segundos. Pressione Enter.
- O display mostrará "Enter tempo Nebulizing 1800", o que significa que o tempo de nebulização está definido para 1.800 sec como padrão. A fim de estender o tempo de nebulização, digite "2400" e pressione enter. NOTA: Durante o ciclo de nebulização, ar sob pressão atomiza a suspensão, gerando pequenas gotículas de aerossol contendo micobactérias. Com o fluxo de ar principal, estas gotículas (cerca de 2-5 mM de tamanho) são transportadas para a câmara de aerossol.
- O display irá mostrar "Enter Time CD 1800", o que significa que o ciclo de decadência leva 1.800 sec. Ajuste para "2400" e pressione enter. NOTA: Durante este ciclo, a nuvem que foi construído up na câmara de aerossol durante o ciclo de nebulização pode decair. As pequenas gotículas são inaladas pelos animais experimentais.
- O display irá mostrar "Enter Time dezembro 900", o que significa que o ciclo de luz UV descontaminação terá 900 segundos. Pressione Enter. A máquina começará a andar de bicicleta através de pré-aquecimento, nebulização, decadência nuvem e descontaminação UV.
CUIDADO: O medidor de fluxo de vácuo deve indicar 60 pés cúbicos / hora (verifique quando o ciclo de pré-aquecimento começa, ajuste a válvula de controle de vácuo, se necessário) eo medidor de fluxo de ar comprimido de 10 metros cúbicos / hora (verificar na nebulização começa ciclo; ajuste a válvula de controle de ar de acordo ). - Quando o ciclo está completo, o teclado irá mostrar "Processo concluído - Retire Specimen". Desligue o programa, UV e interruptor principal.
- Verificar se a suspensão de micobactérias foi nebulizada completamente e se não, registrar o volume restante, removendo cuidadosamente a suspensão com uma seringa apropriada equipada comuma agulha romba 18 G. O volume restante não deve ser superior a 1 ml.
- Remover o nebulizador das articulações e colocá-lo em uma panela contendo 2% Buraton durante um mínimo de 2 horas, geralmente de desinfecção é feito S / N. Em seguida, transferir o nebulizador para uma nova panela e enxaguar bem com água. Deixe nebulizador para ar seco.
- Abrir a câmara de aerossol e devolver os animais para as suas gaiolas. Saco dos cestos em sacos de autoclave e manter. Limpe as superfícies do interior da câmara de aerossol com 2% Buraton NOTA:. Por razões de segurança, um respirador purificador de ar motorizado deve ser usado durante este procedimento.
- Usando os restantes 500 ul da suspensão de micobactérias (ver passo 1.3) da placa de diluições de 10 vezes de uma técnica triplicado (3 x 100 ul) em placas de ágar 7H11.
2. Verifique Captação de UFC desejado em Pulmões
Um dia após infecção por aerossol de animais experimentais determinar o lo bacterianaanúncio nos pulmões de animais de controle designados, a fim de verificar a absorção do UFC desejado. NOTA: Nós geralmente designa um grupo extra de 3-5 camundongos para o dia 1 determinação UFC.
Para monitorizar o curso da infecção por M. tuberculosis ao longo do tempo, o peso do tecido de micobactérias podem ser examinadas por plaqueamento de diluições em série de homogeneizados de órgãos inteiros para a determinação de CFU. O pulmão é o principal local para a manifestação da doença em tuberculose no entanto baço, fígado e linfonodos são geralmente analisadas em conformidade. As diluições para ser plaqueadas depender da carga micobacteriana esperado nos órgãos, que dependem do inoculo inicial (dose baixa versus dose elevada), o que dá origem a diferentes cargas bacterianas em tecido, assim como sobre o órgão e ponto de tempo para ser analisado. Após a infecção dose baixa, a carga bacteriana de Mtb H37Rv no pulmão geralmente atinge um patamar entre o dia 25-30.
- Coloque animais sacrificados (eutanásia: CO 2 asfixia ouanestesia terminal) em papel absorvente em uma placa de dissecação em uma cabine de segurança biológica classe II e desinfectar ratos com etanol 70%. NOTA: álcool 70% é apenas para a descontaminação de superfície e não vai matar Mtb.
- Fazer uma pequena incisão no meio do abdómen e retrair a pele do rato por cima da cabeça.
- Abra o abdômen e caixa torácica, com uma tesoura cirúrgica e retirar da parede torácica para que os pulmões estão acessíveis.
- Retirar os pulmões e transferir para um tubo de 15 ml com tampão de homogeneização (água estéril / 1% v / v de Tween 80/1% w / v de albumina).
- Usando o êmbolo de uma pulmões 5 ml de deformação da seringa através de 100 mM peneiras numa pequena placa de Petri.
- Lave peneiras várias vezes utilizando uma pipeta 1 ml equipado com uma ponta de barreira e distribuem o homogeneizado de pulmão entre 8 placas de agar (cerca de 250 mL / placa;. Verifique se eles têm uma superfície bem seca).
- Placa cuidadosamente as amostras usando espalhadores descartáveis que são rejeitados em 2%Buraton.
- Deixe placas de ágar para secar dentro do gabinete. Seal cada prato único com parafilme, embrulhe em papel alumínio e incubar na vertical a 37 ° C durante pelo menos 4 semanas.
3. Construção de Gaiolas Mosquito à prova de escape
Linhagens de roedores Plasmodium não são prejudiciais aos seres humanos. No entanto, uma vez que camundongos infectados com Mtb são os destinatários do parasita eo trabalho é feito sob BSL 3 condições, precauções são necessárias para evitar que os mosquitos de escapar suas gaiolas. Dependendo do regime de infecção planejado, autoclave e gaiolas de metal com estrutura ou gaiolas descartáveis self-made reutilizáveis podem ser utilizados. Estas últimas são recomendadas se por infecção aguda de animais experimentais é necessário para ser realizado por um número definido de mosquitos por ratinho. Se forem necessárias gaiolas self-made, prepare gaiolas com as especificações exatas como a saúde dos mosquitos e da segurança do laboratório depende da sua sound construção (Figura 2).
- Pegue uma caixa de papelão, como um meio-litro de sorvete caixa ou copo de café de papel (Figura 2).
- Cortar uma pequena abertura para dentro do lado da caixa de cartão e cobrir com uma camada dupla de látex com uma fenda cortada em cada pedaço para criar uma entrada de segurança para os mosquitos. NOTA: A abertura tem um tamanho total de 2 cm x 2 cm, o tubo (dispositivo de aspiração) que usamos para trazer e / ou take-out mosquitos é um tubo de 15 ml Falcon modificado ligado a uma bomba de vácuo e, portanto, serve como um aspirador, com um diâmetro de 1,5 cm.
- Cole um pedaço de papel de filtro na parte inferior interna da caixa para absorver gotas.
- Feche fora taças de sorvete com rede (dupla camada de malha de nylon, tamanho 1 mm x 1 mm) e fixar a caixa com fita e elástico.
- Para as experiências de infecção onde são necessários números definidos de mosquitos por ratinho, preparar gaiolas com mosquitos infectados 10-15, cada uma das quais contém uma idealmente avtura de 10.000 do tipo selvagem glândula salivar P. esporozoítos berghei.
- O ideal é que morrer de fome mosquitos para 24 horas antes de realizar a refeição de sangue.
4. Infecção por malária de Ratos por picada de mosquito
O parasita da malária de roedores aqui utilizado é P. berghei no entanto qualquer outra estirpe de Plasmodium de roedor de interesse pode ser utilizado. Para obter os mosquitos infecciosos para a transmissão de esporozoítos de todo o ciclo de vida do parasita seja mantida tanto no hospedeiro vertebrado (rato) e o vector mosquito. Manutenção parasita é realizada num insectary. Para as experiências de transmissão natural, o número mínimo de esporozoítos por glândula salivar não deve ser inferior a 10.000. Para protocolos detalhados sobre a manutenção do parasita nos referimos Métodos em Malaria Research por Moll et al., 2013.
- Anestesiar ratos ou animais preinfected por 40 dias com Mtb com Ketamina ingênuos (100 mg / kg)solução e Xilazina (7 mg / kg) por injecção intraperitoneal (200 ul / ratinho). NOTA: O tempo entre a infecção pelo Mtb e Plasmodium pode ser ajustado de acordo com a questão de pesquisa subjacente. Da mesma forma, a fim de desafios de agentes patogénicos pode ser invertida, isto é, os ratos podem ser expostos a infeccioso picada de mosquito antes da infecção por M. tuberculosis.
- Coloque os ratos anestesiados para a compensação das gaiolas de mosquitos (um rato por gaiola mosquito para mosquito definido para relação de rato) e permitir que os mosquitos se alimentar através da membrana por 10-15 min. NOTA: A presença de sangue nas vísceras de mosquito de alimentação e implica portanto, a transmissão de esporozoítos.
- Transferir ratos de volta para suas gaiolas e supervisionar constantemente até que eles acordam da anestesia. Nota: Coloque camundongos sobre toalha de papel e não na cama (perigo de asfixia) e manter aquecido (local juntos e cobrir corpos com toalha de papel).
- Matar os mosquitos de pulverização com 70% de etanol ou outros desinfectantes através do nettção da gaiola. Gaiolas autoclave e descartar se foram utilizadas as descartáveis.
5. Monitoramento parasitemia
- Punção veias da cauda no final do percurso com uma agulha e recolher uma gota de sangue em cada extremidade de uma lâmina.
- Use outro slide para puxar uma gota de sangue sobre a metade do comprimento da lâmina. Vire o espalhador de usar a outra ponta para o segundo esfregaço. Deixe slides para ar seco.
- Giemsa
- Colocar as lâminas em suportes de lâmina e fixar os esfregaços de sangue por breve imersão em metanol absoluto. NOTA: Como o uso de utensílios de vidro devem ser mantidos no mínimo no BSL 3 usamos tinas de polipropileno para todas as soluções.
- Mergulhe as manchas em Giemsa (1:10 em água deionizada). Após 10 min, mergulhe os slides dentro e fora do tinas de coloração com água deionizada algumas vezes para lavar afastado o excesso de corante.
- Finalmente, as lâminas secas de ar em uma posição vertical.
- MANCHA ALTERNATIVA: Wright & #180; s mancha
- Dissolve-se o corante de Wright, a uma concentração de 1 mg / ml em metanol.
- Filtrar através de um filtro dobrado antes da utilização.
- Mergulhe as manchas de sangue em solução de coloração e incubar por 4 min (Nota: a fixação de esfregaços metanol não é necessário que a solução de coloração é o metanol com base).
- Lavar por lâminas de enxaguamento em água desionizada, como descrito acima e deixar as lâminas de ar seco.
- Uma vez que mancha Giemsa / 's Wright está completa, gentilmente transferir todos os reagentes utilizados em um pote contendo Buraton disposição.
- Análise esfregaço de sangue
- Analisar esfregaços de sangue corados por microscopia de luz com uma ampliação de 100 vezes, com imersão em óleo.
- Contagem eritrócitos não infectados e infectados em uma área do esfregaço de sangue, onde os eritrócitos são dispostos em uma monocamada.
- A fim de alcançar uma parasitemia bem definida, contar pelo menos 10 campos de vista diferentes, que apresentam uma monocamada de eritrócitos.
- CalculComeram a parasitemia relativo (em%) é calculada dividindo o número de eritrócitos parasitados por o número de eritrócitos, e multiplicando por 100.
Resultados
Infecção de camundongos com Mtb e P. berghei através da via natural, ou seja, de aerossol e picada de mosquito, respectivamente, resulta em infecção consistente e reprodutível de todos os animais (Tabela 1) 1. Podemos monitorar a infecção bem sucedida eo curso de ambos a malária ea tuberculose, determinando a ocorrência inicial (pré-patente) e número de parasitas no sangue (P. berghei parasitemia) ea carga de Mtb em diferentes órgãos, respectivamente. Um exemplo de uma transmissão com sucesso pelo parasita da malária infecciosa picada de mosquito é mostrada na Tabela 1 e na Figura 3. A alimentação de 10 mosquitos infectados com esporozoítos em cada rato resultou em uma taxa de infecção de 100%, como confirmado pela presença de parasitas no sangue em fase de 4-5 dias mais tarde (Tabela 1 e Figura 3A). É importante ressaltar que encontramos números semelhantes parasitas no sangue de camundongos individual do mesmo gr experimentalOUP, indicando que a transmissão de esporozoítos por resultados picada de mosquito em uma infecção consistente e reproduzível. Ao comparar o pré-patente em camundongos controle ingênuos com que, em animais Mtb-co-infectados, podemos ver que a pré-patente é um pouco atrasado em ratos que tinham sido preinfected com Mtb (Tabela 1, Figura 3B) 1. Como já relatado anteriormente 1, podemos determinar o impacto da co-infecção M. tuberculosis no curso de malária por parasitemia acompanhamento diário em esfregaços de sangue corados pelo Giemsa, como mostrado na Figura 3B.
Infecção de murganhos com Mtb através da utilização de um sistema de exposição de inalação resulta na deposição de sucesso de bactérias nos pulmões com relativamente baixa variabilidade entre ratos individuais (Figura 4A). Podemos acompanhar cargas de micobactérias em pulmões e outros órgãos de interesse ao longo do tempo por determinação UFC. Um exemplo para a carga micobacteriana nos pulmõesMtb infectados ratinhos C57BL / 6 na ausência ou na presença de P. berghei é mostrado na Figura 4B.
Tabela 1. Pré-patente após a transmissão de esporozoítos por picada de mosquito. Todos os ratos desenvolveram infecções do sangue em estágio após a transmissão natural de P. berghei esporozoítos por picada de mosquito. Adaptado de um PLoS One, 7 (10), e48110 com permissão.
| Grupo experimental de rato (C57BL / 6) | Desafie por 10 picadas de mosquitos infecciosos | N º de sangue em estágio positivo animais / N º de animais por grupo | A média pré-patente [d] |
| ingênua | P. berghei | 7/7 | 4,4 |
| Mtb infectados | P. berghei | 7/7 | 5,5 d> |
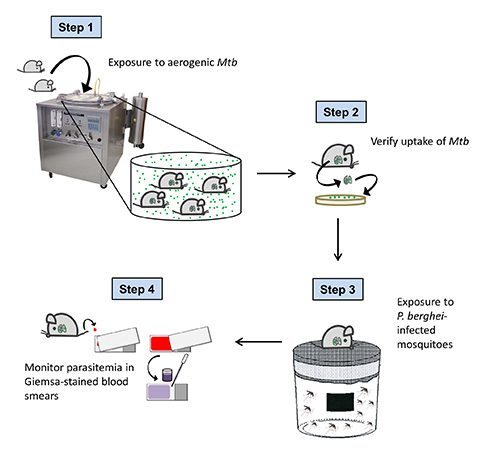
Figura 1. Esquema geral do procedimento experimental. Ratinhos C57BL / 6 são expostos ao Mtb contendo gotículas de aerossóis na câmara de aerossol Glas-Col. Um dia após infecção por aerossol, a absorção de M. tuberculosis é verificada por análise de UFC do pulmão. 40 dias após o desafio Mtb (quando a tuberculose tornou-se crônica em camundongos infectados), os animais são expostos a P. berghei infectados mosquitos. Para confirmar a transmissão bem sucedida de esporozoítos e para seguir o curso da infecção por Plasmodium, parasitemia é monitorizado diariamente em esfregaços de sangue coradas com Giemsa a partir de 3 dias após a picada de mosquito.
/ Files/ftp_upload/50829/50829fig2highres.jpg "src =" / files/ftp_upload/50829/50829fig2.jpg "/>
Figura 2. Esboço de uma gaiola mosquito. Mosquitos infecciosos estão contidos dentro de uma caixa, como um meio-litro de sorvete de cartão. Uma pequena abertura é cortada no lado da caixa e coberto com uma camada dupla de látex com uma fenda de corte em cada pedaço para criar uma entrada de segurança para os mosquitos. Um pedaço de papel de filtro é colado na parte inferior interna da caixa para absorver gotas. Taças de sorvete são fechadas com compensação (Nylon mesh), que é fixada à caixa com fita e elástico.

Figura 3. Parasitemia Sangue. A) Exemplo de um `s Wright esfregaço de sangue manchado mostrando eritrócitos parasitados (barra de escala, 20 & #181;. M) B) parasitemia no sangue do rato foi monitorada através da análise esfregaços de sangue corados pelo Giemsa diárias. Camundongos co-infectados têm uma parasitemia reduzida em comparação com camundongos Plasmodium únicos infectados (n = 10); resultados são apresentados como média ± SD; *** p <0,001. Reproduzido a partir de 1 PLoS One, 7 (10), e48110 com permissão.
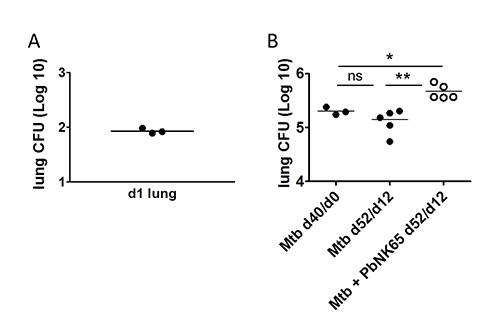
Figura 4. Detecção de M. tuberculosis no pulmão. Ratinhos C57BL / 6 foram provocados com aerossol de 100 CFU de M. tuberculosis e 40 dias mais tarde, co-infectadas com P. berghei por picada de mosquito. A) Um dia após a infecção aerossol a captação do número desejado de Mtb foi verificado por plaqueamento homogeneizados de pulmão integrais para a determinação de UFC. b) Bactériasl cargas no momento da co-infecção foi determinado em lisados pulmonares de três ratinhos por meio de análise de CFU (Mtb d40/d0). 12 dias após a co-infecção, lisados de pulmão foram semeadas para análise CFU para determinar o impacto da co-infecção por Plasmodium no controle de M. tuberculosis. Note-se, que os números de Mtb nos pulmões aumentou durante a co-infecção com P. berghei NK65. Rotulagem Eixo X: tempo após Mtb -infection/time após co-infecção. Adaptado de um PLoS One, 7 (10), e48110 com permissão.
Discussão
Nós descrevemos como ratos podem ser produtivamente infectados com Mtb e P. berghei através de suas rotas naturais de infecção. Nós aplicamos estabelecidos protocolos de infecção para estudar a tuberculose ou a malária experimental 13 12 e, recentemente adoptada-los a estudar a co-infecção entre Mtb e Plasmodium no modelo do rato 1.
Os passos mais críticos para infecções bem sucedidas são a transmissão de ambos os patógenos para os números desejados. Estoques de micobactérias não deve ser mais de 2 anos, porque eles vão perder a viabilidade ao longo do tempo, eo título originalmente determinado das ações provavelmente não será mais preciso. Como resultado, as doses de infecção seria muito menor do que o esperado. Por isso, os títulos de UFC de culturas de deve ser determinada a cada poucos meses. Igualmente importante é o cultivo padronizado e geração de estoques de Mtb em primeiro lugar. Condições de cultura, tais comomédio, suplementos, tempo e volume devem ser padronizados, a fim de poder comparar os dados de experimentos usando diferentes estoques de Mtb. Micobactérias tendem a aglutinar-se durante a cultura, por isso é importante para manter as condições de cultivo padronizado, as bactérias colheita na mesma fase de crescimento e ressuspender com freqüência durante alíquotas. Caso contrário, pode haver uma grande variação nos títulos de UFC e desfecho infecção.
A geração de lotes de mosquitos infectados de forma homogênea é mais um passo crítico. Uma vez que diferentes mosquitos se alimentam de cada ratinho individual, é importante que todos os mosquitos utilizados para um ensaio de infecção vêm do mesmo lote e que apenas os lotes em que mais de 90% dos mosquitos infectados são utilizados.
O actual modelo pode ser usado para dissecar as respostas imunes e modulações imunes num hospedeiro co-infectados por comparação com as respostas imunitárias nos hospedeiros infectados individuais. Podemos aplicar various metodologias como histologia, imuno-histoquímica, citometria de análise de populações de células do sistema imunológico, ou PCR e ELISA para detecção de citocinas e quimiocinas no tecido ou fluidos corporais de interesse bem estabelecidos. Deve notar-se, que tais modelos de ratos têm certas limitações. Considerando que a maioria das pessoas infectadas com M. tuberculosis vão desenvolver uma infecção latente, sem sinais de sintomas clínicos, os ratos desenvolvem uma doença crônica com patologia pulmonar progressiva. Ainda, ratinhos C57BL / 6 são relativamente resistentes a infecção por M. tuberculosis e não se desenvolvem os granulomas clássicos como observado em pacientes com tuberculose humana. Como resultado, as reações imunopatológicos no rato nem refletem a doença tuberculose humana latente nem ativo de forma adequada. Apesar da discrepância entre a doença latente e crônica no homem e rato, ratos têm sido amplamente utilizados para identificar e estudar os fatores do hospedeiro que controlam a infecção por M. tuberculosis e que são ferramentas valiosas e indispensáveis para investigarrespostas imunitárias em doenças infecciosas. Importante, a susceptibilidade à infecção por M. tuberculosis varia consideravelmente entre estirpes de ratos consanguíneos comumente utilizados e as estirpes mais sensíveis, tais como DBA ou C3H podem ser incluídas em estudos de co-e com somente uma infecção. Além disso, para além das espécies de agentes patogénicos aqui descritos, quaisquer outras espécies de Mycobacterium de interesse (por exemplo, isolados clínicos) poderia ser utilizado. Da mesma forma, enquanto um modelo único malária reproduz todos os aspectos da doença humana diferentes modelos de ratos que se assemelham muito diferentes aspectos da infecção da malária humana adquirida naturalmente. Por exemplo, P. berghei e P. ANKA yoelii YM/17XL são amplamente modelos de humano (induzida por P. falciparum) malária grave estudada, com P. berghei ANKA ser considerado um excelente modelo para cerebral humano Malari s 14,15. P. berghei NK65 é um excelente modelo para hyperparasitaemia e anemia malária aguda, e tem sido recentementedescrito como um modelo experimental para a síndrome associada à malária do desconforto respiratório agudo (SDRA MA-16). Utilizando o modelo de co-infecção descrito, podemos mostrar que recentemente concomitante P. infecção berghei NK65 agrava a tuberculose crônica 1.
Além de usar diferentes parasitas da malária de roedores, a ordem eo tempo dos eventos de infecção podem ser adaptadas de acordo com a questão de pesquisa subjacente. No campo, infecções Plasmodium concomitantes podem estar presentes na altura da infecção por M. tuberculosis ou adquirida posteriormente. Em ambos os cenários das respostas imunes a Mtb e Plasmodium podem ser afetados de forma diferente. Portanto, os ratinhos podem ser infectados com Plasmodium esporozoítos, quer antes ou depois da infecção por M. tuberculosis. Além disso, os ratos podem ser contestadas em diferentes momentos após a infecção Mtb para avaliar o impacto da resposta imune induzida por Plasmodium em aguda contra crônicatuberculose. É importante ressaltar que quando se escolhe um parasita da malária para estudar malária tuberculose co-infecção, deve-se estar ciente de que algumas estirpes de Plasmodium roedores causar doença aguda em certas linhagens de camundongos e sucumbir à infecção dentro de poucos dias ou semanas, enquanto Mtb causa crônica e infecções de longa duração em imunocompetentes ratinhos. Assim, o tempo de co-infecção é fundamental para evitar a morte prematura dos animais experimentais.
A modulação da imunidade do hospedeiro por infecção simultânea com várias espécies de patógenos ainda é mal-compreendido. Nosso modelo de co-infecção experimental fornece uma ferramenta poderosa para investigar Mycobacterium - interação Plasmodium com o sistema imunológico de uma série co-infectados e vai contribuir para a nossa compreensão como co-infecções podem afetar a patogênese, evolução da doença, a vacinação, imunodiagnóstico, e terapia.
Divulgações
Os autores não têm nada a revelar.
Agradecimentos
Os autores gostariam de agradecer a Miriam Ester para reprodução do mosquito. Este trabalho foi apoiado por in-house financiamento do Centro de Pesquisa Borstel e juntou-se o financiamento pelo Infecção Leibniz Center.
Materiais
| Name | Company | Catalog Number | Comments |
| Buraton | Schülke | active ingredients: aldehyds (formaldehyde, glutaraldehyde, oxalaldehyde, ethyl hexanal) | |
| Middlebrook 7H9 | Sigma | M0178 | For Mtb broth cultures |
| Middlebrook 7H11 | BD Biosciences | 283810 | Agar medium for Mtb culture |
| Middlebrook OADC enrichment medium | BD Biosciences | 212240 | Add to 7H9 and 7H11 for Mtb culture |
| Staining Dish | Science Services | E62542-12 | |
| 24-slide Holder w/Handle | Science Services | E62543-06 | |
| Giemsas Azur-Eosin-Methylene blue solution | Merck Millipore | 109204 | |
| Wright´s stain | Sigma | W0625 | |
| Inhalation Exposure System | Glas-Col | ||
| Nebulizer-Venturi | Glas-Col | ||
| Ice cream cups | Häagen-Dazs | Used as mosquito cages | |
| Metal-frame mosquito cages | BioQuip Products | 1450A |
Referências
- Mueller, A. -. K., et al. Natural Transmission of Plasmodium berghei Exacerbates Chronic Tuberculosis in an Experimental Co-Infection Model. PLoS ONE. 7, e48110 (2012).
- Korbel, D. S., Schneider, B. E., Schaible, U. E. Innate immunity in tuberculosis: myths and truth. Microbes Infect. 10, 995-1004 (2008).
- Aly, A. S., Vaughan, A. M., Kappe, S. H. Malaria parasite development in the mosquito and infection of the mammalian host. Annu. Rev. Microbiol. 63, 195-221 (2009).
- Cirimotich, C. M., Dong, Y., Garver, L. S., Sim, S., Dimopoulos, G. Mosquito immune defenses against Plasmodium infection. Dev. Compar. Immuno. 34, 387-395 (2010).
- Page, K. R., et al. Mycobacterium-induced potentiation of type 1 immune responses and protection against malaria are host specific. Infect. Immun. 73, 8369-8380 (2005).
- Hawkes, M., et al. Malaria exacerbates experimental mycobacterial infection in vitro and in vivo. Microbes Infect. 12, 864-874 (2010).
- Scott, C. P., Kumar, N., Bishai, W. R., Manabe, Y. C. Short report: modulation of Mycobacterium tuberculosis infection by Plasmodium in the murine model. Am. J. Trop. Med. Hyg. 70, 144-148 (2004).
- Hoffman, S. L., Doolan, D. L. Malaria vaccines-targeting infected hepatocytes. Nat. Med. 6, 1218-1219 (2000).
- Mueller, A. K., et al. Genetically attenuated Plasmodium berghei liver stages persist and elicit sterile protection primarily via CD8 T cells. Am. J. Pathol. 171, 107-115 (2007).
- Mueller, A. K., Labaied, M., Kappe, S. H., Matuschewski, K. Genetically modified Plasmodium parasites as a protective experimental malaria vaccine. Nature. 433, 164-167 (2005).
- Nussenzweig, R. S., Vanderberg, J., Most, H., Orton, C. Protective immunity produced by the injection of x-irradiated sporozoites of plasmodium berghei. Nature. 216, 160-162 (1967).
- Vaughan, J. A., Scheller, L. F., Wirtz, R. A., Azad, A. F. Infectivity of Plasmodium berghei sporozoites delivered by intravenous inoculation versus mosquito bite: implications for sporozoite vaccine trials. Infect. Immun. 67, 4285-4289 (1999).
- Coleman, J., Juhn, J., James, A. A. Dissection of midgut and salivary glands from Ae. aegypti mosquitoes. J. Vis. Exp. , e228 (2007).
- Franke-Fayard, B., et al. A Plasmodium berghei reference line that constitutively expresses GFP at a high level throughout the complete life cycle. Mol. Biochem. Parasitol. 137, 23-33 (2004).
- Lin, J. W., et al. Loss-of-function analyses defines vital and redundant functions of the Plasmodium rhomboid protease family. Mol. Microbiol. 88, 318-338 (2013).
- Bancroft, J. D. G., M, . Theory and Practice of Histological Techniques. , (2007).
- Schneider, B. E., et al. A role for IL-18 in protective immunity against Mycobacterium tuberculosis. Eur. J. Immunol. 40, 396-405 (2010).
- Craig, A. G., et al. The role of animal models for research on severe malaria. PLoS Pathog. 8, e1002401 (2012).
- de Souza, J. B., Hafalla, J. C., Riley, E. M., Couper, K. N. Cerebral malaria: why experimental murine models are required to understand the pathogenesis of disease. Parasitology. 137, 755-772 (2010).
- Van den Steen, P. E., et al. Immunopathology and dexamethasone therapy in a new model for malaria-associated acute respiratory distress syndrome. Am. J. Respir. Crit. Care Med. 181, 957-968 (2010).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados