É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Coleta simultânea de dados de medições de fMRI e fNIRS usando um arranjo de optode de cabeça inteira e canais de curta distância
Neste Artigo
Resumo
Apresentamos um método para coletar simultaneamente sinais de RMf e fNIRS dos mesmos indivíduos com cobertura de fNIRS de cabeça inteira. O protocolo foi testado com três adultos jovens e pode ser adaptado para coleta de dados para estudos de desenvolvimento e populações clínicas.
Resumo
A espectroscopia funcional no infravermelho próximo (fNIRS) é uma metodologia de neuroimagem portátil, mais robusta ao movimento e mais econômica do que a ressonância magnética funcional (fMRI), o que a torna altamente adequada para a realização de estudos naturalísticos da função cerebral e para uso com populações clínicas e de desenvolvimento. Tanto a metodologia fNIRS quanto a fMRI detectam alterações na oxigenação sanguínea cerebral durante a ativação cerebral funcional, e estudos anteriores mostraram alta correspondência espacial e temporal entre os dois sinais. Não há, no entanto, comparação quantitativa dos dois sinais coletados simultaneamente dos mesmos indivíduos com cobertura fNIRS de cabeça inteira. Essa comparação é necessária para validar de forma abrangente as ativações em nível de área e a conectividade funcional em relação ao padrão-ouro de RMf, que, por sua vez, tem o potencial de facilitar as comparações dos dois sinais ao longo da vida. Abordamos essa lacuna descrevendo um protocolo para coleta simultânea de dados de sinais de RMf e fNIRS que: i) fornece cobertura de fNIRS de cabeça inteira; ii) inclui medidas de curta distância para regressão do sinal fisiológico sistêmico não cortical; e iii) implementa dois métodos diferentes para o co-registro opto-couro cabeludo das medidas da fNIRS. Dados de RMf e fNIRS de três indivíduos são apresentados, e recomendações para adaptar o protocolo para testar populações clínicas e de desenvolvimento são discutidas. A configuração atual com adultos permite sessões de varredura por uma média de aproximadamente 40 min, o que inclui varreduras funcionais e estruturais. O protocolo descreve as etapas necessárias para adaptar o equipamento fNIRS para uso no ambiente de ressonância magnética (RM), fornece recomendações tanto para o registro de dados quanto para o co-registro opto-couro cabeludo e discute possíveis modificações do protocolo para se adequar às especificidades do sistema fNIRS disponível para RM-safe. Respostas representativas específicas do assunto de uma tarefa de xadrez intermitente ilustram a viabilidade do protocolo para medir sinais fNIRS de cabeça inteira no ambiente de RM. Este protocolo será particularmente relevante para pesquisadores interessados em validar sinais fNIRS contra fMRI ao longo da vida.
Introdução
A função cognitiva tem sido estudada no cérebro humano adulto por meio de ressonância magnética funcional (RMf) há quase três décadas. Embora a RMf forneça alta resolução espacial e imagens funcionais e estruturais, muitas vezes não é prática para estudos realizados em contextos naturalísticos ou para uso com lactentes e populações clínicas. Essas restrições limitam substancialmente nossa compreensão da função cerebral. Uma alternativa à RMf é o uso de metodologias portáteis mais econômicas e robustas ao movimento, como a espectroscopia funcional no infravermelho próximo (fNIRS)1,2,3. A fNIRS tem sido utilizada com lactentes e crianças pequenas para avaliar a função cerebral em uma variedade de domínios cognitivos, como desenvolvimento da linguagem, processamento de informações socialmente relevantes e processamento de objetos 4,5,6. A fNIRS também é uma modalidade de neuroimagem especialmente adequada para testar populações clínicas devido ao seu potencial para testes repetidos e monitoramento através de idades 7,8,9. Apesar de sua ampla aplicabilidade, não há estudos comparando quantitativamente os sinais de RMf e fNIRS coletados simultaneamente dos mesmos indivíduos com cobertura de cabeça inteira. Essa comparação é necessária para validar de forma abrangente as ativações em nível de área e a conectividade funcional entre regiões de interesse (ROIs) em relação ao padrão-ouro de RMf. Além disso, o estabelecimento dessa correspondência intermodalidade tem o potencial de melhorar a interpretação da fNIRS quando é o único sinal coletado em ambos os desenvolvimentos típicos e atípicos.
Tanto a RMf quanto os sinais da fNIRS detectam alterações na oxigenação sanguínea (OCC) cerebral durante a ativação funcional cerebral10,11. A RMf baseia-se em mudanças em campos eletromagnéticos e fornece uma alta resolução espacial das alterações da CBO12. O fNIRS, por outro lado, mede os níveis de absorção de luz infravermelha próxima usando uma série de optodes emissores e detectores de luz2. Uma vez que o fNIRS mede mudanças na absorção em diferentes comprimentos de onda, ele pode avaliar mudanças de concentração tanto na oxi- quanto na desoxihemoglobina. Estudos anteriores utilizando registros simultâneos de sinais de RMf e fNIRS com um pequeno número de optódios mostraram que os dois sinais têm alta correspondência espacial e temporal10. Existem fortes correlações entre RMf dependente do nível de oxigênio no sangue (BOLD) e medidas ópticas11,13, com a desoxihemoglobina apresentando a maior correlação com a resposta BOLD, como relatado por trabalhos anteriores comparando a dinâmica temporal das funções de resposta hemodinâmica (FCR) da RMf e da RMf14. Esses primeiros estudos implementaram paradigmas de resposta motora (isto é, toque dos dedos) e usaram um número limitado de optódios cobrindo áreas motoras primárias e córtex pré-motor. Na última década, os estudos expandiram o foco para incluir uma bateria maior de tarefas cognitivas e sessões de repouso, embora ainda usando um número limitado de optódios cobrindo ROIs específicas. Esses estudos mostraram que a variabilidade nas correlações fNIRS/fMRI é dependente da distância do optode do couro cabeludo e do cérebro15. Além disso, a fNIRS pode fornecer medidas de conectividade funcional em repouso comparáveis à RMf16,17.
O protocolo atual baseia-se em trabalhos anteriores e aborda as principais limitações, i) fornecendo cobertura fNIRS de cabeça inteira, ii) incluindo medições de curta distância para regressão de sinais fisiológicos não corticais, iii) implementando dois métodos diferentes para o co-registro opto-couro cabeludo das medidas fNIRS e iv) permitindo a avaliação da confiabilidade teste-reteste do sinal em duas sessões independentes. Este protocolo para coleta simultânea de dados de sinais de RMf e fNIRS foi inicialmente desenvolvido para testar adultos jovens. No entanto, um dos objetivos do estudo foi criar um arranjo experimental para coletar sinais simultâneos de RMf/fNIRS que possam ser posteriormente adaptados para testar populações de desenvolvimento. Portanto, o protocolo atual também pode ser usado como ponto de partida para o desenvolvimento de um protocolo para testar crianças pequenas. Além de utilizar a cobertura de fNIRS de cabeça inteira, o protocolo também visa incorporar avanços recentes no campo do hardware de fNIRS, como a inclusão de canais de curta distância para medir o sinal fisiológico sistêmico (ou seja, alterações vasculares decorrentes de fontes não corticais, como pressão arterial, sinais respiratórios e cardíacos)18,19 ; e o uso de um sensor de estrutura 3D para o co-registro opto-couro cabeludo20. Embora o foco do presente protocolo esteja nos resultados de uma tarefa de xadrez piscante visual, todo o experimento inclui duas sessões com uma mistura de designs tradicionais de tarefas em bloco, sessões de repouso e paradigmas naturalistas de visualização de filmes.
O protocolo descreve as etapas necessárias para adaptar o equipamento fNIRS para uso no ambiente de RM, incluindo o desenho da tampa, o alinhamento temporal via sincronização do gatilho e os testes simuladores necessários antes do início da coleta de dados. Como observado, o foco aqui está nos resultados da tarefa de xadrez intermitente, mas o procedimento geral não é específico da tarefa e pode ser apropriado para qualquer número de paradigmas experimentais. O protocolo descreve ainda as etapas necessárias durante a coleta de dados, que incluem a colocação da tampa fNIRS e calibração do sinal, a configuração do equipamento participante e experimental, bem como a limpeza pós-experimento e o armazenamento dos dados. O protocolo termina fornecendo uma visão geral dos pipelines analíticos específicos para o pré-processamento de dados de fNIRS e fMRI.
Access restricted. Please log in or start a trial to view this content.
Protocolo
A pesquisa foi aprovada pelo Comitê de Ética em Pesquisa (CEP) da Universidade de Yale. Consentimento informado foi obtido para todos os sujeitos. Os indivíduos tiveram que passar por exames de ressonância magnética para garantir sua participação segura. Eles foram excluídos se tivessem uma história de transtorno médico ou neurológico grave que provavelmente afetaria o funcionamento cognitivo (ou seja, um transtorno neurocognitivo ou depressivo, trauma, esquizofrenia ou transtorno obsessivo-compulsivo).
NOTA: O protocolo atual utiliza um dispositivo CW-NIRS com 100 canais de longa distância e 8 canais de curta distância (32 fontes de diodo laser, λ = 785/830 nm com potência média de 20mW/comprimento de onda, e 38 detectores de fotodiodo de avalanche) amostrados a 1,95 Hz. Os exames de RM e RMf foram coletados em um scanner Siemens 3 Tesla Prisma usando uma bobina de cabeça de 20 canais. Todos os dados foram coletados no Yale Brain Imaging Center (https://brainimaging.yale.edu/). Modificações específicas do sistema para coletar dados simultâneos de RMf e fNIRS são observadas em todo o protocolo.
1. Modificações e desenvolvimento de equipamentos fNIRS para coleta simultânea de dados
NOTA: As etapas 3 a 6 são específicas para o sistema NIRScoutXP e podem não se aplicar a outros sistemas fNIRS devido à variação no software de aquisição e nos simuladores disponíveis para avaliação de optodos.
- Preparação das tampas fNIRS
- Identificar as tampas fNIRS necessárias para o estudo. Para um estudo com adultos, certifique-se de que os seguintes tamanhos de tampa estão disponíveis (em cm): 54, 56, 58 e 60.
- NOTA: Os tamanhos de tampa são específicos para o sistema usado neste protocolo. Portanto, pode haver variação nos tamanhos específicos necessários para diferentes sistemas NIRS.
- Usando cápsulas de vitamina E e um material repelente à água (por exemplo, tecido de nylon com revestimento de PU), prepare os fiduciais. Embrulhe as cápsulas com o material de escolha e costure (ou cole) as fiduciais nas áreas escolhidas (ver Figura 1A). As cápsulas de vitamina E servem como marcadores fiduciais para identificar a posição dos canais fNIRS em relação ao tecido cerebral subjacente usando a imagem T1w.
- Determine o número de fiduciários dependendo da matriz optode e do método de co-registro. Alguns estudos exigirão apenas a detecção de alguns pontos anatômicos, enquanto outros podem se beneficiar da colocação de fiduciais ao lado de cada optode.
- Se a tampa fNIRS estiver muito solta na parte de trás da cabeça, prenda duas alças em cada lado da tampa usando tecido elástico (com botoeiras pré-cortadas) e botões para aumentar a capacidade de ajuste da tampa. Em todos os participantes e independentemente de quão apertada seja a tampa, prenda as alças para garantir uma configuração consistente da tampa.
- Se a frente da tampa estiver muito apertada na testa, coloque tampões de borracha nos optódios que estão em contato direto com a pele. Se o fornecedor fNIRS não fornecer buffers, crie-os usando adesivos de tecido de feltro. Se estiver usando amortecedores de borracha, use-os para todos os participantes, independentemente do ajuste da tampa, para garantir uma configuração consistente da tampa. Certifique-se de que os ingredientes nos buffers de borracha não tenham componentes metálicos para proteger contra artefatos nas imagens de RM.
- Configuração do equipamento fNIRS nas salas de controle e scanner de RM
- Coloque o dispositivo fNIRS na sala de controle perto de uma das guias de onda que levam à sala do scanner. Use uma superfície elevada (por exemplo, uma banqueta de degrau) se necessário para garantir que o dispositivo fNIRS esteja o mais próximo possível das guias de onda, a fim de maximizar o comprimento da fibra.
- Usando redes de cabos de malha, agrupe as fibras ópticas em grupos. Determine esses grupos com base na matriz optode escolhida. Idealmente, as fibras ópticas serão agrupadas de modo que todos os optodes do grupo sejam colocados no mesmo lado da cabeça (esquerda versus direita).
- Conecte as fibras ópticas ao dispositivo fNIRS e guie os feixes para a sala do scanner através das guias de onda. Antes de encomendar as fibras ópticas, meça a distância entre o dispositivo fNIRS e o centro do furo do scanner para se certificar de que o comprimento das fibras ópticas será suficiente.
- Leve as fibras ópticas para a mesa do scanner. Use uma ponte segura para ressonância magnética para segurar as fibras ópticas para garantir que o peso das fibras não faça com que as fibras caiam e para evitar que elas puxem a tampa para longe da cabeça do sujeito (ver Figura 1B).
- Configurando a caixa do replicador de porta paralela
- Instale a versão mais recente do software NIRStar no computador de aquisição de dados fNIRS.
- Conecte o replicador de porta paralela ao cabo que transmite o pulso semelhante ao transistor-transistor Logic (TTL) do scanner, conforme indicado no manual de disparo do fabricante (versão R2.1; consulte a Figura 1C). O pulso TTL corresponde a um pulso de temporização de fatia enviado diretamente do scanner. Quando o scanner está enviando um pulso, um dos indicadores LED acende.
- Conecte a caixa replicadora de porta paralela ao dispositivo fNIRS por meio de uma entrada de porta paralela. Isso enviará um gatilho para o software NIRStar sempre que um pulso TTL do scanner for detectado. O sinal de disparo será refletido na tela de gravação de aquisição de dados como uma linha pontilhada. Essa configuração garante a sincronização da coleta de dados de fNIRS e fMRI, pois toda vez que um pulso de temporização de corte é coletado no scanner, isso será refletido no fluxo de dados fNIRS registrado pelo software de aquisição NIRStar.
- Preparação do simulador estático para avaliação de optodos
- Coloque os optodes no dispositivo simulador estático fornecido pelo fornecedor fNIRS. A disposição dos optodes no simulador dependerá do tipo de instrumento fNIRS e do número de fontes e detectores disponíveis. Verifique a disposição correta do optode no guia de introdução do provedor do fabricante.
- Certifique-se de que o fantasma está completamente protegido de qualquer fonte de luz. Alguns fornecedores fornecem um estojo de encaixe que ajuda a proteger os optodes de qualquer fonte de luz externa.
- Conecte todas as fontes disponíveis e feixes de detectores ao simulador fNIRS de acordo com o arranjo optode especificado.
- Conecte o simulador fNIRS ao computador de aquisição e inicie o software de aquisição NIRStar.
- Realização de um teste de instrumento fantasma de ruído escuro
- No item de menu Configurar hardware do software de aquisição NIRStar, abra a guia Configuração de canal. Certifique-se de que, em Número de Fontes e Número de Detectores, o número total de fontes e detectores disponíveis esteja definido corretamente. Confirme essas configurações clicando em OK.
- Inicie a janela de teste de ruído escuro clicando no item de menu Diagnóstico no menu principal da janela NIRStar.
- Execute o teste pressionando o botão Executar teste . Salve os resultados do teste pressionando o botão Salvar resultados .
Observação : consulte o fabricante "Guia de introdução: solução de problemas de fantasma estático" do fabricante para obter orientação sobre como interpretar os resultados.
- Realizando um teste de calibração de simulador
- No item de menu Configurar hardware no software de aquisição NIRStar, abra a guia Configuração de canal . Certifique-se de que, em Número de Fontes e Número de Detectores , o número total de fontes e detectores disponíveis esteja definido corretamente.
- No item de menu Configurar Hardware , abra a guia Mascaramento de Canal . Mascare todos os canais pressionando o botão Selecionar tudo .
- No item de menu Configurar Hardware, na guia Especificação de Hardware, escolha Fantasma Estático em Tipo de Estudo. Confirme essas configurações clicando em OK.
- Inicie a calibração pressionando o botão Calibrar . Quando a calibração estiver concluída, pressione o botão Detalhes para visualizar os resultados detalhados da calibração.
Observação : consulte o fabricante "Guia de introdução: solução de problemas de fantasma estático" do fabricante para obter orientação sobre como interpretar os resultados.
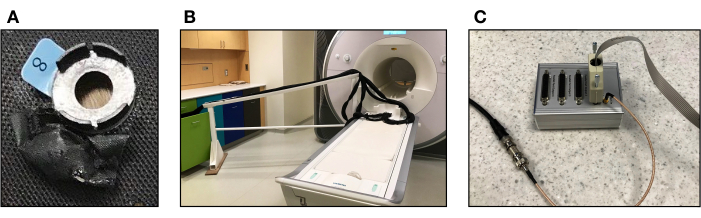
Gráfico 1. Equipamento para coleta simultânea de dados de medidas de RMf e fNIRS. (A) Bolsa feita de material preto repelente à água para armazenar cápsulas de vitamina E costuradas na tampa fNIRS adjacente a cada optode. (B) Ponte segura para RM para segurar as fibras ópticas acima do chão para que possam alcançar a cabeça do participante durante a coleta de dados. (C) Replicador de porta paralela que transmite pulsos do scanner para o dispositivo fNIRS. Clique aqui para ver uma versão maior desta figura.
2. Desenho de tarefas experimentais
- Decida sobre a duração da sessão de digitalização levando em consideração o conforto do participante dentro do scanner. Por exemplo, o estudo aqui destacado inclui duas imagens estruturais (T1w e T2w) para uma duração total de aproximadamente 14 min, e cinco corridas funcionais para uma duração adicional de aproximadamente 25 min.
NOTA: O piloto do estudo com vários participantes será necessário para identificar a duração apropriada do estudo, uma vez que fatores específicos do estudo (por exemplo, idade do participante, tamanho da tampa) determinarão o nível de conforto. - Projetar as tarefas de neuroimagem de acordo com os objetivos da pesquisa. Este será um estudo específico. Aqui, o procedimento (e os resultados representativos) de uma tarefa de xadrez intermitente são apresentados.
3. Colocação da tampa fNIRS e calibração do sinal no dia do teste
NOTA: Todas as etapas abaixo ocorrem nas salas de controle ou consentimento de ressonância magnética, a menos que indicado de outra forma.
- Medidas da cabeça de coleta e seleção da tampa fNIRS
- Uma vez que o participante tenha assinado os termos de consentimento relevantes e recebido as instruções para as próximas tarefas, oriente-o a sentar-se em uma cadeira localizada na sala de controle.
- Usando uma fita métrica macia padrão, enrole a fita em torno da maior circunferência possível da cabeça do participante; da parte mais proeminente da testa (geralmente 1 ou 2 dedos acima da sobrancelha) para a parte mais larga da parte de trás da cabeça e para trás. Tente encontrar a circunferência mais larga.
- Escolha o tamanho da tampa mais próximo da circunferência medida.
- Fixação das sondas do detector de curta distância na tampa
NOTA: Esta etapa é específica para sistemas NIRx e pode não se aplicar a outros dispositivos fNIRS.- Coloque as sondas do detector de curta distância segurando firmemente a base e deslizando-a em torno da parte do grommet que atravessa a malha da tampa fNIRS (ver Figura 2A). Tenha cuidado para não puxar as sondas do detector de curta distância do cabo, pois isso pode danificar o cabo.
NOTA: Ao decidir a distribuição das sondas, consulte um trabalho recente comparando distribuições específicas de cabeça inteira versus ROI18. - Use os clipes organizadores de fibra fornecidos pelo fabricante para gerenciamento de cabos, se necessário. Certifique-se de que os cabos do detector de curta distância estejam orientados para a parte de trás da tampa, a fim de manter a área ao redor da face clara.
- Coloque as sondas do detector de curta distância segurando firmemente a base e deslizando-a em torno da parte do grommet que atravessa a malha da tampa fNIRS (ver Figura 2A). Tenha cuidado para não puxar as sondas do detector de curta distância do cabo, pois isso pode danificar o cabo.
- Colocação da tampa fNIRS e optodes na cabeça do participante
- Peça ao participante que coloque o boné deslizando-o diretamente do topo da cabeça, como se estivesse colocando um chapéu de inverno. Certifique-se de que a tampa está reta e que as orelhas estão nos orifícios da orelha.
- Peça ao participante que aperte a alça do queixo o máximo que for confortável. Aperte as correias traseiras e certifique-se de que a tampa está firmemente presa e os soquetes optode estão firmes à cabeça.
- Coloque adesivos verdes para marcar os principais locais fiduciais de acordo com as 10-20 posições do sistema (ínion, násio, pontos pré-auriculares anteriores à orelha e Cz)21.
NOTA: Os adesivos verdes são necessários se usar o sensor de estrutura 3D para determinar as coordenadas espaciais da fonte e locais do detector de optodos. Isso pode variar dependendo do tipo de sensor de estrutura 3D. O protocolo atual utiliza um sensor de estrutura (Mark II) da marca Occipital20. - Com o uso de uma fita métrica, alinhe simetricamente os pontos da tampa com os pontos do couro cabeludo, certificando-se de que i) os pontos pré-auriculares estejam equidistantes do ponto Cz e ii) o ínion e o ponto násio estejam equidistantes do ponto Cz. Certifique-se de que a posição do limite seja idêntica para todos os participantes.
- Obtenção de um modelo da cabeça do participante usando um digitalizador de sensor de estrutura 3D
- Instrua o participante a sentar-se para criar um modelo 3D de sua cabeça.
- Abra a estrutura do aplicativo em um tablet ou iPad.
NOTA: O protocolo descreve os passos necessários para criar uma malha de cabeça com o sensor de estrutura (Mark II) do Occipital20. Essas etapas podem variar entre os sistemas. - Verifique se as seguintes configurações estão desativadas: Cor de alta resolução, Exposição automática de infravermelho e Rastreador aprimorado.
- Centralize o participante de modo que toda a sua cabeça esteja dentro do quadrado 3D na tela, toda a sua cabeça seja renderizada e não haja muito de seus ombros no quadro.
- Faça cuidadosamente uma caminhada de 360° ao redor do participante para criar a digitalização 3D. Aguarde até que o aplicativo capture a imagem aproximadamente a cada 90° antes de prosseguir (consulte a Figura 3A).
- Depois que toda a digitalização tiver sido capturada, pressione o botão à direita da tela para criar a renderização 3D.
- Verifique a renderização para se certificar de que está clara e há detalhes suficientes para verificar a colocação dos optodes e adesivos fiduciais verdes. Armazene a digitalização 3D em um servidor protegido pela HIPAA.
- Preparando o participante para entrar na sala de scanner
- Após a geração do modelo 3D, remova os adesivos verdes e instrua o participante a colocar protetores auriculares em seus ouvidos.
- Siga as instruções em vigor no centro de imagens de RM para garantir que o participante esteja seguro para entrar na sala do scanner. Essa etapa geralmente envolve confirmar com o participante que não há metais em seu corpo e passar por um detector de metais como uma verificação final. Um questionário de segurança de RM preenchido pelo indivíduo antes da chegada é frequentemente exigido pela maioria dos centros de imagem.
- Colocação das sondas da fonte e do detector na tampa do fNIRS
- Na sala do scanner, oriente o participante a sentar-se confortavelmente na mesa do scanner.
- Ao estabilizar cada grommet optode com uma mão, use um aplicador seguro para ressonância magnética com a outra mão para afastar o cabelo do centro do grommet (ver Figura 2B). Quando o cabelo tiver sido suficientemente movido para fora da área (idealmente para que o couro cabeludo seja visível), pressione firmemente o optode no grommet.
- Certifique-se de que, uma vez que a tensão no grommet é liberada, o cabelo não volta a ocluir o centro do optode. Se estiver usando uma matriz de cabeça inteira, recomenda-se orientar os optodes na parte de trás da cabeça com suas fibras voltadas para a frente e aqueles optodes na frente da cabeça com suas fibras apontadas para trás. Essa configuração das fibras ópticas evitará que elas fiquem emaranhadas ou cravadas quando o participante se deitar e colocar a cabeça na bobina de ressonância magnética.
NOTA: Este processo de inserção e alinhamento de fibras é mais rápido e facilmente realizado com dois experimentadores localizados em cada lado do participante, tampando simultaneamente. - Organize as fibras ópticas ordenadamente em feixes usando organizadores de cabos (consulte a Figura 2B e a Figura 3B). Realizar um teste de calibração e medição da intensidade do sinal usando o software NIRStar. A colocação e calibração do optode realizada por dois pesquisadores experientes levará aproximadamente 10 min.
- Ajuste os optodes individuais conforme necessário até que seja alcançada uma qualidade de sinal suficiente, deslocando o cabelo interferente dos optodes problemáticos. Remova os optódios da tampa para deslocar o cabelo usando uma pinça de plástico (ver Figura 2B).

Gráfico 2. Detectores de curta distância e ferramentas para preparação de tampas fNIRS. (A) Sondas detectoras de curta distância e tampões de borracha a serem fixados à tampa fNIRS sobre áreas frontais onde há pelos mínimos. (B) Da esquerda para a direita: Organizadores de cabos para organizar as fibras ópticas em feixes, aplicadores seguros para ressonância magnética para afastar o cabelo durante a colocação do optode e pinças de plástico para remover os optodes da tampa, se necessário, durante a configuração da tampa NIRS para deslocar o cabelo. Clique aqui para ver uma versão maior desta figura.

Gráfico 3. Digitalizador do sensor de estrutura 3D e colocação da tampa fNIRS. (A) Experimentador usando o digitalizador de sensor de estrutura 3D para criar um modelo 3D da cabeça do participante. Adesivos verdes são usados para identificar locais fiduciários. (B) Fibras ópticas inseridas na tampa fNIRS na cabeça do participante e dispostas em feixes usando organizadores de cabos antes da calibração do sinal. Clique aqui para ver uma versão maior desta figura.
4. Configuração do participante
Observação : as etapas a seguir são realizadas na sala de scanner de ressonância magnética. O uso de cinta respiratória e oxímetro de pulso é opcional e necessário apenas se os pesquisadores estiverem interessados em regredir esses sinais a partir dos dados do fNIRS22. O protocolo utiliza uma cinta respiratória, que faz parte da unidade respiratória para a aquisição da amplitude respiratória por meio de uma cinta de contenção. Da mesma forma, a unidade de pulso fisiológico consiste em um sensor óptico de pletismografia que permite a aquisição do ritmo cardíaco.
- Verifique se a bobina de cabeça de 20 canais está colocada no scanner. Se usar uma matriz fNIRS de cabeça inteira, as bobinas de cabeça de 32 e 64 canais serão muito apertadas para os participantes adultos.
- Coloque um travesseiro de espuma dentro da parte inferior da bobina da cabeça da RM para apoiar a parte de trás da cabeça do participante (ver Figura 4A).
- Peça ao participante que se deite devagar e com cuidado para que seu movimento não mova a tampa ou puxe as fibras ópticas. Ajuste os feixes de fibra óptica conforme necessário para permitir que a cabeça do participante descanse confortavelmente dentro da bobina principal (ver Figura 4B). A mesa do scanner pode precisar ser levantada durante essa etapa, dependendo de onde os cabos estão localizados a partir da guia de onda.
- Coloque um travesseiro sob as pernas do participante para garantir que ele esteja confortável. Coloque o cinto respiratório ao redor da cintura do participante.
- Peça ao participante que coloque os fones de ouvido com cancelamento de ruído ao redor de suas orelhas, estando atento para não interferir na colocação da sonda fNIRS. Para evitar que os fones de ouvido deslizem, use almofadas seguras para ressonância magnética em ambos os lados da cabeça entre os fones de ouvido e o lado interno da bobina da cabeça. Uma capa de travesseiro pode ser usada para evitar que os fones de ouvido entrem em contato com a bobina da cabeça.
- Coloque o oxímetro de pulso no dedo indicador da mão não dominante do indivíduo. Se estiver usando uma caixa de botões para as tarefas experimentais, peça ao participante que a segure com a mão dominante. Forneça ao participante instruções sobre como usar a caixa de botão.
- Coloque a bola de aperto ou o botão de alarme na mão não dominante do sujeito e instrua o participante como usá-lo. Teste o alarme solicitando ao participante que o pressione.
- Deslize o participante alguns centímetros para dentro do furo do scanner para alinhar a cabeça. Posicione a parte superior da bobina da cabeça. Em seguida, insira o microfone e o espelho nas pastilhas da bobina correspondentes.
- Deslize o participante lentamente para dentro do furo do scanner enquanto segura as fibras ópticas. Esse processo exigirá duas pessoas, que estarão localizadas em cada lado da mesa do scanner. Certifique-se de que as fibras ópticas sejam cuidadosamente guiadas para dentro do furo do scanner para evitar puxar os optodes ou beliscar as fibras entre a bobina principal e o furo do scanner.
- Após confirmar com o participante que está pronto para a sessão de escaneamento, retorne à sala de controle e confirme via áudio do interfone que o participante pode ouvir o experimentador e o experimentador pode ouvir o participante.
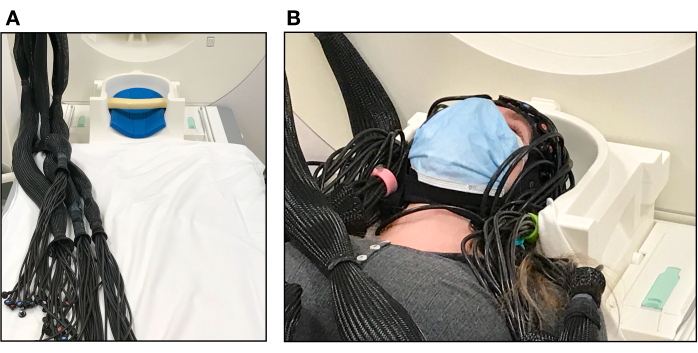
Gráfico 4. Participante configurado no aparelho de ressonância magnética. (A) Almofadas dentro da bobina da cabeça de RM utilizadas para apoiar a cabeça do participante e fibras ópticas dispostas em feixes antes da montagem do participante. (B) Participante deitado no leito do scanner com a tampa fNIRS pronta para o teste. A parte superior da bobina ainda não foi colocada sobre o rosto do participante. Clique aqui para ver uma versão maior desta figura.
5. Configuração do scanner e do equipamento fNIRS antes da gravação do sinal
- No computador scanner, selecione as sequências estruturais e funcionais relevantes para o estudo. Ao calcular um modelo de sensibilidade à luz dos dados do fNIRS, colete imagens de T1w e T2w para obter a melhor resolução de contraste tecidual.
- Verifique o localizador para confirmar uma boa posição da cabeça dentro do furo do scanner. Verifique se a cobertura cerebral completa é obtida do topo da cabeça até o cerebelo.
- Confirme com o participante que a tela do computador está visível através do espelho da bobina da cabeça.
- Execute a primeira varredura estrutural. Em paralelo, execute outro teste de calibração dos optodes fNIRS para verificar se a configuração do participante afetou a intensidade do sinal de qualquer um dos canais.
- Depois de executar a primeira ressonância magnética estrutural, colete as sequências do mapa de campo de eco gradiente e calibre os fones de ouvido com cancelamento de ruído para garantir que os fones de ouvido sejam capazes de fornecer estímulos auditivos ao participante, bem como bloquear qualquer ruído ambiente.
NOTA: Alguns participantes podem precisar que seus fones de ouvido sejam ajustados. Se este for o caso, entre novamente na sala do scanner e ajuste o preenchimento ao redor dos fones de ouvido, ficando atento para não interferir na colocação da sonda fNIRS. Execute outro localizador, sequências de mapa de campo de eco gradiente e teste de calibração dos optodes fNIRS antes de prosseguir.
6. Gravação simultânea de sinais
- Verifique com o participante através do interfone para se certificar de que ele está confortável e fazendo OK. Forneça as instruções para a tarefa e lembre os participantes de manter a cabeça e o corpo imóveis.
- Forneça as instruções a seguir, específicas para a tarefa de xadrez intermitente (Figura 5).
- Nesta tarefa, instrua o participante a sempre olhar para o meio da tela que está à sua frente (através do espelho). Às vezes, a tela mostrará um quadriculado com blocos piscando em frequências diferentes. Outras vezes, o participante verá um círculo branco no meio da tela.
- Quando o círculo branco aparecer na tela, peça ao participante que pressione a caixa de botões com o dedo indicador. Depois que o botão pressionar, o círculo ficará vermelho.
- Esta tarefa usa um design de bloco alternado. Permita que os participantes completem uma única corrida de 6 min, que inclui 11 blocos quadriculados piscantes de 10 s cada e 11 blocos de círculo de 20 s cada.
- Inicie a gravação de dados do fNIRS no computador do fNIRS e inicie as tarefas no computador de apresentação do estímulo. O roteiro para as tarefas experimentais será exibido como instruções da tarefa.
- Inicie a primeira execução funcional. Uma vez que o scanner envia o primeiro pulso TTL, ele aparecerá como um sinal de gatilho na tela de gravação de dados do software NIRStar. Este primeiro pulso também dará início à tarefa experimental.
- Monitore o desempenho e o movimento dos participantes em todas as tarefas. Em alguns casos, especialmente ao usar um conjunto de optodos de cabeça inteira e bonés de tamanho pequeno, alguns participantes podem sentir algum desconforto ao usar o boné. É importante sempre monitorar o conforto do participante.
- Se necessário, providencie uma pausa para o participante no meio da sessão. Durante esse intervalo, se os participantes precisarem se sentar, colete um localizador e execute as sequências de mapa de campo de eco gradiente, calibração de fone de ouvido e calibração de teste fNIRS novamente antes de prosseguir. Essa etapa geralmente não é necessária ao testar adultos jovens no scanner se as etapas exatas do presente protocolo forem seguidas.
- Durante a coleta de dados, faça anotações sobre a sessão (por exemplo, tamanho da tampa, hora do dia, optodes que não estavam bem calibrados ou qualquer coisa incomum).
- No final de todas as execuções funcionais, pare de coletar dados fNIRS. Execute uma segunda varredura estrutural, se necessário.
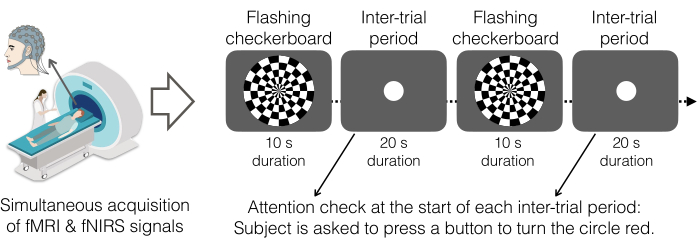
Gráfico 5. Paradigma xadrez intermitente como tarefa experimental. Os participantes visualizaram um padrão quadriculado preto e branco com quadrados brancos piscando oito vezes por segundo que alternavam com uma tela cinza mostrando um círculo branco. Como uma verificação de atenção, os participantes foram instruídos a pressionar um botão com a mão direita ao ver um círculo branco aparecer no meio da tela. Ao pressionar o botão, o círculo fica vermelho. A tarefa foi concluída em uma única corrida composta por 22 blocos no total: 11 blocos quadriculados intermitentes e 11 períodos inter-experimentais. Os períodos de xadrez intermitente duraram 10 s e os períodos inter-experimentais duraram 20 s. Assim, o início do xadrez intermitente ocorreu a cada 30 s (0,033 Hz). Os monitores foram gerados pelo PsychoPy v2021.2.4 e projetados no espelho retrovisor na parte superior da bobina principal por meio de um sistema de projeção DLP de 1080p. Os participantes completaram uma execução desta tarefa (~6 min). Clique aqui para ver uma versão maior desta figura.
7. Limpeza pós-experimento e armazenamento de dados
- Utilize a cama motorizada do scanner para retirar lentamente o participante do furo do scanner, tomando cuidado para não beliscar nenhuma das fibras ópticas. Retire a parte superior da bobina de cabeça e peça ao participante que se sente lentamente.
- Retire a tampa fNIRS da cabeça do participante e remova cada optode dos respectivos grommets. O cabelo muitas vezes fica preso nos grommets mesmo depois que os optodes foram removidos, então instrua os participantes a remover a tampa lenta e cuidadosamente.
- Alguns grommets podem se desalojar no processo de desencapamento. Certifique-se de localizar todas as peças do grommet e substituir as que estão faltando antes da próxima sessão de digitalização do participante.
- Peça aos participantes que deslizem da cama do scanner, agradeçam por seu tempo e forneçam compensação monetária, se aplicável.
- Certifique-se de que os logs de tarefas, fNIRS e dados de fMRI sejam armazenados e armazenados em backup. Desinfete a tampa com uma solução de limpeza por pulverização, conforme recomendado pelo fornecedor fNIRS, e limpe as pontas optode com lenços de álcool de plástico e borracha.
8. Pré-processamento de dados de RMf
NOTA: Os dados de fMRI foram pré-processados seguindo os pipelines mínimos de pré-processamento do Human Connectome Project23 usando QuNex24, um pacote de software de código aberto que suporta organização de dados, pré-processamento, garantia de qualidade e análises em todas as modalidades de neuroimagem. A documentação detalhada sobre as configurações e parâmetros específicos para cada uma das etapas destacadas abaixo pode ser encontrada no site do QuNex em https://qunex.yale.edu/. As principais etapas e parâmetros utilizados para processar os dados são apresentados a seguir.
- Pré-processar os dados estruturais
- Pipeline PreFreeSurfer. Execute as seguintes etapas: correção de distorção de gradiente, alinhamento de repetidas execuções de imagens T1w e T2w com uma transformação de corpo rígido de 6 graus de liberdade (DOF), alinhamento AC-PC de imagens T1w e T2w ao molde espacial MNI, extração cerebral inicial, correção de distorção de leitura, registro cross-modal de T1w e T2w no espaço de volume nativo, correção de campo de viés e registro de volume não linear MNI.
- Pipeline de freesurfer. Execute as seguintes etapas: Reduza a amostra T1w para 1mm com interpolação spline e execute recon-all para gerar superfícies de substância branca, o que inclui o ajuste fino do registro T2w para T1w usando o algoritmo BBRegister do Freesurfer (veja23 para obter mais detalhes).
- Pipeline PostFreeSurfer. Execute as seguintes etapas: Converter saídas de reconhecimento para GIFTI e NIFTI no espaço de volume nativo, gerar a máscara cerebral final e o volume da fita cortical, gerar mapas de mielina e executar a transformação de volume não linear nativa para MNI.
- Pré-processar os dados funcionais
- Pipeline de volume de RMf. Execute as seguintes etapas: correção de distorção, correção de movimento baseada em FLIRT, pré-processamento de mapa de campo baseado em TOPUP usando um mapa de campo de eco de spin, correção de distorção de imagem EPI e registro de EPI para T1w, reamostragem de spline de uma etapa para o espaço atlas (MNI), normalização da intensidade via remoção de campo de viés e mascaramento cerebral.
- Tubulação de superfície fMRI. Execute as seguintes etapas para mapear a série temporal de volume para uma representação combinada de superfície e volume, em ordem cinza, armazenada no formato CIFTI: construção de fita fMRI, suavização de superfície, processamento subcortical e geração de séries temporais densas.
- Prepare dados BOLD. Calcule estatísticas quantitativas de CQ que reflitam o movimento e suas propriedades artefatuais para identificar quadros defeituosos. Consulte a documentação do QuNex para obter as opções disponíveis para gerar estatísticas quantitativas de CQ. Essas estatísticas geralmente incluem estatísticas de sinal para ruído temporal BOLD e depuração de movimento, como limiar de deslocamento de quadro e limiar de erro quadrático médio (RMSE) de raiz normalizada da intensidade da imagem. Dependendo dos critérios específicos do estudo, ignorar ou interpolar os quadros problemáticos identificados.
- Extraia o sinal de incômodo. Extraia sinais de incômodo de ventrículos cerebrais, substância branca e substância cinzenta para realizar a regressão do sinal de incômodo nas etapas subsequentes.
9. Pré-processamento de dados fNIRS
NOTA: Os dados do fNIRS foram analisados seguindo as melhores práticas na análise de dados do fNIRS25 usando o NeuroDOT26, um ambiente de código aberto para análise de dados ópticos de níveis de luz bruta em mapas de função cerebral em nível de voxel, que são co-registrados na anatomia de um participante específico ou em um atlas. Todas as etapas descritas abaixo podem ser realizadas com o NeuroDOT. Documentação adicional sobre as configurações e parâmetros específicos para cada uma das etapas destacadas abaixo pode ser encontrada nos tutoriais e scripts em https://github.com/WUSTL-ORL/NeuroDOT_Beta. Finalmente, o registro de optodo para couro cabeludo requer a obtenção das coordenadas de optode fNIRS em relação ao tecido cerebral subjacente, o que pode ser feito usando um digitalizador 3D ou cápsulas de vitamina E como fiduciais, se disponíveis. Ambos os métodos são descritos nesta seção e referências aos pacotes de software relevantes são fornecidas.
- Geração de uma malha de cabeça específica para cada assunto e criação do modelo de luz
- Segmente a imagem T1w nos tipos de tecido relevantes para criar um modelo de cabeça segmentada: couro cabeludo, crânio, líquido cefalorraquidiano (LCR), substância cinzenta e substância branca. Utilize imagens T1w e T2w, se disponíveis, uma vez que cada uma delas contribui com informações complementares sobre os tipos de tecidos relevantes.
NOTA: Esta etapa é realizada no protocolo atual com a função "Segment5R_fs", do NeuroDOT, que toma como entrada informações da segmentação volumétrica doFreesurfer28. Outros pacotes de software comumente disponíveis para segmentação de tecido cerebral são SPM29 e AFNI30. - Gere uma malha de cabeça a partir do modelo de cabeça segmentada usando o pacote de software Mimics via NeuroDOT. Se um digitalizador 3D for usado para colocar os locais do optode no modelo principal, siga as recomendações do Fieldtrip para localização do optode31. Alternativamente, se as cápsulas de vitamina E forem usadas como fiduciais para identificação de coordenadas de pares fonte-detector, identifique manualmente as posições das fontes e detectores na imagem T1w (veja32 para um exemplo).
- Coloque os locais da fonte e do detector obtidos através do digitalizador 3D ou das cápsulas de vitamina E nos loci relevantes na malha usando o NeuroDOT.
- Defina os seguintes parâmetros para calcular a matriz de sensibilidade para o modelo de cabeça específico do sujeito usando o pacote de software NIRFAST via NeuroDOT: resolução de voxelação: 2; rótulos da região: LCR, branco, cinza, osso, pele; coeficientes de absorção para regiões: CSF [0,004, 0,004], branco [0,0167, 0,0208]; cinza [0,018 0,0192], osso [0,0116, 0,0139], pele [0,74, 0,64]; coeficientes de espalhamento por regiões: CSF [0,3; 0,3], branco [1,1908, 1,0107]; cinza [0,8359, 0,6726], osso [0,94; 0,84], pele [0,64; 0,74], índice de refração para regiões: LCR [1,4; 1,4], branco [1,4; 1,4]; cinza [1,4; 1,4], osso [1,4; 1,4], pele [1,4; 1,4].
NOTA: O protocolo utiliza o software NIRFAST (versão 9.1)33,34, que utiliza um modelo de luz direta de elementos finitos baseado na aproximação da difusão à equação de transporte radiativo. Para calcular o modelo de luz, o NIRFAST baseia-se em três tipos de informação: i) a forma do limite do tecido, ii) a distribuição interna das propriedades ópticas basais e iii) a localização das fontes e detectores na superfície (ver 35,36 para mais detalhes). O método de Monte Carlo pode ser empregado como alternativa para calcular soluções para a equação de difusão para diferentes tipos de tecidos37,38. - Visualize um exemplo da sensibilidade da medida como uma avaliação qualitativa.
- Segmente a imagem T1w nos tipos de tecido relevantes para criar um modelo de cabeça segmentada: couro cabeludo, crânio, líquido cefalorraquidiano (LCR), substância cinzenta e substância branca. Utilize imagens T1w e T2w, se disponíveis, uma vez que cada uma delas contribui com informações complementares sobre os tipos de tecidos relevantes.
- Processamento dos dados brutos das medições do detector de origem
- Exiba o nível médio de luz para cada fonte e detector em uma representação 2D da matriz de imagens. Remover pares fonte-detector com desvio padrão temporal maior que 7,5%36. Se os dados forem adquiridos a uma taxa de quadros de pelo menos 3Hz, use o limiar de potência cardíaca para rejeitar medidas do par fonte-detector, uma vez que um bom acoplamento optode-couro cabeludo exibirá características consistentes com a frequência da frequência de pulso (~1 Hz).
- Destenda os dados para remover a tendência linear em cada medição. Filtro passa-alta (ponto de corte de 0,02 Hz) para remover desvio de baixa frequência. Em vez de filtrar, uma alternativa é adicionar um fator de deriva no GLM como um regressor.
- Filtro passa-baixa (1 Hz) dos dados para remover oscilações cardíacas.
- Estime o sinal superficial global calculando a média de todas as medições do par fonte-detector de 8 mm. Use medidas de curta distância como uma estimativa de sinais fisiológicos sistêmicos não corticais à medida que coletam amostras principalmente do couro cabeludo e do crânio.
- Regressar o sinal global de todas as medições39.
- Low-pass filtra os dados (ponto de corte de 0,5 Hz) para focar ainda mais os dados restantes em torno da frequência do estímulo e reduz a amostra dos dados para 1 Hz 40,41,42 a fim de reduzir a carga computacional.
- Implementar censura de movimento usando a variância global das derivadas temporais (GVTD)43. A GVTD é calculada como a raiz quadrada média das derivadas temporais através de um conjunto de medidas ou voxels43. Implemente censura ou depuração de movimento excluindo os pontos de tempo que excedem o limite de ruído GVTD.
- Reconstruindo o modelo de luz e os dados pré-processados em um volume de neuroimagem funcional
- Reconstruir mudanças relativas na absorção a 785 nm e 830 nm com base em uma inversão regularizada da matriz de sensibilidade usando regularização de Tikhonov e regularização espacialmente variante44.
- Calcular mudanças relativas na concentração de hemoglobina através de uma decomposição espectral dos dados de absorção dependentes do comprimento de onda44,45.
10. Análise de dados evocados por tarefa de RMf/fNIRS
- Executar uma única sessão de análise GLM de primeiro nível (modelagem de FCR, regressão de sinais fisiológicos, incluindo medições de fNIRS de curta distância) para avaliar como a atividade cerebral se relaciona com a hipótese estatística para um determinado sujeito.
NOTA: Uma alternativa ao GLM é a média de blocos, que evita suposições a priori sobre a forma do HRF. A média dos bloqueios, entretanto, não permite modelar fatores de confusão relevantes no sinal da fNIRS juntamente com a resposta hemodinâmica ao estímulo. - Execute a análise GLM de grupo ou de segundo nível para combinar estimativas de primeiro nível de ativação entre sujeitos.
- Extraia estimativas de efeito relevantes dos arquivos GLM individuais e combine-os em arquivos de grupo.
- Calcule as estatísticas desejadas. Um pacote bem estabelecido para executar métodos de reamostragem de permutação de modelos GLM uni e multivariados para inferência estatística é o FSL PALM46.
- Obter estimativas beta de GLM de cérebro inteiro.
Access restricted. Please log in or start a trial to view this content.
Resultados
Esta seção apresenta respostas representativas específicas do assunto para a tarefa de xadrez intermitente para sinais fMRI e fNIRS. Primeiro, dados brutos representativos do fNIRS e avaliações de qualidade são mostrados na Figura 6 e na Figura 7 para ilustrar a viabilidade do arranjo experimental para medir sinais fNIRS no ambiente de RM. Um diagrama de toda a matriz de optodos da cabeça e do perfil de sensibilidade é mostrado na
Access restricted. Please log in or start a trial to view this content.
Discussão
Este protocolo para coleta simultânea de dados de sinais de RMf e fNIRS usa um arranjo de optodos fNIRS de cabeça inteira e canais de curta distância para medir e regredir os sinais fisiológicos sistêmicos não corticais. Etapas críticas neste protocolo incluem a modificação e desenvolvimento do equipamento fNIRS para coleta de sinais fNIRS no ambiente de RM. Até onde sabemos, não há um sistema comercial turn-key que seja totalmente otimizado para capturar medições simultâneas de fMRI e fNIRS usando um arra...
Access restricted. Please log in or start a trial to view this content.
Divulgações
As taxas de publicação deste artigo são patrocinadas pela NIRx. Os autores não têm mais nada a revelar.
Agradecimentos
Esta pesquisa foi apoiada pelas seguintes fontes de financiamento: Uma Bolsa NARSAD Young Investigator Award da Brain and Behavior Research Foundation (Grant #29736) (SSA), uma Global Grand Challenges Grant da Fundação Bill e Melinda Gates (Grant #INV-005792) (RNA) e uma Discovery Fund Grant do Departamento de Psicologia da Universidade de Yale (RNA). Os autores também agradecem a Richard Watts (Yale Brain Imaging Center) por seu apoio durante a coleta de dados e a Adam Eggebrecht, Ari Segel e Emma Speh (Washington University in St Louis) por sua assistência na análise de dados.
Access restricted. Please log in or start a trial to view this content.
Materiais
| Name | Company | Catalog Number | Comments |
| 280 low-profile MRI-compatible grommets for NIRs caps | NIRx | GRM-LOP | |
| 4 128-position NIRS caps with 128x unpopulated slits in 10-5 layout | NIRx | CP-128-128S | Sizes: 52, 54, 56, 60 |
| 8 bundles of 4x detector fibers with low-profile tip; MRI-, MEG-, and TMS-compatible. | NIRx | DET-FBO- LOW | 10 m long |
| 8 bundles of 4x laser source fibers with MRI-compatible low-profile tip | NIRx | SRC-FBO- LAS-LOW | 10 m long |
| Bundle set of 8 short-channel detectors with specialized ring grommets that fit to low-profile grommets | NIRx | DET-SHRT-SET | Splits a single detector into 8 short channels that may be placed anywhere on a single NIRS cap |
| Magnetom 3T PRISMA | Siemens | N/A | 128 channel capacity, 64/32/20 channel head coils, 80 mT/m max gradient amplitude, 200 T/m/s slew rate, full neuro sequences |
| NIRScout XP Core System Unit | NIRx | NSXP- CHS | Up to 64x Laser-2 (or 32x laser-4) illuminators or 64 LED-2 illuminators; up to 32x detectors; capable of tandem (multi-system) and hyperscanning (multi-subject) measurements; compatible with EEG, tDCS, eye-tracking, and other modalities; modules available for fMRI, TMS, MEG compatibility |
| NIRStar software | NIRx | N/A | Version 15.3 |
| NIRx parallel port replicator | NIRx | ACC-LPT-REP | The parallel prot replicator comes with three components: parallel port replicator box, USB power cable and BNC adapter |
| Physiological pulse unit | Siemens | PPU098 | Optical plethysmography allowing the acquisiton of the cardiac rhythm. |
| Respiratory unit | Siemens | PERU098 | Unit intended for the acquisition of the respiratory amplitude (by means of a pneumatic system and a restraint belt). |
| Structure Sensor Mark II | Occipital | 101866 (SN) | 3D structure sensor for optode digitization. |
Referências
- Pinti, P., et al. The present and future use of functional near-infrared spectroscopy (fNIRS) for cognitive neuroscience. Annals of the New York Academy of Sciences. 1464 (1), 5-29 (2020).
- Quaresima, V., Ferrari, M. Functional Near-Infrared Spectroscopy (fNIRS) for Assessing Cerebral Cortex Function During Human Behavior in Natural/Social Situations: A Concise Review. Organizational Research Methods. 22 (1), 46-68 (2016).
- Pinti, P., et al. A Review on the Use of Wearable Functional Near-Infrared Spectroscopy in Naturalistic Environments. The Japanese Psychological Research. 60 (4), 347-373 (2018).
- Wilcox, T., Biondi, M. fNIRS in the developmental sciences. Wiley Interdisciplinary Reviews: Cognitive Science. 6 (3), 263-283 (2015).
- Blasi, A., Lloyd-Fox, S., Katus, L., Elwell, C. E. fNIRS for Tracking Brain Development in the Context of Global Health Projects. Photonics. 6 (3), 89(2019).
- Aslin, R. N. Questioning the questions that have been asked about the infant brain using near-infrared spectroscopy. Cognitive Neuropsychology. (1-2), 7-33 (2012).
- Chen, W. L., et al. Functional Near-Infrared Spectroscopy and Its Clinical Application in the Field of Neuroscience: Advances and Future Directions. Frontiers in Neuroscience. 14, 724(2020).
- Lee, Y. J., Kim, M., Kim, J. S., Lee, Y. S., Shin, J. E. Clinical Applications of Functional Near-Infrared Spectroscopy in Children and Adolescents with Psychiatric Disorders. Journal of Child & Adolescent Psychiatry. 32 (3), 99-103 (2021).
- Bonilauri, A., Sangiuliano Intra, F., Baselli, G., Baglio, F. Assessment of fNIRS Signal Processing Pipelines: Towards Clinical Applications. Applied Sciences. 12 (1), 316(2021).
- Kleinschmidt, A., et al. Simultaneous recording of cerebral blood oxygenation changes during human brain activation by magnetic resonance imaging and near-infrared spectroscopy. Journal of Cerebral Blood Flow and Metabolism. 16 (5), 817-826 (1996).
- Strangman, G., Culver, J. P., Thompson, J. H., Boas, D. A. A Quantitative Comparison of Simultaneous BOLD fMRI and NIRS Recordings during Functional Brain Activation. NeuroImage. 17 (2), 719-731 (2002).
- Glover, G. H. Overview of functional magnetic resonance imaging. Neurosurgery Clinics of North America. 22 (2), (2011).
- Toronov, V., et al. Investigation of human brain hemodynamics by simultaneous near-infrared spectroscopy and functional magnetic resonance imaging. Medical Physics. 28 (4), 521-527 (2001).
- Huppert, T. J., Hoge, R. D., Diamond, S. G., Franceschini, M. A., Boas, D. A. A temporal comparison of BOLD, ASL, and NIRS hemodynamic responses to motor stimuli in adult humans. NeuroImage. 29 (2), 368-382 (2006).
- Cui, X., Bray, S., Bryant, D. M., Glover, G. H., Reiss, A. L. A quantitative comparison of NIRS and fMRI across multiple cognitive tasks. NeuroImage. 54 (4), 2808-2821 (2011).
- Duan, L., Zhang, Y. J., Zhu, C. Z. Quantitative comparison of resting-state functional connectivity derived from fNIRS and fMRI: a simultaneous recording study. NeuroImage. 60 (4), 2008-2018 (2012).
- Sasai, S., et al. A NIRS-fMRI study of resting state network. NeuroImage. 63 (1), 179-193 (2012).
- Noah, J. A., et al. Comparison of short-channel separation and spatial domain filtering for removal of non-neural components in functional near-infrared spectroscopy signals. Neurophotonics. 8 (1), 015004(2021).
- Wyser, D., et al. Short-channel regression in functional near-infrared spectroscopy is more effective when considering heterogeneous scalp hemodynamics. Neurophotonics. 7 (3), 035011(2020).
- Homolle, S., Oostenveld, R. Using a structured-light 3D scanner to improve EEG source modeling with more accurate electrode positions. Journal of Neuroscience Methods. 326, 108378(2019).
- Jasper, H. H. The ten-twenty electrode system of the International Federation. Electroencephalography and Clinical Neurophysiology. 10, 370-375 (1958).
- von Luhmann, A., Li, X., Muller, K. R., Boas, D. A., Yucel, M. A. Improved physiological noise regression in fNIRS: A multimodal extension of the General Linear Model using temporally embedded Canonical Correlation Analysis. NeuroImage. 208, 116472(2020).
- Glasser, M. F., et al. The minimal preprocessing pipelines for the Human Connectome Project. NeuroImage. 80, 105-124 (2013).
- Ji, J. L., et al. QuNex-An integrative platform for reproducible neuroimaging analytics. Frontiers in Neuroinformation. 17, 1104508(2023).
- Yucel, M. A., et al. Best practices for fNIRS publications. Neurophotonics. 8 (1), 012101(2021).
- Eggebrecht, A., Muccigrosso, D., Culver, J. NeuroDOT: an extensible Matlab toolbox for streamlined optical brain mapping. Diffuse Optical Spectroscopy and Imaging VII. , (2019).
- Jenkinson, M., Beckmann, C. F., Behrens, T. W., Woolrich, M. W., Smith, S. M. FSL. NeuroImage. 62 (2), 782-790 (2012).
- Fischl, B. FreeSurfer. NeuroImage. 62 (2), 774-781 (2012).
- Penny, W. D., Friston, K. J., Ashburner, J. T., Kiebel, S. J., Nichols, T. E. Statistical parametric mapping: the analysis of functional brain images. , Academic Press, Elsevier. (2011).
- Cox, R. W. AFNI: software for analysis and visualization of functional magnetic resonance neuroimages. Computers and Biomedical Research. 29 (3), 162-173 (1996).
- Oostenveld, R., Fries, P., Maris, E., Schoffelen, J. M. FieldTrip: Open source software for advanced analysis of MEG, EEG, and invasive electrophysiological data. Computational Intelligence and Neuroscience. 2011, 156869(2011).
- Sato, H., et al. A NIRS-fMRI investigation of prefrontal cortex activity during a working memory task. NeuroImage. 83, 158-173 (2013).
- Jermyn, M., et al. Fast segmentation and high-quality three-dimensional volume mesh creation from medical images for diffuse optical tomography. Journal of Biomedical Optics. 18 (8), 86007(2013).
- Dehghani, H., et al. Near infrared optical tomography using NIRFAST: Algorithm for numerical model and image reconstruction. Communications in Numerical Methods in Engineering. 25 (6), 711-732 (2008).
- Wheelock, M. D., Culver, J. P., Eggebrecht, A. T. High-density diffuse optical tomography for imaging human brain function. The Review of Scientific Instruments. 90 (5), 051101(2019).
- Eggebrecht, A. T., et al. A quantitative spatial comparison of high-density diffuse optical tomography and fMRI cortical mapping. NeuroImage. 61 (4), 1120-1128 (2012).
- Boas, D. A., Culver, J. P., Stott, J. J., Dunn, A. K. Three dimensional Monte Carlo code for photon migration through complex heterogeneous media including the adult human head. Optics Express. 10 (3), 159-170 (2002).
- Wang, L., Jacques, S. L., Zheng, L. MCML-Monte Carlo modeling of light transport in multi-layered tissues. Computer Methods and Programs in Biomedicine. 47 (2), 131-146 (1995).
- Gregg, N. M., White, B. R., Zeff, B. W., Berger, A. J., Culver, J. P. Brain specificity of diffuse optical imaging: improvements from superficial signal regression and tomography. Frontiers in Neuroenergetics. 2, 14(2010).
- Brigadoi, S., et al. Motion artifacts in functional near-infrared spectroscopy: a comparison of motion correction techniques applied to real cognitive data. NeuroImage. 85, 181-191 (2014).
- Pelphrey, K. A., Shultz, S., Hudac, C. M., Vander Wyk, B. C. Research review: Constraining heterogeneity: the social brain and its development in autism spectrum disorder. Journal of Child Psychology and Psychiatry, and Allied Disciplines. 52 (6), 631-644 (2011).
- Cui, X., Bray, S., Reiss, A. L. Functional near infrared spectroscopy (NIRS) signal improvement based on negative correlation between oxygenated and deoxygenated hemoglobin dynamics. NeuroImage. 49 (4), 3039-3046 (2010).
- Sherafati, A., et al. Global motion detection and censoring in high-density diffuse optical tomography. Human Brain Mapping. 41 (14), 4093-4112 (2020).
- Eggebrecht, A. T., et al. Mapping distributed brain function and networks with diffuse optical tomography. Nature Photonics. 8 (6), 448-454 (2014).
- Ferradal, S. L., et al. Functional Imaging of the Developing Brain at the Bedside Using Diffuse Optical Tomography. Cerebral Cortex. 26 (4), 1558-1568 (2016).
- Winkler, A. M., Ridgway, G. R., Webster, M. A., Smith, S. M., Nichols, T. E. Permutation inference for the general linear model. NeuroImage. 92, 381-397 (2014).
- Hassanpour, M. S., et al. Statistical analysis of high density diffuse optical tomography. NeuroImage. 85, 104-106 (2014).
- Zhang, F., et al. Correcting physiological noise in whole-head functional near-infrared spectroscopy. Journal of Neuroscience Methods. 360, 109262(2021).
- Duan, L., et al. Wavelet-based method for removing global physiological noise in functional near-infrared spectroscopy. Biomedical Optics Express. 9 (8), 3805-3820 (2018).
- Klein, F., Kranczioch, C. Signal Processing in fNIRS: A Case for the Removal of Systemic Activity for Single Trial Data. Frontiers in Human Neuroscience. 13, 331(2019).
- Zhou, X., Sobczak, G., McKay, C. M., Litovsky, R. Y. Comparing fNIRS signal qualities between approaches with and without short channels. PLoS One. 15 (12), 0244186(2020).
- Santosa, H., Zhai, X., Fishburn, F., Sparto, P. J., Huppert, T. J. Quantitative comparison of correction techniques for removing systemic physiological signal in functional near-infrared spectroscopy studies. Neurophotonics. 7 (3), 035009(2020).
- Emberson, L. L., Crosswhite, S. L., Goodwin, J. R., Berger, A. J., Aslin, R. N. Isolating the effects of surface vasculature in infant neuroimaging using short-distance optical channels: a combination of local and global effects. Neurophotonics. 3 (3), 031406(2016).
- Frijia, E. M., et al. Functional imaging of the developing brain with wearable high-density diffuse optical tomography: A new benchmark for infant neuroimaging outside the scanner environment. NeuroImage. 225, 117490(2021).
- Brigadoi, S., Cooper, R. J. How short is short? Optimum source-detector distance for short-separation channels in functional near-infrared spectroscopy. Neurophotonics. 2 (2), 025005(2015).
Access restricted. Please log in or start a trial to view this content.
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados