Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Прямое измерение целевого взаимодействия KDM1A с использованием иммуноанализов на основе хемозондов
В этой статье
Резюме
Здесь мы представляем протокол для измерения участия kDM1A в клетках человека или животного, тканях или образцах крови, обработанных ингибиторами KDM1A. Протокол использует хемозонд маркировки свободного фермента KDM1A и прямой количественной оценки целевого занятия с использованием химиозонда на основе иммуноанализов и могут быть использованы в доклинических и клинических исследованиях.
Аннотация
Оценка целевого взаимодействия, определяемого как взаимодействие препарата с разработанным для него белком, является основным требованием для интерпретации биологической активности любого соединения при разработке лекарств или в фундаментальных исследовательских проектах. В эпигенетике целевое взаимодействие чаще всего оценивается путем анализа прокси-маркеров вместо измерения соединения с целью. Ниже по течению биологических считывания, которые были проанализированы включают гистон знак модуляции или изменения экспрессии генов. KDM1A является лизин деметилаза, которая удаляет метиловые группы из моно- и диметилированного H3K4, модификация, связанная с глушинием экспрессии генов. Модуляция прокси-маркеров зависит от типа клеток и функции генетического состава исследуемых клеток, что может сделать интерпретацию и сравнение кросс-кейса довольно трудным. Для обхода этих проблем представлен универсальный протокол для оценки эффектов дози и динамики прямого целевого взаимодействия КДМ1А. Анализ описано использует KDM1A хемозонд для захвата и количественно раскованный фермент, может быть широко применяется к клеткам или образцам тканей без необходимости генетической модификации, имеет отличное окно обнаружения, и может быть использован как для фундаментальных исследований и анализ клинических образцов.
Введение
Лизин специфическая деметилаза 1 (KDM1A)1 является деметилазой, участвующих в контроле транскрипции генов. Этот белок стал кандидатом фармакологических целевой2 в онкологии; в том числе острый миелоидный лейкоз3 (AML), Синдром миелодисплазии (MDS)4, миелофиброз (MF)5,6, Малый рак легких (SCLC)7; при серповидно-клеточной болезни (SCD)8,9, и при заболеваниях центральной нервной системы, включая болезнь Альцгеймера (Ад), рассеянный склероз (Ms); и в агрессии10.
Большинство ингибирующих соединений KDM1A в клиническом развитии являются производными циклопропиламина и ингибируют белок ковалентным связыванием с его лавина аденин динуклеотид (FAD) кофактор11. Ингибирование KDM1A вызывает изменения экспрессии генов, но эти изменения сильно различаются по тканям, типам клеток или случаям заболевания. Ингибиция KDM1A также изменяет признаки гистона12, но эти изменения, как правило, производятся локально на определенном участке в геноме, и снова, высоко ткани и клеток конкретных.
Протокол был разработан для непосредственного измерения целевого участия KDM1A в биологических образцах и был оптимизирован для использования с ингибиторами производных циклопропиламина. Анализ основан на технологии ELISA и анализирует, параллельно, Total и Free (т.е. не связанный ингибитором) KDM1A в родном белковом экстракте из биологического образца в твердой фазе анализа. В качестве первого шага, биологический образец лизируется в присутствии биотинилапопром KDM1A селективного хемозонда OG-88113,14, полученных из селективного ингибитора KDM1A ORY-1001 (iadademstat), мощный ингибитор KDM1A в клинических развитие для лечения онкологических заболеваний. Химиозонд имеет IC50 для KDM1A 120 нм и включает в себя ФАД связывающий муаети, связанный с биотинилатированным полиэтиленовым гликолем (PEG).-хвост. Химиозонд исключительно связывается с свободным KDM1A, но не с ингибитором KDM1A в образце. После привязки хемозонда, KDM1A, содержащие комплексы в образце, фиксируются на микротитерных пластинах с стрептавидиновой поверхностью с покрытием для определения свободного KDM1A, или на пластинах, покрытых моноклональным анти-KDM1A захвата антитела для определения общего KDM1A. После мытья, обе пластины инкубируются антителами обнаружения к KDM1A, промывают снова и инкубируются вторичным HRP-конъюгированным антикроликом IgG антитела для обнаружения с помощью люминесцентного субстрата и количественной оценки путем измерения относительного световые единицы (RLU) в люминометре(рисунок 1).
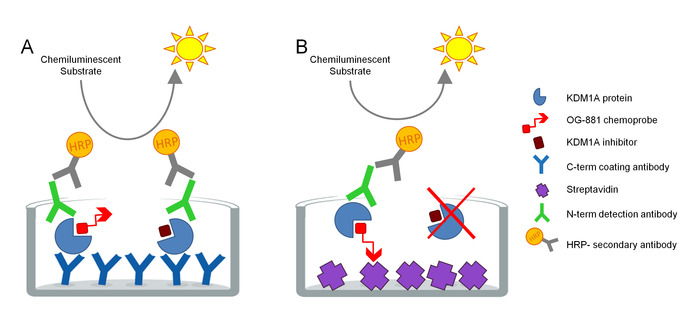
Рисунок 1. Схема ELISA Enzyme связана химиозонд иммуноабсорбент анализа для KDM1A целевого участия: A) Определение общего KDM1A с использованием бутерброда ELISA и B) Определение бесплатного KDM1A с использованием химиозонда ELISA. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
Стандартная кривая включена в обе пластины ELISA для проверки линейности каждого анализа. Определение целевого участия KDM1A в каждой выборке затем рассчитывается как относительная стоимость предварительной дозы или образца, обработанного транспортным средством.
Access restricted. Please log in or start a trial to view this content.
протокол
Образцы крови были получены из Института investigacion Biom'dica Sant Pau Biobank в соответствии с испанским законодательством (Real Decreto de Biobancos 1716/2011) и одобрения местных комитетов по этике. Исследования с тканями животных проводились в соответствии с институциональными руководящими принципами по уходу и использованию лабораторных животных (Директива Совета Европейских сообществ 86/609/EEC), установленных Этическим комитетом по экспериментам на животных ПРААЛ-ПКБ.
1. Подготовка биологических образцов для проведения асссе.
ВНИМАНИЕ: Этот протокол включает в себя манипуляции биологических образцов, которые могут быть подвергнуты профессиональной безопасности и здоровья администрации (OSHA) Крови Борн патогенов стандарт (29 CFR 1910.1030), Директива 2000/54/EC Европейского парламента и Совет от 18 сентября 2000 года или эквивалентные правила. Кроме того, биологические образцы могут содержать следы биологически активных исследуемых химических соединений, а протокол может предусматривать дальнейшие манипуляции такими соединениями. Просмотрите лист данных о безопасности (СДС) соединений, используемых до начала эксперимента, и строго соблюдайте все применимые меры безопасности, установленные в исследовательском центре, включая использование надлежащего средств индивидуальной защиты (СИЗ). Носите надлежащую защитную одежду и используйте надлежащее экранирование в ходе эксперимента. Отбрасывайте остатки в соответствующих контейнерах для отходов (биологические/цитоттоксичные отходы).
ПРИМЕЧАНИЕ: Этот протокол начинается с клеток или образцов субъектов, обработанных ингибитором KDM1A и их необработанных или транспортного средства / плацебо обработанных элементовуправления 3.
- Клетки, обработанные транспортным средством или ингибитором KDM1A in vitro
- Для клеток, выращенных в подвеске, как 10 мл культур, передача подвески в чистой 15 мл конических труб и перейти к 1.1.3.
- Для клеток адептов (выращенных в 75 см2 колбы), удалить среду из колбы и кратко вымыть с помощью 4 мл PBS. Отсоедините клетки от своих сосудов, используя 1,5 мл 0,5% трипсин-ЭДТА в течение 2 - 5 мин (условия трипсинации могут варьироваться, следуйте рекомендациям поставщика для клеточной линии), добавьте 4 мл PBS и перенесите клетки в чистые конические трубки 15 мл.
- Вставьте трубки в скамейке верхней центрифуги и собирать клетки центрифуги в течение 5 мин при 400 х г при 4 c. Удалите супернатант, отдохните гранулы в 1 мл PBS обойтись с помощью микропипетта и перенести подвеску в 1,5 мл микроцентрифуговой трубки.
- Вставьте образцы в центрифугу микротрубки и центрифуги их в течение 5 мин при 400 х г при 4 градусах Цельсия. Удалите PBS с помощью микропипетта и либо держите гранулы на льду и переходите к шагу 2; или заморозить гранулы на сухом льду и хранить их при -80 градусов по Цельсию до шага 3.
- Образцы, взятые у субъектов или животных, обработанных ингибитором транспортного средства/плацебо или KDM1A
- Ткани: Разрежьте ткань небольшими, 1 см3 штуки с помощью скальпеля. Заморозить кусочки тканей в жидкости N2 в контейнере Dewar и хранить их при -80 градусов по Цельсию до шага 3.
- Полиморфные моноядерные клетки крови (ПБМК): Разбавлять 10 мл свежей крови (процесс максимум 2 ч после вывода крови), собранных в трубках K2-EDTA с 2 томами PBS в конической трубке 50 мл. Изолировать PBMCs от крови с использованием коммерчески полученных PBMC разделения труб в соответствии с инструкциями производителя. Держите гранулы на льду и перейдите к шагу 3.2; или заморозить гранулы на сухом льду и хранить их при -80 градусов по Цельсию до шага 3.
ПРИМЕЧАНИЕ: Влажные клеточные гранулы от 20 до 50 кв. м содержит 1 х 107 ячеек, в зависимости от размера ячейки. Влажные гранулы PBMC, полученные из 10 мл здоровой человеческой крови, имеет объем 20 кЛ и содержат 1 х 107 PBMCs. Ткани или клеточные гранулы могут храниться при -80 oC в течение 6 месяцев.
2. Подготовка решения
- Подготовка 2 ММ OG-881 рабочего решения: Возьмите 10 мЛ одноразового аликута 20 мМ биотинилатированный зонд OG-881 запаса из 4 кс холодильники и оставить его при комнатной температуре (RT) в течение 10 мин. Подготовка 2 мКм рабочего решения последовательного разбавления OG-881 запасsolut ион в PBS, используя микропайпет с фильтром советы и изменение кончика между различными шагами разбавления.
- Приготовьте 10-разный ингибитор протеазы: растворите 1 таблетку в 1 мл PBS в микроцентрифуговой трубке.
- Подготовьте необходимый объем буфера лиза 1x Cell с помощью хемозина 25 нМ OG-881. Для каждого мЛ смешайте 100 мл коммерчески полученного буфера 10x Cell lysis, 150 л 10-кратных ингибиторов протеазы, 12,5 л из 2 ММ OG-881 и 737,5 л двойной дистиллированной воды типа 1.
- Дополнительно подготовить желаемый объем 1x Cell lysis буфера, но с 25 нм ORY-1001 вместо OG-881, как в шаге 2.3. Менее мощные ингибиторы могут быть использованы, но может потребовать более высоких концентраций, для использования в положительном контроле со 100% ингибирование (см. Шаг 3.5).
ПРИМЕЧАНИЕ: Принять соответствующие меры, чтобы избежать непреднамеренного загрязнения растворов или образцов с помощью ингибиторных растворов OG-881 или KDM1A. Для расчета желаемого объема буфера лизиса 1x Cell с 25 нм OG-881, предположим, что 400 л требуется на 40 мг распыленной ткани, или 200 л на влажные гранулы из 107 клеток.
3. Родная экстракция белка
- Из тканей:
- Распылять и гомогенизировать 1 см3 кубика замороженной ткани с помощью раствора и пестика, охлажденных на сухом льду. Aliquot образцы в одноразовых флаконах, содержащих 40 мг порошка ткани, избежать оттаивания во все времена. Приступай к шагу 3.1.2. для немедленной обработки или хранения при -80 градусах Цельсия.
- Resuspend 40 мг порошкообразной ткани в 400 л 1x Cell Lysis буфера с 25 нМ OG-881, вихрь для 10 с, и заставить образец по крайней мере пять раз через 18-калибровочный тупой шприц иглы до лиза ткани достигается и мутный свет желтый до оранжевого Получить. Избегайте образования пузырьков.
- Продолжить шаг 3.3
- Из клеточных гранул (ПБМК и клеточных линий):
- Отдохните гранулы из 1 х 107 клеток в 200 Л 1x-клеточного лисиса буфера, содержащего 25 nM OG-881. Vortex образцы кратко и держать их на льду в течение 5 минут.
- Снофид образцы в звуковой, используя 3 импульса по 20 с каждый при 45 кГц; поместите их на лед в течение 20 с между импульсами.
ПРИМЕЧАНИЕ: Как только биологические образцы были повторно приостановлены в буфере 1x клетки лиза, держать их на льду во время остальной части процесса.
- Держите образцы на льду еще 5 мин, вихрь кратко и центрифуги образцов в течение 10 минут на 14 000 х г в предварительно охлажденных центрифуги при 4 градусах По Цельсия.
- Используя микропипетет мощностью 1 мл, перенесите супернацианты в свежие микроцентрифугные трубки мощностью 1,5 мл и оставьте их на льду в течение 2 ч. Продолжайте шаг 4.
- Дополнительно, положительный контроль для имитации 100% целевого взаимодействия может быть подготовлен следующим образом:
- Resuspend клетки гранулы или порошкообразной ткани из транспортного средства или необработанных (предоза) образца в требуемом объеме 1x Cell Lysis буфера с 25 нм ORY-1001 и процесс, как указано в шаге 3.1 до 3.3.
- Перенесите супернационты положительного контроля в свежие микроцентрифугные трубки объемом 1,5 мл и оставьте их на льду на 1 ч. ОРИ-1001 умышленно ингибирует КДМ1А и блокирует связывание хемозоза.
- Добавьте 5 юл из 2 мкм OG-881 рабочего решения к положительному супернатанте управления (объем для положительного контроля, генерируемого из образца ткани 40 мг) или 2,5 л из 2 ткового раствора ММ OG-881 (объем для положительного контроля, генерируемого из 10 7-клеточного образца) для получения той же концентрации OG-881, как и другие образцы и оставить на льду в течение 2 ч. Продолжить шаг 4.
4. Количественная оценка родного белка с использованием Брэдфордского анализа
- Разбавить коммерчески источников Брэдфорд Протеина Ассей реагент 5 раз с H2O Тип 1 двойной дистиллированной воды. Рассчитайте объем реагента, необходимый для общего количества образцов и стандартов (1 мл на образец или стандартный 5 мл сверхтого объема).
- Для стандартной кривой Сыворотки (BSA) приготовьте одну микроцентрифугую трубку с 1 мл разбавленного раствора Протеинового асссеа Брэдфорда (пустой) и семью микроцентрифугами с 995 л разбавленного решения Bradford Protein Assay. Добавьте 5 кЛ каждого из стандартов BSA (концентрация от 125 до 2000 мкг/мл) к каждой из 7 микроцентрифуговых трубок и смешайте их, несколько раз аккуратно инвертируя трубки. Инкубировать в течение 5 мин на RT.
- Перенесите разбавленные стандарты в кюветы и прочитайте OD пустых и крупноватовых образцов сыворотки в спектрофотометре на 280 нм.
- Для биологических образцов, подготовить один микроцентрифуг трубки с 1 мл разбавленного Брэдфорд Протеина Ассае решение (пустой) и столько микроцентрифуговых труб с 999 Зл из разбавленного Брэдфорд Протеина Ассей реагент в качестве образцов, которые должны быть количественно. Используя автоматический микропипетт P2, добавьте 1 злицу экстракта родного белка, подготовленного в шаге 3, к каждой микроцентрифуговой трубке и перемешайте, несколько раз аккуратно инвертируя трубки. Инкубировать образцы 5 мин на RT.
- Перенесите тома в кюветы и прочитайте ОД образцов в спектрофотометре на 280 нм.
- Предпочтительно, немедленно перейдите к шагу 5. Кроме того, храните экстракты родного белка при -80 градусов по Цельсию до шага 5. Избегайте циклов оттепели.
5. Люминесцентные ELISA для total и свободного определения KDM1A
ПРИМЕЧАНИЕ: Держите температуру в лаборатории постоянной на уровне 23-24 градусов по Цельсию (RT).
- Покрытие микротитерных пластин с захватом антител KDM1A или стрептавидина
- Всего KDM1A ELISA: для каждой пластины, подготовить 10 мл KDM1A захвата антитела до конечной концентрации 2 мкг/мл в PBS. Перенесите 100 л в каждую скважину пластины.
- Бесплатный KDM1A ELISA: для каждой пластины, подготовить 10 мл стрептавидина на 10 мкг/мл в PBS. Перенесите 100 л в каждую скважину пластины.
- Топ-печать Всего и бесплатно KDM1A ELISA пластин с клейкой пленкой и инкубировать пластины на ночь при 4 градусов по Цельсию в холодильнике.
- Мытье и блокирование пластин
- Возьмите пластины из холодильника и дайте им уравновесить около 45 минут на RT перед использованием.
- Подготовьте буфер для мытья 1000 мл (0,1% tween в PBS) и 50 мл блокирующего буфера (1% BSA в PBS) на тарелку.
- Вымойте тарелки 3 раза с мытьем буфера. В этом и последующих шагах, нажмите тарелку на бумажные полотенца после каждого шага стирки, чтобы удалить остаточный раствор.
- Добавьте 200 л блокирующего буфера на колодец к обеим пластинам, уплотня обе пластины клейкой пленкой и инкубину 2 ч на RT.
- Подготовка биологического образца
- Разбавить экстракты родного белка, полученные в конце шага 3, до соответствующей концентрации с помощью PBS. Рекомендуемая концентрация будет варьироваться в зависимости от уровня экспрессии КДМ1А в биологическом образце. Примерами соответствующих диапазонов являются (1) клеточные гранулы: 0,5 - 10 мкг на скважину. (2) PBMCs: 5 - 30 мкг на скважину. (3) Пульверизованная ткань (мозг, легкие, кожа): 20 - 100 мкг на скважину. Держите образцы на льду во время подготовки. Когда это возможно, запустите технический анализ тройного образца.
- Подготовьте стандартную кривую с помощью человеческого rKDM1A:
- Для подготовки рабочего решения KDM1A Standard, пайпт соответствующий объем rKDM1A для окончательной концентрации 25 пг/ Л, добавить 75 л из 2 ММ OG-881, и в комплекте с 1 х PBS в общей объеме 6 мл в 15 мл сокола трубки. Держите стандартное решение KDM1A на льду в течение 1 ч и аккуратно перемешайте раствор, инвертируя соколиную трубку 15 мл несколько раз каждые 20 минут.
- Подготовка KDM1A Стандартная серия разбавления в 1,5 мл микроцентрифуговых труб в соответствии с таблицей 1 (Стандартная подготовка), в объеме достаточно для тройного анализа двух 96 хорошо микротитер пластин.
| СТАНДАРТНАЯ СЕРИЯ | Стандартное рабочее решение KDM1A (Зл) | |
| (pg KDM1A/well) | PBS (КЛ) | |
| 2500 за C- | 800 | - |
| 2500 г. | 800 | - |
| 1750 год | 560 г. | 240 г. |
| 1250 г. | 400 | 400 |
| 750 г. | 240 г. | 560 г. |
| 250 г. | 80 | 720 г. |
| 25 | 8 | 792 год |
| 0.00 | 0.00 | 800 |
| Примечание: | ||
| (1) Объем подготовлен каждого разбавления достаточно, чтобы работать в тройной 2 пластины асссе. | ||
| (2) Рекомендуемый диапазон составляет от 2,5 до 5000 пг / хорошо | ||
| Для отрицательного контроля C-, без антитела обнаружения KDM1A | ||
Таблица 1: Стандартная подготовка. Для подготовки стандартной серии белка KDM1A, pipette указанные объемы KDM1A Стандартный рабочий раствор и PBS в восемь правильно помечены 1,5 мл микроцентрифуговых труб.
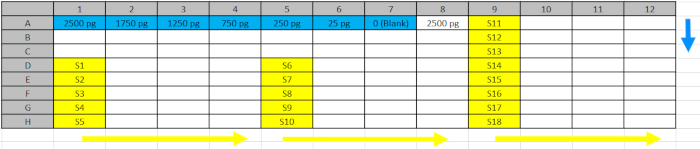
Таблица 2: Глубокий дизайн плиты. Стандарты (синий) и образцы (желтый) от шага 5.4.2. были пипсированы в отраженные позиции Deep Well Plate для облегчения загрузки в пластины ELISA по направлению синих (стандартных) и желтых (образцов) стрелок. Пожалуйста, нажмите здесь, чтобы загрузить этот файл.
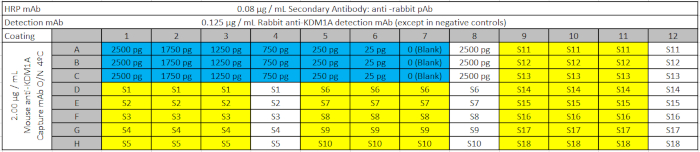
Таблица 3: Дизайн плиты ELISA. Пластина асссея включает стандартную кривую с уменьшением количества рекомбинантной цели KDM1A (синим цветом); биологические образцы (S) желтым цветом; и соответствующие отрицательные элементы управления (содержат образцы, но не первичное обнаружение антитела) в белом, которые будут загружены на пластины ELISA из Deep Well Plate. Пустой (0 в стандартной кривой) содержит все реагенты захвата и обнаружения, но не образец. Пожалуйста, нажмите здесь, чтобы загрузить этот файл.
- Элиза
- (Продолжение от шага 5.2.4.) После 2 ч инкубации отбросьте блокирующий буфер и промойте тарелки буфером для мытья.
- Перенесите надлежащим образом разбавленные образцы (экстракты родного белка и стандартная кривая от шага 5.3.) в охлажденный блок хранения 96 глубоких скважин после распределения пластин, показанного в таблице 2 (Deep Well Plate Design).
- Держите этот блок на льду до pipetting 100 л образца / хорошо в общей и бесплатной ELISA пластин после распределения пластин, показанных в таблице 3 (ELISA плиты дизайн).
- Инкубировать в течение 1 ч на RT, отбросить образцы и промыть пластины 5 раз с мытьем буфера.
- Приготовьте 20 мл антитела кобнаружению кролика против KDM1A при 0,125 мкг/мл в блокирующем буфере, добавьте 100 л л на колодец в каждой тарелке асссея, за исключением колодцев, соответствующих отрицательным элементам управления C-. Сверху запечатайте тарелку и насигните 1 ч на RT.
- Отбросьте раствор антитела обнаружения и промойте пластины 6 раз с помощью буфера для мытья.
- Приготовьте 25 мл вторичного козла анти-кроличьего антитела HRP к разбавлению 1:5,000 в блокирующем буфере, добавьте 100 л на колодец к пластинам микротитера; и инкубировать 1 ч на RT.
-
Обнаружение хемилюминесцентных
- 30 мин до конца шага 5.4.7. и при мягких легких условиях смешайте равные части раствора Luminol-Enhancer и Peroxide (10,5 мл: 10,5 мл, для 2 пластин) в янтарной бутылке и оставьте ее на RT.
ПРИМЕЧАНИЕ: Держите Luminol Рабочее решение в янтарной бутылке и избежать длительного воздействия любого интенсивного света. Краткосрочное воздействие типичного лабораторного освещения не повредит работающей работе. - По крайней мере 20 минут до измерения люминесценции, включите микроплиту читателя на 25 градусов по Цельсию и настроить считыватели до 1000 мс время интеграции и 150 мс урегулировать время. Параметры параметров могут потребовать оптимизации функции инструмента.
- После 1 ч инкубации в шаге 5.4.7., отбросить вторичный раствор антитела и промыть пластины 6 раз с мытьем буфера.
- Пипетка 100 л л на скважину рабочего раствора Люминола (Chemiluminescent Substrate), подготовленную в шаге 5.5.1. Пипетка очень медленно и избежать образования пузырьков. Используйте таймер, чтобы контролировать время между добавлением добавления раствора и измерения люминесценции пластин и держать это время постоянным для достижения хорошего межпромьчаемого воспроизводимости.
- Топ-печать пластин и центрифуги до 500 х г на RT для 45 с в тарелке центрифуги для устранения оставшихся пузырьков. Инкубировать тарелки в течение 1 мин на тарелку шейкер ажиотаж при 100 об/мин.
- Вставьте пластину внутри считывателя и оставьте его на 3 мин, чтобы стабилизировать температуру при температуре 25 градусов по Цельсию (без клейкой пленки). Всегда начинайте с бесплатной пластины ELISA.
- Прочитайте относительные единицы люминесценции (RLU) каждого анализа пластины ELISA (бесплатно и в общей сложности KDM1A).
- Сохранить и скопировать значения Raw RLU из файлов Raw Data Excel для дальнейшего анализа результатов.
- 30 мин до конца шага 5.4.7. и при мягких легких условиях смешайте равные части раствора Luminol-Enhancer и Peroxide (10,5 мл: 10,5 мл, для 2 пластин) в янтарной бутылке и оставьте ее на RT.
6. Расчет целевого участия
- В программном обеспечении электронной таблицы вычислите rLU Free и RLU Общие значения образцов SX и эталонных образцов REF (необработанные, транспортные средства или преддоза образец) из их технической репликации Сырье данных, как описано ниже:
- Введите отдельные данные Raw RLUi Total и Raw RLUi Free из пробелов, стандартной кривой, отрицательных элементов управления C- и биологических образцов (SX и REF) в таблицу данных анализа (например, Excel). Кроме того, введите суммы (в pg) KDM1A из стандартной кривой в таблице данных.
- Рассчитайте среднее rLU raw,стандартные отклонения и коэффициент вариации CVRLU от индивидуальных данных Raw Total и Raw Free RLUi для каждой технической точки обработки данных.
- Примените ликвидацию выброса (например, для тройных): для каждого отдельного Raw RLU Total и Raw RLU Free data point RLUi с технической точки данных тройни, примените критерии Grubbs, когда cv для тройного значения 0,15, и откажитесь от одного подозреваемого Сырье RLU значение Когда
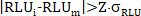 ,
,
в которой 1,148 евро для n no 3 и 90 % доверительного интервала (CI). - Если была применена ликвидация выброса, пересчет средней RLU Raw, стандартного отклоненияRLU и CVRLU от неотклоненых (nr) Raw RLUi Total и Raw RLUi Free значений для каждой точки данных.
- Примените фоновой коррекции: Рассчитайте средние значения RLU Free и RLU Total для каждого стандартного образца, а каждый образец SX и эталонный образец REF:


- Графически представляют данные следующим образом:
- Участок RLUFree и RLUОбщие значения (Y-оси) по отношению к их идентификации образца (X-оси) в барном графике.
- Также участок значения RLU (Y-ось) стандартов в рассеивание сюжета относительно их количества пг белка rKDM1A (X-оси) для свободных и всего измерений, а также соответствующие линейные линии тренда и вычислить r2 (квадрат линейного корреляционный коэффициент) значения.
- Рассчитать целевое взаимодействие (TE); т.е. процентная доля KDM1A, связанного ингибитором KDM1A в каждом образце SX по отношению к эталонному образцу REF (необработанный, транспортный или преддоза образец) следующим образом:
- Рассчитайте соотношение R среднее RLU Free к общим значениям для образцов SX и REF по следующим причинам:

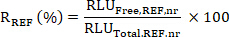
- Затем вычислите целевое участие (TE) образца SX по следующим образом:
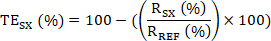
Необязательно: (1) Если N биологических повторений эксперименты были проведены, каждый с n технических реплик; сначала вычислить TESX для технических наборов репликации. Впоследствии вычислите средние значения TE, SD и CV для набора биологической репликации.
- Рассчитайте соотношение R среднее RLU Free к общим значениям для образцов SX и REF по следующим причинам:
- Пересмотреть ли критерии принятия ассеидов выполнены: Проверить, что (1) ассеа фон является приемлемым и среднее пустое lt; 0,05 х 107 RLU; (2) образец автолюминесценции отсутствует, и RLUs отрицательных элементов управления C- находятся ниже Нижнего предела количественной оценки (LLO) - Средний пустой й 10x SD); (3) стандартная кривая rKDM1A линейная и r2 0,98; (4) биологические образцы имеют значения RLU, которые попадают в динамический и линейный диапазон асссеа, т.е. между LLO и 2500 пг/хорошо.
ПРИМЕЧАНИЕ: Шаги 6.1. до 6,4. может быть легко автоматизирован в таблице данных исчисления. - Экспорт данных TE в открытый исходный код или коммерчески полученное статистическое программное обеспечение по выбору для графического представления значений Т и дополнительных статистических оценок.
Access restricted. Please log in or start a trial to view this content.
Результаты
Линейность определения Total и Free KDM1A.
Стандартная серия была подготовлена, как описано в шаге 5.3.2., используя от 0 до 2500 пг полнометражного человеческого рекомбинантного фермента KDM1A. Значения RLU Total и Free rKDM1A были оценены для провер...
Access restricted. Please log in or start a trial to view this content.
Обсуждение
Представленный здесь протокол был разработан для непосредственного измерения целевого взаимодействия KDM1A с помощью нового хемозонда KDM1A, основанного на ELISA. Метод был проверен на культивированных человеческих клеточных линий и ex vivo образцов из человека, крысы и мыши и бабуина (в том чи?...
Access restricted. Please log in or start a trial to view this content.
Раскрытие информации
Автор Тамара Маес является исполнительным директором и акционером, а авторы Кристина Маскаре и Ракель Руис Родригес являются сотрудниками Oryzon Genomics S.A. Oryzon Genomics S.A. разрабатывает ингибиторы KDM1A и имеет патенты, охватывающие соединения и методы, используемые в этой статье.
Благодарности
Это исследование было профинансировано Oryzon Genomics. S.A., Hoffman-La Roche, и частично поддерживается CIIP-20152001 и RETOS программы сотрудничества RTC-2015-3332-1.
Access restricted. Please log in or start a trial to view this content.
Материалы
| Name | Company | Catalog Number | Comments |
| 0,05% Trypsin-EDTA (1X) | Thermo Scientific | #25300-062 | |
| 10 X Protease Inhibitor Tablets | Roche | #11836153001 | |
| 96 deep well storage block | VWR | #734-1679 | |
| 96 well ELISA plates | Nunc | #436110 | |
| Adhesive black Film | Perkin Elmer | #6050173 | |
| Adhesive transparent Film | VWR | #60941-062 | |
| Biotinylated KDM1A probe OG-881 | Oryzon Genomics S.A. | NA | |
| Bovine Serum Albumin | Sigma | # 3117057001 | |
| Bovine Serum Albumin Standard | Thermo Scientific | #23208) | |
| Bradford Protein Assay | BioRad | #500-0001 | |
| Cell lysis buffer 10X | Cell Signaling | #9803 | |
| Centrifuge for 96- well plates | Hettich | Rotina 420R | |
| Flask | Thermo Scientific | #156499 | |
| Full length, enzymatically active human Recombinant LSD1 / KDM1A | Active Motif | #31426 | |
| Graphpad Prism 5 Project | GraphPad Software | NA | |
| Luminol-Enhacer and Peroxide Solution (Chemiluminescent Substrate) | Thermo Scientific | #37074 | |
| Micro Centrifuge | Eppendorf | 5415 R | |
| Microplate reader Infinite 200-Tecan | Tecan | Infinite 200 | |
| Mouse monoclonal capture antibody Anti-KDM1A (N-terminal epitope) | Abcam | #ab53269 | |
| Needle G18 gauge blunt | BD | #303129 | |
| ORY-1001 (iadademstat) | Oryzon Genomics S.A. | NA | |
| PBMC separation tubes 10 ml | Greiner bio-one | #163288 | |
| PBMC separation tubes 50 ml | Greiner bio-one | #227288 | |
| PBS 1x | Sigma | #D8537 | |
| Plate shaker | Heidolph Instruments | Rotamax 120 | |
| Polysorbate 20 | Sigma | #P7949 | |
| Rabbit monoclonal detection antibody Anti-KDM1A (C-terminal epitope) | Cell Signaling | #672184BF-100 | |
| Secondary antibody Peroxidase-conjugated Donkey Anti-rabbit IgG | Thermo Scientific | #31458 | |
| Spectrophotometer cuvette 1.5 | Deltalab | #302100 | |
| Spectrophotometer for cuvette | GE Healthcare | GeneQuant 1300 | |
| Streptavidin | Promega | #Z704A | |
| Syringe | BD | #303172 | |
| Type 1 ultrapure water | Millipore | Milli-Q Advantage A10 | |
| Ultrasonic cleaner | VWR | USC200T |
Ссылки
- Shi, Y. Histone demethylation mediated by the nuclear amine oxidase homolog LSD1. Cell. 119 (7), 941-953 (2004).
- Maiques-Diaz, A., Somervaille, T. C. LSD1: biologic roles and therapeutic targeting. Epigenomics. 8 (8), 1103-1116 (2016).
- Maes, T. ORY-1001, a Potent and Selective Covalent KDM1A Inhibitor, for the Treatment of Acute Leukemia. Cancer Cell. 33 (3), 495-511 (2018).
- Sugino, N. A novel LSD1 inhibitor NCD38 ameliorates MDS-related leukemia with complex karyotype by attenuating leukemia programs via activating super-enhancers. Leukemia. 31 (11), 2303-2314 (2017).
- Kleppe, M., Shank, K., Efthymia, P., Riehnhoff, H., Levine, R. L. Lysine-Specific Histone Demethylase, LSD1, (KDM1A) As a Novel Therapeutic Target in Myeloproliferative Neoplasms. Blood. 126, 601(2015).
- Jutzi, J. S., et al. LSD1 Inhibition Prolongs Survival in Mouse Models of MPN by Selectively Targeting the Disease Clone. HemaSphere. 2 (3), 54(2018).
- Mohammad, H. P. DNA Hypomethylation Signature Predicts Antitumor Activity of LSD1 Inhibitors in SCLC. Cancer Cell. 28 (1), 57-69 (2015).
- Rivers, A., et al. RN-1, a potent and selective lysine-specific demethylase 1 inhibitor, increases γ-globin expression, F reticulocytes, and F cells in a sickle cell disease mouse model. Experimental Hematology. 43 (7), 546-553 (2015).
- Rivers, A. Oral administration of the LSD1 inhibitor ORY-3001 increases fetal hemoglobin in sickle cell mice and baboons. Experimental Hematology. 67, 60-64 (2018).
- Buesa, C., et al. The dual LSD1/MAO-B inhibitor ORY-2001 prevents the development of the memory deficit in samp8 mice through induction of neuronal plasticity and reduction of neuroinflammation. Alzheimer’s & Dementia. 11 (7), P905(2015).
- Schmidt, D. M., McCafferty, D. G. Trans-2-Phenylcyclopropylamine is a mechanism-based inactivator of the histone demethylase LSD1. Biochemistry. 46 (14), 4408-4416 (2007).
- Forneris, F., Binda, C., Vanoni, M. A., Battaglioli, E., Mattevi, A. Human histone demethylase LSD1 reads the histone code. Journal of Biological Chemistry. 280 (50), 41360-41365 (2005).
- Oryzon Genomics, Methods to determine kdm1a target engagement and chemoprobes useful therefor. , WO2017158136 (2016).
- Mascaró, C., Ortega, A., Carceller, E., Rruiz Rodriguez, R., Cicero, F., Lunardi, S., Yu, L., Hilbert, M., Maes, T. Chemoprobe-based assays of histone lysine demethylase 1A target occupation enable in vivo pharmacokinetics and -dynamics studies of KDM1A inhibitors. Journal of Biological Chemistry. , In Press (2019).
- Rodriguez-Suarez, R. Development of Homogeneous Nonradioactive Methyltransferase and Demethylase Assays Targeting Histone H3 Lysine 4. Journal of Biomolecular Screening. 17 (1), 49-58 (2011).
- Lynch, J. T., Cockerill, M. J., Hitchin, J. R., Wiseman, D. H., Somervaille, T. C. CD86 expression as a surrogate cellular biomarker for pharmacological inhibition of the histone demethylase lysine-specific demethylase 1. Analytical Biochemistry. 442 (1), 104-106 (2013).
- Schulz-Fincke, J. Structure-activity studies on N-Substituted tranylcypromine derivatives lead to selective inhibitors of lysine specific demethylase 1 (LSD1) and potent inducers of leukemic cell differentiation. European Journal of Medicinal Chemistry. 144, 52-67 (2018).
- Ishii, T., et al. CETSA quantitatively verifies in vivo target engagement of novel RIPK1 inhibitors in various biospecimens. Scientific Report. 7, 13000(2017).
- Maes, T. ORY-2001: An Epigenetic drug for the treatment of cognition defects in Alzheimer’s disease and other neurodegenerative disorders. Alzheimer’s & Dementia. 12 (7), P1192(2017).
Access restricted. Please log in or start a trial to view this content.
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены