Method Article
Сбор и обработка данных нейтронной кристаллографии для моделирования атомов водорода в белковых структурах
В этой статье
Резюме
Кристаллография нейтронного белка является структурным методом, который позволяет локализовать атомы водорода, тем самым обеспечивая важные механистические детали функции белка. Здесь представлен рабочий процесс монтажа кристалла белка, сбор данных о дифракции нейтронов, уточнение структуры и анализ карт плотности длин рассеяния нейтронов.
Аннотация
Нейтронная кристаллография - это структурный метод, который позволяет определять положения атомов водорода в биологических макромолекулах, давая механистически важную информацию о состояниях протонации и гидратации, не вызывая радиационного повреждения. Рентгеновская дифракция, напротив, дает лишь ограниченную информацию о положении атомов света, а рентгеновский пучок быстро индуцирует радиационное повреждение светочувствительных кофакторов и металлических центров. Здесь представлен рабочий процесс, используемый для лучевых линий IMAGINE и MaNDi в Национальной лаборатории Оук-Ридж (ORNL) для получения структуры дифракции нейтронов после выращивания кристалла белка подходящего размера (> 0,1 мм3). Показано монтирование гидрогенизированных кристаллов белка в кварцевых капиллярах для сбора данных о нейтронной дифракции. Также представлен процесс парообмена смонтированных кристаллов с D2O-содержащим буфером для обеспечения замещения атомов водорода в обменных местах дейтерием. Включение дейтерия уменьшает фон, возникающий в результате некогерентного рассеяния атомов водорода, и предотвращает подавление плотности, вызванное их отрицательной когерентной длиной рассеяния. Стратегии выравнивания образцов и сбора данных о комнатной температуре иллюстрируются с использованием квази-Лауэ сбора данных в IMAGINE на изотопном реакторе с высоким потоком (HFIR). Кроме того, установка кристаллов и быстрое замораживание в жидком азоте для сбора криоданных для улавливания промежуточных продуктов лабильной реакции демонстрируется на приборе MaNDi по времени пролета в источнике нейтронов spallation (SNS). Также будет рассмотрен вопрос о подготовке файлов координатных и дифракционных данных модели и визуализации карт плотности плотности рассеяния нейтронов (SLD). Наконец, будет обсуждаться уточнение структуры по нейтронным данным только или по совместным рентгеновским/нейтронным данным для получения полноатомной структуры интересующего белка. Процесс определения нейтронной структуры будет продемонстрирован с использованием кристаллов литического полисахарида монооксигеназы Neurospora crassa LPMO9D, медьсодержащего металлопротеина, участвующего в деградации непокорных полисахаридов посредством окислительного расщепления гликозидной связи.
Введение
Нейтронная макромолекулярная кристаллография - это метод, который обеспечивает уникальное окно в структуру и основную химию белков. Концептуально похожая на рентгеновскую дифракцию, нейтронная дифракция обеспечивает атомистические детали макромолекулярной структуры, однако взаимодействие нейтронов с ядрами позволяет локализовать атомы света, которые часто трудно обнаружить при рентгеновской дифракции1. Во время дифракции рентгеновских лучей рентгеновские лучи рассеиваются из электронного облака, делая легкие атомы, такие как водород (H), плохо видимыми на картах электронной плотности, которые не имеют почти суб-Ångström разрешения2. Напротив, интенсивность рассеяния нейтронов зависит от сложных взаимодействий с ядром, при этом изотопы одного и того же элемента демонстрируют разную длину рассеяния. Таким образом, легкие атомы и их изотопы, такие как водород (1H) и дейтерий (2H или D), имеют сопоставимую видимость с основными атомами углерода, азота и кислорода в картах плотности рассеяния нейтронов (SLD). Кроме того, поскольку величина рассеяния нейтронов не зависит от количества электронов, рассеяние от легких элементов не затемняется тяжелыми элементами, когда они находятся в непосредственной близости друг от друга, как это наблюдается при рентгеновском рассеянии. Улучшенная видимость H и его изотопа D при использовании нейтронной дифракции дает ценную информацию о состоянии протонирования каталитически важных остатков, кофакторов и лигандов и облегчает ориентацию молекул воды, раскрывая важную информацию о каталитических механизмах и химии белка3. Нейтронная дифракция также предлагает преимущество в том, что она является неразрушающей техникой, особенно подходящей для биологических образцов, чувствительных к ионизации, таких как белки с металлическими центрами или светочувствительные окислительно-восстановительные кофакторы2. Основное внимание в этой статье уделяется обзору рабочего процесса для получения высококачественной кристаллической структуры нейтронного белка. Мы отсылаем заинтересованного читателя к Podjarny et al.4, Blakeley5, Blakeley et al.6 и O'Dell et al.3 для отличного обзора дифракции нейтронного белка и Ashkar et al.7 для дальнейшего применения рассеяния нейтронов.
Нейтроны в основном образуются в ходе ядерных реакций с использованием одного из двух процессов: ядерного деления в реакторных источниках или расщепления в ускорительных источниках8. Реакторные источники обеспечивают непрерывный пучок нейтронов, используя ядерное деление изотопа 235U, в то время как спальтационные источники нейтронов производят импульсный пучок нейтронов, бомбардируя мишень, например жидкий металл, такой как ртуть, протонами9. Национальная лаборатория Оук-Ридж (ORNL) в Оук-Ридже, штат Теннесси, содержит как стационарный источник нейтронов в изотопном реакторе с высоким потоком (HFIR), так и импульсный источник 60 Гц в источнике нейтронов сползания (SNS). Лучевая линия IMAGINE, расположенная в HFIR, представляет собой нейтронный дифрактометр, оптимизированный для биологических макромолекул (дополнительный рисунок 1)10. IMAGINE использует детектор нейтронных изображений для измерения квази-лауэских данных с использованием узкой полосы пропускания в диапазоне 2,8 – 4,5 Å от монокристаллов с единичными краями ячейки <150 Å. Макромолекулярный нейтронный дифрактометр (MaNDi), расположенный в SNS, представляет собой нейтронный дифрактометр времени пролета (TOF) Лауэ, оснащенный сферической системой детекторной решетки (DAF) (дополнительный рисунок 2)11. MaNDi измеряет данные от монокристаллов с краями элементных ячеек в диапазоне 10 – 300 Å, используя перестраиваемую полосу пропускания 2 Å-длин волны между 2,0 – 6,0 Å12.
Процесс генерации нейтронов является высокоэнергоемким, что приводит к относительно слабым потокам пучка нейтронов при контрастировании с потоками рентгеновского пучка на источниках синхротронов13. Для обеспечения достаточного соотношения сигнал/шум при сборе данных необходимо выращивать кристаллы подходящего размера и качества14. Как правило, кристаллы с объемами > 0,1 мм3 нужны для сбора данных с адекватной статистикой15. В дополнение к более низким потокам необходимо учитывать неотъемлемые свойства взаимодействия между нейтронами и ядрами образца16. Длина рассеяния нейтронов различается для изотопов одного и того же элемента, свойство, которое может быть выгодно использовано в рассеянии нейтронов под малым углом (SANS) для маскировки или выделения областей образца - процесс, известный как контрастное сопоставление17. В дифракционных экспериментах длина отрицательного когерентного рассеяния нейтронов H (-3,741 fm для 1H) может привести к подавлению характеристик карты плотности рассеяния нейтронов, поскольку длина рассеяния когерентных нейтронов других биологически значимых атомов, включая углерод (6,6511 fm для 12C), азот (9,37 fm для 14N), кислород (5,803 fm для 16O), фосфор (5,13 fm для 31P) и сера (2,804 fm для 32S), являются положительными (таблица 1)12,14. Кроме того, большая некогерентная длина рассеяния H (25,274 fm) увеличивает фон во время сбора данных, затрудняя качество набора данных и ставя под угрозу разрешение данных7. Чтобы обойти эти ограничения, введенные H, необходимо для дифракции нейтронов обменять H на его изотоп дейтерия, 2H(D), который имеет положительную длину когерентного рассеяния нейтронов (6,671 fm) и значительно меньшую длину некогерентного рассеяния (4,04 fm)19. Это может быть достигнуто путем пердеутерации, процесса, в котором белок экспрессируется организмами, выращенными в полностью дейтерированных средах, обеспечивая полное включение D в H-участки20. Также возможно частично дейтерировать белок, заменив H на D исключительно на обменных участках (титруемых группах), в то время как необменяемые углерод-связанные участки остаются гидрированными21. Это может быть достигнуто путем роста гидрогенизированных кристаллов белка в дейтерированном материнском ликворе22. Однако чаще всего H/D обмен гидрогенизированных белков осуществляется путем парообмена после роста достаточно крупных кристаллов в буфере на основе H2O23. В таких случаях кристаллы устанавливаются в кварцевый капилляр и уравновешиваются парами материнским щелоком на основе D20.
Ограниченные потоки нейтронов в источниках нейтронов приводят к увеличению времени сбора данных, от нескольких дней до нескольких недель24. В ORNL и IMAGINE, и MaNDi используют узкую полосу пропускания длин волн в диапазоне 2–6 Å для оптимизации сбора данных25. Данные могут собираться при комнатной температуре или при криотемпературе. Сбор криозданных может потенциально улучшить качество данных и открывает возможность для замораживания каталитических промежуточных продуктов. После сбора данных о нейтронной дифракции набор рентгеновских данных обычно собирается на одном кристалле при той же температуре или на кристалле, выращенном в идентичных условиях26. Сбор данных при одинаковой температуре позволяет выполнять уточнение структуры как по рентгеновским, так и по нейтронным данным, предотвращая любые потенциальные артефакты, вызванные температурой, такие как изменения видимости и положения вод или заполнение остатков с альтернативными конформациями27. Совместная уточнение рентгеновских нейтронных данных увеличивает отношение данных к параметрам и обеспечивает преимущество, позволяющее уточнять координаты белковой магистрали по сравнению с данными рентгеновского излучения, в то время как данные дифракции нейтронов используются для уточнения положения атомов H/D28. Это особенно полезно при использовании частично дейтерированных образцов, где присутствует подавление плотности из-за атомов Н в необменяемых участках белка. Хотя количество рентгеновских структур намного превышает количество нейтронных структур, депонированных в Банке белковых данных (PDB), пакеты программного обеспечения, первоначально предназначенные для уточнения рентгеновских данных, были расширены, чтобы охватить нейтронные данные, а также 3,29,30. После сбора данных модели могут быть уточнены с использованием пакетов уточнения, таких как phenix.refine, CNSsolve (nCNS) или SHELXL28,31,32,33. В процессе уточнения карты плотности рассеяния нейтронов могут быть визуализированы для ручной установки с использованием COOT34. Следуя структурному решению, координаты и файлы данных нейтронной и/или рентгеновской дифракции могут быть представлены в PDB, который проверит и депонирует модель, сделав ее доступной для публичного доступа18,29,30.
Структурный анализ белков представляет собой многогранный подход, в котором используются многочисленные методы для исследования их функции и механизма35. Кристаллография нейтронного белка дает ценную химическую информацию для расширения и дополнения результатов дополнительных исследований, таких как рентгеновская дифракция, спектроскопия, ядерный магнитный резонанс (ЯМР) или микрокристаллическая дифракция электронов (microED)36. Дифракция нейтронного белка обладает уникальными возможностями для понимания ферментативных механизмов, поскольку атомы H занимают центральное место в их химии. Отсутствие радиационных повреждений, индуцированных нейтронами, делают их зондом, исключительно подходящим для изучения металлопротеинов37. Здесь мы представляем репрезентативный пример процесса дифракции нейтронного белка от подготовки образца до сбора, уточнения и анализа данных (рисунок 1). Кристаллы достаточного размера для экспериментов по дифракции нейтронов были выращены из металлопротеина Neurospora crassa LPMO9D (NcLPMO9D). Nc LPMO9D представляет собой медьсодержащий металлопротеин, участвующий в деградации непокорной целлюлозы путем введения атома кислорода в гликозидную связь38,39. Активный сайт NcLPMO9D содержит мононуклеарный медный центр в характерной «гистидин-скобке», состоящей из N-концевого гистидина и второго законсервированного гистидина (дополнительный рисунок 3)40. N-терминал грибковых ЛПМО метилирован, но постпереходная модификация не происходит во время рекомбинантной экспрессии в дрожжах. В состоянии покоя NcLPMO9D медный центр присутствует в состоянии окисления Cu2+ и активируется восстановлением одиночных электронов до Cu1+, что позволяет молекулярному кислороду связываться и активироваться путем быстрого восстановления до супероксидных частиц41,42. Общая реакция NcLPMO9D требует дальнейшего добавления одного электрона и двух протонов для образования гидроксилированного полисахаридного продукта43. Идентичность активированных форм кислорода, ответственных за абстракцию атомов водорода (HAA), из полисахаридной подложки не была идентифицирована, и в настоящее время продолжаются интенсивные структурные и вычислительные исследования44,45. Учитывая окислительно-восстановительную химию на активном объекте NcLPMO9D, смягчение радиационного ущерба особенно актуально. Здесь мы проиллюстрировали сбор данных о комнатной температуре и криомпературе на кристаллах NcLPMO9D для определения структуры NcLPMO9D в состоянии покоя и в активированном восстановленном виде соответственно46. Особое внимание будет уделяться монтажу кристаллов белка, настройке прибора лучевой линии для сбора данных, подготовке данных и файлов координат, а также этапам уточнения, необходимым для моделирования полноатомной нейтронной структуры.
протокол
1. Оценка размера кристалла
- Измерьте размер кристаллов с помощью микроскопа, оснащенного нормальным и поляризованным светом. Выберите кристаллы с минимальным объемом ~0,1 мм3 (дополнительный рисунок 4).
- Маркируйте скважины с достаточно крупными кристаллами и отмечайте условия кристаллизации, используемые для генерации этих кристаллов.
2. Подготовка дейтерированного кристаллизационного буфера
- Растворите компоненты кристаллизационного буфера в D2O для создания дейтерированного буфера кристаллизации.
- Отрегулируйте pH буфера, вычислив pD решения с помощью следующего уравнения:
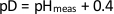 (1)
(1)
где pHmeas - pH, измеренный стандартным стеклянным электродом. Первоначальный pH буфера кристаллизации NcLPMO9D составлял 6,0, поэтому мы будем использовать pHmeas 5,6 для дейтерированного буфера кристаллизации при pD 6,0. - Погрузите электрод рН-метра в D2O на десять минут перед использованием (дополнительный рисунок 5).
- Отрегулируйте pHmeas до 5,6 с помощью основания NaOD или кислоты DCl.
3. Сбор кристаллов
- Поместите силиконизированные круглые стеклянные слайды диаметром 22 мм рядом с кристаллизационным лотком, из которого будут собираться кристаллы. Используйте чистый стеклянный слайд на кристалл (рисунок 2A).
- Откройте запечатанную сэндвич-коробку, содержащую кристаллы белка, в 9-луночной силиконизированной стеклянной пластине большого объема.
- Удалите 10-20 мкл из кристаллизационного резервуарного раствора с помощью микропипетки и поместите раствор на стеклянный слайд (рисунок 2B).
- Соберите кристалл с помощью микролупа соответствующего размера и поместите кристалл в резервуарную каплю раствора на стеклянную горку, чтобы удалить мусор, который часто собирают вместе с кристаллом (рисунок 2C и рисунок 2D).
ПРИМЕЧАНИЕ: Необходимо будет работать быстро, так как капли малого объема могут испаряться. Собранные кристаллы также подвержены риску высыхания при воздействии атмосферы. Возможно, потребуется добавить некоторый резервуарный раствор к белковой капле, чтобы предотвратить высыхание кристаллов в небольших кристаллизационных каплях.
4. Хрустальный монтаж
ПРИМЕЧАНИЕ: Протоколы капиллярного монтажа варьируются в зависимости от предпочтений экспериментаторов. Чтобы предотвратить повреждение кристаллов, капилляры, которые необходимо укоротить, должны быть забиты режущим камнем или наждачной бумагой, чтобы обеспечить плавный разрыв.
- Заполните один конец кварцевого капилляра диаметром 2 мм длиной 50 мм резервуарным буфером путем капиллярного действия или путем непосредственного пипетирования ~10 мкл резервуарного буфера в капилляр (рисунок 3A).
ПРИМЕЧАНИЕ: Пользователям рекомендуется использовать кварцевые капиллярные трубки, поскольку, помимо их механической прочности, важно ограничить поглощение пучка нейтронов и снизить фоновые вклады капилляра. Стеклянные капилляры вносят высокий фон и поглощают нейтроны, снижая качество данных. - Аккуратно поместите кристалл в резервуарный буфер в кварцевом капилляре с помощью монтажной петли (рисунок 3B и рисунок 3C).
- Осторожно постучите по трубке, чтобы переместить резервуарный буфер и погруженный в него кристалл вниз по капилляру (рисунок 3D).
- Поместите кристалл не ближе 13,5 мм и не более чем на 27,5 мм от одного конца капилляра; это будет монтажный конец (дополнительный рисунок 6).
- Аспирируйте буферный раствор вокруг кристалла, используя длинный тонкий наконечник пипетки, оставляя кристалл слегка влажным. Не прикасайтесь к кристаллу (дополнительный рисунок 7А).
- Высушите стенки капилляров тонким бумажным фитилем (дополнительный рисунок 7B).
- Пипетка 20-50 мкл дейтерированного буферного раствора в конец капилляра напротив монтажного конца (рисунок 4А).
- Расплавите пчелиный воск тепловой «палочкой» и аккуратно вставьте капилляр в этот расплавленный пчелиный воск. Повторяйте до тех пор, пока не образуется герметичное уплотнение (рисунок 4B и рисунок 4C).
- Пипетка очень небольшого количества дейтерированного буфера, примерно 5 мкл в монтажном конце капилляра, чтобы действовать как «радиатор» для горячего пчелиного воска. Окуните этот конец в расплавленный пчелиный воск, чтобы создать герметичное уплотнение, как описано ранее, чтобы сформировать капилляр, герметизированный на обоих концах (рисунок 4D).
- Осмотрите установленный кристалл с помощью микроскопа после установки, чтобы обеспечить герметичность (рисунок 4E).
- Тщательно закрепите установленные кристаллы салфетками Kim в контейнере, таком как 15-мл Falcon tube или Petri Dish, и храните горизонтально при температуре, при которой кристаллы были выращены (рисунок 4F).
5. Парообмен
- Замените дейтерированный буфер на свежий буфер через два дня после монтажа кристалла.
- Расплавьте восковую печать дальше всего от кристалла с помощью нагревательной петли и используйте пипетку и бумажные фитили, чтобы удалить буфер.
- Залейте капилляр 20-50 мкл дейтерированного буферного раствора и запечатайте воском.
- Повторите замену дейтерированного буфера еще дважды с интервалом в четыре дня, чтобы убедиться, что обмен дейтерированным буферным паром завершен и позволяет парообмен в течение не менее двух недель.
6. Дифракция нейтронного белка
ПРИМЕЧАНИЕ: Читателям, заинтересованным в особенностях линии луча IMAGINE, рекомендуется обратиться к Meilleur et al. 2013, Meilleur et al. 201810,47.
- Сбор данных о комнатной температуре на линии луча IMAGINE в HFIR
- Монтаж образцов
- Закрепите капиллярный кристалл на гониометре шпаклевкой.
- Установите гониометр на палочку образца и центрируйте кристалл в луче с помощью автономной станции выравнивания.
- Закрепите рукоятку образца на сцене образца прибора (дополнительный рисунок 1В).
- Убедитесь, что экспериментальная хижина освобождена, и откройте затвор лучевой линии для сбора нейтронных данных.
- Сбор данных
- Откройте программу сбора данных на компьютере управления линией луча и перейдите на вкладку Настройка , чтобы настроить стратегию сбора данных. В разделе Параметры эксперимента введите имя образца рядом с полем Имя образца и введите номер предложения рядом с полем Предложение. В разделе Именование изображений выберите Шаблон папки и задайте место назначения для сохраненных полученных данных, а затем выберите Префикс изображения и введите соответствующее имя кадра (дополнительный рисунок 8).
- Откройте графический интерфейс Optics и нажмите 2,78 для λmin и 4,78 для λmax , чтобы установить квази-Laue диапазон для сбора данных (дополнительный рисунок 9).
- Переключитесь на вкладку Сбор и в разделе Параметры следующего сканирования вставьте время экспозиции в секундах в поле Экспозиция, количество кадров в разделе N кадров и углы сбора данных в разделе Δ φ/кадр. Назовите кадр, который будет собираться, в поле Image Prefix и начните сбор данных, нажав кнопку Start Scan (дополнительный рисунок 10).
- Дифрагированные нейтроны будут обнаружены детектором имиджевых пластин. В конце каждой экспозиции будет считываться пластина изображения и отображаться рисунок на графическом интерфейсе сбора данных (дополнительный рисунок 11).
- Кадры индексируются, интегрируются, нормируются по длине волны и масштабируются с использованием Lauegen, Lscale50 и Scala ответственным ученым по лучевой линии, который предоставит пользователю объединенный файл отражения после сбора данных (дополнительный рисунок 12).
ПРИМЕЧАНИЕ: Сбор данных как в IMAGINE, так и в MaNDi будет осуществляться в квазилауэ-режиме с использованием методологии и программного обеспечения, разработанных для сбора дифракционных данных Лауэ, как это было разработано Helliwell et al.48 и Nieh et al.49. - Сбор соответствующего набора рентгеновских данных на том же кристалле при той же температуре после сбора данных о нейтронной дифракции (дополнительный рисунок 13).
ПРИМЕЧАНИЕ: Кристалл, выращенный из той же капли или в тех же условиях кристаллизации, также может быть использован для сбора данных рентгеновской дифракции для совместного нейтронно-рентгеновского уточнения.
- Монтаж образцов
- Сбор криозданных на лучевой линии MaNDi в социальных сетях
ПРИМЕЧАНИЕ: Читателям, заинтересованным в особенностях линии луча, рекомендуется проконсультироваться с Coates et al. (2015), Meilleur et al. 201810,11.- Монтаж образцов
- Приготовьте раствор для замачивания дейтерированного аскорбата для восстановления кристаллов и дейтерированного криопротектора. Поместите 20 мкл капель каждого из этих растворов в сидячие лунки в кристаллизационной пластине.
ПРИМЕЧАНИЕ: Раствор криопротектора обычно является криопротектором, который доказал свою эффективность для сбора криомпературных рентгеновских дифракционных данных, приготовленных в D2O. Этот криопротектор может быть дополнительно оптимизирован (например, концентрация) для сбора нейтронных данных, если это необходимо. - Выберите петли для монтажа образца и прикрепите их к магнитному крио-основанию в соответствии с рекомендациями MaNDi (дополнительный рисунок 14).
- Наполните пену крио-Дьюара жидким азотом. Поместите металлическую криозащитную втулку в жидкий азот для охлаждения (дополнительный рисунок 15А).
- Снимите восковые пробки с обоих концов капилляра и постучите по капилляру, чтобы переместить буферную пробку так, чтобы установленный кристалл был погружен в буфер. Вымойте кристалл в 20 мкл раствора капли в сидячем капельном колодце (дополнительный рисунок 15B и дополнительный рисунок 15C).
ПРИМЕЧАНИЕ: Этот этап не требуется, если H/D обмен был выполнен путем уравновешивания капель кристаллизации против дейтерированного буфера или путем прямого замачивания кристалла в дейтерированном буфере. - Погрузите кристалл в раствор для замачивания аскорбата на два часа. Установите кристалл в микротрубрику, прикрепленную к магнитному криоосновну. Погрузите установленный кристалл в криопротектор на 10 секунд и погрузите кристалл и криомонтаж в жидкий азот для замораживания (дополнительный рисунок 15D).
- После замораживания кристалла используйте предварительно охлажденный криоконтафтовый щипц и установите кристалл на ступень образца MaNDi, оснащенную криопотоком. Осторожно откройте криоконтафтовый щипц и убедитесь, что кристалл остается в криотоке (дополнительный рисунок 2C).
- Приготовьте раствор для замачивания дейтерированного аскорбата для восстановления кристаллов и дейтерированного криопротектора. Поместите 20 мкл капель каждого из этих растворов в сидячие лунки в кристаллизационной пластине.
- Сбор данных
- Откройте программное обеспечение для сбора данных, в котором информация об эксперименте будет заполняться автоматически.
- Нажмите на центр кристалла, чтобы центрировать его с помощью управляемого компьютером гониометра (дополнительный рисунок 16).
- В разделе Таблица настройте стратегию сбора данных, введя углы сбора данных под "phi", а также общую экспозицию пучка нейтронов на кадр в поле Value (Дополнительный рисунок 17).
- Нажмите кнопку Отправить , чтобы начать сбор данных.
- По мере сбора данных будут видны дифрагированные нейтроны (дополнительный рисунок 17). Дифракционные пятна станут более четкими по мере увеличения времени экспозиции, улучшая отношение сигнал/шум (рисунок 5).
- Кадры будут индексироваться, интегрироваться, нормироваться и масштабироваться с использованием Mantid и Lauenorm ответственным ученым по линии луча, который предоставит пользователю объединенный файл интенсивности после сбора данных51.
- Монтаж образцов
7. Уточнение структуры
- Совместная уточнение рентгеновских и нейтронных данных
- Подготовка структуры
- Уточните рентгеновские данные для получения структуры белка с помощью программного пакета phenix.refine и Coot для ручного построения для получения завершенной структуры.
- Откройте CCP4 и выберите программу Convert to/modify/extend MTZ , чтобы сопоставить флаги данных нейтронных данных без R с флагами рентгеновских данных. Выберите для импорта файла отражения в формате MTZ . В разделе В загрузите полученный нейтронный MTZ-файл и загрузите рентгеновский mtz-файл в разделе Импорт FreeR MTZ (Дополнительный рисунок 18). Присвойте имя новому MTZ-файлу в разделе Выход и нажмите кнопку Выполнить.
- Откройте пакет программного обеспечения Phenix и нажмите ReadySet в разделе Инструменты уточнения. Рядом с PDB-файлом загрузите файл координат PDB, уточненный по данным рентгеновского излучения. Выберите Добавить водород в модель, если он отсутствует , и выберите H/D на заменяемых участках, H в другом месте в раскрывающемся меню. Выберите Добавить дейтерий к молекулам растворителя и оставьте оставшиеся параметры на их значениях по умолчанию (дополнительный рисунок 19A).
ПРИМЕЧАНИЕ: Если используется пердойтерированный белок, выберите опцию Добавить водород в модель, если она отсутствует , и выберите H/D в обменных местах, D в другом месте.
- Уточнение структуры
- Откройте программу phenix.refine на вкладке Уточнение , чтобы настроить уточнение с использованием как рентгеновских, так и нейтронных данных. На вкладке Настройка во входных файлах введите PDB-файл из рентгеновской структуры, которая была обработана с помощью ReadySet, и необходимый файл CIF удерживает для любых соответствующих лигандов. Загрузите файл MTZ из нейтронных данных с флагами Rfree, назначенными с помощью CCP4, и назначьте его как «Нейтронные данные» и «Нейтрон R-свободный» под заголовком Тип данных. Загрузите файл MTZ из рентгеновских данных и назначьте его как «Рентгеновские данные» и «X-ray R-free» под заголовком Тип данных. Метки Space group и Data будут автоматически заполняться после загрузки данных (дополнительный рисунок 19B).
ПРИМЕЧАНИЕ: При выполнении уточнения и вводе информации о кристалле используйте единичную ячейку, определенную по рентгеновским данным. - На вкладке Настройка в параметрах Уточнения сохраните стандартную стратегию уточнения. Увеличение числа циклов до пяти (дополнительный рисунок 20)
- Выберите Все параметры, нажмите «Дополнительно» и выберите «Водороды...». Измените модель очистки водорода на индивидуальную и отключите Force riding adp (Дополнительный рисунок 20).
- Выберите Все параметры и откройте опцию Поиск параметров . Найдите слово ядерный и выберите Использовать ядерные расстояния для X-H/D (дополнительный рисунок 20).
- Выберите Выполнить , чтобы инициировать уточнение.
- Откройте программу phenix.refine на вкладке Уточнение , чтобы настроить уточнение с использованием как рентгеновских, так и нейтронных данных. На вкладке Настройка во входных файлах введите PDB-файл из рентгеновской структуры, которая была обработана с помощью ReadySet, и необходимый файл CIF удерживает для любых соответствующих лигандов. Загрузите файл MTZ из нейтронных данных с флагами Rfree, назначенными с помощью CCP4, и назначьте его как «Нейтронные данные» и «Нейтрон R-свободный» под заголовком Тип данных. Загрузите файл MTZ из рентгеновских данных и назначьте его как «Рентгеновские данные» и «X-ray R-free» под заголовком Тип данных. Метки Space group и Data будут автоматически заполняться после загрузки данных (дополнительный рисунок 19B).
- Модельное строительство
- После уточнения в Phenix нажмите «Открыть в Coot» на вкладке «Результаты», чтобы визуализировать карты электронной плотности рентгеновского излучения и SLD нейтронов. Перейдите на вкладку Display Manager и в разделе Maps нажмите удалить карту рядом с картами _neutron, чтобы удалить нейтронные карты (дополнительный рисунок 21). Нажмите файл > Открыть MTZ, mmCIF fcf или phs.... Выберите текущие файлы уточнения и откройте MTZ-файл. Для опции Амплитуды и Фазы выберите данные 2FOFC WT_no_fill_neutron в раскрывающемся меню. Повторите это и откройте данные FOFC WT_neutron. Откройте Display Manager и переключите кнопку Scroll для карт нейтронов и рентгеновских лучей 2FOFCWT, затем прокрутите, чтобы уменьшить rmsd карт 2FOFCWT до 1,00 (дополнительный рисунок 21). Переключите прокрутку для нейтронных и рентгеновских карт FOFCWT и прокрутите, чтобы уменьшить rmsd карт FOFCWT до 3,00.
- Выполните визуальный осмотр остатков, чтобы определить, соответствует ли модель данным. Определите правильную ориентацию и заполненность H/D всех сменных участков, проанализировав пики карты разностной плотности. Сюда входят гидроксильные группы серинов, треонинов и тирозинов; азот гистидина, глутамина, аспарагина и лизина; сульфгидрил цистеина; карбоксильные группы аспартата и глутамата; магистральные амидные группы; лиганды; кофакторы и любые потенциальные функционализированные остатки (рисунок 6).
- Переориентируйте молекулы воды в соответствии с плотностью нейтронов и взаимодействиями водородных связей, вращая их с помощью функции Rotate Translate Zone/Chain/Molecule (дополнительный рисунок 22A и дополнительный рисунок 22B). Отрегулируйте положения заменяемых участков H/D белкового остатка с помощью инструмента «Редактировать углы ши » и функции «Повернуть зону/цепь/молекулу » (дополнительный рисунок 22C и дополнительный рисунок 22D).
- Подготовка структуры
- Уточнение структуры – уточнение только нейтронных данных
- Подготовка структуры
- Откройте Phenix и выберите «Молекулярная замена» и выберите «Phaser-MR (полнофункциональный)», чтобы получить фазу масштабированных интенсивностей, предоставленных ученым-прибором путем молекулярной замены для генерации исходного файла координат в формате pdb. Введите начальную структуру pdb на вкладке «Ввод и общие параметры » и заполните параметры Ансамбли, содержимое ASU и Процедура поиска .
- Откройте Инструменты моделирования и выберите Инструменты PDB. Вставьте pdb-файл в качестве входного файла. Перейдите на вкладку Параметры и в разделе Удалить выделение атома выберите названия растворителя, лигандов, кофакторов и металлов. Это удаляет все молекулы воды, кофакторы, лиганды и ионы металлов для создания минимальной модели. Кроме того, установите флажок Удалить альтернативные конформеры из модели (дополнительный рисунок 23).
- Выберите Уточнение в Phenix и откройте ReadySet. Введите отредактированный файл координат pdb рядом с PDB-файлом. Выберите Добавить водород в модель, если он отсутствует , и выберите H/D на заменяемых участках, H в другом месте из раскрывающегося меню параметров нейтронной очистки (дополнительный рисунок 23).
- Уточнение структуры
- Откройте программу phenix.refine на вкладке Уточнение в Phenix. На вкладке Настройка введите PDB-файл, который был обработан с помощью ReadySet, в поле Входные файлы . В поле Входные файлы загрузите MTZ-файл из нейтронных данных и назначьте его как рентгеновские данные и X-ray R-free в столбце Тип данных , даже если это данные нейтронов. Конфигурация уточнения, настроенная на следующем шаге, будет использоваться для обработки файла отражения как нейтронных данных. Метки Space group и Data будут автоматически заполняться после загрузки данных (дополнительный рисунок 24A).
- На вкладке Настройка в параметрах Уточнения сохраните стандартную стратегию уточнения. Увеличьте количество циклов до пяти. В разделе Другие параметры выберите нейтрон в раскрывающемся меню Таблица рассеяния . Снимите флажок Обновить воды (дополнительный рисунок 24B).
- Выберите Все параметры>Расширенные>Водороды. В новом окне выберите Individual из выпадающего меню Модель уточнения водорода и отключите Force riding adp (Дополнительный рисунок 20).
- Выберите Все параметры > Параметры поиска... выбор. Найдите слово ядерный и выберите Использовать ядерные расстояния для X-H/D (дополнительный рисунок 20).
- Выберите Выполнить , чтобы инициировать уточнение.
ПРИМЕЧАНИЕ: После первоначальной доработки необходимо будет визуально осмотреть карты SLD нейтронов и выполнить ручное построение модели в Coot. Может потребоваться вставить лиганды/кофакторы, присутствующие в модели. Последующие уточнения потребуют необходимого файла ограничений CIF для любых соответствующих лигандов, и они должны быть загружены на вкладке Configure (Настройка ) phenix.refine.
- Модельное строительство
- После уточнения в Phenix нажмите «Открыть в Coot» на вкладке «Результаты», чтобы визуализировать карты и структуру SLD нейтронов. Перейдите на вкладку Менеджер отображения и в разделе Карты щелкните Удалить карту, чтобы удалить карты 2FOFCWT и FOFCWT (дополнительный рисунок 25). Нажмите на Файл > Открыть MTZ, mmCIF fcf или phs.... Выберите текущую папку уточнения и выберите MTZ-файл. Для опции Амплитуды и Фазы выберите данные 2FOFC WT_no_fill в раскрывающемся меню. Повторите это, щелкнув Файл > Открыть MTZ, mmCIF fcf или phs... и выберите данные FOFCWT в раскрывающемся меню для опции Амплитуды и Фазы. Откройте Display Manager и переключитесь на прокрутку для карты 2FOFC WT_no_fill затем прокрутите, чтобы уменьшить rmsd данных 2FOFC WT_no_fill до 1,00 (дополнительный рисунок 25). Переключите кнопку Прокрутка для карты FOFCWT и прокрутите, чтобы уменьшить rmsd данных FOFCWT до 3.00.
- Выполните визуальный осмотр структуры белка, чтобы определить, соответствует ли модель нейтронной карте SLD.
- Как описано в пункте 7.1.3.2, определить правильную ориентацию и заполненность H/D остатков и групп с заменяемыми H/D участками. Отрегулируйте положение остатков с помощью инструмента «Поворот перевода» и «Редактирование углов chi» (рисунок 6). При необходимости можно использовать Real Space Refine Zone . Исправление атомов D, которые взрываются от остатка вручную с помощью текстового редактора для вставки правильных координат атомов
ПРИМЕЧАНИЕ: Зона уточнения реального пространства не оптимизирована для нейтронных карт SLD в Coot и может привести к нерегулярным длинам связи для атомов, связанных с D, называемых взрывающимися остатками (дополнительный рисунок 26). Предпочтительно вручную редактировать необходимые атомные координаты и избегать использования Real Space Refine Zone. - Вставляйте и переориентируйте молекулы воды в соответствии с плотностью нейтронов. Чтобы добавить воды в Coot, выберите значок Поместить атом в указатель и выберите вставку молекулы воды (дополнительный рисунок 27A). По умолчанию Coot вставляет атом O в это положение.
- Чтобы добавить атомы D к атомам O вод, вставленных в Coot, используйте Phenix. Откройте меню Уточнение и нажмите ReadySet. Рядом с параметрами нейтронного уточнения выберите только опцию Добавить дейтерии в молекулы растворителя. Снимите флажок Добавить водород в модель, если он отсутствует (дополнительный рисунок 27B и дополнительный рисунок 27C).
ПРИМЕЧАНИЕ: Построение модели с использованием только нейтронных данных отличается от построения модели совместной рентгеновско-нейтронной структуры тем, что нет рентгеновских данных, способствующих уточнению координат позвоночника и более тяжелых атомов. При совместном уточнении карта электронной плотности первоначально используется для определения координат белковой магистрали и боковой цепи. Эта модель впоследствии используется при совместной уточнении рентгеновских/нейтронных данных, в которой ориентация и занятость атомов H/D выводится из карты нейтронных SLD. При уточнении только нейтронов вся структура выводится из анализа карт SLD нейтронов, требующих построения молекул воды, основы, боковых цепей и лигандов в дополнение к атомам H/D (рисунок 6). Отношение данных к параметрам является низким в уточнениях только по сравнению с нейтронными данными, и следует проявлять осторожность, чтобы не переусердствовать с данными.
- Подготовка структуры
Результаты
Данные о нейтронной дифракции кристаллов литической полисахаридмоноксигеназы из Neurospora crassa (NcLPMO9D) были собраны на IMAGINE при HFIR при комнатной температуре и на MaNDi в SNS в крио-условиях в соответствии с протоколом, описанным выше. Использовались кристаллы гидрогенизированного белка, выращенного в буфере на основе H2O с объемом более 0,1 мм3 (иллюстративный пример крупных кристаллов показан на дополнительном рисунке 4 и последующих рисунках). Кристаллы монтировали в кварцевые капилляры, а парообмен с буфером на основе D2O выполняли в течение трех недель до сбора данных (рисунок 4).
Сбор данных о комнатной температуре осуществлялся на линии луча IMAGINE (рисунок 1). Четырехчасовое испытание белым лучом привело к дифракции с высоким разрешением, предполагая, что кристалл был подходящего размера и качества для сбора полного набора данных. В дополнение к предоставлению предварительной информации о дифракционном качестве кристалла, начальная широкополосная экспозиция может быть использована для индексации дифракционной картины и определения матрицы ориентации кристалла. Учитывая пространственную группу P21 кристалла, была реализована стратегия сбора данных из 18 кадров со временем сбора 20 часов на кадр. Как и при сборе данных о дифракции рентгеновских лучей, группы пространства с более высокой симметрией требуют меньшего количества кадров (т.е. меньшего углового покрытия) для сбора полного набора данных. Данные собирались в квазилауэ-режиме с использованием диапазона длин волн 2,8 – 4,0 Å. После сбора данных данные были проиндексированы, интегрированы, масштабированы и объединены, чтобы получить нейтронный SLD-файл в формате MTZ с разрешением 2,14 Å. Данные были оценены как имеющие достаточное качество в соответствии с аналогичными руководящими принципами для анализа рентгеновских данных, хотя полнота 80% и CC1/2 не менее 0,3 были признаны приемлемыми, поскольку дифракция нейтронного белка является методом, ограниченным потоком.
После сбора данных о нейтронной дифракции при комнатной температуре тот же кристалл использовался для сбора набора данных о дифракции рентгеновских лучей комнатной температуры с разрешением 1,90 Å (дополнительный рисунок 13). Рентгеновские данные использовались для определения положений «более тяжелых» атомов, включая C, N, O и S. Структура, уточненная только на основе рентгеновских данных, затем использовалась в качестве исходной модели для выполнения совместной уточнения данных рентгеновского излучения и нейтронов. Phenix ReadySet использовался для добавления атомов H в необменяемых местах, атомов H и D в обменных местах и атомов D в молекулы воды исходной рентгеновской модели. После подготовки этой модели были выполнены итеративные уточнения для обоих наборов данных (дополнительный рисунок 19 и дополнительный рисунок 20). Интерактивное построение модели было выполнено в Coot путем визуального осмотра карт плотности для соответствующей ориентации боковых цепей и молекул воды (дополнительный рисунок 22). Данные нейтронов в основном использовались для определения состояний протонации и ориентации молекул воды. Сравнение карты электронной плотности остатков, таких как серин и триптофан, и соответствующей карты нейтронов SLD иллюстрирует информацию, которая может быть получена о состояниях протонирования в обменных участках H/D от дифракции нейтронного белка (рисунок 7). Наложение карт электронных и нейтронных карт SLD для молекул воды также указывает на то, что, хотя взаимодействия водородных связей могут быть выведены из рентгеновских данных, нейтроны предоставляют четкую информацию относительно ориентации этих водородных связей (рисунок 8). Для определения состояний протонации и ориентации боковых цепей были сгенерированы карты опущения нейтронов SLD FO-FC. Проиллюстрированы нейтронные карты SLD, полученные для остатков тирозина и треонина, в которых карты нейтронов Fo-FC четко указывают на положительные пики, означающие присутствие H/D (рисунок 9). Собранные данные нейтронной дифракции также предоставили ценную информацию о множественных состояниях протонирования, таких как группа -ND3+ Lys (рисунок 10). Статистика уточнений (Rwork и Rfree) тщательно отслеживалась во время оптимизации модели, чтобы предотвратить переподготовку. Окончательная статистика дала рентгеновский Rwork 12,77 % и Rfree 18,21%, а также нейтронный Rwork 14,48% и Rfree 21,41% с 389 молекулами воды (дополнительный рисунок 28).
Данные о криотемпературе были собраны на NcLPMO9D после замачивания аскорбата для уменьшения активного участка меди от CuII до CuI на лучевой линии MaNDi (дополнительный рисунок 2 и дополнительный рисунок 15)45. Данные были собраны с использованием режима TOF Laue после нейтронно-дифракционного теста с использованием 4-часового воздействия для проверки качества дифракции. Учитывая пространственную группу кристалла, была разработана стратегия сбора данных из 18 кадров с дозой сбора 80 кулонов на кадр. Данные были собраны в режиме TOF-Laue в диапазоне длин волн 2,0 – 4,0 Å. После сбора данных данные индексировались, интегрировались, масштабировались и объединялись для получения файла отражения в формате MTZ с разрешением 2,40 Å51,52.
После сбора данных для уточнения данных только нейтронной дифракции использовался набор данных о нейтронной дифракции 2,40 Å NcLPMO9D. Данные нейтронов были фазированы молекулярной заменой с использованием PDB 5TKH в качестве исходной модели. Phenix ReadySet использовался для добавления атомов H в необменяемых участках и атомов H/D с частичным заполнением в обменных участках. Молекулы воды были удалены из исходной модели с помощью инструментов PDB (дополнительный рисунок 23). Подготовка модели сопровождалась уточнением с помощью phenix.refine с использованием таблицы рассеяния нейтронов (дополнительный рисунок 24). Интерактивное построение модели было выполнено в Coot, при этом молекулы воды были добавлены с использованием положительных пиков карты FO-Fc и позиционированы в соответствии с потенциальными взаимодействиями водородных связей (рисунок 11A и рисунок 11B). При анализе нейтронных карт SLD молекулы воды хорошо видны, если они сильно упорядочены, однако их плотность может быть сферической или эллипсоидальной, если они плохо упорядочены (рисунок 11C-E). Нейтронные карты SLD были использованы для предоставления ценной информации об ориентации остатков, таких как аспарагин, в которых дифференциация между карбонильной и аминогруппами может быть сложной задачей при использовании только данных дифракции рентгеновских лучей (рисунок 12A и рисунок 12B). Пики в картах FO-FC нейтронов SLD также были очень информативны при определении состояний протонации остатков гистидина в N δ- или N ε положении (рисунок 12C и рисунок 12D). Состояние протонации остатков с несколькими H/D обменными участками также может быть определено с помощью нейтронных карт SLD. Это было ясно проиллюстрировано картой нейтронов FO-FC SLD без аргинина, который, как известно, имеет положительный заряд (рисунок 12E и рисунок 12F). Как и ранее, переподготовку предотвратили путем мониторинга Rwork и Rfree. Окончательная статистика дала Rwork 22,58% и Rfree 30,84% (Дополнительный рисунок 29). Учитывая, что дифракция нейтронного белка представляет собой метод с ограниченным потоком, в котором необходимо учитывать отрицательную длину рассеяния и большой коэффициент некогерентного рассеяния H, можно ожидать, что уточнение только нейтронных данных будет иметь более плохую статистику, чем совместная очистка рентгеновских /нейтронных данных с меньшим количеством видимых молекул воды (дополнительный рисунок 28 и дополнительный рисунок 29).
При анализе нейтронных SLD-карт станет очевидным, что отмена плотности из-за отрицательной длины рассеяния нейтронов H будет происходить для гидрогенизированных белков, которые подверглись парообмену с D2O-содержащим буфером кристаллизации. По этой причине карты SLD нейтронов, в которых необменные атомы H присоединены к углероду, кажутся неполными по сравнению с их аналогом по карте электронной плотности (рисунок 13A). Эффект отмены часто более очевиден при более низких разрешениях, что делает необходимым получение кристаллов белка высокого качества. Поэтому предпочтительно выполнять совместную очистку образца как с рентгеновскими, так и с нейтронными данными, в которой рентгеновские данные могут быть использованы для определения положения белковой основы (рисунок 13B). Кроме того, атомы серы в цистеине и метионине могут быть плохо видны, что требует рентгеновских данных для точного размещения атомов (рисунок 13C и рисунок 13D). Металлы со слабой длиной рассеяния нейтронов также могут быть сложными для моделирования на картах SLD нейтронов, как это видно на наших картах LPMO9D. Поэтому сбор набора рентгеновских данных низкой дозы (без радиационного повреждения) на одном и том же кристалле полезен, поскольку он позволяет позиционировать атом металла с использованием карт электронной плотности (рисунок 13E и рисунок 13F).
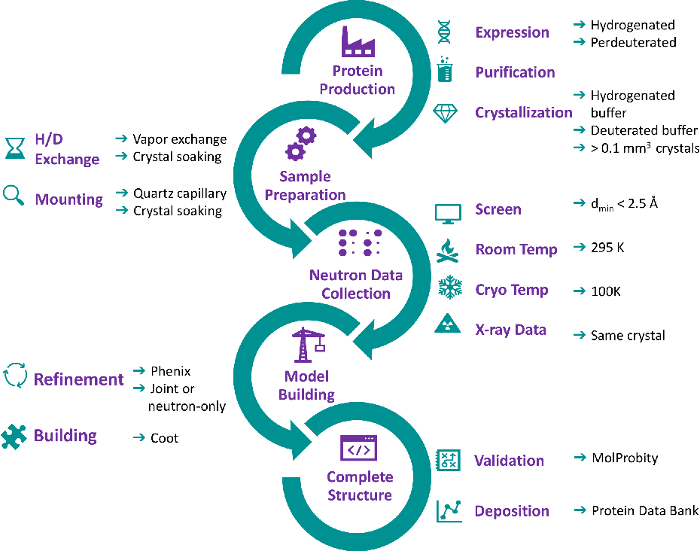
Рисунок 1: Блок-схема рабочего процесса кристаллографии нейтронного белка. Производство белка. Для того чтобы получить нейтронную структуру, сначала экспрессируют белок. Бактериальная экспрессия в средах на основе H2O или D2O обычно используется для получения высокого выхода гидрогенизированного или пердоутерированного рекомбинантного белка, соответственно. Белок очищают в буфере на основе H2O, а затем кристаллизуют в буфер кристаллизации на основе H2O или D2O для выращивания кристаллов до минимального размера 0,1 мм3. Пробоподготовка: Перед сбором данных о дифракции нейтронов выращенные H2O кристаллы подвергаются H/D обмену для обмена титруемых атомов H белка с D. H/D обмен может быть выполнен путем прямого замачивания кристаллов в дейтерированном кристаллизационном буфере, уравновешивания кристаллизационной капли с резервуаром на основе D2O или путем установки кристаллов в кварцевых капиллярах для обмена пара с дейтерированным буфером кристаллизации. Сбор нейтронных данных: После обмена H/D потенциальные кристаллы просеиваются для определения дифракционного качества. Кристаллы с минимальным разрешением 2,5 Å считаются подходящими для сбора полного набора данных. Кристаллы монтируются в кварцевые капилляры для сбора данных при комнатной температуре или застыли в криопетле для сбора данных при криогенной температуре. Набор рентгеновских данных собирается на том же (или идентичном) кристалле при той же температуре. Модель здания: Уточнение выполняется с использованием phenix.refine как по нейтронным, так и по рентгеновским данным или только по нейтронным данным. Ручное построение модели структуры белка выполняется в Coot с использованием нейтронных карт SLD. Полная структура: После завершения структуры белка координатная модель проверяется и депонируется в Банке данных белка. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
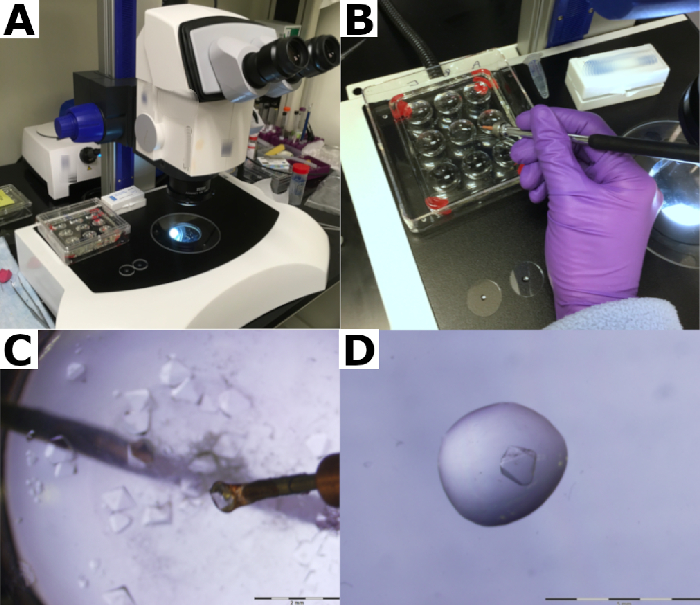
Рисунок 2: Сбор кристаллов белка. (A) Кристаллы обрабатываются под микроскопом. (B) Закрывается герметичная сэндвич-коробка, содержащая силиконизированную стеклянную пластину. Резервуарный буфер пипетируется на силиконизированные стеклянные слайды. (C) Кристалл собирается с помощью микролупа. (D) Кристалл помещается в каплю материнского щелока, чтобы смыть любой мусор, который часто собирают вместе с кристаллом. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
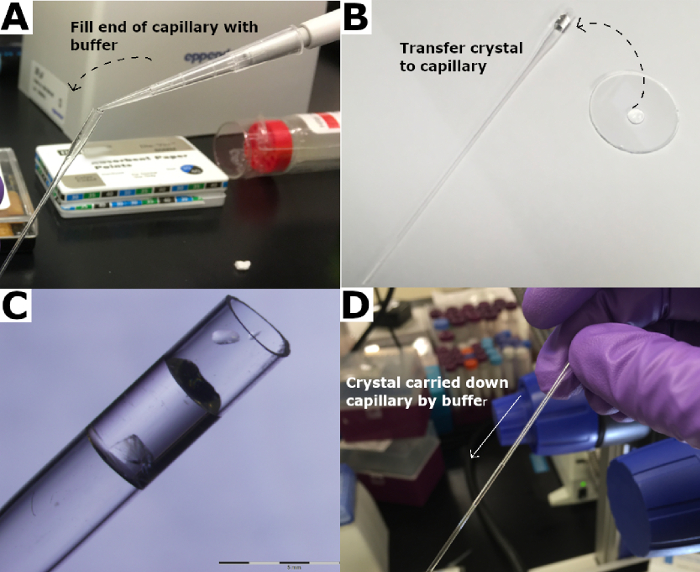
Рисунок 3: Перенос кристалла в кварцевый капилляр. (A) Конец кварцевого капилляра заполнен резервуарным буфером. (B) Кристалл переносится в кварцевый капилляр и (C) погружается в резервуарный буфер. (D) Кристалл переносится вниз по капилляру с помощью резервуарного буфера. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
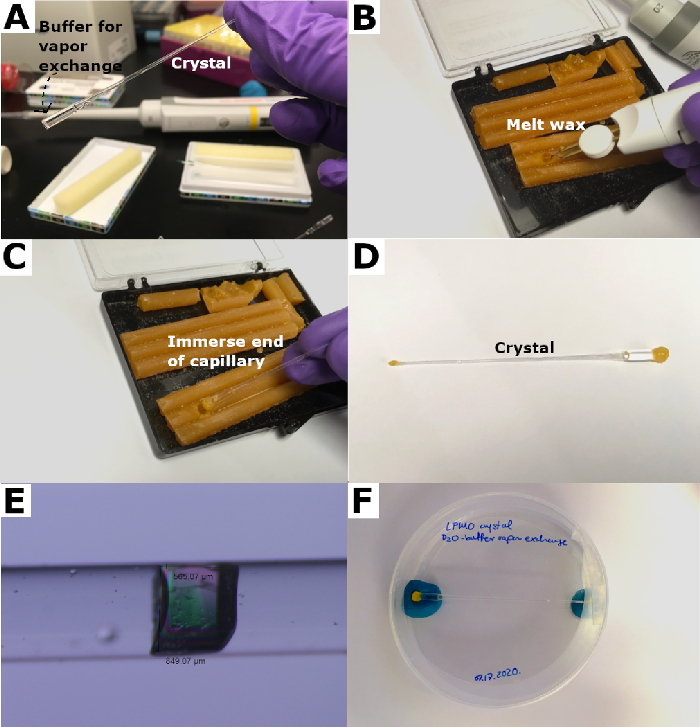
Рисунок 4: Герметизация кварцевого капилляра. (A) Дейтерированный буфер добавляется в конце капилляра с образованием "пробки". (Б) Воск расплавляется «палочкой». (C) Капилляр помещают в расплавленный воск для запечатывания. (D) Восковые пробки образуются на обоих концах для уплотнения капилляра. (E) Кристалл после монтажа. (F) Запечатанный капилляр помещают в чашку Петри и удерживают на месте шпаклевкой. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.

Рисунок 5: Повышенный сигнал-шум нейтронной дифракционной картины. По мере сбора данных дифрагированные пятна становятся более интенсивными. (ПРИМЕЧАНИЕ: живые дифракционные изображения, представленные здесь, предназначены для иллюстрации и были взяты из разных кристаллов.) Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
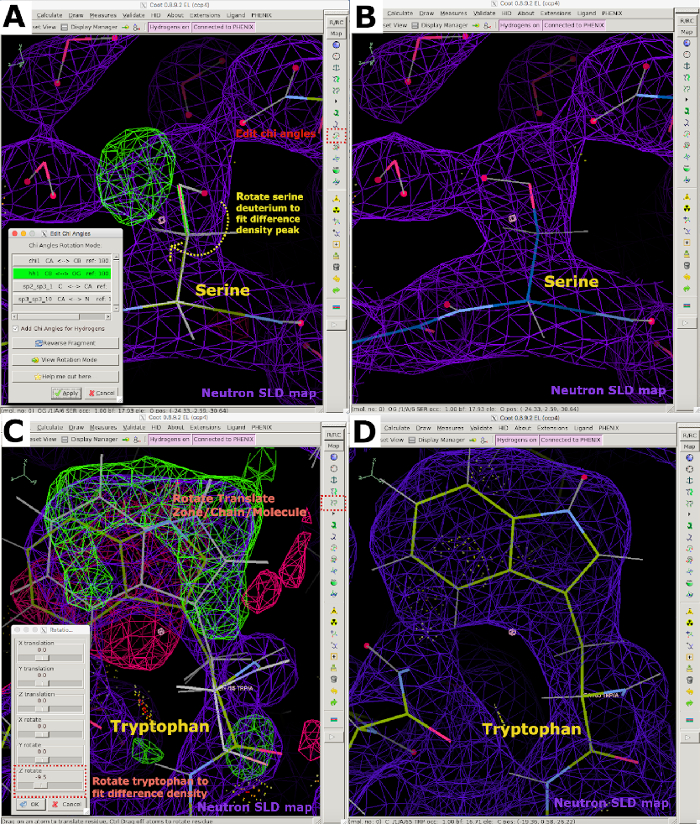
Рисунок 6: Построение интерактивной модели с использованием нейтронных данных в Coot. (A) Положительный пик плотности нейтронов FO-FC SLD (зеленый), указывающий на серин, должен быть переориентирован путем редактирования углов ци. Карта нейтронов SLD 2FO-FC отображается фиолетовым цветом, а карта электронной плотности 2FO-FC отображается синим цветом. (B) Правильно позиционированный серин. (C) Положительные и отрицательные пики плотности FO-FC нейтронов SLD (зеленый и красный, соответственно), указывающие на то, что триптофан должен быть повернут/переведен в соответствии с пиком разностной плотности. (D) Правильно ориентированный триптофан. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
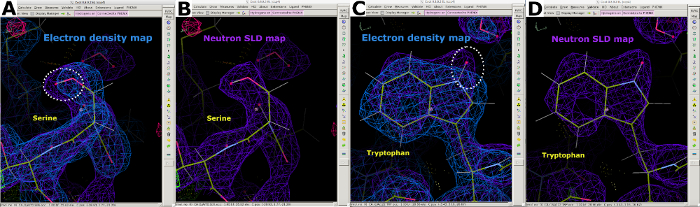
Рисунок 7: Дополнительная информация из нейтронных карт SLD. (A) Карта электронной плотности 2FO-FC (синий) отображает положения «более тяжелых» атомов в серине. (B) Карта нейтронов SLD 2FO-FC (фиолетовый) четко отображает положение "более легкого" атома D в серине. (C) Карта электронной плотности 2FO-FC (синий) отображает положения «более тяжелых» атомов в триптофане. (D) Карта нейтронов SLD 2FO-FC (фиолетовый) четко отображает положение "более легкого" атома D в триптофане. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
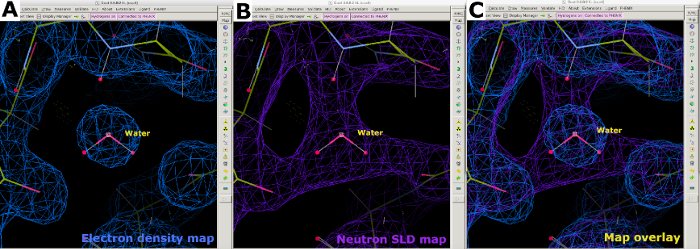
Рисунок 8: Позиционирование молекулы воды. (A) Сферическая форма карты электронной плотности 2FO-FC (синий) для воды. (B) Нейтронная карта SLD 2FO-FC (фиолетовый) предоставляет информацию о ориентации воды и взаимодействии водородных связей. (C) Картографическое наложение электронных и нейтронных SLD карт воды. Карта нейтронов SLD 2FO-FC отображается фиолетовым цветом, а карта электронной плотности 2FO-FC отображается синим цветом. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
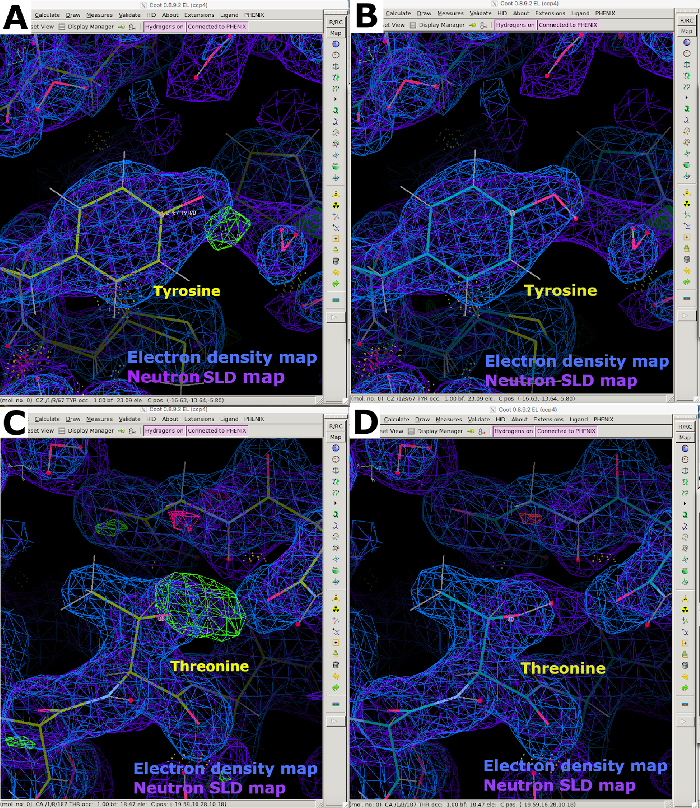
Рисунок 9: Нейтронные карты SLD FO-FComit. (A) Карта FO-FC нейтронов SLD (зеленая) предоставляет четкую информацию о H/D ориентации остатков тирозина. Карта нейтронов SLD 2FO-FC отображается фиолетовым цветом, а карта электронной плотности 2FO-FC отображается синим цветом. (B) Остаток тирозина с правильной ориентацией H/D. (C) Карта нейтронов FO-FC SLD (зеленая) содержит четкую информацию о ориентации H/D остатков треонина. (D) Остаток треонина с правильной ориентацией H/D. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
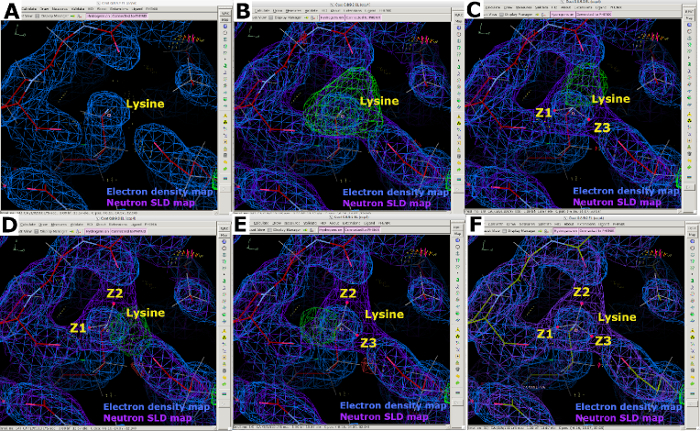
Рисунок 10: Множественные состояния протонации, отображаемые с помощью нейтронных карт SLD. (A) Карта электронной плотности 2FO-FC (синий) предоставляет только положение атома N лизина ε-аммониевой группы. (B-E) Карта опускания нейтронов FO-FC SLD (зеленый) ясно демонстрирует положительно заряженную группу -NH3. Карта нейтронов SLD 2FO-FC отображается фиолетовым цветом, а карта электронной плотности 2FO-FC отображается синим цветом. (F) Наложение карт электронной плотности и нейтронов SLD. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.

Рисунок 11: Появление молекул воды в нейтронных картах SLD. (A) Молекулы воды позиционируются в соответствии с нейтронными картами FO-FC SLD (зеленый) и потенциальными водородными связями. Карта нейтронов SLD 2FO-FC отображается фиолетовым цветом. (B) Правильно позиционированная молекула воды. (С-Е) Различные формы нейтронов SLD сопоставляются с молекулами воды в зависимости от В-факторов и взаимодействий водородных связей. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
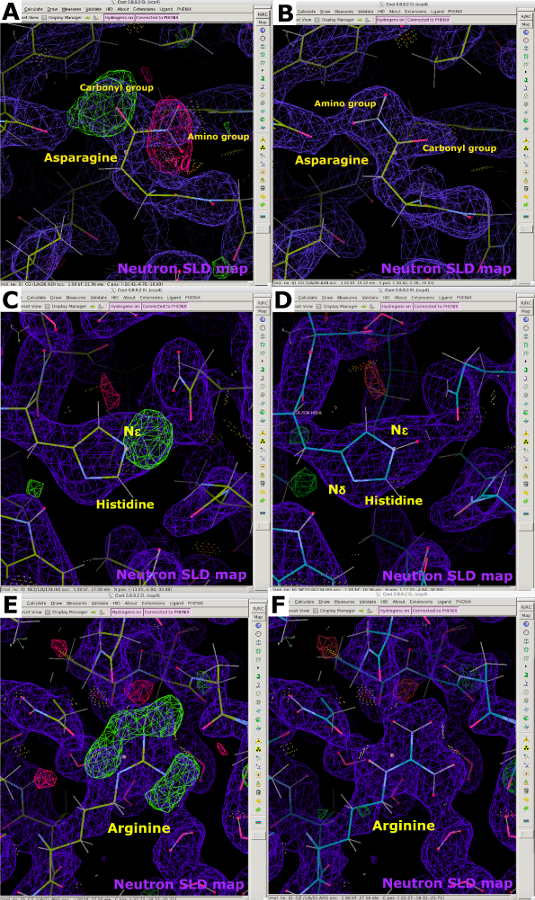
Рисунок 12: Информация об ориентации аминокислот и протонации, предоставляемая нейтронными картами SLD. (A) Пики нейтронной карты SLD FO-FC (зеленый) указывают на неправильную ориентацию остатка аспарагина. Карта нейтронов SLD 2FO-FC отображается фиолетовым цветом, а карта электронной плотности 2FO-FC отображается синим цветом. (B) 2FO-FC нейтронная карта SLD (фиолетовая) правильной ориентации аспарагина. (C) Пик нейтронной карты SLD FO-FC (зеленый) указывает на одиночное протонирование гистидина в N ε. (D) 2FO-FC нейтронная карта SLD (фиолетовая) гистидина N ε-протонации. (E) Нейтрон SLD FO-FC опускает пики карты (зеленый) подтверждает положительный заряд аргинина. (F) Карта нейтронов SLD 2FO-FC (фиолетовый) положительно заряженного аргинина. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
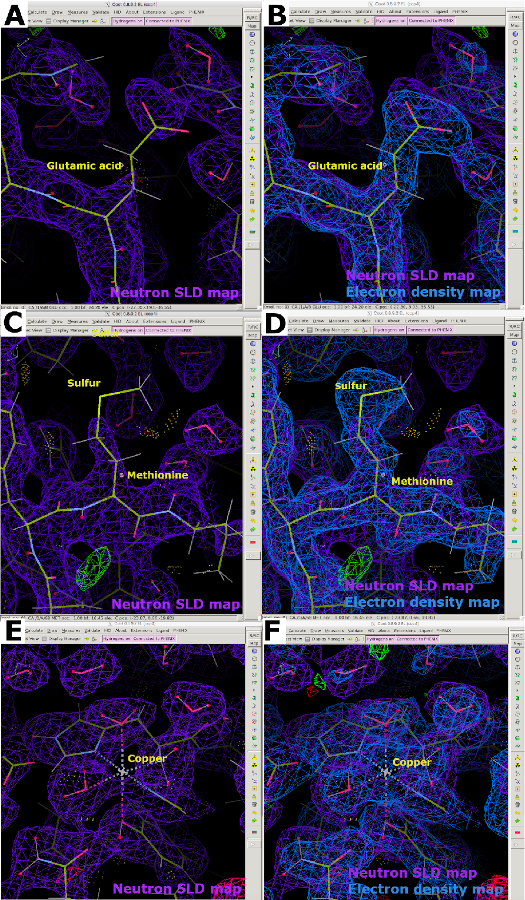
Рисунок 13: Прерывистые нейтронные карты SLD. (A) 2FO-FC нейтронная SLD карта (фиолетовая) гидрогенизированного, парового H/D обменного белка. Глутаминовая кислота отображает отклонение карты SLD нейтронов из-за отрицательной длины рассеяния необменяемых атомов H. (B) Наложенная карта электронной плотности 2FO-FC (синий) четко отображает плотность глутаминовой кислоты. (C) Атом серы в метионине плохо виден на картах 2FO-FC нейтронов SLD (фиолетовый). (D) Наложенная карта электронной плотности четко отображает плотность метионина. (E) Атомы металла, здесь меди, плохо видны на картах SLD нейтронов 2FO-FC (фиолетовый). (F) Наложенная карта электронной плотности 2FO-FC (синий) четко отображает плотность скоординированного атома меди. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
| Изотоп | Длина когерентного рассеяния (fm) | Длина некогерентного рассеяния (fm) |
| 1Ч | -3.741 | 25.274 |
| 2Ч | 6.671 | 4.04 |
| 12С | 6.6511 | 0 |
| 14Н | 9.37 | 2 |
| 16О | 5.803 | 0 |
| 23На | 3.63 | 3.59 |
| 24Мг | 5.66 | 0 |
| 31П | 5.13 | 0.2 |
| 32С | 2.804 | 0 |
| 35Кл | 11.65 | 6.1 |
| 39 тыс. | 3.74 | 1.4 |
| 40Ка | 4.8 | 0 |
| 55Мн | -3.73 | 1.79 |
| 56Фе | 9.94 | 0 |
| 63Cu | 6.43 | 0.22 |
| 64Зн | 5.22 | 0 |
Таблица 1: Длины рассеяния нейтронов и значения некогерентного рассеяния. Адаптировано из Sears, 199216.
Дополнительный рисунок 1: Прибор IMAGINE на изотопном реакторе с высоким потоком. (A) Прибор IMAGINE в зале направляющих холодных нейтронов. (B) Образец, установленный в кварцевом капилляре, прикрепленном шпаклевкой к гониометру. Таблица образцов и детекторов закрывается, чтобы расположить кристалл и цилиндрическую пластину изображения в пучке нейтронов. Изменено с разрешения Международного союза кристаллографии53. Изображения предоставлены с разрешения Женевьевы Мартин, Национальная лаборатория Оук-Ридж. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 2: Прибор MaNDi на источнике нейтронов расщепления. (A) Матрица детекторов камер MaNDi Anger. Воспроизводится с разрешения Международного союза кристаллографии11. (B) Подвижная выборочная ступень MaNDi. (C) Образец, установленный в кварцевом капилляре, установленном на гониометре в MaNDi для сбора данных о комнатной температуре. Изображения предоставлены с разрешения Женевьевы Мартин, Национальная лаборатория Оук-Ридж. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 3: Структура литической полисахаридной монооксигеназы NcLPMO9D. Медно-активный сайт NcLPMO9D расположен на плоской полисахаридной связывающей поверхности. Медь координируется двумя остатками гистидина в классической «гистидоновой скобке», а также осевым остатком тирозина. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 4: Кристалл с достаточным объемом в сидячем каплекристаллизационном лотке. (A) Крупные кристаллы выращиваются в сидячих каплях, установленных в 9-луночных силиконизированных стеклянных пластинах. (B и C) Кристаллы измеряются для идентификации кристаллов с объемом > 0,1 мм3. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 5: рН-метр, установленный для дейтерированных буферных показаний. РН-электрод замачивают в D2O перед использованием. NaOD и DCl используются для регулировки рН дейтерированных буферов. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 6: Рекомендации по монтажу образцов MaNDi. Максимальные размеры кварцевого капилляра и положение образца для сбора данных о комнатной температуре.
Воспроизводится из: https://neutrons.ornl.gov/mandi/sample-environment Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 7: Удаление избыточного буфера. (А) Избыточный буфер аспирируется из кварцевого капилляра с микрокапиллярными наконечниками. (B) Оставшийся буфер удаляется тонким бумажным фитилем для полного высыхания капилляра. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 8: Графический интерфейс сбора данных. Окно ввода "Параметры эксперимента" для сбора данных. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 9: Графический интерфейс оптики. Выбор квазилауэйского диапазона для сбора данных и мониторинга скорости подсчета нейтронов. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 10: Сбор данных в графическом интерфейсе сбора данных. Время экспозиции, количество кадров и углы сбора данных указаны во вкладке «Сбор». Затем сбор данных инициируется с помощью «Начать сканирование». Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 11: Обнаружены и отображены дифракционные нейтроны. В конце экспозиционного времени детектор нейтронно-чувствительной пластины считывается, а дифракционная картина отображается в графическом интерфейсе сбора данных. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 12: Обработка данных после дифракции нейтронов. Кадры индексируются, интегрируются, нормализуются и масштабируются с использованием Lauegen, Lscale и Scala для создания объединенного файла отражения после сбора данных. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 13: Сбор рентгеновских данных. Домашний источник рентгеновского генератора, установленный кварцевым капиллярным кристаллом для сбора данных о комнатной температуре. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 14: Руководящие принципы монтажа для сбора криоданных MaNDi. Размеры Кристаллических Колпачков и высота штырей для сбора криоданных в MaNDi.
Воспроизводится из: https://neutrons.ornl.gov/mandi/sample-environment Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 15: Мгновенная заморозка для сбора данных о крионейтронной дифракции. (A) Установка для замачивания кристаллов, сбора с помощью микролупа и замораживания в жидком азоте с использованием криосовместимого контейнера, такого как пена Dewar. Установленный кристалл переносится непосредственно на криогониометр с помощью предварительно охлажденных криоконтафтовых щипцов. (B) Восковое уплотнение расплавляется для удаления кристаллов. (C) Кристалл промывается до конца кварцевого капилляра для сбора урожая. (D) Кристалл последовательно вымачивают в буфере для впитывания аскорбата, а затем в криопротекторе с последующим мгновенным замораживанием в жидком азоте. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 16: Пример интерфейса выравнивания. Выравнивание кристаллов в нейтронном пучке, представленном синим крестом, производится центрированием по точкам и щелчкам. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 17: Графический интерфейс CSS для сбора данных. Стратегия сбора данных, включая дозы и углы воздействия, загружается в графический интерфейс CSS. По мере сбора данных дифрагированные нейтроны, обнаруженные на детекторе реального времени, будут отображаться на верхней панели. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 18: Сопоставление флагов без R в CCP4. R-свободные флаги нейтронных данных сопоставляются с R-свободными флагами рентгеновских данных, собранных на том же или идентичном кристалле для совместной очистки. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 19: Подготовка и уточнение структуры. (A) Инструмент Phenix ReadySet используется для добавления двойного H/D заполняемости на сменных участках. (B) Как нейтронные данные, так и рентгеновские данные используются для совместной уточнения, в то время как первоначальная входная модель была уточнена на основе набора рентгеновских данных, собранных на одном и том же кристалле или идентичном кристалле. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 20: Настройка параметров уточнения. Модель уточнения, а также ядерные расстояния сконфигурированы для совместного уточнения рентгеновских/нейтронных данных. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 21: Выбор данных для построения модели Coot. Файловый выход phenix MTZ, содержащий рентгеновские и незаполненные нейтронные данные, открывается в Coot для создания электронных и нейтронных SLD-карт для интерактивного построения моделей. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 22: Интерактивное построение модели в Coot во время совместной доработки. (A) Положительный и отрицательный пик плотности FO-FC нейтронов SLD (зеленый и красный, соответственно), указывающий на то, что вода должна быть переориентирована путем вращения/перемещения. Карта нейтронов SLD 2FO-FC отображается фиолетовым цветом, а карта электронной плотности 2FO-FC отображается синим цветом. (B) Правильно расположенная вода. (C) Положительный пик FO-FC нейтронов SLD (зеленый) указывает на то, что треонин должен быть повернут в соответствии с пиком разностной плотности путем редактирования углов chi. (D) Правильно ориентированный треонин. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 23: Подготовка структуры к уточнению только нейтронных данных. Исходный файл координат подготавливается для уточнения путем удаления атомов воды в PDBTools и путем добавления двойного H/D заполнения на сменных участках. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 24: Уточнение только нейтронных данных. (A) Нейтронные данные загружаются, а также подготовленная начальная модель. (B) Настройки для уточнения нейтронных данных используют таблицу рассеяния нейтронов. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 25: Выбор данных для построения модели Coot. Незаполненные нейтронные данные открываются в Coot для интерактивного построения моделей. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 26: Уточнение реального пространства в лысухе для дейтерированных остатков. (A) Положительные и отрицательные пики плотности FO-FC нейтронов SLD (зеленый и красный, соответственно), указывающие на то, что остаток аргинина должен быть перемещен в соответствии с пиком плотности FO-FC. Карта нейтронов SLD 2FO-FC отображается фиолетовым цветом, а карта электронной плотности 2FO-FC отображается синим цветом. (B) Использование Real Space Refine приводит к «взрыву» атомов D из-за отсутствия библиотек ограничений геометрии Лысухи. (C) Атомы D не движутся вместе с остальными остаточными атомами. (D) Положения атомов D могут быть исправлены вручную с помощью текстового редактора. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 27: Добавление молекул воды. (A) Молекулы воды могут быть вручную добавлены к положительным пикам плотности FO-FC нейтронов SLD (зеленый). Вставленные молекулы воды первоначально будут представлены атомом O в Coot. (B) Phenix ReadySet используется для добавления атомов D к атомам O для молекул воды. (C) Молекула дейтерированной воды успешно добавляется. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 28: Уточнение статистических данных. Окончательная статистика уточнения данных после совместной рентгеновско-нейтронной очистки. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Дополнительный рисунок 29: Уточнение статистики. Окончательная статистика уточнения данных после уточнения только нейтронных данных. Пожалуйста, нажмите здесь, чтобы загрузить этот рисунок.
Обсуждение
Кристаллография нейтронного белка является высокочувствительным методом для зондирования состояний протонирования и ориентации молекул воды в белках. Эта информация проливает свет на белковые каталитические механизмы, поскольку изменения в протонировании и взаимодействиях водородных связей часто занимают центральное место в химии ферментов10. Кристаллография нейтронного белка, хоть и информативная методика, имеет ряд факторов, которые следует учесть перед планированием проведения эксперимента по дифракции нейтронов, а именно:
- Потребность в крупных кристаллах белка для сбора данных.
- Рассеивающие свойства водорода и других элементов, таких как ионы металлов.
- Ограничения в программном обеспечении для уточнения структуры и построения моделей при работе с дейтерированными образцами.
Кристаллография нейтронного белка является методом ограниченного потока. В отличие от наборов данных дифракции рентгеновских лучей, для наборов данных нейтронов ожидаются более высокие R-факторы и более низкая полнота, избыточность и отношение сигнал-шум из-за присущих методу ограничений (ограниченный поток, квази-Лауэ, более длинные волны). Сбор данных одного кадра обычно занимает 12–18 часов. Успех эксперимента в значительной степени зависит от размера и качества образца, причем кристаллы размером 0,1 мм3 часто являются минимальным требованием3. Нейтронная дифракция требует производства большого количества белка для создания кристаллизационных капель в диапазоне от 10 до 800 мкл. Минимальный объем для выращивания достаточно крупных кристаллов можно оценить с помощью калькулятора объема с учетом параметров кристалла и образца (https://neutrons.ornl.gov/imagine). Рост крупных кристаллов чаще всего осуществлялся путем диффузии пара3. Кристаллизация подвесных капель позволяет выращивать кристаллы в больших каплях в диапазоне от 10-25 мкл, в то время как более крупные капли в диапазоне до ~ 50 мкл могут быть настроены с использованием коммерчески доступного оборудования для сидячей капли14,54. Силиконизированные девятилуночные стеклянные пластины можно использовать для установки очень больших капель с объемом до 800 мкл. Эти стеклянные пластины помещаются в «сэндвич-боксы», коммерчески доступные от Hampton Research. Дальнейшие методы кристаллизации включают пакетную кристаллизацию, при которой предел размера капли диктуется сосудом. Эксперимент по периодической кристаллизации может варьироваться от микролитров до миллилитров55. Кристаллизация также может быть выполнена с использованием метода диализа, в котором белок уравновешивается с осадком через мембрану диализа или путем контрдиффузии вдоль градиента концентрации осадка или через пористую пробку, такую как агароза56,57. Посев предлагает еще одну альтернативу получению кристаллов нужного объема. Микро- и макропосев успешно применяются для роста крупных кристаллов, в том числе крупных кристаллов NcLPMO9D45. Некоторые знания о диаграмме фаз белка, включая влияние температуры на растворимость, помогают в большом росте кристаллов.
При планировании эксперимента по дифракции нейтронов необходима оптимизация препарата белка для максимизации отношения сигнал/шум при сборе дифракционных данных7. Чтобы обойти подавление плотности и высокое некогерентное рассеяние, вызванное атомами H, карты SLD нейтронов могут быть улучшены путем обмена атомов H на его изотоп D, который обладает положительной длиной когерентного рассеяния и низкой длиной некогерентного рассеяния. Для этого осуществляется парообмен гидрогенизированного кристалла белка против дейтерированного кристаллизационного буфера. Это обеспечивает H/D обмен молекул растворителя и лабильных, титруемых атомов H белка H23. Парообмен осуществляется путем монтажа гидрогенизированного кристалла в кварцевый капилляр с дейтерированными кристаллизационными буферными «заглушками» на основе D2O и представляет собой эффективный, щадящий метод, который чаще всего применяется14,23,35. Обмен может занять несколько недель и предпочтительно требует, чтобы дейтерированный буфер часто менялся для обеспечения максимального обмена H/D. H/D обмен также может быть выполнен путем непосредственного замачивания кристалла в дейтерированном буфере. Чтобы избежать напряжения кристалла из-за воздействия D2O, процесс замачивания следует выполнять постепенно, постепенно увеличивая соотношение D2O: H2O58. В дополнение к этому, кристаллизация гидрогенизированного белка также может быть выполнена в дейтерированном буфере для обмена H/D на лабильных участках H22,59. Следует, однако, отметить, что буфер на основе D2O оказывает влияние на растворимость белка, требуя дальнейшей корректировки известных условий на основе H2O3,59. Было также замечено, что буферы на основе D2O в некоторых случаях приводят к образованию кристаллов меньшего размера59. Полный обмен титруемых и связанных с углеродом атомов H на D может быть достигнут путем экспрессии белков в дейтерированных средах для получения пердоутерированного образца20. Полученные нейтронные карты SLD пердоутерированного образца будут значительно улучшены, больше не отображая подавление плотности гидрогенизированного образца. Это полезно при характеристике H/D, связанного в необменяемых участках в белке или кофакторе. Тем не менее, экспрессия пердойтерированного белка является как высокой по стоимости, так и низкой по выходу60. Центр структурной молекулярной биологии (CSMB) Национальной лаборатории Оук-Ридж (ORNL) предлагает механизм дейтерации для пользователей, стремящихся создать пердевтерированный образец (https://www.ornl.gov/facility/csmb). Пердойтерированная экспрессия обычно выполняется в биореакторе на шкале 1 л, получая ~50 мг очищенного белка61.
После сбора данных о дифракции нейтронов выполняется уточнение и построение интерактивной модели. Уточнение может быть выполнено с использованием нескольких пакетов программного обеспечения, включая phenix.refine, nCNS или SHELXL28,31,32,33. Пакет Phenix является наиболее часто используемым программным обеспечением для уточнения данных о дифракции нейтронов в сочетании с Coot, которое используется для ручного построения модели из нейтронных карт SLD34. Хотя и Phenix, и Coot позволяют обрабатывать данные о дифракции нейтронов, им могут не хватать определенных функций, необходимых для обработки особенностей, связанных с нейтронными данными и дейтерированными образцами. Например, Coot не содержит оптимизации геометрии для дейтерированных остатков, что может привести к осложнениям во время построения модели, поскольку функция «Real Space Refine» приводит к «взрывающимся» остаткам (дополнительный рисунок 26)62. Это может быть решено путем создания файлов ограничений для всех дейтерированных остатков. Однако это интенсивный процесс, и такие библиотеки в настоящее время не являются общедоступными. При выполнении доработок в Фениксе сменные H/D участки первоначально будут установлены на 0,50 заполняемости для H и D. По мере выполнения уточнений заполняемость H и D будет уточняться в соответствии с нейтронными картами SLD. Во время построения интерактивных моделей карты разной плотности Fo-Fc очень информативны при оценке занятости H/D. Карты могут быть использованы для определения того, какие участки обладают высокой заполняемостью D, что особенно информативно на активном участке, где состояния протонирования каталитически значимы63. Однако неоднозначные ситуации возникают, когда H:D Заполняемость близка к 0.70:0.30, что приводит к полному подавлению сигнала в нейтронных SLD maps64. Следует также учитывать, что квази-лауэ нейтронные наборы данных часто имеют полноту около 80%, что ниже, чем обычно наблюдаемые ≥ 98% для данных рентгеновской дифракции. Поэтому при уточнении данных о дифракции нейтронов в Фениксе недостающие наблюдаемые амплитуды (Fo) вычисляются из модели для заполнения списка отражений, что приводит к смещению модели. Чтобы учесть это потенциальное смещение, «no_fill» карты должны быть изучены во время интерактивного построения моделей, а не «заполненные» карты.
Пользователи могут выбрать совместное уточнение рентгеновских/нейтронных данных своей структуры или только уточнение нейтронных данных. Визуализация нейтронных карт SLD, особенно при более низком разрешении, может первоначально сбивать с толку, особенно для гидрогенизированного белка, в котором H все еще присутствует в необменяемых участках, несмотря на парообмен H/D. Это приводит к отмене карт плотности нейтронов, создавая впечатление прерывистых карт65,66. Сбор соответствующего набора рентгеновских данных выгодно дополняет эти отмены в совместном уточнении (рисунок 13A и рисунок 13B). Стратегия совместного уточнения обычно включает уточнение координат белковой магистрали по рентгеновским данным, в то время как данные нейтронной дифракции используются для уточнения положения и занятости атомов H/D в обменных местах28. Поскольку введение совместного заполнения H/D на обменных участках увеличивает количество уточняемых параметров, совместная доработка с рентгеновскими данными также увеличивает отношение данных к параметрам. Совместная очистка требует, чтобы соответствующий набор рентгеновских данных был собран при той же температуре на том же кристалле или кристалле, выращенном в тех же условиях. Для данных о нейтронной дифракции, собранных при комнатной температуре (300 К), соответствующий набор рентгеновских данных должен быть собран при комнатной температуре с использованием стратегии сбора данных с низкой дозой для ограничения радиационного ущерба. Пердойтерированные образцы, напротив, обеспечивают улучшенные и непрерывные нейтронные SLD-карты, поскольку они не обладают одинаковой величиной подавления сигнала H/D. Однако длина рассеяния нейтронов некоторых элементов, включая металлы и серу, делает их плохо видимыми на картах SLD нейтронов, даже если белок был пердойтерирован (рисунок 13C-F)18. Если металл нуждается в характеристике, лучше всего использовать рентгеновскую дифракцию в совместном уточнении или применять спектроскопические методы для дополнения дифракционных экспериментов. Уточнение данных только нейтронами часто выполняется, когда набор данных нейтронов имеет высокое разрешение или если использовался пердоутерированный белок. Кроме того, уточнение данных только на нейтронах особенно полезно, если изучается белок, высокочувствительный к радиационному повреждению, поскольку структура, полученная из рентгеновского излучения, может обладать радиационно-индуцированными артефактами. Если необходимо выполнить уточнение только нейтронных данных, необходимо выяснить, обладает ли соответствующий набор нейтронных данных достаточной полнотой и разрешением.
ORNL предлагает два средства для сбора данных о дифракции нейтронов: лучевую линию IMAGINE на HFIR, а также лучевую линию MaNDi на SNS36,67. Хотя оба прибора обеспечивают эффективные средства для сбора набора данных о дифракции нейтронов с использованием аналогичных принципов, каждый прибор имеет уникальные спецификации, которые следует учитывать при подаче заявки на время луча. IMAGINE собирает квази-Лауэ данные и оптимизирован для сбора данных о комнатной температуре кристаллов с единичными ячейками до ~100 Å. MaNDi может использоваться для сбора данных о комнатной температуре и криотемпературе с использованием сбора TOF-Laue на кристаллах с единичными ячейками до ~ 300 Å. Перед сбором полного набора данных на кристалле проводится тест для оценки качества полученной дифракционной картины, в которой кристалл подвергается воздействию пучка нейтронов в течение одного кадра. Если кристалл имеет достаточное качество, полный набор данных нейтронной дифракции будет собран, проиндексирован, интегрирован, масштабирован и объединен в процессе, аналогичном обработке рентгеновских данных. IMAGINE использует Lauegen и Lscale, а MaNDi использует пакет Mantid и использует трехмерную подгонку профиля48,50,51,68,69,70. Ученым, которые станут пользователями любого из этих объектов, будет предоставлен набор данных в формате MTZ или HKL для дальнейшего анализа.
Нейтронная дифракция является неразрушающим, высокочувствительным методом зондирования состояния протонации и взаимодействия водородных связей биологических макромолекул. Он особенно полезен для фоточувствительных белков и металлопротеинов. Перед проведением эксперимента необходимо принять во внимание несколько соображений, касающихся метода, а также обработки данных, однако результат дает результаты, которые могут дать ценное представление о каталитическом механизме интересующего белка. Кристаллография нейтронного белка дополняет вычислительные, структурные, биохимические и спектроскопические исследования, что делает ее ценным инструментом в наборе методов биолога, используемых для характеристики биологических макромолекул.
Раскрытие информации
Авторам нечего раскрывать.
Благодарности
Эксперименты по экспрессии, очистке и кристаллизации белка проводились в Центре структурной молекулярной биологии (CSMB), пользовательском центре биологических и экологических исследований Министерства энергетики США в Национальной лаборатории Оук-Ридж. Данные о дифракции нейтронов были собраны в BL-11B MaNDi в источнике нейтронов Spallation (SNS) в ORNL, который спонсируется Отделом научных пользовательских установок Управления фундаментальных энергетических наук Министерства энергетики США. Авторы благодарят Брендана Салливана за помощь в сокращении данных. Данные о дифракции рентгеновских лучей были собраны на объектах Центра молекулярного образования, технологий и исследований (METRIC) в Университете штата Северная Каролина, который поддерживается штатом Северная Каролина. GCS частично признает поддержку со стороны Национального исследовательского фонда (NRF), Южной Африки и программы Graduate Opportunities (GO!) в ORNL. FM признает поддержку со стороны USDA NIFA Hatch 211001.
Материалы
| Name | Company | Catalog Number | Comments |
| Absorbent Paper Points Size #30-#40, 60 mm length | DiaDent/DiaVet | 218-292 | |
| Capillary wax | Hampton | HR4-328 | |
| CCP4 | Version 7.0.077 | ||
| Conical Centrifuge Tubes (15 mL) | Corning | CLS430790 | |
| Conical Centrifuge Tubes (50mL) | Corning | CLS430828 | |
| Coot | Version 0.8.9.2 | ||
| CrystalCap ALS | Hampton | HR4-779 | |
| Curved-Tip Forceps | Mitegen | TW-CTF-1 | |
| Deuterium chloride solution, 35 wt. % in D2O, ≥99 atom % D | Sigma-Aldrich | 543047 | |
| Deuterium oxide 99.9 atom % D | Sigma-Aldrich | 151882 | |
| Dual Thickness MicroLoops 1000 µm | Mitegen | M5-L18SP-1000 | |
| FiveEasy pH meter F20-Std-Kit | Mettler Toledo | 30266626 | |
| Foam Dewars Standard Vessel 800 ml | Spearlab | M-FD-800 | |
| Four Color Mounting Clay | Hampton | HR4-326 | |
| HEPES, BioUltra, for molecular biology, ≥99.5% (T), | Sigma-Aldrich | 54457 | |
| High flux rotating anode X-ray diffractomemeter with EIGER 4M detector | Rigaku, Oxford Cryostream and Dectris | XtaLAB Synergy-R | Home source X-ray diffractometer |
| Magnetic Wand Straight | Mitegen | M-R-1013198 | |
| Microloader, tip for filling Femtotips and other glass microcapillaries (for research use only), 0.5 – 20 µL, 100 mm, light gray, 192 pcs. (2 racks × 96 pcs.) | Eppendorf | 930001007 | |
| Microtubes volume 1.5 mL | Eppendorf | Z606340 | |
| Petri Dishes with Clear Lid 100 mm diameter | Fischerbrand | FB0875713 | |
| Phenix | Version 1.14-3260 | ||
| Pin Tong 18 mm | Mitegen | M-R-1013196 | |
| Pipette Volume 0.1-2.5 μL | Eppendorf Research | Z683779 | |
| Pipette Volume 100-1000 μL | Eppendorf Research | Z683825 | |
| Pipette Volume 10-100 μL | Eppendorf Research | Z683809 | |
| Pipette Volume 20-200 μL | Eppendorf Research | Z683817 | |
| Poly(ethylene glycol) BioXtra, average mol wt 3,350, powder | Sigma-Aldrich | P4338 | |
| Quartz Capillary , 1.00 mm inner diameter, 80 mm length | Hampton | HR6-146 | Thin-walled capillary |
| Research Stereomicroscope System | Olympus | SZX16 | |
| Reusable B3 (SSRL/SAM Style) Goniometer Bases | Mitegen | GB-B3-R | |
| Round - Miniature Hollow Glass Tubing (VitroTubes) Clear Fused Quartz / 1.00 mm inner diameter, 100 mm length | VitroCom | CV1012 | Thick-walled capillary |
| Sandwich Box with cover | Hampton | HR3-132 | |
| Siliconized 9 Well Glass Plate | Hampton | HR3-134 | |
| Sitting Drop Crystallization Plate (24 Big Well) | Mitegen | XQ-P-24S-A | |
| Sodium deuteroxide solution, 40 wt. % in D2O, 99 atom % D | Sigma-Aldrich | 176788 | |
| Thick Siliconized circle cover slides (22 mm x 0.96 mm) | Hampton | HR3-247 | |
| Universal Pipet Tips, 0.1 - 10 µL | VWR | 76322-528 | |
| Universal Pipet Tips, 1 - 100 µL | VWR | 76322-136 | |
| Universal Pipet Tips, 100 - 1000 µL | VWR | 76322-154 | |
| Universal Pipet Tips, 20 - 200 µL | VWR | 76322-150 | |
| Universal Pipet Tips, 1 - 20 µL | VWR | 76322-134 | |
| Wax pen | Hampton | HR4-342 |
Ссылки
- Neumann, P., Tittmann, K. Marvels of enzyme catalysis at true atomic resolution: distortions, bond elongations, hidden flips, protonation states and atom identities. Current Opinion in Structural Biology. 29, 122-133 (2014).
- Pynn, R. Neutron Scattering-A Non-destructive Microscope for Seeing Inside Matter. Neutron Applications in Earth, Energy and Environmental Sciences. , 15-36 (2009).
- O'Dell, W. B., Bodenheimer, A. M., Meilleur, F. Neutron protein crystallography: A complementary tool for locating hydrogens in proteins. Archives of Biochemistry and Biophysics. 602, 48-60 (2016).
- Niimura, N., Podjarny, A. . Neutron Protein Crystallography: Hydrogen, Protons, and Hydration in Bio-macromolecules. , (2011).
- Blakeley, M. P. P. Neutron macromolecular crystallography. Crystallography Reviews. 15 (3), 157-218 (2009).
- Blakeley, M. P., Cianci, M., Helliwell, J. R., Rizkallah, P. J. Synchrotron and neutron techniques in biological crystallography. Chemical Society Reviews. 33 (8), 548-557 (2004).
- Ashkar, R., et al. Neutron scattering in the biological sciences: progress and prospects. Acta Crystallographica Section D: Structural Biology. 74 (12), (2018).
- Teixeira, S. C. M., et al. New sources and instrumentation for neutrons in biology. Chemical Physics. 345 (2-3), 133-151 (2008).
- Furrer, A., Mesot, J., Strässle, T. . Neutron Scattering in Condensed Matter Physics. , (2009).
- Meilleur, F., Coates, L., Cuneo, M. J., Kovalevsky, A., Myles, D. A. A. The neutron macromolecular crystallography instruments at Oak Ridge national laboratory: Advances, challenges, and opportunities. Crystals. 8 (10), 1-10 (2018).
- Coates, L., et al. The Macromolecular Neutron Diffractometer MaNDi at the Spallation Neutron Source. Journal of Applied Crystallography. 48, 1302-1306 (2015).
- Coates, L., Stoica, A. D., Hoffmann, C., Richards, J., Cooper, R. The macromolecular neutron diffractometer (MaNDi) at the Spallation Neutron Source, Oak Ridge: enhanced optics design, high-resolution neutron detectors and simulated diffraction. Journal of Applied Crystallography. 43 (3), 570-577 (2010).
- Koetzle, T. F., Piccoli, P. M. B., Schultz, A. J. Single-crystal neutron diffraction studies of hydrogen-bonded systems: Two recent examples from IPNS. Nuclear Instruments and Methods in Physics Research, Section A: Accelerators, Spectrometers, Detectors and Associated Equipment. 600 (1), 260-262 (2009).
- Ng, J. D., et al. Large-volume protein crystal growth for neutron macromolecular crystallography. Acta Crystallographica Section F:Structural Biology Communications. 71, 358-370 (2015).
- Blakeley, M. P., Langan, P., Niimura, N., Podjarny, A. Neutron crystallography: opportunities, challenges, and limitations. Current Opinion in Structural Biology. 18 (5), 593-600 (2008).
- Sears, V. F. Neutron scattering lengths and cross sections. Neutron News. 3 (3), 26-37 (1992).
- Weik, M., Patzelt, H., Zaccai, G., Oesterhelt, D. Localization of glycolipids in membranes by in vivo labeling and neutron diffraction. Molecular Cell. 1 (3), 411-419 (1998).
- Helliwell, J. R. Fundamentals of neutron crystallography in structural biology. Methods in Enzymology. 634, (2020).
- Niimura, N., Bau, R. Neutron protein crystallography: Beyond the folding structure of biological macromolecules. Acta Crystallographica Section A: Foundations of Crystallography. 64 (1), 12-22 (2008).
- Hazemann, I., et al. High-resolution neutron protein crystallography with radically small crystal volumes: Application of perdeuteration to human aldose reductase. Acta Crystallographica Section D: Biological Crystallography. 61 (10), 1413-1417 (2005).
- Niimura, N., Chatake, T., Ostermann, A., Kurihara, K., Tanaka, I. High resolution neutron protein crystallography. Hydrogen and hydration in proteins. Zeitschrift für Kristallographie - Crystalline Materials. 218 (2), (2003).
- Meilleur, F., Contzen, J., Myles, D. A. A., Jung, C. Structural stability and dynamics of hydrogenated and perdeuterated cytochrome P450cam (CYP101). Biochemistry. 43 (27), 8744-8753 (2004).
- Bennett, B. C., Gardberg, A. S., Blair, M. D., Dealwis, C. G. On the determinants of amide backbone exchange in proteins: A neutron crystallographic comparative study. Acta Crystallographica Section D: Biological Crystallography. 64 (7), 764-783 (2008).
- Meilleur, F., Kovalevsky, A., Myles, D. A. A. IMAGINE: The neutron protein crystallography beamline at the high flux isotope reactor. Methods in Enzymology. 634, (2020).
- Wang, X. P., et al. A suite-level review of the neutron single-crystal diffraction instruments at Oak Ridge National Laboratory. Review of Scientific Instruments. 89 (9), 092802 (2018).
- Wlodawer, A., Hendrickson, W. A. A procedure for joint refinement of macromolecular structures with X-ray and neutron diffraction data from single crystals. Acta Crystallographica Section A. 38 (2), 239-247 (1982).
- Halle, B. Biomolecular cryocrystallography: Structural changes during flash-cooling. Proceedings of the National Academy of Sciences of the United States of America. 101 (14), 4793-4798 (2004).
- Adams, P. D., Mustyakimov, M., Afonine, P. V., Langan, P. Generalized X-ray and neutron crystallographic analysis: More accurate and complete structures for biological macromolecules. Acta Crystallographica Section D: Biological Crystallography. 65 (6), 567-573 (2009).
- Berman, H. M., et al. The Protein Data Bank. Acta Crystallographica Section D Biological Crystallography. 58 (6), 899-907 (2002).
- Liebschner, D., Afonine, P. V., Moriarty, N. W., Langan, P., Adams, P. D. Evaluation of models determined by neutron diffraction and proposed improvements to their validation and deposition. Acta Crystallographica Section D: Structural Biology. 74, 800-813 (2018).
- Afonine, P. V., Mustyakimov, M., Grosse-Kunstleve, R. W., Moriarty, N. W., Langan, P., Adams, P. D. Joint X-ray and neutron refinement with phenix.refine. Acta Crystallographica Section D: Biological Crystallography. 66 (11), 1153-1163 (2010).
- Brünger, A. T., et al. Crystallography & NMR system: A new software suite for macromolecular structure determination. Acta Crystallographica Section D: Biological Crystallography. 54 (5), 905-921 (1998).
- Gruene, T., Hahn, H. W., Luebben, A. V., Meilleur, F., Sheldrick, G. M. Refinement of macromolecular structures against neutron data with SHELXL2013. Journal of Applied Crystallography. 47 (1), 462-466 (2014).
- Emsley, P., Lohkamp, B., Scott, W. G., Cowtan, K. Features and development of Coot. Acta Crystallographica Section D Biological Crystallography. 66 (4), 486-501 (2010).
- Lakey, J. H. Neutrons for biologists: A beginner's guide, or why you should consider using neutrons. Journal of the Royal Society Interface. 6, (2009).
- Schröder, G. C., O'Dell, W. B., Myles, D. A. A., Kovalevsky, A., Meilleur, F. IMAGINE: Neutrons reveal enzyme chemistry. Acta Crystallographica Section D: Structural Biology. 74, 778-786 (2018).
- Halsted, T. P., et al. Catalytically important damage-free structures of a copper nitrite reductase obtained by femtosecond X-ray laser and room-temperature neutron crystallography. IUCrJ. 6, 761-772 (2019).
- Meier, K. K., et al. Oxygen Activation by Cu LPMOs in Recalcitrant Carbohydrate Polysaccharide Conversion to Monomer Sugars. Chemical Reviews. 118 (5), 2593-2635 (2018).
- Beeson, W. T., Vu, V. V., Span, E. A., Phillips, C. M., Marletta, M. A. Cellulose Degradation by Polysaccharide Monooxygenases. Annual Review of Biochemistry. 84 (1), 923-946 (2015).
- Walton, P. H., Davies, G. J. On the catalytic mechanisms of lytic polysaccharide monooxygenases. Current Opinion in Chemical Biology. 31, 195-207 (2016).
- Bertini, L., et al. Catalytic Mechanism of Fungal Lytic Polysaccharide Monooxygenases Investigated by First-Principles Calculations. Inorganic Chemistry. 57 (1), 86-97 (2018).
- Hedegård, E. D., Ryde, U. Molecular mechanism of lytic polysaccharide monooxygenases. Chemical Science. 9 (15), 3866-3880 (2018).
- Hangasky, J. A., Detomasi, T. C., Marletta, M. A. Glycosidic Bond Hydroxylation by Polysaccharide Monooxygenases. Trends in Chemistry. 1 (2), 198-209 (2019).
- Bacik, J. P., et al. Neutron and Atomic Resolution X-ray Structures of a Lytic Polysaccharide Monooxygenase Reveal Copper-Mediated Dioxygen Binding and Evidence for N-Terminal Deprotonation. Biochemistry. 56 (20), 2529-2532 (2017).
- O'Dell, W. B., Agarwal, P. K., Meilleur, F. Oxygen Activation at the Active Site of a Fungal Lytic Polysaccharide Monooxygenase. Angewandte Chemie - International Edition. 56 (3), 767-770 (2017).
- O'Dell, W. B., Swartz, P. D., Weiss, K. L., Meilleur, F. Crystallization of a fungal lytic polysaccharide monooxygenase expressed from glycoengineered Pichia pastoris for X-ray and neutron diffraction. Acta Crystallographica Section:F Structural Biology Communications. 73 (2), 70-78 (2017).
- Meilleur, F., et al. The IMAGINE instrument: First neutron protein structure and new capabilities for neutron macromolecular crystallography. Acta Crystallographica Section D: Biological Crystallography. 69 (10), 2157-2160 (2013).
- Helliwell, J. R., et al. The recording and analysis of synchrotron X-radiation Laue diffraction photographs. Journal of Applied Crystallography. 22 (5), 483-497 (1989).
- Nieh, Y. P., et al. Accurate and highly complete synchrotron protein crystal Laue diffraction data using the ESRF CCD and the Daresbury Laue software. Journal of Synchrotron Radiation. 6 (5), 995-1006 (1999).
- Arzt, S., Campbell, J. W., Harding, M. M., Hao, Q., Helliwell, J. R. LSCALE - The new normalization, scaling and absorption correction program in the Daresbury Laue software suite. Journal of Applied Crystallography. 32 (3), 554-562 (1999).
- Sullivan, B., et al. Improving the accuracy and resolution of neutron crystallographic data by three-dimensional profile fitting of Bragg peaks in reciprocal space. Acta Crystallographica Section D: Structural Biology. 74 (11), 1085-1095 (2018).
- Sullivan, B., et al. BraggNet: integrating Bragg peaks using neural networks. Journal of Applied Crystallography. 52 (4), 854-863 (2019).
- Schröder, G. C., O'Dell, W. B., Myles, D. A. A., Kovalevsky, A., Meilleur, F. IMAGINE: Neutrons reveal enzyme chemistry. Acta Crystallographica Section D: Structural Biology. 74, (2018).
- Blum, M. M., et al. Preliminary time-of-flight neutron diffraction study on diisopropyl fluorophosphatase (DFPase) from Loligo vulgaris. Acta Crystallographica Section F: Structural Biology and Crystallization Communications. 63 (1), 42-45 (2007).
- Tomanicek, S. J., et al. Neutron and X-ray crystal structures of a perdeuterated enzyme inhibitor complex reveal the catalytic proton network of the Toho-1 β-lactamase for the acylation reaction. Journal of Biological Chemistry. 288 (7), 4715-4722 (2013).
- Metcalfe, C., et al. The tuberculosis prodrug isoniazid bound to activating peroxidases. Journal of Biological Chemistry. 283 (10), 6193-6200 (2008).
- Hughes, R. C., et al. Inorganic pyrophosphatase crystals from Thermococcus thioreducens for X-ray and neutron diffraction. Acta Crystallographica Section F: Structural Biology and Crystallization Communications. 68 (12), 1482-1487 (2012).
- Bennett, B. C., Meilleur, F., Myles, D. A. A., Howell, E. E., Dealwis, C. G. Preliminary neutron diffraction studies of Escherichia coli dihydrofolate reductase bound to the anticancer drug methotrexate. Acta Crystallographica Section D: Biological Crystallography. 61 (5), 574-579 (2005).
- Snell, E. H., et al. Optimizing crystal volume for neutron diffraction: D-xylose isomerase. European Biophysics Journal. 35 (7), 621-632 (2006).
- Golden, E., Attwood, P. V., Duff, A. P., Meilleur, F., Vrielink, A. Production and characterization of recombinant perdeuterated cholesterol oxidase. Analytical Biochemistry. 485, 102-108 (2015).
- Munshi, P., et al. Rapid visualization of hydrogen positions in protein neutron crystallographic structures. Acta Crystallographica Section D: Biological Crystallography. 68 (1), 35-41 (2012).
- Logan, D. T. Interactive model building in neutron macromolecular crystallography. Methods in Enzymology. 634, (2020).
- Koruza, K., Lafumat, B., Végvári, W., Knecht, S. Z., Fisher, Deuteration of human carbonic anhydrase for neutron crystallography: Cell culture media, protein thermostability, and crystallization behavior. Archives of Biochemistry and Biophysics. 645, 26-33 (2018).
- Fisher, S. J., et al. Perdeuteration: Improved visualization of solvent structure in neutron macromolecular crystallography. Acta Crystallographica Section D: Biological Crystallography. 70 (12), 3266-3272 (2014).
- Chen, J. C. H., Hanson, B. L., Fisher, S. Z., Langan, P., Kovalevsky, a. Y. Direct observation of hydrogen atom dynamics and interactions by ultrahigh resolution neutron protein crystallography. Proceedings of the National Academy of Sciences. 109 (38), 15301-15306 (2012).
- Cuypers, M. G., et al. Near-atomic resolution neutron crystallography on perdeuterated Pyrococcus furiosus rubredoxin: Implication of hydronium ions and protonation state equilibria in redox changes. Angewandte Chemie - International Edition. 52 (3), 1022-1025 (2013).
- Coates, L., Sullivan, B. The macromolecular neutron diffractometer at the spallation neutron source. Methods in Enzymology. 634, (2020).
- Ren, Z., Kingman, N. G., Borgstahl, G. E. O., Getzoff, E. D., Moffat, K. Quantitative Analysis of Time-Resolved Laue Diffraction Patterns. Journal of Applied Crystallography. 29 (3), 246-260 (1996).
- Campbell, J. W., Hao, Q., Harding, M. M., Nguti, N. D., Wilkinson, C. LAUEGEN version 6.0 and INTLDM. Journal of Applied Crystallography. 31 (3), 496-502 (1998).
- Arnold, O., et al. Mantid - Data analysis and visualization package for neutron scattering and μ SR experiments. Nuclear Instruments and Methods in Physics Research, Section A: Accelerators, Spectrometers, Detectors and Associated Equipment. 764, 156-166 (2014).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены