Method Article
Полная и субрегиональная количественная оценка бета-амилоидной нагрузки на участки мозга мыши
В этой статье
Резюме
Настоящий протокол описывает и сравнивает процедуру выполнения анализа полной области или субрегиона, представляющего интерес, сагиттальных участков мозга мыши для количественной оценки бета-амилоидной нагрузки в трансгенной мышиной модели болезни Альцгеймера APP/PS1.
Аннотация
Внеклеточное накопление бета-амилоидных (Aβ) бляшек является одним из основных патологических признаков болезни Альцгеймера (AD) и является целью единственного одобренного FDA лечения AD, модифицирующего заболевание. Соответственно, использование трансгенных мышиных моделей, которые чрезмерно экспрессируют белок-предшественник амилоида и тем самым накапливают церебральные Aβ-бляшки, широко используются для моделирования БА человека у мышей. Поэтому иммуноанализы, включая иммуноферментный анализ (ИФА) и иммуноокрашивание, обычно измеряют нагрузку Aβ в тканях мозга, полученных от трансгенных мышей AD. Хотя методы обнаружения и количественной оценки Aβ были хорошо установлены и задокументированы, о влиянии размера интересующей области, выбранной в ткани мозга, на измерения нагрузки Aβ после иммуноокрашивания не сообщалось. Таким образом, текущий протокол направлен на сравнение измерений нагрузки Aβ в полных и подобластных областях, представляющих интерес, с использованием программного обеспечения для анализа изображений. Этапы, связанные с подготовкой мозговой ткани, иммуноокрашиванием свободно плавающей секции мозга, визуализацией и количественной оценкой нагрузки Aβ в полных и подобластях, представляющих интерес, описаны с использованием участков мозга, полученных от 13-месячных двойных трансгенных самцов мышей APP / PS1. Текущий протокол и результаты предоставляют ценную информацию о влиянии размера интересующей области на количественную оценку Aβ-положительной области и показывают сильную корреляцию между Aβ-положительной областью, полученной с использованием полного и суб-областей, представляющих интерес для анализов участков мозга, полученных от 13-месячных самцов мышей APP / PS1, которые показывают широко распространенное осаждение Aβ.
Введение
Болезнь Альцгеймера (БА), шестая по значимости причина смерти в Соединенных Штатах, продолжает представлять угрозу общественному здравоохранению, и, по оценкам, 6,2 миллиона американцев живут с БА. Ожидается, что к 2060году этот показатель достигнет 13,8 млн. На сегодняшний день симптоматическое лечение с помощью таких препаратов, как ингибиторы холинэстеразы и мемантин, является основным курсом лечения2. АД характеризуется нейропатологическими проявлениями, такими как внеклеточное отложение бета-амилоид-(Aβ) бляшек и внутриклеточное гиперфосфорилированное накопление тау в виде нейрофибриллярных клубков 3,4. Образуясь эндопротеолитическим расщеплением белка-предшественника амилоида (APP) через бета- и гамма-секретазу, Aβ агрегируется с образованием олигомеров и фибрилл, что приводит к нейротоксическим эффектам5. Предполагается, что Aβ выполняет основную патологическую роль с 1980-х годов и является терапевтической мишенью единственной одобренной FDA терапии, модифицирующей заболевание для AD6. В результате трансгенные мышиные модели AD, содержащие мутации в генах, приводящие к надежному накоплению Aβ в мозге, широко используются для доклинических исследований AD с начала 1990-х годов7.
Обнаружение видов Aβ в этих трансгенных мозгах мышей AD обычно осуществляется с использованием двух иммуноанализов: иммуноферментного анализа (ИФА) и иммуноокрашивания. Первый анализ позволяет количественно определять различные виды Aβ и является менее трудоемким по сравнению с иммуноокрашиванием, которое требует нескольких последовательных этапов обработки и визуализации тканей, включая сечение ткани, иммуноокрашивание, визуализацию и количественную оценку8. Далее результаты, полученные после иммуноокрашивания, являются полуколичественными8. Однако способность пространственно локализовать Aβ делает иммуноокрашивание привлекательным подходом для обнаружения Aβ в тканях мозга8.
При использовании иммуноокрашивания Aβ различными исследовательскими группами было использовано несколько различных парадигм количественной оценки. Например, некоторые исследовательские группы количественно оценивают нагрузку Aβ во всей интересующей области (кора или гиппокамп), в то время как другие количественно оценивают нагрузку Aβ в определенной подобласти интереса (часть коры или гиппокампа) 9,10,11. Хотя методы обнаружения и количественной оценки Aβ были хорошо установлены и задокументированы, о влиянии размера интересующей области на измерения нагрузки Aβ после иммуноокрашения не сообщалось. Таким образом, текущий протокол направлен на сравнение измерений нагрузки Aβ в полных и подрайонах, представляющих интерес, с использованием программного обеспечения для анализа изображений ImageJ.
В текущем исследовании использовались 13-месячные двойные трансгенные самцы мышей APP / PS1, которые экспрессируют химерную мышь / человека APP и мутантный пресенилин 1, для моделирования раннего начала AD12. Отложения Aβ начинают развиваться к 6-7-месячному возрасту, а обильное накопление Aβ наблюдается как в коре, так и в гиппокампе этих мышей к 9-10 месяцам12-летнего возраста. Трансгенные амилоидные пептиды и голопротеин могут быть обнаружены с помощью 6E10-иммуноокрашивания13, что делает его желательной моделью животного для настоящего протокола. Процедура, описанная в настоящем описании, включает подготовку ткани головного мозга, иммуноокрашивание свободно плавающих участков, визуализацию и количественную оценку нагрузки Aβ в полных по сравнению с субрегистраторами, представляющими интерес. Анализ показывает сильную корреляцию между полной и субрегиональной количественной оценкой, что указывает на надежное согласие между этими двумя методами в участках мозговой ткани, полученных от 13-месячных самцов мышей APP / PS1, которые показывают обильные отложения Aβ.
протокол
Все эксперименты на животных проводились в соответствии с Университетскими лабораторными ресурсами животных в соответствии с протоколами, утвержденными Калифорнийским университетом в Ирвине, Институциональным комитетом по уходу за животными и их использованию. Эксперименты проводились на самцах мышей B6C3-Tg(APPswe, PSEN1dE9)85Dbo/Mmjax (APP/PS1) (13-месячный, n = 35). Мыши были получены из коммерческих источников (см. Таблицу материалов).
1. Подготовка мозговой ткани
- Обезболивание мышей с использованием смертельной дозы анестетика на основе фенитоина/пентобарбитала (150 мг/кг), вводимого внутрибрюшинно (см. Таблицу материалов) в соответствии с утвержденными протоколами для животных. Выполняйте сердечную перфузию ледяным фосфатно-буферным физиологическим раствором (1x PBS) в течение 5 мин со скоростью 5 мл/мин для очистки сосудистой системы мозга14.
- Соберите мозговую ткань после ранее опубликованного отчета15, разделите на левое и правое полушария головного мозга и поместите правый геми-мозг каждой мыши в коническую трубку объемом 15 мл, содержащую 5 мл свежеприготовленного 4% раствора параформальдегида (PFA) в 1x PBS в течение 72 ч при 4 °C.
ПРИМЕЧАНИЕ: Мозг может фиксироваться погружением от 24 до 72 ч в зависимости от изучаемого антигена. Левый геми-мозг, без мозжечка, может быть заморожен в жидком азоте, а затем сохранен при -80 ° C с последующей обработкой для биохимических анализов, таких как ИФА и биохимическое обнаружение Aβ16.
ВНИМАНИЕ: PFA является вероятным канцерогеном, и контакт кожи с PFA может привести к аллергическим кожным симптомам. Используйте нитриловые или бутиловые перчатки, маски и средства защиты глаз для работы с ним и готовьтесь под химическим вытяжным капюшоном. - После инкубации в 4% PFA инкубируют геми-мозг последовательно в 5 мл 10%, 20% и 30% растворов сахарозы, приготовленных в 1x PBS в течение 24 ч, каждый при 4 °C до тех пор, пока ткань мозга не опустится на дно конической трубки.
- После инкубации в 30% растворе сахарозы удалить геми-мозг, аккуратно нанести мозг на фильтровальную бумагу, чтобы удалить лишний раствор сахарозы, и заморозить неподвижный геми-мозг в порошкообразном сухом льду на 30 мин. Храните замороженный геми-мозг в хорошо маркированной алюминиевой фольге при -80 °C до криосекции.
ПРИМЕЧАНИЕ: В текущем протоколе геми-мозг хранился при -80 °C в течение 6-8 месяцев. - Разделите замороженный геми-мозг на участки толщиной 20 мкм с помощью криостата (см. Таблицу материалов).
ПРИМЕЧАНИЕ: Для текущего протокола геми-мозги были разделены на сагиттальные сечения, и при необходимости корональные сечения также могут быть подготовлены17. Шаг 2 предназначен для иммунофлуоресцентного окрашивания Aβ на фиксированных и криопротещенных образцах тканей головного мозга.
2. Иммунофлуоресценция
- Поместите сагиттальные участки мозговой ткани (шаг 1,5) в 24-луночную пластину (до шести участков мозга мыши на 300 мкл на лунку). Мойте в течение 5 мин с 1x PBS три раза при комнатной температуре (23 °C), поместив тарелку на шейкер с легким закручиванием.
- Инкубируют участки мозговой ткани 70% муравьиной кислотой в dH20 при комнатной температуре в течение 10 мин.
ВНИМАНИЕ: Муравьиная кислота является коррозионной, поэтому избегайте контакта с кожей и глазами. - Промыть участки мозговой ткани в течение 5 мин с dH20 три раза при комнатной температуре.
- Блокируют неспецифическое связывание с 0,5% бычьим сывороточным альбумином (BSA) и 0,3% TritonX 100 (см. Таблицу материалов) в 1x PBS при комнатной температуре в течение 1 ч.
- Инкубируют участки мозговой ткани меченым флуорофором первичным антителом (6E10, см. Таблицу материалов), разбавленным (1:1000) в 1x PBS, содержащем 0,3% TritonX 100 при 4 °C в течение 24 ч.
ПРИМЕЧАНИЕ: Поскольку первичное антитело является флуорофор-конъюгированным, пластина должна быть покрыта с этого шага вперед, или вся работа должна быть выполнена в темной комнате для поддержания эффективности флуорофора. - Промывайте участки мозговой ткани в течение 10 мин с 1x PBS три раза при комнатной температуре.
- Установите участки мозговой ткани на положительно заряженные стеклянные слайды (см. Таблицу материалов), которые хорошо маркированы (информация о этикетке на слайде основана на предпочтениях), после кратковременной промывки с dH20 для удаления оставшихся солей. Дайте слайдам высохнуть на воздухе в темноте.
ПРИМЕЧАНИЕ: Секции мозга должны быть смонтированы осторожно, чтобы избежать складок и разрывов, влияющих на количественную оценку данных. В случае разрывов и/или складок, которые лежат в интересующей области и могут помешать количественной оценке данных, рекомендуется повторное окрашивание и повторный монтаж. - Установите участки мозговой ткани с помощью водной крепежной среды (см. Таблицу материалов) и поместите стеклянный покров поверх ткани. Запечатайте концы крышки прозрачным лаком для ногтей и храните слайды в слайд-боксе при температуре 4 °C до получения изображения.
ПРИМЕЧАНИЕ: В текущем протоколе слайды были изображены в течение 1 месяца после окрашивания.
3. Визуализация
- Изобразите окрашенные 6E10 участки мозга с помощью флуоресцентного (эпифлуоресцентного или конфокального) микроскопа (см. Таблицу материалов), который имеет 2-кратную цель для захвата всего участка ткани мозга на одном изображении и оснащен соответствующим фильтром (GFP в этой работе).
ПРИМЕЧАНИЕ: Параметры изображения должны быть согласованы на разных слайдах. - Сохраните захваченные изображения в виде файла TIFF или по мере необходимости и откройте их в программном обеспечении для анализа изображений (см. Таблицу материалов), как описано в шаге 4.2 ниже для количественной оценки 6E10.
ПРИМЕЧАНИЕ: Включите шкалу масштаба перед захватом изображения для количественной оценки в программном обеспечении для анализа изображений ImageJ.
4. Анализ полной области интереса
ПРИМЕЧАНИЕ: Двумя областями, представляющими интерес для настоящей работы, являются гиппокамп и изокора. Анализ полной области интереса представляет собой анализ всей изокоре (называемой корой в будущем) или гиппокампа в изображенном участке ткани мозга.
- Загрузите программное обеспечение для анализа изображений (см. Таблицу материалов) и запустите программное обеспечение после установки.
- Как только программное обеспечение запустится, нажмите «Файл | Открыть | Выберите изображение для анализа.
- Нажмите на Анализ | Установить масштаб| Нажмите, чтобы удалить масштаб. Выберите инструмент «Прямой» на панели инструментов программного обеспечения и нарисуйте прямую линию по длине шкалы. Нажмите на Анализ | Мера. Обратите внимание на длину или расстояние шкалы масштаба в пикселях. Нажмите на Анализ | Установите масштаб.
- Во всплывающем окне введите расстояние в пикселях, известное расстояние шкалы (в данном случае в мкм) и единицу длины как мкм. Установите флажок Глобальный, чтобы применить новый параметр масштабирования ко всем следующим изображениям, если обрабатывается несколько изображений. Нажмите кнопку ОК, чтобы применить параметры.
ПРИМЕЧАНИЕ: Перед дальнейшим анализом всегда рекомендуется проверить, применяется ли к изображению точная шкала.
- Во всплывающем окне введите расстояние в пикселях, известное расстояние шкалы (в данном случае в мкм) и единицу длины как мкм. Установите флажок Глобальный, чтобы применить новый параметр масштабирования ко всем следующим изображениям, если обрабатывается несколько изображений. Нажмите кнопку ОК, чтобы применить параметры.
- Чтобы задать нужное измерение по площади участка, перейдите в раздел Анализ | Установка | измерений Выберите поля Область и Отображаемая метка. Убедитесь, что анализируемое изображение выбрано в разделе Перенаправить на.
- Для удобства визуализации гиппокампа или коры перейдите в image | Отрегулируйте | Яркость/Контрастность. Постепенно перетаскивайте ползунок «Максимум » влево, чтобы увеличить прозрачность тканей до тех пор, пока не будут идентифицированы интересующие области мозга.
ПРИМЕЧАНИЕ: Не применяйте эту настройку, чтобы избежать ложных измерений во время анализа, вместо этого переходите к следующему шагу. - Используйте инструмент «Выделение «Полигон» или «Свободная от руки», чтобы очертить область гиппокампа. Нажмите на опцию «Сброс» настроек «Яркость/контрастность », как только гиппокамп будет очерчен, чтобы вернуться к исходной яркости.
ПРИМЕЧАНИЕ: Шаги должны быть повторены отдельно для кортикальной области. - Чтобы измерить общую площадь ткани выбранной области, нажмите на Редактировать | Очистите снаружи. После того, как выбранная область станет единственным изображением на экране, нажмите «Анализировать | Измерьте , чтобы получить общую площадь ткани , проанализированную во всплывающем окне. Сохраните данные в файле Excel для последующего использования.
- Чтобы измерить положительную область 6E10, перейдите в раздел Image | Отрегулируйте | Цветовой порог. Готовый фильтр в соответствии с методом Thresholding обычно обеспечивает желаемые результаты, выделяя самые сильные сигналы красным цветом.
ПРИМЕЧАНИЕ: Оптимальный выбор порога будет зависеть от фона изображения и интенсивности окрашивания. Выберите пороговое значение, которое подбирает пятно, а не фон. - После выбора соответствующего порогового значения установите флажок Темный фон. Это подчеркнет пятна Aβ (пятно, представляющее интерес) на черном фоне. Нажмите на Выбрать | Оригинал | Выбирайте, подавая темные сигналы (отложения Aβ) на белом фоне. Нажмите на Анализ | Проанализируйте частицы и нажмите кнопку «ОК » при создании всплывающего окна.
- Скопируйте сводные выходные данные, сгенерированные программным обеспечением, щелкнув Редактировать | Копия. Вставьте в ранее запущенный файл Excel с соответствующими метками. Это 6E10-положительная область в выбранных областях интереса (гиппокамп или кора).
ПРИМЕЧАНИЕ: В Excel будет столбец для общей положительной площади 6E10 (шаг 4.10) и общей площади ткани (шаг 4.7). - Рассчитайте 6E10-положительную площадь (%) следующим образом16: (Общая 6E10-положительная площадь / Общая проанализированная площадь ткани) x 100.
5. Анализ интересующего субрегиона
ПРИМЕЧАНИЕ: Анализ подобласти представляет собой анализ части коры или гиппокампа в изображенном участке ткани мозга.
- Загрузите программное обеспечение для анализа изображений и запустите программное обеспечение после установки.
- Как только программное обеспечение запустится, нажмите «Файл | Открыть | Выберите изображение для анализа.
- Нажмите на Анализ | Установить масштаб| Нажмите, чтобы удалить масштаб. Выберите инструмент «Прямая» на панели инструментов программного обеспечения и нарисуйте прямую линию по длине шкалы. Нажмите на Анализ | Мера. Обратите внимание на длину или расстояние шкалы масштаба в пикселях. Нажмите на Анализ | Установите масштаб.
- Во всплывающем окне введите расстояние в пикселях, известное расстояние шкалы (в данном случае в мкм), и введите единицу длины как мкм. Установите флажок Глобальный, чтобы применить новый параметр масштабирования ко всем следующим изображениям, если обрабатывается несколько изображений. Нажмите кнопку ОК, чтобы применить параметры.
ПРИМЕЧАНИЕ: Перед дальнейшим анализом всегда рекомендуется проверить, применяется ли к изображению точная шкала.
- Во всплывающем окне введите расстояние в пикселях, известное расстояние шкалы (в данном случае в мкм), и введите единицу длины как мкм. Установите флажок Глобальный, чтобы применить новый параметр масштабирования ко всем следующим изображениям, если обрабатывается несколько изображений. Нажмите кнопку ОК, чтобы применить параметры.
- Чтобы установить нужное измерение по площади участка, перейдите в раздел Анализ | Установка | измерений выберите поля Область и Отображаемая метка. Убедитесь, что анализируемое изображение выбрано в разделе Перенаправить на.
- Отрегулируйте яркость и контрастность, если изображение слишком тусклое, а области мозга (например, гиппокамп или кора в данном случае) не могут быть легко идентифицированы. Используйте панель инструментов программного обеспечения и нажмите на Image | Отрегулируйте | Яркость/Контрастность и перетащите ползунки «Максимальное значение » влево по мере необходимости, чтобы увеличить видимость ткани.
ПРИМЕЧАНИЕ: Не применяйте эту настройку, чтобы избежать ложных измерений во время анализа, вместо этого переходите к следующему шагу. - С помощью инструмента «Прямоугольник» выберите интересующую область в коре головного мозга или гиппокампе. Используйте панель инструментов и нажмите редактировать | | выбора Укажите, изменив высоту и ширину на заданное значение. Отрегулируйте коробку, чтобы она была полностью покрыта тканью. Сбросьте яркость/контрастность, чтобы вернуться к исходной яркости.
ПРИМЕЧАНИЕ: Размер поля, используемого для выбора областей интереса, должен быть одинаковым для всех изображений. Для настоящего анализа размер коробки составлял либо 300 пикселей x 300 пикселей (что эквивалентно 1177 мкм x 1177 мкм), либо 400 пикселей x 200 пикселей (что эквивалентно 1569 мкм x 784 мкм). - Продублируйте выбранную область интереса, щелкнув правой кнопкой мыши поле и выбрав Дублировать. Откроется новое окно с выбранным регионом. Переименуйте дублированное изображение, чтобы отобразить область, в которой оно находится (например, кора или гиппокамп).
- Отрегулируйте повторяющийся тип изображения, используя панель инструментов и щелкнув Изображение | Тип | 8-бит для преобразования дублированного RGB-изображения в 8-битное для лучшего анализа бляшек. Инвертируйте изображение, нажав на Редактировать | Инвертировать.
- Чтобы измерить положительную область 6E10, перейдите в раздел Image | Отрегулируйте | Порог. Предопределенный фильтр в методе Thresholding обычно обеспечивает желаемые результаты, выделяя самые сильные сигналы красным цветом.
ПРИМЕЧАНИЕ: Оптимальный выбор порога будет зависеть от фона изображения и интенсивности окрашивания. Выберите пороговое значение, которое подбирает пятно, а не фон. - После выбора соответствующего порогового значения нажмите кнопку Применить.
- Чтобы проанализировать область 6E10-positive, воспользуйтесь панелью инструментов и нажмите « Анализировать | Анализируйте частицы, проверяя «Итоговые результаты».
- Скопируйте выходные данные Сводки с %Областью , сгенерированной программным обеспечением, щелкнув Изменить | Копия. Вставьте в ранее запущенный файл Excel с соответствующими метками.
- Повторите шаги 5.3-5.12 для различных областей в ткани. Убедитесь, что расположение каждого поля для очерчивания интересующей области согласовано между каждым изображением.
ПРИМЕЧАНИЕ: Инструмент поворота можно использовать, если размеры прямоугольного набора инструментов не могут поместиться в указанную область из-за искривления ткани. - Чтобы повернуть прямоугольник, используйте панель инструментов и нажмите редактировать | | выбора При необходимости поверните и отрегулируйте степень вращения. Продублируйте изображение, как указано в шаге 5.7, и очистите его снаружи, используя панель инструментов и нажав « Редактировать | Очистка снаружи, которая очищает пятна 6E10 за пределами указанного прямоугольника. Перейдите к шагу 5.8, описанному выше.
Результаты
Здесь сравниваются два разных метода для количественной оценки 6E10-положительной области в гиппокампе и коре тканей мозга мыши. Этими двумя методами являются анализ всего региона и субрегиона, представляющего интерес (рисунок 1). Анализ полной области интереса, как следует из названия, включает в себя выделение всей интересующей области (в данном случае либо изокоры, либо гиппокампа) для определения положительной области 6E10 (рисунок 1A, B). Анализ подрайона, представляющего интерес, включает в себя выбор заранее определенного региона в интересующем регионе для определения положительной области 6E10 (рисунок 1C, D). Пошаговый протокол ImageJ для двух методов показан на рисунке 2, рисунке 3 и рисунке 4.
В этом исследовании использовались три читателя; два независимых читателя выполнили анализ субрегиона интереса, а третий читатель выполнил полный анализ области интереса. Как видно на рисунке 5A,B, наблюдалась сильная значимая положительная корреляция (p < 0,0001) между 6E10-положительной областью, о которой сообщили два читателя, выполняющие анализ подобласти (коэффициент корреляции Пирсона r = 0,97 для коры и r = 0,96 для гиппокампа). 6E10-положительные области, о которых сообщили два читателя для анализа подрайона интереса, были усреднены, а усредненная подобласть интереса 6E10-положительная область имела сильную значительную положительную корреляцию (p < 0,0001) с 6E10-положительной областью, полученной с использованием анализа полной области интереса для обеих коры (коэффициент корреляции Пирсона r = 0,96; Рисунок 5C) и гиппокамп (коэффициент корреляции Пирсона r = 0,95; Рисунок 5D). Средняя кортикальная и гиппокампальная-6E10-положительная область, полученная анализами полной области и субрегиона, представляющей интерес, была сопоставима без существенных различий, что подтверждает согласие между двумя методами (рисунок 5E). Кроме того, нерастворимый Aβ1-42 измеряли в гомогенатах всего мозга у подмножества мышей, а кортикальная (рисунок 5F) и гиппокампальная (рисунок 5G) 6E10-положительная область, определенная анализом полной области интереса, была достоверно (p < 0,01) коррелировала с нерастворимой нагрузкой Aβ1-42 с использованием ИФА (см. Таблицу материалов).
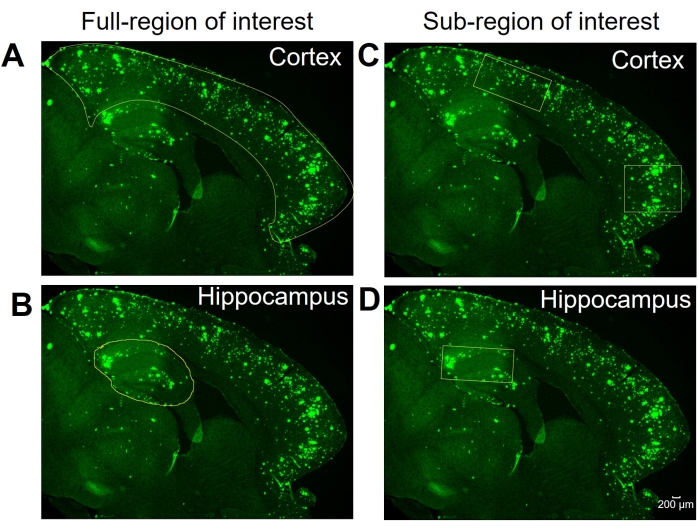
Рисунок 1: Выбор полных и подрайонов, представляющих интерес. Репрезентативные изображения, показывающие полную изокорку (кору) и гиппокамп, очерченные для анализа полной области интереса в (A) и (B) соответственно. Репрезентативные изображения показывают выбор подобластий коры головного мозга и гиппокампа для анализа интересующей субрегионы в (C) и (D) соответственно. Шкала = 200 мкм. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
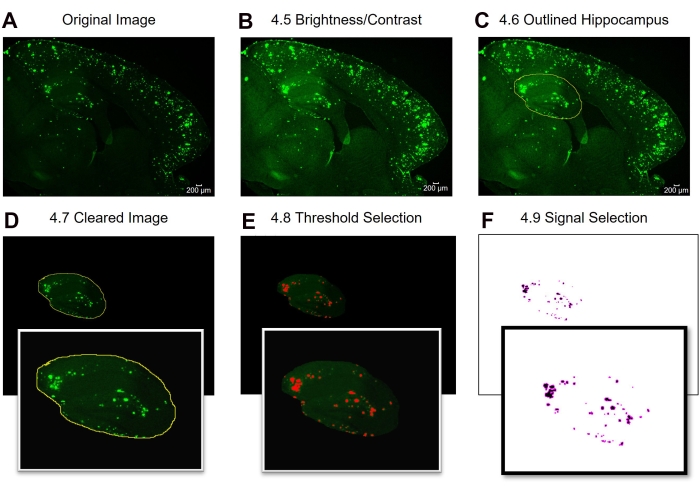
Рисунок 2: Протокол для полной области, представляющей интерес 6E10- положительной количественной оценки области. Этапы анализа изображения, показывающие исходное изображение (A), изображение после регулировки яркости / контрастности (B), выбор интересующей области (C), очистку (D), настройку порога (E) и окончательное изображение, готовое к анализу (F). Цифры на рисунке обозначают номера шагов в протоколе. Шкала = 200 мкм. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
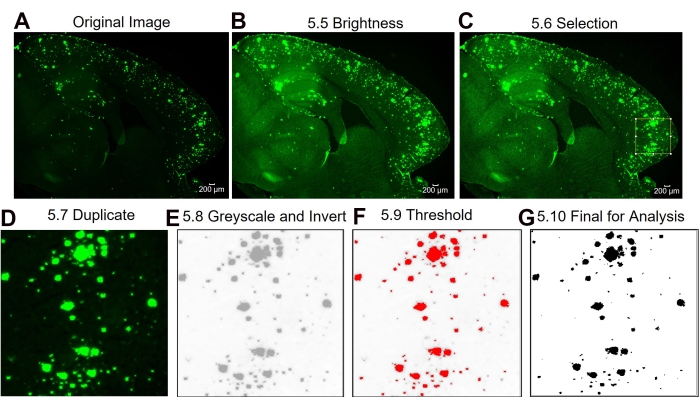
Рисунок 3: Протокол для субрегиона, представляющего интерес 6E10 - количественная оценка положительной области. Этапы анализа изображения, показывающие исходное изображение (A), изображение после регулировки яркости / контрастности (B), выбор области интереса (C), дублирование изображения интересующей области (D), изменение изображения на 8-бит и инвертирование изображения (E), регулировка порога (F) и окончательное изображение, готовое к анализу (G). Цифры на рисунке обозначают номера шагов в протоколе. Шкала = 200 мкм. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
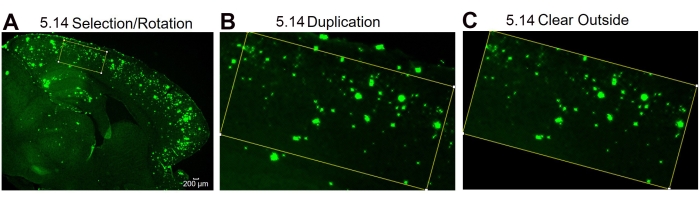
Рисунок 4: Протокол для региона ротации интересов. Этапы анализа изображения, показывающие выделение интересующей области и вращение поля выделения в соответствии с кривизной ткани (A), изображение интересующей области после дублирования (B) и изображение после очистки внешней (не представляющей интерес области) области (C). Цифры на рисунке обозначают номер шага в протоколе. Шкала бара = 200 мкм. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
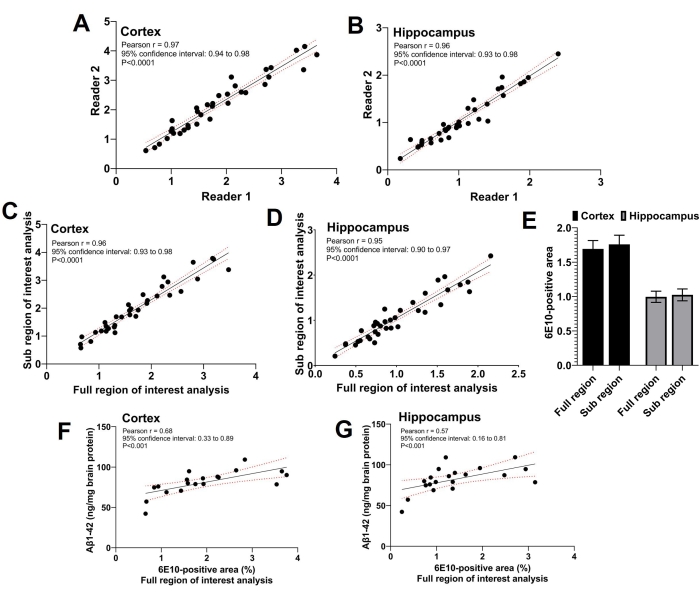
Рисунок 5: Корреляция между полным и субрегионами, представляющими интерес для анализа. Точечные графики показывают корреляцию между 6E10-положительной областью двумя независимыми читателями, выполняющими анализ подобласти интереса для коры (A) и гиппокампа (B). Сильная положительная корреляция наблюдается между 6E10-положительной областью, полученной в результате анализа субобласти интереса, и анализа полной области интереса как для коры (C), так и для гиппокампа (D). Статистически значимой разницы в средней 6E10-положительной области по полной интересующей области и субобласти интереса в коре и гиппокампе (E) нет статистически значимой разницы. Наблюдается значительная корреляция между гомогенатными нерастворимыми измерениями Aβ1-42 всего мозга с использованием ИФА и анализом полной области интереса как для коры (F), так и для гиппокампа (G). Данные анализировались с использованием коэффициента корреляции Пирсона, r, в (A-D) и (F-G), и с использованием двусторонних повторных измерений ANOVA в (E) с использованием графического и статистического программного обеспечения. Данные представлены в виде средней ± стандартной погрешности среднего (SEM) n = 35 мышей в (E), а двуххвостый p < 0,05 считался статистически значимым. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Обсуждение
Протокол, описанный в настоящем описании, описывает процедуру подготовки геми-мозга к сагиттальному сечению, иммунофлуоресцентное окрашивание отложений Aβ с использованием антитела 6E10 на свободно плавающих участках, визуализацию окрашенных Aβ участков мозга с последующей количественной оценкой отложений Aβ в коре и гиппокампе ткани мозга мыши с использованием программного обеспечения для анализа изображений. Хотя существуют опубликованные протоколы для количественной оценки нагрузки Aβ в разделах 8,10 ткани мозга, этот протокол описывает этапы, участвующие в количественной оценке нагрузки Aβ во всей изокоре (называемой корой) и гиппокампе по сравнению с нагрузкой Aβ в подобласти, представляющей интерес в коре и гиппокампе, когда это может быть желательно. Также приведена корреляция между полным и субрегионами, представляющими интерес для анализа.
В протоколе есть несколько критических шагов. Во-первых, описанный протокол предназначен для участков мозговой ткани толщиной 20 мкм, подвергающихся свободно плавающему иммуноокрашиванию, что приводит к оптимальному проникновению антител в участок18 ткани. Метод свободного плавания может потребовать ручного переноса участков ткани между различными растворами во время иммунофлуоресцентного окрашивания и тщательного обращения с участками ткани на протяжении всей процедуры. Это особенно важно, когда участки ткани погружены в 70% раствор муравьиной кислоты для извлечения антигена в текущем протоколе, увеличивая хрупкость тканей для тонких участков. Альтернативные подходы к описанному протоколу включают использование более толстых участков ткани (например, 30-40 мкм) или использование участков ткани, которые непосредственно монтируются на положительно заряженные слайды перед иммунофлуоресцентным окрашиванием. Во-вторых, в протоколе, описанном в настоящем описании, используется флуоресцентно меченое антитело 6E10. Помимо использования флуоресцентно меченого антитела 6E10, нефлуоресцентные антитела 6E10 (например, конъюгированное антитело 6E10 с пероксидазой хрена) также могут быть использованы для обнаружения нагрузки Aβ в участках ткани мозга, и текущий протокол может быть адаптирован для количественной оценки Aβ-положительных иммунохимических пятен в участках ткани мозга, как описано ранее8 . В-третьих, точность результатов количественной оценки нагрузки Aβ будет зависеть от соответствующего порогового выбора в аналитическом программном обеспечении, которое зависит от фона ткани и интенсивности сигнала. Выбор порогового значения должен быть выполнен конечным пользователем таким образом, чтобы для количественной оценки отбирались только Aβ-положительные пятна. Вмешательство конечного пользователя требуется для оптимизации конкретного порогового значения, которое может быть применено ко всем изображениям для обеспечения точности установки порога. В-четвертых, поскольку анализ подрайона интереса требует выбора небольшой области интереса в тканевом разделе, для этого анализа были использованы два независимых читателя. Для сохранения независимости и ослепления во время сбора данных все изображения были закодированы номером; последовательность анализа изображений была рандомизирована между читателями таким образом, что разные читатели анализировали разные изображения в любой момент времени, и данные представлялись в конце каждой недели. В связи с повышенной вероятностью межсчитывающей изменчивости в области выбора интересующей области в анализе подрайон интереса, читатели были обучены с использованием нескольких образцов изображений для оптимизации выбора области в коре головного мозга и гиппокампе перед началом сбора данных. Это обучение имеет решающее значение для снижения вариабельности между читателями, и, как видно (рисунок 5A, B), положительная область 6E10, о которой сообщают оба читателя, показывает сильное относительное согласие в текущем исследовании.
Текущий протокол и результаты предоставляют ценную информацию о влиянии размера интересующей области на количественную оценку Aβ-положительной области. Ожидается, что большая область интереса будет представлять ткань больше, чем меньшая область интереса. Поэтому отбор проб более крупной ткани желателен для точной количественной оценки нагрузки Aβ в тканях. Однако в случае однородного распределения нагрузки Aβ внутри ткани меньшая область выборки обычно считается хорошим представлением более крупной исследуемой ткани. Текущие результаты исследования подтверждают это, и нагрузка Aβ во всей коре головного мозга и гиппокампе была сильным коррелятом нагрузки Aβ в выбранной подобласти коры и гиппокампа (рисунок 5C, D). Чтобы еще больше подтвердить согласие между полным и субрегистраторами, представляющими интерес, сравнивали среднюю 6E10-положительную область в коре головного мозга и гиппокампе, и не было обнаружено никакой разницы между двумя методами (рисунок 5E). Это подтверждает, что любой из этих методов (полный или субрегиональный анализ) дает сопоставимые измерения нагрузки Aβ.
Текущий протокол имеет некоторые ограничения. Эти два метода (анализ всего региона и субрегиона) не всегда могут использоваться взаимозаменяемо. Выбор использования полного или субрегионального анализа будет зависеть от регионального распределения Aβ в ткани, на которое влияет возраст, пол и штамм мышиной модели AD. Через 13 месяцев нагрузка Aβ распределяется по всей коре и гиппокампу мышей APP/PS1. Однако в 6 месяцев отложения Aβ ограничиваются корой, а минимальные отложения наблюдаются в гиппокампе12. В таких условиях анализ полной области интереса может быть желательным подходом для увеличения площади выборки ткани и, следовательно, сигнала Aβ. С другой стороны, анализ субрегион может быть методом выбора, когда нагрузка Aβ в определенной области мозга представляет интерес (например, соматосенсорная кора). Кроме того, через 13 месяцев самцы мышей APP/PS1 демонстрируют интенсивные 6E10-положительные пятна, а иммунофлуоресцентное окрашивание приводит к отличному сигналу с очень низким фоном, что делает текущий протокол очень подходящим для количественной оценки в данных условиях. Неясно, может ли этот метод количественной оценки быть успешно применен к менее интенсивному окрашиванию, и для ответа на этот вопрос потребуется будущая работа. Иммунофлуоресцентный способ количественной оценки и способ количественной оценки изображений, представленный в настоящем описании, обнаруживает все формы Aβ, включая форму предшественника13. В результате, если есть интерес к обнаружению конкретного вида Aβ (например, Aβ1-40 или Aβ1-42), могут быть использованы антитела, специфичные для этих изоформ Aβ. Поэтому, хотя метод иммунофлуоресцентного окрашивания и обнаружения 6E10 коррелировал с измерениями измерений Aβ1-42 в гомогенатах всего мозга с использованием ИФА (рисунок 5F, G), корреляция была лишь скромной. Это можно объяснить измерением только Aβ1-42 с использованием ИФА и обнаружением всех видов Aβ с использованием иммуноокрашивания 6E10. В настоящем исследовании используются три читателя для оценки согласия и корреляции между полным и субрегиональным анализом. Наличие дополнительных читателей может повысить надежность исследования и может дополнительно подтвердить соглашения между двумя методами, представленными здесь. Кроме того, мы используем корреляцию Пирсона в качестве меры согласия, которая широко используется среди других методов для описания согласия между непрерывными переменными19. Однако одним из ограничений использования корреляции Пирсона для определения согласия является то, что два способа, используемые в настоящем описании, могут давать связанные результаты, но один способ может привести к общим более высоким значениям, чем другой, из-за систематической предвзятости. Таким образом, корреляция Пирсона является хорошей мерой относительного согласия19. Для повышения надежности протокола могутбыть использованы дополнительные методы подтверждения абсолютного согласия, такие как сравнение средней 6E10-положительной области двумя методами (рисунок 5E). Взятый вместе, текущий протокол сравнивает нагрузку Aβ, обнаруженную иммунофлуоресцентным окрашиванием, и анализирует полные и субобласти, представляющие интерес в участках ткани мозга. Результаты показывают сильную корреляцию между этими двумя методами для участков мозговой ткани, полученных от 13-месячных самцов мышей APP / PS1, которые показывают обильные отложения Aβ.
Раскрытие информации
Авторам нечего раскрывать.
Благодарности
Исследования, представленные в этой публикации, были поддержаны Национальным институтом старения Национальных институтов здравоохранения под номерами R01AG062840 (для RKS) и R01AG072896 (для RKS). Содержание является исключительной ответственностью авторов и не обязательно отражает официальную точку зрения Национальных институтов здравоохранения. Около $200 тыс. (100%) федеральных средств поддержали этот проект. Мы также хотели бы поблагодарить д-ра Джошуа Яна за его помощь в редактировании рукописей.
Материалы
| Name | Company | Catalog Number | Comments |
| 15 mL conical tubes | ThermoFisher Scientific, MA, USA | 339650 | |
| 24-well plates | Fisher Scientific, NH, USA | FB012929 | |
| Amyloid beta 42 human ELISA kit | ThermoFisher Scientific, MA, USA | KHB3441 | |
| Aqueous mounting media | Vector laboratories, CA, USA | H-5501-60 | |
| Bovine serum albumin | Sigmaaldrich, MO, USA | A2153-50G | |
| BZ-X710 Keyence all-in-one fluorescence microscope | Keyence, IL, USA | BZ-X710 | |
| Clear nail poilsh | User preference | NA | |
| Cryostat | Leica Biosystems, IL, USA | Leica CM1860 Cryostat | |
| Formic acid | Sigmaaldrich, MO, USA | F0507-500ML | |
| Glass coverslips | VWR, PA, USA | 48393-081 | |
| GraphPad Prism | GraphPad Software, CA, USA | Version 8 | |
| ImageJ 1.51k | National Institutes of Health, MD, USA | Version 1.53e | |
| Mice | Jackson Laboratories, ME, USA | 034829-JAX | |
| Paraformaldehyde | Sigmaaldrich, MO, USA | P6148-500G | |
| Phenytoin/pentobarbital based anesthetic (Euthasol) | Patterson Veterinary, MA, USA | 07-805-9296 | |
| Phosphate-buffered saline | Fisher Scientific, NH, USA | BP661-50 | |
| Plus (+) microscope slides | Ted Pella, Inc., CA, USA | 260100 | |
| Primary antibody (6E10) | Biolegend, CA, USA | 803013 | |
| Sucrose | Sigmaaldrich, MO, USA | 47289 | |
| Triton X 100 | Sigmaaldrich, MO, USA | T8787-100ML |
Ссылки
- Alzheimer's Association. 2021 Alzheimer's disease facts and figures. Alzheimer's & Dementia. 17 (3), 327-406 (2021).
- Langa, K. M., Foster, N. L., Larson, E. B. Mixed dementia: emerging concepts and therapeutic implications. Journal of the American Medical Association. 292 (23), 2901-2908 (2004).
- Gandy, S., DeKosky, S. T. Toward the treatment and prevention of Alzheimer's disease: rational strategies and recent progress. Annual Review of Medicine. 64, 367-383 (2013).
- Bloom, G. S. Amyloid-beta and tau: the trigger and bullet in Alzheimer disease pathogenesis. JAMA Neurology. 71 (4), 505-508 (2014).
- Gremer, L., et al. Fibril structure of amyloid-beta(1-42) by cryo-electron microscopy. Science. 358 (6359), 116-119 (2017).
- Ferrero, J., et al. First-in-human, double-blind, placebo-controlled, single-dose escalation study of aducanumab (BIIB037) in mild-to-moderate Alzheimer's disease. Alzheimer's & Dementia Translational Research & Clinical Interventions. 2 (3), 169-176 (2016).
- Poon, C. H., Wang, Y., Fung, M. L., Zhang, C., Lim, L. W. Rodent models of amyloid-beta feature of Alzheimer's disease: development and potential treatment implications. Aging and Disease. 11 (5), 1235-1259 (2020).
- Christensen, A., Pike, C. J. Staining and quantification of beta-amyloid pathology in transgenic mouse models of Alzheimer's disease. Methods in Molecular Biology. 2144, 221(2020).
- Thakker, D. R., et al. Intracerebroventricular amyloid-beta antibodies reduce cerebral amyloid angiopathy and associated micro-hemorrhages in aged Tg2576 mice. Proceedings of the National Academy of Sciences of the United States of America. 106 (11), 4501-4506 (2009).
- Song, Z., et al. Detecting amyloid-beta accumulation via immunofluorescent staining in a mouse model of Alzheimer's disease. Journal of Visualized Experiments. (170), e62254(2021).
- Sun, J., et al. Hematologic safety of chronic brain-penetrating erythropoietin dosing in APP/PS1 mice. Alzheimer's & DementiaTranslational Research & Clinical Interventions. 5, 627-636 (2019).
- Jankowsky, J. L., et al. Mutant presenilins specifically elevate the levels of the 42 residue beta-amyloid peptide in vivo: evidence for augmentation of a 42-specific gamma secretase. Human Molecular Genetics. 13 (2), 159-170 (2004).
- Grant, M. K. O., et al. Human cerebrospinal fluid 6E10-immunoreactive protein species contain amyloid precursor protein fragments. PloS One. 14 (2), 0212815(2019).
- Gage, G. J., Kipke, D. R., Shain, W. Whole animal perfusion fixation for rodents. Journal of Visualized Experiments. (65), e3564(2012).
- Eichenbaum, K. D., et al. Minimally invasive method for murine brain fixation. Biotechniques. 39 (4), 487-490 (2005).
- Chang, R., et al. Blood-brain barrier penetrating biologic tnf-alpha inhibitor for Alzheimer's disease. Molecular Pharmaceutics. 14 (7), 2340-2349 (2017).
- Pinskiy, V., et al. High-throughput method of whole-brain sectioning, using the tape-transfer technique. PloS One. 10 (7), 0102363(2015).
- Potts, E. M., Coppotelli, G., Ross, J. M. Histological-based stainings using free-floating tissue sections. Journal of Visualized Experiments. (162), e61622(2020).
- van Stralen, K. J., Dekker, F. W., Zoccali, C., Jager, K. J. Measuring agreement, more complicated than it seems. Nephron Clinical Practice. 120 (3), 162-167 (2012).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены