Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Spécifique au patient Modeling of the Heart: Estimation des orientations des fibres ventriculaires
Dans cet article
Résumé
Une méthodologie pour estimer les orientations des fibres ventriculaires à partir des images in vivo de géométries cardiaques des patients pour la modélisation personnalisée est décrite. Validation de la méthodologie effectuée à l'aide normaux et défaillants coeurs canins démontrer que qu'il n'y a pas de différences significatives entre les orientations des fibres estimés et acquis à un niveau cliniquement observable.
Résumé
Spécifiques au patient des simulations de coeur (dys) fonction vise à personnaliser thérapie cardiaque sont entravés par l'absence de la technologie d'imagerie in vivo pour l'acquisition cliniquement orientations des fibres myocardiques. L'objectif de ce projet était de développer une méthodologie pour estimer orientations des fibres cardiaques à partir des images in vivo de géométries cardiaques des patients. Une représentation précise de la géométrie ventriculaire et des orientations de fibres a été reconstruite, respectivement, de haute résolution, ex vivo par résonance magnétique structurelle (MR) et tenseur de diffusion (DT) des images RM d'un coeur humain normal, dénommé atlas. Géométrie ventriculaire d'un cœur patient a été extrait, par l'intermédiaire de segmentation semi-automatique, à partir d'une in vivo la tomodensitométrie (TDM) image. En utilisant des algorithmes de transformation d'image, la géométrie ventriculaire atlas a été déformée pour correspondre à celle du patient. Enfin, le champ de déformation a été appliquée à la fibre orientat atlasions pour obtenir une estimation des orientations de fibres de patients. La précision des estimations de fibres a été évaluée au moyen de six normales et trois à défaut coeurs canins. La différence absolue moyenne entre les angles d'inclinaison des orientations des fibres acquises et estimé était de 15,4 °. Simulations numériques de cartes d'activation ventriculaire et pseudo-ECG en rythme sinusal et la tachycardie ventriculaire indiqué qu'il n'y ait pas de différences significatives entre les orientations des fibres estimés et acquis à une clinique observables level.The de nouvelles connaissances obtenues à partir du projet ouvrira la voie pour le développement de spécifiques au patient modèles du cœur qui peuvent aider les médecins dans le diagnostic personnalisé et des décisions concernant les interventions électrophysiologiques.
Introduction
L'approche de calcul devient centrale pour l'avancement de la compréhension de la fonction du cœur dans la santé et la maladie. State-of-the-art tout-cardiaques modèles de l'électrophysiologie et de l'électromécanique sont actuellement utilisées pour étudier un large éventail de phénomènes, comme la propagation ventriculaire normale, de l'arythmie, la défibrillation, couplage électromécanique et de resynchronisation cardiaque 1. Cependant, à l'approche de calcul pour être directement applicable dans l'environnement clinique, il est impératif que les modèles soient spécifiques au patient, à savoir les modèles doivent être basés sur l'architecture spécifique et les propriétés électrophysiologiques ou électromécanique du cœur malade du patient. Simulation avec ces modèles aideront les médecins à prendre des décisions hautement personnalisés pour les interventions électrophysiologiques ainsi que la prophylaxie, ce qui améliore considérablement la santé cardiaque 2-4.
contenu "> Création de modèles réalistes cardiaque nécessite l'acquisition de la structure de la géométrie et de la fibre d'un cœur patient. orientations de fibre de déterminer les orientations de la propagation électrique et les distributions de contrainte dans le cœur, et donc de les acquérir est essentiel à la modélisation cardiaque 5, 6. Avec les progrès récents de l'imagerie médicale, il est maintenant possible d'obtenir la géométrie d'un patient cardiaque, remodelage includingstructural comme un infarctus, in vivo à haute résolution à l'aide imagerie par résonance magnétique (IRM) et la tomodensitométrie (TDM) technologies. Toutefois, il n'est pas méthode pratique pour l'acquisition d'une structure de fibre cardiaque du patient in vivo. du tenseur de diffusion (DT) IRM 7, 8, la seule technique pour acquérir des orientations des fibres du cœur intact, n'est pas largement disponible in vivo en raison de certaines limitations 9. Une brève description des efforts précédents pour traduire IRMtd à la clinique peut être trouvé elsewhavant 2. Bien que des méthodologies telles que fondé sur des règles d'affectation des orientations des fibres offrir des alternatives aux IRMtd, ces méthodes présentent certaines limitations graves 2, 10. Ainsi, des difficultés à acquérir structure de fibre cardiaque in vivo actuellement obstacle à l'application de électrophysiologiques cardiaques et électromécaniques simulations en milieu clinique. L'objectif de cette recherche était de s'attaquer directement à ce besoin.Nous avons supposé que des orientations de fibres ventriculaires d'un cœur peut être prédit avec précision compte tenu de la géométrie du cœur et un atlas, où l'atlas est un cœur dont la géométrie et de la fibre orientations sont disponibles. En conséquence, nous avons utilisé l'état de l'art des techniques pour développer une méthodologie pour l'estimation des orientations des fibres cardiaques in vivo, et testé l'hypothèse normale et de ne pas ventricules canines 2. L'idée centrale de notre méthode d'estimation de la fibre est d'exploiter similarities dans les orientations des fibres, par rapport à la géométrie, entre les différents cœurs afin de rapprocher la structure des fibres d'un cœur (cible) pour lesquels l'information est disponible géométrie. Au cœur de notre méthode d'estimation est l'enregistrement de la géométrie de l'atlas avec la géométrie de la cible à l'aide cartographie à grande difféomorphe déformation métrique (LDDMM) 11, et le morphing des orientations des fibres atlas en utilisant la préservation des composantes principales (PPD) 2, 12. L'diffeomorphicproperty des garanties LDDMM que l'atlas ne «repliement» lui-même lors de la déformation, ce qui préserve les structures anatomiques integrityof. Figure 1 illustre le pipeline de traitement de notre méthodologie. La section texte du protocole § 1 décrit les divers composants du pipeline en démontrant comment l'estimation peut être réalisée pour un patient par exemple. Les chiffres à l'intérieur une partie des blocs de la figure 1 se référer au correspondantparagraphes vertu de l'article § 1 du texte du protocole.
Nous avons évalué les performances de la méthode proposée par la quantification de l'erreur d'estimation et de mesurer l'effet de cette erreur onsimulations de l'électrophysiologie cardiaque, par calcul simulant les cartes locales activation électrique ainsi que les pseudo-électrocardiogrammes (ECG pseudo-). En raison de l'indisponibilité du cœur de l'homme, l'évaluation de la performance a été réalisée à l'aide coeurs canins disponibles à partir des études antérieures 13-15. L'erreur d'estimation a été calculée au moyen d'angles d'inclinaison 16, de la tradition de followingthe histologie, où les mesures d'angle sont des coupes de tissus qui sont coupés performedon parallèle à la epicardialsurface. Depuis le anglebetween la direction des fibres et épicardique plan tangent est generallysmall 17, 18, la perte d'informations dans la description d'un fiberdirection entièrement à l'aide de son angle d'inclinaison est insignifiante. Pour l'ordisimulations ational, l'image des modèles ont été construits comme indiqué précédemment 19, 20, et le tissu cardiaque dans des modèles a été représenté établies sur la base de techniques mathématiques et les données expérimentales 21-25. Rythme sinusal a été simulé par une activation de réplication provenant du réseau de Purkinje 26, et une tachycardie ventriculaire, par une stimulation S1-S2 protocole 27. Les pseudo-ECG ont été calculés par rapport à l'aide 28 et l'écart absolu moyen (EAM) métrique 29.
Protocole
1. Fibre Orientations Estimation
- Acquérir des images IRM structurelles et IRMtd d'un cœur humain adulte normal en diastole, à une résolution de 1 mm 3. Utiliser ImageJ, extraire le myocarde ventriculaire de l'image structurelle de l'atlas raccord, pour chaque tranche de petit axe, est fermée par des cannelures d'un ensemble de points de repère sont placées le long des frontières endocardique et épicardique de la tranche (figure 2A et la figure 2B). Effectuer la mise en place de points de repère manuellement pour chaque tranche de 10 e dans l'image. Obtenir des points de repère pour les tranches restantes en interpolant linéairement les points identifiés manuellement, à l'aide MATLAB.Reconstruct les orientations des fibres du coeur atlas en calculant les vecteurs propres principaux des DTS dans l'image IRMd (figure 2C).
- Acquérir une image de la géométrie du coeur du patient en utilisant la diastole cardiaque in vivo CT ou IRM. Reconstruct de la géométrie cardiaque du patient à partir de l'image de manière similaire à la façon dont l'atlas a été construit (figure 3A et la figure 3B). L'image de patient doit être ré-échantillonnée avant la reconstruction de sorte que la résolution dans le plan est de 1 mm 2. De même, le nombre de tranches pour lesquelles repères sont cueillies manuellement, et l'intervalle de out-of-plan d'interpolation doit être ajustée de sorte que l'image du patient segmenté coeur a une épaisseur de coupe de 1 mm.
- Déformer l'image ventriculaire atlas pour correspondre à l'image géométrie du patient en deux étapes. Dans la première étape, effectuer une transformation affine basée sur un ensemble de points de repères treize: le ventricule gauche (LV) apex, le ventricule droit deux (RV) des points d'insertion, à la base, le deux points d'insertion RV à mi-chemin entre la base et le sommet, et quatre ensembles de deux points qui divisent équitablement RV et les contours LV épicardiques à la base, et à mi-chemin entre la base et le sommet (figure 4A & Figure 4B). Dans la seconde étape, la déformation affine transformée atlas ventricules en outre en fonction de la géométrie du patient, en utilisant la cartographie à grande déformation difféomorphique métrique (LDDMM) (figure 4C).
- Morph l'image IRMtd de l'atlas par le repositionnement de voxels d'image et de réorienter les DTS en fonction de la matrice de transformation affine de l'appariement et le champ de déformation de la transformation LDDMM. Effectuer la réorientation des DTS à l'aide de la préservation des directions principales (PPD) de la méthode.
- Obtenir l'estimation des orientations des fibres de patients de l'image morphed atlas IRMtd en calculant le vecteur propre principal de la DT (figure 5).
2. Mesure de l'erreur d'estimation
- Acquérir ex vivo par résonance magnétique structurelle et images DTMR de six normales et trois coeurs canins à défaut, à une résolution de 312,5 × 312,5 × 800 um 3. Ici, le cœur faiappât doit être généré dans les canines par l'ablation par radiofréquence de la gauche de branche suivie de 3 semaines de tachypacing à 210 min -1.
- Segmenter les ventricules du cœur canines de même du cœur humain atlas, telles que décrites au § 1.1. Notons ventricules segmentés à partir normales coeurs canins que les coeurs 1 à 6, et ceux segmenté de cœurs défaillants canines que les cœurs 7 à 9 (figure 6).
- Obtenir des cinq estimations différentes orientations de fibres ventriculaires du coeur 1 en utilisant chacun des coeurs 2 à 6 comme un atlas (figure 7).
- Estimation des orientations de fibres pour chacun des ventricules cardiaques défaillantes en utilisant 1, comme l'atlas (figure 8).
- Foreach point de données dans chaque ensemble d'orientations de fibres estimé, calculer l'erreur d'estimation en tant que | θ c-θ a |, où θ c θ et A sont les angles d'inclinaison des estimations d'd acquise orientations des fibres à ce point, respectivement.
- Pour chaque point de données dans chaque ensemble d'orientations de fibres estimé, calculer l'angle aigu et betweenestimated acquis directions des fibres dans trois dimensions (3D) par l'intermédiaire d'thevector produit scalaire.
3. La mesure des effets de l'erreur d'estimation sur les simulations
- De coeur 1, de construire six modèles, l'un avec les orientations IRMtd acquises fibre de coeur 1 (appelé modèle 1), et cinq avec les cinq orientations de fibres estimé ensembles de données (modèles 2 à 6). Pour chacun des trois coeur défaillant géométries, construire deux modèles ventriculaires, une des IRMtd acquises orientations des fibres et l'autre avec les orientations des fibres estimés. Voici la résolution spatiale des modèles, calculé en fonction de la longueur moyenne des arêtes des mailles, devrait être d'environ 600 um. Représentent les modèles d'insuffisance cardiaque avec des fibres IRMtd acquises en tant que modèles de 7 à 9, et ceux avec estimated fibres que les modèles de 10 à 12.In les modèles, utiliser la représentation monodomaine pour décrire le tissu cardiaque, avec des équations régissant:
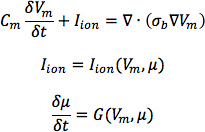
où σ b est le tenseur de conductivité en vrac, qui est calculée à partir des tenseurs de conductivité bidomaine comme décrit par Potse et al 30, V m est le potentiel transmembranaire; C m est la capacité membranaire spécifique, et I d'ions est la densité de courant la transmembranaire, qui à son tour dépend de V m et un ensemble de variables d'état μ décrit la dynamique des flux ioniques à travers la m membrane.For C, utilisez une valeur de 1 μ F / cm 2. Pour i σ dans des conditions normales modèles cardiaque canine, utilisez longitudinalesLes valeurs de conductivité internes et transversale de 0,34 S / m et 0,06 S / m, respectivement. Représenter l lon par les modèles Greenstein-Winslow ioniques de la myocyte ventriculaire canine. Diminution de la conductivité électrique dans les modèles cardiaques ventriculaires canins échec de 30% (figure 9).
- Utilisation du logiciel CARP (CardioSolv, LLC), le rythme sinusal simuler avec tous les modèles. Provoquer réentrante tachycardie ventriculaire (VT) dans les six modèles défaillants en utilisant un protocole de stimulation S1-S2. Choisissez l'intervalle entre S1 et S2 pour obtenir une activité soutenue VT pendant 2 secondes après la livraison S2. Si VT n'est pas induite pour n'importe quelle synchronisation S1-S2, diminuer les conductivités jusqu'à 70% jusqu'au VT a été induite (figure 10).
- Pour chaque simulation, le calcul des pseudo-ECG en prenant la différence des potentiels extracellulaires entre deux points dans un bain isotrope entourant le cœur. Placez les deux points près de la base du cœur séparéspar 18 cm, de sorte que la ligne qui les relie est perpendiculaire au plan de base-sommet de la cloison comme illustré sur la Figure 10. Pour chaque simulation, avec des orientations de fibres estimé, calculer la métrique comme MAD
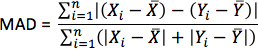
où X est la forme d'onde ECG de la simulation avec des orientations de fibres estimées, Y est la forme d'onde ECG de thecorresponding simulation avec des orientations de fibres acquises, X est la valeur moyenne de X, Y est la valeur moyenne de Y, et n est la longueur de X et Y.
Résultats
Figure 11, ca affiche des visualisations rationalisation des estimations ainsi que les orientations des fibres IRMtd dérivés dans les cœurs normaux et défaillants. Examen qualitatif montre que les orientations de fibres estimé cadrent bien avec IRMtd dérivés de ceux. Panneau D illustre, superposées sur la géométrie du cœur 1, la distribution de l'erreur dans les angles d'inclinaison des cœurs normaux », en moyenne sur les cinq estimations. Panneau E montre la répartition moyenne de...
Discussion
Cette recherche montre que quantitativement, en l'absence de IRMtd, des orientations de fibres myocardiques normales et des ventricules défaut peut être estimé à partir des images in vivo de leurs géométries pour l'utilisation dans des simulations de l'électrophysiologie cardiaque. La méthodologie proposée est démontrée avec des données in vivo CT, mais elle est également applicable aux images IRM in vivo de la géométrie ventriculaire, pallier le ma...
Déclarations de divulgation
Aucun conflit d'intérêt déclaré.
Remerciements
Nous remercions les Drs. Raimond Winslow, Elliot McVeigh, et Helm Patrick à la Johns Hopkins University de fournir les bases de données ex vivo ligne.C recherche a été financée par le National Institutes of Health subvention R01-HL082729, et la National Science Foundation subvention CBET-0933029.
matériels
| Name | Company | Catalog Number | Comments |
| LDDMM | Johns Hopkins University | http://cis.jhu.edu/software/lddmm-volume/index.php | |
| MATLAB | Mathworks, Inc | R2011b | http://www.mathworks.com/products/matlab/ |
| ImageJ | National Institutes of Health | http://rsbweb.nih.gov/ij/ | |
| Tarentule | CAE Software Solutions | http://www.meshing.at/Spiderhome/Tarantula.html | |
| CARP | CardioSolv | http://cardiosolv.com/ | |
| Images Canine | Johns Hopkins University | http://www.ccbm.jhu.edu/research/DTMRIDS.php |
Références
- Trayanova, N. Whole Heart Modeling: Applications to Cardiac Electrophysiology and Electromechanics. Circulation Research. 108, 113-128 .
- Vadakkumpadan, F., Arevalo, H., Ceritoglu, C., Miller, M., Trayanova, N. Image-Based Estimation of Ventricular Fiber Orientations for Personalized Modeling of Cardiac Electrophysiology. IEEE Transactions on Medical Imaging. 31 (5), 1051-1060 .
- Vadakkumpadan, F., Gurev, V., Constantino, J., Arevalo, H., Trayanova, N., Kerckhoffs, R. Modeling of Whole-Heart Electrophysiology and Mechanics: Towards Patient-Specific Simulations. Patient-Specific Modeling of the Cardiovascular System: Technology-Driven Personalized Medicine. , 145-165 (2010).
- Buxton, A. E., Lee, K. L., DiCarlo, L., Gold, M. R., Greer, G. S., Prystowsky, E. N., O'Toole, M. F., Tang, A., Fisher, J. D., Coromilas, J., Talajic, M., Hafley, G. Electrophysiologic testing to identify patients with coronary artery disease who are at risk for sudden death. Multicenter Unsustained Tachycardia Trial Investigators. The New England Journal of Medicine. 342 (26), 1937-1945 (2000).
- Wei, D., Okazaki, O., Harumi, K., Harasawa, E., Hosaka, H. Comparative simulation of excitation and body surface electrocardiogram with isotropic and anisotropic computer heart models. IEEE Transactions on Biomedical Engineering. 42 (4), 343-357 (1995).
- Leon, L. J., Horacek, B. M. Computer model of excitation and recovery in the anisotropic myocardium. II. Excitation in the simplified left ventricle. Journal of Electrocardiology. 24 (1), 17-31 (1991).
- Rohmer, D., Sitek, A., Gullberg, G. T. Reconstruction and Visualization of Fiber and Laminar Structure in the Normal Human Heart from Ex Vivo Diffusion Tensor Magnetic Resonance Imaging (DTMRI) Data. Investigative Radiology. 42 (11), 777-789 (2007).
- Daubert, J. P., Zareba, W., Hall, W. J., Schuger, C., Corsello, A., Leon, A. R., Andrews, M. L., McNitt, S., Huang, D. T., Moss, A. J., Investigators, M. I. S. Predictive value of ventricular arrhythmia inducibility for subsequent ventricular tachycardia or ventricular fibrillation in Multicenter Automatic Defibrillator Implantation Trial (MADIT) II patients. Journal of Americal College of Cardiology. 47 (1), 98-107 (2006).
- Sosnovik, D. E., Wang, R., Dai, G., Reese, T. G., Wedeen, V. J. Diffusion MR tractography of the heart. Journal of Cardiovascular Magnetic Resonance. 11 (1), 47-61 (2009).
- Sundar, H., Shen, D., Biros, G., Litt, H., Davatzikos, C. Estimating myocardial fiber orientations by template warping. Proc. IEEE International Symposium on Biomedical Imaging. , 73-76 (2006).
- Beg, M. F., Helm, P. A., McVeigh, E., Miller, M. I., Winslow, R. L. Computational Cardiac Anatomy Using MRI. Magnetic Resonance in Medicine. 52 (5), 1167-1174 (2004).
- Alexander, D. C., Pierpaoli, C., Basser, P. J., Gee, J. C. Spatial Transformations of Diffusion Tensor Magnetic Resonance Images. IEEE Transactions on Medical Imaging. 20, 1131-1139 (2001).
- Helm, P. A., Younes, L., Beg, M. F., Ennis, D. B., Leclercq, C., Faris, O. P., McVeigh, E., Kass, D., Miller, M. I., Winslow, R. L. Evidence of Structural Remodeling in the Dyssynchronous Failing Heart. Circulation Research. 98, 125-132 (2006).
- Helm, P., Beg, M. F., Miller, M., Winslow, R. Measuring and mapping cardiac fiber and laminar architecture using diffusion tensor MR imaging. Annals of the New York Academy of Sciences. 1047, 296-307 (2005).
- Helm, P. A., Tseng, H. -. J., Younes, L., McVeigh, E. R., Winslow, R. L. Ex vivo 3D diffusion tensor imaging and quantification of cardiac laminar structure. Magnetic Resonance in Imaging. 54, 850-859 (2005).
- Scollan, D. F., Holmes, A., Winslow, R., Forder, J. Histological validation of myocardial microstructure obtained from diffusion tensor magnetic resonance imaging. American Journal of Physiology - Heart and Circulatory Physiology. 275 (6), H2308-H2318 (1998).
- Lombaert, H., Peyrat, J., Croisille, P., Rapacchi, S., Fanton, L., Cheriet, F., Clarysse, P., Magnin, I., Delingette, H., Ayache, N. Human Atlas of the Cardiac Fiber Architecture: Study on a Healthy Population. IEEE Transactions on Medical Imaging. 31 (7), 1436-1447 (2012).
- Streeter, D. D. . Gross morphology and fiber geometry of the heart. , (1979).
- Vadakkumpadan, F., Rantner, L. J., Tice, B., Boyle, P., Prassl, A. J., Vigmond, E., Plank, G., Trayanova, N. Image-Based Models of Cardiac Structure with Applications in Arrhythmia and Defibrillation Studies. Journal of Electrocardiology. 42, 151.e1-151.e10 (2009).
- Plank, G., Zhou, L., Greenstein, J. L., Plank, G., Zhou, L., Greenstein, J. L., Cortassa, S., Winslow, R. L., O'Rourke, B., Trayanova, N. A. From mitochondrial ion channels to arrhythmias in the heart: computational techniques to bridge the spatio-temporal scales. Philosophical Transactions Series A, Mathematical, Physical, and Engineering Sciences. 366 (1879), 3381-3409 (2008).
- Roberts, D. E., Scher, A. M. Effect of tissue anisotropy on extracellular potential fields in canine myocardium in situ. Circulation Research. 50, 342-351 (1982).
- Greenstein, J., Wu, R., Po, S., Tomaselli, G. F., Winslow, R. L. Role of the Calcium-Independent Transient Outward Current I(to1) in Shaping Action Potential Morphology and Duration. Circulation Research. 87, 1026-1033 (2000).
- Winslow, R., Rice, J., Jafri, S., Marbán, E., O'Rourke, B. Mechanisms of altered excitation-contraction coupling in canine tachycardia-induced heart failure, II: model studies. Circulation Research. 84 (5), 571-586 (1999).
- Akar, F., Nass, R., Hahn, S., Cingolani, E., Shah, M., Hesketh, G., DiSilvestre, D., Tunin, R., Kass, D., Tomaselli, G. Dynamic Changes in Conduction Velocity and Gap Junction Properties During Development of Pacing-Induced Heart Failure. American Journal of Physiology - Heart and Circulatory Physiology. 293 (2), H1223-H1230 (2007).
- Gurev, V., Constantino, J., Rice, J. J., Trayanova, N. Distribution of Electromechanical Delay in the Ventricles:Insights from a 3D Electromechanical Model of the Heart. Biophysical Journal. 99 (3), 745-754 .
- Ten Tusscher, K. H. W. J., Hren, R., Panfilov, A. V. Organization of Ventricular Fibrillation in the Human Heart. Circulation Research. 100 (12), e87-e101 (2007).
- Gima, K., Rudy, Y. Ionic Current Basis of Electrocardiographic Waveforms. Circulation Research. 90, 889-896 (2002).
- Gerstenfeld, E., Dixit, S., Callans, D., Rajawat, Y., Rho, R., Marchlinski, F. Quantitative comparison of spontaneous and paced 12-lead electrocardiogram during right ventricular outflow tract ventricular tachycardia. Journal of Americal College of Cardiology. 41 (11), 2046-2053 (2003).
- Potse, M., Dube, B., Richer, J., Vinet, A., Gulrajani, R. M. A comparison of monodomain and bidomain reaction-diffusion models for action potential propagation in the human heart. IEEE Transactions on Biomedical Engineering. 53 (12), 2425-2435 (2006).
- Peyrat, J. -. M., Sermesant, M., Pennec, X., Delingette, H., Chenyang, X., McVeigh, E. R., Ayache, N. A Computational Framework for the Statistical Analysis of Cardiac Diffusion Tensors: Application to a Small Database of Canine Hearts. IEEE Transactions on Medical Imaging. 26, 1500-1514 (2007).
- Chen, J., Song, S. -. K., Liu, W., McLean, M., Allen, S. J., Tan, J., Wickline, S. A., Yu, X. Remodeling of cardiac fiber structure after infarction in rats quantified with diffusion tensor MRI. American Journal of Physiology - Heart and Circulatory Physiology. 285 (3), H946-H954 (2003).
- Stecker, E. C., Chugh, S. S. Prediction of sudden cardiac death: next steps in pursuit of effective methodology. Journal of Interventional Cardiac Electrophysiolog. 31 (2), 101-107 (2011).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon