È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Elaborazione azoto supercritica per la purificazione di reattivi materiali porosi
In questo articolo
Riepilogo
L'azoto è un fluido supercritico efficace per processi di estrazione o di essiccazione a causa della sua piccola dimensione molecolare, alta densità nel regime supercritico quasi liquido, e inerzia chimica. Presentiamo un protocollo di essiccazione azoto supercritico per il trattamento di purificazione dei reattivi, materiali porosi.
Abstract
Supercritical fluid extraction and drying methods are well established in numerous applications for the synthesis and processing of porous materials. Herein, nitrogen is presented as a novel supercritical drying fluid for specialized applications such as in the processing of reactive porous materials, where carbon dioxide and other fluids are not appropriate due to their higher chemical reactivity. Nitrogen exhibits similar physical properties in the near-critical region of its phase diagram as compared to carbon dioxide: a widely tunable density up to ~1 g ml-1, modest critical pressure (3.4 MPa), and small molecular diameter of ~3.6 Å. The key to achieving a high solvation power of nitrogen is to apply a processing temperature in the range of 80-150 K, where the density of nitrogen is an order of magnitude higher than at similar pressures near ambient temperature. The detailed solvation properties of nitrogen, and especially its selectivity, across a wide range of common target species of extraction still require further investigation. Herein we describe a protocol for the supercritical nitrogen processing of porous magnesium borohydride.
Introduzione
Estrazione con fluidi supercritici (SFE) ed essiccamento (SCD) metodi sono ben stabiliti in una vasta gamma di applicazioni pratiche, soprattutto nelle industrie alimentari e del petrolio, ma anche nella sintesi chimica, analisi e trattamento dei materiali. 1-6 L'uso di essiccazione o supporto di estrazione a condizioni sopra loro punti critici è spesso più veloce, pulito, e più efficiente rispetto alle tecniche tradizionali (liquidi), e ha il vantaggio di essere altamente regolabili rispetto alla potenza solvatazione del fluido da leggero aggiustamento delle condizioni operative . 3,7 Un metodo semplice ScD si compone di tre fasi fondamentali. Il primo passo è esporre il materiale solido (o forse liquido) partendo che contiene il composto di destinazione impurezza di un fluido ScD opportunamente scelto nel liquido (o quasi liquido supercritico) di fase, in cui la sua alta densità corrisponde ad un alto (e forse selettiva 7) potere solvente rispetto alle specie bersaglio. Tche secondo passo è il riscaldamento e la compressione del sistema sopra punto critico del ScD fluido prescelto in un contenitore chiuso in modo che il fluido e le sue specie bersaglio disciolte non passano un confine di fase che potrebbe provocare la separazione. Il passo finale si sta riducendo lentamente la pressione del fluido ScD per vuoto ad una temperatura superiore alla temperatura critica, permettendo la soluzione fluido contenente specie bersaglio di fuggire, di nuovo senza incontrare un confine fase o eventuali effetti negativi di tensione superficiale lungo la strada.
Il materiale di partenza è lasciato impoverito di specie bersaglio e può essere sottoposto a trattamenti ripetuti, se necessario. In caso di estrazione con fluido supercritico, la specie bersaglio soluto è il prodotto desiderato, e sono raccolti da soluzione per un ulteriore uso. 8,9 In altri casi, il materiale di partenza secche o purificato è il prodotto desiderato, e le impurità estratte vengono scartati. Quest'ultimo scenario, qui indicatacome l'approccio ScD, è stato scoperto di essere una strategia efficace per il pretrattamento di elevata area superficiale, materiali microporosi quali strutture metallo-organici (MOF), dove i metodi tradizionali di trattamento termico sotto vuoto in molti casi non è sufficiente a chiarire i pori di tutti gli ospiti indesiderati, o provocare il collasso dei pori. anidride carbonica 10 ScD (CSCD) il trattamento è ora un processo di post-sintetico di routine per MOF, 11 che porta ad un aumento delle superfici di azoto accessibile rispetto ai materiali non trattati fino a 1.000% e 12 altri miglioramenti, come in attività catalitica. 13 Altre applicazioni fluidi supercritici sono notevoli come mezzo ampiamente accordabile per reazioni chimiche, 14-16 supercritico cromatografia fluido (SCFC) 6,17,18 e sintesi di aerogel e materiali compositi avanzati. 19- 22
Per asciugare le applicazioni, un fluido ScD viene scelta in base a due criteri: a) la vicinanza del suopunto critico alle condizioni ambientali (per comodità e per ridurre i costi energetici e la complessità dei processi) e b) il suo potere solvatazione rispetto alle specie bersaglio. L'anidride carbonica (CO 2) ha dimostrato di essere una comoda fluido ScD in molte applicazioni poiché è non tossico, non infiammabile, e poco costoso, e può essere sintonizzata per esibire un elevato potere di solvatazione verso un numero di comuni specie bersaglio organiche nel suo quasi-liquido stato (a pressioni di <10 MPa e temperature di 273-323 K). 1-3,7-9 Altri solventi supercritici comuni (o co-solventi) si annoverano acqua (che copre una notevole gamma di proprietà solventi tra il suo ambiente e stato supercritico 23), acetone, etilene, metanolo, etanolo, ed etano, coprendo lo spettro da polare (protici e aprotici) per non polare, ed aventi punti critici relativamente vicino alle condizioni ambientali.
L'anidride carbonica è di gran lunga il fluido più comune ScD utilizzato. Nei metodi cscd stabiliti, la reattivitàdel materiale di partenza non è un fattore inibitorio dal CO 2 è molto debolmente reattivo a temperature vicine suo punto critico. Tuttavia, alcune classi di materiali come cosiddetti idruri complessi (ad esempio, alanati e boroidruri) presentano sfide uniche nella maneggevolezza grazie alla loro forte reattività in presenza di acqua o CO 2 in aggiunta alla loro (forse volutamente su misura) instabilità sotto riscaldamento . 24-26 Inoltre, vi è un grande interesse internazionale in materiali quali composti stoccaggio di idrogeno ad alta densità, 27-30 e quindi anche in nanostrutturati e / o varietà porosi 31-33. Per l'efficace purificazione di tali reattivi, instabili e materiali nanostrutturati, metodi SCD sono una strategia promettente. Fluido 34 Un ScD deve essere utilizzato che ha un piccolo diametro molecolare appropriato per la penetrazione in cavità strette e che ha anche un elevato potere solvatazione verso la impurità bersaglio, WHIle rimanenti non reattiva verso il materiale di partenza stessa. Qui, l'uso di azoto supercritico (N 2) come fluido efficace per tale estrazione e applicazioni soprattutto essiccazione è presentato. Una metodologia specifica supercritico essiccazione azoto (nscd) è descritta di seguito per la purificazione di γ-fase boroidruro magnesio una specie bersaglio comprendono sia diborano e un composto n butile (simile ma non specificamente identificabili come n butano). Il seguente protocollo può essere facilmente modificato per estensione globale ad altri processi di essiccazione di azoto o di estrazione supercritica.
Protocollo
1. Apparecchiatura
- Utilizzare un essiccamento supercritico (SCD) Apparecchiatura di base costituito da quattro componenti principali connesso con un tubo di gas ad alta pressione: la fornitura di gas, un sistema a vuoto, sensori (temperatura e pressione), e l'ambiente campione (che può essere immerso in un bagno). Assicurarsi che la costruzione è di valvole di alta qualità in acciaio inox, raccordi e tubi, pressione votate almeno 10 MPa entro l'intervallo di temperatura tra 80-300 K.
Nota: Lo schema è mostrato in Figura 1. - Per azoto ScD (nscd) trattamenti, in modo che l'alimentazione del gas è la purezza della ricerca (> 99.999%) azoto gassoso dotato di un regolatore di pressione per il controllo della pressione di uscita tra 0-10 MPa. Collegare un contenitore 50 L (20 MPa) all'apparato, e spurgare il sistema con azoto puro più volte prima dell'uso.
- Assicurarsi che il sistema di vuoto è in grado di raggiungere pressioni di vuoto fino a <0,1 Pa ed è collegato all'apparecchio conValvola ago sottile controllo. Preferibilmente usare una pompa di diffusione senza olio e una pompa turbo molecolare resistenza, posti in serie.
- Utilizzare almeno due sensori di pressione per la misurazione della pressione durante i trattamenti SCD: un sensore di bassa pressione per la misurazione di vuoto e sensore di alta pressione per ottenere un intervallo di pressione misurabile totale tra 0,1-10 7 Pa.
- Utilizzare almeno due sensori di temperatura per l'accuratezza minima necessaria per eseguire trattamenti tipici SCD: un sensore a contatto termico con il campione e un sensore all'interno del collettore di dosaggio gas primario per misurazioni accurate tra 77-300 K (ad esempio, tipo K) .
- Verificare che il supporto del campione ha un volume interno appropriato per contenere la quantità di campione necessaria per il trattamento, ed è costruito in acciaio inossidabile.
Nota: A allungate aids progettazione cilindrici in contatto termico con la vasca. - Assicurarsi che il raccordo che chiude il contenitore del campione è approprIATE per alte pressioni e ripetuto uso (ad esempio, Swagelok VCR). Collegare il contenitore volume del campione ad una valvola per l'isolamento dall'ambiente esterno attraverso un tubo di lunghezza appropriata (pescante) per completa immersione del supporto del campione nella vasca.
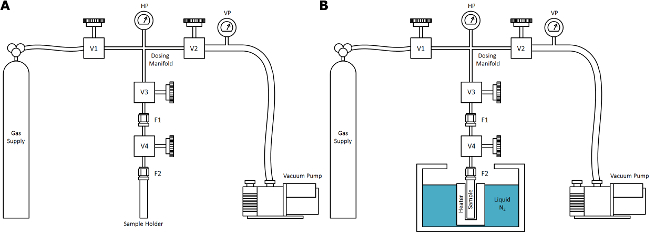
. Figura 1. supercritica azoto essiccazione (nscd) Apparecchiatura Una rappresentazione schematica dell'apparecchiatura nscd semplificato per l'uso nel tipico laboratorio: (A) a temperatura ambiente e (B) dopo l'immersione del campione nel bagno. L'alimentazione del gas per il processo descritto in questo lavoro è azoto, ma questo apparato generale è generalizzabile ad altri fluidi SCD con un punto critico compresa in una gamma pratica di temperatura e pressione, come il CO 2. I componenti sono etichettati per coerenza con the protocollo qui descritto. Cliccate qui per vedere una versione più grande di questa figura.
2. Preparazione
- Carico 0,2-0,5 g di campione (γ-Mg (BH 4) 2, in forma di polvere, dopo la sintesi wet-chimica e metodi di essiccazione normali) nel supporto del campione in condizioni appropriate, tipicamente in atmosfera inerte come un vano portaoggetti argon, a temperatura ambiente o inferiore. Chiudere il portacampioni (raccordo F2) con una guarnizione del filtro e quindi chiudere la valvola (valvola V4). Trasferire il portacampioni all'apparato e fissare (raccordo F1).
- Aprire il collettore di dosaggio per aspirare via V2 ed evacuare. Aprire V3 ed evacuare. Spurgare l'apparecchio con azoto tramite V1 e V2 evacuare via. Aprire V4 e evacuare il campione a temperatura ambiente fino a 24 ore, per raggiungere la pressione minima del sistema (<0,1 Pa).
- Installare il bagno del campione (vedi Figura 2) intorno al supporto del campione. Eseguire questa alzando la vasca in posizione su una piattaforma a forbice o meccanismo simile.
- Impostare il riscaldatore per il futuro desiderato temperatura del liquido (T l, vedere il punto 3.1) di 110 K, e continuano a portare l 'apparecchio fino a quando la temperatura si equilibra.
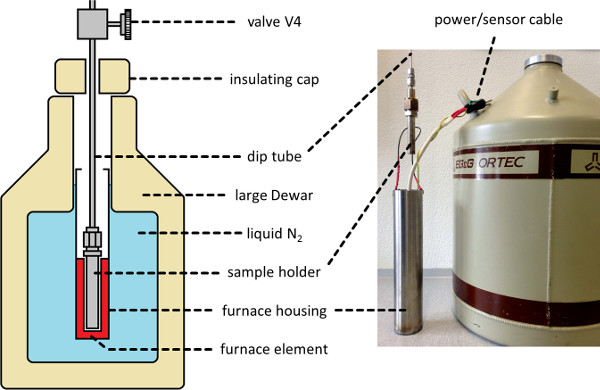
Figura 2. criogenico forno a bagno del campione. Una rappresentazione schematica (a sinistra) e la fotografia (a destra) di un ambiente criostatiche bagno termale adeguato per contenere il supporto del campione durante l'elaborazione nscd, consentendo la misurazione e il controllo della temperatura del campione tra i 77-298 K. Per favore clicca qui per vedere una versione più grande di questa figura.
3. supercritico azoto Esposizione
- Per NSCD trattamento di γ-Mg (BH 4) 2, (oggetto di dimostrazione in questo protocollo) seleziona una temperatura del liquido (T l) di 110 K. Ciò corrisponde ad una densità di solvente liquido moderata (~ 0,6 g ml -1) ; Regolare come necessario per l'applicazione di questo protocollo per altri procedimenti di trattamento nscd (vedi nota sotto).
- Chiudere l'impianto al vuoto chiudendo V2. Gas aperto V1 lentamente, permettendo la pressione per aumentare nella regione liquido del diagramma di fase. Equilibrare il sistema a 2 MPa e T l.
- Immergere il campione in N liquido 2 per 4 ore.
- Impostare il riscaldatore a 150 K con un min -1 rampa ≤2 K. Lasciare la pressione per aumentare non superiore alla pressione nominale massima dell'apparecchio (questo P max dovrebbe essere ≥10 MPa); se necessario, spurgare accuratamente la pressione in eccesso di aspirare via V2. Equilibrare il sistema a P max e 150 K.
- Immergere il campione in supercritical N 2 per 1 ora.
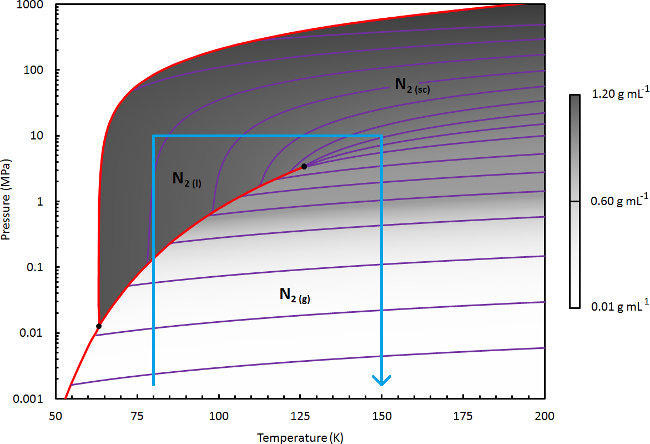
Figura 3. Fase Schema di Azoto. Un diagramma di fase dettagliata di azoto, dove la densità del fluido (mostrata in scala di grigi lineare) viene calcolato utilizzando Refprop (un'equazione Webb-Benedetto-Rubin modificato di stato). 41 diverse linee di densità costante sono mostrati in viola. I confini di fase solida e linee di transizione di ebollizione sono mostrati in rosso. Le linee blu indicano il confine della regione del diagramma di fase che è rilevante per l'essiccazione o di estrazione lavorazione con N 2. Clicca qui per vedere una versione più grande di questa figura.
Nota: Per l'applicazione di questo protocollo per altri materiali, istituire un adeguato trattamento schem nscde scegliendo le condizioni necessarie per una efficace solvatazione delle specie bersaglio. Fare riferimento al diagramma di fase di N 2, illustrata in figura 3. Per ottenere una elevata densità del fluido in fase liquida (ad esempio, 0.8-1 g ml -1), selezionare una T l di 80-90 K. Per densità del liquido moderata (ad esempio, 0,6-0,8 g ml -1), selezionare una T l di 90-115 K. Una prova e l'approccio di errore può essere necessario.
4. supercritico azoto uscita
- Rompere attenzione al sistema di vuoto mediante strozzamento V2, permettendo la pressione per diminuire più lentamente possibile. Rompere ripetutamente il sistema di tassi di vuoto più elevati necessari per conseguire un graduale declino per alto vuoto (<0,1 Pa) nell'arco approssimativa di tempo di 12-24 ore.
- Rimuovere il bagno di campione e completamente V2 aperto di evacuare completamente il campione. Equilibrare a RT ed alto vuoto (<0,1 Pa).
- Degassare il campione a temperatura ambiente e <0,1 Pa per 1-24 ore, come desired.
5. Messaggio Trattamento
- Chiudere le valvole V3 e V4, e rimuovere il supporto del campione l'apparato (raccordo F1).
- Trasferire il portacampione per ambiente inerte per la manipolazione, come un cassetto portaoggetti argon-riempita. Togliere il campione dal supporto (montaggio F2) e riporla in un contenitore sigillato a temperatura ambiente o inferiore.
Risultati
Boroidruri metalli alcalini e alcalino-terrosi sono potenziali materiali per lo stoccaggio dell'idrogeno, che offrono un grande contenuto di idrogeno gassoso su decomposizione. 27,29 Altri prodotti di decomposizione come diborano sono anche talvolta stato rilevato nel gas desorbita, ma la loro origine non è a priori chiaro ; è possibile che sono prodotti della decomposizione pura fase, ma possono anche essere impurità o prodotti di reazioni di impurità residue mediante sintesi chimica. 35 L...
Discussione
Forse a causa della sua relativamente bassa temperatura critica (126 K), N 2 è stato storicamente trascurato come un efficace solvente ScD. In relazioni precedenti, 3,17,42,43 è stata solo accennato nel contesto di elaborare temperatura uguale o superiore ambiente, dove si esibisce solo il potere solvatazione modesta a causa della sua bassa densità del fluido in questa regione del suo diagramma di fase (ad eccezione a pressioni estremamente elevate 43). Il passaggio chiave nella reali...
Divulgazioni
Gli autori non hanno nulla da rivelare.
Riconoscimenti
Questo lavoro è stato sostenuto da Celle a combustibile europee e Hydruogen impresa comune sotto BOR4STORE collaborativo progetto (accordo di sovvenzione n ° 303428) e il programma di infrastrutture H2FC (Grant Agreement No. FP7-284522).
Materiali
| Name | Company | Catalog Number | Comments |
| Compressed Nitrogen Gas | Messer Schweiz AG | 50 L bottle, purity > 99.999%, <3 ppmv H2O | |
| Liquid Nitrogen | Pan Gas AG | Bulk storage, on site | |
| Custom Supercritical Drying Apparatus | Empa | Swagelok (compression fitting and VCR) components | |
| Custom Cryogenic Furnace Bath | Empa | ||
| Custom Labview Interface | Empa |
Riferimenti
- McHugh, M. A., Krukonis, V. J. . Supercritical Fluid Extraction. , (1986).
- Schneider, G. M. Physicochemical Principles of Extraction with Supercritical Gases. Angew. Chem. lnt. Ed. 17, 716-727 (1978).
- Williams, D. F. Extraction with Supercritical Gases. Chem. Eng. Sci. 36 (11), 1769-1788 (1981).
- Eckert, C. A., Knutson, B. I., Debenedetti, P. G. Supercritical fluids as solvents for chemical and materials processing. Nature. 383, 313-318 (1996).
- Cooper, A. I. Polymer synthesis and processing using supercritical carbon dioxide. J. Mater. Chem. 10, 207-234 (2000).
- Klesper, E., Corwin, A. H., Turner, D. A. High pressure gas chromatography above critical temperatures. J. Org. Chem. 27, 700-701 (1962).
- Tucker, S. C. Solvent Density Inhomogeneities in Supercritical Fluids. Chem. Rev. 99 (2), 391-418 (1999).
- Hubert, P., Vitzthum, O. G. Fluid Extraction of Hops, Spices, and Tobacco with Supercritical Gases. Angew. Chem. Int. Ed. 17 (10), 710-715 (1978).
- Zosel, K. Separation with Supercritical Gases: Practical Applications. Angew. Chem. Int. Ed. 17 (10), 702-709 (1978).
- Nelson, A. P., Farha, O. K., Mulfort, K. L., Hupp, J. T. Supercritical Processing as a Route to High Internal Surface Areas and Permanent Microporosity in Metal−Organic Framework Materials. J. Am. Chem. Soc. 131, 458-460 (2009).
- Liu, B., Wong-Foy, A. G., Matzger, A. J. Rapid and enhanced activation of microporous coordination polymers by flowing supercritical CO2. Chem. Commun. 49, 1419-1421 (2013).
- Cooper, A. I., Rosseinsky, M. J. Metal–organic frameworks: improving pore performance. Nat. Chem. 1, 26-27 (2009).
- Totten, R. K., et al. Enhanced Catalytic Activity through the Tuning of Micropore Environment and Supercritical CO2 Processing: Al(Porphyrin)-Based Porous Organic Polymers for the Degradation of a Nerve Agent Simulant. J. Am. Chem. Soc. 135, 11720-11723 (2013).
- Savage, P. E., Gopalan, S., Mizan, T. I., Martino, C. J., Brock, E. E. Reactions at supercritical conditions: Applications and fundamentals. AIChE J. 41 (7), 1723-1778 (1995).
- Baiker, A. Supercritical Fluids in Heterogeneous Catalysis. Chem. Rev. 99 (2), 453-474 (1999).
- Jessop, P. G., Ikariya, T., Noyori, R. Homogeneous Catalysis in Supercritical Fluids. Chem. Rev. 99 (2), 475-494 (1999).
- Giddings, J. C., Myers, M. N., McLaren, L., Keller, R. A. High Pressure Gas Chromatography Of Nonvolatile Species. Science. 162 (3849), 67-73 (1968).
- Gere, D. R. Supercritical Fluid Chromatography. Science. 222, 253-259 (1983).
- Kistler, S. S. Coherent Expanded Aerogels and Jellies. Nature. 127, 741-741 (1931).
- Biener, J., et al. Advanced carbon aerogels for energy applications. Energy Environ. Sci. 4, 656-667 (2011).
- Morère, J., et al. Deposition of Pd into mesoporous silica SBA-15 using supercritical carbon dioxide. J. Supercrit. Fluids. 56 (2), 213-222 (2011).
- Sathish, M., Mitani, S., Tomai, T., Honma, I. Supercritical fluid assisted synthesis of N-doped graphene nanosheets and their capacitance behavior in ionic liquid and aqueous electrolytes. J. Mater. Chem. A. 2, 4731-4738 (2014).
- Toews, K. L., Shroll, R. M., Wai, C. M., Smart, N. G. pH-Defining Equilibrium between Water and Supercritical CO2. Influence on SFE of Organics and Metal Chelates. Anal. Chem. 67 (22), 4040-4043 (1995).
- Barbaras, G., Barbaras, G. D., Finholt, A. E., Schlesinger, H. I. Cause Of Explosions Occasionally Observed During Evaporation Of Solutions Of Aluminum Hydride And Related Compounds. J. Am. Chem. Soc. 70, 877 (1948).
- Burr, J. G., Brown, W. G., Heller, H. E. The Reduction of Carbon Dioxide to Formic Acid. J. Am. Chem. Soc. 72 (6), 2560-2562 (1950).
- Hugelshofer, C. L., et al. Gas−Solid Reaction of Carbon Dioxide with Alanates. J. Phys. Chem. C. 118, 15940-15945 (2014).
- Orimo, S. I., Nakamori, Y., Eliseo, J. R., Züttel, A., Jensen, C. M. Complex Hydrides for Hydrogen Storage. Chem. Rev. 107 (10), 4111-4132 (2007).
- Gross, K. J., Thomas, G. J., Jensen, C. M. Catalyzed alanates for hydrogen storage. J. Alloys Compd. 330-332, 683-690 (2002).
- Li, H. W., Yan, Y., Orimo, S. I., Züttel, A., Jensen, C. M. Recent Progress in Metal Borohydrides for Hydrogen Storage. Energies. 4 (1), 185-214 (2011).
- Frankcombe, T. J. Proposed Mechanisms for the Catalytic Activity of Ti in NaAlH4. Chem. Rev. 112, 2164 (2012).
- Vajo, J. J., Olson, G. L. Hydrogen storage in destabilized chemical systems. Scr. Mater. 56, 829 (2007).
- Zhang, Y., et al. LiBH4 nanoparticles supported by disordered mesoporous carbon: Hydrogen storage performances and destabilization mechanisms. Int. J. Hyd. Energ. 32 (16), 3976-3980 (2007).
- Christian, M. L., Aguey-Zinsou, K. F. Core–Shell Strategy Leading to High Reversible Hydrogen Storage Capacity for NaBH4. ACS Nano. 6 (9), 7739-7751 (2012).
- Stadie, N. P., et al. Supercritical N2 Processing as a Route to the Clean Dehydrogenation of Porous Mg(BH4)2. J. Am. Chem. Soc. 136 (23), 8181-8184 (2014).
- Borgschulte, A., et al. Impurity Gas Analysis of the Decomposition of Complex Hydrides. J. Phys. Chem. C. 115, 17220-17226 (2011).
- Filinchuk, Y., et al. Porous and Dense Magnesium Borohydride Frameworks: Synthesis, Stability, and Reversible Absorption of Guest Species. Angew. Chem. Int. Ed. 50, 11162-11166 (2011).
- Li, H. W., et al. Dehydriding and rehydriding processes of well-crystallized Mg(BH4)2 accompanying with formation of intermediate compounds. Acta Mater. 56 (6), 1342-1347 (2008).
- Schüth, F., Bogdanovic, B., Felderhoff, M. Light metal hydrides and complex hydrides for hydrogen storage. Chem. Comm. , 2249-2258 (2004).
- Vitillo, J. G., Groppo, E., Bardají, E. G., Baricco, M., Bordiga, S. Fast carbon dioxide recycling by reaction with γ-Mg(BH4)2. Phys. Chem. Chem. Phys. 16, 22482-22486 (2014).
- Paskevicius, M., et al. In-Situ X-ray Diffraction Study of γ-Mg(BH4)2 Decomposition. J. Phys. Chem. C. 116, 15321-15240 (2012).
- Lemmon, E. W., Huber, M. L., McLinden, M. O. NIST standard reference database 23: reference fluid thermodynamic and transport properties. Standard Reference Data Program. , (2008).
- Moquin, P. H. L., Temelli, F. J. Kinetic modeling of hydrolysis of canola oil in supercritical media. J. Supercrit. Fluid. 45, 94-101 (2008).
- Myers, M. N., Giddings, J. C. Ultra-High-Pressure Gas Chromatography in Micro Columns to 2000 Atmospheres. Sep. Sci. 1 (6), 761-776 (1966).
- McLeary, E. E., Jansen, J. C., Kapteijn, F. Zeolite based films, membranes and membrane reactors: Progress and prospects. Microporous Mesoporous Mater. 90, 198-220 (2006).
- Richter, B., Ravnsbæk, D. B., Tumanov, N., Filinchuk, Y., Jensen, T. R. Manganese borohydride; synthesis and characterization. Dalton Trans. , (2015).
- Liang, S., Tilotta, D. C. Extraction of petroleum hydrocarbons from soil using supercritical argon. Anal. Chem. 70 (3), 616-622 (1998).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon