Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Boyuna morfolojik ve fizyolojik izleme optik koherens tomografi kullanarak üç boyutlu tümör pulcuklarının
Bu Makalede
Özet
Optik koherens tomografi (OCT), üç boyutlu görüntüleme teknolojisi, izlemek ve çok hücreli tümör pulcuklarının büyüme kinetik karakterize etmek için kullanıldı. Tümör pulcuklarının yaklaşım ve içsel optik zayıflama Karşıtlık'dayalı pulcuklarının etiket içermeyen ölü dokuyu algılama sayma Voksel kullanarak hassas hacimsel miktar gösterdi.
Özet
Tümör pulcuklarının üç boyutlu (3D) hücre kültür model kanser araştırma ve anti-kanser ilaç keşif olarak geliştirilmiştir. Ancak, şu anda, yüksek-den geçerek görüntüleme yöntemleri kullanan parlak alan veya floresan algılama, tümör küresel nedeniyle sınırlı ışık penetrasyon, difüzyon floresan boyalar ve genel olarak 3D yapısını çözümleyemediği ve Derinlik-resolvability. Son zamanlarda, bizim laboratuvar optik koherens tomografi (OCT), çok hücreli tümör pulcuklarının boyuna karakterizasyonu bir 96-şey tabak içinde gerçekleştirmek için modality, Imaging 3D etiket içermeyen ve tahribatsız kullanımı gösterilmiştir. OCT yüksekliği yaklaşık 600 µm kadar büyüyen tümör pulcuklarının 3D morfolojik ve fizyolojik bilgi alma yeteneğine sahip. Bu makalede, tüm çok iyi plaka tarayan ve tümör pulcuklarının, 3D OCT verilerini otomatik olarak alır yüksek üretilen iş OCT (HT-Ekim) görüntüleme sistemi göstermektedir. Biz protokol HT-Ekim sistemi ve inşaat kurallarda ayrıntıları açıklamak. 3D OCT verilerden bir 3D render ile küresel genel yapısını görselleştirebilirsiniz ve ortogonal dilimleri, boyut ve hacim morfolojik bilgilere göre tümör küresel boyuna büyüme eğrisi karakterize ve gelişimini izlemek Optik içsel zayıflama Karşıtlık'göre tümör küresel ölü hücre bölgelerde. HT-Ekim için eleme yanı sıra biofabricated örnekleri karakterize uyuşturucu yüksek üretilen iş görüntüleme yöntemi kullanılabileceğini göstermektedir.
Giriş
Kanser Dünya1' deki ölüm ikinci önde gelen nedenidir. Kanser hedefleme uyuşturucu gelişmekte olan hastalar için çok önemli önem taşımaktadır. Ancak, bu yeni anti-kanser ilaçlar fazla % 90 etkinlik ve klinik çalışmalarda2beklenmedik toksisite eksikliği nedeniyle geliştirme aşamasında başarısız tahmin edilmektedir. Nedeni basit iki boyutlu (2D) hücre kültür modelleri kullanımını ilaç bulma2 aşağıdaki aşamaları için bileşik etkinlik ve toksisite sınırlı tahmini değerleri ile sonuçları sağlayan bileşik filtreleme için bağlanabilir , 3 , 4. son zamanlarda, üç boyutlu (3D) tümör küresel modelleri anti-kanser ilacı discovery3,4,5 için klinik fizyolojik ve farmakolojik veri sağlamak için geliştirilmiştir ,6,7,8,9,10,11,12,13,14, 15,16,17,18,19,20,21,22,23, 24,25. Beri bu pulcuklarının tümörler vivo içindedoku özgü özelliklerini taklit edebilen, besin ve oksijen gibi ilaç direnci19, bu modellerin kullanımı yanı sıra degrade, hipoksik çekirdek potansiyel olarak ilaç bulma zaman çizelgeleri kısaltabilir, yatırım maliyetleri azaltmak ve yeni ilaçlar hastalara daha etkili bir şekilde getir. 3D tümör küresel kalkınma bileşik etkinliğini değerlendirmek için bir kritik yaklaşım küresel büyüme ve yineleme tedaviler9,26altında izlemektir. Bunu yapmak için onun çapı ve hacmi, yüksek çözünürlüklü görüntüleme yöntemleri ile ilgili tümör morfolojisi nicel karakterizasyonu zorunludur.
Konvansiyonel görüntüleme yöntemleri, alan parlak, faz kontrast7,9,22,24ve floresan mikroskopi8,9,16gibi 18,22 küresel'ın çapı ölçüsü sağlayabilirsiniz ancak küresel 3B alanda genel yapısını çözümlenemiyor. Pek çok faktör penetrasyon problama ışığın içinde küresel dahil olmak üzere bu kısıtlamalar katkıda bulunmak; küresel içine floresan boyalar difüzyon; heyecanlı floresan boyalar içinde veya küresel güçlü emme ve saçılma nedeniyle ters yüzeyine flüoresan sinyalleri yayan; ve derinlik-resolvability bu yöntemleri görüntüleme. Bu kez bir yanlış cilt ölçüde yol açar. Pulcuklarının nekrotik çekirdek geliştirilmesi nekroz vivo içinde tümör6,10,15,19,25taklit eder. Bu patolojik özellik 2D hücre kültürleri19,25,27,28çoğaltılamaz düşüktür. Küresel boyutu 500 µm çapı, üç kat konsantrik yapısı, daha büyük olan Proliferasyona hücreler dış tabakası, orta tabaka deneniyor hücre ve nekrotik bir çekirdek, dahil olmak üzere küresel6',10 görülebilir ,15,19,25, oksijen ve besin yetersizliği nedeniyle. Canlı ve ölü hücre floresans görüntüleme nekrotik çekirdek sınırına etiketlemek için standart bir yaklaşımdır. Ancak, yine, bu floresan boyalar ve görünür ışık penetrations gerçek şeklini gelişimini izlemek için nekrotik çekirdek içine sonda potansiyeline engel.
Modalite Imaging alternatif bir 3D optik koherens tomografi (OCT) tümör pulcuklarının karakterize tanıştırdı. OCT ilâ etiket içermeyen, tahribatsız 3D verileri alınıyor kapasitesine sahip bir tekniktir Biyomedikal görüntüleme 1-2 mm biyolojik doku29,30,31,32,33 derinliklerinde ,34. OCT düşük tutarlılık Interferometry örnek farklı derinliklerinden gelen sinyalleri arka dağınık algılamak için kullanır ve yatay ve dikey yönlere mikron düzeyinde mekansal çözünürlükte yeniden oluşturulan derinlik çözüldü görüntüleri sağlar. OCT göz hastalıkları35,36,37 ve anjiyografi38,39yaygın olarak benimsemiştir. Önceki çalışmalarda OCT vitro morfolojisi tümör pulcuklarının membran matris (Örneğin, Matrigel) gözlemlemek ve fotodinamik tedavi40,41onların yanıtları değerlendirmek için kullandık. Son zamanlarda, bizim grup sistematik olarak izlemek ve çok iyi plakaları423D tümör pulcuklarının büyüme kinetik ölçmek için bir yüksek-den geçerek OCT görüntüleme platformu kuruldu. Yaklaşım ve içsel optik zayıflama Karşıtlık'dayalı pulcuklarının etiket içermeyen nekrotik doku algılama sayma Voksel kullanarak 3D tümör pulcuklarının kesin hacimsel miktar gösterdi. Bu yazıda nasıl OCT görüntüleme platformu inşa ve tümör pulcuklarının yüksek çözünürlüklü 3 boyutlu görüntüleri elde etmek için istihdam ayrıntılarını açıklar. Büyüme kinetik 3D tümör pulcuklarının, küresel çapı ve birimlerin, doğru ölçümler de dahil olmak üzere, adım adım kantitatif analiz konusunda açıklanmıştır. Ayrıca, içsel optik zayıflama Karşıtlık'dayalı EKM kullanarak nekrotik doku bölgeleri tahribatsız algılama yöntemi gösterilir.
Protokol
1. hücre hazırlanması
- Hücre hatları nitelikli bir tedarikçiden edinin.
Not: hücreleri ilgi hücre satırlarından küresel kültür ortamda veya bir substrat (Matrigel gibi membran matris) yardımıyla oluşturabilir doğrulayın. Bir tur öncesi bir deneme için bir denetimi gerçekleştirmek ya da edebiyat9 içine bak. - Aşağıdaki hücre kültürünü tedarikçi tarafından sağlanan belirli yordamı donmuş hücreleri çözülme. Genel yordam43başka bir yerde bulunabilir.
- 1-2 pasajlar 25 cm2 kültür şişeler için hücreleri kültür. Hücreleri sonra 3D hücre kültürü için kullanmaya hazırsınız.
- Her gün hücreleri sağlık durumunu izlemek ve bir kuluçka (37 ° C, % 5 CO2, % 95 nem) standart koşullarda proje. Medya gerektiği gibi yenileyin.
Not: Kültür orta DMEM (4,5 g/M glikoz), %1 antibiyotik antimycotic, % 10 fetal Sığır serum oluşur. Onlar izdiham içinde kültür şişeye ulaşmadan alt kültür hücreleri. Tedarikçi tarafından sağlanan hücre kültür kılavuz izleyin. Genel bir prosedür-ebilmek bulunmak elsehwhere44. - 3D hücre kültürü çok iyi plakaları üzerinde aşağıdaki genel Protokolü9dayalı gerçekleştirin.
- Kültür balonun kültür ortamını çıkarın ve sterilize edilmiş fosfat tamponlu tuz (PBS, 37 ° C'ye ısıtılmış) ile yıkayın.
- Hücreleri tripsin ethylenediaminetetraacetic asit (EDTA, % 0.5) 1 mL ekleyerek 3 min için balonun içine resuspend. Daha sonra kültür tripsin sulandırmak için medya ekleyin.
- Hücre süspansiyon 15 mL santrifüj tüpü ve santrifüj 500 x g ve oda sıcaklığında 5 min için içine aktarın.
- Süpernatant kaldırmak ve önceden ısıtılmış kültür ortamının 4 mL içeren hücreleri resuspend. Örnek hücre konsantrasyonu belirlemek için hücre sayımı için bir hemasitometre üzerine bir damla pipet. (Örneğin, 3.000 hücre/mL) tohum için uygun toplama hücrelere sulandırmak.
Not: ilk hücre konsantrasyonu küresel her hücre kültürünü ve çok iyi plaka (96-şey, 384-şey veya 1536-şey) her tür için en iyi duruma getirme. - Tohum hücrelere bir ultra düşük eki (ULA) yuvarlak popolu çok iyi plaka. Her şey yaklaşık 600 hücreleri olan hücre süspansiyon, 200 µL 3.000 hücre/mL konsantrasyonu her kuyuda içine ekleyin.
- RT santrifüj kapasitesi 7 dk, 350 g x hızında veya kullanılabilir en düşük hız tohum sonra doğru bir plaka bağdaştırıcısı kullanan bütün tabağı.
Not: Santrifüj hücreleri tek, tek bir küresel şekillendirme kolaylaştırmak için kuyu ortasına doğru toplamak yardımcı olur. Santrifüj adım başlangıçta tümör pulcuklarının oluşturmak için yalnızca bir kez gerçekleştirilir. Tümör pulcuklarının büyüyen başlattığınızda bu yinelenir değil. - Çok iyi plaka 37 ° C ve % 5 CO2 bir kültür kuluçka korumak ve Kültür medya 3 günde yenileyin.
Not: Büyüme zaman farklı 3D kültür koşulları için değişebilir. Böylece küresel ~ 500 mikron 4\u20127 gün HCT 116 hücrelerin içinde büyüyebilir bizim çalışmada, 96-şey kaplamalar, U-87 MG ve HCT 116 hücre hatlarında 3.000 hücre/mL kullanılır. Medya takviyeleri ve büyüme faktörleri için farklı küresel modelleri, bağlı genel 3D kültür Protokolü eklemeyi düşünün. - OCT görüntüleme tümör pulcuklarının 3\u20124 günde onların büyüme boyuna bir çalışma için gerçekleştirin.
Not: OCT görüntüleme için önerilen zaman puan 4. gün, gün 7, gün 11, gün 14, gün 18 ve 21 gün olurdu.
2. yüksek-Platform Imaging üretilen iş Ekim
Not: başvuruda bulunulan bkz: iş29,30,31,32,33,34 için ayrıntılı bir inceleme ilkeleri ve uygulamaları, Ekim. Bkz: Şekil 1 ve Huang vd. 42 , görüntüleme sistemi bu çalışmada kullanılan özel Ekim Ayrıntılar için.
- Tümör küresel görüntüleme için OCT sistemi için uygun bir geniş bant ışık kaynağı seçin.
Not: Burada, merkezi bir dalga boyu ~ 1,320 ile superluminescent diyot (SLD, Şekil 1A,B) nm ve ~ 110 nm bant genişliği geniş bant bir ışık kaynağı olarak kullanıldı. - Başvuru kol ve örnek kol ( Şekil 1A,B Ayrıntılar için bakınız) şemaları takip OCT sistemi oluşturmak. OCT sistem inşa Malzemeleri tablo optik bileşenlerinin bir listesi için bkz. Başvuru kol ve örnek kol optik yol uzunluğu yakından eşleşen emin olun.
- Ekim tasarımını Spektrometre ayrıntılarını alternatif olarak, eşleşen bir ticari Spektrometre seçmek için bir Kolimatör, bir ızgara, bir F-theta lens ve bir satır taramalı kamera (bkz: Şekil 1 c için kurulum34) de dahil olmak üzere spektrometre, inşa Merkezi dalgaboyu ışık kaynağı. Spektrometre düzgün tüm Lazer bant genişliği, yüksek foton toplama verimliliği elde etmek için ve yavaş wash-out kesişim deseni sağlamak için kapsayacak şekilde hizalanmış emin olun.
- Örnek kol gücü, görüntüleme derinliği, derinlik bağımlı duyarlılık, eksenel çözünürlük, odak ve lateral çözünürlük derinliği toplam gibi aşağıdaki ölçümler de dahil olmak üzere OCT sisteminin performansını karakterize. Zayıf bir yansıtıcı (Örneğin, bir ayna ile bir nötr yoğunluk filtresi) derinlik bağımlı duyarlılık, eksenel çözünürlük ve odak derinliği ölçmek için bir örnek olarak yerleştirin. Bir USAF çözünürlük testi grafik hedef yanal çözünürlük kontrol etmek için örnek yerleştirin.
Not:34,45 tanımları ölçümler OCT performansı ve bu ölçümler45karakterize etmek için iletişim kuralları için bkz: başvurur. Bizim çalışmada kullanılan özel OCT sistemi için ölçülen parametrelerinin bir listesi için bkz. Tablo 1 . - Görüntü tümör pulcuklarının farklı Wells (bkz: Şekil 1B) çok iyi plakasına yatay hareketi sağlamak için bir motorlu çeviri sahne alanı seçin. Bir sahne ile bir seyahat sıra-108 mm x 72 mm çaptan çok iyi plaka tüm Kuyu yapımı tam bir tarama sağlamak için kullanın. Bir 2D veya 3D motorlu çeviri sahne yazılım kontrolü ile her şey tam yerini ve otomasyon OCT sistem yüksek üretilen iş görüntüleme için etkinleştirmek için kullanın.
- Bir plaka adaptörü kullanın veya bir plaka sahibi (3D baskı tarafından) çok iyi plaka sabit bir pozisyonda tutmak için tasarım.
- Yatırma ve rotasyon sahne ve çevirim sahne alanı'nda (bkz: Şekil 1 D), monte edilmiş bir rotasyon sahne devirme bir 2D kullanarak çok iyi plaka farklı kuyulardan odak düzlem varyasyonu en aza indirmek için herhangi bir OCT Imaging gerçekleştirmeden önce düzeltin. D2, D11, B6, D6, G6 yol gösterici wells göreli konumlarını (Şekil 1A) OCT görüntüleri izlerken kullanın.
- Döndürme kuyuları, OCT görüntüler (Şekil 1E) aynı yatay pozisyonlarda kadın plaka kenarlarını sahne hareket yönü ile paralel olduğundan emin olmak için plaka ayarlayın. Böylece kuyu OCT (Şekil 1F) görüntüleme için aynı dikey konumlarda kalır optik tabloya paralel olması için plaka devirme ayarlayın.
Not: Uyum devirme açı ve odak yardımcı OCT görüntü kalitesi bütün kuyuları için en iyi duruma getirme. Ancak, Kültür medya farklı Wells yüksekliğini varyasyonları küresel görüntü defocusing için yol açabilir optik yolları değişiklikler neden olabilir. Auto-odak iyi görüntü kalitesi elde etmek için OCT Imaging odak düzlemi kontrol etmek için uygulanabilir. Ayarlama adım OCT görüntü kalitesiz tümör küresel nedeniyle aşağıdaki sorunları gidermez: küresel ilk tohumlama konumu nedeniyle; decentering biofabricated hücre dışı matrisler katıştırılmış küresel yükselmesi; Zavallı plaka kaliteli iyi dipleri boy büyük farklılıklar nedeniyle. Ek yazılım denetim ile auto-odak ya da otomatik hizalama görev görüntüleme sistemi OKT performansını optimize etmek için uygulanabilir. - OCT resim alma ve her birinden de sırayla veri toplamak için sahne hareketi kontrol etmek için bir özel bilgisayar programı kullanın.
3. tarama ve tümör pulcuklarının işleme Ekim
- Tümör pulcuklarının OCT görüntüleme günü, çok iyi plaka kuluçka makinesi al. Görüntüleme sistemi OKT altında çok iyi plaka aktarın. Plaka bağdaştırıcısı üstüne yerleştirin.
Not: Tümör pulcuklarının OCT görüntüleme Polistren levha kapak açma veya kapatma ile gerçekleştirilebilir. Ancak, kuyulardan buharlaşma nedeniyle kapağındaki su yoğunlaşmaları ışık geçirgenliği etkiler ve en uygun daha az OCT görüntüleri pulcuklarının verimli ışık yolunu deforme. - Z-yönünü çeviri sahne hareket ettirerek plaka yüksekliğini ayarlayın. ~ 100-200 odak düzlemi konumunu korumak mikron depth-wise üniform olmayan etkisini en aza indirmek için her küresel üst yüzeyinin altında odak profil.
- Bir uygun OCT tarama aralığı (Örneğin, 1 mm x 1 mm) onun gelişme evrelerine göre bütün tümör küresel karşılamak için özel yazılım ayarlayın. Ayarı kaydetmek için Kaydet parametreler ' i tıklatın.
- Tümör pulcuklarının teker teker pulcuklarının içeren plaka bütün kuyuları için 3 boyutlu OCT görüntüleri elde etmek için özel yazılım kullanmak. Önizleme resmi görüntülemek ve OCT görüntü elde etmek için Al düğmesini tıklatın için Önizleme düğmesini tıklatın.
Not: sahne hareket halinde değilken OCT küresel veri toplanan olun. Küresel U alt Merkezi'nde de genellikle bulunur. Ancak, sahne hızlanan veya küresel kültür medya atalet nedeniyle yavaşlatma küresel kültür medyada kaydırılır. - İşlem 3D OCT veri kümeleri, tümör pulcuklarının özel C++ işleme kodu ile OCT yapısal görüntüler oluşturmak için. Şekil 2A post-processing OCT veri akış çizelgesi için bkz.
Not: Şekil 4A oluşturulan 3D OCT yapısal görüntüleri için bkz.- Bkz: Bölüm 5, Drexler ve Fujimoto34 ve Jian vd. 46 OCT veri işleme adımları ayrıntılı açıklaması için. Tüm üç boyutlu piksel boyutunu ayarlamak. OCT yapısal görüntü düzeltilmiş ölçeklerde yeniden ölçeklendirme.
Not: Başvuru kol ve örnek kol optik yol farkı ölçüsü eksenel yönde (z-yön) OCT görüntülerin mesafedir. Böylece, kırılma indisi (n) örneğinin rescaling için eksenel yönde piksel boyutunu ayarlama zaman dikkate alınması gerekir. Bizim çalışmada, n kullandığımız 1.37 tümör küresel42kırılma indisi =.
- Bkz: Bölüm 5, Drexler ve Fujimoto34 ve Jian vd. 46 OCT veri işleme adımları ayrıntılı açıklaması için. Tüm üç boyutlu piksel boyutunu ayarlamak. OCT yapısal görüntü düzeltilmiş ölçeklerde yeniden ölçeklendirme.
- Küresel görüntüleri 2B OCT görüntüleri üç kesitsel XY, XZ ve YZ uçak içinde küresel centroid kullanarak kolaj oluşturmak. Şekil 3 c-E kolajlar küresel görüntüleri temsilcisi çıkışı için bkz. Tüm küresel cisimlerin yaklaşık aynı yerde konumlandığından emin olmak için MATLAB işlevi dftregistration47, kullanarak tüm pulcuklarının için görüntü kaydı gerçekleştirmek.
- Bir ticari veya özel yazılım kullanarak küresel 3D render edinin.
Not: Aşağıdaki adımlar tümör pulcuklarının ticari bir yazılım kullanarak 3D render edinme gösterir.- 3D OCT veri belgili tanımlık bilgisayar yazılımı yükleyin.
- Surpass Masası'nı tıklatın. Sonra Eklemek Yeni Birim'itıklatın. 3D render için kullanılacak karışım modu seçin.
- Görüş açısı fare işaretçisini kullanarak görüntü sürükleyerek ayarlayın.
3D tümör pulcuklarının 4. morfolojik miktar
Not: Bu miktar özel bir yazılı kod MATLAB içinde işler. İşlemi başlatmak için Çalıştır düğmesini tıklatın. Şekil 2B pulcuklarının morfolojik miktar adımları akış çizelgesi için bkz.
- Küresel çapı, yükseklik ve çapı tabanlı birim ölçmek.
- 2D OCT görüntüleri küresel centroid geçen üç kesitsel XY, XZ ve YZ uçak içinde seçin.
- Çapı ölçmek ve küresel XY ve XZ yüksekliğini uçak, anılan sıraya göre.
- Küresel çapı tabanlı birim kullanarak hesaplama:
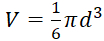 , tümör küresel şeklinde bir varsayım ile.
, tümör küresel şeklinde bir varsayım ile.
- Voksel tabanlı küresel güç ölçmek.
- Speckles kaldırmak için küresel OCT yapısal Datası 3D ortalama filtre uygulayın.
- Açıkgöz kenar algılama48 filtre, kare kare, tümör küresel bölge iyi alttan ayıran uygun bir eşik ile kullanarak tümör pulcuklarının kesiminde.
- 3D verileri için bağ voxels grubu (yerleşik işlev bkz: bwconncomp).
- Her bağ Voksel grubunda ve (el ile seçilmiş), küresel centroid her grup için arasındaki uzaklığı hesaplamak. Küresel bölge grup olarak en az ortalama mesafe ile tanımlayın.
- Voxels küresel bölgesi içinde saymak ve küresel toplam hacmi verimli gerçek birim (birim/Voksel), bir tek tek Voksel tarafından çarpın.
5. ölü hücre bölge 3D tümör pulcuklarının tespiti
Not: homojen bir ortamda bira-Lambert hukuk49tarafından OCT geri dağınık yoğunluğu Derinlik (ı(z)) bir fonksiyonu olarak algılanan tanımlanabilir: 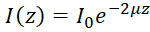 , z derinliğini gösterir nerede μ optik zayıflama olduğunu katsayısı, ve ben0 örnek olay yoğunluğu. Bu nedenle türetilmiş optik zayıflatma katsayısı olarak ifade edilebilir:
, z derinliğini gösterir nerede μ optik zayıflama olduğunu katsayısı, ve ben0 örnek olay yoğunluğu. Bu nedenle türetilmiş optik zayıflatma katsayısı olarak ifade edilebilir: 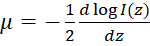 . OCT görüntüleri kez logaritmik bir ölçekte çizilen ilişkili beri OCT yoğunluğu profil eğimi optik zayıflatma katsayısı türetmek için alınabilir. Şekil 2C optik zayıflatma haritaların üretimi bir akış çizelgesi için bkz:.
. OCT görüntüleri kez logaritmik bir ölçekte çizilen ilişkili beri OCT yoğunluğu profil eğimi optik zayıflatma katsayısı türetmek için alınabilir. Şekil 2C optik zayıflatma haritaların üretimi bir akış çizelgesi için bkz:.
- Küresel dışında istenmeyen bölgeleri kaldırmak için segment gerçekleştirin. OCT Albümdeki doğasında vardır benek gürültü bastırmak için 3D ortalama filtre uygulayın.
- Pixel-Wise edinmek optik zayıflama katsayıları doğrusal tarafından belirli bir derinlik Aralık üzerinde (hareketli pencere), günlük ölçekli OCT yoğunluğu profiline uyan onun yamaç ayıklamak ve yamaç -1 tarafından çarpın/2.
Not: Her Voksel parçalı Küresel bölgesi içinde zayıflatma katsayısı OCT yoğunluğu profil 10-Voksel derinlik penceresindeki (derinlemesine ~ 40 mikron), eğimi dayalı ortasındaki pencerede yer alan Voksel ile hesaplanır. - Bir çerçeve içinde eksenel her tarama ve optik zayıflama katsayıları parçalı Küresel bölgesinin tüm voxels için hesaplanır kadar parçalı Küresel bölge içeren bir 3B veri kümesi her çerçevede yukarıda (merdiven 5.1 ve 5.2) yöntemleri uygulayın.
- Yüksek-zayıflama bölgesi vurgulamak için ikili eşik gerçekleştirin.
Not: Bkz: Huang vd. 42 eşik çubuk grafik analizi ile yüksek-zayıflama bölgesinin belirlenmesi için. - Binarized optik zayıflama harita (karıştırma) ölü hücre bölge etiketlemek için orijinal görüntü üzerinde vurgulayın. Ölü hücre bölgesinin 3D dağılımını görselleştirmenizi karışımlı zayıflama harita 3D olarak işlenen görüntü oluşturmak.
6. Histoloji ve immünhistokimya
Not: Histoloji ve tümör pulcuklarının görüntülerini lekeli immünhistokimya (IHC) karşılık gelen OCT sonuçları ile ilişkilendirmek için elde edilir.
- Seçilen zaman noktalarda, 1-2 tümör pulcuklarının Histoloji ve IHC boyama çok iyi plaka seçin. Bir pipet 1 mL pipet ipuçları ile küresel bir 1,5 mL santrifüj tüpü kuyudan aktarmak için kullanın.
Not: 1 mL pipet ucu ucunu açılışı küresel yapısını zarar görmesini önlemek için tümör küresel boyutundan büyük olduğundan emin olmak için transfer önce kesilmiş. - % 10 formaldehit ve düzeltme 48 h için dolu bir tek 1.5 mL microcentrifuge tüp her tümör küresel toplayın.
- Histoloji ve IHC işlemleri standart parafin katıştırma teknikleri kullanarak her küresel için gerçekleştirin.
Not: Leke 5 mikron kalınlığında kesitler tümör pulcuklarının Hematoksilen ve eozin (H & E) ve terminal deoksinükleotidil transferaz dUTP nick bitiş (tünel) apoptosis algılama etiketleme için. Hematoksilen counterstaining tünel için uygulanır. Dijital slayt tarayıcı lekeli örnek inceden inceye gözden geçirmek ve yüksek çözünürlüklü elde etmek için kullanılan histolojik ve IHC görüntüler.
Sonuçlar
Yüksek işlem hacmi optik koherens tomografi görüntüleme pulcuklarının bir 96-şey plaka
Şekil 3 gün 3 HCT 116 tümör pulcuklarının 96-şey plakalı HT-Ekim tarama sonucu sergiler. Koca tabağı sıralı tarama (H12) sağ alt kuyudan başlar. Şekil 3B HT-Ekim sisteminin yazılım uygulama Akış grafiğini gösterir. Bir küresel veriler toplanır ve işlenen s...
Tartışmalar
Tümör faaliyet morfolojik yapısı için son derece uygundur. Karakteristik büyüme eğrisi 2D hücre kültürleri için izleme, izleme için 3D tümör pulcuklarının büyüme eğrisi de uzun vadeli küresel büyüme davranış farklı hücre hatları için karakterize etmek için geleneksel bir yaklaşım benzer. Özellikle, biz tümör bozulma ya da doğrudan büyüme eğrisi yansır tümör büyütme analiz ederek uyuşturucu yanıt karakterize olabilir. Bu nedenle, boyutu ve büyüme eğrisi türetmek için ses ...
Açıklamalar
Yazarlar hiçbir rakip faiz ifşa.
Teşekkürler
Bu eser NSF tarafından desteklenen IDBR (DBI-1455613), PFI:AIR verir-TT (dudak-1640707), NIH hibe R21EY026380, R15EB019704 ve R01EB025209 ve Lehigh Üniversitesi başlangıç fonu.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Custom Spectral Domain OCT imaging system | Developed in our lab | ||
| Superluminescent Diode (SLD) | Thorlabs | SLD1325 | light source |
| 2×2 single mode fused fiber coupler, 50:50 splitting ratio | AC Photonics | WP13500202B201 | |
| Reference Arm | |||
| Lens Tube | Thorlabs | ||
| Adapter | Thorlabs | ||
| Collimating Lens | Thorlabs | AC080-020-C | |
| Focusing Lens | Thorlabs | ||
| Kinematic Mirror Mount | Thorlabs | ||
| Mirror | Thorlabs | ||
| 1D Translational Stage | Thorlabs | ||
| Continuous neutral density filter | Thorlabs | ||
| Pedestrial Post | Thorlabs | ||
| Clamping Fork | Thorlabs | ||
| Sample Arm | |||
| Lens Tube | Thorlabs | ||
| Adapter | Thorlabs | ||
| Collimating Lens | Thorlabs | AC080-020-C | |
| Galvanometer | Thorlabs | ||
| Relay Lens | Thorlabs | AC254-100-C | two Relay lens to make a telescope setup |
| Triangle Mirror Mount | Thorlabs | ||
| Mirror | Thorlabs | ||
| Objective | Mitutoyo | ||
| Pedestrial Post | Thorlabs | ||
| Clamping Fork | Thorlabs | ||
| Polarization Controller | Thorlabs | ||
| 30mm Cage Mount | Thorlabs | ||
| Cage Rod | Thorlabs | ||
| Stage | |||
| 3D motorized translation stage | Beijing Mao Feng Optoelectronics Technology Co., Ltd. | JTH360XY | |
| 2D Tilting Stage | |||
| Rotation Stage | |||
| Plate Holder | 3D printed | ||
| Spectrometer | |||
| Lens Tube | Thorlabs | ||
| Adapter | Thorlabs | ||
| Collimating Lens | Thorlabs | AC080-020-C | |
| Grating | Wasatch | G = 1145 lpmm | |
| F-theta Lens | Thorlabs | FTH-1064-100 | |
| InGaAs Line-scan Camera | Sensor Unlimited | SU1024-LDH2 | |
| Name | Company | Catalog Number | Comments |
| Cell Culture Component | |||
| HCT 116 Cell line | ATCC | CCL-247 | |
| Cell Culture Flask | SPL Life Sciences | 70025 | |
| Pipette | Fisherbrand | 14388100 | |
| Pipette tips | Sorenson Bioscience | 10340 | |
| Gibco GlutaMax DMEM | Thermo Fisher Scientific | 10569044 | |
| Fetal Bovine Serum, certified, US origin | Thermo Fisher Scientific | 16000044 | |
| Antibiotic-Antimycotic (100X) | Thermo Fisher Scientific | 15240062 | |
| Corning 96-well Clear Round Bottom Ultra-Low Attachment Microplate | Corning | 7007 | |
| Gibco PBS, pH 7.4 | Thermo Fisher Scientific | 10010023 | |
| Gibco Trypsin-EDTA (0.5%) | Thermo Fisher Scientific | 15400054 | |
| Forma Series II 3110 Water-Jacketed CO2 Incubators | Thermo Fisher Scientific | 3120 | |
| Gloves | VWR | 89428-750 | |
| Parafilm | Sigma-Aldrich | P7793 | |
| Transfer pipets | Globe Scientific | 138080 | |
| Centrifuge | Eppendorf | 5702 R | To centrifuge the 15 mL tube |
| Centrifuge | NUAIRE | AWEL CF 48-R | To centrifuge the 96-well plate |
| Microscope | Olympus | ||
| Name | Company | Catalog Number | Comments |
| Histology & IHC | |||
| Digital slide scanner | Leica | Aperio AT2 | Obtain high-resolution histological images |
| Histology Service | Histowiz | Request service for histological and immunohistological staining of tumor spheroid | |
| Name | Company | Catalog Number | Comments |
| List of Commerical OCTs | |||
| SD-OCT system | Thorlabs | Telesto Series | |
| SD-OCT system | Wasatch Photonics | WP OCT 1300 nm | |
| Name | Company | Catalog Number | Comments |
| Software for Data Analyses | |||
| Basic Image Analysis | NIH | ImageJ | Fiji also works. |
| 3D Rendering | Thermo Fisher Scientific | Amira | Commercial software. Option 1 |
| 3D Rendering | Bitplane | Imaris | Commercial software. Option 2. Used in the protocol |
| OCT acquisition software | custom developed in C++. | ||
| Stage Control | Beijing Mao Feng Optoelectronics Technology Co., Ltd. | MRC_3 | Incorporated into the custom OCT acquisition code |
| OCT processing software | custom developed in C++. Utilize GPU. Incorporated into the custom OCT acquisition code. | ||
| Morphological and Physiological Analysis | custom developed in MATLAB |
Referanslar
- Kola, I., Landis, J. Can the pharmaceutical industry reduce attrition rates?. Nature Reviews Drug Discovery. 3 (8), 711-716 (2004).
- Breslin, S., O'Driscoll, L. Three-dimensional cell culture: the missing link in drug discovery. Drug Discovery Today. 18, 240-249 (2013).
- Hickman, J. A., et al. Three-dimensional models of cancer for pharmacology and cancer cell biology: Capturing tumor complexity in vitro/ex vivo. Biotechnology Journal. 9 (9), 1115-1128 (2014).
- Sutherland, R. M. Cell and environment interactions in tumor microregions: the multicell spheroid model. Science. 240 (4849), 177-184 (1988).
- Mueller-Klieser, W. Three-dimensional cell cultures: from molecular mechanisms to clinical applications. American Journal of Physiology - Cell Physiology. 273, C1109-C1123 (1997).
- Friedrich, J., Seidel, C., Ebner, R., Kunz-Schughart, L. A. Spheroid-based drug screen: considerations and practical approach. Nature Protocols. 4 (3), 309-324 (2009).
- Tung, Y. -. C., et al. High-throughput 3D spheroid culture and drug testing using a 384 hanging drop array. The Analyst. 136 (3), 473-478 (2011).
- Vinci, M., et al. Advances in establishment and analysis of three-dimensional tumor spheroid-based functional assays for target validation and drug evaluation. BMC biology. 10, 29 (2012).
- LaBarbera, D. V., Reid, B. G., Yoo, B. H. The multicellular tumor spheroid model for high-throughput cancer drug discovery. Expert Opinion on Drug Discovery. 7, 819-830 (2012).
- Pampaloni, F., Ansari, N., Stelzer, E. H. K. High-resolution deep imaging of live cellular spheroids with light-sheet-based fluorescence microscopy. Cell and Tissue Research. 352, 161-177 (2013).
- Lovitt, C. J., Shelper, T. B., Avery, V. M. Miniaturized three-dimensional cancer model for drug evaluation. Assay and Drug Development Technologies. 11 (7), 435-448 (2013).
- Wenzel, C., et al. 3D high-content screening for the identification of compounds that target cells in dormant tumor spheroid regions. Experimental Cell Research. 323 (1), 131-143 (2014).
- Astashkina, A., Grainger, D. W. Critical analysis of 3-D organoid in vitro cell culture models for high-throughput drug candidate toxicity assessments. Innovative tissue models for drug discovery and development. 69, 1-18 (2014).
- Edmondson, R., Broglie, J. J., Adcock, A. F., Yang, L. Three-dimensional cell culture systems and their applications in drug discovery and cell-based biosensors. Assay and Drug Development Technologies. 12 (4), 207-218 (2014).
- Gong, X., et al. Generation of multicellular tumor spheroids with microwell-based agarose scaffolds for drug testing. PLoS ONE. 10 (6), e0130348 (2015).
- Hoffmann, O. I., et al. Impact of the spheroid model complexity on drug response. Journal of biotechnology. 205, 14-23 (2015).
- Martinez, N. J., Titus, S. A., Wagner, A. K., Simeonov, A. High-throughput fluorescence imaging approaches for drug discovery using in vitroand in vivothree-dimensional models. Expert Opinion on Drug Discovery. 10, 1347-1361 (2015).
- Nath, S., Devi, G. R. Three-dimensional culture systems in cancer research: Focus on tumor spheroid model. Pharmacology, Therapeutics. 163, 94-108 (2016).
- Li, L., Zhou, Q., Voss, T. C., Quick, K. L., LaBarbera, D. V. High-throughput imaging: Focusing in on drug discovery in 3D. Methods. 96, 97-102 (2016).
- Ham, S. L., Joshi, R., Thakuri, P. S., Tavana, H. Liquid-based three-dimensional tumor models for cancer research and drug discovery. Experimental Biology and Medicine. 241 (9), 939-954 (2016).
- Kessel, S., et al. High-Throughput 3D Tumor Spheroid Screening Method for Cancer Drug Discovery Using Celigo Image Cytometry. Journal of Laboratory Automation. , 2211068216652846 (2016).
- Stock, K., et al. Capturing tumor complexity in vitro: Comparative analysis of 2D and 3D tumor models for drug discovery. Scientific Reports. 6, 28951 (2016).
- Thakuri, P. S., Ham, S. L., Luker, G. D., Tavana, H. Multiparametric analysis of oncology drug screening with aqueous two-phase tumor spheroids. Molecular Pharmaceutics. 13 (11), 3724-3735 (2016).
- Lin, R. Z., Chang, H. Y. Recent advances in three-dimensional multicellular spheroid culture for biomedical research. Biotechnology Journal. 3 (9-10), 1172-1184 (2008).
- Piccinini, F., Tesei, A., Arienti, C., Bevilacqua, A. Cancer multicellular spheroids: Volume assessment from a single 2D projection. Computer Methods and Programs in Biomedicine. 118 (2), 95-106 (2015).
- Zanoni, M., et al. 3D tumor spheroid models for in vitro therapeutic screening: a systematic approach to enhance the biological relevance of data obtained. Scientific Reports. 6, 19103 (2016).
- Debnath, J., Brugge, J. S. Modelling glandular epithelial cancers in three-dimensional cultures. Nature Reviews Cancer. 5 (9), 675-688 (2005).
- Huang, D., et al. Optical coherence tomography. Science. 254 (5035), 1178-1181 (1991).
- Drexler, W., et al. Optical coherence tomography today: speed, contrast, and multimodality. Journal of Biomedical Optics. 19 (7), 071412 (2014).
- Fujimoto, J., Swanson, E. The development, commercialization, and impact of optical coherence tomography. Investigative Ophthalmology, Visual Science. 57 (9), (2016).
- Vakoc, B. J., Fukumura, D., Jain, R. K., Bouma, B. E. Cancer imaging by optical coherence tomography: preclinical progress and clinical potential. Nature Reviews Cancer. 12 (5), 363-368 (2012).
- Wojtkowski, M. High-speed optical coherence tomography: basics and applications. Applied optics. 49 (16), D30-D61 (2010).
- Drexler, W., Fujimoto, J. G. . Optical coherence tomography: technology and applications. , (2008).
- Geitzenauer, W., Hitzenberger, C. K., Schmidt-Erfurth, U. M. Retinal optical coherence tomography: past, present and future perspectives. British Journal of Ophthalmology. 95 (2), 171 (2011).
- Sakata, L. M., DeLeon-Ortega, J., Sakata, V., Girkin, C. A. Optical coherence tomography of the retina and optic nerve - a review. Clinical, Experimental Ophthalmology. 37 (1), 90-99 (2009).
- van Velthoven, M. E. J., Faber, D. J., Verbraak, F. D., van Leeuwen, T. G., de Smet, M. D. Recent developments in optical coherence tomography for imaging the retina. Progress in Retinal and Eye Research. 26 (1), 57-77 (2007).
- Kashani, A. H., et al. Optical coherence tomography angiography: A comprehensive review of current methods and clinical applications. Progress in Retinal and Eye Research. 60, 66-100 (2017).
- de Carlo, T. E., Romano, A., Waheed, N. K., Duker, J. S. A review of optical coherence tomography angiography (OCTA). International Journal of Retina and Vitreous. 1 (1), 5 (2015).
- Sharma, M., Verma, Y., Rao, K. D., Nair, R., Gupta, P. K. Imaging growth dynamics of tumour spheroids using optical coherence tomography. Biotechnology Letters. 29 (2), 273-278 (2006).
- Jung, Y., Nichols, A. J., Klein, O. J., Roussakis, E., Evans, C. L. Label-Free, Longitudinal Visualization of PDT Response In Vitro with Optical Coherence Tomography. Israel Journal of Chemistry. 52 (8-9), 728-744 (2012).
- Huang, Y., et al. Optical coherence tomography detects necrotic regions and volumetrically quantifies multicellular tumor spheroids. Cancer Research. 77 (21), 6011-6020 (2017).
- Spalteholz, W. . Über das Durchsightigmachen von menschlichen und tierischen Präparaten: nebst Anhang, Über Knochenfärbung. , (1911).
- Dodt, H. -. U., et al. Ultramicroscopy: three-dimensional visualization of neuronal networks in the whole mouse brain. Nature Methods. 4 (4), 331 (2007).
- Leitgeb, R., Hitzenberger, C., Fercher, A. F. Performance of fourier domain vs. time domain optical coherence tomography. Optics express. 11 (8), 889-894 (2003).
- Jian, Y., Wong, K., Sarunic, M. V. . Optical Coherence Tomography and Coherence Domain Optical Methods in Biomedicine XVII. , 85710Z (2013).
- Guizar-Sicairos, M., Thurman, S. T., Fienup, J. R. Efficient subpixel image registration algorithms. Optics Letters. 33 (2), 156-158 (2008).
- Canny, J. A computational approach to edge detection. IEEE Transactions on Pattern Analysis and Machine Intelligence. (6), 679-698 (1986).
- Vermeer, K. A., Mo, J., Weda, J. J. A., Lemij, H. G., de Boer, J. F. Depth-resolved model-based reconstruction of attenuation coefficients in optical coherence tomography. Biomedical Optics Express. 5 (1), 322-337 (2014).
- Klein, T., et al. Multi-MHz retinal OCT. Biomedical Optics Express. 4, 1890-1908 (2013).
- Klein, T., Huber, R. High-speed OCT light sources and systems [Invited]. Biomedical Optics Express. 8 (2), 828-859 (2017).
- Zhou, C., Alex, A., Rasakanthan, J., Ma, Y. Space-division multiplexing optical coherence tomography. Optics Express. 21, 19219-19227 (2013).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır