Method Article
توليد خلايا T - Multivirus محددة لمنع / علاج الالتهابات الفيروسية خيفي بعد زرع الخلايا الجذعية المكونة للدم
In This Article
Summary
والسريع ، وبروتوكول بسيطة وفعالة من حيث التكلفة لتوليد المانحة المستمدة multivirus محددة CTLs (rCTL) للتسريب لخيفي الخلايا الجذعية المكونة للدم المستلمين (HSCT) زرع في خطر لتطوير CMV ، المحامي أو EBV العدوى. هذا هو عملية التصنيع GMP المتوافقة ، وينبغي ضمان تنفيذ أوسع تي خلية المناعي خارج المراكز المتخصصة.
Abstract
الالتهابات الفيروسية تسبب الاعتلال والوفيات في خيفي زرع الخلايا الجذعية المكونة للدم (HSCT) المتلقين. لقد ولدت نحن وغيرنا بنجاح وأكسب خلايا تي محددة للفيروس ابشتاين بار (EBV) ، الفيروس المضخم للخلايا (CMV) واتش (إيج) باستخدام وحيدات الخلية تتحول EBV - lymphoblastoid (EBV ، LCL) الجينات المعدلة وراثيا مع ناقلات واتش خلايا مولدة تقديم (ناقلات الجنود المدرعة). عدد قليل من 2x10 5 / كغ trivirus محددة اللمفاويات التائية السامة للخلايا (CTL) التي انتشرت بعد عدة سجلات التسريب ويبدو لمنع وعلاج مرض فيروسي حاد حتى مقاومة للعلاجات المتوفرة الأخرى. يقتصر على نطاق أوسع تنفيذ هذا النهج تشجيع ارتفاع تكاليف الإنتاج والتعقيد الصنع والوقت لفترات طويلة (4-6 أسابيع لEBV LCL - جيل ، و4-8 أسابيع لصنع CTL -- المجموع 10-14 أسبوعا) للتحضير. للتغلب على هذه القيود وضعت لدينا جديد ، GMP المتوافقة مع بروتوكول إنتاج CTL. أولا ، في مكان adenovectors لتحفيز خلايا تي نستخدم الخلايا الجذعية (DCS) nucleofected مع الحمض النووي البلازميدات ترميز LMP2 ، وEBNA1 BZLF1 (EBV) ، وHexon بينتون (إيج) ، وpp65 وIE1 (CMV) وتقديم مستضد الخلايا. هذه ناقلات الجنود المدرعة تنشيط خلايا تي محددة لجميع مستضدات محفزة. الثانية ، وثقافة تنشيط خلايا تي في وجود IL - 4 (1000 يو / مل) ، وIL - 7 (10ng/ml) الزيادات وتحافظ على ذخيرة وتيرة معينة في الخلايا التائية خطوطنا. الثالثة ، وقد استخدمنا جديدة والغاز نفاذية الجهاز الثقافة (G - ريكس) أن يشجع على التوسع وبقاء أعداد كبيرة الخلية بعد التحفيز واحد ، وبالتالي إزالة شرط EBV ، والحد من التدخل LCLs فني. من خلال تنفيذ هذه التغييرات يمكن أن ننتج الآن CTL multispecific استهداف EBV ، CMV ، وإيج بتكلفة 6 10 في الخلايا التي خفضت بنسبة 90 ٪> ، وفقط في 10 يوما بدلا من 10 أسابيع باستخدام النهج الذي يمكن تمديدها إلى إضافية المستضدات الفيروسية واقية. وينبغي لنا وافقت عليها الهيئة النهج تكون ذات قيمة لتطبيقات والعلاج الوقائي للمستلمين خطر HSCT خيفي عالية.
Protocol
1. DC nucleofection
- حصاد الوحيدات المستمدة من البلدان النامية ، والتي تم الالتزام به المخصب البلاستيك ، ومثقف لمدة 5 أيام باستخدام خلية Genix تستكمل مع وسائل الإعلام IL4 (1000U/ml) ، GMCSF (800IU/ml) ونضجت لمزيد من 24hrs باستخدام السيتوكينات نضوج العاصمة IL4 (1000U / مل) ، GMCSF (800IU/ml) ، IL6100ng/ml ، TNF - α 10ng/ml ، 10ng/ml IL1 - β وPGE2 (1μg/ml) 1 ، عن طريق إعادة تعليق لطيف مع ماصة نقل 3ml.
- عدد البلدان النامية قادرة على البقاء به التريبان الأزرق ، ونقل إلى أنابيب 3X مع 15ml مما لا يقل عن 6 و 0.5x10 لا يزيد على 6 خلايا 2x10 / أنبوب.
- الطرد المركزي للبلدان النامية 10mins @ 200G. خلال هذا الوقت قبل وسائل الاعلام الحارة خلية Genix تستكمل مع السيتوكينات نضوج العاصمة (وسائل الإعلام نضوج DC) -- 2ml/well في ثلاثة آبار لزراعة الأنسجة 12 يعامل بشكل جيد لوحة في 37 ° / C 5 ٪ CO 2 الحاضنة.
- بمجرد الانتهاء من الخلايا الغزل ، ونضح وطاف وإضافة البلازميدات الحمض النووي ذات الصلة في كل من الأنابيب في التركيز النهائي من الحمض النووي 5μg / أنبوب. في هذه الحالة إضافة ترميز البلازميد IE1 pp65 - إلى أنبوب رقم 1 ، Hexon - بينتون إلى أنبوب رقم 2 ، وEBNA1 - LMP2 - BZLF1 إلى أنبوب # 3.
- Resuspend البلدان النامية والحمض النووي مع 100μl حل nucloefection Amaxa ، تخلط جيدا ونقل إلى cuvettes nucleofection.
- cuvettes مكان في nucleofector 4D ، واختيار البرنامج CB150 (Amaxa / Lonza) ، ثم اضغط على بدء.
- مزيج مباشرة بعد إضافة nucleofection 500μl 2ml من قبل وسائل الإعلام تحسنت الخلية Genix نضوج العاصمة لكفيت ، بلطف صعودا ونزولا pipetting 2-3 مرات ، ونقل nucleofected البلدان النامية إلى لوحة 12 - المعدة إعدادا جيدا المتبقية التي تحتوي على 1.5 مل من prewarmed وسائل الاعلام العاصمة النضج. نقل إلى 37 لمزيد من 18hrs - 12 C / 5 ٪ CO 2 حاضنة درجة.
2. تي الخلية التحفيز
- الحصاد وعدد البلدان النامية nucleofected ، وأشرق في 30Gy. يغسل مرة واحدة مع 10ML CTL المتوسطة (45 ٪ RPMI ، الزيارات EHAA 45 ٪ ، 10 ٪ FBS ، 2mm وGlutamax) وresuspend @ 3 × 10 5 مل من البلدان النامية في وسائل الاعلام CTL.
- تجمع ما لا يقل عن 7.5x10 5 (2.5ml) وبحد أقصى 15x10 5 (5ml) من البلدان النامية التي تحتوي على كل من البلازميدات ونقل البلدان النامية المجمعة للجهاز G - ركس والتي سوف ثم يوضع في الحاضنة.
- لإعداد الرد إما استخدام خلايا مجمدة PBMCs سابقا أو غير ملتصقة الخلايا وحيدة النواة التي تبقى بعد اختيار العاصمة (التقيد أو التحديد CD14). أذاب الخلايا ، ونقل إلى مستنبت prewarmed ، ويغسل مرة واحدة مع وسائل الاعلام CTL. Resuspend الخلايا في وسائل الإعلام CTL ، عد الخلايا وتقديمهم للتركيز الخلايا 6 2x10 لكل مليلتر. تأخذ 15x10 6 خلايا أو 7.5ml والملحق مع 30000U IL4 (1000U/ml -- اضرب النهائي) و300ng IL7 (10ng/ml -- اضرب النهائي).
- نقل 7.5ml من PBMC (15x10 6 خلايا) إلى G - ريكس وأعلى حتى من مفاعل حيوي مع وسائل الاعلام CTL إلى إجمالي حجم 30ml.
- ثقافة G - ركس ل6-7 أيام في 37 درجة مئوية / 5 ٪ CO 2 حاضنة مرطب.
3. تي خلية التوسع
- في يوم 07/06 ، 10ML نضح من وسائل الإعلام ، ثم خليط الخلايا في 20ml المتبقية من وسائل الاعلام مع ماصة 10ML والعد باستخدام خلايا قابلة للحياة التريبان الأزرق. إذا كان هناك <50x10 6 تجديد مع وسائل الاعلام الطازج + السيتوكينات. إذا كان هناك> 50x10 6 خلايا إزالة 10ML التعليق الخلية ، ونقل إلى ريكس - G الجديد ، ومن ثم خدمة كل من G - Rexs مع وسائل الاعلام CTL + السيتوكينات الطازجة.
- الثقافة ل4-6 أيام إضافية. مرة واحدة وقد تم توسيع خلايا كافية ، وأداء الخصائص المظهرية والوظيفية للفائض CTL وcryopreserve لاستخدامها في المستقبل.
4. ممثل النتائج :
ويرد التخطيطي لدينا وافقت عليها الهيئة multivirus محددة عملية توليد CTL في الشكل 1. وعلى النقيض من بروتوكولات الاتفاقية CTL multivirus التي تستخدم adenovectors وEBV LCL - الفيروس لتحفيز التفاعل خلايا تي 2 لدينا استبدال المواد المعدية فيروس البلازميدات مع الحمض النووي تكود المستضدات المتعددة المستمدة من كل من الفيروسات 3. لتحفيز trivirus CTL مصممة لدينا ثلاثة multicistronic البلازميدات ترميز Hexon وبينتون واتش ، وIE1 pp65 من CMV ، وEBNA1 ، LMP2 ، وBZLF1 من EBV. وقد تم اختيار هذه المستضدات على أساس نتائج مشجعة السريرية لمنطقتنا والمجموعات الأخرى التي تبين أن الخلايا T - الموجهة ضد أدفانسد hexon وبينتون 2،4-6 ، وCMV - 1E1 وCMV - pp65 وقائية في الجسم الحي 7. لEBV ، EBNA1 هو سائد مناعيا CD4 + T مستضد الخلية المستهدفة التي أعرب عنها في جميع الأورام الخبيثة المرتبطة EBV في الخلايا الطبيعية وباء EBV المصابين 8،9 ، LMP2 يولد مناعة عبر أنواع HLA متعددة ، وأعرب عن معظم الأورام الخبيثة في EBV ، في حين أن 10،11 BZLF1 بترميز آن ، على الفور في وقت مبكر سائد مناعيا مستضد دورة lytic التي تحفز كلا CD4 + CD8 + وخلايا تي من معظم الأفراد والمهم المحتمل للتعاونntrol الخلايا تكرار الفيروس 12. لمزيد من تحسين طرق التصنيع لدينا تعاونا مع تقنية الطبيعة الذي ولدت minimalized ، خالية من المضادات الحيوية (FDA المتوافقة) البلازميدات لتحفيز CTL 13،14. باستخدام هذه الاستراتيجية أن نحقق الكفاءة باستمرار nucleofection من 35 ٪> عالية مع المحافظة على سلامة الخلية (لا تظهر البيانات) 3. الشكل 2 يبين أن تواتر الفيروس الخلايا T محددة ردا على الحمض النووي البلازميدات الأمثل مقاسا ELIspot IFNγ ، كان أكبر من ردا على التعبير البلازميدات pShuttle التقليدية المستندة إلى التعبير عن مستضدات نفس (ن = 8 اتش ، ن = 4 CMV ، و n = 2 EBV). وكان PBMC هامة لتحفيز الخلايا التائية قوية كما هو مبين في الشكل رقم 3 حيث نسبة 01:50 المنتجة دون المستوى الأمثل تفعيل مقارنة 01:20 S : النسبة المثلى من العاصمة R نسبة (ن = 2 المانحين). إنتاج أعداد كافية CTL مع خصوصية المستضد واسع هو شرط مسبق لالفعالية السريرية ضد جميع الفيروسات الثلاثة. ويتحقق ذلك من خلال ثقافة CTL في G - ريكس ، الذي يدعم التوسع متفوقة مقارنة مع الخلايا التائية 24 لوحات جيدة التقليدية (الشكل 4A) 15 ، في حين أن إضافة IL4 وIL7 إلى زيادات الثقافات ذخيرة والنوعية كما هو مبين في الشكل 4B حيث تردد الخلايا التائية المتفاعلة ضد A2 - HLA - CMV pp65 - مشتقة resticted قيمت NLV الببتيد في الثقافات ولدت في وجود أو غياب IL4 و / أو 16،17 IL7. لتقييم قدرة النمط الظاهري والوظيفية للخلايا وسعنا لتحليل تدفق cytometric ، جواني خلوى ELIspot تلطيخ / IFNγ ، وإطلاق سراح 51 المقايسات الكروم على المنتج النهائي لحفظ البرودة / التسريب. عادة الخلايا المولدة والنسائل المتعددة التي يبلغ عدد سكانها خليط من CD4 + و CD8 + الخلايا التائية مع خصوصية مستضد اكتشافها في كل من المقصورات الخلايا التائية. وCTL قادرون على التعبير عن قتل مستضد الفيروسية الخلايا المستهدفة ولكن ليس الفيروس السلبية جزئيا HLA الأهداف المتطابقة ، مشيرا الى انه لا ينبغي لها أن تحفز الطعم ضد المضيف المرض (GvHD) في الجسم الحي (الشكل 5).
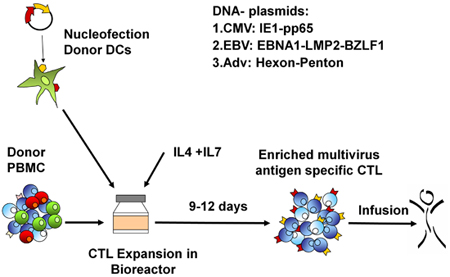
الشكل 1. rCTL بروتوكول جيل. الأولى ، هي nucleofected البلدان النامية مع البلازميدات مستضد الفيروسية ترميز ثم يخلط مع ذاتي في PBMCs على البحث : S 10 أو 20:01. يتم توسيع الخلايا في G - ركس لمدة 10-14 يوما في وجود IL4 IL7 ، ثم حصادها ، محسوبة ، واختبارها من أجل الهوية والوظيفة والعقم ، وcryopreserved ثم للاستخدام السريري.

الشكل 2. البلازميدات الحمض النووي محسن العلوي حمل تفعيل الخلايا التائية في المختبر. وكانت البلدان النامية nucleofected مع محسن وادارة الاغذية والعقاقير المتوافقة Hexon ترميز البلازميدات وبينتون (إيج) ، وIE1 pp65 (CMV) ، وEBNA1 ، LMP2 ، وBZLF1 (EBV) أو البلازميدات pShuttle التقليدية ترميز المستضدات نفسها. وقد استخدمت لتحفيز هذه الخلايا التائية والتي تم تحليل خصوصية ELIspot IFNγ 10 يوما بعد التحفيز.
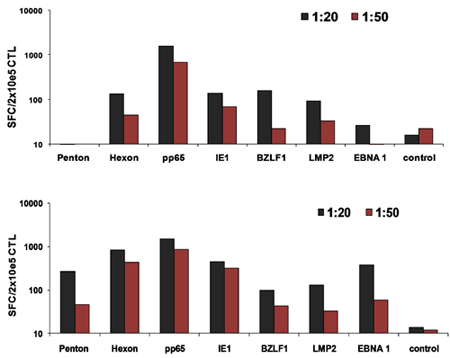
الشكل 3 العاصمة الأمثل : نسب الخلايا التائية لتفعيل CTL. وكانت البلدان النامية في الفترة من 2 nucleofected مع جميع الجهات المانحة البلازميدات three الوجه الأمثل ، واستخدمت بعد ذلك لتحفيز PBMCs ذاتي في 1:20 أو 1:50 العاصمة : نسبة PBMC. وجرى تقييم تواتر تنشيط خلايا تي في يوم 10 من ELIspot IFNγ.
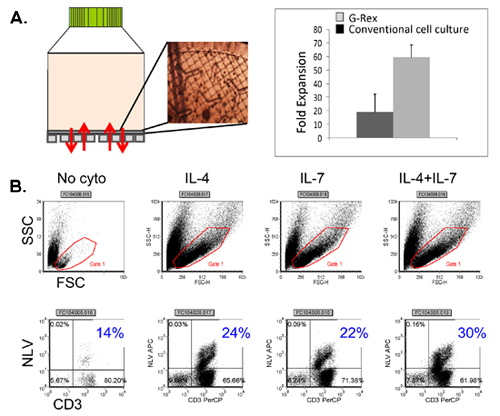
الشكل 4. T التوسع في الخلية G - ريكس باستخدام السيتوكينات تعزيز. لوحة ويظهر الجهاز G - ريكس فضلا عن ظهور CTL على الغاز نفاذية الغشاء وتقييمها من خلال الفحص المجهري. ويرد أيضا مقارنة بين الخلية التي تحققت في الانتاج وزراعة الأنسجة لوحات الاتفاقية معاملة مقابل G - ريكس. لوحة باء يبين تواتر CTL مخموس CMV الإيجابية التي تحققت في الثقافات الموسعة في حضور أي خلوى ، IL4 وحده ، وحده ، وIL7 IL4 IL7 +.
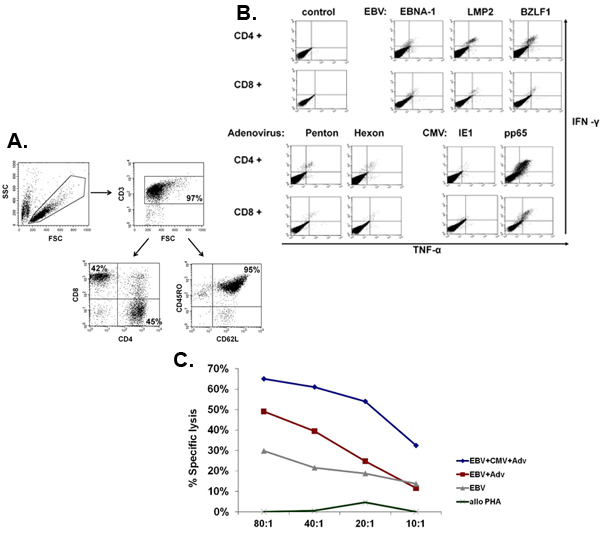
الشكل 5. النمط الظاهري ووظيفة CTL الموسعة. لوحة ويظهر المثال ممثل النمط الظاهري للCTL multivirus الموسعة ، التي النسائل المتعددة مع خليط من CD4 + (45 ٪ -- مساعد) وCD8 + (42 ٪ -- السامة للخلايا) تي الخلايا ، والتي غالبية (95 ٪) أعربوا عن ذاكرة علامة CD45RO + / CD62L +. وحة باء تبين أن هذه الخلايا هي محددة لمستضدات جميع تحفيز وpolyfunctional النحو الذي تقدره تلطيخ خلوى الخلايا للكشف عن إنتاج IFNΓ وTNFα بعد التحفيز مستضد جيم لوحة يظهر أن CTL توسيع وظيفية وفقا للقياس بواسطة مقايسة 51 ساعة معتمدة. واستخدمت LCL ذاتي ، إما وحدها أو مع transduced متجه فارغة أو متجه الفيروسة الغدانية معربا عن CMV - pp65 والقطرانيحصل. وجرى تقييم Alloreactivity باستخدام خيفي الانفجارات PHA كهدف.
Discussion
العدوى الفيروسية لحساب معدلات الاعتلال والوفيات كبيرة في المرضى الذين يعانون من ضعف المناعة بسبب المرض أو علاجه. بعد HSCT ، على سبيل المثال ، من المعروف جيدا الالتهابات التي تسببها herpesviruses الثابتة مثل وEBV CMV ، فضلا عن الفيروسات مثل فيروس الجهاز التنفسي المخلوي التنفسي (RSV) ، في حين أن أهمية الالتهابات التي تسببها أدفانسد ، BK الفيروس ، وحقوق الإنسان هربس (HHV) وقد تم مؤخرا -6 أكثر تقدير. في حين أن وكلاء الدوائية والعلاج القياسية لبعض الالتهابات ، لديهم السميات كبيرة ، وتوليد البدائل المقاومة ، وغير فعالة في كثير من الأحيان. في المقابل ، أثبتت خلايا تي فيروس محددة مستمدة من المتبرعين بالخلايا الجذعية آمنة وفعالة للوقاية والعلاج من عدوى فيروسية أو مرض في زرع الخلايا الجذعية مكون الدم (HSCT) 2،5،6،18-21 الإعداد. ومع ذلك ، هو في نهاية المطاف محدودة الأوسع تنفيذ المناعي الخلايا التائية من التعقيد والتكلفة والوقت اللازم لإنتاج CTL.
وينبغي لنا الرواية ومقاربة سريعة لتوليد multivirus CTL ، وصفت في المخطوطة الحالية ، زيادة كبيرة في جدوى العلاج بالخلايا السامة للخلايا T للأمراض الفيروسية ، وتمكين استراتيجية لتصبح في مستوى من الرعاية للمضيف المناعة. استخدام البلدان النامية وناقلات الجنود المدرعة nucleofected البلازميد يتيح العرض مستضد على كلا الصف الأول والثاني MHC دون منافسة من ناقلات فيروسية أو مولدات المضادات الفيروسية في الواقع من عدة يجري التعبير عنه داخل خلية واحدة منذ تستخدم مجموعات سكانية مختلفة DC لكل 3 البلازميد. استخدام IL - 07/04 يزيد بقاء الخلايا التائية والانتشار ، والتي تساعد في المقابل زيادة وتيرة وذخيرة من الاستجابة محددة مستضد الخلايا التائية 16،17. أخيرا ، والثقافة في G - T ركس يقلل بشكل كبير من موت الخلايا المبرمج الخلية خلال الثقافة. تبادل الغازات (O 2 في 2 من أصل وأول أكسيد الكربون) ويحدث عبر غشاء السيليكون نفاذية الغاز في قاعدة القارورة ، ومنع نقص الأكسجين ، مما يسمح لقدر أكبر من عمق متوسط فوق الخلايا ، وتوفير مزيد من المواد الغذائية وتخفيف النفايات والمنتجات. ويمكن أيضا أن يمتد هذا المنبر للفيروسات إضافية كما هو الحال عندما يتم تحديد مستضدات الواقية.
Disclosures
Acknowledgements
ويؤيد هذا العمل من خلال تقديم المساعدة لإنتاج العلاجات الخلوية (المعاهد الوطنية للصحة العقد ، NHLBI (HB - 10 - 03) HHSN26820100000C) (CMR) ، ومراكز متخصصة لعلاج خلية مقرها المنح NIH - U54 HL081007 NHLBI 1 (CMR) ، وهو ASBMT جائزة الباحث الشاب (UG وJV) ، وزميل جمعية سرطان الدم والغدد اللمفاوية الخاصة في جائزة البحوث السريرية (UG) ، والباحث العلمي جائزة ايمي Manasevit Strelzer (AML).
Materials
| Name | Company | Catalog Number | Comments |
| اسم كاشف | شركة | فهرس العدد | |
|---|---|---|---|
| CellGenix | CellGenix | 2005 | |
| IL4 | R + D نظم | 204-IL/CF | |
| IL7 | Peprotech | 200-15 | |
| Hyclone RPMI 1640 | الحرارية العلمية | SH30096.01 | |
| مصل الإنسان AB | شركة وادي الطبية الحيوية | HP1022 | |
| Nucleofector | Amaxa / Lonza | AAF - 1001B & AAF - 1001X | |
| Nucleofection كيت | Amaxa / Lonza | V4XP - 3012 | |
| البلازميدات | NTC | ن / أ | |
| GM - CSF | R & D | 215-GM/CF | |
| IL1 | R & D | 201 - LB - 025 | |
| IL6 | R & D | 206 - IL - CF | |
| TNFα | R & D | 210 - TA - 010 | |
| PGE2 | سيغما | P6532 - 1MG | |
| G - ريكس | ويلسون وولف التصنيع | AY11 - 00027 |
References
- Kaka, A. S., Foster, A. E., Weiss, H. L., Rooney, C. M., Leen, A. M. Using dendritic cell maturation and IL-12 producing capacity as markers of function: a cautionary tale. J Immunother. 31, 359-369 (2008).
- Leen, A. M., Myers, G. D., Sili, U., Huls, M. H., Weiss, H., Leung, K. S., Carrum, G., Krance, R. A., Chang, C. C., Molldrem, J. J. Monoculture-derived T lymphocytes specific for multiple viruses expand and produce clinically relevant effects in immunocompromised individuals. Nat. Med. 12, 1160-1166 (2006).
- Gerdemann, U., Christin, A. S., Vera, J. F., Ramos, C. A., Fujita, Y., Liu, H., Dilloo, D., Heslop, H. E., Brenner, M. K., Rooney, C. M., Leen, A. M. Nucleofection of DCs to generate Multivirus-specific T cells for prevention or treatment of viral infections in the immunocompromised host. Mol. Ther. 17, 1616-1625 (2009).
- Leen, A. M., Christin, A., Khalil, M., Weiss, H., Gee, A. P., Brenner, M. K., Heslop, H. E., Rooney, C. M., Bollard, C. M. Identification of hexon-specific CD4 and CD8 T-cell epitopes for vaccine and immunotherapy. J Virol. 82, 546-554 (2008).
- Leen, A. M., Christin, A., Myers, G. D., Liu, H., Cruz, C. R., Hanley, P. J., Kennedy-Nasser, A. A., Leung, K. S., Gee, A. P., Krance, R. A., Brenner, M. K., Heslop, H. E., Rooney, C. M., Bollard, C. M. Cytotoxic T lymphocyte therapy with donor T cells prevents and treats adenovirus and Epstein-Barr virus infections after haploidentical and matched unrelated stem cell transplantation. Blood. 114, 4283-4292 (2009).
- Feuchtinger, T., Matthes-Martin, S., Richard, C., Lion, T., Fuhrer, M., Hamprecht, K., Handgretinger, R., Peters, C., Schuster, F. R., Beck, R., Schumm, M., Lotfi, R., Jahn, G., Lang, P. Safe adoptive transfer of virus-specific T-cell immunity for the treatment of systemic adenovirus infection after allogeneic stem cell transplantation. Br J Haematol. 134, 64-76 (2006).
- Bunde, T., Kirchner, A., Hoffmeister, B., Habedank, D., Hetzer, R., Cherepnev, G., Proesch, S., Reinke, P., Volk, H. D., Lehmkuhl, H., Kern, F. Protection from cytomegalovirus after transplantation is correlated with immediate early 1-specific CD8 T cells. J. Exp. Med. 201, 1031-1036 (2005).
- Leen, A., Meij, P., Redchenko, I., Middeldorp, J., Bloemena, E., Rickinson, A., Blake, N. Differential immunogenicity of Epstein-Barr virus latent-cycle proteins for human CD4(+) T-helper 1 responses. J Virol. 75, 8649-8659 (2001).
- Bickham, K., Munz, C., Tsang, M. L., Larsson, M., Fonteneau, J. F., Bhardwaj, N., Steinman, R. EBNA1-specific CD4+ T cells in healthy carriers of Epstein-Barr virus are primarily Th1 in function. J. Clin. Invest. 107, 121-130 (2001).
- Straathof, K. C., Leen, A. M., Buza, E. L., Taylor, G., Huls, M. H., Heslop, H. E., Rooney, C. M., Bollard, C. M. Characterization of latent membrane protein 2 specificity in CTL lines from patients with EBV-positive nasopharyngeal carcinoma and lymphoma. J. Immunol. 175, 4137-4147 (2005).
- Hislop, A. D., Taylor, G. S., Sauce, D., Rickinson, A. B. Cellular responses to viral infection in humans: lessons from Epstein-Barr virus. Annu. Rev. Immunol. 25, 587-617 (2007).
- Steven, N. M., Annels, N. E., Kumar, A., Leese, A. M., Kurilla, M. G., Rickinson, A. B. Immediate early and early lytic cycle proteins are frequent targets of the Epstein-Barr virus-induced cytotoxic T cell response. J. Exp. Med. 185, 1605-1617 (1997).
- Luke, J., Carnes, A. E., Hodgson, C. P., Williams, J. A. Improved antibiotic-free DNA vaccine vectors utilizing a novel RNA based plasmid selection system. Vaccine. 27, 6454-6459 (2009).
- Williams, J. A., Luke, J., Johnson, L., Hodgson, C. pDNAVACCultra vector family: high throughput intracellular targeting DNA vaccine plasmids. Vaccine. 24, 4671-4676 (2006).
- Vera, J. F., Brenner, L. J., Gerdemann, U., Ngo, M. C., Sili, U., Liu, H., Wilson, J., Dotti, G., Heslop, H. E., Leen, A. M., Rooney, C. M. Accelerated production of antigen-specific T-cells for pre-clinical and clinical applications using Gas-permeable Rapid Expansion cultureware (G-Rex. Journal of Immunotherapy. , (2009).
- Vella, A. T., Dow, S., Potter, T. A., Kappler, J., Marrack, P. Cytokine-induced survival of activated T cells in vitro and in vivo. Proc. Natl. Acad. Sci. U. S. A. 95, 3810-3815 (1998).
- Vella, A., Teague, T. K., Ihle, J., Kappler, J., Marrack, P. Interleukin 4 (IL-4) or IL-7 prevents the death of resting T cells: stat6 is probably not required for the effect of IL-4. J. Exp. Med. 186, 325-330 (1997).
- Heslop, H. E., Ng, C., Li, Y. C., Smith, C., A, C., Loftin, S. K., Krance, R. A., Brenner, M. K., Rooney, C. M. Long-term restoration of immunity against Epstein-Barr virus infection by adoptive transfer of gene-modified virus-specific T lymphocytes. Nature Medicine. 2, 551-555 (1996).
- Rooney, C. M., Smith, C. A., Ng, C., Loftin, S. K., Li, C., Krance, R. A., Brenner, M. K., Heslop, H. E. Use of gene-modified virus-specific T lymphocytes to control Epstein-Barr virus-related lymphoproliferation. Lancet. 345, 9-13 (1995).
- Einsele, H., Roosnek, E., Rufer, N., Sinzger, C., Riegler, S., Loffler, J., Grigoleit, U., Moris, A., Rammensee, H. G., Kanz, L., Kleihauer, A., Frank, F., Jahn, G., Hebart, H. Infusion of cytomegalovirus (CMV)-specific T cells for the treatment of CMV infection not responding to antiviral chemotherapy. Blood. 99, 3916-3922 (2002).
- Walter, E. A., Greenberg, P. D., Gilbert, M. J., Finch, R. J., Watanabe, K. S., Thomas, E. D., Riddell, S. R. Reconstitution of cellular immunity against cytomegalovirus in recipients of allogeneic bone marrow by transfer of T-cell clones from the donor. N. Engl. J. Med. 333, 1038-1044 (1995).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved