Method Article
الجيل القادم التسلسل للكشف عن المنحى الطفرات في الأورام الصلبة والسائلة
In This Article
Summary
This manuscript describes clinical protocols for two next-generation sequencing panels. One panel interrogates hematologic malignancies while the other panel targets genes commonly mutated in solid tumors. Molecular classification of driver mutations in human malignancies offers valuable prognostic and predictive information.
Abstract
As our understanding of the driver mutations necessary for initiation and progression of cancers improves, we gain critical information on how specific molecular profiles of a tumor may predict responsiveness to therapeutic agents or provide knowledge about prognosis. At our institution a tumor genotyping program was established as part of routine clinical care, screening both hematologic and solid tumors for a wide spectrum of mutations using two next-generation sequencing (NGS) panels: a custom, 33 gene hematological malignancies panel for use with peripheral blood and bone marrow, and a commercially produced solid tumor panel for use with formalin-fixed paraffin-embedded tissue that targets 47 genes commonly mutated in cancer. Our workflow includes a pathologist review of the biopsy to ensure there is adequate amount of tumor for the assay followed by customized DNA extraction is performed on the specimen. Quality control of the specimen includes steps for quantity, quality and integrity and only after the extracted DNA passes these metrics an amplicon library is generated and sequenced. The resulting data is analyzed through an in-house bioinformatics pipeline and the variants are reviewed and interpreted for pathogenicity. Here we provide a snapshot of the utility of each panel using two clinical cases to provide insight into how a well-designed NGS workflow can contribute to optimizing clinical outcomes.
Introduction
أصبح الجيل التالي من التسلسل (خ ع) من عينات الأورام السريرية متاحة على نطاق أوسع خلال السنوات القليلة الماضية مع تزايد نقاط الأدب العلمية إلى أهمية تحديد التغيرات الجينية قابلة للاستهداف و/ الواسمات الجزيئية النذير التنبؤية. تحليلات لوحة متعددة الجينات ودراسات exome التسلسل كاملة في كل الظهارية 1،2 و 3 الدموية الخبيثة قد رسخ مفهوم التجانس الورم والتطور نسيلي كما تقدم المرض والانتكاسات. بالإضافة إلى ذلك، على عكس التكنولوجيات المتنافسة مثل تفاعل البلمرة المتسلسل (PCR) أو سانجر تسلسل، يمكن NGS الكشف عن معظم التعديلات الجينوم في جميع جينات السرطان ذات الصلة سريريا في فحص واحد (4).
مركز تشخيص شخصية انطلقت مع فريقين السريرية خ ع، مخصص الدموية لوحة (هيم-خ ع و لوحة) ولوحة السرطان لعينات FFPE (الصلبة خ ع و لوحة) وقبالة الجاهزة للاستخدام (انظر الشكل 1). وتغطي هذه الألواح المناطق الفائدة ذات الصلة سريريا أو عالية من الجينات مختارة؛ ليس كل الجينات أو الإكسونات تمت تغطيتها بالكامل. يتم إنشاؤها Amplicons بواسطة التهجين التحقيق تليها الإرشاد وربط. وتتضخم المناطق المستهدفة باستخدام مزيد من PCR مع الاشعال المزدوج فهرستها عالمية، والسماح لتصل إلى 96 العينات المراد المجمعة عن التسلسل.
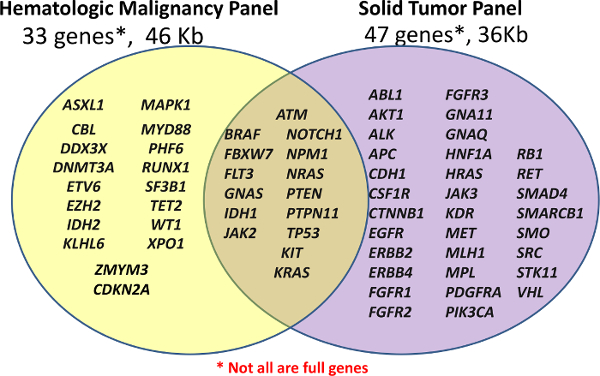
الشكل 1: قائمة من الجينات التي تمت تغطيتها في لوحات يتم تنفيذ إعداد مكتبة باستخدام إما الدموية لوحة (لوحة هيم-خ ع) من 33 الجينات أو خارج على الرف Amplicon لوحة السرطان (الصلبة خ ع) من 47 الجينات المخصصة. لا تغطيها كل من الجينات أو الإكسونات بالكامل، حيث أن بعض amplicons قد لا تغطي سوى بعض النقاط الساخنة. الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم. </ أ>
وقد استمدت محتوى لوحة هيم-خ ع من مصادر متعددة، ولكن مراكز حوالي 16 الجينات الطافرة في سرطان الدم النخاعي الحاد (AML) التي سبق وصفها كما يدل على مستوى عال من فائدة سريرية 5. يتم إنتاج-خ ع الصلبة لوحة تجاريا مع المناطق المستهدفة بناء على الجينات الطافرة عادة في السرطان كما ورد في فهرس الجسدية الطفرات في السرطان قاعدة البيانات (COSMIC) 6.
عدة خطوات أساسية تميز سير العمل الشامل لخ ع السريرية. بعد الطبيب أوامر الاختبار، ويحدد الطبيب الشرعي كفاية العينة بعد تحليل لنسبة الورم وحجم العينة. في مؤسستنا، نطلب لا يقل عن 10٪ الورم يرجع ذلك إلى معدل خلفية التسلسل خطأ ( "الضوضاء") للتكنولوجيا وكفاءة نهج المستهدفة. إذا كانت الأنسجة كافية للاختبار، يتم استخراج الحمض النووي الجيني. ثم تعرض هذا الحمض النووي لمراقبة الجودة متعددة (QC) الخطوات. اذا أقر الحمض النووي QC، يتم إنشاء مكتبة amplicon والتسلسل. ويتم تحليل البيانات الناتجة عن طريق خط أنابيب المعلوماتية الحيوية في المنزل. بعد تحليل المعلوماتية الحيوية، يتم مراجعة المتغيرات يدويا وتفسيرها لالمرضية قبل إدراجها في التقرير الطبي. أدناه وصفنا حالتين الذي ذهب من خلال هذا العمل الدقيق وفي النهاية أدت إلى تغييرات في إدارة السريرية.
حالة 1 - النخاعي الحاد سرطان الدم
وكان خزعة نخاع العظم من المريض والتشخيص لمكافحة غسل الأموال، دون النضج. وأرسلت الدراسات الوراثية الخلوية على عينة نخاع العظم وأظهرت النمط النووي الإناث العادي. كان هناك 95٪ الانفجارات تعميم الحالية، لذلك تم إرسال عينة الدم الطرفية للالاختبارات التشخيصية شخصية على لوحة هيم-خ ع.
سرطان الدم النخاعي الحاد (AML) هي خباثة دموية من سلالة الدم النخاعي من خلايا الدم البيضاء. كشفمن الطفرات الجينية في مكافحة غسل الأموال وأصبحت ذات أهمية متزايدة للتشخيص والعلاج، مع الطفرات الجينية المتكررة اعترفت بأنها مهمة في المرضية والتشخيص 7. وقد ارتبطت طفرات في NPM1 وCEBPA مع خطر النذير مواتية، في حين الازدواجية جنبا إلى جنب الداخلية (ITDS) في FLT3 ارتبطت نتيجة أقل مواتاة 8. وهناك مجموعة متزايدة من الأدلة تدعم دور الممرضة لهذه وغيرها من الطفرات في مكافحة غسل الأموال و9.
حالة 2 - الرئة غدية
أظهر خزعة من كتلة فوق الترقوة اليسرى من المريض ب غدية الرئة. تم إرسال المواد خزعة من جزءا لا يتجزأ من البارافين (FFPE) كتلة العقدة الليمفاوية الثابتة الفورمالين للاختبار الجيني (لوحة الصلبة خ ع) كما فات / تجعيد الشعر مع أكثر من 50٪ الورم، لتحديد ما إذا كانت الطفرة الحالية للتدخل العلاجي المستهدفة.
الرئة كانكونإيه هو السبب الرئيسي للوفيات المرتبطة بالسرطان في الولايات المتحدة، وينقسم إلى نوعين رئيسيين، سرطان الرئة ذو الخلايا غير الصغيرة (NSCLC) وسرطان الرئة (مؤتمر القيادة المسيحية الجنوبية). يمكن كذلك تعريف NSCLC إما غدية أو سرطان الخلايا الحرشفية، استنادا إلى الأنسجة الآفة. الرئة غدية هو نوع فرعي الأكثر شيوعا من سرطان الرئة، وينظر في كل من المدخنين وغير المدخنين، وهو الشكل الأكثر شيوعا من سرطان الرئة لغير المدخنين 10. وقد حددت الدراسات الجزيئية للسرطانات الغدد الرئة طفرة في الجينات المسرطنة متعددة 11. الطفرات السائق الأكثر شيوعا التي تم تحديدها في المدخنين هي الطفرات في KRAS وBRAF. الطفرات الأكثر شيوعا لدى غير المدخنين هي الطفرات في EGFR، وإعادة ترتيب تنطوي على الجينات ALK، RET وROS1. وقد وصفت أورام الرئة مع في الإطار اكسون 20 الإدراج في ERBB2 الجين (HER2 / NEU). الشذوذ الأكثر شيوعا في سعادةR2 / NEU هو التضخيم من هذا الموضع في سرطان الثدي الذي العلاج المستهدف هو متاح (تراستوزوماب: الأجسام المضادة وحيدة النسيلة أنسنة ضد HER2 / NEU). وHER2 / NEU اكسون 20 الإدراج الذي لوحظ في 2-4٪ من الرئة adenocarcimomas 12 أظهرت استجابة جزئية للعلاج بالاشتراك مع HER2 / NEU ومثبطات mTOR س (neratinib وtemsirolimus، على التوالي) 13.
Protocol
ويضم هذا البروتوكول الخطوات البارزة اثنين من الاختبارات المعملية المتقدمة التحقق من صحة لالتنميط الجيني من الأورام الصلبة والسائلة، على التوالي. ويتم اختبار أجريت في المختبر وفقا لمتطلبات التعديلات تحسين المختبرات الإكلينيكية (CLIA) لسنة 1988.
1. استخراج الحمض النووي من الدم المحيطي أو نخاع العظم
- تحديد مقدار الدم أو نخاع العظم لتأخذ على أساس الجدول 1.
| عينة / WBC | المبلغ الذي يتعين التعامل معها على أنها 1 مل من الدم |
| نخاع العظم | 250 ميكرولتر |
| WBC الدم 12،000 - 50،000 | 1 مل |
| WBC الدم 50،000 - 100،000 | 500 ميكرولتر |
| WBC الدم 100،000 - 200،000 | 200 ميكرولتر |
| WBC الدم> 200000 | 100 ميكرولتر |
| * للحصول على الدم WBC <12000، واتخاذ 2 مل من الدم | |
الجدول 1: الدم / نخاع العظم حجم لاستخدام الرسم البياني منذ عدد خلايا الدم البيضاء سوف تختلف من عينة لعينة، فإنه من الصعب تحديد حجم معين من الدم للاستخدام. ولذلك، فإن كمية الدم لاستخدامه في فحص يجب أن يتحدد من خلال النظر في عدد خلايا الدم البيضاء (WBC) قبل بدء الفحص. وعلى الرغم من استخدام كمية أقل من الدم، لا يزال ينبغي أن يعامل كما لو كان على 1 مل منذ حجم الدم المستخدمة يتم تخفيض لأن عدد الخلايا الحالية أكبر من المعتاد.
- اتبع بروتوكول عدة متوافرة تجاريا لعزل الحمض النووي الجيني.
2. استخراج الحمض النووي من جزءا لا يتجزأ من البارافين (FFPE) الأنسجة الثابتة الفورمالين،
- مرتكز علىمنطقة الورم دائري الطبيب الشرعي على الشريحة H & E، تصطف الشرائح غير ملوثين مع دليل H & E الشرائح وتوضح منطقة مشابهة لاستخراج. لتشريح الكلي، العملية فقط عينة واحدة / مجموعة المريض من الشرائح في وقت واحد.
- تسخين الشرائح على كتلة C الحرارة 45 درجة إلى تذوب قليلا البارافين. كشط بعناية الأنسجة داخل خطوط التي تم وضع علامة على الشريحة، وذلك باستخدام مشرط جديد لكل عينة ليكون استخراجه. وضع مأخوذة الشمع في أنبوب 1.5 مل المسمى بشكل مناسب. كن حذرا لأن الشمع كشط هو كهرباء جدا ويمكن أن تقفز من الأنبوب.
- إضافة 320 ميكرولتر من Deparaffinization الحل لكل 5-6 5 ميكرون أقسام (25 - 30 ميكرون المجموع). على سبيل المثال، إذا كان الأنبوب الذي يحتوي 3 أقسام من 10 ميكرون لفة / حليقة سوف تتم معالجتها، ثم استخدم 320 ميكرولتر، ولكن إذا تم الحصول على 5 أقسام في نفس سمك ثم استخدام 640 ميكرولتر.
- دوامة بقوة لمدة 10 ثانية على الأقل وأداء عبد القديرتدور uick في microcentrifuge لإزالة الأنسجة / الشمع من الجانبين، وسقف وفي الحل. احتضان عند 56 درجة مئوية لمدة 3 دقائق، ثم في احتضان RT لمدة 5 - 10 دقائق.
- بعد حضانة RT، إضافة 180 ميكرولتر من العازلة ATL لكل 320 ميكرولتر من Deparaffinization الحل المضافة. فرم الأنسجة عشر مرات باستخدام معقم مصغرة مدقة باستخدام مدقة جديدة لكل عينة. ضمان عدم وجود الأنسجة تمسك مدقة، لأنها يمكن أن تكون لزجة جدا. دوامة تعليق بقوة لمدة 3 ثوان، ثم الطرد المركزي في أقصى سرعة لمدة 1 دقيقة.
- إضافة 10 ميكرولتر من بروتين كاف للمرحلة واضحة أقل. المزيج بلطف pipetting صعودا وهبوطا لضمان معلق الأنسجة. لا الدوامة. احتضان عند 56 درجة مئوية خلال الليل مع اهتزاز عند 400-500 دورة في الدقيقة.
- في صباح اليوم التالي، والتحقق من حالة فسخ الأنسجة بالكامل (هذا حدث إذا كان هذا الحل انخفاض واضح). إذا كان هذا الحل أقل ليست واضحة، ثم دوامة بقوة لمدة 3 ثوان وأجهزة الطرد المركزي في أقصى سرعة FOص 1 دقيقة. إضافة اضافي 5-10 ميكرولتر من بروتين كاف واحتضان عند 56 درجة مئوية لمدة 30 إضافي - 60 دقيقة.
- احتضان عند 90 درجة مئوية لمدة 1 ساعة للمساعدة على عكس الفورمالديهايد عبر ربط. السماح للعينات لتبرد إلى درجة حرارة الغرفة ل5-10 دقائق ثم لفترة وجيزة أجهزة الطرد المركزي كل أنبوب لتعزيز السائل.
- نقل المرحلة واضحة أقل إلى المسمى أنبوب 1.5 مل. إذا كانت هناك أنابيب متعددة من نفس عينة المريض (مثل حالة إذا كان يتم استخدامها لفات متعددة)، تتحد المراحل الدنيا في أنبوب واحد في هذه المرحلة. ملاحظة: نقل كميات صغيرة من الحل Deparaffinization لا ينبغي أن تتداخل مع إجراء تنقية، ولكن هناك خطر إذا تم نقل كمية كبيرة.
- إضافة 2 ميكرولتر من ريبونوكلياز الحل. دوامة بلطف أو عكس 25 مرة ودوران سريع في microcentrifuge. في احتضان RT لمدة 5 دقائق.
- إضافة 200 ميكرولتر من البروتين الهطول الحل. إذا فعل واحد أو اثنين من لفات، استخدم 200 ميكرولتر. إذا فعل ثلاثة لفةق في آن واحد، ثم استخدم 400 ميكرولتر. دوامة بقوة على سرعة عالية لمدة 30 ثانية لمزيج متجانس مخازن تحلل. احتضان على الجليد لمدة 5 دقائق أو يمكن أن العينات البقاء على الجليد لمدة تصل إلى ساعة.
- أجهزة الطرد المركزي في 5000 x ج لمدة 5 دقائق. البروتين عجلت ينبغي أن تشكل ضيق، بيليه الأبيض. صب طاف في المسمى أنبوب 1.5 مل، ومن ثم احتضان العينات على الجليد لمدة 3 دقائق على الأقل. أجهزة الطرد المركزي في 5000 x ج لمدة 3 دقائق.
- إضافة 200 ميكرولتر من 2-بروبانول (كحولالأيسوبروبيل) لكل 180 ميكرولتر من الاحتياطي ATL أضافت في وقت سابق إلى المسمى أنبوب مل 1.5 (قد يكون من الضروري استخدام أنبوب 2 مل). على سبيل المثال، إذا به ثلاث لفات إضافة 600 ميكرولتر من الأيزوبروبانول. إضافة 1 ميكرولتر من الجليكوجين لكل 180 ميكرولتر من الاحتياطي ATL وأضاف في وقت سابق إلى الأيسوبروبانول وعكس الأنبوب عدة مرات لخلط.
- إضافة بعناية طاف من الخطوة البروتين الهطول في خليط كحولالأيسوبروبيل. مزيج الأنبوب بواسطة قلب بلطف 50 مرات على الأقل.
- أجهزة الطرد المركزي في الحد الأقصى ليرة سوريةعيد لمدة 3 دقائق. فإن الحمض النووي أن تكون واضحة كما بيليه صغيرة بيضاء في الجزء السفلي من الأنبوب.
- صب أو نضح من طاف في أنبوب النفايات المناسب. الحفاظ على أنبوب 1.5 مل النفايات منفصل لكل عينة في حالة تأتي طردت بيليه لذلك لن تضيع أو مختلطة مع النفايات من عينات أخرى. استنزاف أنبوب على منشفة ورقية والتأكد من إزالة الغالبية العظمى من كحولالأيسوبروبيل.
- إضافة 300 ميكرولتر من تقدم طازجة 70٪ من الإيثانول. عكس الأنبوب بلطف عدة مرات لغسل بيليه. محاولة لضمان بيليه يأتي فكها لضمان تنظيف أكثر شمولا.
- أجهزة الطرد المركزي في أقصى سرعة لمدة 5 دقائق. ثم إزالة بعناية الإيثانول. قد يكون بيليه فضفاضة، لذلك صب أو نضح ببطء ومشاهدة بيليه. إزالة الايثانول الزائدة من داخل الأنبوب، دون لمس بيليه. السماح للعينات للهواء الجاف ل5-15 دقائق، والحرص على عدم جفاف خلال عينة.
- إضافة ما بين 25-100 ميكرولتر من الحمض النووي الترطيب الحل إلى البريدعينة منظمة العمل ضد الجوع على أساس حجم بيليه الحمض النووي وكمية بدءا من الأنسجة. دوامة الأنابيب بقوة لفترة وجيزة تدور في microcentrifuge. احتضان لمدة 1 ساعة على 65 درجة مئوية لترطيب تماما الحمض النووي.
3. الحمض النووي الجينوم مراقبة الجودة
ملاحظة: هناك ثلاث خطوات مستقلة لمراقبة الجودة الحمض النووي (QC). انظر الجدول 2 لمزيد من التوضيح لماذا يتم تنفيذ كل خطوة مراقبة الجودة.
| صك | نتيجة | إشارة | المدى المثالي |
| DropSense96 | A260 / A230 | تحديد الملوثات الكيميائية (مثل الإيثانول) | 1،50-2،2 |
| DropSense96 | A260 / A280 | تحديد الملوثات البروتين | 1،60-2،2 |
| DropSense96 | تركيز | الكمي الحمض النووي | > 1 نانوغرام / ميكرولتر |
| TapeStation | الحمض النووي مسحة | تقرير النزاهة الحمض النووي (على سبيل المثال، وتدهور / تفتيت الحمض النووي المستخرج) | 50٪> 1000 بي بي |
| و qubit 2.0 | تركيز | أكثر دقة القياس الكمي الحمض النووي | > 1 نانوغرام / ميكرولتر |
الجدول 2: الحمض النووي QC النتائج المتوقعة تؤخذ جميع هذه القيم في الاعتبار قبل تشغيل السماح عينة للشروع في مرحلة إعداد المكتبة.
- بعد بروتوكول الشركة المصنعة، تشغيل 2 ميكرولتر من الحمض النووي المستخرج على التألق للحصول على تركيز العمل (نانوغرام / ميكرولتر) من العينة.
- تشغيل 1-2 ميكرولتر من كل عينة على الأشعة فوق البنفسجية / VIS معمل للتحقق من جودة العينة (A260 / A230 و A260 / A280 الفئراندائرة الرقابة الداخلية) وفقا لتعليمات الشركة الصانعة.
- للحصول على عينات FFPE: بعد تعليمات الشركة الصانعة، تشغيل 1 ميكرولتر من كل عينة على نظام هلام الكهربائي ميكروفلويديك لتقييم تدهور / تفتيت الحمض النووي. انظر الشكل 2 للحصول على أمثلة.
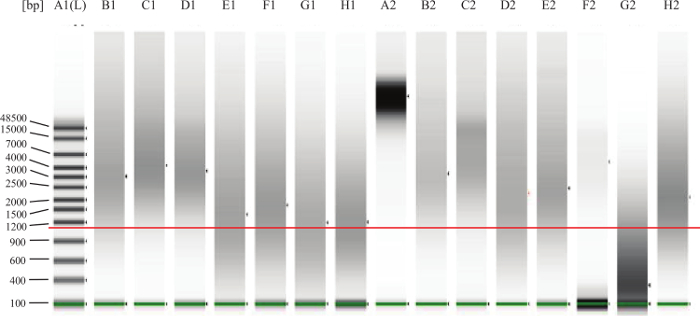
الشكل 2: الحمض النووي الجينوم مراقبة الجودة جل مثال الخط الأخضر على العصابات الدنيا هو للدلالة على علامة أقل. الخط الأحمر المضافة في هو الإشارة إلى ما يقرب من 1000 سنة مضت. يمثل حارة A2 الحمض النووي سليمة تماما، كما هو متوقع من مقاضاة تيس جديدة (على سبيل المثال، الدم المحيطي أو نخاع العظام). الممرات B1، C1، D1، B2، C2، E2 أمثلة جيدة، الحمض النووي FFPE سليمة. ويبدو أن الحمض النووي في F2 حارة أن تكون سليمة، ولكن في منخفض جدا التركيز. الحمض النووي في G2 حارة هو المتدهورة أو مجزأة، وسوف لا تعمل في الفحص. الممرات E1، F1، G1، H1، D2،H2 تمثيل الحمض النووي الذي يقع في "منطقة رمادية" وهذا يعني أن الفحص قد تعمل بشكل جيد، ولكن بعض من الحمض النووي يمكن أن تتضرر جدا أو عبر ربط، وبالتالي فإنه لن أداء جيدا في الفحص. الرجاء انقر هنا لعرض أكبر نسخة من هذا الرقم.
4. إعداد مكتبة Amplicon
- التهجين من بركة جزئية والإرشاد، من ربط Oligos منضم
- في غرفة ما قبل PCR، إضافة الحجم اللازم من انخفاض EDTA TE، 5 ميكرولتر من أنبوب جزئية الفريق (على سبيل المثال، الصلبة خ ع وحة أو هيم-خ ع و لوحة)، و100-250 نانوغرام من الحمض النووي الجيني لكل المقابلة بشكل جيد في على بعد تلتف شبه 96 جيدا لوحة المسمى باسم (HYB) لوحة التهجين.
- إضافة 40 ميكرولتر من جزئية التهجين لتسلسل الكاشف 1 (OHS1) إلى كل عينة في لوحة HYB. ماصة بلطف صعودا ونزولا لا يقل عن 5 - 6 مرات لخلط. تغيير نصائح بعد كل عمود لتجنبانتقال التلوث.
- ختم لوحة HYB مع رقائق الألومنيوم لاصقة وأجهزة الطرد المركزي في 1000 x ج لمدة 30 ثانية.
- احتضان لوحة HYB في الحاضنة التهجين ما قبل ساخنة في درجة حرارة 95 درجة مئوية لمدة 1 دقيقة. ضبط درجة حرارة الحاضنة التهجين إلى 40 درجة مئوية. مواصلة احتضان طالما أنه يأخذ الحاضنة لتقليل من 95 درجة مئوية إلى 40 درجة مئوية (~ 90 دقيقة). ملاحظة: هذا التبريد التدريجي هو أمر حاسم لالتهجين الصحيح.
- خلال آخر 15-20 دقيقة من حضانة التهجين، قبل غسل وحدة تصفية لوحة (فبو). إعداد فقط الآبار لاستخدامها في فحص الحالي، أي فقط استخدام / الآبار غير المستخدمة جديدة من لوحة مرشح فتح سابقا، ولكن أبدا إعادة استخدام الآبار التي تم استخدامها. ملاحظة: يجب أن يكون واضحا استنادا إلى عدد كيت على لوحة مرشح، وعلامات على لوحة التصفية، وتسرب استخدامها عبر لوحة.
- باستخدام ماصة متعدد القنوات، إضافة 45 ميكرولتر من الصارم غسل 1 (SW1) إلى كل بئر.
تحذير: يحتوي الفورماميد. غطاء وأجهزة الطرد المركزي في فبو في 2250 x ج لمدة 3 دقائق عند 20 درجة مئوية. التحقق من كل بئر واحدة من السوائل المتبقية (> 15 ميكرولتر / جيد). - في حالة وجود السائل المتبقي، وتناوب على درجة فبو 180 وكرر الخطوة الطرد المركزي مرة أخرى لمدة 3 دقائق إضافية. إذا يدور السائل المتبقي من خلال المرة الثانية، ثم انتقل إلى الخطوة التالية، إذا لم يكن ثم قد يكون هناك خلل في لوحة تصفية وسوف لوحة الحالية تحتاج إلى استبداله.
- باستخدام ماصة متعدد القنوات، إضافة 45 ميكرولتر من الصارم غسل 1 (SW1) إلى كل بئر.
- بمجرد أن يبرد الحاضنة التهجين إلى 40 درجة مئوية، وأجهزة الطرد المركزي لوحة في 1000 x ج لمدة لا تقل عن 30 ثانية عند 20 درجة مئوية لجمع التكثيف. نقل كامل حجم كل عينة من لوحة HYB على مركز المقابلة الآبار قبل غسلها من فبو. تغيير نصائح بعد كل عمود لتجنب انتقال التلوث. تغطية فبو وأجهزة الطرد المركزي في 2250 x ج لمدة 3 دقائق عند 20 درجة مئوية.
- إضافة 45 ميكرولتر من SW1 وأجهزة الطرد المركزي في 2250 x ج لمدة 3 دقائق عند 20 درجة مئوية. كرر ما مجموعه اثنين من يغسل. تدوير فبو 180 درجة وأجهزة الطرد المركزي مرة أخرى في 2250 x ج لمدة 3 دقائق لإزالة جميع SW1.
- راءى فبو. تجاهل كل التدفق من خلال (التي تحتوي على الفورماميد) في حاوية النفايات المناسبة. إعادة تجميع فبو باستخدام مختلف MIDI جمع النفايات لوحة. إضافة 45 ميكرولتر من الاحتياطي العالمي 1 (UB1) إلى كل بئر عينة وأجهزة الطرد المركزي في 2250 x ج لمدة 3 دقائق عند 20 درجة مئوية. تحذير: يحتوي الفورماميد.
- إضافة 45 ميكرولتر من تمديد من ربط ميكس 3 (ELM3) لكل عينة جيدا على لوحة فبو وماصة صعودا وهبوطا 3 مرات لخلط. ملاحظة: رد فعل تمديد-من ربط يحدث على غشاء فلتر لوحة.
- ختم لوحة فبو مع رقائق الألومنيوم لاصقة واحتضان الجمعية فبو بأكمله في مرحلة ما قبل ساخنة الحاضنة 37 درجة مئوية لمدة 45 دقيقة.
- الفهرسة وPCR التضخيم
- قسامة المؤشرات المستخدمة في الآبار المقابلة في المفهرسة التضخيم ررأكل (IAP) عن طريق ترتيب الاشعال في تركيبات مؤشر لوحة، وترتيبها على النحو التالي: أنابيب التمهيدي i5 و (قبعات بيضاء، والحل واضح) عموديا، تتماشى مع الصفوف من A إلى H، وأنابيب i7 من التمهيدي (قبعات برتقالية، حل الأصفر) أفقيا ، تتماشى مع الأعمدة 1 إلى 12. باستخدام P10 متعدد القنوات ماصة، إضافة 4 ميكرولتر من التمهيدي I7 (حل الصفراء) إلى كل صف من IAP وإضافة 4 ميكرولتر من التمهيدي i5 و (حل واضح) إلى كل عمود من IAP.
- على الجليد أو كتلة التبريد، وإعداد ميكس ماجستير PCR وذلك بإضافة 0.5 ميكرولتر من البلمرة DNA 1 (TDP1) إلى 25 ميكرولتر من PCR ميكس ماجستير 2 (PMM2) لكل عينة. قلب، وبسرعة دوامة، لفترة وجيزة الطرد المركزي ميكس ماجستير PCR إلى المزيج.
- إضافة 22 ميكرولتر من مزيج ماجستير PCR إلى كل بئر من الأكاديميات وماصة صعودا وهبوطا 3 مرات لخلط. تغيير نصائح بين الآبار. الحفاظ على IAP في 4 درجات مئوية.
- بعد 45 دقيقة تمديد-من ربط رد فعل (الخطوة 4.1.10)، وإزالة فبو من الحاضنة وإزالة بعناية اللهuminum احباط ختم. مع تغطية الغطاء وأجهزة الطرد المركزي في 2250 x ج لمدة 3 دقائق عند 20 درجة مئوية.
- إضافة 25 ميكرولتر من 50 ملي هيدروكسيد الصوديوم إلى كل عينة جيدا على فبو. ماصة صعودا وهبوطا 6 مرات على الأقل. ضمان نصائح ماصة تأتي في اتصال مع الغشاء. تغيير نصائح بعد كل عمود. يحضن في درجة حرارة الغرفة لمدة 5 دقائق.
- بنقل العينات مزال من فبو إلى IAP على النحو التالي:
- باستخدام P100 ماصة متعدد القنوات لتعيين 20 ميكرولتر، ماصة هيدروكسيد الصوديوم على لوحة فبو صعودا وهبوطا 6 مرات على الأقل. قليلا إمالة لوحة فبو لضمان طموح كاملة قبالة لوحة.
- نقل 20 ميكرولتر من فبو إلى العمود المقابل للIAP. ماصة بلطف صعودا وهبوطا 6 مرات على الأقل لتجمع بدقة الحمض النووي مع مزيج ماجستير PCR. ختم IAP مع الفيلم لاصقة وأجهزة الطرد المركزي في 1000 x ج لمدة 1 دقيقة عند 20 درجة مئوية.
- تقديم لوحة PCR في غرفة ما بعد PCR وتحميل لوحة الصعود إلى cycler الحرارية. تشغيل PCR صrogram تتألف من الحرارة تغيير طبيعة الخطوة في درجة حرارة 95 درجة مئوية لمدة 3 دقائق. تليها 25 دورة من 95 درجة مئوية لمدة 30 ثانية، 62 درجة مئوية لمدة 30 ثانية، 72 درجة مئوية لمدة 60 ثانية؛ متبوعا ملحق النهائي من 72 درجة مئوية لمدة 5 دقائق. مع الانتهاء من تغيير عند 10 درجة مئوية. إن لم يكن الانتقال إلى المرحلة المقبلة بعد الانتهاء من PCR، يمكن أن تبقى لوحة على cycler الحرارية بين عشية وضحاها، أو يمكن تخزينه في 2-8 درجة مئوية تصل إلى يومين.
- PCR تنقية والتطبيع الخرزة القائم على
- إزالة حبات تنقية المغناطيسية، شطف العازلة (EBT)، والكواشف هلام الكهربائي من 4 درجات مئوية الثلاجة ومكان في RT 20 دقيقة على الأقل قبل المرحلة المقبلة.
- وبمجرد أن PCR كاملة، الطرد المركزي في 1000 x ج لمدة 1 دقيقة عند 20 درجة مئوية لجمع التكثيف. نقل 1 ميكرولتر من كل رد فعل PCR لتجريد أنابيب / آبار لوحة تحتوي على 4 ميكرولتر من الماء لتخفيف العينات 1/5. ماصة صعودا وهبوطا إلى المزيج.
- إضافة 2 ميكرولتر منالمخفف عينات PCRed إلى 2 ميكرولتر من العازلة ميكروفلويديك هلام. ختم شرائط / لوحة. هزة في 1800 دورة في الدقيقة لمدة 30 ثانية على الأقل وأجهزة الطرد المركزي في 1000 x ج لمدة 30 ثانية. بعد بروتوكول الشركة المصنعة، تشغيل الخليط على هلام ميكروفلويديك لتقييم ما إذا أسفرت إعداد مكتبة مكتبة مقبولة (انظر الشكل 3).
- دوامة حبات تنقية المغناطيسية حتى أنها علقت بشكل جيد ويظهر اللون متجانس. إضافة 45 ميكرولتر من الخرز على كل عينة.
- ختم لوحة مع فيلم لاصق واضحة ويهز لوحة عند 1800 دورة في الدقيقة لمدة 2 دقيقة. يحضن في درجة حرارة الغرفة دون أن تهتز لمدة 10 دقيقة.
- وضع لوحة على موقف المغناطيسي. بمجرد مسح طاف، وإزالة بعناية وتجاهل طاف. إذا يستنشق أي الخرز عن غير قصد في نصائح، الاستغناء عن الخرز إلى لوحة وترك بقية لوحة على مغناطيس لمدة 2 دقيقة وتأكد من أن طاف وتطهيرها.
- مع لوحة على رانه موقف المغناطيسي، إضافة 200 ميكرولتر من الطازجة 80٪ من الإيثانول على كل عينة جيدا. نقل لوحة ذهابا وإيابا عدة مرات. احتضان لوحة على الوقوف المغناطيسي لمدة 30 ثانية. إزالة بعناية وتجاهل طاف. كرر ما مجموعه اثنين من يغسل.
- إزالة الايثانول الزائد عن طريق الطرد المركزي لفترة وجيزة لوحة في 1000 x ج لخفض أي الإيثانول على جانبي أنبوب، ووضع لوحة ليعيدوه الى الوقوف المغناطيسي، واستخدام ماصة P10 متعددة تعيين القناة إلى 10 ميكرولتر لإزالة الإيثانول. السماح حبات لتجف في الهواء ل5-8 دقيقة.
- باستخدام P100 ماصة متعدد القنوات، وإضافة 30 ميكرولتر من إبت إلى كل بئر. ماصة صعودا وهبوطا عدة مرات لضمان حبات تأتي قبالة الجانب من الأنبوب. ختم لوحة مع فيلم لاصق واضحة ويهز لوحة عند 1800 دورة في الدقيقة لمدة 2 دقيقة.
- يحضن في درجة حرارة الغرفة دون أن تهتز لمدة 3 دقائق. إذا كان هناك عينات التي لم يتم معلق الخرز تماما، ماصة بلطف صعودا وهبوطا ل resuspend الخرز.
- وضع لوحة على الوقوف المغناطيسي. باستخدام P100 ماصة متعدد القنوات، ونقل 20 ميكرولتر من طاف لوحة جديدة كاملة تسمى لوحة مكتبة التطبيع (الشرطة الوطنية الليبيرية). نقل المتبقية ~ 10 ميكرولتر من المكتبات تسلسل الفردية إلى لوحة منفصلة تسمى باقي تنظيفها الهاتفي مكتبة لوحة (RCLP). تخزين هذا الطبق إلى جانب الإعدادية مكتبة النهائي، كما يمكن استخدامه كاحتياطي لتشغيل التسلسل الثاني، إذا لزم الأمر. إن لم يكن الانتقال إلى المرحلة التالية، والشرطة الوطنية الليبيرية وRCLP يمكن تخزينها في -15 إلى -25 درجة مئوية.
- بقوة دوامة و resuspend مكتبة التطبيع الخرز 1 (LNB1). ومن الأهمية بمكان ل resuspend تماما بيليه LNB1 حبة في الجزء السفلي من الأنبوب. تحضير مزيج التطبيع، عن طريق خلط 8 ميكرولتر من LNB1 مع 44 ميكرولتر من مكتبة التطبيع إضافات 1 (LNA1) لكل عينة. بقوة دوامة مزيج التطبيع ل10-20 ثانية.
تنبيه: LNA1 يحتوي الفورماميد. - مع متقطعة انعكاس لالثانية vortexing لمن مزيج التطبيع، إضافة 45 ميكرولتر من كل عينة من الشرطة الوطنية الليبيرية. ختم لوحة مع فيلم لاصق واضحة ويهز لوحة عند 1800 دورة في الدقيقة لمدة 30 دقيقة. هذا 30 دقيقة الحضانة هو أمر حاسم لتطبيع مكتبة المناسب كما حضانات من أكبر أو أقل من 30 دقيقة قد تؤثر على التمثيل مكتبة وكثافة الكتلة.
- أثناء الحضانة 30 دقيقة، وإعداد الكواشف لتسلسل من قبل ذوبان خرطوشة كاشف وHYB العازلة (HT1) [تنبيه: تحتوى كل من الفورماميد]. وبالإضافة إلى ذلك، الحصول على الجليد لخطوة لاحقة، وضمان كتلة حرارة مناسبة لمدة 1.5 مل أنابيب الطرد المركزي تم تعيين إلى 96 درجة مئوية.
- عندما الخطوة خلط 30 دقيقة كاملة، ضع الشرطة الوطنية الليبيرية على الوقوف المغناطيسي. بمجرد مسح طاف، واستخدام ماصة متعدد القنوات لإزالة بعناية وتجاهل طاف في حاوية النفايات المناسبة.
- إزالة الشرطة الوطنية الليبيرية من الوقوف المغناطيسي وتغسل حبات مع مكتبة التطبيع غسل 1 (LNW1) على النحو التالي:
- إضافة 45ميكرولتر من LNW1 لكل عينة جيدا.
تحذير: يحتوي الفورماميد. ختم لوحة مع فيلم لاصق واضحة ويهز لوحة عند 1800 دورة في الدقيقة لمدة 5 دقائق. كرر ما مجموعه اثنين من يغسل. ضمان لإزالة كافة LNW1 بعد غسل الثاني.
- إضافة 45ميكرولتر من LNW1 لكل عينة جيدا.
- إزالة الشرطة الوطنية الليبيرية من الوقوف المغناطيسي، وذلك باستخدام ماصة متعدد القنوات، وإضافة 30 ميكرولتر من 0.1 N هيدروكسيد الصوديوم (أقل من أسبوع من العمر) إلى كل بئر إلى أزل العينة. ختم لوحة مع فيلم لاصق واضحة ويهز لوحة عند 1800 دورة في الدقيقة لمدة 5 دقائق.
- أثناء شطف 5 دقائق، إضافة 30 ميكرولتر من مكتبة التطبيع التخزين العازلة 1 (LNS1) إلى كل بئر لاستخدامها في لوحة جديدة تسمى لوحة التخزين (SGP).
- وضع الشرطة الوطنية الليبيرية على الوقوف المغناطيسي. بمجرد مسح طاف، ونقل شطف 30 ميكرولتر إلى LNS1 في برنامج المنح الصغيرة. تغيير نصائح بين العينات لتجنب التلوث المتبادل.
- ختم لوحة مع الفيلم لاصقة وأجهزة الطرد المركزي في 1000 x ج لمدة لا تقل عن 30 ثانية.
- إضافة 5 1؛ لتر من كل عينة لتكون متسلسلة إلى المسمى Amplicon مكتبة مجمع (PAL) أنبوب 1.5 مل. دوامة PAL لخلط وتدور باستمرار في microcentrifuge لفترة وجيزة.
- اعتمادا على ما الكيمياء التسلسل المستخدمة (V2 أو V3) إضافة 4-10 ميكرولتر من PAL الى 590-596 ميكرولتر من HT1. عموما، إضافة 5.8 ميكرولتر من PAL إلى 595 ميكرولتر من HT1 للكيمياء V2 و 8.5 ميكرولتر من PAL إلى 592 ميكرولتر من HT1 للكيمياء V3. تسمية هذا الأنبوب كما أنبوب المخفض مكتبة Amplicon (DAL).
- دوامة DAL لفترة وجيزة تدور باستمرار في microcentrifuge. احتضان DAL في 96 درجة مئوية لمدة 2 دقيقة. عكس الأنبوب DAL 3 مرات ووضع DAL على الجليد لمدة 5 دقائق على الأقل، في حين تستعد المنظم للتسلسل. بعد 5 دقائق، وDAL غير جاهزة للتحميل.
- إذا انتهت مع برنامج المنح الصغيرة، وختم لوحة مع لاصق فيلم الألومنيوم احباط وتسميته مع التاريخ ولوحة معرف. تخزين برنامج المنح الصغيرة مختومة وPAL في -15 إلى -25 درجة مئوية.
ther.within الصفحات = "1"> 
الرقم 3: مكتبة الإعدادية مراقبة الجودة جل مثال الخط الأخضر على العصابات الدنيا هو الإشارة إلى انخفاض علامة والخط الأرجواني على العصابات العليا هي للدلالة على علامة أعلى. كل شيء يعمل بشكل جيد لالممرات H1، A2، B2، C2، E2، وG2. لم الإعدادية مكتبة لا تعمل على النحو الأمثل، لالممرات D2، F2، و H2، ولكن لا يزال الحصول على النتائج التي للتو قد لا تحظى بتغطية كافية. لA3، الإعدادية مكتبة بالكاد عملت وعلى الأرجح كان هذا عينة من الحمض النووي غير كاف للمقايسة. العصابات السفلى فوق علامة أقل هي الاشعال غير المستخدمة، وذلك لأن أخذ قسامة مباشرة من PCRed جيدا. يجب أن يكون عينة المجلس الوطني الانتقالي سوى الفرقة التمهيدي غير المستخدمة، ولا شيء غير ذلك. يرجى النقر هنا لمشاهدة نسخة أكبر من هذا الرقم.
5. التسلسل
- ضمان بذلت SampleSheet.csv الصحيح لتشغيل. انظر الشكل التكميلي 1 على سبيل المثال.
- شطف وتجفيف خلية تدفق وإضافة 600 ميكرولتر من DAL إلى خرطوشة كاشف مذاب.
- إعداد المنظم لتسلسل باتباع التعليمات التي تظهر على الشاشة.
تحليل 6. البيانات
- تنفيذ خط أنابيب المعلوماتية الحيوية. الاستفادة من خط أنابيب بيوينفورمتيك في المنزل، مصمم خصيصا لتحديد الطفرات، الإدراج والحذف والتكبير 18.
- بعد اكتمال خط الأنابيب، والتحقق من ملفات السجل عن الأخطاء / تحذير، لأن أي مساعدات أخطاء / التحذيرات كبيرة في مراقبة الجودة من تجهيز خط أنابيب.
- تحليل الإحصاءات المدى (الجدول رقم 3) لضمان مكتبة التسلسل اجتاز مختبر تحديد مقاييس مراقبة الجودة (الشكل 4). استعراض كل البديل يدويا عن طريق عرض ملفات .bam في المشاهد بيانات الجينوم (على سبيل المثال، والتكاملية الجينوم السادسإبريق 16 (IGV)).
ملاحظة: فقط المتغيرات ضمن نطاق أليل الترددات التحقق من صحة وأعلى من الحد الأدنى عمق التغطية بعد تصفية جودة وذكرت (باستخدام HGVS) التسميات الجينوم جمعية التغيير الإنسان و(). للإبلاغ النهائي، تم تصنيف كل البديل exonic إلى: المسببة للأمراض، ربما الأمراض المصاحبة، البديل من أهمية مجهولة (VUS)، من المحتمل حميدة، وحميدة. ، تم الإبلاغ عن المتغيرات فوق معايير الإبلاغ عن 5٪ تردد أليل، باستثناء تلك المتغيرات حميدة تعتبر والتغيرات مرادفة.
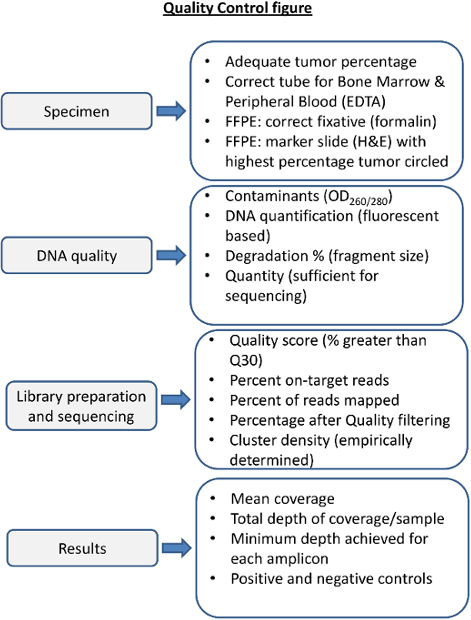
الشكل 4. نظرة عامة على خطوات ضبط الجودة لخ ع. مراقبة الجودة في كل خطوة في العملية اللازمة لضمان تسلسل سوف تسفر عن نتائج تلك المقاييس التي تتابع ما قبل وما بعد تؤخذ في الاعتبار. العلاج العينة المناسبة أمر ضروري لDNA جودة عالية. الدم ونخاع العظام في مثبتات غير مناسبة يمكن أن تسفر عن تدني نوعية الحمض النووي. تثبيت غير لائق من عينات الأورام الصلبة يمكن أن تتحلل الحمض النووي (على سبيل المثال، تثبيت في B5). ينبغي تقييم نوعية الحمض النووي للبروتين وتلوث RNA عن طريق طيفية، وتقييمها بدقة عن كمية وسلامة الحمض النووي. تحتاج إلى أن تحدد تجريبيا في المختبر التسلسل واتباعها لكل رد فعل التسلسل وكل عينة المقاييس التسلسل. قبل الإبلاغ عن نتائج التسلسل لكل عينة وينبغي تقييم للتغطية، وعمق، وأداء كافية من الضوابط الإيجابية والسلبية. الرجاء انقر هنا لعرض نسخة أكبر من هذا الرقم.
النتائج
حالة 1 - هيم-خ ع وحة
وكان الحمض النووي المستخرج من الدم المحيطي اللوكيميا ذات نوعية كافية وكمية (176 نانوغرام / ميكرولتر) لوحة هيم-خ ع. كان على عمق متوسط العام لتغطية 4،933x (أعلى من الحد الأدنى عمق متوسط تغطية 1،000x). إحصاءات المدى إضافية في الجدول 3. ومن بين المناطق 8 أدناه تغطية 250X، كانت 3 نظرا لتقليم غير لائق من الاشعال (أي لم تتم إزالة تسلسل التمهيدي بشكل صحيح بسبب أخطاء التسلسل)، كان 1 قطعة أثرية معروفة للمقايسة، و4 آخرين كانوا مناطق جزئية الإكسونات من جينات مختلفة مع عدم وجود بدائل الإبلاغ عنها. على الرغم من أن بروتوكول السريري لدينا فقط وتشمل المتغيرات التي لا يقل عن 250 يقرأ تغطيها التقارير، يقرأ يتم استيراد كافة البيانات مع لا يقل عن 100 في قاعدة البيانات للمراجعة.
معالجة البيانات ومدمج خط أنابيب المعلوماتية الحيوية الكشف عن ثلاثة، والطفرات الأمراض المرتبطة الإبلاغ عنها. طفرة مغلطة في FLT3، طفرة مغلطة في IDH2، وطفرة انزياح الإطار في NPM1. ووصف المتغيرات exonic مع الترددات أليل في الجدول 4. تحور المشتركة في FLT3 هي FLT3 -الداخلية جنبا إلى جنب الازدواجية (إدارة تقنية المعلومات) التي لا يتم استدعاء تلقائيا عن طريق خط أنابيب لدينا، ويتطلب الفحص البصري من اكسون 14. البصرية التفتيش من اكسون 14 من FLT3 لم تظهر أي الإدراج أو الازدواجية في العينة المقدمة. كان FLT3 I836del بنسبة 1٪ تردد أليل ولم تدرج في التقرير النهائي لأنها انخفضت إلى أقل من الحد الأدنى للتردد أليل التحقق من 5٪. هذه الطفرة ليست على نفس الجزيء DNA كما تغير FLT3 D835Y (أي التي لوحظت في المنطقة amplicon نفسها، ولكن ليس في "رابطة الدول المستقلة" في أي من التسلسل قراءة) ولوحظ إلا عن طريق المراجعة اليدوية من فاي .bamليه عند التحقق التغيير p.D835Y. الترددات أليل أقل من الطفرات FLT3 اثنين تشير هذه الطفرات قد تمثل التجانس و / أو تطور نسيلي. ومع ذلك، يمكن أن يكون راجعا إلى أداء الفحص لذلك amplicon أو تعدد الأشكال النووية المنفردة (SNP) قرب أو تداخل تسلسل التمهيدي التي أثرت على التضخيم من هذا الأليل الفرق.
نتائج لوحة هيم-خ ع عن حالة 1 مع مكافحة غسل الأموال وتحديد الطفرات في FLT3، IDH2، وNPM1، لوحظ ثلاثة جينات تحور عادة في مكافحة غسل الأموال. الطفرات في FLT3 في ~ 25٪ من المرضى البالغين مع مكافحة غسل الأموال (قاعدة بيانات COSMIC 17) وإما الازدواجية جنبا إلى جنب الداخلي (ITDS) أو الطفرات مغلطة في المجال التيروزين كيناز. و-ITDS FLT3 هي الطفرة أكثر شيوعا وترتبط مع ضعف الاستجابة للعلاج الكيميائي القياسي، في حين أن أهمية النذير من FLT3 كيناز دالطفرات نقطة omain، كما رأينا في هذا المريض لمكافحة غسل الأموال، له تأثير واضح على تشخيص 14. الإيزوسيترات نازعة 2 (NADP +)، الميتوكوندريا (IDH2) هو الجين الذي يشفر والتعديل الجيني الذي تحور عادة في مكافحة غسل الأموال. طفرات في معدلات جينية شائعة نسبيا في مكافحة غسل الأموال، مع الطفرات في IDH1 وDNMT3A تمثل طفرات أخرى في هذا النوع من الجينات التي تؤدي إلى التقلبات الجينات. الطفرات في جين nucleophosmin (NPM1) هي واحدة من الطفرات المكتسبة الأكثر شيوعا في مكافحة غسل الأموال وتعتبر عموما أن يكون عاملا النذير جيد (في حالة عدم وجود FLT3 - إدارة تقنية المعلومات).
وقد وصفت المشارك الطفرات من NPM1 وIDH2 في الأدب كمؤشر النذير مواتية 5، مع البقاء على قيد الحياة من 89٪ لمدة 3 سنوات. وهذا يمثل فائدة البقاء على قيد الحياة كبيرة بالمقارنة مع البقاء على قيد الحياة لمدة 3 سنوات منالنوع البري NPM1 وIDH2 من 31٪. على سبيل المثال، يتضمن المعايير من ممارسة الرعاية تحليل طفرة لالآلية الوقائية الوطنية 1 والطفرات FLT3-إدارة تقنية المعلومات. في هذا السيناريو، فإن الكشف عن مجرد طفرة NPM1 تفشل في بشكل مناسب المريض تطبق للخطر، كما هو الطفرات الثانوية يمكن أن تكون مواتية (على سبيل المثال، IDH2) أو غير مواتية (على سبيل المثال، TET2)، والحد من الثقة لتخفيف عملية زرع نخاع العظام.
حالة 2 - الصلبة خ ع وحة
كان الحمض النووي المستخرج من الأنسجة FFPE ذات نوعية كافية وكمية من أجل الصلبة خ ع الفريق، مع تركيز من 252 نانوغرام / ميكرولتر و 4٪ فقط من الحمض النووي أدناه 1000 أزواج قاعدة (بي بي). بعد تحليل البيانات وعمق متوسط تغطية 9167 يقرأ (أعلى بكثير من الحد الأدنى لدينا عمق قطع من 1000 قراءة) مع عدم وجود مناطق أقل من 250 عمق القراءة. مقاييس مراقبة الجودة إضافية هي SHOسفل في الجدول 3.
الكشف عن البيانات التي تمت معالجتها من خلال خط أنابيب المعلوماتية الحيوية اثنين من الطفرات المرتبطة المرض: الإدراج في الإطار في اكسون 20 من ERBB2 (HER2 / NEU) وطفرة مغلطة في TP53. يتم تمثيل كافة المتغيرات exonic مع الترددات أليل في الجدول 5. والإدراج في ERBB2 يمثل في الواقع تسلسل جنبا إلى جنب تكرار (HER2 / NEU)، على النحو المبين في التسميات. تحديد وتأكيد المراجعة اليدوية في الإطار الإدراج المطلوب من التسلسل يقرأ من خلال IGV. الكشف عن ترددات تحور أكثر من 50٪، كما رأينا لكل من TP53 وHER2 / الطفرات NEU هو موح من فقدان تغاير (لوه) الحدث (انظر المناقشة).
و-خ ع الصلبة نتائج الفريق لحالة 2 مع الطفرات السرطان الرئوي الكشف عن طن ERBB2 (HER2 / NEU) وTP53، اثنين من الجينات لم تختبر عادة لكجزء من الرعاية القياسية من الحالية لمرضى سرطان الرئة. HER2 / NEU يشفر مستقبلات التيروزين كيناز مماثل لجين آخر تحور شيوعا في سرطان الرئة، EGFR . تفعيل HER2 / NEU اكسون يتم رصد 20 المدرجة في 2-4٪ من سرطانات الغدد الرئة، وتمثل غالبية HER2 الطفرات / NEU لوحظ في سرطان الرئة، وعادة ما تصيب الأورام دون طفرات في الجينات سائق أخرى مثل EGFR وALK 12 . هناك عدة أسطر من إمكانات الأدلة التي تظهر لخيارات العلاج المختلفة للمرضى الذين يعانون تفعيل الإدراج HER2 / NEU، بما في ذلك استجابة جزئية للعلاج بالاشتراك مع HER2 / NEU ومثبطات mTOR س 13 و مكافحة الأمراض الهامة مع الأجسام المضادة وحيدة النسيلة تراستوزوماب بالتزامن مع العلاج الكيميائي (15). اكتشاف تغيير TP53 ليس غير متحدmmon في السرطان، ولكن في هذا الوقت لا توجد علاجات للتنفيذ.
| حالة 1 | حالة 2 | |
| يقرأ مجموع ابتداء | 2215926 | 2129110 |
| النسبة المئوية من يقرأ الخرائط | 98.42٪ | 98.29٪ |
| النسبة المئوية لليقرأ على الهدف | 99.01٪ | 97.29٪ |
| النسبة المئوية لليقرأ على الهدف بعد تصفية | 97.60٪ | 95.45٪ |
| نسبة يمكن استخدامها يقرأ | 94.87٪ | 91.79٪ |
| النسبة المئوية للقواعد فوق التغطية 250X | 98.40٪ | 100٪ |
| النسبة المئوية للقواعد وتغطية بوف 1000X | 95.90٪ | 99.70٪ |
| تغطية أدناه 250X - Amplicon عدد | 8 | 0 |
الجدول 3: تسلسل تشغيل QC القياسات هذا هو ملخص للإحصاءات المدى أهم، وليس بما في ذلك تغطية المتوسط، التي تستخدم للمراجعة البيانات لتحديد ما إذا كان نموذج مكتبة الإعدادية قد مرت مراقبة الجودة. العملية كلها ناجحة إذا كانت كل النسب فوق 90٪، ولكن من الممكن مع جزء من SW1 أو UB1 في خطوة فبو غسل أو التمهيدي عبر الحديث، أن يكون أقل "النسبي على الهدف" في حدود 80 - 90٪. إذا كانت "النسبة المعينة" منخفضة جدا، التي من شأنها أن تشير إلى وجود تلوث البكتيريا أو الحمض النووي الأخرى، حيث أن جميع العينات يجب محاذاة إلى الإنسان. عند أي من هذه المواصفات هي أقل من 80٪، وترفع علم العينة لمزيد من المراجعة للمساعدة في تحديد كيفية عroceed وتحسين العملية.
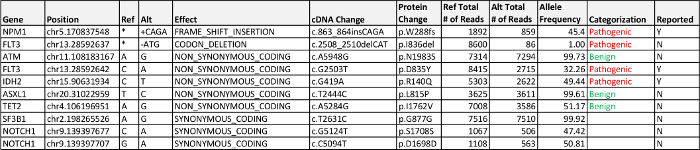
الجدول 4: حالة 1 نتائج الكشف عن العدوى والأمراض المرتبطة بها، البديل من أهمية مجهولة (VUS)، والمتغيرات exonic المرجح حميدة فوق معايير الإبلاغ مدرجة تردد أليل 5٪ يرجى النقر هنا لتحميل هذا الجدول.
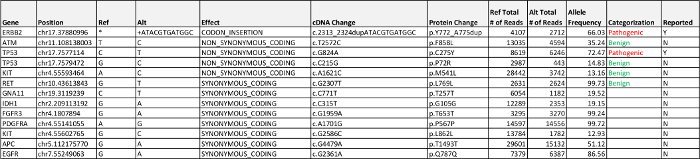
الجدول 5: حالة 2 نتائج الكشف عن العدوى والأمراض المرتبطة بها، البديل من أهمية مجهولة (VUS)، والمتغيرات exonic المرجح حميدة فوق معايير الإبلاغ عن 5٪ تردد أليل مدرجة الرجاء انقر هنا لتحميل هذا الجدول.
التكميلي الشكل 1: مثال SampleSheet.csv القائم على amplicon. هذه الورقة ينقل إلى المنظم ما الكيمياء لتشغيل (في هذه الحالة Amplicon)، ما العمل (على سبيل المثال، GenerateFastq)، ما التطبيق والفحص (على سبيل المثال، FastqOnly)، وعدد القواعد (أو قراءة) إلى تسلسل (في هذه الحالة 186 شركة بريتيش بتروليوم س 186 بي بي)، وأخيرا ما ترتبط العينات مع بعض الفهارس (في هذه الحالة الفهرسة المزدوجة). الأجزاء التي باللون الأصفر يمكن أن تتغير إلى ما يريد المجرب، ولكن في هذه الحالة يستخدم المختبر هذه المعايير. الرجاء النقر هنا لتحميل هذا الرقم.
Discussion
كما وتقدم الاثنان خ ع الاختبارات وصفها في هذه المخطوطة سريريا، والاعتبار العملي الأكثر أهمية هو مراقبة الجودة. على وجه التحديد، يجب أن تدفع النظر عن كثب إلى نوعية وكمية من الحمض النووي المستخرج. وهذا أمر مهم خاصة بالنسبة للعينات FFPE التي غالبا ما تكون متدهورة للغاية مع العائد DNA متغير. وقد تم تطوير طريقة الأيسوبروبانول هطول الأمطار من أجل تعظيم العائد من الحمض النووي من عينات FFPE كما تم العثور على أساليب تعتمد على عامود لتؤدي أحيانا إلى تقطيع الحمض النووي مع وحدات التخزين شطف محدودة. لذلك، أكثر من مرة عندما ينتج عينة تركيز منخفض جدا أو هي المتدهورة جدا للمقايسة، فمن الأرجح نظرا لحجم الأنسجة، نوع، أو تثبيت وليس عملية الاستخراج. لعينات الدم / نخاع العظام، وإذا كان هناك فشل الاستخراج، فإنه عادة ما يكون نتيجة لعينة يجري hemodilute (أي عدم وجود عدد كاف من الدم أو ورم الخلايا البيضاء في أن التعادل) أو العلاج الكيماوي ذاب.
. الإقليم الشمالي "> وأثناء عملية التحقق، ينبغي إنشاء انقطاع لقبول نوعية الحمض النووي وكمية المدخلات الموصى بها من 100 - كثيرا ما يستخدم 250 نانوغرام في الفحص، ولكن إذا كانت نوعية الحمض النووي هو جيد، ثم أقل كميات المدخلات يمكن أن تكون ناجحة. وبالإضافة إلى ذلك، إذا كانت نوعية الحمض النووي الفقراء (أي كمية من الحمض النووي amplifiable أقل من 100-250 نانوغرام) ثم ارتفاع كميات المدخلات يمكن أن يحسن من نوعية النتائج التسلسل (لأن كمية من الحمض النووي amplifiable ستصل إلى مدخلات موصى به) ويجب أن تطبق مقاييس للجودة الحمض النووي وكمية كل عينة قبل المضي قدما في الحمض النووي في إعداد مكتبة. هذه العينات في "المنطقة الرمادية" (انظر الشكل 2) يجب أن تدار وفقا لتقدير مدير المختبر أو من ينوب عنه في الوقت الحالي أفضل طريقة للتنبؤ إذا فإن الحمض النووي لا أداء جيدا خلال التسلسل هو إجراء فحص على أساس QPCR التي تسمح لتقدير وتقييم نوعية من الحمض النووي الإدخال. ويتناول هذا النهج bioavailability من شظايا مختلفة الحجم في العينة، من خلال التضخيم من شظايا مختلفة الحجم (على سبيل المثال، 100 نقطة أساس و 150 نقطة أساس و 200 نقطة أساس و 300 نقطة أساس) ومقارنة العائد.حاليا، إعداد مكتبة ينطوي على عدد كبير من الخطوات اليدوية حيث خطوة خاطئة في واحدة من العديد من المراحل يمكن أن تتسبب في مكتبة إما تفشل أو أن تكون ذات نوعية رديئة. تحليل هلام ميكروفلويديك هو QC الخطوة الوحيدة للتحقق من قضية مكتبة الإعدادية قبل التسلسل. وفقا لذلك، هناك العديد من الخطوات الحاسمة حيث الذهن إضافية يمكن أن تزيد من احتمال رد فعل ناجح. لا بد من ضمان يتم استخدام العينة الصحيحة وتجمع النوكليوتيد لكل عينة. ضمان وتسجيل صحيح أن كل عينة على واحد من 96 مجموعات فريدة من ثنائي فهرستها أزواج التمهيدي PCR يقلل فرصة لعينة خلط. أيضا، من المهم للتأكد من لوحة تصفية (فبو) تستنزف بشكل صحيح؛ إذا كان لا تستنزف بشكل مناسب يمكن أن يسبب هذا يكستيخطوة nsion-ربط إعداد مكتبة لأداء في الحالات النادرة ويؤدي إلى نوعية البيانات التسلسل الفقيرة. بعد مراقبة الجودة مكتبة، فمن الأهمية بمكان لضمان أن تكون حبات LNB1 ومعلق بالكامل وأن الحل LNB1 / LNA1 مختلطة جيدا قبل إضافتها إلى العينات كما يتم استخدام تركيز من هذا الخليط لتحديد المولية للمكتبة. وأخيرا، إذا كانت الخطوة حبة شطف يؤدي إلى كمية الأمثل للمكتبة يبلغ حجمه من الخرز فإنه سيتم خفض كثافة التكتل وربما تتسبب في مكتبة لعدم الحصول على ما يكفي تغطية متوسط. على العكس من ذلك، فإن وجود فائض من مكتبة يؤدي إلى يقرأ أقل جودة. وبالتالي، فمن المهم أن تكون متسقة في خطوة تطبيع القائم على حبة لضمان تجميع الأمثل وتجميع المكتبات على المنظم.
بالإضافة إلى إعداد مكتبة، فمن الأهمية بمكان للتحقق من خط أنابيب المعلوماتية الحيوية التي من شأنها أن تنتج المكالمات طفرة دقيقة من الخام، وملفات دي المضاعفة fastq. اختيارقد تكون الحلول مخصصة تستغرق وقتا طويلا كما أن هناك العديد من المصادر المفتوحة والمتاحة تجاريا aligners، المتصلين البديل، وحزم البرمجيات خ ع أن المرء لابد للتدقيق من خلال. سوف تحتاج خوارزميات مخصصة لتكون مصممة لاستخراج إحصائيات الأداء الأساسية، وتحديد الطفرات المتكررة الفريدة التي استعصت أدوات المصدر الأكثر انفتاحا، وتحديد وضع عدد النسخ على كل من مواضع. أثناء عملية التحقق من خط أنابيب المعلوماتية الحيوية، فمن المهم تحديد انقطاع الإبلاغ عنها للمتغيرات التي تلبي أو تتجاوز كلا عمق الحد الأدنى من التغطية بعد تصفية جودة (على سبيل المثال، ما لا يقل عن 250 يقرأ) وتردد الحد الأدنى أليل (على سبيل المثال، 4 ٪). منذ هذا الفحص على أساس amplicon المضاعفة، فمن المهم تحديد الحد الأدنى يعني عمق التغطية (على سبيل المثال، 1،000x) أن المكتبة تحتاج إلى تحقيق لتكون قادرة على الحصول على أدنى amplicon أداء الحد الأدنى لعمق يقرأ. وبالإضافة إلى ذلك، فإن طبيعة المضاعفة للمقايسة يفعل جause من آثار الهدف وهذه "التحف" سوف تحتاج إلى من يكتشفها وفحصها بالكامل قبل الاطلاق. آخر القيد المهم الفحص وصفها هو الحاجة إلى عينات لاحتواء أكبر من 10٪ ورم من أجل تحقيق الحد الأدنى لتردد أليل التحقق من صحتها.
الكشف عن التردد المنخفض، 1٪، الإدراج FLT3 أدلة على أن المراجعة اليدوية لا يزال مرغوبا فيه في هذه العملية. حتى مع تردد أليل قطع من 5٪، وبعض الطفرات مهمة ربما غاب وسوف بالتالي المراجعة اليدوية ستكون ضرورية للتأكد من هذه المتغيرات. لFLT3-ITDS، يتم إجراء الفحص البصري من اكسون 14 لجميع المرضى مكافحة غسل الأموال لضمان مستوى منخفض أو كبيرة الإدراج / الازدواجية لا تذهب دون أن يلاحظها أحد. وبالإضافة إلى ذلك، HER2 اكسون 20 الملاحق التي هي عادة بجانب تسلسل التمهيدي، تحتاج تدخل يدوي. وعلى الرغم من وجود خط أنابيب المعلوماتية الحيوية القوية، وبعض المتغيرات يمكن أن تذهب التغاضي الذي هو مجرد طبيعة وجود قطع الصلبإيقاف لمعظم الإحصاءات المذكورة أعلاه. وستكون هناك حاجة المعلوماتية الحيوية أفضل للمساعدة في تخفيف هذه المسألة، وكذلك مكتبة أفضل إعداد و / أو التسلسل المنهجيات، لأنه أكثر فائدة الحصول على بيانات ذات نوعية جيدة في انقطاع حتى أقل التي تحتوي على عدد أقل من القطع الأثرية وايجابيات كاذبة.
كشف وتفسير الترددات أليل يمكن أن يكون صعبا نظرا لصعوبة في الورم تحديد نسبة والتحيز التضخيم من بعض مناطق الجينوم. وبالإضافة إلى ذلك، الترددات أليل أكثر من 50٪ منه يمكن أن يتم الكشف عن، كما لوحظ في حالة 2. وهو ما يفسر على أنه فقدان تغاير (لوه) الحدث، إما بسبب فقدان أليل العادي، مما يؤدي إلى زيادة واضحة في متحولة يقرأ، ل كسب أليل متحولة (على سبيل المثال، 2 متحولة ونسخة عادية) أو غيرها من الآليات. هذه الآليات يمكن توضيحها من خلال الاستفادة من مجموعة التهجين الجينومي المقارن (aCGH 19) و / أو مجموعة التنميط الجيني SNP. 20.
المنهجيات تخصيب الهدف الحالية تعتمد على إجراءات لمدة يوم كامل إما التقاط هجين غير فعالة أو تقنيات PCR المضاعفة التي تؤدي إلى الحاجة إلى المزيد من التغطية تسلسل عينة واحدة وأكثر من التسلسل المستهدف يقرأ. سوف تطبيقات إضافية لخ ع الأورام الجزيئي المتوقع في المستقبل القريب تشمل أسهل طرق إعداد المكتبة التي يمكن أن تكون automatable بالكامل وتكون قادرة على معالجة العينات مع كميات قليلة جدا من الحمض النووي المدخلات (أي أقل من 1 نانوغرام) وكذلك العينات مع تدهورت للغاية الحمض النووي. ولمواجهة هذه التحديات، فإن معظم وسائل المفترض أن يكون PCR يعتمد، إما أن يكون نهج PCR متعددة الخطوات أو نهج PCR singleplex نطاق واسع مواز. وبالإضافة إلى ذلك، وقد تبين المتوازية الجزيئية من amplicons الفردية إلى الحد بشكل كبير من الضوضاء الخلفية التسلسل وسوف تتيح اختبار العينات مع نسب أقل من الخلايا السرطانية لتحقيق خفض ترددات الأليل والتحرك نحو التقاط circulatجي الخلايا السرطانية.
وقد تم الكشف عن الطفرات الأمراض المرتبطة في عينات سرطان معيار الرعاية على مدى عقود. تاريخيا، كانت في كثير من الأحيان اختبار الجينات بالتتابع، جين واحد / اكسون في وقت واحد، مع تحديد طفرة تؤدي إلى نهاية تسلسل الاختبار. وقد سمح ظهور خ ع لنهج أقل انحيازا لتسلسل الجينات المتعددة المرتبطة مع العديد من أنواع السرطان في موازاة ذلك يؤدي إلى تحديد الطفرات المتعددة التي ترتبط مع الأورام. الأداة المساعدة السريرية للخ ع للكشف عن الطفرات الجسدية في السرطان هو واضح على نحو متزايد. في الواقع، التحليل القائم خ ع لعينات الورم يمثل نموذجا جديدا يتحدى التقليدية، اختبار جين واحد، ولكن فائدة سريرية واضحة جدا. المختبرات الطبية اليوم لديها فرصة مثيرة للزواج التحقق من صحة الأسلوب الدقيق واختبار التفسير مع تطبيق هذه التكنولوجيا القوية.
Disclosures
الكتاب ليس لديهم ما يكشف.
Acknowledgements
فإن الكتاب أن نعترف المساعدة دانيال البرية لقراءة المخطوط والمساعدة في الإنتاج.
Materials
| Name | Company | Catalog Number | Comments |
| Genomic DNA ScreenTape | Agilent Technology | 5067-5365 | |
| Genomic DNA Reagents | Agilent Technology | 5067-5366 | |
| High Sensitivity D1000 ScreenTape | Agilent Technology | 5067-5584 | |
| High Sensitivity D1000 Reagents | Agilent Technology | 5067-5585 | |
| TapeStation 2200 | Agilent Technology | G2965A | |
| TapeStation Analysis Software | Agilent Technology | A.01.04 or higher | |
| 96-well Tube Storage Racks | Any Vendor | ||
| 15/50 ml Tube Rack | Any Vendor | ||
| 96-well Plate Rack | Any Vendor | ||
| Pipette, single-channel, 0.5–2.5 μl | Any Vendor | ||
| Pipette, single-channel, 1–10 μl | Any Vendor | ||
| Pipette, single-channel, 2–20 μl | Any Vendor | ||
| Pipette, single-channel, 10–100 μl | Any Vendor | ||
| Pipette, single-channel, 20–200 μl | Any Vendor | ||
| Pipette, single-channel, 100–1,000 μl | Any Vendor | ||
| Serological Pipettor | Any Vendor | ||
| Vortexer | Any Vendor | ||
| Ice bucket | Any Vendor | ||
| Microcentrifuge (for tubes and strip tubes) | Any Vendor | ||
| Freezer, -20 °C | Any Vendor | ||
| 4 °C Refrigerator | Any Vendor | ||
| Water or Bead Bath | Any Vendor | ||
| Incubator (37 °C) | Any Vendor | ||
| Serological Pipettes, 1 ml | Any Vendor | ||
| Serological Pipettes, 5 ml | Any Vendor | ||
| Serological Pipettes, 10 ml | Any Vendor | ||
| Serological Pipettes, 25 ml | Any Vendor | ||
| Gloves | Any Vendor | ||
| Razor Blades/Scaples | Any Vendor | ||
| KimWipes | Any Vendor | ||
| 15 ml Conical Tube | Any Vendor | ||
| 50 ml Conical Tube | Any Vendor | ||
| Paper Towels | Any Vendor | ||
| 200 proof Ethanol | Any Vendor | Store in Flammable Cabinet | |
| 2-Propanol (Isopropanol) | Any Vendor | Store in Flammable Cabinet | |
| 25 ml Reservoirs | Any Vendor | ||
| 10 N NaOH | Any Vendor | ||
| Pipette, 8-channel, 1 – 10 μl | Any Vendor | ||
| Pipette, 8-channel, 10 – 100 μl | Any Vendor | ||
| Pipette, 8-channel, 20 – 300 μl | Any Vendor | ||
| Ice Bucket | Any Vendor | ||
| Water Squirt Bottle | Any Vendor | ||
| Alcohol Squirt Bottle | Any Vendor | ||
| Lens Cleaning Paper | Any Vendor | ||
| Plates, 96-well PCR, Semi-Skirted | Any Vendor | ||
| Tube strips, 8-well, 0.2 ml | Any Vendor | ||
| Agencourt AMPure XP Beads | Beckman Coulter | A63881 | |
| BioShake IQ or 3000-T elm | Bulldog Bio/Q.Instruments | 1808-0506/ 1808-0517 | |
| DropPlate96 S - LabChipDS | Caliper | 128876 | |
| DropPlate96 D - LabChipDS | Caliper | 132848 | |
| DropSense96 | Caliper (Trinean) | ||
| DropQuant Software | Caliper (Trinean) | ||
| Plate Sealing Film | Denville | B1212-5S | |
| Aluminum Seal Foil | Denville | B1212-6S | |
| Nuclease-Free, Pure Water System | EMD Millipore | ||
| 5424 centrifuge | Eppendorf | 22621408 | |
| 5804R centrifuge | Eppendorf | 22623508 | Both 15 ml tube and plate rotators, preferably a centrifuge that can go up to 2,500 x g. |
| Safe-Lock Tube 1.5 ml, Natural | Eppendorf | 22431021 | |
| 5 ml Tube, DNA LoBind Tube | Eppendorf | 30108310 | |
| 5430R Centrifuge | Eppendorf | 022620645 | Any plate rotator centrifuge will work |
| Hybex Microsample Incubator | Fisher Scientific | 1057-30-0 | |
| Hybex 0.2 ml Tube Block | Fisher Scientific | 1057-31-0 | |
| TruSeq Amplicon – Cancer Panel | Illumina | FC-130-1008 | 96 reactions |
| TruSeq Custom Amplicon | Illumina | PE-940-1011 | 96 reactions |
| TruSeq Custom Amplicon Index Kit | Illumina | FC-130-1003 | 96 Indices, 384 Samples |
| MiSeq Reagent Kit v3, 500 Cycles | Illumina | MS-102-3003 | |
| MiSeq Reagent Kit v2, 300 Cycles | Illumina | MS-102-2002 | |
| MiSeq Reagent Kit v2, 500 Cycles | Illumina | MS-102-2003 | |
| Experiment Manager | Illumina | 1.3 or higher | |
| MiSeq Reporter | Illumina | 2.0 or higher | |
| Sequencing Analysis Viewer | Illumina | 1.8 or higher | |
| TruSeq Index Plate Fixture and Collar Kit | Illumina | FC-130-1007 | |
| MiSeq v2 | Illumina | SY-410-1003 | |
| TruSeq Custom Amplicon Filter Plate | Illumina | FC-130-1006 | |
| Index Adapter Replacement Caps | Illumina | 11294657 | |
| Qubit 2.0 | Invitrogen | Q32866 | |
| Qubit 0.5 ml Tubes | Invitrogen | Q32856 | |
| Qubit dsDNA Broad Range Assay Kit | Invitrogen | Q32853 | |
| DynaMa6-96 Magnetic Stand, Side Skirted | Invitrogen | 120.27 | |
| GeneAmp PCR System 9700 (gold/silver block) | Life Technologies | N8050200 | |
| Gentra Puregene Blood Kit | Qiagen | 158489 | |
| Deparaffinization Solution (16 ml) | Qiagen | 19093 | |
| Buffer ATL (4 x 50ml) | Qiagen | 939011 | |
| Protein Precipitation Solution (50 ml) | Qiagen | 158910 | |
| DNA Hydration Solution (100 ml) | Qiagen | 158914 | |
| Glycogen Solution (500 μl) | Qiagen | 158930 | |
| Qiagen Proteinase K | Qiagen | 19133 | |
| Rnase (5 ml) | Qiagen | 158924 | |
| Nuclease-Free Water (10 x 50 ml) | Qiagen | 129114 | |
| Pestles | USA Scientific | 1415-5390 | |
| TipOne RPT 10 µl elongated filter pipet tips in sterilized racks, 10 racks of 96 tips (960 tips). | USA Scientific | 1180-3810 | |
| TipOne RPT 100 µl natural, beveled filter pipet tips in sterilized racks, 10 racks of 96 tips (960 tips) | USA Scientific | 1180-1840 | |
| TipOne RPT 200 μl natural, beveled filter pipet tips in racks, sterilized racks, 10 racks of 96 tips (960 tips) | USA Scientific | 1180-8810 | |
| TipOne RPT 20 μl natural, beveled filter pipet tips in racks, sterilized racks, 10 racks of 96 tips (960 tips) | USA Scientific | 1180-1810 | |
| TipOne RPT 1,000 μl natural, graduated XL filter pipet tips in | USA Scientific | 1182-1830 |
References
- Gerlinger, M., et al. Intratumor heterogeneity and branched evolution revealed by multiregion sequencing. N Engl J Med. 366 (10), 883-892 (2012).
- Campbell, P. J., et al. The patterns and dynamics of genomic instability in metastatic pancreatic cancer. Nature. 467 (7319), 1109-1113 (2010).
- Ding, L., et al. Clonal evolution in relapsed acute myeloid leukaemia revealed by whole-genome sequencing. Nature. 481 (7382), 506-509 (2012).
- Frampton, G. M., et al. Development and validation of a clinical cancer genomic profiling test based on massively parallel DNA sequencing. Nature Biotechnol. 31 (11), 1023-1031 (2013).
- Patel, J. P., et al. Prognostic relevance of integrated genetic profiling in acute myeloid leukemia. N Engl J Med. 366 (12), 1079-1089 (2012).
- Forbes, S. A., et al. COSMIC (the Catalogue of Somatic Mutations in Cancer ): a resource to investigate acquired mutations in human cancer. Nucleic Acids Res. 38 (Database Issue), 652-657 (2010).
- Shih, A. H., Abdel-wahab, O., Patel, J. P., Levine, R. L. The role of mutations in epigenetic regulators in myeloid malignancies. Nat Rev Cancer. 12 (9), 599-612 (2012).
- Liersch, R., Müller-Tidow, C., Berdel, W. E., Krug, U. Prognostic factors for acute myeloid leukaemia in adults - biological significance and clinical use. Br J Haematol. 165 (1), 17-38 (2014).
- Bacher, U., Schnittger, S., Haferlach, T. Molecular genetics in acute myeloid leukemia. Curr Opin Oncol. 22 (6), 646-655 (2010).
- Subramanian, J., Govindan, R. Lung cancer in "Never-smokers": a unique entity. Oncology (Williston Park). 24 (1), 29-35 (2010).
- Sakashita, S., Sakashita, M., Tsao, M. S. Genes and pathology of non-small cell lung carcinoma. Semin Oncol. 41 (1), 28-39 (2014).
- Arcila, M. E., Chaft, J. E., Nafa, K. Prevalence clinicopathologic associations, and molecular spectrum of ERBB2 (HER2) tyrosine kinase mutations in lung adenocarcinomas. Clin Cancer Res. 18 (18), (2012).
- Gandhi, L., et al. Phase I study of neratinib in combination with temsirolimus in patients with human epidermal growth factor receptor 2-dependent and other solid tumors. J Clin Oncol. 32 (2), 68-75 (2014).
- Sheikhha, M. H., Awan, A., Tobal, K., Liu Yin, J. A. Prognostic significance of FLT3 ITD and D835 mutations in AML patients. Hematol J. 4 (1), 41-46 (2003).
- Mazières, J., et al. Lung cancer that harbors an HER2 mutation epidemiologic characteristics and therapeutic perspectives. J Clin Oncol. 31 (16), 1-8 (2014).
- Robinson, J. T., et al. Integrative Genomics Viewer. Nat Biotechnol. 29 (1), 495-500 (2011).
- Forbes, S. A., et al. COSMIC: exploring the world's knowledge of somatic mutations in human cancer. Nucleic Acids Res. 43 (Database issue), D805-D811 (2014).
- Daber, R., Sukhadia, S., Morrissette, J. J. Understanding the limitations of next generation sequencing informatics, an approach to clinical pipeline validation using artificial data sets. Cancer Genetics. 206 (12), 441-448 (2013).
- Haraksingh, R. R., et al. Genome-Wide Mapping of Copy Number Variation in Humans: Comparative Analysis of High Resolution Array Platforms. PLoS ONE. 6 (11), e27859(2011).
- de Leeuw, N., et al. SNP Array Analysis in Constitutional and Cancer Genome Diagnostics - Copy Number Variants, Genotyping and Quality Control. Cytogenet Genome Res. 135 (3-4), 212-221 (2011).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved