A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
توليف استرات عبر أكثر اخضرارا الأسترة ستيجليتش في الاسيتو الانيتريل
In This Article
Summary
واستخدمت فعل الأسترة ستيجليتش معدلة لتجميع مكتبة صغيرة من مشتقات إستر مع الكحول الأولية والثانوية. المنهجية يستخدم الاسيتو الانيتريل المذيبات، غير المهلجنة وخضرة، ويمكن عزل المنتج في غلة عالية دون الحاجة لتنقية الكروماتوغرافي.
Abstract
الأسترة ستيجليتش تستخدم على نطاق واسع رد فعل للتوليف من استرات من الأحماض الكربوكسيلية والكحول. في حين تتسم بالكفاءة وخفيفة، هو رد فعل يقوم عادة باستخدام الكلور أو نظم أميد المذيبات، التي تشكل خطرا على صحة الإنسان والبيئة. ويستخدم منهجيتنا الاسيتو الانيتريل كأكثر خضرة وأقل نظام المذيبات الخطرة. هذا البروتوكول يسلك معدلات والغلة التي يمكن مقارنتها بالنظم التقليدية للمذيبات وتوظف استخراج وتسلسل الغسيل الذي يلغي الحاجة لتنقية المنتج إستر عبر الفصل اللوني للعمود. يمكن استخدام هذا الأسلوب العام الزوجين مجموعة متنوعة من الأحماض الكربوكسيلية مع 1° وكحول الاليفاتيه 2°، وكحول بينزيليك والليليتش والفينولات الحصول على استرات نقية في الغلات العالية. وهدف البروتوكول بالتفصيل هنا هو توفير بديل أكثر خضرة إلى تفاعل الأسترة مشتركة، التي يمكن أن تكون مفيدة لتوليف إستر في التطبيقات الأكاديمية والصناعية على حد سواء.
Introduction
وتستخدم مركبات إستر على نطاق واسع للتطبيقات مثل مركبات النكهة والمستحضرات الصيدلانية ومستحضرات التجميل والمواد. عادة، يتم استخدام كاربودييميدي اقتران الكواشف تسهيل تكوين إستر من حمض الكربوكسيلية وعلى الكحول1. على سبيل المثال، في الأسترة ستيجليتش، ديسيكلوهيكسيلكاربودييميدي (DCC) هو رد فعل مع حمض الكربوكسيلية حضور 4-ديميثيلامينوبيريديني (دماب) تشكل مشتقات حمض المنشط، عموما في نظام المذيبات مكلورة أو dimethylformamide (DMF)2،،من34. ثم يخضع مشتق حمض المنشط استبدال اشيل تفاعلات مع الكحول لتشكيل المنتج إستر، والذي هو عادة تنقيته عن طريق الفصل اللوني. الأسترة ستيجليتش يمكن اقتران معتدل من الأحماض الكربوكسيلية الكبيرة والمعقدة، والكحول، بما في ذلك ستيريكالي أعاق الكحول الثانوي والعالي2،،من56. والهدف من هذا العمل لتعديل البروتوكول الأسترة ستيجليتش القياسية لتوفير خيار اصطناعية أكثر اخضرارا لتفاعل الأسترة المشترك هذا.
أحد الجوانب الهامة في تصميم منهجية الاصطناعية الجديدة السعي للتقليل من استخدام وتشكيل المواد الخطرة. "المبادئ الإثني عشر للكيمياء الخضراء"7 يمكن استخدامها لتوفير مبادئ توجيهية لإنشاء تجميعات أكثر أماناً. بعض هذه تشمل منع توليد النفايات (المبدأ 1) واستخدام المذيبات أكثر أماناً (المبدأ 5). على وجه الخصوص، تمثل المذيبات 80-90% الكتلة غير المائية للمواد في الصناعة الصيدلانية8. وهكذا، تعديل بروتوكول لاستخدام مذيب أقل خطورة يمكن جعل أثر كبير على الخضرة من فعل العضوية.
تفاعلات الأسترة ستيجليتش غالباً ما تستخدم نظم المذيبات المكلورة اللامائى أو DMF؛ ومع ذلك، يتم هذه المذيبات للقلق لكل من البيئة وصحة الإنسان. الميثان (CH2Cl2) وكلوروفورم (تشكل3) مسرطنين محتملين للإنسان، وقد DMF السمية الإنجابية الشواغل9. وبالإضافة إلى ذلك، يتم الفصل2Cl2 10المستنفدة لﻷوزون. وهكذا، سيكون مذيب أقل خطورة الأسترة ستيجليتش من فائدة كبيرة. بينما هناك لا الخضراء بعد الاستبدال للمذيبات القطبية أبروتيك، ينصح الاسيتو الانيتريل كبديل أكثر اخضرارا للفصل2Cl2وشكل3DMF9. الاسيتو الانيتريل حاليا ينتج كمنتج ثانوي في صناعة أكريلونيتريل؛ ومع ذلك، توليفة خضراء من الاسيتو الانيتريل من الكتلة الأحيائية على نطاق أكاديمية قد أبلغ عنها11، والخيارات المحتملة لإعادة الاستخدام والاسترداد من مجاري النفايات السائلة التي يجري التحقيق فيها12. سابقا استخدمت الاسيتو الانيتريل كبديل أكثر اخضرارا المذيبات لاقتران ردود الفعل في توليف المرحلة الصلبة الببتيد كاربودييميدي لتشكيل روابط أميد13. استخدام الاسيتو الانيتريل كنظام المذيبات استيريفيكاتيونس ستيجليتش قد أظهر14،،من1516،17،،من1819، ،من 2021؛ بيد أن هذه الأساليب لم تركز على الجانب الأخضر من المذيب وتوظف أيضا تنقية إضافية عن طريق الفصل اللوني للعمود.
تقليل الحاجة إلى عمود الفصل اللوني كخطوة تنقية أيضا يقلل من خطرة نفايات المذيبات/8. بالإضافة إلى استخدام مادة مذيبة رد فعل أقل خطورة، تمكن المنهجية عزلة منتج نقي جداً دون الحاجة للفصل اللوني. يتم استبدال الكاشف اقتران المستخدمة تقليديا ديسيكلوهيكسيلكاربودييميدي (DCC) مع 1-إيثيل-3-(3-ديميثيلامينوبروبيل) هيدروكلوريد كاربودييميدي (EDC). تمكن المجموعة الوظيفية الأساسية أمين على هذا الكاشف تركات رد فعل أي والكواشف المتبقية المراد إزالتها عن طريق خطوات الغسيل الحمضي والأساسية.
يمكن استخدام البروتوكول المعروضة هنا مع مجموعة متنوعة من الشركاء الحامض والكحول (الشكل 1). فكان يستخدم لتجميع مكتبة صغيرة من مشتقات إستر سيناميل استخدام الابتدائي والثانوي، ونزيل، واليل الكحول والفينول22. بالإضافة إلى ذلك، معدل تفاعل الأسترة في الاسيتو الانيتريل مماثلة للتي في الكلور ونظم المذيبات DMF، دون حاجة إلى الجاف أو التقطير في الاسيتو الانيتريل قبل رد فعل22. استرات توليفها من الكحول العالي لم تكن معزولة، وهو حاليا تحديد منهجية مقارنة الأسترة ستيجليتش التقليدية في المكلورة المذيبات23. وباﻹضافة إلى ذلك، حمض مجا مجموعات أخرى يمكن أن تتأثر خطوات الغسيل الحمضي، يحتمل أن تكون مما استلزم كروماتوغرافيا العمود لتنقية بعد إزالة الاسيتو الانيتريل. وعلى الرغم من هذه القيود، رد فعل طريقة سهلة وعامة تخليق استرات في الغلات العالية باستخدام مجموعة من المكونات الكحول وحمض الكربوكسيلية. استخدام نظام المذيب أكثر اخضرارا ودرجة نقاء عالية دون الحاجة إلى اتخاذ خطوات اللوني جعل هذا البروتوكول بديلاً جذاباً الأسترة ستيجليتش تقليدية.
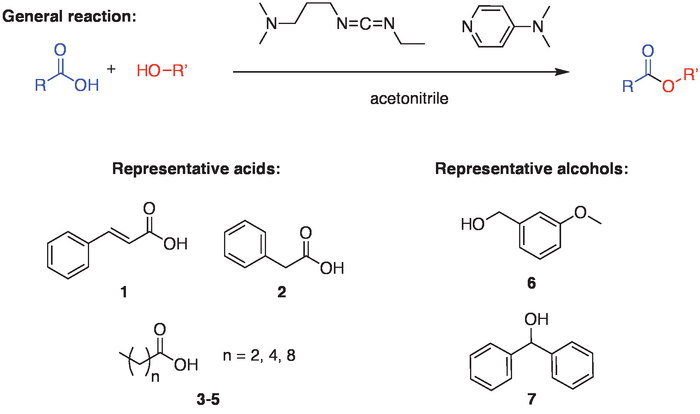
رقم 1. نظام رد الفعل العام. المخطط العام لرد فعل ينطوي على اقتران حمض الكربوكسيلية والكحول، التي تيسر استخدام كاشف اقتران كاربودييميدي (1-إيثيل-3-هيدروكلوريد كاربودييميدي (3-ديميثيلامينوبروبيل)، أو تنمية الصادرات) و (4-ديميثيلامينوبيريديني دماب) في الاسيتو الانيتريل. وللتدليل على اتساع نطاق رد الفعل، شكلت استرات استخدام الأحماض المختلفة (1-5) مع الابتدائية (6) أو الكحول الثانوية (7). الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-
Protocol
تنبيه: راجع "صحائف بيانات السلامة" (الديمقراطيين) قبل استخدام المواد الكيميائية في هذا الإجراء. نظارات الاستخدام المناسب معدات الوقاية الشخصية (معدات الوقاية الشخصية) بما في ذلك البداية، معطف مختبر، والنتريل أو قفازات بوتيل كالعديد من الكواشف والمواد المذيبة أكالة أو القابلة للاشتعال. القيام بجميع ردود الفعل في غطاء دخان. من غير الضروري للأواني الجافة أو استخدام جو من نيتروجين لهذا البروتوكول.
1-كاربودييميدي اقتران رد فعل للكحول الأولية
- في 50 مل جولة أسفل قارورة، الجمع بين (E)-حمض السيناميك (مغ 151، ملمول 1.02، يعادل 1.2)، دماب (312 مجم، 2.55 ملمول، يعادل 3)، وتنمية الصادرات (244 ملغ، 1.28 ملمول، يعادل 1.5). إضافة الاسيتو الانيتريل (15 مل) والكحول 3-ميثوكسيبينزيل (ميكروليتر 98، 0.85 ملمول، يعادل 1) إلى الخليط جنبا إلى جنب مع شريط إثارة.
تنبيه: الاسيتو الانيتريل من المذيبات القابلة للاشتعال. - المشبك قارورة في حمام مائي 40 درجة مئوية وآثاره رد فعل.
ملاحظة: إذا كان رد فعل ينطوي على الكحول عطرية، رصد رد فعل لفقدان الكحول عبر طبقة رقيقة اللوني (TLC) استخدام وخلات الإيثيل/الهكسين 1:3. اكتمال رد فعل عند بقعة الكحول لم يعد مرئياً على صفيحة TLC تشعيع مع مصباح الأشعة فوق البنفسجية.
2-استخراج Workup
- بمجرد اكتمال رد فعل كما هو مبين من TLC أو بعد 45 دقيقة، إزالة الاسيتو الانيتريل تحت ضغط انخفاض استخدام مبخر دوراني للحصول على النفط خام صلبة.
ملاحظة: يرجى الاطلاع على موارد إضافية للمعلومات بشأن الاستخدام مبخر دوراني24،25. - للمخلفات، إضافة الاثير ثنائي إثيل (20 مل) و 1 M HCl (20 مل). دوامة قارورة لإذابة هذه البقايا إلى الطبقات الموسرة.
تنبيه: إثيل الاثير مادة مذيبة الاشتعال.
ملاحظة: لتقليل الخطر المذيبات، وخلات الإيثيل يمكن استخدامها بدلاً من الاثير ثنائي إثيل؛ ومع ذلك، هناك إمكانية أكبر لتشكيل مستحلب خلال خطوات الاستخراج، والمياه والصرف الصحي. - من أجل الحل في قمع سيباراتوري. شطف قارورة يتبدد مع إضافية إثيل الاثير (5 مل) وإضافة الشطف للقمع سيباراتوري.
- بلطف يهز القمع سيباراتوري لاستخراج المنتج في طبقة الاثير، التنفيس بشكل دوري. السماح للطبقات لفصل، ثم قم بإزالة الطبقة المائية بتجفيف من أسفل القمع في قارورة Erlenmeyer أو الكأس.
ملاحظة: يرجى الاطلاع على موارد إضافية للمعلومات المتعلقة بعمليات الاستخراج واستخدام القمع سيباراتوري24،25.
3-الغسيل الداخلي
- الطبقة العضوية المتبقية في القمع سيباراتوري، أضف 1 M HCl (20 مل) وهزه بلطف قارورة سيباراتوري، التنفيس بشكل دوري. السماح للطبقات لفصل، ثم قم بإزالة الطبقة المائية بتجفيف من أسفل القمع في قارورة Erlenmeyer أو الكأس.
- كرر الإجراء الغسيل بمحلول بيكربونات الصوديوم المشبعة (2 × 20 مل)، ومن ثم بمحلول كلوريد الصوديوم المشبعة (20 مل).
- صب الطبقة العضوية من الجزء العلوي من القمع سيباراتوري إلى قارورة Erlenmeyer نظيفة، الجاف للطبقة مع سلفات المغنيزيوم، والجاذبية تصفية الحل عن طريق تصفية الورق في قارورة تبخر حشدت.
ملاحظة: الرجاء مراجعة موارد إضافية للحصول على معلومات بشأن عمليات الاستخراج واستخدام سلفات المغنيزيوم عامل تجفيف24،25. - إزالة المذيب إثيل الاثير تحت ضغط انخفاض استخدام مبخر دوراني.
- تحليل عينة من المنتج 1ح وأطياف "الرنين المغناطيسي النووي ج" 13في كدكل3 والطيف الكتلي.
ملاحظة: يرجى الاطلاع على موارد إضافية للمعلومات المتعلقة بإعداد العينات للرنين المغناطيسي النووي التحليل24،25.
4-كاربودييميدي اقتران رد فعل للكحول الثانوي وتفتقر إلى إلكترون
- في 50 مل جولة أسفل قارورة، الجمع بين (E)-حمض السيناميك (مغ 151، ملمول 1.02، يعادل 1.2)، دماب (312 مجم، 2.55 ملمول، يعادل 3)، وتنمية الصادرات (244 ملغ، 1.28 ملمول، يعادل 1.5). إضافة الاسيتو الانيتريل (15 مل) وديفينيلميثانول (مغ 157، 0.85 ملمول، يعادل 1) إلى الخليط جنبا إلى جنب مع شريط إثارة.
تنبيه: الاسيتو الانيتريل من المذيبات القابلة للاشتعال. - المشبك قارورة وآثاره رد فعل في درجة حرارة الغرفة ل 24 h. إدراج مكثف هواء في عنق قارورة للتقليل من تبخر المذيبات.
- اتبع workup الاستخراج والغسيل الداخلي هو موضح في الخطوات من 2-3 أعلاه.
5-كاربودييميدي اقتران رد فعل لسلسلة طويلة أو الأحماض الكربوكسيلية مسعور
- في 50 مل جولة أسفل قارورة، الجمع بين حمض ديكانويك (146 مغ، 0.85 ملمول، يعادل 1)، دماب (312 مجم، 2.55 ملمول، يعادل 3)، وتنمية الصادرات (244 ملغ، 1.28 ملمول، يعادل 1.5). إضافة الاسيتو الانيتريل (15 مل) وديفينيلميثانول (مغ 157، 0.85 ملمول، يعادل 1) إلى الخليط جنبا إلى جنب مع شريط إثارة.
تنبيه: الاسيتو الانيتريل من المذيبات القابلة للاشتعال. - المشبك قارورة وآثاره رد فعل في درجة حرارة الغرفة ل 24 h. إدراج مكثف هواء في عنق قارورة للتقليل من تبخر المذيبات. إذا تم استخدام الكحول الأولية إثارة رد فعل في حمام مائي عند 40 درجة مئوية ح 1.
- اتبع workup الاستخراج والغسيل الداخلي هو موضح في الخطوات من 2-3 أعلاه.
النتائج
استخدام الأسترة ستيجليتش معدلة في الاسيتو الانيتريل متبوعاً استخراج حمض-قاعدة workup، سينامات 3-ميثوكسيبينزيل (8) تم الحصول على زيت الضوء الأصفر (مغ 205، الغلة 90%) دون الحاجة للفصل اللوني للعمود. 1 أطياف الرنين المغناطيسي النووي ج ح و 13ترد في الش...
Discussion
ووضعت في المنهجية المقدمة هنا لتقليل المخاطر من المذيبات المقترنة الأسترة ستيجليتش تقليدية باستخدام نظام مذيب أكثر اخضرارا وتقليل الحاجة إلى عمود الفصل اللوني8،9. يمكن تحقيق غلة رد فعل مماثل ومعدلات باستخدام الاسيتو الانيتريل بدلاً من المذيبات المكلورة ا...
Disclosures
الكتاب ليس لها علاقة بالكشف عن.
Acknowledgements
كان يدعمها هذا البحث كلية سيينا والمركز للبحوث الجامعية والنشاط الإبداعي. ونحن نشكر الدكتور توماس هيوز والدكتور كولونكو واسطة كريستوفر لمحادثات مفيدة، السيدة الليسيا باربيرا لمرحلة مبكرة والعمل على هذه المنهجية، والأجهزة المتقدمة ستيوارت كلية سيينا والتكنولوجيا (سانت) مركز لموارد الأجهزة.
Materials
| Name | Company | Catalog Number | Comments |
| trans -cinnamic acid | Acros Organics | 158571000 | |
| butyric acid | Sigma-Aldrich | B103500 | Caution: corrosive |
| hexanoic acid | Sigma-Aldrich | 153745-100G | Caution: corrosive |
| decanoic acid | Sigma-Aldrich | 21409-5G | Caution: corrosive |
| phenylacetic acid | Sigma-Aldrich | P16621-5G | |
| 3-methoxybenzyl alcohol | Sigma-Aldrich | M11006-25G | |
| diphenylmethanol | Acros Organics | 105391000 | Benzhydrol |
| chloroform-d | Acros Organics | 166260250 | 99.8% with 1% v/v tetramethylsilane, Caution: toxic |
| hexane | BDH Chemicals | BDH1129-4LP | Caution: flammable |
| ethyl acetate | Sigma-Aldrich | 650528 | Caution: flammable |
| diethyl ether | Fisher Scientific | E138-500 | Caution: flammable |
| acetonitrile | Fisher Scientific | A21-1 | ACS Certified, >99.5%, Caution: flammable |
| 4-dimethylaminopyridine | Acros Organics | 148270250 | Caution: toxic |
| magnesium sulfate | Fisher Scientific | M65-3 | |
| hydrochloric acid, 1 M | Fisher Scientific | S848-4 | Caution: corrosive |
| sodium chloride | BDH Chemicals | BDH8014 | |
| sodium bicarbonate | Fisher Scientific | S25533B | |
| 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide hydrochloride | Chem-Impex | 00050 | Caution: skin and eye irritant |
| thin layer chromatography plates | EMD Millipore | 1055540001 | aluminum backed sheets |
| Note: All commercially available reagents and solvents were used as received without further purification. |
References
- Williams, A., Ibrahim, I. T. Carbodiimide chemistry: recent advances. Chemical Reviews. 81 (6), 589-636 (1981).
- Höfle, G., Steglich, W., Vorbrüggen, H. 4-Dialkylaminopyridines as Highly Active Acylation Catalysts. [New synthetic method (25)]. Angewandte Chemie International Edition in English. 17 (8), 569-583 (1978).
- Neises, B., Steglich, W. Simple Method for the Esterification of Carboxylic Acids. Angewandte Chemie International Edition in English. 17 (7), 522-524 (1978).
- Tsvetkova, B., Tencheva, J., Peikov, P. Esterification of 7-theophyllineacetic acid with diethylene glycol monomethyl ether. Acta pharmaceutica. 56 (2), 251-257 (2006).
- Tsakos, M., Schaffert, E. S., Clement, L. L., Villadsen, N. L., Poulsen, T. B. Ester coupling reactions - an enduring challenge in the chemical synthesis of bioactive natural products. Natural Product Reports. 32 (4), (2015).
- Morales-Serna, J., et al. Using Benzotriazole Esters as a Strategy in the Esterification of Tertiary Alcohols. Synthesis. 2010 (24), 4261-4267 (2010).
- Anastas, P., Eghbali, N. Green Chemistry: Principles and Practice. Chemical Society Reviews. 39 (1), 301-312 (2010).
- Constable, D. J. C., Jimenez-Gonzalez, C., Henderson, R. K. Perspective on solvent use in the pharmaceutical industry. Organic Process Research and Development. 11 (1), 133-137 (2007).
- Byrne, F. P., et al. Tools and techniques for solvent selection: green solvent selection guides. Sustainable Chemical Processes. 4 (1), 7 (2016).
- Hossaini, R., Chipperfield, M. P., Montzka, S. A., Rap, A., Dhomse, S., Feng, W. Efficiency of short-lived halogens at influencing climate through depletion of stratospheric ozone. Nature Geoscience. 8 (3), (2015).
- Corker, E. C., Mentzel, U. V., Mielby, J., Riisager, A., Fehrmann, R. An alternative pathway for production of acetonitrile: ruthenium catalysed aerobic dehydrogenation of ethylamine. Green Chemistry. 15 (4), 928-933 (2013).
- McConvey, I. F., Woods, D., Lewis, M., Gan, Q., Nancarrow, P. The Importance of Acetonitrile in the Pharmaceutical Industry and Opportunities for its Recovery from Waste. Organic Process Research & Development. 16 (4), 612-624 (2012).
- Jad, Y. E., et al. Peptide synthesis beyond DMF: THF and ACN as excellent and friendlier alternatives. Organic & Biomolecular Chemistry. 13 (8), 2393-2398 (2015).
- Williams, J., et al. Quantitative method for the profiling of the endocannabinoid metabolome by LC-atmospheric pressure chemical ionization-MS. Analytical Chemistry. 79 (15), 5582-5593 (2007).
- Benmansour, F., et al. Discovery of novel dengue virus NS5 methyltransferase non-nucleoside inhibitors by fragment-based drug design. European Journal of Medicinal Chemistry. 125, 865-880 (2017).
- Maier, W., Corrie, J. E. T., Papageorgiou, G., Laube, B., Grewer, C. Comparative analysis of inhibitory effects of caged ligands for the NMDA receptor. Journal of Neuroscience Methods. 142 (1), 1-9 (2005).
- Schwartz, E., et al. Water soluble azido polyisocyanopeptides as functional β-sheet mimics. Journal of Polymer Science Part A: Polymer Chemistry. 47 (16), 4150-4164 (2009).
- Hangauer, M. J., Bertozzi, C. R. A FRET-Based Fluorogenic Phosphine for Live-Cell Imaging with the Staudinger Ligation. Angewandte Chemie International Edition. 47 (13), 2394-2397 (2008).
- Hsieh, P. -. W., Chen, W. -. Y., Aljuffali, I., Chen, C. -. C., Fang, J. -. Y. Co-Drug Strategy for Promoting Skin Targeting and Minimizing the Transdermal Diffusion of Hydroquinone and Tranexamic Acid. Current Medicinal Chemistry. 20 (32), 4080-4092 (2013).
- Moretto, A., et al. A Rigid Helical Peptide Axle for a [2]Rotaxane Molecular Machine. Angewandte Chemie International Edition. 48 (47), 8986-8989 (2009).
- Hanessian, S., McNaughton-Smith, G. A versatile synthesis of a β-turn peptidomimetic scaffold: An approach towards a designed model antagonist of the tachykinin NK-2 receptor. Bioorganic & Medicinal Chemistry Letters. 6 (13), 1567-1572 (1996).
- Lutjen, A. B., Quirk, M. A., Barbera, A. M., Kolonko, E. M. Synthesis of (E)-cinnamyl ester derivatives via a greener Steglich esterification (In Press). Bioorganic & Medicinal Chemistry. , (2018).
- Wang, Z. Steglich Esterification. Comprehensive Organic Name Reactions and Reagents. , (2010).
- Padias, A. B. . Making the Connections: A How-To Guide for Organic Chemistry Lab Techniques. , (2011).
- Zubrick, J. W. . The Organic Chem Lab Survival Manual: A Student's Guide to Techniques. , (2015).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved