需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
乙腈绿色 Steglich 酯化合成酯的研究
摘要
采用改良的 Steglich 酯化反应, 合成了一个小的酯类衍生物与初级和二醇。该方法使用非卤化和更环保的溶剂, 乙腈, 并使产品在高产量的隔离, 而无需色谱纯化。
摘要
Steglich 酯化是一种广泛使用的反应, 用于合成羧酸和醇类酯。虽然效率和温和, 反应通常使用氯化或酰胺溶剂系统, 这是危险的人类健康和环境。我们的方法采用乙腈作为绿色和低危险的溶剂体系。该协议展示了与传统溶剂系统相媲美的速率和产量, 并采用了萃取和洗涤序列, 无需通过柱层析纯化酯类产品。这种通用方法可用于将各种羧酸与1°和2°脂肪醇、苄基和烯丙基醇、酚类结合, 以获得高产量的纯酯。这里详细介绍的协议的目标是提供一个更绿色的替代通用酯化反应, 这可能有助于酯合成在学术和工业应用。
引言
酯类化合物广泛用于香精化合物、药品、化妆品和材料等应用领域。通常, 使用氢化物偶联试剂用于促进酯的形成从羧酸和酒精1。例如, 在 Steglich 酯化中, 碳 (DCC) 在存在 4-dimethylaminopyridine (DMAP) 时与羧酸反应, 形成活性酸衍生物, 通常在氯化溶剂体系中或二甲基甲酰胺 (DMF)2,3,4。激活后的酸衍生物, 然后经历一个亲核酰取代与酒精形成酯产品, 通常通过色谱纯化。Steglich 酯化可实现大型、复杂羧酸和醇的温和耦合, 包括空间位阻阻碍的二次和第三醇2、5、6。这项工作的目标是修改标准的 Steglich 酯化协议, 为这种常见的酯化反应提供更绿色的合成选项。
新合成方法设计的一个重要方面是力求尽量减少有害物质的使用和形成。十二绿色化学7原则可用于为创建更安全的合成提供指导。其中一些措施包括防止废物产生 (原则 1) 和使用更安全的溶剂 (原则 5)。特别是, 在制药制造8中, 溶剂占材料非水质量的80-90%。因此, 修改协议以使用更少的危险溶剂会对有机反应的绿色产生很大的影响。
Steglich 酯化反应常使用无水氯化溶剂体系或 DMF;然而, 这些溶剂是对环境和人类健康的关注。二氯甲烷 (CH2Cl2) 和氯仿 (氯仿3) 是可能的人类致癌物, 并且 DMF 具有生殖毒性问题9。此外, CH2Cl2是消耗臭氧的10。因此, Steglich 酯化的低危险溶剂将是非常有用的。虽然尚无极性非质子溶剂的绿色替代品, 但推荐使用乙腈作为绿色替代 CH2Cl2、氯仿3和 DMF9。乙腈是目前生产丙烯腈生产的副产品;然而, 从生物量上的一个绿色合成乙腈的学术规模已报告11, 并正在调查从废物流的重复使用和回收的潜在选择12。乙腈在固相肽合成中作为氢化物偶联反应的一种更环保的溶剂替代剂, 可形成酰胺链13。使用乙腈作为溶剂系统的 Steglich 酯化已经证明了14,15,16,17,18,19, 20,21;然而, 这些方法并没有侧重于溶剂的绿色方面, 也采用柱层析法进一步纯化。
减少对柱层析的需要作为纯化步骤, 也可最大限度地减少有害溶剂浪费8。除了使用不太危险的反应溶剂, 该方法还能在不需要色谱的情况下分离出高纯度的产品。传统上使用的碳 (DCC) 耦合试剂被取代 1-乙基 3-(3-丙基) 氢化物盐酸盐 (EDC)。该试剂的碱性胺官能团可使反应副产品和任何残留试剂通过酸性和基本洗涤步骤去除。
本文提供的协议可与各种酸性和酒精合作伙伴一起使用 (图 1)。它被用来合成一个小库肉桂酯衍生物使用初级, 二次, 苄基, 和烯丙醇和酚22。此外, 乙腈中酯化反应的速率与氯化和 DMF 溶剂体系中的相媲美, 在反应22之前无需干燥或蒸馏乙腈。从第三醇合成的酯类尚未分离, 这是目前的方法的局限性与传统的 Steglich 酯化在氯化溶剂23。此外, 其他酸不稳定基团可能会受到酸性洗涤步骤的影响, 可能需要柱层析来纯化乙腈后去除。尽管存在这些局限性, 该反应是一种简便而通用的方法, 用于在高产量中使用多种醇和羧酸组分合成酯。使用更环保的溶剂系统和高纯度而不需要色谱步骤, 使本协议成为传统 Steglich 酯化的诱人替代品。
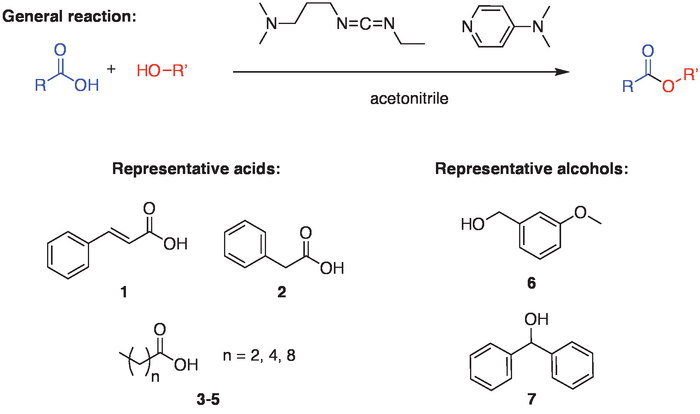
图1。一般反应方案.反应的一般方案包括羧酸和酒精的耦合, 这是使用氢化物耦合试剂 (1-乙基-3-(3-丙基) 氢化物盐酸盐, 或 EDC) 和 4-dimethylaminopyridine (DMAP) 乙腈。为了证明反应的广度, 酯的形成使用各种酸 (1-5) 与主要 (6) 或次要 (7) 酒精。请点击这里查看这个数字的更大版本.
研究方案
注意: 在本程序使用化学品之前, 请查阅安全数据表 (SDSs)。使用适当的个人防护设备 (PPE), 包括飞溅护目镜、实验室大衣、丁腈橡胶或丁基手套, 因为许多试剂和溶剂都是腐蚀性或易燃的。在烟雾罩中进行所有反应。不需要干燥的玻璃器皿或使用氮气气氛的协议。
1. 初级醇的氢化物偶联反应
- 在一个50毫升圆底烧瓶, 结合(E)-肉桂酸 (151 毫克, 1.02 毫摩尔, 1.2 等效), DMAP (312 毫克, 2.55 毫摩尔, 3 等效), 和 EDC (244 毫克, 1.28 毫摩尔, 1.5 等效)。加入乙腈 (15 毫升) 和 3-氧苄酒精 (98 微升, 0.85 毫摩尔, 1 等效) 与搅拌棒混合在一起。
注意: 乙腈是一种易燃溶剂。 - 将烧瓶夹在40摄氏度的水浴中, 搅拌反应。
注意: 如果反应涉及芳香醇, 通过使用1:3 乙酸乙酯/己烷的薄层层析 (TLC) 监测酒精损失的反应。当酒精斑点不再在 TLC 板上通过 UV 灯照射时, 反应就完成了。
2. 萃取检查
- 一旦反应完成, 如 TLC 或45分钟后, 使用旋转蒸发器在减压下去除乙腈, 以获得粗固体。
注: 有关使用旋转蒸发器24、25的信息, 请参阅其他资源。 - 对残余物, 加入乙醚 (20 毫升) 和1米盐酸 (20 毫升)。旋转烧瓶将残渣溶解到溶剂层中。
注意: 乙醚是一种高度易燃的溶剂。
注: 为降低溶剂危害, 醋酸乙酯可代替乙醚;然而, 在萃取和洗涤步骤中, 乳液形成的可能性更大。 - 将溶液倒入分液漏斗。用额外的乙醚 (5 毫升) 冲洗蒸发烧瓶, 并将漂洗添加到分液漏斗中。
- 轻轻摇动分液漏斗, 将产品提取到醚层, 定期排出。允许层分开, 然后将水层从漏斗底部排出到锥形烧瓶或烧杯中。
注: 有关提取和使用分液漏斗24、25的信息, 请参阅其他资源。
3. 洗涤程序
- 在分液漏斗中剩余的有机层, 加入 1 M HCl (20 毫升), 轻轻摇动分液烧瓶, 定期排出。允许层分开, 然后将水层从漏斗底部排出到锥形烧瓶或烧杯中。
- 使用饱和碳酸氢钠溶液 (2 x 20 mL) 重复洗涤过程, 然后使用饱和氯化钠溶液 (20 mL)。
- 将有机层从分液漏斗顶部倒入干净的锥形烧瓶中, 用硫酸镁干燥层, 然后通过过滤纸将溶液过滤成聚集的蒸发瓶。
注: 有关提取和使用硫酸镁作为干燥剂24、25的信息, 请参阅其他资源。 - 使用旋转蒸发器在减压下去除二乙醚溶剂。
- 用1H 和13C NMR 光谱在 CDCl3和质谱仪中分析产品样品。
注: 有关制备 NMR 分析样品24、25的信息, 请参阅其他资源。
4. 二次和电子缺陷醇的氢化物耦合反应
- 在一个50毫升圆底烧瓶, 结合(E)-肉桂酸 (151 毫克, 1.02 毫摩尔, 1.2 等效), DMAP (312 毫克, 2.55 毫摩尔, 3 等效), 和 EDC (244 毫克, 1.28 毫摩尔, 1.5 等效)。加入乙腈 (15 毫升) 和二苯基甲醇 (157 毫克, 0.85 毫摩尔, 1 等效) 与搅拌棒混合在一起。
注意: 乙腈是一种易燃溶剂。 - 夹紧烧瓶, 在室温下搅动反应24小时. 将空气冷凝器插入烧瓶颈部, 以尽量减少溶剂蒸发。
- 按照上述步骤2-3 中所述的萃取检查和洗涤程序进行操作。
5. 长链或疏水性羧酸的氢化物耦合反应
- 在一个50毫升圆底烧瓶, 结合癸酸 (146 毫克, 0.85 毫摩尔, 1 等效), DMAP (312 毫克, 2.55 毫摩尔, 3 等效), 和 EDC (244 毫克, 1.28 毫摩尔, 1.5 等效)。加入乙腈 (15 毫升) 和二苯基甲醇 (157 毫克, 0.85 毫摩尔, 1 等效) 与搅拌棒混合在一起。
注意: 乙腈是一种易燃溶剂。 - 夹紧烧瓶, 在室温下搅动反应24小时. 将空气冷凝器插入烧瓶颈部, 以尽量减少溶剂蒸发。如果使用主要酒精, 在40摄氏度的水浴中搅动1小时的反应。
- 按照上述步骤2-3 中所述的萃取检查和洗涤程序进行操作。
结果
在乙腈改性 Steglich 酯化反应后进行酸碱萃取检查后, 3-氧苄肉桂 (8) 获得了淡黄色油 (205 毫克, 90% 屈服), 不需要柱层析。1图 2给出了 H 和13C 核磁共振谱, 以确认结构并表示纯度。
化合物9-17是使用类似的协议 (图 3) 合成的, 产量为...
讨论
本文介绍的方法是通过使用更环保的溶剂系统和减少对柱层析8、9的需求, 将与传统 Steglich 酯化相关的溶剂的危害降至最低。可以通过使用乙腈代替干氯化溶剂或 DMF22来实现可比的反应屈服率和速率。
几个关键步骤可实现产品的高效纯化, 而无需进行色谱分析。反应后, 乙腈首先通过旋转蒸发去除。溶剂的去除是必...
披露声明
作者没有什么可透露的。
致谢
这项研究得到了锡耶纳学院和本科生研究和创意活动中心的支持。我们感谢托马斯休斯博士和克里斯托 Kolonko 博士的帮助对话, Allycia 女士为早期阶段的工作, 这一方法, 和锡耶纳学院斯图尔特的先进仪器仪表和技术 (圣) 仪器资源中心。
材料
| Name | Company | Catalog Number | Comments |
| trans -cinnamic acid | Acros Organics | 158571000 | |
| butyric acid | Sigma-Aldrich | B103500 | Caution: corrosive |
| hexanoic acid | Sigma-Aldrich | 153745-100G | Caution: corrosive |
| decanoic acid | Sigma-Aldrich | 21409-5G | Caution: corrosive |
| phenylacetic acid | Sigma-Aldrich | P16621-5G | |
| 3-methoxybenzyl alcohol | Sigma-Aldrich | M11006-25G | |
| diphenylmethanol | Acros Organics | 105391000 | Benzhydrol |
| chloroform-d | Acros Organics | 166260250 | 99.8% with 1% v/v tetramethylsilane, Caution: toxic |
| hexane | BDH Chemicals | BDH1129-4LP | Caution: flammable |
| ethyl acetate | Sigma-Aldrich | 650528 | Caution: flammable |
| diethyl ether | Fisher Scientific | E138-500 | Caution: flammable |
| acetonitrile | Fisher Scientific | A21-1 | ACS Certified, >99.5%, Caution: flammable |
| 4-dimethylaminopyridine | Acros Organics | 148270250 | Caution: toxic |
| magnesium sulfate | Fisher Scientific | M65-3 | |
| hydrochloric acid, 1 M | Fisher Scientific | S848-4 | Caution: corrosive |
| sodium chloride | BDH Chemicals | BDH8014 | |
| sodium bicarbonate | Fisher Scientific | S25533B | |
| 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide hydrochloride | Chem-Impex | 00050 | Caution: skin and eye irritant |
| thin layer chromatography plates | EMD Millipore | 1055540001 | aluminum backed sheets |
| Note: All commercially available reagents and solvents were used as received without further purification. |
参考文献
- Williams, A., Ibrahim, I. T. Carbodiimide chemistry: recent advances. Chemical Reviews. 81 (6), 589-636 (1981).
- Höfle, G., Steglich, W., Vorbrüggen, H. 4-Dialkylaminopyridines as Highly Active Acylation Catalysts. [New synthetic method (25)]. Angewandte Chemie International Edition in English. 17 (8), 569-583 (1978).
- Neises, B., Steglich, W. Simple Method for the Esterification of Carboxylic Acids. Angewandte Chemie International Edition in English. 17 (7), 522-524 (1978).
- Tsvetkova, B., Tencheva, J., Peikov, P. Esterification of 7-theophyllineacetic acid with diethylene glycol monomethyl ether. Acta pharmaceutica. 56 (2), 251-257 (2006).
- Tsakos, M., Schaffert, E. S., Clement, L. L., Villadsen, N. L., Poulsen, T. B. Ester coupling reactions - an enduring challenge in the chemical synthesis of bioactive natural products. Natural Product Reports. 32 (4), (2015).
- Morales-Serna, J., et al. Using Benzotriazole Esters as a Strategy in the Esterification of Tertiary Alcohols. Synthesis. 2010 (24), 4261-4267 (2010).
- Anastas, P., Eghbali, N. Green Chemistry: Principles and Practice. Chemical Society Reviews. 39 (1), 301-312 (2010).
- Constable, D. J. C., Jimenez-Gonzalez, C., Henderson, R. K. Perspective on solvent use in the pharmaceutical industry. Organic Process Research and Development. 11 (1), 133-137 (2007).
- Byrne, F. P., et al. Tools and techniques for solvent selection: green solvent selection guides. Sustainable Chemical Processes. 4 (1), 7 (2016).
- Hossaini, R., Chipperfield, M. P., Montzka, S. A., Rap, A., Dhomse, S., Feng, W. Efficiency of short-lived halogens at influencing climate through depletion of stratospheric ozone. Nature Geoscience. 8 (3), (2015).
- Corker, E. C., Mentzel, U. V., Mielby, J., Riisager, A., Fehrmann, R. An alternative pathway for production of acetonitrile: ruthenium catalysed aerobic dehydrogenation of ethylamine. Green Chemistry. 15 (4), 928-933 (2013).
- McConvey, I. F., Woods, D., Lewis, M., Gan, Q., Nancarrow, P. The Importance of Acetonitrile in the Pharmaceutical Industry and Opportunities for its Recovery from Waste. Organic Process Research & Development. 16 (4), 612-624 (2012).
- Jad, Y. E., et al. Peptide synthesis beyond DMF: THF and ACN as excellent and friendlier alternatives. Organic & Biomolecular Chemistry. 13 (8), 2393-2398 (2015).
- Williams, J., et al. Quantitative method for the profiling of the endocannabinoid metabolome by LC-atmospheric pressure chemical ionization-MS. Analytical Chemistry. 79 (15), 5582-5593 (2007).
- Benmansour, F., et al. Discovery of novel dengue virus NS5 methyltransferase non-nucleoside inhibitors by fragment-based drug design. European Journal of Medicinal Chemistry. 125, 865-880 (2017).
- Maier, W., Corrie, J. E. T., Papageorgiou, G., Laube, B., Grewer, C. Comparative analysis of inhibitory effects of caged ligands for the NMDA receptor. Journal of Neuroscience Methods. 142 (1), 1-9 (2005).
- Schwartz, E., et al. Water soluble azido polyisocyanopeptides as functional β-sheet mimics. Journal of Polymer Science Part A: Polymer Chemistry. 47 (16), 4150-4164 (2009).
- Hangauer, M. J., Bertozzi, C. R. A FRET-Based Fluorogenic Phosphine for Live-Cell Imaging with the Staudinger Ligation. Angewandte Chemie International Edition. 47 (13), 2394-2397 (2008).
- Hsieh, P. -. W., Chen, W. -. Y., Aljuffali, I., Chen, C. -. C., Fang, J. -. Y. Co-Drug Strategy for Promoting Skin Targeting and Minimizing the Transdermal Diffusion of Hydroquinone and Tranexamic Acid. Current Medicinal Chemistry. 20 (32), 4080-4092 (2013).
- Moretto, A., et al. A Rigid Helical Peptide Axle for a [2]Rotaxane Molecular Machine. Angewandte Chemie International Edition. 48 (47), 8986-8989 (2009).
- Hanessian, S., McNaughton-Smith, G. A versatile synthesis of a β-turn peptidomimetic scaffold: An approach towards a designed model antagonist of the tachykinin NK-2 receptor. Bioorganic & Medicinal Chemistry Letters. 6 (13), 1567-1572 (1996).
- Lutjen, A. B., Quirk, M. A., Barbera, A. M., Kolonko, E. M. Synthesis of (E)-cinnamyl ester derivatives via a greener Steglich esterification (In Press). Bioorganic & Medicinal Chemistry. , (2018).
- Wang, Z. Steglich Esterification. Comprehensive Organic Name Reactions and Reagents. , (2010).
- Padias, A. B. . Making the Connections: A How-To Guide for Organic Chemistry Lab Techniques. , (2011).
- Zubrick, J. W. . The Organic Chem Lab Survival Manual: A Student's Guide to Techniques. , (2015).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。