Method Article
الإنسان السابق الجسم الحي الجرح نموذج ونهج تلطيخ جبل كامل لتقييم بدقة إصلاح الجلد
In This Article
Summary
هنا نظهر تقنية محسنة لتقييم إصلاح الجروح باستخدام الجلد البشري السابق vivo جنبا إلى جنب مع نهج تلطيخ جبل كامل. توفر هذه المنهجية منصة ما قبل السريرية لتقييم علاجات الجروح المحتملة.
Abstract
الجروح المزمنة غير التئام، والتي تؤثر في المقام الأول على كبار السن والسكري، هي مجال كبير من الاحتياجات السريرية التي لم تلب. لسوء الحظ، علاجات الجروح المزمنة الحالية غير كافية، في حين أن النماذج المتاحة قبل السريرية لا تتنبأ بشكل جيد بالفعالية السريرية للعلاجات الجديدة. هنا نصف إنتاجية عالية، نموذج ما قبل السريرية لتقييم جوانب متعددة من استجابة إصلاح الجلد البشري. تم إنشاء جروح سمك جزئي في الجلد الجسم الحي السابق الإنسان ومثقفة عبر مسار زمني الشفاء. تم جمع خزعات جرح الجلد في مثبت لإجراء تلطيخ الجبل بأكمله. تم حجب العينات الثابتة واحتضانها في الأجسام المضادة الأولية ، مع تحقيق الكشف عن طريق الأجسام المضادة الثانوية المقترنة بالفلورسنت. كانت الجروح ملطخة وصورة عن طريق المجهر الكونفوجكال قبل حساب نسبة إغلاق الجرح (إعادة الظهارة) في كل خزعة. تطبيق هذا البروتوكول، ونحن نكشف عن أن 2 مم الجروح الإستئصالية التي تم إنشاؤها في الجلد المانحة صحية يتم إعادة ظهارة تماما من قبل اليوم 4-5 بعد الجرح. بل على العكس من ذلك، فإن معدلات إغلاق الجروح الجلدية السكرية تنخفض بشكل كبير، مصحوبة بإصلاح الحواجز المضطربة. الجمع بين جرح الجلد البشري مع نهج جديد تلطيخ جبل كامل يسمح لطريقة سريعة وقابلة للاستنساخ لقياس إصلاح الجرح في الجسم الحي السابق. يوفر هذا البروتوكول بشكل جماعي منصة بشرية قيمة لتقييم فعالية علاجات الجروح المحتملة، وتحويل الاختبار قبل السريري والتحقق من الصحة.
Introduction
الجروح المزمنة غير التئام، والتي هي منتشرة للغاية في كبار السن والسكري، هي منطقة لا يقدرها أحد بشكل رئيسي من الحاجة السريرية غير الملباة. هذه الجروح تشكل عبئا جسديا ونفسيا كبيرا على المرضى وتكلف مقدمي الرعاية الصحية المليارات كل عام لعلاج1. على الرغم من تحسن فهم بيولوجيا الجروح والتقدم في التكنولوجيا ، لا يزال ما يصل إلى 40٪ من الجروح المزمنة يفشل في التئام بعد أفضل رعاية قياسية2. وهكذا، 14-26٪ من المرضى الذين يعانون من قرحة القدم السكري تتطلب في وقت لاحق بتر3،في حين أن معدل وفيات ما بعد البتر لمدة 5 سنوات يبلغ حوالي 70٪4. ونتيجة لذلك، هناك حاجة ملحة لتطوير علاجات جديدة فعالة لتحسين نوعية حياة المرضى مع الحد من عبء الرعاية الصحية الكبير الذي تفرضه الجروح التئام الفقراء. لا تزال النماذج السابقة للسريرية التنبؤية السيئة تشكل عقبة كبيرة أمام تطوير علاجات جديدة فعالة.
إصلاح الجرح هو عملية ديناميكية ومتعددة الأوجه تنطوي على مجموعة متنوعة من أنواع الخلايا، ومستويات لا تحصى من الاتصالات وبيئة الأنسجة التي يتم تشكيلها زمنيا. ويدعم شفاء الجلد من قبل أربع مراحل إعادة تحديد رئيسية: التهاب الكبد، التهاب، والانتشار، وإعادة عرض مصفوفة. هذه المراحل تعمل في نهاية المطاف لمنع فقدان الدم والعدوى، وإغلاق سطح الجرح (عملية يطلق عليها إعادة الظهارة) وإعادة الجلد إلى حالة غيرمصابة 5. ترتبط الجروح المزمنة بعوامل مختلفة واضطرابات واسعة النطاق لعملياتالتئام 6، مما يزيد من تعقيد تحديد الأهداف العلاجية. ومع ذلك ، تم تطوير مجموعة واسعة من النماذج لتوضيح كل من الدوافع الجزيئية والخلوية لأمراض الجروح واختبار نهج علاجية جديدة7.
نموذج إصلاح الجرح الأكثر استخداما هو الجرح الحاد في الماوس. الفئران هي قابلة للسحب للغاية للدراسات الميكانيكية وتوفير نماذج التحقق من صحة الشيخوخة والسكري8. على الرغم من أوجه التشابه العامة التي تظهر بين الماوس والشفاء البشري ، لا تزال الاختلافات بين الأنواع في بنية الجلد وديناميكيات الشفاء قائمة. وهذا يعني أن معظم البحوث الجرح مورين لا تترجم بسهولة إلى العيادة9. وبالتالي، كان هناك دفع نحو الإنسان في المختبر وأنظمة الجسم الحي السابق مع قابلية عالية للتطبيق وقابلية الترجمة10،11.
هنا نقدم بروتوكول متعمق لأداء الجروح استئصال سمك جزئي في الجلد البشري في الجسم الحي السابق. كما نحدد نهجنا الكامل للتلطيخ كطريقة قابلة للاستنساخ للغاية لتقييم شفاء الجلد البشري في الجسم الحي السابق. نحن نظهر مسار إصلاح البشرة (إعادة الظهارة) وتشكيل الحاجز اللاحق ، وتقييم معدل إغلاق الجروح في الجلد البشري الصحي مقابل السكري. وأخيرا، فإننا نظهر كيف يمكن تكييف تلطيخ كامل جبل للاستخدام مع مجموعة من الأجسام المضادة لتقييم جوانب مختلفة من الاستجابة الشفاء.
Protocol
تم الحصول على بشرة بشرية من المرضى الذين يخضعون لجراحة ترميمية في مستشفى كاسل هيل ومستوصف هال الملكي (هال، المملكة المتحدة) تحت موافقة كاملة مستنيرة ومكتوبة للمرضى، ومبادئ توجيهية مؤسسية، وموافقة أخلاقية (LRECs: 17/SC/0220 و 19/NE/0150). تم جمع الجلد غير السكري من المرضى الذين يخضعون لعملية جراحية روتينية (متوسط العمر = 68). تم اختيار الجلد السكري من بين المتبرعين الذين أنشأوا مرض السكري من النوع الثاني وتاريخ من التقرح (متوسط العمر = 81). ونقلت عينات من الجراحة في وسائط احتجاز وعالجت فور وصولها إلى المختبر. تم تنفيذ جميع الخطوات التجريبية باستخدام الأنسجة البشرية غير المثبتة في مستوى السلامة البيولوجية -2 (BSL-2) في خزانة السلامة البيولوجية لتدفق الصفيحة من الفئة الثانية.
1. إعداد وسائل الإعلام ثقافة الجلد والكواشف تلطيخ
ملاحظة: يتم توفير جميع التفاصيل الكاشفة والمستهلكة في جدول المواد. ضمان جميع الكواشف والمعدات المستخدمة لمعالجة وزراعة الأنسجة البشرية هي عقيمة. تعقيم الأدوات قبل الاستخدام وإزالة التلوث بالمطهر بعد ملامسة الأنسجة. إزالة التلوث من النفايات في 1٪ مطهر قبل التخلص منها.
- وسائل الإعلام القابضة: تكملة عالية الجلوكوز Dulbecco المعدلة النسر المتوسط (DMEM) مع 2 MM L-الجلوتامين و 4٪ (v/v) المضادة للمضادات الحيوية المضادة للميكون الحل.
- محلول الملح المتوازن من هانك (HBSS) مع المضادات الحيوية: أضف 4٪ (v/v) محلول مضاد للمضادات الحيوية المضادة للذهان إلى HBSS. يخزن عند درجة حرارة 4 درجات مئوية حتى الاستخدام.
- ملحي الفوسفات في دولبيكو (DPBS): إعداد DPBS عن طريق إذابة 9.6 غرام من مسحوق DPBS لكل لتر من الماء المقطر (dH2O). أوتوكلاف لتعقيم وتخزينها في 4 درجة مئوية حتى الاستخدام.
- وسائل الإعلام نمو الجلد البشري: تكملة عالية الجلوكوز DMEM مع 2 MM L-الجلوتامين, 1٪ (v/v) محلول مضاد للمضادات الحيوية المضادة للميكون و 10٪ (v/v) مصل البقر الجنيني. يخزن عند درجة حرارة 4 درجات مئوية حتى الاستخدام.
- مثبت البشرة: إلى 450 مل من dH2O، أضف 40 مل من محلول الفورمالديهايد، و10 مل من حمض الخليك الجليدي، و4.5 جرام من كلوريد الصوديوم و0.25 جرام من بروميد الألكيلتريميثلامنيومنيوميوم. يخزن في درجة حرارة الغرفة (RT) ويستخدم في غضون أيام قليلة.
تنبيه: المثبت خطر (مهيج و قابل للاشتعال). التعامل مع بعناية والتخلص من عبر الطريق المناسب. - الفوسفات العازلة المالحة (PBS): إعداد برنامج تلفزيوني لتلطيخ كامل جبل بإضافة 6 غرام من كلوريد الصوديوم إلى 100 مل من محلول عازل الفوسفات و 900 مل من DH2O.
- تلطيخ غسل العازلة: حل 0.5٪ (v/v) تريتون X-100 في برنامج تلفزيوني.
- حظر العازلة: إضافة 0.2٪ (ث / v) أزيد الصوديوم و 2٪ (v/v) مصل الحيوان إلى تلطيخ العازلة غسل. يخزن عند درجة حرارة 4 درجات مئوية لمدة تصل إلى أسبوعين.
ملاحظة: كتلة في مصل الأنواع المضيفة الأجسام المضادة الثانوية. سوف أزيد الصوديوم منع نمو البكتيريا أثناء الحضانة. - DAPI حل العمل: إعداد 5 ملغ / مل من المخزون 4′,6-diamidino-2-phenylindole (DAPI) في ثنائي ميثيل سلفوإكسيد. تمييع المخزون 1:1,000 في تلطيخ غسل العازلة لإعطاء 5 ميكروغرام / مل DAPI حل العمل.
- كتلة البيروكسيديز: إضافة 0.3٪ (v/v) بيروكسيد الهيدروجين إلى تلطيخ عازلة غسل. يخزن عند درجة حرارة 4 درجات مئوية حتى الاستخدام. تبقي في الظلام لمنع التحلل.
- ABC-HRP كيت:
- HRP-اقتران الأجسام المضادة الثانوية: 1 قطرة من الأرنب البيوتينيلات المضادة للماعز IgG في 5 مل من العازلة تلطيخ. يخزن عند درجة حرارة 4 درجات مئوية لمدة تصل إلى أسبوعين.
ملاحظة: تعتمد المجموعة/الثانوية المستخدمة على الأنواع المضيفة للأجسام المضادة الأولية. - مجمع أفيدين البيوتين (ABC) كاشف: 2 قطرات من الكاشف A و 2 قطرات من الكاشف B في 5 مل من تلطيخ عازلة غسل. يجب إعداد كاشف ABC قبل 30 دقيقة على الأقل من الاستخدام. يخزن عند درجة حرارة 4 درجات مئوية لمدة تصل إلى أسبوعين.
- HRP-اقتران الأجسام المضادة الثانوية: 1 قطرة من الأرنب البيوتينيلات المضادة للماعز IgG في 5 مل من العازلة تلطيخ. يخزن عند درجة حرارة 4 درجات مئوية لمدة تصل إلى أسبوعين.
- ركيزة البيروكسيداز: 3 قطرات من الكاشف 1، 2 قطرات من الكاشف 2، 2 قطرات من الكاشف 3 و 2 قطرات من بيروكسيد الهيدروجين في 5 مل من DH2O. Peroxidase الركيزة ينبغي أن تكون طازجة على الفور قبل الاستخدام ولا يمكن تخزينها.
2. إعداد الجلد للجرح
ملاحظة: يجب تنفيذ هذه الخطوات في خزانة السلامة الحيوية تدفق صفح فئة II.
- جمع الجلد في وسائل الإعلام عقد والنقل إلى مجلس الوزراء BSL-2.
- ضع جانب الأدمة الجلدية لأسفل داخل طبق بيتري معقم عيار 90 مم وأزل الأنسجة الدهنية بمقص معقم.
- ضع الجلد في أنبوب 50 مل يحتوي على 25 مل من HBSS مع المضادات الحيوية لمدة 10 دقائق في RT. يهز بشكل متقطع لإزالة أي دم متبقي وأنسجة الدهنية.
- كرر الخطوة 2.3 باستخدام أنبوب جديد سعة 50 مل.
- ضع الجلد في أنبوب 50 مل طازج يحتوي على 25 مل من HBSS ، وهذه المرة بدون مضادات حيوية لمدة 10 دقائق في RT. Shake كما هو الحال في الخطوة 2.3.
- قم بإجراء شطف الجلد النهائي عن طريق وضع الجلد في أنبوب جديد مع 25 مل من DPBS. الجلد الآن جاهز للجرح.
3. خلق ex vivo جروح الجلد البشري
ملاحظة: يجب تنفيذ هذه الخطوات في خزانة السلامة الحيوية تدفق صفح فئة II.
- إعداد أطباق زراعة الجلد قبل الجرح. في طبق بيتري 60 ملم، كومة اثنين من منصات ماصة معقمة وإضافة 4 مل من وسائل الإعلام الجلد البشري عبر الجانب من الطبق. ضع غشاء فلتر نايلون معقم على كومة الوسادة الماصة.
ملاحظة: يمكن تغيير وسائط البشرة اعتمادا على ظروف العلاج المطلوبة. يمكن استزراع ما يصل إلى ثلاثة نباتات خارجية للجروح على كل كومة. - جفف الجانب الجلدي من الجلد على شاش معقم في طبق بيتري عيار 90 مم لإزالة DPBS المتبقية.
ملاحظة: هذا يمنع الجلد من الانزلاق حولها عند الجرح. - وضع الجلد الأدمة الجانب إلى أسفل على غطاء طبق بيتري نظيفة 90 ملم وداب البشرة الجافة مع الشاش العقيم الطازج.
ملاحظة: من الأسهل جرح الجلد في غطاء طبق بيتري من القاعدة. وينبغي أن يتم العمل اللاحق بسرعة لمنع جفاف الجلد. - أمسك الجلد مشدودا، واضغط على لكمة خزعة من عيار 2 ملم على الجلد وتويست بلطف. لا لكمة تماما من خلال الجلد.
ملاحظة: تم تصميم جروح سمك جزئي لكمة من خلال البشرة وجزئيا في الأدمة. قد يكون هناك تباين من مانح إلى مانح ومن موقع إلى موقع في القوة المطلوبة لخلق جرح سمك جزئي. - استخدام ملقط الأنسجة المسننة المنحنية لالتقاط كل جانب من الجرح 2 ملم وربط مقص القزحية المنحنية تحت الجرح 2 ملم لقطع عليه بشكل موحد.
- خزعة حول الجرح المركزي 2 ملم باستخدام لكمة خزعة 6 ملم لخلق explant 6 ملم مع سمك جزئي 2 ملم الجرح في المركز.
ملاحظة: يمكن استخدام لكمة خزعة 6 مم لتسجيل الجلد لتحديد المكان الذي يجب أن يكون فيه كل جرح 2 مم. الحرص على عدم اختراق الأنسجة تماما. إنشاء explants الجرح في نمط العسل للحد من الهدر. - مكان الجرح explants البشرة الجانب حتى على كومة غشاء مرشح النايلون (أعدت في الخطوة 3.1).
ملاحظة: عند التعامل مع الجروح، يجب الحرص على عدم إتلاف الجرح المركزي. استخدام ملقط صغير والتقاط كل explant في الجانبين المعاكس. - حضانة الجروح في 32-37 درجة مئوية و 5٪ثاني أكسيد الكربون في جو رطب (90-95٪) لمدة 1-7 أيام. استبدال وسائل الإعلام كل 2-3 أيام.
4. كامل جبل تلطيخ الجروح في الجسم الحي السابق
ملاحظة: يصف هذا القسم طرق تلطيخ المناعة و تلطيخ الأكسدة المناعية. تخلط جميع الكواشف جيدا قبل الاستخدام.
- طريقة تلطيخ الفلورسنت
- جمع الجروح في أنابيب الطرد المركزي الدقيق 1.5 مل تحتوي على 500 ميكرولتر من تثبيت الجلد واحتضان في 4 درجة مئوية بين عشية وضحاها.
ملاحظة: المثبت المستخدمة في هذا البروتوكول يعمل بشكل جيد للأجسام المضادة الموصوفة. وسوف تكون هناك حاجة الأمثل للأجسام المضادة الأخرى. تثبيت الأنسجة أطول من 24 ساعة قد يؤدي إلى الإفراط في التثبيت. - في اليوم التالي إزالة المثبت واستبدالها مع 1 مل من تلطيخ غسل العازلة. يمكن تخزين الخزعات في مخزن الغسيل المؤقت عند 4 درجات مئوية حتى أسبوعين قبل التلطيخ.
ملاحظة: لجميع الخطوات العازلة غسل، استخدم ماصة المصلية أو تلميح ماصة، مع الحرص على عدم تلف الجرح. - يستنشق العازلة غسل تلطيخ وأداء شطف واحد أكثر مع 1 مل من تلطيخ غسل العازلة.
- حساب مقدار حظر المخزن المؤقت المطلوبة للخطوات 4.1.5-4.1.6 (عدد العينات x 300 μL = مقدار المخزن المؤقت حظر في μL). جعل عازلة إضافية إذا لزم الأمر.
- أضف 150 ميكرولتر من حاجز الحجب إلى كل عينة واحتضن لمدة ساعة واحدة في RT. لجميع خطوات تلطيخ، تأكد من تغطية كل عينة بما فيه الكفاية وأنه لا توجد فقاعات تغطي سطح الجرح خزعة.
ملاحظة: يمكن تنفيذ هذه الخطوة فصاعدا في أنابيب 1.5 مل من أجهزة الطرد المركزي الدقيق أو في لوحة بئر 48. إذا كنت تستخدم لوحة بئر 48، واحتضان الجروح وجهه إلى أسفل في كل بئر. - تمييع الأجسام المضادة الأساسية في العازلة حجب المتبقية.
ملاحظة: مكافحة الماوس الكيراتين 14 (K14) المخفف 1:1,000 في حظر المخزن المؤقت يعمل بشكل جيد. تحسين هذه الخطوة للاستخدام مع الأجسام المضادة الأخرى أو تحقيقات متعددة. - يستنشق العازلة حجب وإضافة 150 ميكرولتر الأجسام المضادة الأولية لكل أنبوب جيدا / microcentrifuge. احتضان الجروح في الأجسام المضادة الأولية في 4 درجة مئوية بين عشية وضحاها.
- في اليوم التالي، يستنشق الأجسام المضادة الأولية وشطف في تلطيخ غسل العازلة التي تحتوي على 0.2٪ من آزيد الصوديوم لمدة 1 ساعة في RT (500 ميكرولتر لكل عينة).
- قم بإجراء ثلاث خطوات شطف أخرى باستخدام حاجز غسل التلطيخ (30 دقيقة لكل غسل، 500 ميكرولتر لكل عينة).
- تمييع الأجسام المضادة الثانوية المترافقة الفلورية في تلطيخ مخزن الغسيل المؤقت (على سبيل المثال ، الماعز المضاد للفأرة 488 في 1:400 التخفيف).
- حساب الكمية المطلوبة من الأجسام المضادة الثانوية (عدد العينات × 150 ميكرولتر = المبلغ في μL).
- إضافة 150 ميكرولتر من الأجسام المضادة الثانوية إلى كل أنبوب جيدا / ميكروسينتريف. حضانة لمدة 1 ساعة في RT. تنفيذ خطوات الحضانة 4.1.10 - 4.1.16 في الظلام كما الأجسام المضادة الثانوية حساسة للضوء.
ملاحظة: يمكن تنفيذ هذه الخطوة عند 4 °C بين عشية وضحاها إذا لزم الأمر. تحسين تركيز الأجسام المضادة الثانوية المطلوبة للإشارة الكافية وتلطيخ الخلفية محدودة. - إزالة الأجسام المضادة الثانوية وإجراء 3 × 30 دقيقة شطف مع تلطيخ غسل العازلة (500 ميكرولتر لكل عينة).
- تجاهل المخزن المؤقت غسل المتبقية وحساب مقدار حل العمل DAPI المطلوبة (وفقا للخطوة 4.1.11).
- مضادةالتي تحتوي على كل explant مع 150 ميكرولتر من حل العمل DAPI لمدة 10 دقيقة في RT.
ملاحظة: DAPI سوف وصمة عار الخلايا النوى الزرقاء. يمكن استخدام صبغة Hoechst كبديل ل DAPI. - قم بإجراء غسلين نهائيين ب 30 دقيقة مع مخزن غسيل تلطيخ (500 ميكرولتر لكل عينة). يمكن تخزين الخزعات في مخزن الغسيل المؤقت عند 4 درجات مئوية في الظلام حتى أسبوعين قبل التصوير.
- جمع الجروح في أنابيب الطرد المركزي الدقيق 1.5 مل تحتوي على 500 ميكرولتر من تثبيت الجلد واحتضان في 4 درجة مئوية بين عشية وضحاها.
- طريقة تلطيخ برايتفيلد.
- تنفيذ الخطوات 4.1.1 - 4.1.3.
- كونش نشاط البيروكسيداز الذاتية مع كتلة البيروكسيديز في 4 درجة مئوية بين عشية وضحاها.
ملاحظة: هذه الخطوة مهمة عند استخدام الأجسام المضادة اقتران HRP للحد من تلطيخ الخلفية غير محددة من الأنسجة. سوف تحتوي الأنسجة ذات الأوعية الدموية العالية على نشاط البيروكسيديز الداخلي. - تجاهل كتلة البيروكسيديز وشطف مرتين لمدة 30 دقيقة في تلطيخ غسل العازلة.
- تنفيذ الخطوات 4.1.4 - 4.1.8.
ملاحظة: يغسل بعد الخطوة 4.1.7 مهمة بشكل خاص لإزالة أزيد الصوديوم من العينات. إذا لم تتم إزالة أزيد الصوديوم بشكل كاف ، فإنه سيتم تعطيل HRP وتتداخل مع الكشف عن تلطيخ. - إضافة 150 ميكرولتر HRP-اقتران الأجسام المضادة الثانوية إلى كل أنبوب جيدا / ميكروسينتريف واحتضان بين عشية وضحاها في 4 درجة مئوية أو 1 ساعة في RT.
- إزالة الأجسام المضادة الثانوية وإجراء يغسل 3 × 30 دقيقة في تلطيخ العازلة غسل.
- أضف 150 ميكرولتر من كاشف ABC إلى كل أنبوب الآبار/أجهزة الطرد المركزي الدقيق واحتضنه بين عشية وضحاها عند 4 درجات مئوية أو ساعة واحدة في RT.
- يستنشق الكاشف ABC وأداء يغسل 3 × 30 دقيقة في تلطيخ العازلة غسل.
- إضافة 150 ميكرولتر peroxidase الركيزة إلى explant واحد وتحديد الوقت اللازم للكشف عن تغيير ملحوظ اللون.
ملاحظة: اختر عينة حيث من المتوقع تلطيخ قوية. في هذه الحالة، حلقة حمراء لإظهار البشرة المهاجرة (K14). 3,3'-diaminobenzidine-4, أو أي ركيزة كروموجينيك مناسبة أخرى, يمكن استخدامها كبديل لهذه الركيزة البيروكسيديز. - بمجرد ملاحظة تغيير اللون، قم بإزالة الركيزة البيروكسيداسية، واستبدلها ب 1 مل من dH2O.
- كرر الكشف عن الركيزة البيروكسيديز للنباتات الأخرى، واحتضان للمرة المحددة في الخطوة 4.2.11.
- شطف جميع explants مع 1 مل من DH2O لإزالة الركيزة البيروكسيديز المتبقية. على الرغم من أنه يمكن تخزين النباتات السابقة لمدة تصل إلى أسبوع واحد عند درجة حرارة 4 درجات مئوية قبل التصوير ، فمن الأفضل تصويرها في أقرب وقت ممكن لمنع ترشيح ركيزة البيروكسيداز في dH2O بمرور الوقت.
5. التصوير والتحديد الكمي
- التصوير الفلوري
ملاحظة: يتم إجراء التصوير الفلوري باستخدام مجهر مسح ليزر كونفوج. ومع ذلك، قد يكون المجهر الفلوري المقلوب كافيا للحصول على صور 2D لتحديد معدلات إغلاق الجرح. عند اختيار الأجسام المضادة الثانوية، تأكد من أن الفلوروشروم المختار متوافق مع أطياف الإثارة والانبعاثات لمعدات الفحص المجهري المتاحة.- استخدم مجهر مسح ليزر كونفوج مجهزا بمسرح 2.5x و 10x و 20x ، و x-y-z الآلية ، والكاميرا الرقمية ، وبرامج الاستحواذ. قم بتشغيل كاشف الضوء المرسل (TPMT) للسماح بالتصور السهل لكل خزعة ولتمكين قياس الإغلاق الكلي للجروح. بدلا من ذلك، قياس كل جرح عن طريق المجهر برايتفيلد بعد التصوير الفلوري.
- ضع قاعدة طبق بيتري مقاس 60 مم على منصة التصوير وأضف طبقة رقيقة (حوالي 1 مل) من DPBS.
ملاحظة: إذا تم استخدام DPBS أكثر من اللازم، فإن الخزعة ستتحرك أثناء التصوير. بدلا من ذلك استخدام لوحة بئر 48 إذا كان حامل لوحة متاحة. - استخدام ملقط الأنسجة الصغيرة لنقل النباتات الجرح من الآبار / أنابيب الطرد الدقيق إلى طبق بيتري التي تحتوي على DPBS. ضع جانب الجرح الخزعة أسفل في طبق بيتري.
- استخدام العدسة ومصباح الفلورسنت لتحديد موقع والتركيز على الجرح. إذا حوصرت الفقاعات تحت العينة في مجال الرؤية ، فالتقط الجرح باستخدام ملقط الأنسجة وإعادة وضعه.
- إعداد برنامج التصوير، وضمان حجم الثقب متساوية بين القنوات لconfocality الأمثل. لهذا، تحقق من قيمة وحدة متجدد الهواء واحدة لكل قناة وحدد أكبر قيمة. حدد سرعة المسح الضوئي وجودة الصورة ومتوسطها.
ملاحظة: سوف الفلوروشرومات من الأجسام المضادة الثانوية المترافقة والطينة المضادة المختارة (على سبيل المثال، DAPI) تملي القنوات المطلوبة. - قم بتشغيل برنامج الاستحواذ المباشر وضبط قوة الليزر وكسب كل قناة إلى المستويات المطلوبة لتصور تلطيخ. قلل من ضوضاء الخلفية بزيادة الإزاحة الرقمية.
- ضع الجرح في مركز الطائرة التصويرية.
ملاحظة: إذا لم يملأ الجرح الصورة بالكامل بسبب استخدام هدف أصغر أو إنشاء جرح أكبر، فاصطح إلى لوحة من الصور وخيطها معا (يدويا أو باستخدام وظيفة تجانب في برنامج التصوير ذي الصلة). - الحصول على صور من خزعات الجرح. استخدم نفس إعدادات التصوير بين النباتات السابقة.
ملاحظة: ستسمح صور الطاقة العالية بتقييم هياكل الأنسجة وتعبير العلامة الخلوية وموقعها. - جمع مداخن Z المسلسل من خلال الجرح، وخصوصا عندما لا تكون مسطحة تماما الأنسجة ضد طبق بيتري. استخدم برنامج التحليل لانهيار المكدس Z إلى صورة إسقاط شدة قصوى واحدة.
- برايتفيلد التصوير
ملاحظة: يمكن إجراء التصوير برايتفيلد من الخزعات الملطخة immunoperoxidase بطرق متعددة.- تصوير مجهر مقلوب: إعداد نباتات الجرح التصويرية عن طريق وضعها في طبق بيتري/كما هو موضح في الخطوات 5.1.2-5.1.3. احصل على صور رقمية تحت إضاءة ساطعة على مجهر مقلوب مجهز بكاميرا رقمية. قم بتجميع صور متعددة معا إذا لزم الأمر.
- التصوير بالمجهر الرقمي اللاسلكي: استخدم مجهر رقمي لاسلكي متصل بهاتف أو كمبيوتر محمول للحصول على صور عالية الجودة بطريقة فعالة من حيث التكلفة. وضع explants الجرح الجانب حتى على بعض الأنسجة وإزالة أي DHالمتبقية 2O (أو تلطيخ غسل العازلة) من تخزين العينة. ضع الجرح في وسط مجال المجهر للعرض. احصل على الصور باستخدام الكاميرا المتصلة.
- التحديد الكمي
ملاحظة: يمكن قياس نسبة إغلاق الجرح في أي برنامج يسمح برسم الأشكال اليدوية وقياسها. يمكن استخدام ImageJ لإجراء القياس الكمي على النحو التالي:- افتح الصورة ليتم قياسها كميا في برنامج ImageJ.
- استخدم أداة الشكل الحر لرسم الجزء الخارجي من الجرح الذي أعيد ظهارته حيث يلتقي بالجلد الطبيعي. اضغط على M (أو تحليل | قياس) للحصول على قياس المنطقة "الخارجية".
ملاحظة: يختلف نسيج أنسجة الجرح الذي أعيد ظهارته عن الجلد الطبيعي. لا تحتاج الصور إلى تحجيم قبل هذا النوع من التحليل. - استخدم أداة الشكل الحر لرسم حول منطقة الجرح المفتوحة. هذا هو المكان الذي يلتقي الجرح المفتوح الحافة الداخلية للأنسجة إعادة الظهارة. اضغط على M (أو تحليل | قياس) للحصول على قياس المنطقة "الداخلية".
- استخدم المعادلة التالية لاستقراء النسبة المئوية لإعادة ظهارة الجرح/إغلاقه:
٪ إغلاق = (منطقة الجرح الخارجي - منطقة الجرح الداخلي) / (منطقة الجرح الخارجي) × 100
ملاحظة: يمكن استنتاج تغطية مساحة النسبة المئوية للأجسام المضادة بنفس الطريقة (على سبيل المثال، K14) أو كنسبة مئوية من إجمالي مساحة الجرح. يمكن أن توفر كثافة النسبة المئوية أيضا معلومات شبه كمية حول التعبير على مستوى الأنسجة عن علامات الاهتمام ، في حين يقدم التصوير عالي الطاقة بيانات التعبير على المستوى الخلوي.
النتائج
في هذا التقرير، نقدم رواية جديدة ex vivo الجلد الجرح وكامل جبل تلطيخ النهج لتقييم العوامل التي تؤثر على استجابة إصلاح الجلد البشري. ويبين الشكل 1 ألف تخطيط خط الأنابيب الإجرائي، الذي يمكن إجراؤه في غضون 3-10 أيام، تبعا لمرات حضانة الجرح. يتم استزراع جروح السمك الجزئي على أكوام الأغشية في الهواء : واجهة الغشاء ويمكن جمعها لتلطيخ التركيب الكامل ، جزءا لا يتجزأ من البارافين أو OCT المتوسطة لعلم الأنسجة العام ، أو المجمدة في النيتروجين السائل للتحليل الكيميائي الحيوي(الشكل 1B). نحن عموما خلق 2 مم الجروح سمك جزئي داخل مركز 6 ملم explants. ومع ذلك، قد يتم تغيير حجم الجرح والزرع المحيط به اعتمادا على المتطلبات. وقد تم تكييف الإجراء كامل جبل بنجاح لكلا immunoperoxidase وطرق تلطيخ immunofluorescence (الشكل 1C).
Immunofluorescence يسمح للتحقيق في الأنسجة مع الأجسام المضادة متعددة. لهذا، ننصح باستخدام الأجسام المضادة الأولية التي أثيرت في أنواع مختلفة، والأنواع المتطابقة مع الأجسام المضادة الثانوية المترافقة بالفلورسنت للحد من التفاعل بين الأنواع. تركيزات الأجسام المضادة وأوقات الحضانة سوف تحتاج إلى تحسين. إذا لوحظ تلطيخ الخلفية، والحد من تركيزات الأجسام المضادة، وزيادة خطوات الغسيل، وإضافة العازلة حجب إلى الأجسام المضادة الثانوية. يمكن تقييم صلاحية الأنسجة الطازجة مباشرة باستخدام الأصباغ التجارية (انظر جدول المواد). كما نظهر أن الأنسجة قد تكون ثابتة بعد تلطيخ البقاء وصورت بنجاح عندما يكون مناسبا عمليا(الشكل 1D).
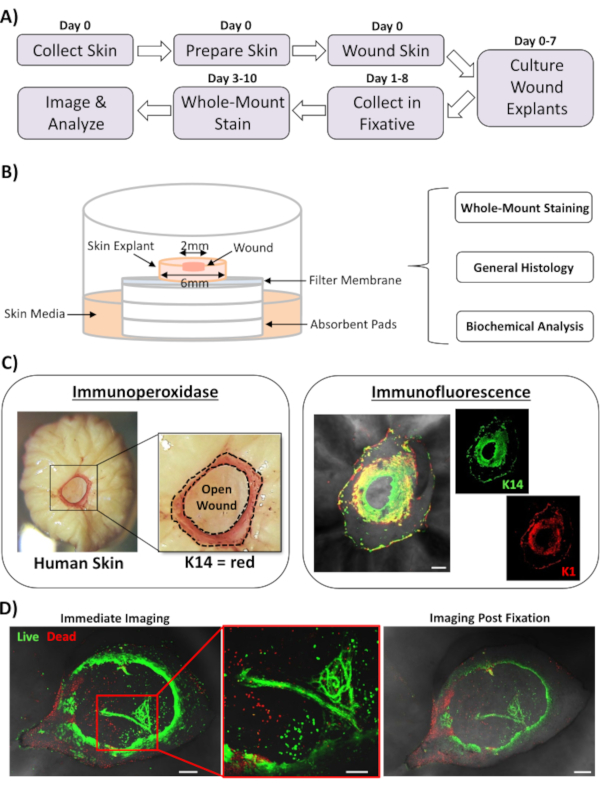
الشكل 1: الإنسان السابق فيفو الجرح وكامل جبل تلطيخ النهج. (أ) خط أنابيب يصور سير العمل الإجرائية من جمع الجلد وأداء الجرح في الجسم الحي السابق، لتلطيخ الأنسجة وتحليل البيانات. (ب) الرسم البياني الذي يدل على الإنسان السابق الجسم الحي الجلد الجرح نظام الثقافة مع التحليلات التي أجريت بشكل روتيني على الأنسجة. (ج)يمكن استخدام تلطيخ كامل الجبل باستخدام كل من تقنيات الأكسدة المناعية والمناعة. K14 = الكيراتين 14. (د)قد تكون ملطخة الأنسجة الحية مع الأصباغ الجدوى التجارية وصورت بنجاح بعد التثبيت. شريط = 100 ميكرومتر. تم إجراء هذا التلطيخ في الجلد غير السكري. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
الاستخدام الأكثر انتشارا لتلطيخ كامل جبل من الجروح هو تحديد معدل إغلاق الجرح بطريقة أكثر استنساخا مما يمكن توفيره عن طريق قسم النسيج. تم تحديد نسبة الإغلاق كنسبة مئوية لإعادة ظهارة سطح الجرح، كما هو موضح في الشكل 2A. يمكن قياس تغطية مساحة النسبة المئوية لعلامات محددة من إجمالي مساحة الجرح أو كنسبة مئوية من الجرح الذي أعيد ظهارته. تميزنا الشفاء في صحية (غير السكري) مقابل الجلد السكري عبر مسار زمني من سبعة أيام، وجمع الجروح في كل يوم بعد الجرح (صور تمثيلية، الشكل 2B). أغلقت جروح الجلد الصحية مع مرور الوقت كما هو متوقع، مع ملاحظة الإغلاق الكامل في معظم العينات بحلول اليوم 4-5. بل على العكس من ذلك، فشلت الجروح الجلدية السكرية في الإغلاق الكامل خلال فترة التحليل التي استمرت سبعة أيام(الشكل 2C). لوحظ تأخير كبير في إغلاق الجروح بين الجروح الجلدية الصحية والسكرية عند مقارنة معدلات الشفاء في كل نقطة زمنية بعد الإصابة(P < 0.001 إلى اليوم 6 ، P < 0.05 في اليوم 6 و P < 0.05 إلى P < 0.001 في اليوم 7).
بعد تقييم المعدلات الإجمالية لإغلاق الجرح؛ قمنا بقياس النسبة المئوية لمنطقة الجرح بأكملها (المنطقة الخارجية في الشكل 2A)حيث يمكن تصور الخلايا الإيجابية K14 (تلطيخ أخضر في الشكل 2B). ومن المثير للاهتمام، لاحظنا أنه في صحية ex vivo الجلد الجروح، K14 تلطيخ بلغت ذروتها في اليوم 2 ثم انخفضت بسرعة (أهمية في كل نقطة زمنية مقابل ذروة اليوم 2، الشكل 2D). وهذا يعكس على الأرجح إعادة تشكيل حاجز البشرة المبكر، باستثناء اختراق الأجسام المضادة K14 من خلال طبقات البشرة المتمايزة (انظر الشكل 2E التخطيطي). أثناء عملية إعادة الظهارة ، تهاجر خلايا القرنية القاعدية (K14 +ve) إلى الداخل فوق الجرح المفتوح بحيث تتشكل البشرة الأقرب إلى حافة الجرح الخارجي في وقت أبكر من البشرة الأقرب إلى حافة الجرح الداخلية (جبهة الهجرة). في حين أن الحافة الأمامية للبشرة التي تشكلت حديثا لا تزال تهاجر لإغلاق الجرح المفتوح المتبقي ، يبدأ البشرة الخارجية في التفريق لإصلاح الطبقات البشرة الأخرى. في الشفاء المبكر ، نتوقع بالتالي أن نرى معظم المنطقة التي أعيد ظهارها تتكون من خلايا القاعدية (K14 +ve) ، بينما في وقت لاحق يتم فقدان تلطيخ K14 حيث يفرق البشرة من الداخل الخارجي (انظر صور التركيب الكامل في الشكل 2E). لذلك ، يرتبط الانخفاض في تلطيخ K14 الموضح في الشكل 2D (الأسهم الهابطة) بزيادة تمايز البشرة. ومن المثير للاهتمام، تلطيخ K14 مرئية بلغت ذروتها في وقت سابق في صحية (اليوم 2) مقابل السكري (اليوم 4) الجروح، مما يدل على أن إعادة الظهارة والتمايز البشرة اللاحقة تتأخر في جروح الجلد السكري.
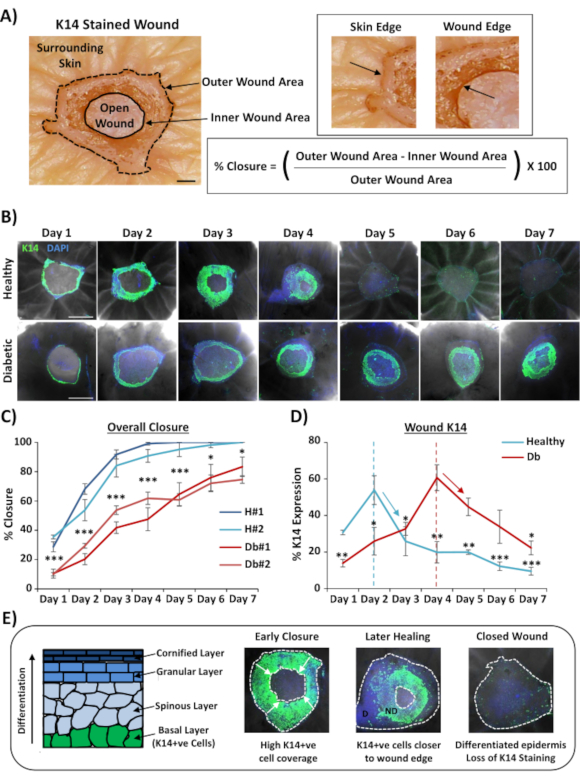
الشكل 2: تلطيخ كامل جبل يكشف عن معدلات الشفاء المضطربة في الجلد السكري مقابل صحة. (أ) الطريقة المستخدمة لقياس إغلاق الجرح من قياسات الجرح الخارجي والداخلي. تظهر صور برايتفيلد الكيراتين 14 (K14) تلطيخ باللون الأحمر. شريط = 300 ميكرومتر. (ب) صور تمثيلية للشفاء مع مرور الوقت (بعد يوم من الجرح) في الجلد صحية والسكري. شريط = 500 ميكرومتر. DAPI = نواة زرقاء. (ج)تحديد كمي لمعدلات إغلاق الجروح (نسبة إعادة الظهارة) تبين أن الجروح الجسم الحي السابق من الجلد السليم إغلاق أسرع بكثير من الجروح في الجسم الحي السابق من الجلد السكري. H = صحية. Db = السكري. (D) النسبة K14 تلطيخ قمم في وقت سابق في صحة الجلد مقابل السكري ثم ينخفض تمشيا مع زيادة التمايز البشرة (أسفل السهام). (E) K14 (خلية البشرة القاعدية) يتم فقدان تلطيخ كما يميز البشرة. D = متمايزة. ND = غير متمايزة. خطوط منقط أبيض تصور حواف الجرح الداخلية والخارجية. الأسهم البيضاء = اتجاه الترحيل. n = 6 جروح لكل متبرع، في كل نقطة زمنية. متوسط +/- SEM. * = P < 0.05، ** = P < 0.01 و *** = P < 0.001. صحية والسكري مقارنة في كل نقطة وقت الشفاء في C (قيمة P للمقارنة أقل أهمية). التغير الزمني في تلطيخ K14 مقارنة بذروة كل مانح في D. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
استخدمنا التالي تلطيخ كامل جبل لاستكشاف التعبير عن الأنسجة وتوطين علامات أخرى ذات الصلة الجرح في الجلد غير السكري(الشكل 3). جميع الأجسام المضادة المستخدمة وتركيزات عملها متوفرة في جدول المواد. الأوعية الدموية في الجرح المفتوح ملطخة إيجابيا مع ألفا العضلات الملساء أكتين (A-SMA) الأجسام المضادة, تستخدم في تركيبة مع K14 لتحديد حواف البشرة في الصور السلطة أقل (الشكل 3A). كانت المصفوفة الجلدية ملطخة بالأجسام المضادة ضد نوع الكولاجين الأول (COL 1) وفيبروكتين (Fn). هنا لوحظ الكولاجين كما وفرة الألياف السميكة في حين كانت ألياف فيبروكتين متناثرة، متموج، ورقيقة(الشكل 3A). لدينا نهج تلطيخ كامل جبل قادر أيضا على توفير قرار مستوى الخلية من تلطيخ، كما هو موضح لK14 إيجابية keratinocytes (الشكل 3B).
وأخيرا، نظهر أن الجروح البشرية في الجسم الحي تمتلك خلايا مناعية مقيمة، مع اكتشاف خلايا لانغرهانز حول البشرة التي تشكلت حديثا في اليوم الثالث بعد الإصابة(الشكل 3C). في الواقع ، تشير هذه النتائج إلى أنه يمكن استخدام تلطيخ التركيب الكامل للتحقيق في السمات الرئيسية للاستجابة العلاجية بما في ذلك الالتهاب والانتشار والمصفوفة خارج الخلية(الشكل 4A). إذا أخذنا معا، تكشف بياناتنا أن إجراء تلطيخ الجلد الجسم الحي المشترك وإجراء تلطيخ التركيب الكامل هو طريقة صالحة لتقييم جوانب مختلفة من إصلاح الجلد البشري الصحي والسكري (المرضي).
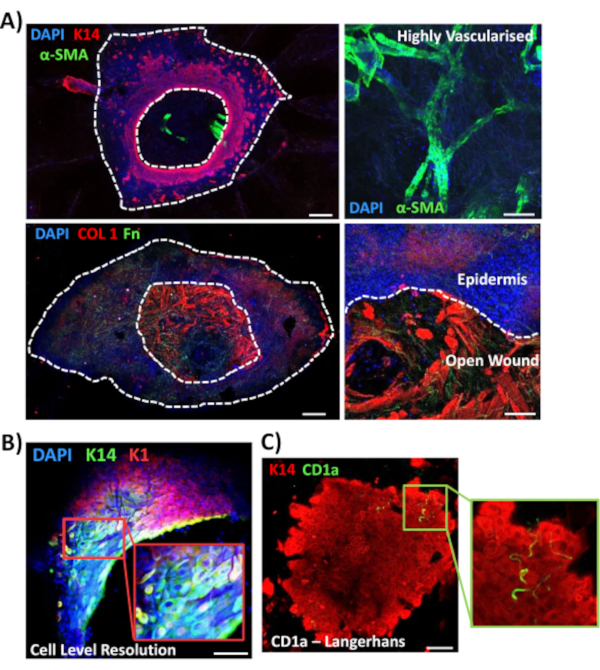
الشكل 3:الأمثل لنهج تلطيخ جبل كامل للاستخدام مع الأجسام المضادة الأخرى. (أ) كانت ملطخة الأوعية الدموية مع ألفا أكتين العضلات الملساء (α-SMA, الأخضر) والكيراتين 14 (K14, أحمر), في حين كانت ملطخة ألياف مصفوفة مع الكولاجين الأول (COL 1, أحمر) وفيبروكتين (Fn, الأخضر). (ب) يوفر إجراء التركيب الكامل دقة مستوى الخلية للتعريب (K14، أخضر؛ K1، أحمر). (C) CD1a + ve خلايا لانغرهانس (الأخضر) لوحظ في البشرة شكلت حديثا. DAPI = نواة زرقاء. شريط = 100 ميكرومتر. خطوط منقط أبيض تظهر حواف الجرح الداخلية والخارجية والجرح منفصلة من البشرة. تم إجراء هذا التلطيخ في الجلد غير السكري. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
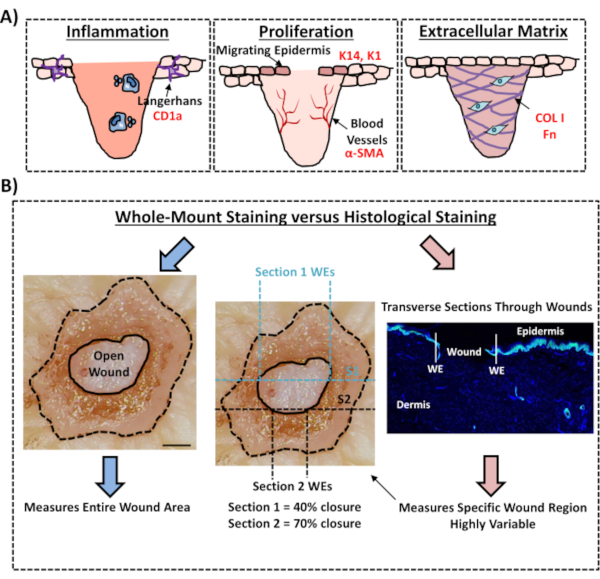
الشكل 4: صلاحية إجراء تلطيخ التركيب الكامل لتقييم التئام الجروح. (A) توضيح يوضح كيف يمكن لتقنية تلطيخ التركيب الكامل تقييم العمليات ذات الصلة بالجروح. الأجسام المضادة المستخدمة = النص الأحمر. K14 = الكيراتين 14. COL 1 = الكولاجين 1. Fn = فيبروكتين. (ب)إجراء تلطيخ كامل جبل (الأسهم الزرقاء) يدخل أقل تقلبا لقياسات إغلاق الجرح من التحليل النسيجي القياسية (السهام الحمراء). S1 = القسم 1. نحن = حافة الجرح. شريط = 300 ميكرومتر. تم إجراء هذا التلطيخ في الجلد غير السكري. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
Discussion
في هذا البروتوكول التجريبي، نقوم بوصف طريقة محسنة لتقييم إغلاق الجرح في جلد الجسم الحي الخارجي البشري باستخدام تلطيخ الأنسجة الكاملة التركيب. هذا هو مورد مهم للسماح بإجراء تقييم نقدي لعلاجات الجروح المحتملة، وتوفير فهم أفضل للاستجابة لإصلاح الجرح البشري. لقد نشرنا تقييم الشفاء في الجروح الجلد في الجسم الحي السابق12,13, ولكن في هذه التقارير لم يستخدم نهج تلطيخ جبل كامل لقياس إغلاق الجروح. تلطيخ كامل جبل أسهل بكثير ويتطلب خبرة تقنية أقل من علم الأنسجة القياسية، والذي ينطوي على البارافين أو أكتوبر تضمين وتقسم العينات. كما يقلل إجراء التركيب الكامل من التباين التجريبي، مما يسمح بتحديد كمي للجرح بأكمله وليس مجرد مقطع عرضي واحد في موضع محدد داخل الأنسجة (انظر الشكل 4B للحصول على توضيح مقارن). ونحن نؤيد تماما أهمية تحديد كميا الشفاء من كامل بنية الجرح غير متناظرة، كما هو موضح بوضوح من قبل ريا ودونوالد للجروح الحادة مورين14. أظهر هؤلاء المؤلفون أهمية القسمة المتسلسلة في الجروح الطاردة في الجسم الحي للقياسات القابلة للاستنساخ والدقيقة لمورفولوجيا الجروح. ويمكن تطبيق الأقسام المتسلسلة على الجروح البشرية في الجسم الحي؛ ومع ذلك ، من أجل التحديد الكمي الدقيق لإغلاق الجرح وإعادة الظهارة ، يجب أن يكون تلطيخ التركيب الكامل عالي الإنتاجية هو الطريقة المفضلة. نلاحظ أن هذا البروتوكول تلطيخ كامل جبل ينبغي أيضا أن تكون متوافقة مع المعالجة اللاحقة (الشمع أو أكتوبر) للتحليل النسيجي التقليدي.
تلطيخ كامل جبل لا يخلو من العيوب. في حين أنه يوفر أعلى استنساخ في تجارب التئام الجروح، فإنه لا يتطلب استخدام المزيد من الأنسجة للتحليل من التقنيات النسيجية القياسية. قد تكون هذه مشكلة حيث يكون الوصول إلى الأنسجة محدودا ، خاصة عندما تحتاج الأجسام المضادة المتعددة إلى تقييم. وهناك نهج بديل هو استخدام طريقة الجرح شقي حيث عرض الجرح موحدة نسبيا ويتم تقليل التباين (كما هو مبين في الماوس والجروح البشرية15،16). ومع ذلك ، تظل الجروح الإستئصالية أكثر قابلية للتطبيق على معظم أنواع الجروح المرضية17.
في هذه الدراسة، تم إنشاء 2 مم جروح سمك جزئي داخل مركز 6 ملم الجلد explants. قد يكون الأمثل لهذه الطريقة للجرح استئصالي بديل وأحجام explant في أعماق الجلد المختلفة18. بالإضافة إلى ذلك، فإن القوة المطلوبة لتوليد الجروح تختلف بين المتبرعين، حيث تتطلب البشرة المسنة قوة أقل للخزعة. ونحن أيضا تجنب استخدام الجلد عرض علامات التمدد البارزة أو غيرها من التعديلات الهيكلية. لقد قمنا بالتحقق من صحة مجموعة من الأجسام المضادة للنظر في جوانب مختلفة من استجابة الشفاء في الجسم الحي السابق. ويمكن أيضا استخدام هذا البروتوكول مع الأجسام المضادة الأخرى ذات الصلة بالبشرة، حيث يجب تحسين تركيزات الأجسام المضادة وأوقات الحضانة. ومع ذلك، نعتقد أن بروتوكولنا هو الأنسب للقياس الكمي المطلق للإغلاق الكلي للجروح، يليه التقييم المكاني لبروتينات محددة ذات أهمية. في حين أن التركيب الكامل يوفر دقة منخفضة من تحديد المواقع المناعية مقابل التحليل النسيجي القياسي لأقسام الأنسجة ، فإنه يوفر معلومات ثلاثية الأبعاد إضافية مفقودة من الأنسجة ثنائية الأبعاد القياسية.
تحذير واحد من تقييم الشفاء في الجلد السابق في الجسم الحي مقابل في نماذج الجسم الحي هو أنه يفتقر إلى استجابة الجهازية. جانب مهم من إصلاح الجرح هو التهاب وتحبيب الأنسجة اللاحقة ، والذي يسببه تدفق الخلايا الالتهابية والخلايا البطانية من الأوعيةالدموية 19. على الرغم من هذا القيد، لا يزال الجلد الحي السابق يوفر خلاصة أفضل للشفاء السريري من فحوصات الجروح القائمة على الخلايا. في المختبر التجارب بشكل عام تنطوي على نوع وحيد من الخلايا أو الثقافات المشتركة التي تزرع على البلاستيك زراعة الأنسجة، في حين أن الجلد السابق فيفو يوفر بيئة أصلية لاستكشاف سلوك الخلية. وفي الآونة الأخيرة، ظهر عدد من أنظمة مكافئة للبشرة، حيث تزرع البشرة في بيئة مختبرية من مصفوفة اصطناعية وخلايا جلدية معزولة20و21. على الرغم من أن هذه النماذج تحاكي الجلد البشري أفضل من معظم النهج في المختبر، فإنها لا تزال لا تحاكي تماما بيئة الأنسجة الأصلية وعموما هشة جدا لإصابة استنساخ. بالإضافة إلى ذلك، نحن (وآخرون) قد أظهرت أن ex vivo أنسجة الجلد البشري يحتفظ الخلايا المناعية المقيمة، والتي لا شك في أن تسهم في إصلاح22،23. وينبغي أن يركز العمل في المستقبل الآن على توسيع نطاق صلاحية ونموذج الجسم الحي السابق للتغلب على الشفاء في المراحل المتأخرة24. أحد الخيارات هو زيادة تقدم تقنيات الجهاز على رقاقة الواعدة القادرة على إطالة صلاحية الأنسجة والحفاظ على بنية الجلد الأصلية لمدة تصل إلى أسبوعين في الثقافة25. كما بدأت نماذج الجسم الحي السابق للنظر في أهمية استجابة التهاب الجلد من خلال دمج الخلايا المناعية بنجاح ، مثل العدلات ، في الأنسجة المضيفة26 أو حقن الأنسجة المضيفة بالأجسام المضادة للحصول على رد فعل مناعي27. ونتوقع أن تمهد هذه النتائج الطريق لتطوير أساليب أكثر دقة وقابلية للترجمة في المستقبل.
فائدة رئيسية لاستخدام الجلد السابق في الجسم الحي لقياس إغلاق الجرح هو القدرة على مقارنة معدلات الشفاء في صحية (على سبيل المثال، غير السكري) مقابل المرضية (على سبيل المثال، السكري أو المسنين) الأنسجة. هنا أظهرنا أن إعادة الظهارة وتشكيل الحاجز تضعف في الواقع في السكري مقابل الجروح الجسم الحي السابق صحية. في الواقع ، يوفر هذا طريقا للتقييم قبل السريري للإصلاح المرضي ، حيث تعد الشيخوخة والسكري عوامل خطر رئيسية لتطوير الجروح المزمنة1. في حين توجد نماذج مرضية في المختبر ، مثل الخلايا المعزولة عن الأنسجة القديمة والسكرية ، أو الخلايا المستزرعة في الجلوكوز العالي لمحاكاة فرط السكر في الدم28،29، يمكن لهذه الخلايا أن تفقد بسرعة النمط الظاهري بمجرد إزالتها من البيئة الدقيقة في الجسم الحي. عنصر مهم من بيئة الشفاء المرضية extrinsic هو مصفوفة الجلد ، والتي يتم تغييرها في كل من الشيخوخة والسكري30. في الواقع ، هذه المصفوفة المضطربة تؤثر على سلوك الخلايا الليفية المقيمة والسذاجة31،32. وبالتالي، لا يمكن التقليل من أهمية دراسة الخلايا في بيئة الأنسجة المضيفة.
باختصار، يوفر بروتوكولنا منصة مهمة لقياس إعادة ظهارة الجرح البشري، واستكشاف العوامل التنظيمية واختبار صحة وفعالية العلاجات المحتملة12و13. في حين أن الاختبارات قبل السريرية لا تزال تتطلب في نهج الجسم الحي، واستراتيجية مشتركة باستخدام الأنسجة البشرية في الجسم الحي السابق والجرح في الجسم الحي مورين ينبغي صقل المسار قبل السريرية، والحد من استخدام الحيوانات مع زيادة قابلية الترجمة عبر الأنواع.
Disclosures
ولا يعلن صاحبا البلاغ عن وجود تضارب في المصالح.
Acknowledgements
نود أن نشكر السيد باولو ماتيوسي والسيد جورج سميث لتوفير الأنسجة المريضة. كما أننا ممتنون للآنسة أمبر روز ستافورد لمساعدتها في جمع الأنسجة ونداء ديزي لتوفير مرافق المختبر.
Materials
| Name | Company | Catalog Number | Comments |
| 50 mL Falcon Tubes | Falcon | 352070 | For skin washing |
| 1.5 ml TubeOne Microcentrifuge Tubes, Natural (Sterile) | Starlab | S1615-5510 | For whole-mount staining |
| 48-Well CytoOne Plate, TC-Treated | Starlab | CC7682-7548 | For whole-mount staining |
| Acetic Acid Glacial | Fisher Chemical | A/0400/PB15 | Part of fixative |
| Alkyltrimethylammonium Bromide | Sigma-Aldrich | M7635 | Part of fixative |
| Anti-Alpha Smooth Muscle Actin Antibody [1A4] | Abcam | ab7817 | Stains blood vessels |
| Anti-Collagen I Antibody | Abcam | ab34710 | Stains collagen |
| Anti-Cytokeratin 14 Antibody [LL002] | Abcam | ab7800 | Stains epidermis |
| CD1A Antibody (CTB6) | Santa Cruz Biotechnology | sc-5265 | Stains Langerhans cells |
| DAPI (4',6-diamidino-2-phenylindole, dihydrochloride) | Thermo Fisher Scientific | 62247 | Counterstain for cell nuclei |
| Falcon 60mm Petri dishes | Falcon | 353004 | Human ex vivo culture |
| Fibronectin Antibody (EP5) | Santa Cruz Biotechnology | sc-8422 | Stains fibronectin |
| Formaldehyde, Extra Pure, Solution 37-41%, SLR | Fisher Chemical | F/1501/PB17 | Part of fixative |
| Gauze Swabs | Medisave | CS1650 | To clean skin |
| Gibco™ Antibiotic-Antimycotic Solution | Thermo Fisher Scientific | 15240062 | Human ex vivo culture |
| Gibco DMEM, high glucose, no glutamine | Thermo Fisher Scientific | 11960044 | Human ex vivo culture |
| Gibco Fetal Bovine Serum | Thermo Fisher Scientific | 10500064 | Human ex vivo culture |
| Gibco HBSS, no calcium, no magnesium | Thermo Fisher Scientific | 14170088 | Human ex vivo culture |
| Gibco L-Glutamine (200 mM) | Thermo Fisher Scientific | 25030081 | Human ex vivo culture |
| Hydrogen Peroxide | Sigma-Aldrich | H1009-100ML | For immunoperoxidase staining |
| ImageJ Software | National Institutes of Health | N/A | For image analysis |
| Invitrogen IgG (H+L) Cross-Adsorbed Goat anti-Mouse, Alexa Fluor 488 | Thermo Fisher Scientific | A11001 | Secondary antibody used depends on required fluorochromes and primary antibody |
| Invitrogen IgG (H+L) Cross-Adsorbed Goat anti-Rabbit, Alexa Fluor 594 | Thermo Fisher Scientific | A11012 | Secondary antibody used depends on required fluorochromes and primary antibody |
| Invitrogen LIVE/DEAD Viability/Cytotoxicity Kit, for mammalian cells | Thermo Fisher Scientific | L3224 | For viability assessment of tissue |
| Iris Forceps, 10 cm, Curved, 1x2 teeth | World Precision Instruments | 15917 | To create wounds |
| Iris Scissors, 11 cm, Curved, SuperCut, Tungsten Carbide | World Precision Instruments | 501264 | To create wounds |
| Iris Scissors, 11 cm, Straight, SuperCut, Tungsten Carbide | World Precision Instruments | 501263 | To remove adipose tissue |
| Keratin 1 Polyclonal Antibody, Purified | Biolegend | 905201 | Stains epidermis |
| Keratin 14 Polyclonal Antibody, Purified | Biolegend | 905301 | Stains epidermis |
| LSM 710 Confocal Laser Scanning Microscope | Carl Zeiss | Discontinued | For fluorescent imaging |
| Merck Millipore Absorbent pads | Merck Millipore | AP10045S0 | Human ex vivo culture |
| Merck Millipore Nylon Hydrophilic Membrane Filters | Merck Millipore | HNWP04700 | Human ex vivo culture |
| Normal Goat Serum Solution | Vector Laboratories | S-1000-20 | Animal serum used depends on secondary antibody |
| Phosphate Buffer Solution | Sigma-Aldrich | P3619 | For wash buffer |
| Sodium Azide | Sigma-Aldrich | S2002 | For blocking buffer |
| Sodium Chloride | Fisher Bioreagents | BP358-212 | Part of fixative |
| Sterilisation Pouches | Medisave | SH3710 | To sterilise instruments |
| Stiefel 2mm biopsy punches | Medisave | BI0500 | For partial thickness wound |
| Stiefel 6mm biopsy punches | Medisave | BI2000 | For outer explant |
| Thermo Scientific Sterilin Standard 90mm Petri Dishes | Thermo Fisher Scientific | 101VR20 | To prepare skin |
| Triton X-100 | Fisher Chemical | T/3751/08 | For wash buffer |
| VECTASTAIN Elite ABC-HRP Kit, Peroxidase (Rabbit IgG) | Vector Laboratories | PK-6101 | For immunoperoxidase staining; HRP kit used depends on primary antibody |
| Vector NovaRED Substrate Kit, Peroxidase (HRP) | Vector Laboratories | SK-4800 | For immunoperoxidase staining |
| Wireless Digital Microscope | Jiusion | N/A | For brightfield imaging |
References
- Lindholm, C., Searle, R. Wound management for the 21st century: combining effectiveness and efficiency. International Wound Journal. 13, 5-15 (2016).
- Guest, J. F., et al. Health economic burden that different wound types impose on the UK's National Health Service. International Wound Journal. 14 (2), 322-330 (2017).
- Guest, J. F., Fuller, G. W., Vowden, P. Diabetic foot ulcer management in clinical practice in the UK: costs and outcomes. International Wound Journal. 15 (1), 43-52 (2018).
- López-Valverde, M. E., et al. Perioperative and long-term all-cause mortality in patients with diabetes who underwent a lower extremity amputation. Diabetes Research and Clinical Practice. 141, 175-180 (2018).
- Wilkinson, H. N., Hardman, M. J. The role of estrogen in cutaneous ageing and repair. Maturitas. 103, 60-64 (2017).
- Frykberg, R. G., Banks, J. Challenges in the treatment of chronic wounds. Advances in Wound Care. 4 (9), 560-582 (2015).
- Wilkinson, H. N., Hardman, M. J. Wound healing: cellular mechanisms and pathological outcomes. Open Biology. 10 (9), 200223 (2020).
- Ansell, D. M., Holden, K. A., Hardman, M. J. Animal models of wound repair: Are they cutting it. Experimental Dermatology. 21 (8), 581-585 (2012).
- Elliot, S., Wikramanayake, T. C., Jozic, I., Tomic-Canic, M. A modeling conundrum: murine models for cutaneous wound healing. Journal of Investigative Dermatology. 138 (4), 736-740 (2018).
- Mazio, C., et al. Pre-vascularized dermis model for fast and functional anastomosis with host vasculature. Biomaterials. 192, 159-170 (2019).
- Wilkinson, H. N., Iveson, S., Catherall, P., Hardman, M. J. A novel silver bioactive glass elicits antimicrobial efficacy against Pseudomonas aeruginosa and Staphylococcus aureus in an ex vivo skin wound biofilm model. Frontiers in Microbiology. 9, 1450 (2018).
- Wilkinson, H. N., et al. Elevated local senescence in diabetic wound healing is linked to pathological repair via CXCR2. Journal of Investigative Dermatology. 139 (5), 1171-1181 (2019).
- Wilkinson, H. N., et al. Tissue iron promotes wound repair via M2 macrophage polarization and the chemokine (CC motif) ligands 17 and 22. The American Journal of Pathology. 189 (11), 2196-2208 (2019).
- Rhea, L., Dunnwald, M. Murine excisional wound healing model and histological morphometric wound analysis. Journal of Visualized Experiments. 162, e61616 (2020).
- Ansell, D. M., Campbell, L., Thomason, H. A., Brass, A., Hardman, M. J. A statistical analysis of murine incisional and excisional acute wound models. Wound Repair and Regeneration. 22 (2), 281-287 (2014).
- Rizzo, A. E., Beckett, L. A., Baier, B. S., Isseroff, R. R. The linear excisional wound: an improved model for human ex vivo wound epithelialization studies. Skin Research and Technology. 18 (1), 125-132 (2012).
- Olsson, M., et al. The humanistic and economic burden of chronic wounds: a systematic review. Wound Repair and Regeneration. 27 (1), 114-125 (2019).
- Mendoza-Garcia, J., Sebastian, A., Alonso-Rasgado, T., Bayat, A. Optimization of an ex vivo wound healing model in the adult human skin: Functional evaluation using photodynamic therapy. Wound Repair and Regeneration. 23 (5), 685-702 (2015).
- Brownhill, V. R., et al. Pre-clinical assessment of single-use negative pressure wound therapy during in vivo porcine wound healing. Advances in Wound Care. , (2020).
- Diekmann, J., et al. A three-dimensional skin equivalent reflecting some aspects of in vivo aged skin. Experimental Dermatology. 25 (1), 56-61 (2016).
- Vidal Yucha, S. E., Tamamoto, K. A., Nguyen, H., Cairns, D. M., Kaplan, D. L. Human skin equivalents demonstrate need for neuro-immuno-cutaneous system. Advanced Biosystems. 3 (1), 1800283 (2019).
- Dijkgraaf, F. E., et al. Tissue patrol by resident memory CD8+ T cells in human skin. Nature Immunology. 20 (6), 756-764 (2019).
- He, X., de Oliveira, V. L., Keijsers, R., Joosten, I., Koenen, H. J. Lymphocyte isolation from human skin for phenotypic analysis and ex vivo cell culture. Journal of Visualized Experiments. (110), e52564 (2016).
- Pupovac, A., et al. Toward immunocompetent 3D skin models. Advanced Healthcare Materials. 7 (12), 1701405 (2018).
- Ataç, B., et al. Skin and hair on-a-chip: in vitro skin models versus ex vivo tissue maintenance with dynamic perfusion. Lab on a Chip. 13 (18), 3555-3561 (2013).
- Kim, J. J., et al. A microscale, full-thickness, human skin on a chip assay simulating neutrophil responses to skin infection and antibiotic treatments. Lab on a Chip. 19 (18), 3094-3103 (2019).
- Jardet, C., et al. Development and characterization of a human Th17-driven ex vivo skin inflammation model. Experimental Dermatology. 29 (10), 993-1003 (2020).
- Chen, J. L., et al. Metformin attenuates diabetes-induced tau hyperphosphorylation in vitro and in vivo by enhancing autophagic clearance. Experimental Neurology. 311, 44-56 (2019).
- Demirovic, D., Rattan, S. I. Curcumin induces stress response and hormetically modulates wound healing ability of human skin fibroblasts undergoing ageing in vitro. Biogerontology. 12 (5), 437-444 (2011).
- Wilkinson, H. N., Hardman, M. J. Wound senescence: A functional link between diabetes and ageing. Experimental Dermatology. 30 (1), 68-73 (2020).
- Fisher, G. J., et al. Collagen fragmentation promotes oxidative stress and elevates matrix metalloproteinase-1 in fibroblasts in aged human skin. The American Journal of Pathology. 174 (1), 101-114 (2009).
- Quan, T., Little, E., Quan, H., Voorhees, J. J., Fisher, G. J. Elevated matrix metalloproteinases and collagen fragmentation in photodamaged human skin: impact of altered extracellular matrix microenvironment on dermal fibroblast function. Journal of Investigative Dermatology. 133 (5), 1362 (2013).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved