Method Article
التصوير الكهرومغناطيسي المصدر في تقييم ما قبل الجراحة للأطفال المصابين بالصرع المقاوم للأدوية
In This Article
Summary
نادرا ما يتم تسجيل تخطيط الدماغ المغناطيسي (MEG) وتخطيط كهربية الدماغ عالي الكثافة (HD-EEG) في وقت واحد ، على الرغم من أنهما يقدمان معلومات تأكيدية وتكميلية. هنا ، نوضح الإعداد التجريبي لتسجيل MEG و HD-EEG في وقت واحد ومنهجية تحليل هذه البيانات التي تهدف إلى توطين مناطق الدماغ الصرع والبليغة لدى الأطفال المصابين بالصرع المقاوم للأدوية.
Abstract
بالنسبة للأطفال المصابين بالصرع المقاوم للأدوية (DRE) ، تعتمد حرية النوبات على تحديد واستئصال (أو استئصال / فصل) منطقة الصرع (EZ) مع الحفاظ على مناطق الدماغ البليغة. لذلك ، فإن تطوير طريقة توطين موثوقة وغير جراحية توفر معلومات مفيدة سريريا لتوطين المنطقة الاقتصادية الحيوية أمر بالغ الأهمية لتحقيق نتائج جراحية ناجحة. تم استخدام التصوير الكهربائي والمغناطيسي المصدر (ESI و MSI) بشكل متزايد في التقييم قبل الجراحة لهؤلاء المرضى مما يدل على نتائج واعدة في تحديد مناطق الصرع وكذلك مناطق الدماغ البليغة. علاوة على ذلك ، فإن الجمع بين ESI و MSI في حل واحد ، وهو تصوير المصدر الكهرومغناطيسي (EMSI) ، الذي يتم إجراؤه على تسجيلات تخطيط كهربية الدماغ عالية الكثافة (HD-EEG) وتخطيط الدماغ المغناطيسي (MEG) في وقت واحد ، أظهر دقة توطين مصدر أعلى من أي من الطريقتين وحدهما. على الرغم من هذه النتائج المشجعة ، يتم تنفيذ هذه التقنيات في عدد قليل فقط من مراكز الصرع من الدرجة الثالثة ، ونادرا ما يتم تسجيلها في وقت واحد ، ويتم استخدامها بشكل غير كاف في مجموعات الأطفال. توضح هذه الدراسة الإعداد التجريبي لتسجيل بيانات MEG و HD-EEG المتزامنة بالإضافة إلى الإطار المنهجي لتحليل هذه البيانات بهدف تحديد المنطقة المهيجة ومنطقة بداية النوبة ومناطق الدماغ البليغة لدى الأطفال المصابين ب DRE. وبشكل أكثر تحديدا ، يتم تقديم الإعدادات التجريبية من أجل (i) تسجيل وتوطين نشاط الصرع بين الصرع و ictal أثناء النوم و (ii) تسجيل الاستجابات البصرية والحركية والسمعية والحسية الجسدية ورسم خرائط لمناطق الدماغ البليغة ذات الصلة (أي البصرية والحركية والسمعية والحسية الجسدية) أثناء المهمة الحركية البصرية ، وكذلك المحفزات السمعية والحسية الجسدية. يتم تقديم الخطوات التفصيلية لخط أنابيب تحليل البيانات لأداء EMSI بالإضافة إلى ESI و MSI الفردية باستخدام ثنائي القطب الحالي المكافئ (ECD) ورسم الخرائط البارامترية الإحصائية الديناميكية (dSPM).
Introduction
الصرع هو واحد من أكثر الاضطرابات العصبية شيوعا وتعطيلا والتي تتميز بنوبات متكررة وغير مبررة يمكن أن تكون إما بؤرية أو معممة بطبيعتها. على الرغم من توفر العديد من العلاجات الدوائية الفعالة (على سبيل المثال ، الأدوية المضادة للنوبات [ASMs]) ، فإن حوالي 20-30٪ من هؤلاء المرضى غير قادرين على التحكم في نوباتهم ويعانون من الصرع المقاوم للأدوية (DRE) 1. بالنسبة لهؤلاء المرضى ، فإن جراحة الصرع هي العلاج الأكثر فعالية للقضاء على النوبات. يمكن تحقيق عملية جراحية ناجحة من خلال الاستئصال الكامل (أو الاستئصال / الانفصال) لمنطقة الصرع (EZ) ، والتي تعرف بأنها الحد الأدنى من المساحة التي لا غنى عنها لتوليد النوبات2. يعد التحديد الدقيق والاستئصال (أو الاستئصال / الانفصال) لمنطقة EZ مع الحفاظ على القشرة البليغة من العوامل الحاسمة في ضمان حرية النوبة. لإثبات الترشيح الجراحي ، يتم استخدام العديد من أدوات التشخيص غير الباضعة من قبل فريق متعدد التخصصات لتحديد المناطق القشرية المختلفة (أي المنطقة المهيجة ، ومنطقة بداية النوبة [SOZ] ، ومنطقة العجز الوظيفي ، والآفة المسببة للصرع) ، والتي تعمل كتقريبيات غير مباشرة ل EZ3. مطلوب مراقبة خارج الجراحة مع EEG داخل الجمجمة (iEEG) عندما لا تحدد أي من هذه الطرق بشكل لا لبس فيه EZ. يتمثل دور iEEG في تحديد EZ بدقة من خلال توطين SOZ (أي منطقة الدماغ التي تتولد فيها النوبات السريرية) ورسم خريطة لمناطق الدماغ البليغة. ومع ذلك ، فإنه يمثل قيودا خطيرة بسبب غزوه4،5،6 ، ويوفر تغطية مكانية محدودة ، ويحتاج إلى فرضية توطين واضحة قبلالجراحة 7. نتيجة لذلك ، قد يتم تفويت التركيز الفعلي ومدى SOZ ، مما يؤدي إلى جراحة غير ناجحة. كما يتطلب تفسيره تسجيل نوبات سريرية نمطية متعددة خلال عدة أيام من الاستشفاء ، مما يزيد من فرص حدوث مضاعفات (مثل العدوى و / أو النزيف)5. وبالتالي ، هناك حاجة غير ملباة لتطوير طرق توطين موثوقة وغير جراحية يمكن أن توفر معلومات مفيدة سريريا وتحسن بشكل عام التقييم قبل الجراحة للأطفال الذين يعانون من DRE.
على مدى العقود الماضية ، تم استخدام التصوير الكهربائي والمغناطيسي (ESI و MSI) بشكل متزايد في التقييم قبل الجراحة للمرضى الذين يعانون من DRE لتحديد مناطق الدماغ الصرع وكذلك الوظيفية. على وجه الخصوص ، يسمح ESI و MSI بإعادة بناء المصادر العصبية من التسجيلات غير الباضعة ، مثل EEG عالي الكثافة (HD-EEG) وتخطيط الدماغ المغناطيسي (MEG) ، للمساعدة في توجيه التخطيط الجراحي أو وضع قطب iEEG. يمكن تطبيق ESI و MSI لتوطين إما إفرازات الصرع البينية (IEDs) ، مثل المسامير والموجات الحادة ، أو نشاط ictal (النوبة). يمكن استخدامه أيضا لتوطين مناطق الدماغ الوظيفية المختلفة المشاركة في الوظائف الحسية والحركية والسمعية والمعرفية. تسمح إعادة بناء الأحداث الفيزيولوجية الكهربية ، مثل العبوات الناسفة والنوبات ، بتحديد المنطقة المهيجة (أي منطقة الدماغ التي تنشأ فيها العبوات الناسفة) و SOZ ، على التوالي ، والتي تعتبر بديلا صالحا لتوطين EZ. يسمح توطين القشرة البليغة (أي مناطق الدماغ التي لا غنى عنها للوظائف القشرية المحددة)3 بدلا من ذلك بتعيين موقع ومدى المناطق البليغة فيما يتعلق بالاستئصال المخطط له ، وبالتالي تقليل العجز الوظيفي المحتمل مسبقا الذي يمكن توقعه من جراحة الصرع8،9،10،11. بحثت العديد من الدراسات في الفائدة السريرية ل ESI و / أو MSI في التقييم قبل الجراحة للصرع ، وأظهرت نتائج واعدة في تحديد EZ12،13،14،15،16،17،18،19. على سبيل المثال ، أجرى Mouthaan et al.14 تحليلا تلويا مكثفا باستخدام بيانات غير جراحية ل 11 دراسة صرع مستقبلية وبأثر رجعي وأفاد أن تقنيات توطين المصدر هذه يمكنها بشكل عام تحديد EZ بحساسية عالية (82٪) وخصوصية منخفضة (53٪). أظهرت دراسات أخرى أيضا أن MSI و ESI يمكنهما تحديد تركيز الصرع بشكل صحيح داخل المنطقة المقطوعة في مرضى الصرع الذين لديهم تصوير بالرنين المغناطيسي الطبيعي (MRI)19،20،21. تعتبر نتائج التوطين هذه مهمة بشكل خاص لأولئك المرضى غير المؤهلين لجراحة الصرع بسبب النتائج السريرية أو التصويرية غير الحاسمة. باختصار ، يمكن أن يساهم ESI و MSI بشكل كبير في رسم خرائط ما قبل الجراحة لمناطق الدماغ الصرعية وكذلك الوظيفية في المرضى الذين يعانون من DRE.
على الرغم من هذه النتائج المشجعة ، يتم تنفيذ هذه التقنيات حاليا في عدد قليل فقط من مراكز الصرع من الدرجة الثالثة على أساس منتظم وغالبا ما يتم استخدامها بشكل غير كاف في مجموعات الأطفال. علاوة على ذلك ، نادرا ما يتم تسجيل HD-EEG و MEG في وقت واحد ، على الرغم من أنهما يوفران معلومات تأكيدية وتكميلية. MEG حساس للكشف عن المصادر السطحية ذات الاتجاه العرضي ولكنه أعمى عن المصادر ذات التوجه الشعاعي الموجودة في الدوران أو المناطق العميقة من الدماغ22،23،24،25،26. علاوة على ذلك ، يوفر MEG دقة مكانية أفضل (ملليمترات) مقارنة ب EEG16،22،25. على عكس إشارات EEG ، فإن إشارات MEG خالية من المراجع ولا تتأثر بشكل أساسي بالتوصيلات المختلفة لأنسجة المخ (أي السحايا والسائل النخاعي والجمجمة وفروة الرأس)25,27 مما يوفر قياسات غير مشوهة للمجالات المغناطيسية التي ينتجها الدماغ. من ناحية أخرى ، يمكن ل EEG اكتشاف مصادر جميع الاتجاهات ، لكنه يوفر دقة مكانية أقل من MEG وهو أكثر عرضة للقطع الأثرية26,28. بسبب هذه الحساسيات التكميلية لاتجاه المصدر وعمقه ، لا يمكن تسجيل ما يقرب من 30٪ من نشاط الصرع (على سبيل المثال ، العبوات الناسفة) إلا على MEG ولكن ليس على EEG ، والعكس صحيح26،29،30،31،32. على عكس EEG ، الذي يسمح بالتسجيلات المطولة ، فإن التقاط النوبات السريرية باستخدام MEG يمثل تحديا بسبب وقت التسجيل المحدود الذي عادة ما يكون غير كاف لتسجيل أحداث ictal في معظم المرضى. علاوة على ذلك ، يمكن أن تتداخل القطع الأثرية الناتجة عن حركات الرأس المرتبطة بالنوبات في كثير من الأحيان مع جودة تسجيلات MEG29،33،34،35. من ناحية أخرى ، تعد تسجيلات MEG أسرع وأسهل مقارنة ب EEG ، خاصة عند الأطفال حيث لا توجد حاجة لتوصيل أجهزة استشعار فوق رأس الأطفال35.
جعلت التطورات في الأجهزة من الممكن تسجيل بيانات MEG و HD-EEG في وقت واحد مع عدد كبير من أجهزة الاستشعار (أكثر من 550 جهاز استشعار) تغطي الرأس بالكامل. علاوة على ذلك ، أدت التطورات الحديثة في تقنيات EEG إلى تقليل وقت التحضير ل HD-EEG إلى أقل من ربع ساعة36. هذا مهم بشكل خاص للأطفال ذوي السلوكيات الصعبة غير القادرين على البقاء ثابتين لفترات طويلة. علاوة على ذلك ، سمحت التطورات في تقنيات البرمجيات بدمج ESI و MSI في حل واحد ، وهو تصوير المصدر الكهرومغناطيسي (EMSI) ، الذي يتم إجراؤه على تسجيلات HD-EEG و MEG المتزامنة. أفادت العديد من الدراسات النظرية والتجريبية عن دقة توطين مصدر أعلى مع EMSI من أي من الطريقتين وحدهما13،30،31،37،38،39،40،41. باستخدام مناهج توطين المصادر المختلفة لإعادة بناء النشاط استجابة للمحفزات الحسية ، شارون وآخرون.وجد 37 أن EMSI كان لديه نتائج توطين أفضل باستمرار من ESI أو MSI وحده مقارنة بالتصوير بالرنين المغناطيسي الوظيفي (fMRI) ، والذي يعمل كمعيار غير جراحي لدقة التوطين الدقيقة. اقترح المؤلفون أن هذا التوطين المحسن يرجع إلى زيادة عدد أجهزة الاستشعار لحل الحل العكسي وأنماط الحساسية المختلفة لطريقتي التصوير37. وبالمثل، فإن يوشيناغا وآخرين.أجرى 31 تحليلا ثنائي القطب على بيانات EEG و MEG المتزامنة للمرضى الذين يعانون من الصرع المرتبط بالتوطين المستعصي وأظهروا أن EMSI قدمت معلومات لا يمكن الحصول عليها باستخدام طريقة واحدة فقط وأدت إلى توطين ناجح لجراحة الصرع في أحد المرضى الذين تم تحليلهم. في دراسة مستقبلية عمياء ، Duez et al.أظهر 13 أن EMSI حققت نسبة احتمالات أعلى بكثير (أي احتمال أن تصبح خالية من النوبات) مقارنة ب ESI و MSI ، ودقة توطين ≥52٪ ، وتوافق ≥53٪ و ≥36٪ مع التهيج و SOZ ، على التوالي. أظهرت دراسة أحدث من مجموعتنا42 أن EMSI قدمت تقديرات توطين متفوقة وأداء أفضل للتنبؤ بالنتائج من ESI أو MSI وحدهما ، مع أخطاء توطين من الاستئصال و SOZ ~ 8 مم و ~ 15 مم ، على التوالي. على الرغم من هذه النتائج الواعدة ، هناك نقص في الدراسات التي توفر الإطار المنهجي فيما يتعلق ب EMSI في الأطفال الذين يعانون من DRE.
توضح هذه الدراسة الإعداد التجريبي لإجراء تسجيلات MEG و HD-EEG المتزامنة بالإضافة إلى الإطار المنهجي لتحليل هذه البيانات بهدف توطين المنطقة المهيجة و SOZ ومناطق الدماغ البليغة لدى الأطفال المصابين ب DRE. وبشكل أكثر تحديدا ، يتم تقديم الإعدادات التجريبية من أجل (i) تسجيل وتوطين نشاط الصرع بين الصرع و ictal أثناء النوم و (ii) تسجيل الاستجابات البصرية والحركية والسمعية والحسية الجسدية ورسم خرائط لمناطق الدماغ البليغة ذات الصلة (أي البصرية والحركية والسمعية والحسية الجسدية) أثناء مهمة حركية بصرية ، بالإضافة إلى المحفزات السمعية والحسية الجسدية. يتم تقديم الخطوات التفصيلية لخط أنابيب تحليل البيانات لأداء EMSI بالإضافة إلى ESI و MSI الفردية باستخدام ثنائي القطب الحالي المكافئ (ECD) ورسم الخرائط البارامترية الإحصائية الديناميكية (dSPM).
Protocol
تمت الموافقة على الإجراءات التجريبية المطبقة هنا من قبل مجلس المراجعة المؤسسية الإقليمي لشمال تكساس (2019-166; الباحث الرئيسي: كريستوس باباديليس). سيصف القسم التالي البروتوكول التجريبي لتوطين المصدر غير الباضع للعبوات الناسفة المرتجلة ، وبدايات ictal ، والاستجابات التي تثيرها الأحداث (أي البصرية والحركية والسمعية والحسية الجسدية) باستخدام تسجيلات MEG و HD-EEG المتزامنة المتبعة في مختبرنا. قدم الاتحاد الدولي للفيزيولوجيا العصبية السريرية43 وجمعية MEG السريريةالأمريكية 44 "الحد الأدنى من المعايير" للتسجيل السريري الروتيني وتحليل بيانات MEG و EEG التلقائية. تنطبق إجراءات تسجيلات HD-EEG الموضحة هنا فقط على أنظمة أقطاب EEG القائمة على الإسفنج. تستغرق عملية الإعداد الشاملة لكل موضوع حوالي 2-3 ساعات ، وتشمل التسجيلات الفعلية ل ~ 1.5 ساعة.
1. إعداد نظام MEG
- قبل وصول الهدف ، قم بإجراء تسجيل MEG في غرفة فارغة لبضع دقائق لالتقاط مستويات ضوضاء الخلفية والتحف المغناطيسية وتحقق من أن جميع مستشعرات MEG تعمل بشكل صحيح.
- باستخدام برنامج ضبط مستشعرات MEG ، تأكد من أن متوسط قيمة الضوضاء البيضاء لجميع مستشعرات MEG يتراوح بين 2 و 5 fT / √ هرتز (fT / cm√ Hz لمقاييس التدرج).
2. إعداد الموضوع
- تأكد من أن الموضوع مريح مع البيئة. في حالة الأطفال الصغار ، اسمح لهم باستكشاف غرفة التسجيل (بما في ذلك الغرفة المحمية مغناطيسيا [MSR]) ورؤية معدات الاختبار التي سيتم استخدامها للحصول على البيانات.
- فحص وتقديم تعليمات الموضوع باستخدام نموذج موافقة الفحص. إذا لزم الأمر ، اشرح الإجراء للأطفال الصغار باستخدام كلمات خاصة وألعاب وألعاب تم تطويرها لكل فئة عمرية. اسأل الموضوع (أو والدي الموضوع) عما إذا كان قد أصيب بنوبة صرع خلال آخر ~ 2 ساعة قبل الزيارة.
ملاحظة: يتضمن نموذج موافقة الفحص وصفا للاختبار ، بالإضافة إلى سلامته ، وسبب إجراء الاختبار ، ووصفا شاملا للدراسة.
- فحص وتقديم تعليمات الموضوع باستخدام نموذج موافقة الفحص. إذا لزم الأمر ، اشرح الإجراء للأطفال الصغار باستخدام كلمات خاصة وألعاب وألعاب تم تطويرها لكل فئة عمرية. اسأل الموضوع (أو والدي الموضوع) عما إذا كان قد أصيب بنوبة صرع خلال آخر ~ 2 ساعة قبل الزيارة.
- قم بإزالة أي مواد معدنية و / أو مغناطيسية من الموضوع وزود الشخص بالملابس المناسبة الصادرة عن المستشفى (على سبيل المثال ، عباءات المستشفى ، الدعك). بالإضافة إلى ذلك ، اطلب من الشخص خلع حذائه لمنع الغبار المغناطيسي من دخول MSR. إذا تعذر إزالة العناصر المغناطيسية الحديدية الأخرى ، مثل أعمال طب الأسنان أو الأجهزة الطبية المزروعة ، فاستخدم جهاز إزالة المغنطيسة (أي مزيل المغناطيسية) لإزالة القطع الأثرية المغناطيسية المتبقية التي يمكن أن تسبب تداخلات أو مستويات ضوضاء عالية أثناء تسجيلات MEG. بعد التأكد من إزالة جميع مصادر الضوضاء المغناطيسية ، اطلب من الشخص الجلوس والراحة على كرسي خشبي حيث سيتم تطبيق إجراءات القياس التالية.
ملاحظة: يجب عدم تطبيق جهاز إزالة الغازات مباشرة على أي أجهزة إلكترونية مزروعة (مثل أجهزة تنظيم ضربات القلب وأجهزة التعديل العصبي). - قم بقياس محيط رأس الشخص لتحديد الحجم الصافي المناسب لتخطيط كهربية الدماغ (عادة 32-34 سم حتى 58-61 سم). باستخدام جانب السنتيمتر من شريط القياس ، قم بقياس محيط الرأس عن طريق تثبيت الشريط من ناسيون الموضوع إلى ~ 1 سم فوق الفتحة ثم العودة إلى الكسر.
ملاحظة: ال nasion هو نقطة قياس الجمجمة بين العينين ، في حين أن inion هو طرف النتوء القذالي الخارجي.- حدد الحجم الصافي الصحيح الذي يناسب محيط رأس الشخص وانقعه لمدة 5 دقائق على الأقل (10 دقائق كحد أقصى) في محلول سائل مختلط يتكون من 1 كوارت طن من ماء الصنبور الدافئ ، و 1 ملعقة كبيرة من الإلكتروليتات (أي كلوريد البوتاسيوم) ، و 1 ملعقة كبيرة من شامبو الأطفال. أثناء عملية النقع هذه ، تأكد من قلب الشبكة من الداخل للخارج مع توجيه الإسفنج للخارج وفك المشابك بالكامل لغمر المستشعرات بالكامل داخل الدلو البلاستيكي الذي يحتوي على المحلول.
ملاحظة: للتأكد من أن مضخم الشبكة لا يقترب من المحلول ويظل جافا دائما ، لف منشفة حول قابس الشبكة المحددة ، وإذا كان ذلك مفضلا ، ضعها على كرسي أو دعامة بالقرب من الحوض حيث يوجد الدلو البلاستيكي.
- حدد الحجم الصافي الصحيح الذي يناسب محيط رأس الشخص وانقعه لمدة 5 دقائق على الأقل (10 دقائق كحد أقصى) في محلول سائل مختلط يتكون من 1 كوارت طن من ماء الصنبور الدافئ ، و 1 ملعقة كبيرة من الإلكتروليتات (أي كلوريد البوتاسيوم) ، و 1 ملعقة كبيرة من شامبو الأطفال. أثناء عملية النقع هذه ، تأكد من قلب الشبكة من الداخل للخارج مع توجيه الإسفنج للخارج وفك المشابك بالكامل لغمر المستشعرات بالكامل داخل الدلو البلاستيكي الذي يحتوي على المحلول.
- ضع خمسة ملفات مغناطيسية تعمل كملفات مؤشر موضع الرأس (HPI) في مواقع معروفة مباشرة على فروة رأس الشخص باستخدام شريط ورقي micropore: واحد على كل جانب من الجبهة بالقرب من خط الشعر ، وواحد على كل عظم خشاء ، وواحد على الجزء العلوي من الرأس.
ملاحظة: تحدد ملفات HPI موضع الرأس بالنسبة لأجهزة التداخل الكمي فائقة التوصيل (SQUIDs) الموضوعة داخل نظام MEG عن طريق إصدار مجالات مغناطيسية معروفة يمكن تحديد موقعها أثناء المسح. يعتمد عدد ملفات HPI على نظام MEG ، ولكنه يتراوح عادة من 3-5 ملفات HPI. - وضع أقطاب كهربائية إضافية باستخدام شريط لقياس معدل ضربات القلب (تخطيط القلب الكهربائي ، تخطيط القلب) ، حركات العين أو الوميض (تخطيط كهربية العين ، EOG) ، ونشاط العضلات (تخطيط كهربية العضل ، EMG) ؛ يسمح وضع هذه الأقطاب الكهربائية أيضا بمراقبة الحالة الصحية للموضوع.
- ضع قطبين كهربائيين لتخطيط القلب على الجانب الأيمن والأيسر من الصدر أسفل عظام الترقوة ، على التوالي ، لتسجيل نبضات قلب الشخص ، وقطبين كهربائيين EOG على الجانب العلوي والسفلي من العين اليمنى ، على التوالي ، لتسجيل حركات العين العمودية أو الوميض.
- لقياس نشاط العضلات أثناء المهمة الحركية البصرية ، بالإضافة إلى ذلك ، امسح أصابع الشخص باستخدام ضمادات كحولية لتحسين التصاق الشريط على الجلد وشريط ما مجموعه زوجان من أقطاب الأكواب غير القابلة للتصرف في كل يد: واحد على أول ظهري بين العظام (FDI) والآخر على الخاطف pollicis brevis (APB).
- قبل لصق كل هذه الأقطاب الكهربائية ، ضع العجينة الموصلة داخل كوب القطب الكهربائي حتى تمتلئ قليلا لتقليل مقاومة الجلد وضمان مزيج مثالي من الالتصاق والتوصيل.
- للتحفيز عن طريق اللمس ، قم بتوصيل أغشية مرنة رفيعة مباشرة بالأجزاء البعيدة والفولارية المكونة من ثلاثة أرقام (أي الإبهام [D1] والإصبع الأوسط [D3] والخنصر [D5]) لكلتا اليدين. قم بنفخ الأغشية بنبضات الهواء المضغوط من خلال أنابيب بلاستيكية صلبة باستخدام جهاز تحفيز نفخة الهواء. حرر نبضات الهواء المضغوط بفاصل تحفيز بيني يبلغ 1.5 ± 0.5 ثانية بعد ترتيب شبه عشوائي. اضبط ضغط محفز اللمس على 50 رطل / بوصة مربعة.
- ضع قطبين كهربائيين لتخطيط القلب على الجانب الأيمن والأيسر من الصدر أسفل عظام الترقوة ، على التوالي ، لتسجيل نبضات قلب الشخص ، وقطبين كهربائيين EOG على الجانب العلوي والسفلي من العين اليمنى ، على التوالي ، لتسجيل حركات العين العمودية أو الوميض.
- بينما لا يزال الموضوع جالسا على الكرسي الخشبي بعيدا عن أي جسم معدني ، حدد المواضع ثلاثية الأبعاد (3D) للمعالم التشريحية الائتمانية ، وخمسة ملفات HPI ، ونقاط شكل الرأس الأخرى باستخدام محول رقمي. أثناء عملية رقمنة الرأس هذه ، اطلب من الشخص أن يجلس بشكل مريح ، وينظر إلى الأمام مباشرة ، ويظل بلا حراك تقريبا لأن الحركات الصغيرة قد تؤثر على دقة التوطين.
- ضع جهاز الاستقبال المرجعي من خلال النظارات البلاستيكية (أي النظارات مع المكعب المرجعي المتصل على جانب واحد) على رأس الموضوع واضبط المشابك لضمان إطار مرجعي ثابت للموضوع يجب أن يظل ثابتا نسبيا أثناء القياس بأكمله.
- من خلال مستقبل القلم الأساسي ، حدد المعالم التشريحية الإيمانية (أي نقاط nasion ونقاط preauricular اليسرى / اليمنى) وموضع ملفات HPI ، وقم بأخذ عينات موحدة من نقاط فروة الرأس الإضافية (100 على الأقل ، ويفضل أن تكون قريبة من ~ 500) لتعزيز إعادة بناء عالية الجودة لسطح الرأس.
ملاحظة: تحدد المعالم التشريحية الإيمانية نظام إحداثيات الموضوع. يقوم محول الأرقام بإنشاء إحداثيات جهاز استشعار في مساحة 3D باستخدام جهاز إرسال واحد (يتم تركيبه عادة خلف الموضوع على ظهر الكرسي الخشبي) وجهازي استقبال (أي القلم وأجهزة الاستقبال المرجعية). - بعد اكتمال الرقمنة ، ضع مستقبل القلم ~ 15 سم بعيدا عن الموضوع وجهاز الإرسال وقم برقمنة نقطة عشوائية لإنهاء عملية الرقمنة.
ملاحظة: قد تختلف هذه الخطوة الأخيرة من عملية الرقمنة عن المنتجات التجارية الأخرى.
- قبل تطبيق شبكة تخطيط كهربية الدماغ، اطلب من الشخص الجلوس على كرسي قريب من مضخم EEG ووضع المناشف على صدره وكتفيه لامتصاص القطرات النهائية بسبب تطبيق الشبكة. قم بإزالة شبكة EEG من الدلو البلاستيكي ، وقم بتدويرها بحيث تواجه الإسفنج من الداخل ، ولفها برفق حول منشفة لامتصاص المحلول المختلط الزائد.
- مع جلوس الشخص على الكرسي وتوجيهه لإبقاء عينيه مغلقتين خلال هذه الخطوة ، ضع كلتا يديه داخل الشبكة وانشرها باستخدام الأصابع ، وأخيرا ضعها على رأس الموضوع.
- بدون تحريك مواضع ملفات HPI ، اضبط الشبكة الممتدة على رأس الهدف باستخدام الأصابع للتأكد من وضع القنوات المرجعية والقنوات بشكل صحيح في وسط فروة الرأس وبين عيني الشخص ، على التوالي ، وأخيرا اربط حزام الذقن بمجرد أن تكون الشبكة في الموضع الصحيح.
- باستخدام مقياس مقاومة EEG ، تأكد من أن جميع معاوقة قطب فروة الرأس في نطاق 0-50 kΩ (يوصى بالقيم ˂5 kΩ) لمنع أي تشوهات في الإشارة. لتقليل مقاومة قطب فروة الرأس ، تحقق من أن كل قطب كهربائي لديه اتصال ميكانيكي وكهربائي جيد مع فروة الرأس باستخدام إما قطعة قطن خشبية لإزالة شعر الشخص بين القطب وفروة الرأس أو ماصة بلاستيكية يمكن التخلص منها لنقل محلول مختلط أكثر توصيلا إلى إسفنج الأقطاب الكهربائية إذا لزم الأمر.
- بمجرد أن تصل جميع المعاوقة بشكل مثالي إلى 50 كيلو أوم ، افصل مكبر الصوت وقم بإعداد الموضوع لرقمنة قطب EEG.
ملاحظة: قم بإجراء رقمنة قطب EEG خارج MSR وتأكد من وجود مساحة كافية حول الموضوع لإدارة عملية المسح.
- بمجرد أن تصل جميع المعاوقة بشكل مثالي إلى 50 كيلو أوم ، افصل مكبر الصوت وقم بإعداد الموضوع لرقمنة قطب EEG.
- تحديد مواضع 3D لأقطاب EEG باستخدام ماسح ضوئي محمول باليد. خلال هذه العملية ، اطلب من الشخص أن يجلس بشكل مريح وينظر إلى الأمام مباشرة ما لم يطلب منه خلاف ذلك.
- أولا ، افتح برنامج الماسح الضوئي ، وحدد قالب المستشعر الذي يطابق تخطيط مستشعر EEG المستخدم أثناء التسجيلات ، ثم ابدأ عملية المسح.
- أثناء المسح ، أمسك الماسح الضوئي على مسافة معينة من شبكة EEG (عادة ~ 45 سم) ، مع فتحات المسح العمودية على سطح المستشعرات ، وحركه ببطء حول رأس الهدف باتباع مساحات مقوسة من أعلى (وسط الرأس) إلى أسفل (آخر صف مستشعرات على طول الرقبة) لتسجيل المواقع المادية لجميع المستشعرات.
ملاحظة: يقوم الماسح الضوئي برقمنة مواقع قطب EEG على رأس الموضوع ويحولها كملف إحداثيات 3D ؛ يتميز عادة بمستشعرين بصريين ينبعثان من مصادر ضوء الأشعة تحت الحمراء (IR). يظهر كل موقع ممسوح ضوئيا عادة على سحابة مستشعر 3D. توفر سحابة مستشعر 3D ملاحظات لمسح وفحص ومحاذاة مواضع المستشعر ، بينما توفر خريطة مستشعر 2D ملاحظات لوضع العلامات على مواضع أجهزة الاستشعار هذه. تتطلب عملية المسح لمواضع قطب EEG ما مجموعه 5-10 دقائق ، بما في ذلك فحص النقاط الائتمانية. ومع ذلك ، قد يعتمد وقت المسح أحيانا على أداء الماسح الضوئي في اكتشاف مواضع القطب.
- بمجرد فحص جميع أقطاب EEG (95٪ على الأقل) ، قم بفحص النقاط الائتمانية (أي نقاط nasion و preauricular اليسرى / اليمنى) وأربعة مستشعرات محاذاة (أي عقد محاذاة أمامية ويسرى ويمين وعقدة REF) باستخدام المسبار البصري اللاسلكي لمحاذاة سحابة مستشعرات 3D إلى قالب المستشعر المحدد.
ملاحظة: يتم ترقيم مستشعرات المحاذاة بناء على تكوين شبكة مستشعر EEG.- لفحص النقاط الإيمانية ، ضع طرف المسبار البصري على جلد الهدف في مركز نقطة الاهتمام الائتمانية من خلال التأكد من أن فتحات المسح الضوئي للماسح الضوئي تشير إلى الأقراص العاكسة للمسبار. وبالمثل ، ضع طرف المسبار البصري في وسط مستشعر المحاذاة الذي يهمك لفحص مستشعرات المحاذاة.
- بمجرد فحص جميع أجهزة الاستشعار وفحصها ، قم بمراجعة مواقعها وملصقاتها على سحابة مستشعر 3D وخريطة مستشعر 2D فيما يتعلق بشبكة EEG الفعلية للتحقق من الأخطاء المحتملة وتصحيحها في النهاية ؛ في حالة عدم حدوث أخطاء أثناء عملية المسح ، قم بتصدير ملف .txt الإحداثيات 3D وقم بتحويله إلى التنسيق المفضل.
ملاحظة: عادة ما يتم تخزين إحداثيات القطب 3D بتنسيق .txt ويمكن تحويلها عبر برنامج الماسح الضوئي بتنسيقات متعددة (على سبيل المثال ، .xml أو .sfp أو .elp أو .nsi). - بعد اكتمال عملية رقمنة قطب EEG (الخطوات 2.9-2.11) ، قم بإعداد الموضوع المراد نقله داخل MSR لأداء بيانات الراحة / النوم (الخطوة 2.13) ، والمهمة الحركية البصرية (الخطوة 2.14) ، والتحفيز السمعي (الخطوة 2.15) ، والتحفيز الحسي الجسدي (الخطوة 2.16).
- للحصول على بيانات الراحة / النوم ، اضبط جسر نظام MEG على وضع الاستلقاء (الشكل 1 أ) وقم بترتيب السرير غير المغناطيسي والمتوافق بحيث يتم محاذاة مسند الرأس القابل للإزالة مع الفتحة على شكل خوذة في الجزء السفلي من ديوار. بعد ضبط السرير على الموضع الصحيح ، اضبط صمام الفرامل الخاص بالسرير على وضع إيقاف القفل. ضع ملاءة أو بطانية فوق السرير ووسادة إسفنجية صغيرة على مسند الرأس القابل للإزالة لتثبيت الرأس والراحة أثناء التسجيل.
ملاحظة: الديوار عبارة عن حاوية تخزين مبردة مملوءة بالهيليوم السائل حيث يتم ترتيب صفائف أجهزة الاستشعار مكانيا في الأسفل عبر فتحة على شكل خوذة مصممة لإحاطة رأس الهدف. الخوذة تناسب محيط الرأس حتى 59-61 سم. القنطرة العملاقة هي النظام الميكانيكي الذي يدعم الديوار الذي يسمح بتعديل ارتفاعه وزاويته بناء على موضع القياس (أي جالسا أو مستلقا).- انقل الموضوع داخل MSR وساعده على الجلوس على حافة السرير والاستلقاء عليه. ضع عدة بطانيات على جسم الشخص لإبقائه دافئا أثناء التسجيل من خلال التأكد من سهولة الوصول إلى كابلات الأقطاب الكهربائية ، واربط أحزمة الأمان برفق (أو اسحب السور إذا كان موجودا) ، موضحا للموضوع أن هذه الخطوة هي منعه من التدحرج من السرير أثناء النوم. إذا لزم الأمر ، ضع منشفة ملفوفة إضافية أسفل الرقبة لتوفير الدعم لرقبة الشخص وكتفيه.
- افتح صمام الفرامل الخاص بالسرير لتحريك رأس الهدف برفق ، والذي يتم وضعه على مسند الرأس القابل للإزالة أسفل فتحة الديوار على شكل خوذة حتى يلامس الجزء الداخلي من الخوذة. لزيادة نسبة الإشارة إلى الضوضاء (SNR) ، اجعل رأس الهدف أقرب ما يمكن إلى الخوذة.
- قم بتوصيل ملفات HPI وأقطاب ECG و EOG على اللوحات المقابلة لنظام MEG ، وقم بتوصيل شبكة EEG بوحدة مكبر الصوت داخل MSR ، وتحقق من قياسات إحداثيات الرأس من محطة عمل الاستحواذ خارج MSR لتقييم ما إذا كان رأس الموضوع في وضع مناسب تحت dewar.
- بموافقة الشخص ، قلل من شدة الضوء داخل MSR للمساعدة في تحفيز الاسترخاء والنوم. عندما يشعر الشخص بالاسترخاء والراحة ، اطلب من الشخص أن يستريح وعيناه مغمضتان أو ينام أثناء التسجيل. طمأنة الشخص بأنه سيتم ملاحظته على الشاشة خارج MSR عبر الكاميرا الملونة المحمية بالترددات الراديوية المثبتة على جدار MSR للتسجيل بأكمله.
- بالنسبة للمهمة الحركية البصرية ، اضبط جسر نظام MEG على الوضع الرأسي (الشكل 1 ب) وقم بترتيب كرسي MEG بحيث يكون رأس الموضوع أسفل القنطرة ، بالقرب من الفتحة على شكل خوذة في الجزء السفلي من dewar. بعد ضبط الكرسي على الموضع الصحيح ، اضبط صمام الفرامل للكرسي على وضع إيقاف القفل ("0").
- نقل الموضوع داخل MSR. ساعده على الجلوس على الكرسي غير المغناطيسي والمتوافق وإيجاد وضع مريح ومريح. ضع عدة بطانيات على جسم الشخص لإبقائه دافئا أثناء التسجيل من خلال التأكد من سهولة الوصول إلى كابلات الأقطاب الكهربائية ، وضع الطاولة القابلة للإزالة حتى يتمكن الشخص من وضع يديه عليها أثناء المهمة. إذا لزم الأمر ، ضع منشفة تحت ركبتي الشخص للمساعدة في الحفاظ على وضع الجلوس ، ولا تنزلق لأسفل.
ملاحظة: نظرا لأن الشخص قد يسترخي أثناء المهمة الحركية البصرية ، وبالتالي ، يتخذ وضعا أقل من الوضع الأولي ، ارفع الكرسي بعناية في نهاية كل جلسة مهمة عبر دواسة الارتفاع (إن وجدت) أو ضع المناشف أو البطانيات على الكرسي بحيث يلامس رأس الشخص الجزء الداخلي من الخوذة مرة أخرى. إذا لزم الأمر ، ضع مناشف أو بطانيات إضافية خلف رأس الشخص ليس فقط للحصول على راحة أفضل ولكن أيضا لمساعدة الهدف على إبقاء الرأس مستقيما قدر الإمكان. يمكن إجراء التحفيز الحركي البصري بدلا من ذلك في وضع ضعيف لتجنب تحريك الديوار في منتصف جلسة التسجيل. - بمجرد أن يصبح الهدف في الموضع الصحيح ، قم بتوصيل ملفات HPI ، وأقطاب ECG ، و EOG ، و FDI ، و APB على اللوحة اليمنى لجهاز MEG ، وقم بتوصيل شبكة EEG بوحدة مكبر الصوت داخل MSR ، وارفع الكرسي من خلال دواسة الارتفاع (إن وجدت) بحركات صغيرة أو ضع مناشف أو بطانيات إضافية على الكرسي حتى يلامس رأس الشخص برفق الجزء الداخلي من الخوذة (تحقق من قياسات إحداثيات الرأس من محطة عمل الاستحواذ خارج MSR).
- ضع شاشة العرض ، حيث سيتم عرض المحفزات البصرية عبر نظام مرآة جهاز عرض موضوع خارج MSR ، أمام الموضوع (الشكل 1 ب) ، واشرح المهمة الحركية البصرية التي يجب القيام بها أثناء التسجيل. على وجه الخصوص ، اطلب من الشخص أن ينقر بإصبعه السبابة على الطاولة فقط عندما يظهر التحفيز البصري (على سبيل المثال ، صورة) على الشاشة ، على التوالي ، لليد اليمنى واليسرى. تأكد من أن الموضوع يفهم المهمة أو يشعر بالراحة في أدائها بمفرده ؛ إذا لزم الأمر ، تدرب على المهمة مع الموضوع عدة مرات لمساعدته على التعرف عليها.
ملاحظة: إذا تم إجراء جلسة تحفيز حركي بصري في وضع الاستلقاء، يتم وضع مرآة على مسافة فوق وجه الهدف لتعكس المحفزات البصرية من جهاز العرض. - قبل إغلاق باب MSR ، اسأل الشخص عما إذا كان يشعر بالراحة لكونه بمفرده داخل الغرفة ؛ في حالة عدم قيامه بذلك ، سيبقى شخص واحد من الفريق أو والديه داخل MSR أثناء جلسات التسجيل. علاوة على ذلك ، طمئن الشخص إلى أنه سيتم ملاحظته على الشاشة خارج MSR للتسجيل بأكمله.
- نقل الموضوع داخل MSR. ساعده على الجلوس على الكرسي غير المغناطيسي والمتوافق وإيجاد وضع مريح ومريح. ضع عدة بطانيات على جسم الشخص لإبقائه دافئا أثناء التسجيل من خلال التأكد من سهولة الوصول إلى كابلات الأقطاب الكهربائية ، وضع الطاولة القابلة للإزالة حتى يتمكن الشخص من وضع يديه عليها أثناء المهمة. إذا لزم الأمر ، ضع منشفة تحت ركبتي الشخص للمساعدة في الحفاظ على وضع الجلوس ، ولا تنزلق لأسفل.
- للتحفيز السمعي ، استخدم الإعداد الموضح في الخطوة 2.14 مع شاشة العرض أمام الهدف الجالس. ساعد الشخص على ارتداء سماعات الرأس (أو سماعات الأذن) التي يتم من خلالها توصيل مشغلات الصوت (على سبيل المثال ، أصوات الزقزقة المعدلة).
- اطلب من الشخص تثبيت المحفزات (على سبيل المثال ، النقطة الخضراء على خلفية سوداء) المعروضة على الشاشة أثناء الاستماع إلى مشغلات الصوت. إذا لزم الأمر ، قم بإجراء جلسة تدريبية لمساعدة الشخص على فهم الإجراء بشكل أفضل. قبل إغلاق باب MSR ، كرر إجراءات السلامة كما هو موضح سابقا.
- للتحفيز الحسي الجسدي ، استخدم الإعداد الموضح في الخطوة 2.14. اسأل الشخص عن الفيديو (أو الفيلم) الذي يريد مشاهدته على شاشة جهاز العرض أمامه.
- اطلب من الشخص الاسترخاء بعيون مفتوحة ، ومشاهدة الفيديو المحدد ، والبقاء ثابتا قدر الإمكان ، وتجاهل المنبهات اللمسية التي يتم تسليمها إلى أصابعه أثناء التسجيل. اشرح للموضوع أنه سيشعر بنقرات لطيفة على الجلد عند طرف الأصابع ، على التوالي ، لكل يد. إذا شعر الشخص بعدم الارتياح ، فقم بإجراء جلسة تدريبية لطمأنته.
ملاحظة: تثبيت العين على هدف مرئي هو تقنية راسخة لتقليل القطع الأثرية البيولوجية التي يمكن أن تؤثر على جودة التسجيل وتشتت انتباه الموضوع عن المنبهات اللمسية التي يتم تسليمها أثناء الحصول على البيانات.
- اطلب من الشخص الاسترخاء بعيون مفتوحة ، ومشاهدة الفيديو المحدد ، والبقاء ثابتا قدر الإمكان ، وتجاهل المنبهات اللمسية التي يتم تسليمها إلى أصابعه أثناء التسجيل. اشرح للموضوع أنه سيشعر بنقرات لطيفة على الجلد عند طرف الأصابع ، على التوالي ، لكل يد. إذا شعر الشخص بعدم الارتياح ، فقم بإجراء جلسة تدريبية لطمأنته.
3. الحصول على البيانات
ملاحظة: يتم الحصول على بيانات MEG و EEG المتزامنة في منشأة MEG في مركز Cook Children's Medical Center (CCMC). يمكن العثور على مزيد من التفاصيل حول الاستخدام السريري ل MEG على الأطفال المصابين بالصرع في مكان آخر8،27،45.
- سجل إشارات MEG باستخدام نظام MEG كامل الرأس (تغطية المستشعر: 1220 سم2) يتميز ب 306 قناة مجمعة في 102 عنصر مستشعر ثلاثي متطابق مع مقياس مغناطيسي واحد واثنين من مقاييس التدرج المستوية المتعامدة. اضبط تردد أخذ العينات على 1 كيلو هرتز على الأقل.
ملاحظة: تقيس مقاييس المغنطيسية أحادية الملف مكون المجال المغناطيسي العمودي على سطح خوذة MEG. تتكون مقاييس التدرج المستوية من تكوين ملف "شكل ثمانية" يتميز بأزواج من مقاييس المغنطيسية الموضوعة على مسافة صغيرة بين بعضها البعض وقياس الفرق في المجال المغناطيسي بين مواقعها (أي الفرق بين حلقتي "ثمانية") ، وتسمى أيضا التدرج المكاني. بالمقارنة مع مقاييس المغناطيسية ، فإن مقاييس التدرج المستوية أقل حساسية لمصادر الدماغ العميقة ولكنها أكثر قوة في اكتشاف المصادر السطحية عن طريق قمع الضوضاء البيئية. يتم غمر هذه القنوات ال 306 وتبريدها في الهيليوم السائل عند -296 درجة مئوية (4.2 كلفن) لتصبح موصلات فائقة. - سجل إشارات EEG في وقت واحد باستخدام شبكة EEG غير المغناطيسية المكونة من 256 قناة مع مستشعرات القطب الكهربائي Ag / AgCl المتباعدة بالتساوي على فروة الرأس والخدين ومؤخرة الرقبة. اضبط تردد أخذ العينات على 1 كيلو هرتز على الأقل.
- أغلق باب MSR لبدء التسجيل. من خلال نظام الاتصال الداخلي الصوتي ، تواصل مع الموضوع ، وتحقق مما إذا كان يشعر بالراحة لكونه بمفرده داخل MSR. راقب الموضوع باستمرار على الفيديو ، وفي حالة الطوارئ ، أدخل MSR على الفور.
ملاحظة: في حالة عدم شعوره بالراحة أو كان باب MSR الضخم يخيفه ، يمكن لأي شخص واحد من الفريق أو والديه البقاء داخل MSR أثناء جلسات التسجيل جالسا على كرسي خشبي قريب من الموضوع ؛ تأكد من إزالة جميع الأشياء المعدنية قبل دخول الغرفة. - قبل كل تسجيل ، قم بتوجيه الموضوع من خلال نظام الاتصال الداخلي الصوتي للحفاظ على موضعه / موضعها ثابتا لمدة ~ 30 ثانية قبل بدء المهمة. بالنسبة للمهمة الحركية البصرية ، قم أيضا بالاتصال عبر الاتصال الداخلي بإصبع السبابة (إما الأيمن أو الأيسر) الذي سيستخدمه في جلسة التسجيل الأولى.
- خلال هذه الفترة التي يظل فيها الموضوع ثابتا ، اضغط على زر القياس من مربع حوار قياس HPI على نظام الحصول على بيانات MEG لقياس المجال المغناطيسي الناتج عن التيار الذي يتم تغذيته في ملفات HPI وتحديد مواضع قياس الرأس فيما يتعلق بمجموعة مستشعر MEG ؛ لذلك ، تأكد من أن الموضوع في وضع جيد (الرأس | إحداثيات z | ˂ 75 مم) واكتب قياسات 3D لكل جلسة.
- إذا كان لا يزال هناك مسافة بين رأس الشخص والخوذة ، فإما أن تدخل مرة أخرى داخل MSR واضبط ارتفاع الكرسي عبر دواسة الارتفاع (إن وجدت) ، أو ضع المناشف أو البطانيات على الكرسي ، أو قم بتوجيه الموضوع عبر الاتصال الداخلي حول كيفية تحويل الرأس في وضع أقرب إلى الخوذة (إذا كان الموضوع جالسا) ، وأخيرا تحقق من مواضع قياس الرأس مرة أخرى. في حالة تسجيلات الراحة / النوم ، أعد إدخال MSR واجعل السرير أقرب إلى الخوذة ، مما يقلل الفجوة المكانية بين خوذة الرأس.
- بمجرد أن يكون الموضوع في وضع جيد فيما يتعلق بخوذة MEG وجاهزا للبدء ، ابدأ جلسة التسجيل الأولى (المدة ~ 10 دقائق) باتباع ترتيب دقيق (انظر الخطوة 3.5.1) لمزامنة MEG و EEG بدقة (انظر الخطوة 3.12).
ملاحظة: لضمان تسجيلات عالية الجودة ، تعد جلسة التسجيل الأولى ضرورية لالتقاط القطع الأثرية الموجودة في البيانات بسبب تحركات الموضوع أو الناتجة عن البيئة الخارجية. إذا لزم الأمر ، أعد الدخول داخل MSR لضبط اتصالات القناة النهائية أو موضع الموضوع على كرسي MEG. يوصى بتدوين ملاحظات عن أي قطع أثرية أو أحداث غير عادية أثناء التسجيلات يمكن مراجعتها بعد ذلك إذا لزم الأمر.- اضغط على زر التسجيل في برنامج الحصول على بيانات EEG لبدء تسجيل EEG. اضغط على زر التسجيل في برنامج الحصول على بيانات MEG لبدء تسجيل MEG. أخيرا ، اضغط على زر البدء من برنامج كمبيوتر التحفيز إما لعرض المحفزات البصرية أو توصيل المحفزات السمعية.
ملاحظة: يتم توصيل كمبيوتر التحفيز الذي يقوم بتشغيل برنامج التحفيز المرئي (أو السمعي) بنظام مرآة جهاز العرض خارج MSR ، والذي يمكن تشغيله أو إيقاف تشغيله حسب نوع التسجيل الذي تم إجراؤه. أثناء تسجيلات الراحة / النوم ، يتم إيقاف تشغيل النظام لأن الموضوع إما يستريح أو ينام ، ولكن تشغيل برنامج التحفيز البصري على كمبيوتر التحفيز يساعد في توقيت كل جلسة تسجيل. أثناء المهمة الحركية البصرية ، وكذلك أثناء التحفيز السمعي والحسي الجسدي ، يتم تشغيل النظام عن طريق السماح للموضوع بمراقبة المحفزات أو مقطع فيديو معروض على الشاشة الموضوعة أمامه أثناء تشغيل البرنامج. لهذه الدراسة ، تم اختيار ما مجموعه (i) 107 محفزات (أي 85 صورة متراكبة على خلفية رقعة الشطرنج و 22 خلفية رقعة الشطرنج) مع فاصل ~ 4 s بين كل حافز للمهمة الحركية البصرية. '2' 200 صوت زقزقة معدل مع فاصل بين التحفيز يبلغ 3 ثوان للتحفيز السمعي؛ و (iii) 200 محفز لمسي لكل إصبع (أي D1 و D3 و D5) بعد تسلسل شبه عشوائي مع فاصل بين التحفيز ~ 1.5 ثانية للتحفيز الحسي الجسدي.
- اضغط على زر التسجيل في برنامج الحصول على بيانات EEG لبدء تسجيل EEG. اضغط على زر التسجيل في برنامج الحصول على بيانات MEG لبدء تسجيل MEG. أخيرا ، اضغط على زر البدء من برنامج كمبيوتر التحفيز إما لعرض المحفزات البصرية أو توصيل المحفزات السمعية.
- لإيقاف التسجيلات ، اضغط على زر الإيقاف في برنامج الحصول على بيانات MEG ثم زر الإيقاف في برنامج الحصول على بيانات EEG. في نهاية كل جلسة تسجيل ، تواصل مع الموضوع عبر الاتصال الداخلي لطمأنته / طمأنتها وإذا لم تكن هناك حاجة إلى اتصالات القناة أو تعديلات الموضع داخل MSR ، فتابع الجلسة التالية.
- بالنسبة للمهمة الحركية البصرية ، حدد محفزات بصرية مختلفة لكل جلسة للحفاظ على تحفيز الموضوع وترفيهه أثناء التسجيل.
- بالنسبة للبيانات الحركية أو بيانات الراحة / النوم ، سجل ما مجموعه ~ 1 ساعة تسجيل MEG و EEG متزامن ، يتميز ب 5-6 جلسات. ومع ذلك ، قد يختلف عدد الجلسات لكل موضوع. علاوة على ذلك ، سجل ما مجموعه ~ 20 دقيقة (1-2 جلسات من ~ 10 دقائق لكل منهما) و ~ 14 دقيقة (1-2 جلسات من ~ 7 دقائق لكل منهما) من تسجيل MEG و EEG المتزامن لبيانات التحفيز السمعي والحسي الجسدي ، على التوالي.
ملاحظة: في هذه الدراسة ، يتم تخزين بيانات MEG و EEG تلقائيا في نهاية التسجيلات بتنسيقات .fif و .mff ، على التوالي ، في نظام تخزين تكنولوجيا المعلومات الخاص ب CCMC. - عند انتهاء التسجيل ، أدخل MSR لمساعدة الشخص على الوقوف من الكرسي أو السرير واطلب منه الجلوس على كرسي خارج MSR لإزالة كل من شبكة EEG والأقطاب الكهربائية.
- اطلب من الشخص أن يغمض عينيه حتى يتم إخباره بخلاف ذلك وساعده على إزالة شبكة تخطيط كهربية الدماغ عن طريق فك أحزمة الذقن بالكامل وسحب الشبكة برفق باستخدام يدين (من الجبهة باتجاه مؤخرة رأس الموضوع) حتى يتم تقشيرها تماما. خلال هذه الخطوة ، تأكد من عدم سحب شعر الشخص أثناء إزالة الشبكة. بالإضافة إلى ذلك ، ساعد الشخص على إزالة الأقطاب الكهربائية المتبقية برفق (مثل ECG و EOG و EMG في حالة المهمة الحركية البصرية) المسجلة مسبقا على جلده.
- بعد إزالة شبكة EEG والأقطاب الكهربائية ، أبلغ الشخص (ووالديه) أن جميع الإجراءات قد اكتملت أخيرا.
- بعد أن يغادر الشخص الغرفة ، قم بتنظيف الماسح الضوئي بعناية (كما هو موضح في دليل المستخدم) وقم بتخزينه داخل العلبة الواقية.
- قم بتنظيف وتطهير أسطح أي معدات مستخدمة أثناء التسجيلات (مثل الكراسي والأسرة والمكاتب) إما بمناديل بيروكسيد الهيدروجين المعتمدة من المستشفى أو رذاذ المطهر والمناشف الورقية ، ووضع البطانيات والمناشف المستخدمة داخل الحاوية التي يوفرها المستشفى ، وتخلص من أي قطعة من الشريط المستخدم.
- قم بتخزين أدوات القياس داخل خزانة التخزين ونظف الجزء الداخلي من أكواب القطب المملوءة بعجينة موصلة باستخدام مسحات قطنية خشبية تحت ماء الصنبور الجاري.
- لشطف شبكة EEG ، املأ الدلو البلاستيكي في الحوض بماء صنبور نظيف ودافئ وكرر الخطوات التالية لما مجموعه أربع مرات.
- اغمر شبكة EEG في الماء وحرك شبكة EEG برفق لمدة 10-20 ثانية (أو اغمسها داخل وخارج الدلو ~ 25 مرة).
- قم بتصريف الماء من الدلو ، وأعد ملء الدلو بماء الصنبور النظيف والدافئ.
- لتطهير شبكة تخطيط كهربية الدماغ، املأ الدلو البلاستيكي في الحوض بمحلول مطهر يتكون من 2 كوارت طن من ماء الصنبور الفاتر و 1 ملعقة كبيرة من المطهر وانقع شبكة تخطيط كهربية الدماغ بداخلها لمدة 10 دقائق. اشطف الدلو من محلول التطهير واتبع عملية الشطف والتصريف ثلاث مرات لإزالة أي محلول متبقي من شبكة EEG.
- إما لعملية الشطف أو التطهير ، قم بإزالة شبكة EEG المغمورة من الدلو ، وجففها عن طريق إزالة الماء الزائد بمساعدة منشفة نظيفة وجافة ، وتخزينها عن طريق تعليقها بالقرب من الحوض.
- لمنع التداخلات المغناطيسية الداخلية والخارجية وآثار القياس / الحركة من بيانات MEG ، قم بتطبيق الامتداد الزمني لطريقة فصل مساحة الإشارة (tSSS) على ملف MEG .fif للبيانات الأولية.
ملاحظة: يعد ترشيح ماكسويل الزماني المكاني (tSSS) مثاليا لقمع مصادر التداخل الموجودة داخل أو بالقرب من مجموعة مستشعر MEG ، أي التداخل الداخلي. - عند إجراء تسجيلات MEG و EEG متزامنة ، قم بمحاذاة أنظمة الإحداثيات لجهازي الاستحواذ مكانيا فيما يتعلق بالمعالم التشريحية على رأس الموضوع (الشكل 2 أ) وتصحيح انحراف الساعة الخطي بين الإشارات التي تحدث بسبب معدلات أخذ العينات المختلفة المحتملة (الشكل 2 ب).
ملاحظة: أثناء التسجيلات، يمكن أن تتأثر إشارات MEG وEEG أيضا بالتحول البطيء بمرور الوقت بسبب التأخيرات المحتملة في الضغط على زري البدء والنهاية وانحراف الساعة الداخلي الذي يحدث عند إرسال المشغلات إلى برنامج الحصول على البيانات MEG وEEG. لضمان التزامن الدقيق بين هذه الإشارات ، تم تطوير رمز داخلي في Python يستخدم أحداث الزناد المرسلة على كلا النظامين أثناء الحصول على البيانات كإشارة تشغيل مشتركة. تتضمن الشفرة ثلاث وظائف متاحة في مكتبة برامج MNE-Python: وظيفتان تقرآن إشارات MEG و EEG ووظيفة واحدة تستخرج معلومات أحداث الزناد من الإشارات ، مثل أسماء القنوات والطوابع الزمنية (أي تاريخ ووقت وقوع الحدث). تحدد الاختلافات في الوقت بين حدوث أحداث الزناد في كل إشارة (أي دلتا) انحراف الساعة الخطي بمرور الوقت (الشكل 2 ب). ويرد وصف مفصل للشفرة المطورة في الخطوات التالية (انظر 3-12-1-3-12-4).- استخدم الفرق بين حدث التشغيل الأول الذي يحدث في كل إشارة كقيمة إزاحة (أي جزء سيتم اقتطاعه من إحدى الإشارتين) لمحاذاة التسجيلات.
ملاحظة: تقوم الدالتان mne.io.read_raw_fif و mne.io.read_raw_egi بتحويل تسجيلات MEG و EEG بتنسيق صفيف 2D ، بينما تستخرج الدالة mne.find_events معلومات الحدث من الإشارات الأولية. - بمجرد محاذاة هذه المشغلات الأولى ، احسب معامل ارتباط بيرسون لتقييم درجة الارتباط بين الإشارات ؛ يوصى باستخدام قيم p < 1 × 10-6 لضمان محاذاة مثالية.
ملاحظة: تقدر دالة بيرسونر من مكتبة scipy معامل ارتباط بيرسون بين إشارات MEG و EEG والقيمة p لهذا الارتباط. - للتحقق من دقة الارتباط هذه ، قم بتقدير معدل الانجراف بين الإشارتين عن طريق إجراء ملاءمة متعددة الحدود من الدرجة الأولى واستخدم مدى التباين الناتج الذي يمثله معامل دالة كثير الحدود لإعادة تشكيل الإشارات على المحور السيني للتركيب متعدد الحدود (الشكل 2 ب).
ملاحظة: تلائم وظيفة polyfit من مكتبة numpy إشارات MEG و EEG داخل دالة متعددة الحدود ؛ ترجع هذه الدالة معاملا يمثل مدى التباين بين الإشارتين. تقوم الدالة mne.resample بإعادة تشكيل إشارات MEG و EEG وفقا لمعامل دالة كثير الحدود. - بعد اكتمال إعادة التشكيل ، قارن الطوابع الزمنية لحدث التشغيل الأخير الذي يحدث على كل إشارة وقم بإزالة تلك النوافذ الزمنية غير الشائعة في كل من إشارات MEG و EEG. أخيرا ، ادمج إشارات MEG و EEG المتزامنة لإنشاء تسجيل واحد يتميز بكل من مستشعرات MEG و EEG التي يمكن استخدامها لمزيد من التحليل.
ملاحظة: تدمج الدالة mne.add_channels الإشارتين لإنشاء تسجيل واحد.
- استخدم الفرق بين حدث التشغيل الأول الذي يحدث في كل إشارة كقيمة إزاحة (أي جزء سيتم اقتطاعه من إحدى الإشارتين) لمحاذاة التسجيلات.
- في نهاية كل تسجيل ~ 1.5 ساعة ، استخدم ما مجموعه 5-6 (~ 10 دقائق لكل منهما) ، 1-2 (~ 10 دقائق لكل منهما) ، و 1-2 (~ 7 دقائق لكل منهما) من تسجيلات MEG و EEG المتزامنة ، على التوالي للحركة البصرية (والراحة / النوم) ، السمعية ، وبيانات التحفيز الحسي الجسدي ، لتحليل البيانات.
ملاحظة: من الناحية المثالية ، يحتاج الشخص إلى إجراء النقر بالإصبع الأيمن لثلاثة تسجيلات بصرية والنقر بالإصبع الأيسر للتسجيلات الحركية المرئية الثلاثة المتبقية.
4. تحليل البيانات
- رسم خرائط المنطقة المهيجة
- قم بتوليد الأسطح القشرية 3D من التصوير بالرنين المغناطيسي للموضوع باستخدام عملية إعادة البناء القشرية ل FreeSurfer ، وهي أداة تصوير عصبي مفتوحة المصدر لمعالجة وتحليل وتصور صور التصوير بالرنين المغناطيسي للدماغ البشري46.
- استيراد التشريح المعاد بناؤه على Brainstorm ، وهو تطبيق مفتوح المصدر ل MATLAB مخصص لتصور ومعالجة بيانات MEG و EEG47 ، لتصور نتائج إعادة البناء القشرية. من العصف الذهني ، قم بتعيين النقاط الإيمانية (على سبيل المثال ، nasion ، و preauricular الأيسر / الأيمن ، و commissure الأمامي / الخلفي ، و interhemispheric) على التصوير بالرنين المغناطيسي المستورد الذي يحدد نظام إحداثيات الموضوع.
- قم باستيراد إشارة MEG و HD-EEG المتزامنة على Brainstorm وتسجيل مستشعرات MEG و EEG على التصوير بالرنين المغناطيسي باستخدام عملية تسجيل التصوير بالرنين المغناطيسي لضبط محاذاتها مع النقاط الائتمانية الرقمية. إذا لزم الأمر ، قم بعرض مستشعرات EEG على السطح القشري.
- افتح تسجيل MEG و HD-EEG المتزامن وافحص البيانات الأولية بصريا لإزالة القنوات السيئة. بالإضافة إلى ذلك ، قم بتطبيق تقنية تصحيح القطع الأثرية لإسقاط مساحة الإشارة (SSP) المتوفرة في Brainstorm لرفض القطع الأثرية البيولوجية (على سبيل المثال ، دقات القلب ووميض العين) من التسجيلات.
- قم بتطبيق الشق (50 أو 60 هرتز ، وفقا لتداخل خط الطاقة) ومرشحات تمرير النطاق (1-70 هرتز) على بيانات MEG و HD-EEG المتزامنة.
- حدد أجزاء من البيانات التي تحتوي على نشاط بيني يتميز بالعبوات الناسفة المتكررة، مثل المسامير والموجات الحادة، ويحتوي على الحد الأدنى من آثار الحركة (إن أمكن).
ملاحظة: العبوات الناسفة المرتجلة هي أشكال موجية عابرة تتميز بتطور زمني <70 مللي ثانية ، وسعة >50 μV ، وشكل حاد يمكن تمييزه بوضوح عن نشاط الخلفية في نطاق التردد 1-70 هرتز48. يمثل الشكل 3A مثالا على أجزاء من إشارات MEG و HD-EEG المتزامنة مع وجود عبوات ناسفة متكررة مرئية في كلا التسجيلين. - باستخدام إعداد العرض القياسي البالغ 10 ثوان لكل صفحة ، حدد الذروة السلبية لكل عبوة ناسفة تحدث في كل من تسجيلات MEG و EEG (الشكل 3A) ، وكذلك على كل طريقة بمفردها. قبل وضع علامة على كل عبوة ناسفة ، تحقق من حقل الطبوغرافيا والخرائط المحتملة ل MEG و EEG ، على التوالي.
ملاحظة: يجب أيضا التحقق من توزيعات الجهد للنقاط الزمنية الإضافية خلال مرحلة صعود كل عبوة ناسفة ، بدلا من ذروتها ، لحساب نشاط الصرع المحتملالانتشار 49. يمكن العثور على مزيد من التفاصيل حول كيفية تحديد أحداث المسامير البينية باستخدام العصف الذهني في مكان آخر (https://neuroimage.usc.edu/brainstorm/Tutorials/Epilepsy). - احسب نموذجا واقعيا للرأس ، يعرف بأنه نموذج هندسي ثلاثي الطبقات (أي فروة الرأس والجمجمة الداخلية والجمجمة الخارجية) (الشكل 3 ب) ، باستخدام برنامج OpenMEEG BEM (طريقة عنصر الحدود المتماثلة) المتاح في العصف الذهني. استخدم وحدة تخزين التصوير بالرنين المغناطيسي كمساحة مصدر (شبكة نقطة المصدر بدقة مكانية 5 مم).
ملاحظة: يستخدم برنامج OpenMEEG BEM طريقة عنصر الحدود المتماثلة لحساب نموذج أمامي واقعي يتميز بفروة الرأس (أي واجهة الهواء وفروة الرأس) والجمجمة الخارجية (أي واجهة فروة الرأس والجمجمة) والجمجمة الداخلية (واجهة الجمجمة والدماغ). كحل بديل ، يمكن استخدام طريقة العناصر المحدودة (FEM) لحل المشكلة الأمامية لأنها تسمح بتمثيل واقعي خاص بالموضوع لموصل حجم الرأس. غالبا ما يتم افتراض قيم الموصلية لأنسجة الرأس من الأدبيات وقد تختلف حسب عمر الشخص50. لحل النموذج الأمامي باستخدام FEM ، احسب نموذج الرأس الواقعي ، الذي يعرف بأنه نموذج هندسي من ثلاث إلى خمس طبقات (أي المادة البيضاء والمادة الرمادية والسائل النخاعي والجمجمة والجلد) ، باستخدام برنامج DUNEuro FEM المتاح في Brainstorm47،50،51. يمكن العثور على مزيد من التفاصيل حول تقدير النموذج الأمامي باستخدام FEM في مكان آخر (https://neuroimage.usc.edu/brainstorm/Tutorials/Duneuro). - تحديد موقع المولدات الأساسية للمسامير البينية المحددة باستخدام طريقة ECD غير المقيدة على مجموعة مستشعرات MEG و EEG و MEG و EEG المدمجة بشكل منفصل. لتوطين مصادر ثنائية القطب هذه ، احسب تباين الضوضاء من تسجيلات MEG للغرفة الفارغة أو قم بتعيينه كمصفوفة هوية.
ملاحظة: ضع في اعتبارك إجراء توطين المصدر على العبوات الناسفة المرتجلة ذات التوزيعات المماثلة للجهد كنهج بديل في حالة انخفاض نسبة الإشارة إلى الضوضاءللعبوات الناسفة المرتجلة 12. - قم بإجراء طريقة المسح ثنائي القطب المتاحة في العصف الذهني في ذروة كل عبوة ناسفة تم وضع علامة عليها مسبقا لتحديد أهم ثنائيات أقطاب المصدر عبر حجم الدماغ بأكمله. حدد فقط ثنائيات أقطاب المصدر ذات الملاءمة الجيدة >60٪ وقم بتقدير عنقودها المحدد لكل ثنائي قطب على أنه عدد ثنائيات الأقطاب الموجودة على بعد 15 مم من مركزها (الشكل 3C).
ملاحظة: يمكن العثور على مزيد من التفاصيل حول مجموعة تنمية الطفولة المبكرة في مكان آخر52.
- رسم خرائط SOZ
- قم بتوليد الأسطح القشرية ثلاثية الأبعاد من التصوير بالرنين المغناطيسي للموضوع باستخدام عملية إعادة البناء القشرية ل FreeSurfer46.
- استيراد التشريح المعاد بناؤه على العصف الذهني47 لتصور نتائج إعادة البناء القشرية. قم بتعيين النقاط الإيمانية على التصوير بالرنين المغناطيسي المستورد والتي تحدد نظام إحداثيات الموضوع.
- قم باستيراد إشارة MEG و HD-EEG المتزامنة (التي تحتوي على حدث ictal) على Brainstorm وتسجيل مستشعرات MEG و EEG على التصوير بالرنين المغناطيسي باستخدام عملية تسجيل التصوير بالرنين المغناطيسي لضبط محاذاتها مع النقاط الائتمانية الرقمية. إذا لزم الأمر ، قم بعرض مستشعرات EEG على السطح القشري.
ملاحظة: إذا كان الشخص قد أصيب بنوبة صرع أثناء التسجيل ، فراجع الملاحظات التي تم تدوينها أثناء التسجيل لتقييم الجلسة التي تم فيها تسجيل حدث ictal. - افتح تسجيل MEG و HD-EEG المتزامن وافحص البيانات الأولية بصريا لإزالة القنوات السيئة. قم بتطبيق تقنية تصحيح القطع الأثرية SSP المتوفرة في العصف الذهني47 لرفض القطع الأثرية البيولوجية (مثل دقات القلب ووميض العين) من التسجيل.
- قم بتطبيق الشق (إما 50 أو 60 هرتز ، وفقا لتداخل خط الطاقة) ومرشحات تمرير النطاق (1-70 هرتز) على بيانات MEG و HD-EEG المتزامنة.
- وفقا لملاحظات التسجيل ، حدد بداية النوبة ونهايتها (إذا لوحظت) وقم بتمييز هذه الأحداث على الإشارة لتحديد الجزء الصحيح من البيانات التي تحتوي على تصريفات الصرع. يتم عرض أمثلة على بداية النوبة في الشكل 4 ل MEG و HD-EEG ، على التوالي.
ملاحظة: عندما يصاب شخص ما بنوبة صرع أثناء اقتناء MEG ، يطلب من الطاقم الطبي مساعدة الشخص على الفور وتقديم رعاية الطوارئ. ومن ثم، فإن مدة أجزاء البيانات هذه التي تتضمن أحداثا انتقالية قد تكون قصيرة. - باستخدام إعداد العرض القياسي البالغ 10 ثوان لكل صفحة ، حدد الذروة السلبية لكل دفعة من تصريفات الصرع (على سبيل المثال ، المسامير المتكررة أو الموجات الحادة أو مجمعات الموجات السنبلة) التي تحدث أثناء حدث ictal على MEG و EEG ، وكذلك على كل طريقة بمفردها. قبل كل علامة ذروة ، تحقق من حقل التضاريس والخرائط المحتملة ل MEG و EEG ، على التوالي (الشكل 4A).
ملاحظة: تصنف النوبات على أنها معممة أو بؤرية اعتمادا على المكان الذي تبدأ فيه بدايتها. على الرغم من اعتمادها على متلازمة الصرع ، إلا أن النوبة هي ظاهرة لا تقل عن 10 ثوان تتميز بتصريفات كهربائية متكررة قد تختلف في التردد والسعة والمورفولوجيا. - احسب نموذج الرأس الواقعي ثلاثي الطبقات (أي فروة الرأس والجمجمة الداخلية والجمجمة الخارجية) لأجهزة استشعار MEG و EEG باستخدام برنامج OpenMEEG BEM المتاح في Brainstorm. استخدم وحدة تخزين التصوير بالرنين المغناطيسي كمساحة مصدر (شبكة نقطة المصدر بدقة مكانية 5 مم).
ملاحظة: لحل النموذج الأمامي باستخدام FEM ، احسب نموذج الرأس الواقعي ، الذي يعرف بأنه نموذج هندسي من ثلاث إلى خمس طبقات (أي المادة البيضاء والمادة الرمادية والسائل النخاعي والجمجمة والجلد) ، باستخدام برنامج DUNEuro FEM المتاح في العصف الذهني47،50،51. يمكن العثور على مزيد من التفاصيل حول تقدير النموذج الأمامي باستخدام FEM في مكان آخر (https://neuroimage.usc.edu/brainstorm/Tutorials/Duneuro). - تحديد موقع المولدات الأساسية لتصريفات ictal المختارة باستخدام طريقة ECD غير المقيدة على MEG و EEG ومجموعة مستشعرات MEG و EEG المدمجة بشكل منفصل. لتوطين مصادر ثنائية القطب هذه ، احسب تباين الضوضاء من تسجيلات MEG للغرفة الفارغة أو قم بتعيينه كمصفوفة هوية.
- قم بإجراء طريقة المسح ثنائي القطب المتاحة في العصف الذهني في ذروة كل شكل موجي ictal تم تحديده مسبقا لتحديد أهم ثنائيات أقطاب المصدر عبر حجم الدماغ بأكمله. حدد فقط ثنائيات أقطاب المصدر ذات الملاءمة الجيدة >60٪ وقم بتقدير عنقودها (مسافة ثنائيات الأقطاب من مركز كل ثنائي القطب مضبوطة على 15 مم)52.
- رسم خرائط القشرة البليغة
- قم بتنفيذ الخطوات الموضحة سابقا 4.2.1-4.2.3 باستخدام الإشارات المسجلة أثناء المهمة الحركية البصرية ، وكذلك أثناء التحفيز السمعي والحسي الجسدي.
- افتح تسجيلات MEG و HD-EEG المتزامنة وافحص البيانات الأولية بصريا لإزالة القنوات السيئة. بشكل منفصل ، لكل جلسة ، قم بتطبيق تقنية تصحيح القطع الأثرية SSP المتوفرة في Brainstorm47 لرفض القطع الأثرية البيولوجية (على سبيل المثال ، دقات القلب ، وميض العين) من التسجيلات. بالإضافة إلى ذلك ، تجاهل أو ضع علامة على "فاصل زمني سيئ" لجميع شرائح البيانات الملوثة بالقطع الأثرية التي لا يمكن استخدامها لمزيد من التحليل.
- قم بتطبيق الشق (إما 50 أو 60 هرتز ، وفقا لتداخل خط الطاقة) ومرشحات تمرير النطاق (1-100 هرتز) على بيانات MEG و HD-EEG المتزامنة.
- لرسم خرائط القشرة الحركية ، افتح إشارات EMG المسجلة من أقطاب FDI و APB وقم يدويا بتمييز حدث التنصت الذي يقوم به الشخص ، بشكل منفصل لليد اليمنى واليسرى ، عن طريق اختيار الذروة الأولى لتنشيط العضلات المختلفة عن خط الأساس على قطب زوج الاستثمار الأجنبي المباشر. قم بتنفيذ هذه الخطوة بشكل منفصل لكل جلسة باستخدام Brainstorm47.
ملاحظة: استخدم علامة التبويب تصفية للتصور فقط في العصف الذهني وحدد نطاقات التردد (على سبيل المثال ، الترددات العالية: 30 هرتز ؛ الترددات المنخفضة: 300 هرتز ؛ الشق: 60 هرتز) التي يمكن أن تساعد في تحديد قمم نشاط EMG بشكل صحيح أثناء النقر. يجب أن يكون اسم الأحداث هو نفسه عبر الجلسات ؛ على سبيل المثال ، يمكن تسمية الأحداث التي يقوم فيها الشخص بالنقر بالإصبع الأيمن (أو الإصبع الأيسر) باسم "Tap_right" (أو "Tap_left"). تتيح لنا هذه الخطوة إجراء تحليل فريد لنفس نوع الحدث الذي حدث في جميع الجلسات. - من كل جلسة ، قم باستيراد الأحداث التي تحدث على مقاطع خالية من القطع الأثرية عن طريق تحديد المعلمات التالية: المحفزات البصرية: [-200 ؛ +500] مللي ثانية نافذة زمنية ، بما في ذلك خط الأساس [-200 ؛ 0] مللي ثانية قبل بداية التحفيز ؛ أحداث التنصت: [-1500؛ +1000] مللي ثانية، بما في ذلك خط الأساس [-1500؛ -1000] مللي ثانية قبل بدء التحفيز البصري؛ أصوات الزقزقة المعدلة: [-500 ؛ +1000] مللي ثانية نافذة زمنية ، بما في ذلك خط الأساس [-500 ؛ 0] مللي ثانية قبل بداية التحفيز ؛ والمحفزات اللمسية: [-100 ؛ +500] مللي ثانية نافذة زمنية ، بما في ذلك خط الأساس [-100 ؛ 0] مللي ثانية قبل بداية التحفيز.
- بمجرد استيراد أحداث مهمة معينة من جميع الجلسات ، قم بتطبيق متوسط المونتاج المرجعي لزيادة نسبة الإشارة إلى الضوضاء على بيانات EEG وتقدير المتوسط عبر المحفزات للحصول على الحقول والإمكانات التي تم استحضارها في الحدث. في حالة المهام الحركية (أي التنصت) والتحفيز عن طريق اللمس ، يتم تنفيذ هذه الخطوة الأخيرة لليد اليمنى واليسرى ، على التوالي.
ملاحظة: تعرض اللوحتان A و B من الشكل 5 والشكل 6 والشكل 7 والشكل 8 أمثلة على الاستجابات البصرية والحركية والسمعية والحسية الجسدية ، على التوالي ، ل MEG و EEG ومجال التضاريس النسبية والخرائط المحتملة. يعتمد العدد الإجمالي للمحفزات لمهمة محددة بشكل صارم على عدد الجلسات المكتملة ؛ في حالة Motor Task ، يعتمد هذا الرقم أيضا على مهمة النقر التي تم تنفيذها بشكل صحيح. - بالنسبة للمجالات والإمكانات البصرية أو الحركية أو السمعية أو الحسية الجسدية ، قم بحساب نموذج الرأس الواقعي ثلاثي الطبقات (أي فروة الرأس والجمجمة الداخلية والجمجمة الخارجية) لأجهزة استشعار MEG و EEG باستخدام برنامج OpenMEEG BEM المتاح في العصف الذهني. استخدام السطح القشري 3D كمساحة المصدر.
ملاحظة: لحل النموذج الأمامي باستخدام FEM ، احسب نموذج الرأس الواقعي ، الذي يعرف بأنه نموذج هندسي من ثلاث إلى خمس طبقات (أي المادة البيضاء والمادة الرمادية والسائل النخاعي والجمجمة والجلد) ، باستخدام برنامج DUNEuro FEM المتاح في العصف الذهني47،50،51. يمكن العثور على مزيد من التفاصيل حول تقدير النموذج الأمامي باستخدام FEM في مكان آخر (https://neuroimage.usc.edu/brainstorm/Tutorials/Duneuro). - لكل حقل وإمكانات مستحضرة للحدث ، احسب المصادر القشرية على الأحداث المتوسطة باستخدام dSPM المطبق في صندوق أدوات العصف الذهني لمصفوفة مستشعرات MEG و EEG و MEG و EEG المدمجة بشكل منفصل. اضبط مصفوفة التباين المشترك للضوضاء باستخدام فترة خط الأساس قبل التحفيز المحددة لكل مهمة (انظر الخطوة 4.3.5).
- اعتمادا على المهمة ، استخرج الحد الأقصى من المصادر القشرية التي لوحظت في منطقة الدماغ البليغة المعنية [القشرة البصرية الأولية (V1) ، القشرة الحركية الأولية (M1) ، القشرة السمعية الأولية (A1) ، أو القشرة الحسية الجسدية الأولية (S1)] التي يمكن تعريفها إما باستخدام أطلس أو من خلال إعادة بناء مستشعر افتراضي (أي منطقة الاهتمام ، عائد الاستثمار) في هذا الموقع (الشكل 5C ، الشكل 6C والشكل 7C والشكل 8C).
- قم بإجراء تحليل مورليت المويجات للتردد الزمني على المجال الذي أثاره الحدث والمصادر المحتملة في منطقة الدماغ البليغة المعنية (V1 أو M1 أو A1 أو S1) بمقياس خطي (نطاق التردد: 1: 1: 100 هرتز).
ملاحظة: لتقدير التذبذبات المستثارة المقفلة زمنيا وطوريا عند بداية التحفيز ، يتم حساب متوسط إشارة MEG / EEG مبدئيا على الأحداث ثم تصبح خاضعة لتحليل التردد الزمني53,54. - قم بإجراء توحيد خرائط المصدر القشري باستخدام طريقة الاضطراب المرتبط بالحدث المتاحة في العصف الذهني لتطبيعها فيما يتعلق بخط الأساس (انظر الخطوة 4.3.5) ، بشكل منفصل لكل حدث (الشكل 5D والشكل 6D والشكل 7D والشكل 8D).
ملاحظة: توحيد خرائط المصدر باستخدام الاضطرابات المتعلقة بالحدث هو مقياس تطبيع لخرائط قدرة التردد الزمني الذي يقدر الانحراف عن المتوسط فوق خط الأساس بالنسبة المئوية. يمكن العثور على مزيد من التفاصيل حول عملية التقييس هذه في مكان آخر (https://neuroimage.usc.edu/brainstorm/Tutorials/TimeFrequency#Normalized_time-frequency_maps).
- التحقق
- الحصول على تسجيل iEEG خارج العملية من خلال زرع شبكات تحت الجافية و / أو أقطاب العمق. يتم تحديد عدد ونوع وموضع الأقطاب الكهربائية داخل الجمجمة من قبل فريق الصرع متعدد التخصصات بناء على الفرضية السريرية الناتجة عن جمع المعلومات التي تم الحصول عليها من الاختبارات التشخيصية غير الباضعة للتقييم قبل الجراحة.
ملاحظة: كجزء من تقييم ما قبل الجراحة ، يتم تسجيل iEEG خارج العملية على مدار عدة أيام عبر نظام EEG الرقمي باستخدام معدل أخذ عينات 1024 هرتز. - حدد SOZ على النحو المحدد من قبل أخصائي الصرع الخبير بناء على المعلومات السريرية المتاحة لكل موضوع.
ملاحظة: يتم تعريف SOZ على أنه منطقة الدماغ التي تظهر أول تفريغ كهربائي لا لبس فيه ، والذي يختلف عن نشاط الخلفية الذي يمكن أن يحدث إما قبل أو مصاحب لبداية ictal المحددة سريريا. تعتبر جميع القنوات المشاركة في هذا التفريغ الكهربي ictal جهات اتصال SOZ ، حتى لو كانت تلتقط النوبات التي تنشأ من مناطق مختلفة من الدماغ. - أثناء الحدث المسجل على iEEG ، حدد ذروة كل دفعة من تصريفات الصرع التي تحدث في كل قطب كهربائي داخل الجمجمة وقم بإجراء توطين المصدر على هذه الأحداث ictal باستخدام طريقة ECD كما هو موضح سابقا في الخطوات 4.1.7-4.1.10.
- قارن نتائج توطين iEEG فيما يتعلق ب SOZ المحدد سريريا كمعيار ذهبي لنتائج توطين المصدر.
- الحصول على تسجيل iEEG خارج العملية من خلال زرع شبكات تحت الجافية و / أو أقطاب العمق. يتم تحديد عدد ونوع وموضع الأقطاب الكهربائية داخل الجمجمة من قبل فريق الصرع متعدد التخصصات بناء على الفرضية السريرية الناتجة عن جمع المعلومات التي تم الحصول عليها من الاختبارات التشخيصية غير الباضعة للتقييم قبل الجراحة.
النتائج
تم تجنيد مرضى الأطفال الذين يعانون من DRE من عيادة الصرع في معهد جين وجون جوستين لصحة العقل ، ونظام الرعاية الصحية للأطفال (CCHCS). هنا ، يتم تقديم بيانات من ثلاثة مرضى تمثيليين: (i) أنثى تبلغ من العمر 10 سنوات ، (ii) ذكر يبلغ من العمر 13 عاما ، و (iii) أنثى تبلغ من العمر 10 سنوات.
الحالة 1: تم إدخال أنثى تبلغ من العمر 10 سنوات مع نوبات تبدأ من سن ثلاث سنوات. كان المريض يعاني من نوبات يومية حتى بعد إعطاء 8 ASMs. تميزت النوبات الأولية بانحراف العين (جانب غير واضح) وتوقف سلوكي. في وقت لاحق ، عانى المريض من نوبات يومية من ~ 30 ثانية تتميز بالعبوس اللاصق ("علامة chapeau de gendarme") ، وانحراف الرأس إلى اليسار ، وتصلب الذراع المنشط الثنائي (الغلبة اليمنى). كشف فيديو EEG طويل المدى عن مجموعتين من النوبات المنشطة غير المتماثلة مع انحراف الرأس إلى اليسار ، تليها ذراعها اليسرى القادمة. كما لوحظت ثلاث نوبات منشط أثناء النوم ، مع تشغيل متكرر من polyspikes السريعة المعممة والموجات البطيئة مع فتح العين المتقطع ، والنظرة الصاعدة ، وارتفاع الذراع الأيسر أو الأيمن. كانت هذه المسامير المتعددة وموجات النوم البطيء بارزة في الغالب من الفص الصدغي الأوسط الأيسر. كشف التصوير بالرنين المغناطيسي للدماغ عن خلل التنسج متعدد البؤر التالي: (i) الفص الجداري الأيسر (التلفيف بعد المركزي) خلل التنسج القشري البؤري (FCD) مع علامة transmantle (النوع II FCD) ، (ii) تقاطع الجداري القذالي الأيمن FCD ، و (iii) القطب الصدغي الأيسر FCD. أظهر التصوير المقطعي بالإصدار البوزيتروني (PET) نقص التمثيل الغذائي في الفص الجداري الأيسر والفص الصدغي الأيسر والوصلة الجدارية القذالية اليمنى المقابلة لبؤر شذوذ الإشارة (أي FCD) في اختبار التصوير بالرنين المغناطيسي. تم تشخيص المريض بالصرع المستعصي ، مع سيميولوجيا نمطية من chapeau تليها تصلب الذراع منشط ، مما يشير إلى بداية أمامية متوسطة أو معزولة / صدغية محتملة. تمت التوصية باستكشاف مكثف ثنائي ل stereo-EEG (sEEG) من خلال استهداف الفص الجبهي ، والحزامية ، والإنسول ، ومناطق خلل التنسج. أثناء مراقبة iEEG ، كان المريض يعاني من نوبات نموذجية مع "chapeau de gendarme" متبوعة بارتفاع / ثني منشط للطرف العلوي الأيمن أو الأيسر يتميز ببداية EEG منتشرة ، بحد أقصى فوق الجزيرة الأمامية الثنائية. لوحظت العبوات الناسفة متعددة البؤر في الغالب في الفص الصدغي الأمامي الأيمن والأيسر والقشرة الأمامية الظهرية الوحشية ، بما في ذلك الجزر الثنائية. أكد ESI الذي تم إجراؤه على تسجيل iEEG موقع SOZ ، والذي تم تحديده سريريا بشكل ثنائي في القشرة الأمامية الظهرية الجانبية اليسرى واليمنى والجزيرة الأمامية.
كجزء من تقييم ما قبل الجراحة ، تم إجراء توطين المصدر على بيانات MEG و HD-EEG المتزامنة. أشارت تسجيلات MEG و HD-EEG إلى وجود عبوات ناسفة متكررة في كلتا المنطقتين الجبهية الصدغية. يوضح الشكل 3A مثالا تمثيليا لعبوة ناسفة على كل من بيانات MEG و HD-EEG ؛ يشير الحقل الطبوغرافي ورسم الخرائط المحتملة من كلتا الطريقتين إلى مصدر أساسي محتمل في المنطقة الأمامية الصدغية اليمنى. أشار ESI إلى مجموعة متناثرة من ثنائيات الأقطاب تغطي مناطق من الفص الجبهي الصدغي والفص الجداري الأيمن والأيسر. أظهر MSI مجموعة بؤرية من ثنائيات الأقطاب في الفص الجبهي الصدغي الأيمن ، وتقع بالقرب من الجزيرة اليمنى. أشار EMSI إلى مجموعات بؤرية من ثنائيات الأقطاب في المناطق الأمامية الصدغية الثنائية ، بما يتماشى مع ESI الذي تم إجراؤه على المعيار الذهبي iEEG ، والذي أكد الملاحظات السريرية (الشكل 3C). أظهرت هذه الأقطاب المقدرة من خلال EMSI متوسط مسافة من SOZ المحدد iEEG يبلغ 9.81 مم (الوسيط: 11.18 ؛ الأمراض المنقولة جنسيا: 2.37).
الحالة 2: تم إدخال رجل يبلغ من العمر 13 عاما يعاني من الصرع المستعصي مع نوبات تبدأ في سن التاسعة. بدأت النوبات بهالة متبوعة بانحراف الرأس / العين إلى اليسار مع الحفاظ على الوعي في بعض الأحيان والنساخ البؤري للرأس إلى اليسار ، واستمر لمدة ~ 30 ثانية ، وحدث عدة مرات في الأسبوع. ولم يحقق أي من المضبوطات الآلية الموصوفة السيطرة على النوبات. من مخطط كهربية الدماغ بالفيديو على المدى الطويل ، لاحظنا طفرات صدغية خلفية يمين وتصريفات متكررة لموجة سبايك في نصف الكرة الأيمن تشمل القشرة الصدغية الوسطى والصدغية والصدغية الجدارية والقشرة الدماغية. كان لدى المريض ست نوبات كهربية سريرية تتميز بتغيير سلوكي ، وانحراف الرأس / العين إلى اليسار مع تمديد الذراع الأيسر ، وأحيانا نشاط رمعي للذراع الأيسر ، وثلاث نوبات مع نشاط تشنجي ثنائي ثانوي. كانت البداية القصوى في الفص الصدغي الأوسط الأيمن مع تطور في الفص الجبهي الصدغي الأيمن. كشف التصوير بالرنين المغناطيسي للدماغ عن تشوه واسع النطاق في القشرة في نصف الكرة المخية الأيمن (سائد حول السيلفيان) وفقدان خفيف للحجم في نصف الكرة المخية الأيمن مع تمدد فراغي سابق للبطين الجانبي الأيمن. تم تشخيص المريض بالصرع المستعصي مع بداية في نصف الكرة الأيمن ، مفضلا بداية الصدغ و perisylvian في منطقة التشوه القشري المنتشر. تم إجراء Stereo-EEG لتحديد مدى المشاركة ، مع وضع أقطاب كهربائية في القشرة الصدغية اليمنى ، و perisylvian ، والجزرية ، و parietooccipital. تم التقاط العديد من النوبات البؤرية الكهروسريرية أثناء مراقبة iEEG مع أقصى ظهور في منطقة واسعة من الفص الجبهي الصدغي الأيمن. قام ESI الذي تم إجراؤه على بيانات iEEG بتوطين هذه النوبات في منطقة أكثر تركيزا تضم كلا من الصدغي الأيمن (بالقرب من التلفيف الصدغي الأوسط الأيمن) والمناطق المحيطة بالسيلفيان.
كجزء من تقييم ما قبل الجراحة ، تم إجراء MEG و HD-EEG في وقت واحد عانى خلاله المريض من نوبتين: واحدة أثناء الجلوس على الكرسي الخشبي أثناء عملية الرقمنة والأخرى تم التقاطها أثناء التسجيل الفعلي مع ظهور البداية على كل من MEG و HD-EEG (الشكل 4 أ). أشار حقل الطبوغرافيا والخرائط المحتملة في بداية النوبة إلى أن المولد الأساسي لبداية النوبة قد يكون في الفص الصدغي الأوسط الأيمن ، كما هو موضح في الشكل 4 أ. قدم توطين المصدر في حدث ictal نتائج مختلفة ل ESI و MSI: أظهر ESI ثنائيات أقطاب موضعية نحو الفص الجبهي الصدغي الأيمن والفص السمينتروباريتي ، بينما أظهر MSI ثنائيات أقطاب ذات تجمعات عالية في الغالب عند الفص الصدغي الأيمن (الشكل 4B) ، مع ثنائيات أقطاب متناثرة إضافية في القشرة الجبهية الصدغية. من خلال الجمع بين هذه الحلول ، كشف EMSI عن توطين بداية ictal داخل الفص الصدغي المتوافق مع ESI على المعيار الذهبي iEEG (الشكل 4B). على وجه الخصوص ، قدم EMSI نتائج التوطين بمسافة متوسطة من SOZ المحددة بواسطة مراقبة iEEG البالغة 12.21 مم (الوسيط: 13.62 ؛ الأمراض المنقولة جنسيا: 2.37).
الحالة 3: تم إدخال أنثى تبلغ من العمر 15 عاما مصابة بالصرع مجهول السبب المرتبط بالتوطين مع نوبات تبدأ في سن 13 عاما ، ولكن ربما في سن 8-9 في وقت لاحق ، عندما تم تشخيص إصابتها بالتشنجات اللاإرادية بسبب حركات الرقبة النمطية المتكررة. كان لدى المريض إمالة قصيرة للرأس إلى اليسار تطورت في بعض الأحيان إلى نوبة خلل الإدراك البؤري مع سلوكيات مفرطة الحركة (أي نوبات تشنجية رمعية معممة) ، بالإضافة إلى نوبات تشنجية ليلية. وأعطيت عدة أجهزة مضادة للجراثيم دون تحقيق السيطرة الكاملة على النوبات. أثناء مراقبة تخطيط كهربية الدماغ بالفيديو على المدى الطويل ، كان المريض يعاني من نوبات كهربية سريرية بؤرية مع تعميم ثانوي مع بداية في الفص الصدغي الخلفي الأيسر ، والعديد من النوبات الحركية البؤرية القصيرة مع إمالة الرأس إلى اليسار ، ونوبة كهربائية خفية مع بداية في القشرة الدماغية اليسرى. كشف التصوير بالرنين المغناطيسي للدماغ عن عدم وجود شذوذ حاد داخل الجمجمة وتشوه خياري I. كان فحص التصوير المقطعي المحوسب بالإصدار البوزيتروني (PET-CT) للرأس سلبيا. تمت التوصية بإجراء اختبارات إضافية ، مثل التصوير المقطعي المحوسب لانبعاث الفوتون المفرد (SPECT) ، و MEG و HD-EEG في وقت واحد ، والأشعة السينية للعمود الفقري العنقي ، وتصوير الأوعية بالرنين المغناطيسي (MRA) للرأس والرقبة ، وفي النهاية استكشاف sEEG لنصف الكرة الأيسر.
كجزء من التقييم ، شارك المريض في تسجيلات MEG و HD-EEG المتزامنة لرسم خرائط لمناطق الدماغ البليغة ، مثل القشرة البصرية والحركية والسمعية والحسية الجسدية الأولية. في البداية ، قام المريض بمهمة حركية بصرية ، تليها المحفزات السمعية والحسية الجسدية. حدثت الاستجابة القشرية الأولى للتحفيز البصري عند ~ 70 مللي ثانية بعد بداية التحفيز لكل من MEG و HD-EEG (الشكل 5 أ). الشكل 5 ب يبلغ عن حقل التضاريس والخرائط المحتملة للمواقع القشرية المشاركة في التحفيز البصري ل MEG و HD-EEG ، على التوالي. بالنسبة ل HD-EEG ، لوحظ تغيير في القطبية في القنوات التي تغطي مناطق الدماغ القذالي ، في حين تم العثور على توزيع مجال أكثر تعقيدا في نفس المناطق ل MEG (الشكل 5 ب). كشف توطين المصدر باستخدام dSPM عن نشاط قشري بؤري في هذه النقطة الزمنية داخل مناطق الدماغ التالية من أطلس ديسيكان-كيلياني: (i) cuneus ل MSI. (ii) القشرة القذالية الجانبية ل ESI ؛ و (iii) cuneus والقشرة القذالية الجانبية ل EMSI (الشكل 5 ج). كشف تحليل التردد الزمني على الاستجابات القشرية البصرية عن تزامن مرتبط بالحدث (ERS) في نطاق تردد جاما ل MSI (المدى التقريبي: 30-50 هرتز) ، ESI (المدى التقريبي: 40-50 هرتز) ، و EMSI (المدى التقريبي: 30-50 هرتز) (الشكل 5 د). بالنسبة للاستجابات الحركية ، لوحظ قمع نشاط mu-rhythm على M1 المقابل أثناء بداية الحركة (الشكل 6 أ). في الشكل 6 ب، أبلغنا عن حقل التضاريس والخرائط المحتملة لمناطق الدماغ التي تم تنشيطها أثناء المهمة الحركية ل MEG و HD-EEG ، على التوالي. أشارت خرائط حقل MEG إلى تغيرات واضحة في التدفق المغناطيسي والتدفق الخارجي في مناطق الدماغ المركزية المقابلة ، مما قد يشير إلى مولد بؤري أساسي في M1 المقابل (الشكل 6 ب). أظهرت خرائط جهد HD-EEG تغيرا في القطبية البؤرية في نفس المناطق ، مع إمكانات كهربائية متعامدة مع المجالات المغناطيسية (الشكل 6 ب). لوحظت قمم تنشيط المصدر الأقصى أثناء أداء مهمة التنصت عند التلفيف قبل المركزي المقابل لأطلس ديسيكان-كيلياني ل MSI و ESI و EMSI ، على التوالي ، كما هو موضح في الشكل 6 ج. أظهرت الاستجابات القشرية المتعلقة بالمحرك التي تحدث أثناء توقع حركة النقر القادمة ERS في نطاقات بيتا وجاما ل MSI (النطاق التقريبي: 20-30 هرتز) و EMSI (النطاق التقريبي: 20-40 هرتز) ونطاق جاما ل ESI (النطاق التقريبي: 30-50 هرتز) ، المشار إليه في الأدبيات باسم mu rhythm suppression (الشكل 6 د).55,56 كان للمجالات والإمكانات المستثارة سمعيا استجابة للتحفيز السمعي ذروة إيجابية قصوى عند ~ 80 مللي ثانية و ~ 120 مللي ثانية بعد تسليم بداية التحفيز ل MEG و HD-EEG ، على التوالي (الشكل 7 أ). في الشكل 7 ب، أبلغنا عن مجال التضاريس والخرائط المحتملة للمواقع القشرية المشاركة في التحفيز السمعي ل MEG و HD-EEG ، على التوالي. في كل من MEG و HD-EEG ، لوحظ تغير واضح في القطبية مع أقطاب سلبية وموجبة محددة بوضوح في أجهزة الاستشعار التي تغطي مناطق الدماغ الصدغية اليسرى. قد تكشف خرائط المجال المغناطيسي العمودي وخرائط الجهد الكهربائي هذه عن مولد بؤري أساسي في V1 (الشكل 7 ب). عند إجراء توطين المصدر على متوسط الحقول والإمكانات المستحثة سمعيا ، لوحظ التنشيط القشري الأقصى عند التلفيف الصدغي المستعرض والجزء الخلفي من التلفيف الصدغي العلوي لأطلس ديسيكان-كيلياني ل MSI و ESI و EMSI ، على التوالي (الشكل 7 ج). كشف تحليل التردد الزمني للاستجابات المستثارة سمعيا عن ERS في نطاق جاما ل MSI (المدى التقريبي: 40-60 هرتز) و EMSI (المدى التقريبي: 35-50 هرتز) ، ونطاقات تردد بيتا وجاما (المدى التقريبي: 25-60 هرتز) ل ESI (الشكل 7 د). أخيرا ، لاحظنا النشاط القشري الأول استجابة للتحفيز اللمسي عند ~ 60 و ~ 50 مللي ثانية بعد بداية التحفيز ل MEG و HD-EEG ، على التوالي (الشكل 8 أ). في الشكل 8 ب، أبلغنا عن مجال التضاريس والخرائط المحتملة لمناطق الدماغ التي تم تنشيطها أثناء التحفيز الحسي الجسدي ل MEG و HD-EEG ، على التوالي. كشفت خرائط مجال MEG عن تغير واضح في القطبية مع تغيرات واضحة في التدفق المغناطيسي في أجهزة الاستشعار التي تغطي المناطق الجدارية المقابلة ، في حين أظهرت خرائط إمكانات HD-EEG تغيرا أقل وضوحا في القطبية في نفس المناطق ذات القطب الموجب الأقوى من القطب السالب. قد تشير خرائط المجال المغناطيسي العمودي وخرائط الجهد الكهربائي هذه إلى مولد قشري بؤري في S1. باستخدام dSPM على متوسط الاستجابات الحسية الجسدية المستثارة ، لوحظ أقصى نشاط مصدر قشري في هذه النقطة الزمنية داخل التلفيف المقابل بعد المركزي لأطلس Desikan-Killiany ل MSI و ESI و EMSI ، على التوالي (الشكل 8 ج). استجابة للمحفزات اللمسية ، ERS في نطاقات تردد بيتا وجاما ل MSI (المدى التقريبي: 15-40 هرتز) و EMSI (المدى التقريبي: 20-40 هرتز) ، ونطاق تردد جاما ل ESI (المدى التقريبي: 30-40 هرتز) (الشكل 8 د) لوحظت أيضا.
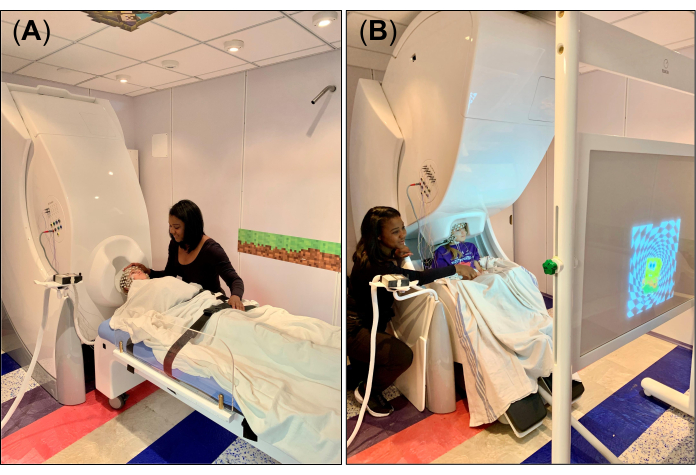
الشكل 1: الإعداد التجريبي ل MEG و HD-EEG في وقت واحد في CCHCS. (أ) أنظمة HD-EEG (256 قناة) و MEG (306 مستشعرات) مع ضبط جسر MEG على وضع ضعيف (90 درجة ، الوضع الأفقي) لتسجيل حالة الراحة / النوم باستخدام السرير غير المغناطيسي المتوافق مع MEG. يقوم الفني بإعداد الموضوع (فتاة تبلغ من العمر 9 سنوات) للتسجيل مع ضمان السلامة والراحة. (B) تم ضبط أنظمة HD-EEG و MEG للتسجيل في وضع الجلوس باستخدام الكرسي غير المغناطيسي المتوافق مع MEG. يقوم الفني بإعداد الموضوع للتسجيل مع ضمان الموضع الصحيح للموضوع أمام الشاشة حيث سيتم عرض المحفزات البصرية أثناء المهمة الحركية البصرية. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
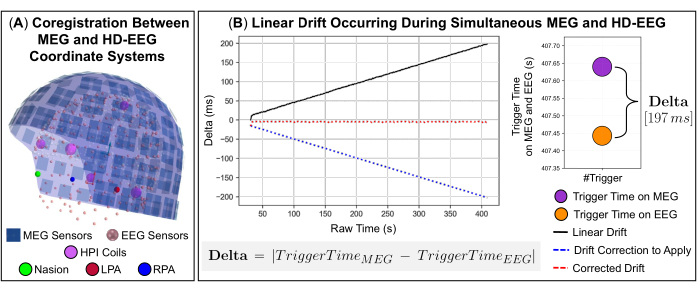
الشكل 2: الجوانب التقنية لدمج البيانات من تسجيلات MEG و HD-EEG المتزامنة باستخدام أنظمة اكتساب مختلفة. (أ) المحاذاة المكانية (التسجيل المشترك) لأجهزة استشعار MEG و HD-EEG في نفس نظام الإحداثيات (المحدد بإحداثيات رأس الموضوع) لموضوع تمثيلي (فتاة تبلغ من العمر 9 سنوات). يتم تمثيل إحداثيات رأس الموضوع بالنقاط الائتمانية التالية: nasion (اللون الأخضر) ونقاط preauricular اليسرى / اليمنى (اللون الأحمر والأزرق ، على التوالي). يتم عرض مستشعرات 306 MEG (زرقاء اللون) - 102 مقياس مغناطيسي و 204 مقياس تدرج مستو - وملفات مؤشر موضع الرأس (HPI) (باللون الأرجواني) ؛ محاذاة في نفس نظام الإحداثيات ، يتم أيضا عرض 256 قناة HD-EEG (باللون الوردي). (ب) اللوحة اليسرى: الانجراف الخطي (أي دلتا ، معروض كخط أسود) لعينات البيانات التي تحدث بين أنظمة MEG و HD-EEG لموضوع تمثيلي (فتاة تبلغ من العمر 9 سنوات). يتم تعريف دلتا على أنها القيمة المطلقة للفرق بين الأوقات التي يتم فيها إرسال نفس المشغل إلى كل من أنظمة MEG و EEG وتزداد باستمرار بمرور الوقت: من القيم المنخفضة (دلتا = 0 مللي ثانية) إلى القيم العالية (دلتا = 197 مللي ثانية). يتم عرض تصحيح الانجراف الخطي المقدر باستخدام دالة كثيرة الحدود ليتم تطبيقها على الإشارات بخط أزرق متقطع. يتم عرض الانجراف المصحح (دلتا ~ 0 مللي ثانية بمرور الوقت) الذي يمثل وقتا متزامنا بين أنظمة MEG و EEG بخط متقطع أحمر. اللوحة اليمنى: يتم عرض تمثيل رسومي للتحول الزمني (دلتا = 197 مللي ثانية) المقدر لآخر مشغل تم إرساله إلى كل من أنظمة MEG و EEG. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
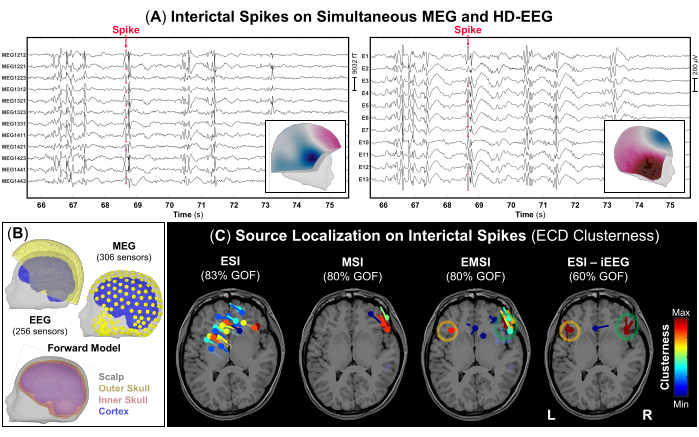
الشكل 3: تصريفات الصرع البينية (IEDs) على بيانات MEG و HD-EEG. (أ) الجزء الزمني من تسجيل MEG و HD-EEG المتزامن (10 ثوان) من أنثى تبلغ من العمر 10 سنوات (الحالة 1) مع عبوات ناسفة متكررة. تم اختيار مجموعة فرعية من مستشعرات 306 MEG و 256 قطبا كهربائيا لأغراض التصور. يتم عرض حقل الطبوغرافيا والخرائط المحتملة في ذروة العبوات الناسفة كلوحات داخلية ل MEG و HD-EEG ، على التوالي. (ب) موقع مستشعرات MEG و HD-EEG (صفراء اللون) مسجلة بشكل مشترك على رأس 3D للموضوع والأسطح القشرية (ذات اللون الأزرق). نموذج رأس طريقة عنصر الحدود الواقعي (BEM) يتكون من ثلاث طبقات [أي فروة الرأس (رمادية اللون) ، والجمجمة الخارجية (صفراء اللون) ، والجمجمة الداخلية (وردية اللون)] أعيد بناؤها من التصوير بالرنين المغناطيسي قبل الجراحة للموضوع. (ج) يتم عرض نتائج تجميع توطين المصدر التي يتم إجراؤها على العبوات الناسفة باستخدام ثنائي القطب الحالي المكافئ (ECD) في التصوير بالرنين المغناطيسي قبل الجراحة للموضوع ل ESI و MSI و EMSI و ESI على iEEG (المعيار الذهبي) 52. يتم عرض الخرائط الحرارية للتجمع ثنائي القطب مع جودة الملاءمة >60٪ من القيم الأدنى (الأزرق) إلى القيم الأعلى (الحمراء). تم اعتبار منطقة بداية النوبة المحددة من خلال ESI التي أجريت على بيانات iEEG على أنها المعيار الذهبي (الدوائر البرتقالية والخضراء). يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
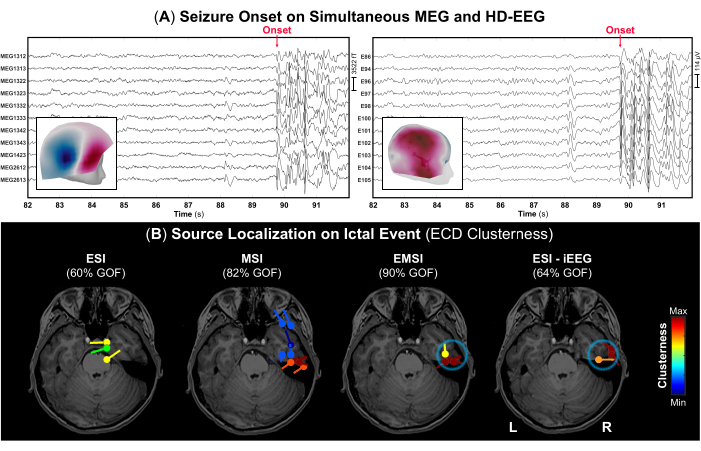
الشكل 4: بداية النوبة على بيانات MEG و HD-EEG. (أ) الجزء الزمني من تسجيل MEG و HD-EEG المتزامن (10 ثوان) من ذكر يبلغ من العمر 13 عاما (الحالة 2) مع بداية النوبة (السهم الأحمر). تم اختيار مجموعة فرعية من مستشعرات 306 MEG و 256 قطبا كهربائيا لأغراض التصور. يتم عرض حقل الطبوغرافيا والخرائط المحتملة في بداية ictal كلوحات داخلية ل MEG و HD-EEG ، على التوالي. (ب) تظهر نتائج تجمع توطين المصدر التي يتم إجراؤها في بداية حدث ictal باستخدام طريقة ثنائي القطب الحالي المكافئ (ECD) في التصوير بالرنين المغناطيسي قبل الجراحة للموضوع ل ESI و MSI و EMSI و ESI على iEEG (المعيار الذهبي) 52. يتم عرض الخرائط الحرارية للتجمع ثنائي القطب مع جودة الملاءمة >60٪ من القيم الأدنى (الأزرق) إلى القيم الأعلى (الحمراء). تم اعتبار منطقة بداية النوبة المحددة من خلال ESI التي أجريت على بيانات iEEG بمثابة المعيار الذهبي (الدائرة الزرقاء). يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
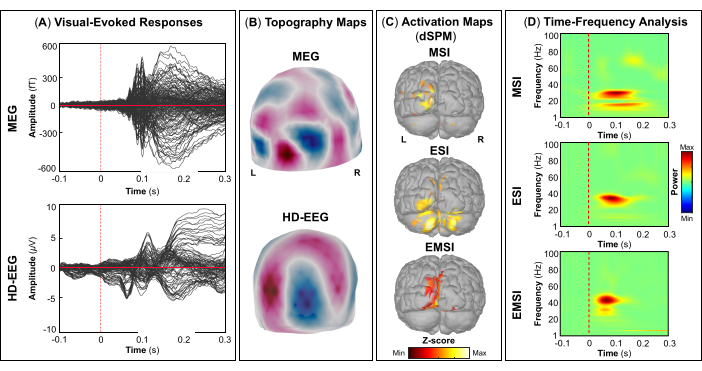
الشكل 5: الحقول والإمكانات المستثارة بصريا من بيانات MEG وHD-EEG. (أ) يتم عرض متوسط الاستجابات المرئية المستثارة لأنثى تبلغ من العمر 15 عاما ل MEG (اللوحة العلوية) و HD-EEG (اللوحة السفلية) للفترة الزمنية بين -100 مللي ثانية و 300 مللي ثانية. (ب) يتم عرض حقل الطبوغرافيا والخرائط المحتملة للقشرة البصرية الأولية ل MEG و HD-EEG ، على التوالي. (ج) خرائط تنشيط المصدر ذات السعة القصوى للتنشيط القشري في مناطق الدماغ من أطلس ديسيكان-كيلياني (أي cuneus والقشرة القذالية الجانبية) المقدرة باستخدام طريقة رسم الخرائط البارامترية الإحصائية الديناميكية (dSPM) ل MSI و ESI و EMSI ، على التوالي. يتم عرض الخرائط الحرارية لتنشيط المصدر (dSPM تطبيع z-score). (د) يتم عرض خرائط التردد الزمني التي تم الحصول عليها باستخدام تحلل التردد الزمني لموجة مورليت على الاستجابات المرئية المستثارة في القشرة البصرية الأولية للنافذة الزمنية من -100 مللي ثانية إلى 300 مللي ثانية. يتم عرض الخرائط الحرارية لقدرة التردد الزمني ، معبرا عنها بالنسب المئوية بناء على انحراف البيانات الطبيعية عن المتوسط فوق خط الأساس [-200 ؛ 0] مللي ثانية. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
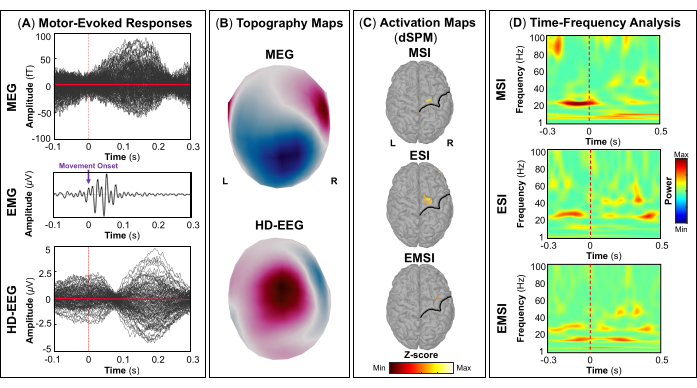
الشكل 6: المجالات والإمكانات المستثارة بالمحرك من بيانات MEG و HD-EEG. (أ) يتم عرض متوسط الاستجابات المثارة بمحرك لأنثى تبلغ من العمر 15 عاما ل MEG (اللوحة العلوية) و HD-EEG (اللوحة السفلية) لمهمة النقر على الفهرس اليسرى في الفترة الزمنية بين -100 و 300 مللي ثانية. يتم عرض إشارة تخطيط كهربية العضل (EMG) (اللوحة الوسطى) مع بداية الحركة (السهم الأرجواني) للفاصل الزمني بين -100 مللي ثانية و 300 مللي ثانية ؛ يتم ترشيح الإشارة في نطاق التردد 30-300 هرتز (مرشح الشق: 60 هرتز). (B) يتم عرض حقل الطبوغرافيا والخرائط المحتملة للقشرة الحركية الأولية ل MEG و HD-EEG ، على التوالي. (ج) خرائط تنشيط المصدر ذات السعة القصوى للتنشيط القشري عند التلفيف قبل المركزي المقابل لأطلس ديسيكان-كيلياني المقدر باستخدام طريقة رسم الخرائط البارامترية الإحصائية الديناميكية (dSPM) ل MSI و ESI و EMSI ، على التوالي. يتم عرض الخرائط الحرارية لتنشيط المصدر (dSPM تطبيع z-score) ، جنبا إلى جنب مع التلم المركزي (الخط الأسود). (د) خرائط التردد الزمني التي تم الحصول عليها باستخدام تحليل التردد الزمني لموجات مورليت على الاستجابات المستحثة بالمحرك في القشرة الحركية الأولية للنافذة الزمنية من -300 مللي ثانية إلى 500 مللي ثانية. يتم عرض الخرائط الحرارية لقدرة التردد الزمني ، معبرا عنها بالنسب المئوية بناء على انحراف البيانات الطبيعية عن المتوسط فوق خط الأساس [-1500 ؛ -1000] مللي ثانية. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
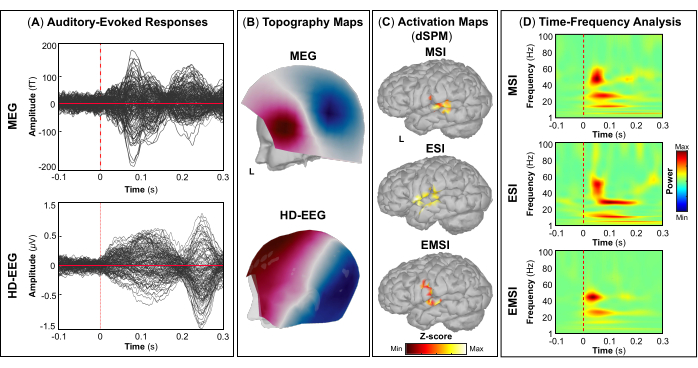
الشكل 7: المجالات والإمكانات المستثارة سمعيا من بيانات MEG و HD-EEG. (أ) يتم عرض متوسط الاستجابات المستحثة سمعيا لأنثى تبلغ من العمر 15 عاما ل MEG (اللوحة العلوية) و HD-EEG (اللوحة السفلية) للفترة الزمنية بين -100 مللي ثانية و 300 مللي ثانية. (ب) يتم عرض حقل الطبوغرافيا والخرائط المحتملة للقشرة السمعية الأولية ل MEG و HD-EEG ، على التوالي. (ج) خرائط تنشيط المصدر مع السعة القصوى للتنشيط القشري عند التلفيف الصدغي المستعرض والجزء الخلفي من التلفيف الصدغي العلوي لأطلس ديسيكان-كيلياني المقدر باستخدام طريقة رسم الخرائط البارامترية الإحصائية الديناميكية (dSPM) ل MSI و ESI و EMSI ، على التوالي. يتم عرض الخرائط الحرارية لتنشيط المصدر (dSPM تطبيع z-score). (د) خرائط التردد الزمني التي تم الحصول عليها باستخدام تحليل التردد الزمني لموجات مورليت على الاستجابات المستحثة سمعيا في القشرة السمعية الأولية للنافذة الزمنية -100 إلى 300 مللي ثانية. يتم عرض الخرائط الحرارية لقدرة التردد الزمني ، معبرا عنها بالنسب المئوية بناء على انحراف البيانات الطبيعية عن المتوسط فوق خط الأساس [-500 ؛ 0] مللي ثانية. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
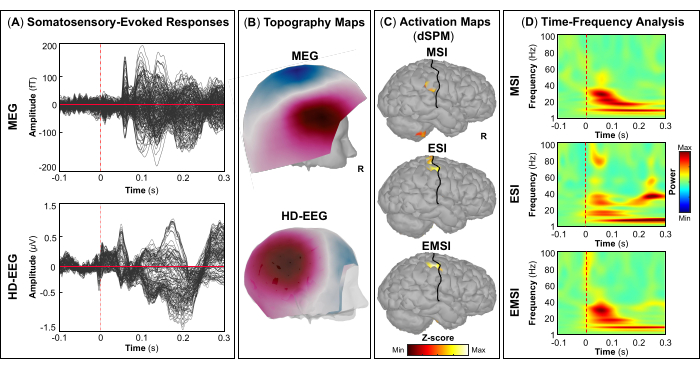
الشكل 8: المجالات والإمكانات المستثارة حسيا جسديا من بيانات MEG وHD-EEG. (أ) يتم عرض متوسط الاستجابات الحسية الجسدية لأنثى تبلغ من العمر 15 عاما ل MEG (اللوحة العلوية) و HD-EEG (اللوحة السفلية) لتحفيز الأرقام اليسرى في الفترة الزمنية بين -100 و 300 مللي ثانية. (ب) يتم عرض حقل الطبوغرافيا والخرائط المحتملة للقشرة الحسية الجسدية الأولية ل MEG و HD-EEG ، على التوالي. (ج) خرائط تنشيط المصدر ذات السعة القصوى للتنشيط القشري عند التلفيف المقابل بعد المركزي لأطلس ديسيكان-كيلياني المقدر باستخدام طريقة رسم الخرائط البارامترية الإحصائية الديناميكية (dSPM) ل MSI و ESI و EMSI ، على التوالي. يتم عرض الخرائط الحرارية لتنشيط المصدر (dSPM تطبيع z-score) ، جنبا إلى جنب مع التلم المركزي (الخط الأسود). (د) خرائط التردد الزمني التي تم الحصول عليها باستخدام تحلل التردد الزمني لموجة مورليت على الاستجابات الحسية الجسدية المستحثة في القشرة الحسية الجسدية الأولية للنافذة الزمنية -100 مللي ثانية إلى 300 مللي ثانية. يتم عرض الخرائط الحرارية لقدرة التردد الزمني ، معبرا عنها بالنسب المئوية بناء على انحراف البيانات الطبيعية عن المتوسط فوق خط الأساس [-100 ؛ 0] مللي ثانية. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
Discussion
في هذه الدراسة ، نوضح الإعداد التجريبي لتسجيل MEG و HD-EEG في وقت واحد في الأطفال الذين يعانون من DRE أثناء الراحة / النوم ، أو أداء مهمة ، أو تلقي المحفزات ، ونقترح إطارا منهجيا لتوطين المنطقة المهيجة ، SOZ ، ومناطق الدماغ البليغة باستخدام EMSI ، وكذلك MSI و ESI الفردية. كما نقدم توصيات فنية لدمج بيانات MEG و HD-EEG من مختلف المنتجات المتاحة تجاريا والتي تقدم ميزات فريدة. نقدم بيانات من ثلاث حالات لتعزيز الفائدة السريرية ل EMSI في توطين مناطق الدماغ الصرع والبليغة. تشير النتائج هنا إلى أن نتائج EMSI تتفوق على تلك التي تم الحصول عليها بأي من الطريقتين وحدهما ، ويرجع ذلك على الأرجح إلى القيمة المضافة للخصائص التكميلية لإشارات MEG و EEG في الحل المشترك وربما بسبب زيادة عدد أجهزة الاستشعار المستخدمة لتسجيل البيانات (>550 مستشعرا). على وجه الخصوص ، قام EMSI بتوطين التهيج و SOZs بشكل غير جراحي مع نتائج متوافقة مثل ESI على المعيار الذهبي iEEG ، مما أكد الملاحظات السريرية.
وتتضمن المنهجية المقترحة الخطوات الحاسمة التالية: '1' اقتناء عالي الجودة لتسجيلات MEG وHD-EEG المتزامنة (أي نسبة الإشارة إلى الضوضاء العالية) مع أخذ عينات مكانية عالية من أجهزة الاستشعار (>550 جهاز استشعار) تغطي كامل دماغ الأنشطة البينية والإشريكية، فضلا عن المجالات والإمكانات البصرية والحركية والسمعية والحسية الجسدية، من الأطفال المصابين ب DRE (الخطوات 3-1-3-2)؛ '2' التزامن الزمني والتسجيل المكاني المشترك لإشارات MEG وHD-EEG المسجلة بأنظمة احتياز مختلفة (الخطوة 12.3)؛ '3' المعالجة المسبقة الدقيقة واختيار أجزاء البيانات التي تحتوي على نشاط بيني (الخطوات 4-1-1-4-1-7)، ونشاط بداية ال ictal (الخطوات 4.2.1-4.2.7)، والاستجابات المتعلقة بالحدث (الخطوات 4.3.1-4.3.6)، على التوالي؛ و (iv) توطين المصدر الدقيق للمنطقة المهيجة ، SOZ ، ومناطق الدماغ البليغة ذات الأهمية باستخدام طرق توطين مصدر موثوقة (على سبيل المثال ، ECDs مع التجميع و dSPM) (الخطوات 4.1.8-4.1.9 ، 4.2.8-4.2.9 ، و 4.3.7-4.3.9 ، على التوالي).
الخطوة الأكثر أهمية عند إجراء تسجيلات MEG و HD-EEG المتزامنة هي مزامنة البيانات المسجلة بواسطة نظامي الاستحواذ مكانيا (المحاذاة بين مساحات الإحداثيات) والزمان (تصحيح انحراف الساعة الخطية). هذا التزامن أمر بالغ الأهمية لضمان التحديد الصحيح للأحداث البينية و ictal والأحداث البصرية / الحركية / السمعية / اللمسية التي تحدث في وقت واحد في إشارات MEG و HD-EEG. قد تؤثر الأخطاء في اختيار النقطة الزمنية لهذه الأحداث على نتائج توطين المصدر وتحديد مناطق الدماغ التي لا تشارك بالضرورة في توليد هذه الأحداث.
غالبا ما تقدم أنظمة MEG أنظمة EEG متوافقة 32 و 64 و 128 قناة مدمجة في المنتج لإجراء قياسات MEG و EEG متزامنة. في هذه الحالات ، ليست هناك حاجة لمزامنة البيانات مؤقتا عن طريق إرسال إشارات تشغيل مشتركة. وبالمثل ، فإن معظم أنظمة EEG متوافقة في الوقت الحاضر مع جميع أنظمة MEG. على الرغم من هذه التطورات في الأجهزة ، يقوم عدد قليل فقط من مراكز الصرع بإجراء تسجيلات MEG و HD-EEG متزامنة كجزء من التقييم قبل الجراحة. هنا ، استفدنا من هذا التكامل وقمنا بدمج أنظمة EEG ذات 306 قناة و 256 قناة لتسجيل نشاط الدماغ في وقت واحد باستخدام مستشعرات >550 تغطي رأس الموضوع. حتى الآن ، يتوفر عدد قليل من البرامج للتحليل المتقدم لبيانات MEG و HD-EEG و iEEG (على سبيل المثال ، العصف الذهني أو CURRY أو EEGLab أو FieldTrip أو MNE أو جوزة الطيب). لذلك فإن الدراسات المستقبلية ضرورية للتحقق من صحة المنهجية المقترحة باستخدام برنامج تحليل التصوير العصبي الجديد. أخيرا ، أدى الجمع بين MSI و ESI في حل فريد (EMSI) إلى زيادة التعقيد الحسابي لتحليل البيانات.
تقدم الطريقة الموصوفة بعض القيود التي يجب معالجتها في الدراسات المستقبلية. اخترنا يدويا العبوات الناسفة التي تحدث على كل من بيانات MEG و HD-EEG لمريضين تمثيليين مع تجاهل المسامير البينية التي حدثت في واحدة فقط من الإشارتين (إما MEG أو EEG). يمكن أن يكون الاختيار اليدوي للمسامير نهجا مستهلكا للوقت وذاتيا يمكن تبسيطه باستخدام الأساليب الآلية للكشف عن العبوات الناسفة التي تم تطويرها خلال العقود الماضية57,58,59. ومع ذلك ، يوصى دائما بالفحص البصري للتحليل الدقيق والكشف الدقيق عن كل عبوة ناسفة. علاوة على ذلك ، استخدمنا SOZ كتقريبي ل EZ. ومع ذلك ، فإن SOZ لا تتنبأ دائما بالنتائج الجراحية60,61,62,63. لذلك ، يمكن للدراسات المستقبلية استخدام النتيجة الجراحية كحقيقة أرضية لتحديد أكثر دقة ل EZ13,14,15,16,17,19,20. على الرغم من أنه يمكن التقاط النوبات بنجاح باستخدام MEG و EEG في وقت واحد وتحديد موقعها باستخدام تقنيات توطين المصدر المناسبة44,64، من النادر نسبيا تسجيل مثل هذه الأحداث في الممارسة السريرية، وخاصة من المرضى الخارجيين الذين يخضعون ل ASMs. ويرجع ذلك في الغالب إلى المدة المحدودة لتسجيلات MEG وحركات الجسم المفرطة التي تحدث أثناء النوبات (على سبيل المثال ، انزلق رأس المريض من الديوار) ، مما قد يتسبب في حدوث قطع أثرية بيولوجية يمكن أن تؤثر بشدة على نتائج توطين المصدر. في مراجعة حديثة ، ستيفان وآخرون. عن حدوث نوبات أثناء تسجيلات MEG في 7٪ -24٪ من المرضى ، بمتوسط وقت تسجيل 30 دقيقة حتى 5.7 ساعة عبر دراسات مختلفة65. في CCMC ، كان لدى 18 من أصل 89 (20.2٪) مرضى أحداث ictal تم التقاطها خلال تسجيلات MEG و HD-EEG المتزامنة التي تم إجراؤها خلال السنوات ~ الماضية ~. ومع ذلك ، تم تحليل 8 فقط من أصل 18 مريضا (44.4٪) بنجاح. في الحالات التي تظهر فيها تسجيلات MEG البينية نتائج طبيعية أو غير حاسمة ، يمكن استخدام ictal MEG أو HD-EEG لتحديد موقع EZ بدقة عالية. ومع ذلك، ينبغي معالجة المتطلبات التقنية واللوجستية لهذه التسجيلات. بالإضافة إلى ذلك ، لم تتم مقارنة البيانات التمثيلية لتوطين القشرة البليغة عبر EMSI بأي معايير ذهبية لتوطين مناطق الدماغ الوظيفية هذه ، مثل التصوير بالرنين المغناطيسي الوظيفي غير الجراحي أو التحفيز الكهربي أثناء العملية. لذلك ، قد تدمج المزيد من التحقيقات EMSI و fMRI نحو أداة تصوير غير باضعة متعددة الوسائط لتحسين دقة توطين مناطق الدماغ البليغة هذه لدى الأطفال المصابين ب DRE. يمكن أيضا توسيع هذا العمل لتوطين مناطق الدماغ الوظيفية الأخرى ، مثل المناطق البليغة للغة. يعد توطين وظائف اللغة ذا أهمية حاسمة أثناء التقييم قبل الجراحة للمرضى الذين يعانون من DRE لتحديد ترشيحهم الجراحي ، والتخطيط لمدى الاستئصال الجراحي ، ومنع العجز الوظيفي الدائم بعد الجراحة66. أظهرت العديد من الدراسات غير الباضعة أن رسم خرائط اللغة باستخدام MEG يمكن أن يوفر نتائج متوافقة ، على غرار اختبار Wada الغازي ، والذي غالبا ما ينظر إليه على أنه المعيار الذهبي لتحديد نصف الكرة الأرضية السائد67,68,69,70. اقترحت دراسة حديثة نهجا متعدد الوسائط يمكن أن يوفر فيه الجمع بين التقنيات المختلفة (أي رسم خرائط التحفيز القشري ، وتخطيط كهربية جاما العالية ، والتصوير بالرنين المغناطيسي الوظيفي ، والتحفيز المغناطيسي عبر الجمجمة) معلومات متبادلة وتأكيدية وتكميلية لرسم خرائط اللغة قبل الجراحة71. على الرغم من هذه المزايا ، لا يزال رسم خرائط المناطق اللغوية يمثل تحديا في مرضى الأطفال الذين لديهم حواجز معرفية وفكرية ولغوية بسبب أعمارهم. وبالتالي ، ينبغي تطوير المزيد من المهام الخاصة بالعمر والإعدادات الصديقة للأطفال في المستقبل القريب. في هذا العمل ، قمنا بتحليل بيانات MEG و HD-EEG باستخدام برنامج غير معتمد للأغراض السريرية. على الرغم من أن هذه الأدوات قد أثبتت قيمتها وفعاليتها ، إلا أنها تحمل قضايا المسؤولية التي يجب مراعاتها عند الإبلاغ عن نتائج التقييم قبل الجراحة للاستخدام السريري. هنا ، نصف إجراءات تسجيلات HD-EEG باستخدام أنظمة قطب EEG القائمة على الإسفنج فقط. تستخدم الأنظمة البديلة التي تستخدم أقطاب EEG القائمة على الهلام على نطاق واسع في كل من الإعدادات السريرية والبحثية. على الرغم من أنها توفر تسجيلات SNR EEG أعلى ، إلا أنها تتطلب وقتا أطول للتحضير (~ 40-60 دقيقة) وبالتالي فهي أقل ملاءمة لاستخدام الأطفال. بدلا من ذلك ، تستخدم العديد من المختبرات أنظمة EEG منخفضة الكثافة القائمة على الهلام أثناء تسجيلات MEG ، والتي تعتبر مفيدة من حيث وقت التحضير (مقارنة بأنظمة HD-EEG) ، ولكنها توفر دقة مكانية أقل بكثير بسبب انخفاض عدد الأقطاب الكهربائية التي تغطي فروة الرأس بأكملها12,16,72,73.
في الوقت الحاضر ، لا يزال توطين مناطق الدماغ الصرع في المرضى الذين يعانون من الصرع يتحقق بشكل رئيسي مع مراقبة iEEG. علاوة على ذلك ، فإن منهجية التوطين الدقيق لمناطق الدماغ البليغة غير محددة بشكل جيد ، كما أن إعدادات التجربة المستخدمة حاليا في مختبرات MEG غير مناسبة لمرضى الأطفال ، في حين أن استخدام HD-EEG لهذا الغرض محدود للغاية. قد يسهل التوطين الدقيق لهذه المناطق التقييم قبل الجراحة ويزيد من التخطيط الجراحي إما للاستئصال أو وضع قطب iEEG. حتى الآن ، بحثت العديد من الدراسات في مساهمة ESI أو MSI في التقييم قبل الجراحة للمرضى الذين يعانون من DRE والصرع البؤري لتحديد EZ12،13،14،15،16،17،18،19 والمناطق البليغة من القشرة الحسية الجسدية41على التوالي. أظهرت دراسات قليلة نتائج توطين مصادر أفضل وأداء تنبؤ بالنتائج باستخدام EMSI مقارنة ب MSI أو ESI وحده13،31،42. على الرغم من هذه النتائج ، نادرا ما يتم إجراء تسجيل MEG و EEG في وقت واحد ، ويتم تنفيذ MSI و ESI في عدد قليل فقط من مراكز الصرع في جميع أنحاء العالم. على حد علمنا ، هذه هي الدراسة الأولى التي تقدم اقتراحات لجمع وتحليل بيانات MEG و HD-EEG المتزامنة ، بالإضافة إلى إجراء EMSI في صرع الأطفال لتحديد المنطقة المهيجة ، SOZ ، ومناطق الدماغ البليغة ، وهي القشرة البصرية والحركية والسمعية والحسية الجسدية.
هنا ، أجرينا EMSI على المسامير البينية والأحداث المتزامنة المكتشفة على البيانات غير الباضعة المتزامنة من مريضين مصابين ب DRE (الحالتان 1 و 2) وحققنا خطأ في توطين المصدر ~ 9 مم و ~ 12 مم من SOZ ، على التوالي ، بما يتماشى مع الدراسات السابقة42. بشكل مثير للإعجاب ، حققت هذه الطريقة دقة توطين مماثلة للنتائج داخل الجمجمة (أي ESI على بيانات iEEG) ، مع ثنائيات أقطاب عنقودية موضعية في منطقة الدماغ تم تحديدها على أنها مصابة بالصرع من خلال الملاحظات السريرية (الشكل 3C والشكل 4B). باستخدام بيانات غير جراحية من مريض تمثيلي ثالث مصاب ب DRE (الحالة 3) ، أجرينا أيضا EMSI على الأنشطة البصرية والحركية والسمعية والحسية الجسدية ووجدنا أنماط تنشيط مصدر بارزة في مناطق الدماغ البليغة المقابلة (أي القشرة البصرية والحركية والسمعية والحسية الجسدية) (الشكل 5C والشكل 6C والشكل 7C والشكل 8C).
تم اشتقاق نتائجنا من دمج المعلومات التكميلية التي تم التقاطها من طرائق MEG و EEG التي قد تحسن دقة التوطين. من المعروف أن EEG يعكس جميع التيارات داخل الجمجمة ، في حين أن MEG حساس في الغالب للمصادر العرضية وأعمى لمصادر الدماغ العميقة29,74. كما هو موضح في هذه الدراسة ، فإن الجمع بين MEG و EEG يمكن أن يتغلب على قيود كل طريقة ، ويوفر نتائج توطين فائقة ، ويحدد مناطق الدماغ الصرعية والبليغة التي قد يفوتها ESI أو MSI إذا تم استخدامها بمفردها. علاوة على ذلك ، نقدم نهجا بديلا غير جراحي لرسم خرائط لمناطق الدماغ البليغة باستخدام EMSI في المرضى الذين لم يخضعوا للتصوير بالرنين المغناطيسي الوظيفي أثناء تقييمهم قبل الجراحة.
يعد توطين مناطق الدماغ الصرعية والبليغة باستخدام تقنيات غير جراحية ، مثل MEG و EEG المتزامنين ، خطوة أساسية أثناء التقييم قبل الجراحة للأطفال الذين يعانون من DRE للإزالة الكاملة أو فصل EZ مع الحفاظ على المناطق القشرية البليغة. تقدم المنهجية المقترحة وصفا مفصلا لاكتساب وتحليل بيانات MEG و EEG المتزامنة التي تدعم تطبيقها ليس فقط في تقييم الصرع قبل الجراحة ولكن أيضا في علوم الأعصاب المعرفية لاستكشاف الوظائف الفسيولوجية للدماغ السليم في كل من الأطفال الذين يتطورون عادة وكذلك البالغين الأصحاء ، وكذلك التغيرات المورفولوجية والوظيفية في الدماغ المرتبطة بالصرع أو الاضطرابات العصبية الأخرى. قد تقوم الدراسات المستقبلية التي تبحث في شبكات الدماغ المسببة للصرع أيضا بتقييم ما إذا كانت محاور الشبكة (أي مناطق الدماغ شديدة الاتصال) المقدرة بشكل غير جراحي باستخدام EMSI على بيانات MEG و HD-EEG المتزامنة يمكن أن تحدد موقع EZ بدقة أكبر في الأطفال المصابين ب DRE من تلك المقدرة باستخدام MSI و / أو ESI وحده75،76،77. علاوة على ذلك ، يمكن أن يساعد رسم الخرائط غير الباضعة للانتشار الزماني المكاني للمسامير والتموجات (أي التذبذبات عالية التردد ، >80 هرتز) ، المقدرة من خلال EMSI ، على فهم أفضل للآليات الفيزيولوجية المرضية لنشر نشاط الصرع وتقييم مولد بداية هذه الانتشار بشكل غير جراحي وهو علامة حيوية دقيقة ل EZ78,79. قد يساعد البروتوكول المقدم على مواصلة التحقيق في تكامل أنظمة MEG و EEG من خلال فحص حساسية صفائف أجهزة استشعار MEG و EEG لمصادر ذات اتجاهات مختلفة. قد يوفر هذا التحليل نظرة ثاقبة للخصائص الفيزيولوجية الكهربية للدماغ أثناء إجراء MEG و HD-EEG في وقت واحد.
Disclosures
لم يبلغ المؤلفون عن أي إفصاحات.
Acknowledgements
تم دعم هذا العمل من قبل المعهد الوطني للاضطرابات العصبية والسكتة الدماغية (R01NS104116; R01NS134944. الباحث الرئيسي: كريستوس باباديليس).
Materials
| Name | Company | Catalog Number | Comments |
| AIRSTIM unit | SD Instruments | N/A | The SDI AIRSTIM system is an alternative unconditioned stimulus to shock |
| Baby Shampoo | Johnson's | N/A | Baby Shampoo is as gentle to the eyes as pure water and is specially designed to gently cleanse baby’s delicate hair and scalp. |
| Control III disinfectant cleaning solution | Maril Products, Inc. | http://www.controlthree.com/ | Disinfectant and germicide solution formulated for hospitals |
| Elekta Neuromag | TRIUX | NM24132A | Comprehensive bioelectromagnetic measurement system characterized by 306-channel neuromagnetometer for functional brain studies |
| FASTRAK | Polhemus technology | NS-7806 | Using A/C electromagnetic technology, FASTRAK delivers accurate position and orientation data, with virtually no latency. With a single magnetic source, FASTRAK delivers data for up to four sensors. The source emits an electromagnetic field, sensors within the field of range are tracked in full 6DOF (6 Degrees-Of-Freedom). Setup is simple and intuitive, with no user calibration required. |
| Genuine Grass Reusable Cup EEG Electrodes | Natus Medical, Inc. | N/A | Each Genuine Grass EEG Electrode undergoes rigorous mechanical and electrical testing to assure long life for unsurpassed recording clarity and dependability. |
| Geodesic Sensor Net | Electrical Geodesics, Inc. | S-MAN-200-GSNR-001 | 32 to 256 electrodes to place on the human head to aquire dense-array electroencephalography data |
| GeoScan Sensor Digitization System | Electrical Geodesics, Inc. | 8100550-03 | Handheld Scanner and Software for 3D electrode position registration |
| Natus Xltek NeuroWorks | Natus Medical, Inc. | https://natus.com/ | The Natus NeuroWorks platform simplifies the process of collecting, monitoring and managing data for routine EEG testing, ambulatory EEG, long-term monitoring, ICU monitoring, and research studies. |
| Natus NeuroWorks EEG Software | Natus Medical, Inc. | https://natus.com/neuro/neuroworks-eeg-software/ | NeuroWorks EEG software simplifies the process of collecting, monitoring, trending and managing EEG testing data, allowing care providers to save time and focus on delivering the best care. |
| ROSA ONE Brain | Zimmer Biomet | https://www.zimmerbiomet.com/en/products-and-solutions/zb-edge/robotics/rosa-brain.html | ROSA ONE Brain is a robotic solution to assist surgeons in planning and performing complex neurosurgical procedures through a small drill hole in the skull. |
| Ten20 Conductive Paste | Weaver and company | N/A | Ten20 contains the right balance of adhesiveness and conductivity, enabling the electrodes to remain in place while allowing the transmittance of electrical signals. |
References
- Oldham, M. S., Horn, P. S., Tsevat, J., Standridge, S. Costs and clinical outcomes of epilepsy surgery in children with drug-resistant epilepsy. Pediatr Neurol. 53 (3), 216-220 (2015).
- Willie, J. T., et al. Real-time magnetic resonance-guided stereotactic laser amygdalohippocampotomy for mesial temporal lobe epilepsy. Neurosurgery. 74 (6), 569-584 (2014).
- Rosenow, F., Lüders, H. Presurgical evaluation of epilepsy. Brain. 124, Pt 9 1683-1700 (2001).
- Önal, Ç, et al. Complications of invasive subdural grid monitoring in children with epilepsy). J Neurosurg. 98 (5), 1017-1026 (2003).
- Hader, W. J., et al. Complications of epilepsy surgery-a systematic review of focal surgical resections and invasive EEG monitoring. Epilepsia. 54 (5), 840-847 (2013).
- Meng, Y., et al. Risk factors for surgical site infection after intracranial electroencephalography monitoring for epilepsy in the pediatric population. J Neurosurg Pediatr. 22 (1), 31-36 (2018).
- Jobst, B. C., et al. Intracranial EEG in the 21st Century. Epilepsy Curr. 20 (4), 180-188 (2020).
- Schwartz, E. S., et al. Magnetoencephalography for pediatric epilepsy: how we do it. AJNR Am J Neuroradiol. 29 (5), 832-837 (2008).
- Michel, C. M., et al. Electric source imaging of human brain functions. Brain Res Rev. 36 (2-3), 108-118 (2001).
- Michel, C. M., He, B. EEG source localization. Handb Clin Neurol. 160, 85-101 (2019).
- Michel, C. M., Brunet, D. EEG source imaging: A practical review of the analysis steps. Front Neurol. 10, 325(2019).
- Plummer, C., et al. Interictal and ictal source localization for epilepsy surgery using high-density EEG with MEG: a prospective long-term study. Brain. 142 (4), 932-951 (2019).
- Duez, L., et al. Electromagnetic source imaging in presurgical workup of patients with epilepsy: A prospective study. Neurology. 92 (6), e576-e586 (2019).
- Mouthaan, B. E., et al. Diagnostic accuracy of interictal source imaging in presurgical epilepsy evaluation: A systematic review from the E-PILEPSY consortium. Clin Neurophysiol. 130 (5), 845-855 (2019).
- Pellegrino, G., et al. Clinical yield of magnetoencephalography distributed source imaging in epilepsy: A comparison with equivalent current dipole method. Hum Brain Mapp. 39 (1), 218-231 (2018).
- Tamilia, E., et al. Assessing the localization accuracy and clinical utility of electric and magnetic source imaging in children with epilepsy. Clin Neurophysiol. 130 (4), 491-504 (2019).
- Coito, A., et al. Interictal epileptogenic zone localization in patients with focal epilepsy using electric source imaging and directed functional connectivity from low-density EEG. Epilepsia Open. 4 (2), 281-292 (2019).
- Singh, J., Ebersole, J. S., Brinkmann, B. H. From theory to practical fundamentals of electroencephalographic source imaging in localizing the epileptogenic zone. Epilepsia. 63 (10), 2476-2490 (2022).
- Brodbeck, V., et al. Electrical source imaging for presurgical focus localization in epilepsy patients with normal MRI. Epilepsia. 51 (4), 583-591 (2010).
- Santalucia, R., et al. Clinical added value of interictal automated electrical source imaging in the presurgical evaluation of MRI-negative epilepsy: A real-life experience in 29 consecutive patients. Epilepsy Behav. 143, 109229(2023).
- Schneider, F., et al. Magnetic source imaging in non-lesional neocortical epilepsy: additional value and comparison with ICEEG. Epilepsy Behav. 24 (2), 234-240 (2012).
- Hämäläinen, M., Hari, R., Ilmoniemi, R. J., Knuutila, J., Lounasmaa, O. V. Magnetoencephalography-theory, instrumentation, and applications to noninvasive studies of the working human brain. Rev Mod Phys. 65, 413-497 (1993).
- Baillet, S., Mosher, J. C., Leahy, R. M. Electromagnetic brain mapping. IEEE Signal Process Mag. 18 (6), 14-30 (2001).
- Fuchs, M., Kastner, J., Tech, R., Wagner, M., Gasca, F. MEG and EEG dipole clusters from extended cortical sources. Biomed Eng Lett. 7 (3), 185-191 (2017).
- Singh, S. P. Magnetoencephalography: Basic principles. Ann Indian Acad Neurol. 17, Suppl 1 S107-S112 (2014).
- Ahlfors, S. P., Han, J., Belliveau, J. W., Hämäläinen, M. S. Sensitivity of MEG and EEG to source orientation. Brain Topogr. 23, 227-232 (2010).
- Kim, H., Chung, C. K., Hwang, H. Magnetoencephalography in pediatric epilepsy. Korean J Pediatr. 56 (10), 431-438 (2013).
- Gorjan, D., Gramann, K., De Pauw, K., Marusic, U. Removal of movement-induced EEG artifacts: Current state of the art and guidelines. J Neural Eng. , (2022).
- Barkley, G. L., Baumgartner, C. MEG and EEG in epilepsy. J Clin Neurophysiol. 20 (3), 163-178 (2003).
- Ebersole, J. S., Ebersole, S. M. Combining MEG and EEG source modeling in epilepsy evaluations. J Clin Neurophysiol. 27 (6), 360-371 (2010).
- Yoshinaga, H., et al. Benefit of simultaneous recording of EEG and MEG in dipole localization. Epilepsia. 43 (8), 924-928 (2002).
- Baumgartner, C. Controversies in clinical neurophysiology. MEG is superior to EEG in the localization of interictal epileptiform activity: Con. Clin Neurophysiol. 115 (5), 1010-1020 (2004).
- Barkley, G. L. Controversies in neurophysiology. MEG is superior to EEG in localization of interictal epileptiform activity: Pro. Clin Neurophysiol. 115 (5), 1001-1009 (2004).
- Braeutigam, S. Magnetoencephalography: Fundamentals and established and emerging clinical applications in radiology. ISRN Radiol. 2013, 529463(2013).
- Papadelis, C., et al. Current and emerging potential for magnetoencephalography in pediatric epilepsy. J Pediatr Epilepsy. 2 (1), 73-85 (2013).
- Fiedler, P., Fonseca, C., Supriyanto, E., Zanow, F., Haueisen, J. A high-density 256-channel cap for dry electroencephalography. Hum Brain Mapp. 43 (4), 1295(2022).
- Sharon, D., Hämäläinen, M. S., Tootell, R. B. H., Halgren, E., Belliveau, J. W. The advantage of combining MEG and EEG: comparison to fMRI in focally-stimulated visual cortex. Neuroimage. 36 (4), 1225(2007).
- Pataraia, E., Lindinger, G., Deecke, L., Mayer, D., Baumgartner, C. Combined MEG/EEG analysis of the interictal spike complex in mesial temporal lobe epilepsy. Neuroimage. 24 (3), 607-614 (2005).
- Ahmed Mahmutoglu, M., Rupp, A., Baumgärtner, U. Simultaneous EEG/MEG yields complementary information of nociceptive evoked responses. Clin Neurophysiol. 143, 21-35 (2022).
- Aydin, Ü, et al. Combined EEG/MEG can outperform single modality EEG or MEG source reconstruction in presurgical epilepsy diagnosis. PLoS One. 10 (3), e0118753(2015).
- Bast, T., et al. Combined EEG and MEG analysis of early somatosensory evoked activity in children and adolescents with focal epilepsies. Clin Neurophysiol. 118 (8), 1721-1735 (2007).
- Chikara, R. K., et al. Electromagnetic source imaging predicts surgical outcome in children with focal cortical dysplasia. Clin Neurophysiol. 153, 88-101 (2023).
- Hari, R., et al. IFCN-endorsed practical guidelines for clinical magnetoencephalography (MEG). Clin Neurophysiol. 129 (8), 1720-1747 (2018).
- Bagić, A. I., Knowlton, R. C., Rose, D. F., Ebersole, J. S. American Clinical Magnetoencephalography Society Clinical Practice Guideline 1: Recording and analysis of spontaneous cerebral activity. J Clin Neurophysiol. 28 (4), 348-354 (2011).
- Papadelis, C., Chen, Y. H. Pediatric magnetoencephalography in clinical practice and research. Neuroimaging Clin N Am. 30 (2), 239-248 (2020).
- De Macedo Rodrigues, K., et al. A FreeSurfer-compliant consistent manual segmentation of infant brains spanning the 0-2 year age range. Front Hum Neurosci. 9, 21(2015).
- Tadel, F., Baillet, S., Mosher, J. C., Pantazis, D., Leahy, R. M. Brainstorm: A user-friendly application for MEG/EEG analysis. Comput Intell Neurosci. 2011, 879716(2011).
- Kane, N., et al. A revised glossary of terms most commonly used by clinical electroencephalographers and updated proposal for the report format of the EEG findings. Revision 2017. Clin Neurophysiol Pract. 2, 170-185 (2017).
- Lantz, G., et al. Propagation of interictal epileptiform activity can lead to erroneous source localizations: a 128-channel EEG mapping study. J Clin Neurophysiol. 20 (5), 311-319 (2003).
- Vorwerk, J., et al. A guideline for head volume conductor modeling in EEG and MEG. Neuroimage. 100, 590-607 (2014).
- Schrader, S., et al. DUNEuro-A software toolbox for forward modeling in bioelectromagnetism. PLoS One. 16 (6), e0252431(2021).
- Ntolkeras, G., et al. Presurgical accuracy of dipole clustering in MRI-negative pediatric patients with epilepsy: Validation against intracranial EEG and resection. Clin Neurophysiol. 141, 126-138 (2022).
- David, O., Kilner, J. M., Friston, K. J. Mechanisms of evoked and induced responses in MEG/EEG. Neuroimage. 31, 1580-1591 (2006).
- Pantev, C. Evoked and induced gamma-band activity of the human cortex. Brain Topogr. 7 (4), 321-330 (1995).
- Fox, N. A., et al. Assessing human mirror activity with EEG mu rhythm: A meta-analysis. Psychol Bull. 142 (3), 291-313 (2016).
- Genzer, S., Ong, D. C., Zaki, J., Perry, A. Mu rhythm suppression over sensorimotor regions is associated with greater empathic accuracy. Soc Cogn Affect Neurosci. 17 (9), 788-801 (2022).
- Janmohamed, M., et al. Moving the field forward: detection of epileptiform abnormalities on scalp electroencephalography using deep learning-clinical application perspectives. Brain Commun. 4 (5), 218(2022).
- Bagheri, E., Jin, J., Dauwels, J., Cash, S., Westover, M. B. A fast machine learning approach to facilitate the detection of interictal epileptiform discharges in the scalp electroencephalogram. J Neurosci Methods. 326, 108362(2019).
- Thomas, J., et al. Automated detection of interictal epileptiform discharges from scalp electroencephalograms by convolutional neural networks. Int J Neural Syst. 30 (11), 2050030(2020).
- Zijlmans, M., Zweiphenning, W., van Klink, N. Changing concepts in presurgical assessment for epilepsy surgery. Nat Rev Neurol. 15 (10), 594-606 (2019).
- Akiyama, T., et al. Focal resection of fast ripples on extraoperative intracranial EEG improves seizure outcome in pediatric epilepsy. Epilepsia. 52 (10), 1802-1811 (2011).
- Duncan, J. S., Winston, G. P., Koepp, M. J., Ourselin, S. Brain imaging in the assessment for epilepsy surgery. Lancet Neurol. 15 (4), 420(2016).
- Jacobs, J., et al. High-frequency electroencephalographic oscillations correlate with outcome of epilepsy surgery. Ann Neurol. 67 (2), 209-220 (2010).
- Ricci, L., et al. Virtual implantation using conventional scalp EEG delineates seizure onset and predicts surgical outcome in children with epilepsy. Clin Neurophysiol. 139, 49-57 (2022).
- Stefan, H., Rampp, S. Interictal and Ictal MEG in presurgical evaluation for epilepsy surgery. Acta Epileptologica. 2, 11(2020).
- Jahangiri, F. R., Chima, G. S., Pearson, M., Jackson, J., Siddiqui, A. A. Mapping of the language cortex. Cureus. 13 (5), e14960(2021).
- Merrifield, W. S., Simos, P. G., Papanicolaou, A. C., Philpott, L. M., Sutherling, W. W. Hemispheric language dominance in magnetoencephalography: sensitivity, specificity, and data reduction techniques. Epilepsy Behav. 10 (1), 120-128 (2007).
- Wheless, J. W., et al. Magnetoencephalography (MEG) and magnetic source imaging (MSI). Neurologist. 10 (3), 138-153 (2004).
- Breier, J. I., Simos, P. G., Zouridakis, G., Papanicolaou, A. C. Lateralization of activity associated with language function using magnetoencephalography: a reliability study. J Clin Neurophysiol. 17 (5), 503-510 (2000).
- Pataraia, E., Baumgartner, C., Lindinger, G., Deecke, L. Magnetoencephalography in presurgical epilepsy evaluation. Neurosurg Rev. 25 (3), 141-159 (2002).
- Babajani-Feremi, A., et al. Language mapping using high gamma electrocorticography, fMRI, and TMS versus electrocortical stimulation. Clin Neurophysiol. 127 (3), 1822-1836 (2016).
- Brodbeck, V., et al. Electroencephalographic source imaging: a prospective study of 152 operated epileptic patients. Brain. 134, Pt 10 2887-2897 (2011).
- Sohrabpour, A., et al. Effect of EEG electrode number on epileptic source localization in pediatric patients. Clin Neurophysiol. 126 (3), 472-480 (2015).
- Laohathai, C., et al. Practical fundamentals of clinical MEG interpretation in epilepsy. Front Neurol. 12, 722986(2021).
- Corona, L., et al. Mapping functional connectivity of epileptogenic networks through virtual implantation. Proceedings of the Annu Int Conf IEEE Eng Med Biol Soc. 2021, 408-411 (2021).
- Corona, L., et al. Non-invasive mapping of epileptogenic networks predicts surgical outcome. Brain. 146 (5), 1916-1931 (2023).
- Rijal, S., et al. Functional connectivity discriminates epileptogenic states and predicts surgical outcome in children with drug resistant epilepsy. Sci Rep. 13 (1), 9622(2023).
- Tamilia, E., et al. Noninvasive mapping of ripple onset predicts outcome in epilepsy surgery. Ann Neurol. 89 (5), 911-925 (2021).
- Matarrese, M. A. G., et al. Spike propagation mapping reveals effective connectivity and predicts surgical outcome in epilepsy. Brain. 146 (9), 3898-3912 (2023).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved