Method Article
약물 내성 간질이 있는 소아의 수술 전 평가에서 전자기 소스 이미징
요약
자기 뇌파(MEG)와 고밀도 뇌파 검사(HD-EEG)는 확증 및 보완 정보를 제공하기는 하지만 동시에 기록되는 경우는 드뭅니다. 여기에서는 MEG 및 HD-EEG를 동시에 기록하기 위한 실험 설정과 약물 내성 간질이 있는 소아의 간질 유발 및 웅변 뇌 영역을 국소화하는 것을 목표로 하는 이러한 데이터를 분석하는 방법론을 설명합니다.
초록
약물 내성 간질(DRE)을 앓고 있는 소아의 경우, 발작의 자유는 간질 유발 영역(EZ)의 묘사 및 절제(또는 절제/분리)에 의존하면서 웅변적인 뇌 영역을 보존하는 데 달려 있습니다. 따라서 EZ의 국소화를 위해 임상적으로 유용한 정보를 제공하는 신뢰할 수 있는 비침습적 국소화 방법을 개발하는 것은 성공적인 수술 결과를 달성하는 데 매우 중요합니다. 전기 및 자기 소스 이미징(ESI 및 MSI)은 이러한 환자의 수술 전 평가에 점점 더 많이 활용되고 있으며, 간질 유발 및 유창한 뇌 영역의 묘사에서 유망한 결과를 보여주고 있습니다. 또한 ESI와 MSI를 단일 솔루션, 즉 전자기 소스 이미징(EMSI)으로 결합하여 고밀도 뇌파(HD-EEG) 및 자기 뇌파(MEG) 기록에서 동시 수행된 것은 두 방식 중 하나를 단독으로 사용하는 것보다 더 높은 소스 위치 파악 정확도를 보여주었습니다. 이러한 고무적인 발견에도 불구하고, 이러한 기법은 소수의 3차 뇌전증 센터에서만 수행되고 있으며, 동시에 기록되는 경우는 드물고, 소아 코호트에서는 충분히 활용되지 않고 있다. 이 연구는 DRE가 있는 소아의 자극 영역, 발작 시작 영역 및 웅변적인 뇌 영역을 국소화하는 것을 목표로 하는 이러한 데이터를 분석하기 위한 방법론적 프레임워크뿐만 아니라 MEG 및 HD-EEG 데이터를 동시에 기록하기 위한 실험 설정을 보여줍니다. 보다 구체적으로, (i) 수면 중 간질 및 간질 활동을 기록하고 국소화하고, (ii) 시각, 운동, 청각 및 체성 감각 유발 반응을 기록하고, 시각 운동 작업 중 관련 웅변 뇌 영역(즉, 시각, 운동, 청각 및 체성 감각)을 매핑하고 청각 및 체성 감각 자극을 매핑하기 위한 실험 설정이 제시됩니다. 등가 전류 쌍극자(ECD) 및 동적 통계 파라메트릭 매핑(dSPM)을 사용하여 EMSI와 개별 ESI 및 MSI를 수행하기 위한 데이터 분석 파이프라인의 자세한 단계가 추가로 제시됩니다.
서문
간질은 가장 흔하고 장애를 일으키는 신경 질환 중 하나로, 본질적으로 국소적이거나 일반화될 수 있는 재발적이고 이유 없는 발작을 특징으로 합니다. 여러 가지 효과적인 약물 요법(예: 항경련제[ASM])을 사용할 수 있음에도 불구하고 이러한 환자의 약 20-30%는 발작을 통제할 수 없으며 약물 내성 간질(DRE)을 앓고 있습니다1. 이러한 환자들에게는 간질 수술이 발작을 없애는 가장 효과적인 치료법입니다. 성공적인 수술은 발작 발생에 필수적인 최소 영역으로 정의되는 간질 유발 영역(EZ)의 완전한 절제(또는 절제/분리)를 통해 이루어질 수 있다2. EZ의 정확한 묘사 및 절제(또는 절제/분리)는 웅변 피질을 보존하면서 발작의 자유를 보장하는 데 중요한 요소입니다. 외과적 후보를 확립하기 위해 다학제 팀은 여러 비침습적 진단 도구를 사용하여 EZ3의 간접 근사치 역할을 하는 다양한 피질 영역(즉, 자극 영역, 발작 시작 영역[SOZ], 기능 결핍 영역 및 간질 유발 병변)을 정의합니다. 두개내 EEG(iEEG)를 사용한 수술 외 모니터링은 이러한 방법 중 어느 것도 EZ를 명확하게 식별하지 못하는 경우 필요합니다. iEEG의 역할은 SOZ(즉, 임상적 발작이 생성되는 뇌 영역)를 국소화하여 EZ를 정확하게 정의하고 웅변적인 뇌 영역을 매핑하는 것입니다. 그러나 침습성으로 인해 심각한 한계가 있고4,5,6 공간적 커버리지가 제한적이며, 명확한 수술 전 국소화 가설(presurgical localization hypothesis)이 필요하다7. 그 결과, SOZ의 실제 초점과 범위를 놓치게 되어 수술에 실패할 수 있습니다. 또한, 이를 해석하려면 며칠 간의 입원 기간 동안 여러 가지 정형화된 임상 발작을 기록해야 하며, 이는 합병증(예: 감염 및/또는 출혈)의 가능성을 증가시킵니다.5. 따라서 임상적으로 유용한 정보를 제공하고 DRE가 있는 소아의 수술 전 평가를 전반적으로 개선할 수 있는 신뢰할 수 있는 비침습적 국소화 방법을 개발해야 할 필요성이 충족되지 않았습니다.
지난 수십 년 동안 전기 및 자기 소스 이미징(ESI 및 MSI)은 간질 유발 및 기능적 뇌 영역을 묘사하기 위해 DRE 환자의 수술 전 평가에 점점 더 많이 활용되고 있습니다. 특히, ESI 및 MSI는 고밀도 EEG(HD-EEG) 및 자기뇌파(MEG)와 같은 비침습적 기록에서 신경 소스를 재구성할 수 있어 수술 계획 또는 iEEG 전극 배치를 안내하는 데 도움이 됩니다. ESI 및 MSI는 스파이크 및 날카로운 파도와 같은 간질 간질 방출(IED) 또는 ictal(발작) 활동의 국소화에 적용할 수 있습니다. 또한 감각, 운동, 청각 및 인지 기능과 관련된 다양한 기능적 뇌 영역의 국소화에 사용될 수 있습니다. IED 및 발작과 같은 전기생리학적 사건의 재구성을 통해 자극 영역(즉, IED가 발생하는 뇌 영역)과 SOZ를 각각 식별할 수 있으며, 이는 EZ 국소화를 위한 유효한 대리물로 간주됩니다. 웅변 피질(즉, 정의된 대뇌 피질 기능에 필수적인 뇌 영역)3의 국소화는 계획된 절제술과 관련하여 웅변 영역의 위치와 범위를 매핑할 수 있게 하며, 따라서 간질 수술에서 예상할 수 있는 잠재적인 기능적 결함을 미리 줄일 수 있다 8,9,10,11. 여러 연구에서 간질의 수술 전 평가에서 ESI 및/또는 MSI의 임상적 유용성을 조사한 결과, EZ 12,13,14,15,16,17,18,19의 설명에서 유망한 결과를 보여주었습니다. 예를 들어, Mouthaan 등[14]은 11건의 전향적 및 후향적 간질 연구의 비침습적 데이터를 사용하여 광범위한 메타 분석을 수행했으며, 이러한 소스 국소화 기법이 전반적으로 높은 민감도(82%)와 낮은 특이성(53%)으로 EZ를 식별할 수 있다고 보고했습니다. 다른 연구에서도 MSI와 ESI가 정상적인 자기 공명 영상(MRI)을 가진 간질 환자의 절제 영역 내에서 간질 초점을 정확하게 국소화할 수 있음을 보여주었습니다19,20,21. 이러한 국소화 결과는 결정적이지 않은 임상 또는 영상 소견으로 인해 뇌전증 수술을 받을 수 없는 환자에게 특히 중요합니다. 요약하면, ESI와 MSI는 DRE 환자의 간질 유발 및 기능적 뇌 영역의 수술 전 매핑에 크게 기여할 수 있습니다.
이러한 고무적인 발견에도 불구하고, 이러한 기법은 현재 소수의 3차 뇌전증 센터에서만 정기적으로 시행되고 있으며, 소아 환자에서는 충분히 활용되지 못하고 있습니다. 더욱이, HD-EEG와 MEG는 확증 및 보완 정보를 모두 제공하기는 하지만, 동시에 기록되는 경우는 드뭅니다. MEG는 접선 방향의 표면 소스를 감지하는 데 민감하지만 뇌의 자이리 또는 더 깊은 영역에 위치한 방사형 방향 소스에는 눈이 멀어있습니다 22,23,24,25,26. 또한 MEG는 EEG 16,22,25에 비해 더 나은 공간 해상도(밀리미터)를 제공합니다. EEG 신호와 달리 MEG 신호는 참조가 없으며 본질적으로 뇌 조직(예: 수막, 뇌척수액, 두개골 및 두피)의 다양한 전도도에 영향을 받지 않으므로 뇌에서 생성되는 자기장을 왜곡 없이 측정할 수 있습니다.25,27 반면에, EEG는 모든 방향의 소스를 검출할 수 있지만, MEG보다 낮은 공간 해상도를 제공하고 인공물26,28에 더 취약하다. 근원 배향 및 깊이에 대한 이러한 상보적인 민감성으로 인해, 간질 활동(예를 들어, IED)의 대략 30%는 MEG에서만 기록될 수 있고 EEG에는 기록될 수 없으며, 그 반대의 경우도 마찬가지이다 26,29,30,31,32. 장시간 기록이 가능한 EEG와 달리, MEG로 임상 발작을 캡처하는 것은 일반적으로 대부분의 환자에서 ictal 이벤트를 기록하기에 충분하지 않은 제한된 기록 시간으로 인해 어렵습니다. 더욱이, 발작과 관련된 머리 움직임에 의해 야기된 아티팩트는 종종 MEG 기록의 품질을 방해할 수 있다(29,33,34,35). 반면에, MEG 기록은 EEG에 비해 더 빠르고 쉬우며, 특히 어린이의 경우 어린이의 머리 위에 센서를 부착할 필요가 없기 때문에 어린이의 경우 더욱 그러하다(35).
하드웨어의 발전으로 머리 전체를 커버하는 많은 수의 센서(550개 이상의 센서)를 사용하여 MEG 및 HD-EEG 데이터를 동시에 기록할 수 있게 되었습니다. 더욱이, 뇌파 기술의 현대적 발전으로 HD-뇌파의 준비 시간이 15분 미만으로 단축되었다36. 이는 오랜 시간 동안 가만히 있을 수 없는 도전적인 행동을 보이는 소아 환자에게 특히 중요합니다. 또한 소프트웨어 기술의 발전으로 ESI와 MSI를 단일 솔루션, 즉 HD-EEG 및 MEG 동시 기록에서 수행되는 전자기 소스 이미징(EMSI)으로 결합할 수 있게 되었습니다. 여러 이론 및 경험적 연구에서 EMSI를 사용한 소스 위치 파악 정확도가 두 양식 중 하나보다 더 높다고 보고했습니다 13,30,31,37,38,39,40,41. 감각 자극에 대한 반응으로 활동을 재구성하기 위해 다양한 소스 위치 파악 접근 방식을 사용하여, Sharon et al.37 연구는 EMSI가 정확한 국소화 정확도의 비침습적 벤치마크 역할을 하는 기능적 MRI(fMRI)에 비해 ESI 또는 MSI 단독보다 일관되게 더 나은 국소화 결과를 제공한다는 것을 발견했습니다. 저자들은 이러한 개선된 국소화가 역해를 풀기 위한 센서의 수가 증가하고 두 이미징 양식의 서로 다른 민감도 패턴 때문이라고 제안했다(37). 마찬가지로, Yoshinaga et al.31은 난치성 국소화 관련 뇌전증 환자의 EEG 및 MEG 동시 데이터에 대해 쌍극자 분석을 수행한 결과, EMSI가 한 가지 양식만으로는 얻을 수 없는 정보를 제공하고 분석 대상 환자 중 한 명에서 간질 수술의 국소화를 성공적으로 이끌었다는 것을 보여주었습니다. 전향적 맹검 연구에서, Duez et al.도 13은 EMSI가 ESI 및 MSI에 비해 유의하게 높은 승산비(즉, 발작이 없을 확률)를 달성했으며, 국소화 정확도≥52%), 자극성 및 SOZ와의 일치율≥53% 및 ≥36%를 각각 달성했음을 보여주었습니다. 그룹42의 보다 최근 연구에 따르면 EMSI는 절제 및 SOZ의 국소화 오류가 각각 ~8mm 및 ~15mm로 ESI 또는 MSI 단독보다 우수한 국소화 추정치와 더 나은 결과 예측 성능을 제공하는 것으로 나타났습니다. 이러한 유망한 연구 결과에도 불구하고, DRE를 앓고 있는 소아의 EMSI에 관한 방법론적 틀을 제공하는 연구는 부족하다.
이 연구는 MEG 및 HD-EEG 동시 기록을 수행하기 위한 실험 설정과 DRE가 있는 소아의 자극 영역, SOZ 및 웅변 뇌 영역을 국소화하는 것을 목표로 하는 이러한 데이터를 분석하기 위한 방법론적 프레임워크를 보여줍니다. 보다 구체적으로, (i) 수면 중 간질 및 간질 간질 활동을 기록하고 국소화하고, (ii) 시각, 운동, 청각 및 체성 감각 유발 반응을 기록하고, 시각 운동 작업 중 관련 웅변 뇌 영역(즉, 시각, 운동, 청각 및 체성 감각)을 매핑하고 청각 및 체성 감각 자극을 매핑하기 위한 실험 설정이 제시됩니다. 등가 전류 쌍극자(ECD) 및 동적 통계 파라메트릭 매핑(dSPM)을 사용하여 EMSI와 개별 ESI 및 MSI를 수행하기 위한 데이터 분석 파이프라인의 자세한 단계가 추가로 제시됩니다.
프로토콜
여기에 적용된 실험 절차는 North Texas Regional Institutional Review Board(2019-166; 수석 연구원: Christos Papadelis). 다음 섹션에서는 우리 실험실에서 수행된 동시 MEG 및 HD-EEG 기록을 사용하여 IED, ictal 발병 및 이벤트 유발 반응(즉, 시각, 운동, 청각 및 체성 감각)의 비침습적 소스 국소화를 위한 실험 프로토콜에 대해 설명합니다. 국제임상신경생리학연맹(International Federation of Clinical Neurophysiology)43 및 미국임상MEG학회(American Clinical MEG Society)44 는 자발적 MEG 및 EEG 데이터의 일상적인 임상 기록 및 분석을 위한 "최소 표준"을 제공하였다. 여기에 설명된 HD-EEG 기록 절차는 스펀지 기반 EEG 전극 시스템에만 적용됩니다. 각 주제에 대한 전체 준비 과정은 약 2-3시간이며 ~1.5시간의 실제 녹음으로 구성됩니다.
1. MEG 시스템 준비
- 피험자가 도착하기 전에 몇 분 동안 빈 방에서 MEG 녹음을 수행하여 배경 소음 수준과 자기 인공물을 캡처하고 모든 MEG 센서가 제대로 작동하는지 확인합니다.
- MEG 센서 튜닝 프로그램을 사용하여 모든 MEG 센서의 평균 백색 잡음 값이 2에서 5fT/√Hz(그래디오미터의 경우 fT/cm√Hz 사이인지 확인합니다).
2. 피험자의 준비
- 피험자가 환경에 편안함을 느끼는지 확인하십시오. 어린이의 경우 기록실(MSR(Magnetically Shielded Room) 포함)을 탐색하고 데이터 수집에 사용할 테스트 장비를 볼 수 있도록 합니다.
- 심사 동의서를 사용하여 주제 지침을 선별하고 제공합니다. 필요한 경우, 각 연령 그룹에 맞게 개발된 특별한 단어, 장난감 및 게임을 사용하여 어린 아이들에게 절차를 설명하십시오. 피험자(또는 피험자의 부모)에게 방문 전 마지막 ~2시간 이내에 발작이 있었는지 물어보십시오.
참고: 선별 동의서에는 검사에 대한 설명, 검사의 안전성, 검사를 수행하는 이유 및 연구에 대한 전반적인 설명이 포함됩니다.
- 심사 동의서를 사용하여 주제 지침을 선별하고 제공합니다. 필요한 경우, 각 연령 그룹에 맞게 개발된 특별한 단어, 장난감 및 게임을 사용하여 어린 아이들에게 절차를 설명하십시오. 피험자(또는 피험자의 부모)에게 방문 전 마지막 ~2시간 이내에 발작이 있었는지 물어보십시오.
- 피험자로부터 금속 및/또는 자성 물질을 제거하고 피험자에게 병원에서 지급한 적절한 의복(예: 병원 가운, 수술복)을 제공합니다. 또한, 자성 먼지가 MSR에 유입되는 것을 방지하기 위해 피험자에게 신발을 벗도록 요청하십시오. 치과 공사 또는 이식된 의료 기기와 같은 다른 강자성 요소를 제거할 수 없는 경우 소자(즉, 소자)를 사용하여 MEG 기록 중에 간섭 또는 높은 노이즈 수준을 유발할 수 있는 잔류 자기 아티팩트를 제거합니다. 모든 자기 노이즈 소스가 제거되었는지 확인한 후, 피험자에게 다음 측정 절차가 적용될 나무 의자에 앉아서 편안하게 앉도록 요청하십시오.
알림: 디가우저는 이식된 전자 장치(예: 심박 조율기, 신경 조절 장치)에 직접 적용해서는 안 됩니다. - 피험자의 머리 둘레를 측정하여 적절한 EEG 그물 크기(보통 32-34cm에서 최대 58-61cm)를 선택합니다. 측정 테이프의 센티미터 쪽을 사용하여 피험자의 내열에서 이니온 위로 ~1cm까지 테이프를 잡은 다음 다시 니온으로 이동하여 머리 둘레를 측정합니다.
참고: 비온(nasion)은 눈 사이의 두개골점(craniometric point)인 반면, 이온(inion)은 외부 후두부 돌출부(external occipital protuberance)의 끝부분입니다.- 피험자의 머리 둘레에 맞는 올바른 그물 크기를 선택하고 따뜻한 수돗물 1qt, 전해질(즉, 염화칼륨) 1tsp, 베이비 샴푸 1tbsp로 구성된 액체 혼합 용액에 최소 5분(최대 10분) 동안 담그십시오. 이 담그는 과정에서 스폰지가 바깥쪽을 향하도록 그물을 뒤집고 걸쇠를 완전히 풀어 용액이 들어있는 플라스틱 통 내부의 센서를 완전히 담그도록 합니다.
알림: 그물의 ampliifier가 용액 근처에 오지 않고 항상 건조한 상태를 유지하려면 선택한 그물의 플러그를 수건으로 감고 바람직한 경우 플라스틱 양동이가 있는 싱크대 가까이의 의자나 지지대에 놓습니다.
- 피험자의 머리 둘레에 맞는 올바른 그물 크기를 선택하고 따뜻한 수돗물 1qt, 전해질(즉, 염화칼륨) 1tsp, 베이비 샴푸 1tbsp로 구성된 액체 혼합 용액에 최소 5분(최대 10분) 동안 담그십시오. 이 담그는 과정에서 스폰지가 바깥쪽을 향하도록 그물을 뒤집고 걸쇠를 완전히 풀어 용액이 들어있는 플라스틱 통 내부의 센서를 완전히 담그도록 합니다.
- 미세기공 종이 테이프를 사용하여 피험자의 두피에 직접 알려진 위치에 머리 위치 지시자(HPI) 코일 역할을 하는 5개의 자기 코일을 배치합니다: 헤어라인 근처 이마의 양쪽에 하나씩, 각 유양돌기 뼈에 하나씩, 머리 꼭대기에 하나씩 놓습니다.
참고: HPI 코일은 스캔 중에 국소화될 수 있는 알려진 자기장을 방출하여 MEG 시스템 내부에 배치된 초전도 양자 간섭 장치(SQUID)에 대한 헤드의 위치를 정의합니다. HPI 코일의 수는 MEG 시스템에 따라 다르지만 일반적으로 3-5 HPI 코일 범위입니다. - 심박수(심전도, ECG), 안구 움직임 또는 깜박임(전기 안구 검사, EOG) 및 근육 활동(근전도, EMG)을 측정하기 위해 테이프를 사용하여 추가 전극을 배치합니다. 이러한 전극을 배치하면 피험자의 건강 상태를 모니터링 할 수도 있습니다.
- 쇄골 아래 가슴의 오른쪽과 왼쪽에 각각 두 개의 ECG 전극을 배치하여 피험자의 심장 박동을 기록하고 오른쪽 눈의 위쪽과 아래쪽에 각각 두 개의 EOG 전극을 배치하여 수직 안구 움직임 또는 깜박임을 기록합니다.
- 시각 운동 작업 중 근육 활동을 측정하려면 테이프가 피부에 더 잘 접착되도록 알코올 패드로 피험자의 손가락을 닦고 각 손에 총 두 쌍의 일회용 컵 전극을 테이프로 붙입니다: 하나는 첫 번째 등쪽 골간(FDI)에, 다른 하나는 외전근 폴리시스 브레비스(APB)에 있습니다.
- 이 모든 전극을 테이프로 붙이기 전에 전도성 페이스트를 전극 컵 내부에 약간 과도하게 채워 피부 임피던스를 줄이고 접착력과 전도성의 최적 혼합을 보장합니다.
- 촉각 자극을 위해 얇은 탄성막을 양손의 세 자리 손가락(즉, 엄지[D1], 중지[D3], 새끼손가락[D5])의 원위부에 직접 부착합니다. 공기 분풍 자극 장치를 사용하여 단단한 플라스틱 튜브를 통해 압축 공기 펄스로 멤브레인을 팽창시킵니다. 의사 난수 순서에 따라 1.5 ± 0.5초의 자극 간 간격으로 압축 공기 펄스를 방출합니다. 촉각 자극기의 압력을 50psi로 조정합니다.
- 쇄골 아래 가슴의 오른쪽과 왼쪽에 각각 두 개의 ECG 전극을 배치하여 피험자의 심장 박동을 기록하고 오른쪽 눈의 위쪽과 아래쪽에 각각 두 개의 EOG 전극을 배치하여 수직 안구 움직임 또는 깜박임을 기록합니다.
- 피험자가 금속 물체에서 멀리 떨어진 나무 의자에 앉아 있는 동안, 디지타이저를 사용하여 기준의 해부학적 랜드마크, 5개의 HPI 코일 및 기타 머리 모양 점의 3차원(3D) 위치를 결정합니다. 이 머리 디지털화 과정 동안, 피험자에게 편안하게 앉아서 앞을 똑바로 바라보고, 작은 움직임이 위치 파악 정확도에 영향을 미칠 수 있으므로 거의 움직이지 않도록 요청하십시오.
- 피사체의 머리에 있는 플라스틱 고글(즉, 기준 큐브가 한쪽에 부착된 안경)을 통해 기준 수신기를 놓고 걸쇠를 조정하여 전체 측정 동안 상대적으로 가만히 있어야 하는 피사체에 대한 고정 기준 프레임을 보장합니다.
- 기본 스타일러스 수신기를 통해 기준 해부학적 랜드마크(즉, 비강 및 좌/오른쪽 귓바퀴 지점)와 HPI 코일의 위치를 찾고 추가 두피 지점(최소 100개, 바람직하게는 ~500에 가까움)을 균일하게 샘플링하여 머리 표면의 고품질 재구성을 향상시킵니다.
참고: 기준 해부학적 랜드마크는 피사체 좌표계를 정의합니다. 디지타이저는 하나의 송신기(일반적으로 나무 의자 등받이의 피사체 뒤에 장착)와 두 개의 수신기(즉, 스타일러스 및 참조 수신기)를 사용하여 3D 공간에서 센서의 좌표를 생성합니다. - 디지털화가 완료되면 스타일러스 수신기를 피사체와 송신기에서 ~15cm 떨어진 곳에 놓고 임의의 지점을 디지털화하여 디지털화 프로세스를 완료합니다.
참고: 디지털화 프로세스의 이 마지막 단계는 다른 상용 제품과 다를 수 있습니다.
- EEG 그물을 적용하기 전에 피험자에게 EEG 증폭기에 가까운 의자에 앉도록 요청하고 가슴과 어깨에 수건을 올려 그물의 적용으로 인해 최종적으로 떨어지는 물방울을 흡수하도록 요청합니다. 플라스틱 양동이에서 EEG 그물을 제거하고 스폰지가 안쪽을 향하도록 뒤집은 다음 수건으로 부드럽게 감싸서 혼합 용액을 과도하게 흡수시킵니다.
- 피험자를 의자에 앉히고 이 단계에서 눈을 감고 있으라는 지시를 받은 후, 두 손을 그물 안에 넣고 손가락을 펴서 마지막으로 피험자의 머리에 올려놓는다.
- HPI 코일의 위치를 움직이지 않고 손가락을 사용하여 피험자의 머리에 있는 늘어난 그물을 조정하여 기준 채널과 비강 채널이 각각 두피 중앙과 피험자의 눈 사이에 올바르게 위치하도록 하고 마지막으로 그물이 올바른 위치에 오면 턱끈을 조입니다.
- EEG 임피던스 미터를 사용하여 신호 왜곡을 방지하기 위해 모든 두피 전극 임피던스가 0-50kΩ 범위(값 ˂5kΩ 권장)에 있는지 확인하십시오. 두피 전극 임피던스를 줄이려면 나무 면봉을 사용하여 전극과 두피 사이의 피험자의 머리카락을 제거하거나 일회용 플라스틱 피펫을 사용하여 필요한 경우 전도성이 더 높은 혼합 용액을 전극의 스폰지로 전달하여 각 전극이 두피와 기계적, 전기적 접촉이 양호한지 확인하십시오.
- 모든 임피던스가 이상적으로 최대 50kΩ이 되면 증폭기를 분리하고 EEG 전극 디지털화를 위해 피사체를 준비합니다.
알림: MSR 외부에서 EEG 전극 디지털화를 수행하고 스캐닝 프로세스를 관리할 수 있는 충분한 공간을 확보하십시오.
- 모든 임피던스가 이상적으로 최대 50kΩ이 되면 증폭기를 분리하고 EEG 전극 디지털화를 위해 피사체를 준비합니다.
- 휴대용 광학 스캐너를 사용하여 EEG 전극의 3D 위치를 결정합니다. 이 과정에서, 피험자에게 달리 지시되지 않는 한 편안하게 앉아서 앞을 똑바로 보도록 요청한다.
- 먼저 광학 스캐너 소프트웨어를 열고 녹화 중에 사용된 EEG 센서 레이아웃과 일치하는 센서 템플릿을 선택한 다음 스캔 프로세스를 시작합니다.
- 스캔하는 동안 스캐너를 EEG 그물에서 일정 거리(보통 ~45cm)를 유지하고 스캔 구멍이 센서 표면에 수직이 되도록 하고 상단(머리 중앙)에서 하단(목을 따라 마지막 센서 열)까지 아치형 띠를 따라 피사체의 머리 주위로 천천히 움직여 모든 센서의 물리적 위치를 기록합니다.
참고: 광학 스캐너는 피험자의 머리에 있는 EEG 전극 위치를 디지털화하여 3D 좌표 파일로 변환합니다. 일반적으로 적외선(IR) 광원을 방출하는 두 개의 광학 센서가 특징입니다. 스캔된 각 위치는 일반적으로 3D 센서 클라우드에 나타납니다. 3D 센서 클라우드는 센서 위치의 스캐닝, 프로빙 및 정렬에 대한 피드백을 제공하는 반면, 2D 센서 맵은 이러한 센서 위치의 라벨링에 대한 피드백을 제공합니다. EEG 전극 위치의 스캐닝 과정에는 기준점 프로빙을 포함하여 총 5-10분이 필요합니다. 그러나 스캐닝 시간은 때때로 전극 위치를 감지하는 광학 스캐너의 성능에 따라 달라질 수 있습니다.
- 모든 EEG 전극이 스캔되면(최소 95%) 무선 광학 프로브를 사용하여 기준점(즉, 비강 및 왼쪽/오른쪽 귓바퀴 지점)과 4개의 정렬 센서(즉, 전면, 왼쪽 및 오른쪽 정렬 노드 및 REF 노드)를 프로브하여 3D 센서 클라우드를 선택한 센서 템플릿에 정렬합니다.
알림: 정렬 센서는 EEG 센서 네트 구성에 따라 번호가 매겨집니다.- 기준점을 조사하려면 스캐너의 스캐닝 조리개가 프로브의 반사 디스크를 가리키도록 하여 광학 프로브의 팁을 관심 기준점의 중앙에 있는 피사체의 피부에 놓습니다. 마찬가지로, 광학 프로브의 팁을 관심 있는 정렬 센서의 중앙에 배치하여 정렬 센서를 프로브합니다.
- 모든 센서를 스캔하고 프로브한 후에는 실제 EEG 네트를 기준으로 3D 센서 클라우드 및 2D 센서 맵에서 센서의 위치와 라벨을 검토하여 가능한 오류를 확인하고 최종적으로 수정합니다. 스캔 프로세스 중에 오류가 발생하지 않으면 3D 좌표 .txt 파일을 내보내고 원하는 형식으로 변환합니다.
참고: 3D 전극 좌표는 일반적으로 .txt 형식으로 저장되며 광학 스캐너 소프트웨어를 통해 여러 형식(예: .xml, .sfp, .elp 또는 .nsi)으로 변환할 수 있습니다. - EEG 전극 디지털화 과정(2.9-2.11단계)이 완료된 후 휴식/수면 데이터(2.13단계), 시운동 작업(2.14단계), 청각 자극(2.15단계) 및 체성 감각 자극(2.16단계)을 수행하기 위해 피험자를 MSR 내부로 전송할 준비를 합니다.
- 휴식/수면 데이터의 경우 MEG 시스템의 갠트리를 누운 자세로 설정하고(그림 1A) 탈착식 머리 받침대가 듀어 하단의 헬멧 모양 개구부와 정렬되도록 비자성 및 호환 가능한 침대를 배치합니다. 침대를 올바른 위치로 조정한 후 침대의 브레이크 밸브를 꺼짐 잠금 위치로 설정하십시오. 침대 위에 시트나 담요를 깔고 탈착식 머리 받침대에 작은 폼 패드 베개를 놓아 녹음하는 동안 머리를 고정하고 편안하게 합니다.
참고: 듀어는 액체 헬륨으로 채워진 극저온 저장 용기로, 센서 어레이는 피사체의 머리를 둘러싸도록 설계된 헬멧 모양의 구멍을 통해 바닥에 공간적으로 배열되어 있습니다. 헬멧은 머리 둘레가 최대 59-61cm에 맞습니다. 갠트리는 듀어를 지원하는 기계 시스템으로, 측정 위치(즉, 앉은 자세 또는 누운 자세)에 따라 고도와 각도를 수정할 수 있습니다.- 피험자를 MSR 안으로 옮기고 침대 가장자리에 앉거나 눕도록 도와줍니다. 피험자의 몸에 담요를 여러 장 덮어 녹음하는 동안 전극의 케이블에 쉽게 접근할 수 있도록 하고, 안전 벨트를 가볍게 조이고(또는 난간이 있는 경우 난간을 당겨 올리며), 이 단계는 피험자가 자는 동안 침대에서 굴러 떨어지는 것을 방지하기 위한 것임을 설명한다. 필요한 경우, 피험자의 목과 어깨를 지지할 수 있도록 목 아래에 돌돌 말아 놓는다.
- 침대의 브레이크 밸브를 열어 피험자의 머리를 부드럽게 움직인 다음, 듀어의 헬멧 모양 개구부 아래에 있는 탈착식 머리 받침대에 올려 헬멧 안쪽에 닿을 때까지 움직입니다. 신호 대 잡음비(SNR)를 높이려면 피험자의 머리를 헬멧에 최대한 가깝게 가져오세요.
- MEG 시스템의 해당 패널에 HPI 코일, ECG 및 EOG 전극을 연결하고, EEG 네트를 MSR 내부의 증폭기 장치에 연결하고, MSR 외부의 획득 워크스테이션에서 머리 좌표 측정값을 확인하여 피험자의 머리가 듀어 아래에 적절하게 위치했는지 평가합니다.
- 피험자의 동의하에 MSR 내부의 빛의 강도를 줄여 이완과 수면을 자극합니다. 피험자가 편안하고 편안하다고 느끼면 녹음 중에 피험자에게 눈을 감고 쉬거나 잠을 자도록 지시하십시오. 전체 녹화 동안 MSR 벽에 장착된 무선 주파수 차폐 컬러 카메라를 통해 MSR 외부의 모니터에서 관찰될 것이라고 피험자를 안심시킵니다.
- 시각 운동 작업을 위해 MEG 시스템의 갠트리를 수직 위치로 설정하고(그림 1B) MEG 의자를 배치하여 피험자의 머리가 듀어 하단의 헬멧 모양 개구부에 가깝게 갠트리 아래에 오도록 합니다. 의자를 올바른 위치로 조정한 후 의자의 브레이크 밸브를 잠금 해제 위치("0")로 설정하십시오.
- MSR 내부로 피사체를 전송합니다. 그/그녀가 비자성적이고 호환 가능한 의자에 앉아서 편안하고 편안한 자세를 찾도록 도와주세요. 피험자의 몸에 담요를 여러 장 깔아 전극의 케이블에 쉽게 접근할 수 있도록 하여 녹음하는 동안 피험자를 따뜻하게 하고, 작업 중에 피험자가 손을 얹을 수 있도록 탈착식 테이블을 배치합니다. 필요한 경우, 앉은 자세를 유지하는 데 도움이 되도록 피험자의 무릎 아래에 수건을 놓고, 아래로 미끄러지지 않도록 한다.
참고: 피험자는 시각 운동 작업 중에 긴장을 풀어 처음 자세보다 낮은 자세를 취할 수 있으므로, 각 작업 세션이 끝날 때 엘리에이트 페달(있는 경우)을 통해 의자를 조심스럽게 들어 올리거나 의자 위에 수건이나 담요를 올려 피험자의 머리가 헬멧 안쪽에 다시 닿도록 한다. 필요한 경우, 피험자의 머리 뒤에 수건이나 담요를 추가로 놓아 편안함을 더할 뿐만 아니라 피험자가 머리를 가능한 한 곧게 유지할 수 있도록 돕는다. Visuomotor 자극은 녹음 세션 중간에 듀어가 움직이지 않도록 앙와위 자세에서 번갈아 수행할 수 있습니다. - 피험자가 올바른 위치에 놓이면, MEG 기계의 오른쪽 패널에 있는 HPI 코일, ECG, EOG, FDI 및 APB 전극을 꽂고, EEG 네트를 MSR 내부의 증폭기 장치에 연결하고, 작은 움직임으로 상승 페달(있는 경우)을 통해 의자를 들어 올리거나 피험자의 머리가 헬멧 안쪽에 가볍게 닿을 때까지 의자에 추가 수건이나 담요를 놓습니다(헬멧 내부의 측정값 확인). MSR 외부의 획득 워크스테이션에서 가져온 head의 좌표).
- MSR 외부에 위치한 프로젝터 미러 시스템을 통해 시각적 자극이 투사되는 프로젝션 스크린을 피사체 앞에 배치하고(그림 1B) 녹화 중에 수행해야 할 시운동 작업을 설명합니다. 특히, 피험자에게 오른손과 왼손에 각각 시각적 자극(예: 이미지)이 화면에 나타날 때만 검지 손가락으로 테이블을 두드리도록 지시합니다. 피험자가 작업을 이해하거나 혼자 수행하는 데 편안함을 느끼는지 확인하십시오. 필요한 경우, 피험자가 과제에 익숙해질 수 있도록 피험자와 함께 과제를 여러 번 연습한다.
알림: 시운동 자극 세션이 누운 자세에서 수행되는 경우 거울은 프로젝터의 시각적 자극을 반사하기 위해 피사체의 얼굴보다 멀리 배치됩니다. - MSR의 문을 닫기 전에, 피험자에게 방 안에 혼자 있는 것이 편한지 물어본다. 그렇지 않은 경우, 팀 중 한 명 또는 부모님은 녹음 세션 동안 MSR 내에 남아 있습니다. 더욱이, 피험자가 전체 녹화 동안 MSR 외부의 모니터에서 관찰될 것이라고 안심시킨다.
- MSR 내부로 피사체를 전송합니다. 그/그녀가 비자성적이고 호환 가능한 의자에 앉아서 편안하고 편안한 자세를 찾도록 도와주세요. 피험자의 몸에 담요를 여러 장 깔아 전극의 케이블에 쉽게 접근할 수 있도록 하여 녹음하는 동안 피험자를 따뜻하게 하고, 작업 중에 피험자가 손을 얹을 수 있도록 탈착식 테이블을 배치합니다. 필요한 경우, 앉은 자세를 유지하는 데 도움이 되도록 피험자의 무릎 아래에 수건을 놓고, 아래로 미끄러지지 않도록 한다.
- 청각 자극을 위해 2.14단계에서 설명한 설정을 앉아 있는 피험자 앞에 투사 스크린을 사용합니다. 피험자가 사운드 트리거(예: 변조된 짹짹거리는 소리)가 전달되는 헤드폰(또는 이어폰)을 착용하도록 도와줍니다.
- 피험자에게 소리 트리거를 듣는 동안 화면에 투사된 자극(예: 검은색 배경의 녹색 점)을 고정하도록 지시합니다. 필요한 경우, 피험자가 절차를 더 잘 이해할 수 있도록 훈련 세션을 수행한다. MSR의 도어를 닫기 전에 앞에서 설명한 대로 안전 절차를 반복하십시오.
- 체성 감각 자극의 경우 2.14단계에서 설명한 설정을 사용합니다. 피험자에게 자신 앞에 있는 프로젝터 스크린에서 어떤 비디오(또는 영화)를 보고 싶은지 물어보십시오.
- 피험자에게 눈을 뜨고 긴장을 풀고, 선택한 비디오를 보고, 가능한 한 가만히 있으고, 녹화 중 손가락에 전달되는 촉각 자극을 무시하도록 지시합니다. 피험자에게 각 손의 손가락 끝에서 각각 피부를 부드럽게 두드리는 것을 느낄 것이라고 설명하십시오. 피험자가 불편함을 느끼면 그를 안심시키기 위해 훈련 세션을 수행하십시오.
참고: 시각적 대상에 눈을 고정하는 것은 녹음 품질에 영향을 미치고 데이터 수집 중에 전달되는 촉각 자극으로부터 피사체의 주의를 산만하게 할 수 있는 생물학적 아티팩트를 최소화하기 위한 잘 정립된 기술입니다.
- 피험자에게 눈을 뜨고 긴장을 풀고, 선택한 비디오를 보고, 가능한 한 가만히 있으고, 녹화 중 손가락에 전달되는 촉각 자극을 무시하도록 지시합니다. 피험자에게 각 손의 손가락 끝에서 각각 피부를 부드럽게 두드리는 것을 느낄 것이라고 설명하십시오. 피험자가 불편함을 느끼면 그를 안심시키기 위해 훈련 세션을 수행하십시오.
3. 데이터 수집
참고: 동시 MEG 및 EEG 데이터 수집은 Cook Children's Medical Center(CCMC)의 MEG 시설에서 수행됩니다. 간질이 있는 소아 소아에 대한 MEG의 임상적 사용에 대한 자세한 내용은 다른 곳에서 찾을 수 있습니다 8,27,45.
- 1개의 자력계와 2개의 직교 평면 그래디오미터가 있는 102개의 동일한 트리플 센서 요소로 그룹화된 306개의 채널이 특징인 전체 헤드 MEG 시스템(센서 범위: 1,220cm2)을 사용하여 MEG 신호를 기록합니다. 샘플링 주파수를 1kHz 이상으로 설정합니다.
알림: 단일 코일 자력계는 MEG 헬멧 표면에 수직인 자기장의 구성 요소를 측정합니다. 평면 그래디오미터는 서로 사이의 작은 거리에 배치된 한 쌍의 자력계를 특징으로 하는 "8자형" 코일 구성으로 구성되며 위치 사이의 자기장 차이(즉, "8"의 두 루프 간의 차이)를 측정하며 공간 구배라고도 합니다. 자력계와 비교했을 때, 평면 그래디오미터는 뇌 심부 소스에 덜 민감하지만 환경 소음을 억제하여 표면 소스를 감지하는 데 더 강력합니다. 이 306 채널은 -296 ° C (4.2 K)의 액체 헬륨에 담그고 냉각되어 초전도체가됩니다. - 두피, 뺨 및 목 뒤쪽에 균일한 간격으로 배치된 Ag/AgCl 전극 센서가 있는 비자기 256채널 EEG 네트를 사용하여 EEG 신호를 동시에 기록합니다. 샘플링 주파수를 1kHz 이상으로 설정합니다.
- MSR의 도어를 닫아 녹음을 시작합니다. 음성 인터콤 시스템을 통해 피험자와 의사소통을 하고, 피험자가 MSR 안에 혼자 있는 것이 편한지 확인한다. 비디오에서 피사체를 지속적으로 모니터링하고 응급 상황 시에는 즉시 MSR에 진입하십시오.
참고: 환자가 불편함을 느끼거나 육중한 MSR 문이 위협적으로 느껴지는 경우, 팀원 중 한 명이나 부모님이 녹음 세션 동안 피험자 가까이의 나무 의자에 앉아 MSR 내부에 머물 수 있습니다. 방에 들어가기 전에 모든 금속 물체가 제거되었는지 확인하십시오. - 각 녹음 전에 음성 인터콤 시스템을 통해 피험자에게 작업을 시작하기 전에 ~30초 동안 위치를 움직이지 않도록 지시합니다. 시각 운동 작업의 경우 첫 번째 녹음 세션에 사용할 검지(오른쪽 또는 왼쪽)를 인터콤을 통해 추가로 통신합니다.
- 피사체가 가만히 있는 이 시간 동안, MEG 데이터 수집 시스템의 HPI 측정 대화 상자에서 측정 버튼을 눌러 HPI 코일에 공급되는 전류에 의해 생성된 자기장을 측정하고 MEG 센서 어레이에 대한 헤드 측정 위치를 결정합니다. 따라서 피사체가 올바른 위치에 있는지 확인하고(머리 |z 좌표| ˂ 75mm) 각 세션에 대한 3D 측정값을 기록하십시오.
- 피험자의 머리와 헬멧 사이에 아직 공간이 남아 있다면, MSR 내부로 다시 들어가 상승 페달(있는 경우)을 통해 의자의 높이를 조정하거나, 의자 위에 수건이나 담요를 놓거나, 인터콤을 통해 피험자에게 머리를 헬멧에 더 가까운 위치로 옮기는 방법을 지시한다(피험자가 앉아 있는 경우). 마지막으로 머리 측정 위치를 다시 확인하십시오. 휴식/수면 녹음의 경우 MSR에 다시 들어가 침대를 헬멧에 더 가깝게 가져와 머리와 헬멧의 공간 간격을 줄입니다.
- 피험자가 MEG 헬멧에 잘 배치되고 시작할 준비가 되면 정확한 MEG 및 EEG 동기화(3.12단계 참조)를 위해 정확한 순서(3.5.1단계 참조)에 따라 첫 번째 녹음 세션(지속 시간 ~10분)을 시작합니다.
참고: 고품질 녹음을 보장하기 위해 첫 번째 녹음 세션은 피사체의 움직임 또는 외부 환경으로 인해 데이터에 존재하는 아티팩트를 캡처하는 데 중요합니다. 필요한 경우, MSR 내부로 다시 들어가 최종 채널 연결 또는 MEG 의자에서 피험자의 위치를 조정한다. 녹음 중에 비정상적인 아티팩트나 이벤트를 기록해 두었다가 나중에 다시view필요한 경우 필요한 경우.- EEG 데이터 수집 소프트웨어의 기록 버튼을 눌러 EEG 기록을 시작합니다. MEG 데이터 수집 소프트웨어의 녹음 버튼을 눌러 MEG 녹음을 시작합니다. 마지막으로 자극 컴퓨터의 소프트웨어에서 시작 버튼을 눌러 시각적 자극을 표시하거나 청각 자극을 전달합니다.
알림: 시각(또는 청각) 자극 소프트웨어를 실행하는 자극 컴퓨터는 MSR 외부의 프로젝터 미러 시스템에 연결되어 수행된 녹화 유형에 따라 켜거나 끌 수 있습니다. 휴식/수면 녹음 중에는 피험자가 쉬고 있거나 잠을 자고 있기 때문에 시스템이 꺼지지만, 자극 컴퓨터에서 시각 자극 소프트웨어를 실행하면 각 녹음 세션의 타이밍을 맞추는 데 도움이 됩니다. 시각 운동 과제 동안, 청각 및 체성 감각 자극 동안, 피험자가 소프트웨어가 실행되는 동안 자신 앞에 놓인 화면에 투사된 자극 또는 비디오를 관찰할 수 있도록 함으로써 시스템이 켜집니다. 이 연구를 위해 총 (i) 시각 운동 작업을 위해 각 자극 사이에 ~ 4 초 간격으로 총 107 개의 자극 (즉, 바둑판 배경과 22 개의 바둑판 배경에 오버레이 된 85 개의 이미지)을 선택했습니다. (ii) 청각 자극을 위해 3초의 자극 간 간격으로 200개의 변조된 짹짹 소리; (iii) 체성 감각 자극에 대해 ~1.5초의 자극 간 간격을 가진 반 무작위 시퀀스를 따르는 각 손가락(즉, D1, D3 및 D5)에 대한 200개의 촉각 자극.
- EEG 데이터 수집 소프트웨어의 기록 버튼을 눌러 EEG 기록을 시작합니다. MEG 데이터 수집 소프트웨어의 녹음 버튼을 눌러 MEG 녹음을 시작합니다. 마지막으로 자극 컴퓨터의 소프트웨어에서 시작 버튼을 눌러 시각적 자극을 표시하거나 청각 자극을 전달합니다.
- 녹음을 중지하려면 MEG 데이터 수집 소프트웨어의 중지 버튼을 누른 다음 EEG 데이터 수집 소프트웨어의 중지 버튼을 누릅니다. 각 녹음 세션이 끝나면 인터콤을 통해 피험자와 의사 소통하여 피험자를 안심시키고 MSR 내부의 채널 연결이나 위치 조정이 필요하지 않은 경우 다음 세션을 진행합니다.
- 시각 운동 작업의 경우 각 세션에 대해 다른 시각적 자극을 선택하여 녹음하는 동안 피험자에게 동기를 부여하고 즐겁게 유지합니다.
- 시각 운동 또는 휴식/수면 데이터의 경우 1-5개의 세션으로 특징지어지는 총 ~6시간의 동시 MEG 및 EEG 기록을 기록합니다. 그러나 세션 수는 과목마다 다를 수 있습니다. 또한 청각 및 체성 감각 자극 데이터에 대해 각각 총 ~20분(각 ~10분씩 1-2개 세션) 및 ~14분(각 ~7분씩 1-2개 세션)의 동시 MEG 및 EEG 기록을 기록합니다.
참고: 이 연구에서 MEG 및 EEG 데이터는 CCMC의 IT 저장 시스템에 각각 .fif 및 .mff 형식으로 녹음의 끝에 자동으로 저장됩니다. - 녹음이 끝나면 MSR을 입력하여 피험자가 의자나 침대에서 일어설 수 있도록 돕고 MSR 외부의 의자에 앉도록 요청하여 EEG 그물과 전극을 모두 제거합니다.
- 다른 지시가 있을 때까지 피험자에게 눈을 감으라고 지시하고, 턱끈을 완전히 풀고 두 손(이마에서 머리 뒤쪽으로)을 사용하여 그물이 완전히 벗겨질 때까지 부드럽게 잡아당겨 EEG 그물을 제거하는 데 도움을 줍니다. 이 단계에서 그물을 제거하는 동안 피사체의 머리카락을 잡아당기지 않도록 하십시오. 또한 피험자가 이전에 피부에 테이프로 붙인 나머지 전극(즉, 시각 운동 작업의 경우 ECG, EOG 및 EMG)을 부드럽게 제거하도록 돕습니다.
- EEG 그물과 전극을 제거한 후 피험자(및 부모)에게 모든 절차가 최종적으로 완료되었음을 알립니다.
- 피험자가 방을 나간 후에는 광학 스캐너를 조심스럽게 청소하고(사용 설명서에 설명된 대로) 보호 케이스 안에 보관하십시오.
- 녹음 중에 사용된 모든 장비(예: 의자, 침대, 책상)의 표면을 병원에서 승인한 과산화수소 물티슈 또는 소독 스프레이 및 종이 타월로 세척 및 소독하고, 사용한 담요와 수건을 병원에서 제공한 용기에 넣고, 사용한 테이프 조각은 버리십시오.
- 측정 도구를 보관 캐비닛 내부에 보관하고 흐르는 수돗물에 나무 면봉을 사용하여 전도성 페이스트로 채워진 전극 컵 내부를 청소합니다.
- EEG 그물을 헹구려면 싱크대의 플라스틱 통에 깨끗하고 따뜻한 수돗물을 채우고 다음 단계를 총 4회 반복합니다.
- EEG 그물을 물에 담그고 EEG 그물을 10-20초 동안 부드럽게 저어줍니다(또는 양동이 안팎에 ~25회 담그십시오).
- 양동이에서 물을 빼내고 깨끗하고 따뜻한 수돗물로 양동이에 다시 채우십시오.
- EEG 그물을 소독하려면 싱크대의 플라스틱 양동이에 미지근한 수돗물 2qt와 소독제 1tbsp로 구성된 소독 용액을 채우고 그 안에 있는 EEG 그물을 10분 동안 담그십시오. 소독 용액에서 버킷을 헹구고 헹굼 및 배수 과정을 세 번 수행하여 EEG 그물에서 잔류 용액을 제거합니다.
- 헹굼 또는 소독 과정을 위해 양동이에서 담근 EEG 그물을 제거하고 깨끗하고 마른 수건으로 과도한 물을 제거하여 건조시킨 다음 싱크대 가까이에 걸어 보관하십시오.
- MEG 데이터에서 내부 및 외부 자기 간섭 및 측정/이동 아티팩트를 억제하려면 tSSS(Signal Space Separation) 방법의 시간 확장을 원시 데이터 MEG .fif 파일에 적용합니다.
알림: tSSS(Spatiotemporal Maxwell Filtering)는 MEG 센서 어레이 내부 또는 매우 가까운 간섭원, 즉 내부 간섭을 억제하는 데 이상적입니다. - MEG 및 EEG 동시 기록을 수행할 때 피사체 머리의 해부학적 랜드마크를 기준으로 두 수집 장치의 좌표계를 공간적으로 정렬하고(그림 2A) 가능한 다른 샘플링 속도로 인해 발생하는 신호 간의 선형 클럭 드리프트를 수정합니다(그림 2B).
참고: 레코딩 중에 MEG 및 EEG 신호는 시작 및 종료 버튼을 누를 때 발생할 수 있는 지연과 트리거가 MEG 및 EEG 데이터 수집 소프트웨어로 전송될 때 발생하는 내부 클럭 드리프트로 인해 시간이 지남에 따라 느린 이동의 영향을 받을 수도 있습니다. 이러한 신호 간의 정확한 동기화를 보장하기 위해 데이터 수집 중에 두 시스템에서 전송된 트리거 이벤트를 공통 트리거 신호로 사용하는 Python으로 사내 코드를 개발했습니다. 이 코드에는 MNE-Python 소프트웨어 라이브러리에서 사용할 수 있는 세 가지 기능, 즉 MEG 및 EEG 신호를 읽는 두 가지 기능과 채널 이름 및 타임스탬프(즉, 이벤트 발생 날짜 및 시간)와 같은 신호에서 트리거 이벤트 정보를 추출하는 한 가지 기능이 포함되어 있습니다. 각 신호(즉, 델타)에서 트리거 이벤트가 발생하는 시점 간의 시간 차이는 시간 경과에 따른 선형 클럭 드리프트를 정의합니다(그림 2B). 개발된 코드에 대한 자세한 설명은 다음 단계에서 제공됩니다(3.12.1-3.12.4 참조).- 각 신호에서 발생하는 첫 번째 트리거 이벤트 간의 차이를 오프셋 값(즉, 두 신호 중 하나에서 트리밍할 부분)으로 사용하여 녹음을 정렬합니다.
참고: mne.io.read_raw_fif 및 mne.io.read_raw_egi 기능은 MEG 및 EEG 기록을 2D 어레이 형식으로 변환하는 반면, mne.find_events 기능은 원시 신호에서 이벤트 정보를 추출합니다. - 이러한 첫 번째 트리거가 정렬되면 Pearson의 상관 계수를 계산하여 신호 간의 상관 정도를 평가합니다. 완벽한 정렬을 위해 1 x 10-6< p-값이 권장됩니다.
참고 : scipy 라이브러리의 pearsonr 함수는 MEG와 EEG 신호 간의 Pearson의 상관 계수와이 상관 관계의 p 값을 추정합니다. - 이 상관 관계의 정확도를 검증하려면 1차 다항식 피팅을 수행하여 두 신호 간의 드리프트 속도를 추정하고 다항식 함수의 계수로 표시되는 결과적인 디스패리티 정도를 사용하여 다항식 피팅의 x축에서 신호를 다시 샘플링합니다(그림 2B).
참고 : numpy 라이브러리의 polyfit 함수는 다항식 함수 내에서 MEG 및 EEG 신호를 피팅합니다. 이 함수는 두 신호 간의 차이 정도를 나타내는 계수를 반환합니다. mne.resample 함수는 다항식 함수의 계수에 따라 MEG 신호와 EEG 신호를 리샘플링합니다. - 리샘플링이 완료된 후 각 신호에서 발생하는 마지막 트리거 이벤트의 타임스탬프를 비교하고 MEG 및 EEG 신호 모두에서 일반적이지 않은 시간 창을 제거합니다. 마지막으로, 동기화된 MEG 및 EEG 신호를 병합하여 추가 분석에 사용할 수 있는 MEG 및 EEG 센서를 모두 특징으로 하는 단일 기록을 만듭니다.
알림: mne.add_channels 기능은 두 신호를 병합하여 단일 녹음을 만듭니다.
- 각 신호에서 발생하는 첫 번째 트리거 이벤트 간의 차이를 오프셋 값(즉, 두 신호 중 하나에서 트리밍할 부분)으로 사용하여 녹음을 정렬합니다.
- 각 ~1.5시간 기록이 끝날 때 데이터 분석을 위해 시각 운동(및 휴식/수면), 청각 및 체성 감각 자극 데이터에 대해 각각 동기화된 MEG 및 EEG 기록의 총 5-6(각 ~10분), 1-2(각 ~10분) 및 1-2(각 ~7분) 세션을 사용합니다.
참고: 이상적으로는, 피험자는 세 번의 시각 운동 녹음에 대해 오른쪽 손가락으로 두드리고, 나머지 세 번의 시각 운동 녹음에 대해 왼쪽 손가락으로 두드려야 합니다.
4. 데이터 분석
- 자극 영역의 매핑
- 인간의 뇌 MR 이미지를 처리, 분석 및 시각화하기 위한 오픈 소스 신경 영상 도구인 FreeSurfer의 대뇌 피질 재구성 프로세스를 사용하여 피험자의 MRI에서 3D 피질 표면을 생성합니다46.
- MEG 및 EEG 데이터 시각화 및 처리47 전용 MATLAB 오픈 소스 응용 프로그램인 Brainstorm에서 재구성된 해부학적 구조를 가져와 대뇌 피질 재건 결과를 시각화합니다. Brainstorm에서 피사체 좌표계를 정의하는 가져온 MRI의 기준점(즉, nasion, left/right preauricular, anterior/posterior commissure 및 interhemispheric)을 설정합니다.
- 브레인스톰에서 동시 MEG 및 HD-EEG 신호를 가져오고 MRI 등록 프로세스를 사용하여 MEG 및 EEG 센서를 MRI에 등록하여 디지털화된 기준점에 대한 정렬을 조정합니다. 필요한 경우 EEG 센서를 피질 표면에 투영합니다.
- MEG 및 HD-EEG 동시 녹화를 열고 원시 데이터를 육안으로 검사하여 불량 채널을 제거합니다. 또한 브레인스톰 에서 사용할 수 있는 SSP(신호 공간 투영) 아티팩트 보정 기술을 적용하여 녹음에서 생물학적 아티팩트(예: 심장 박동, 눈 깜박임)를 거부합니다.
- 동시 MEG 및 HD-EEG 데이터에 노치(전력선 간섭에 따라 50 또는 60Hz) 및 대역 통과(1-70Hz) 필터를 적용합니다.
- 스파이크 및 날카로운 파도와 같은 빈번한 IED를 특징으로 하는 내부 활동이 포함되고 최소한의 모션 아티팩트(가능한 경우)가 있는 데이터 부분을 선택합니다.
참고: IED는 <70ms의 시간적 진화, >50μV 진폭 및 1-70Hz 주파수 대역48의 배경 활동과 명확하게 구별할 수 있는 날카로운 모양을 특징으로 하는 과도 파형입니다. 그림 3A 는 동시 MEG 및 HD-EEG 신호에서 빈번한 IED를 볼 수 있는 부분의 예를 나타냅니다. - 페이지당 10초의 표준 디스플레이 설정을 사용하여 MEG 및 EEG 기록(그림 3A)과 각 양식에서만 발생하는 각 IED의 음의 피크를 표시합니다. 각 IED를 표시하기 전에 MEG 및 EEG에 대한 지형 필드와 전위 지도를 각각 확인하십시오.
주의: 각 IED의 상승 단계 동안의 추가 시점의 전압 분포는, 그 피크가 아니라, 가능한 전파 간질 활동49을 설명하기 위해 또한 확인되어야 한다. 브레인스톰 을 사용하여 간극 스파이크 이벤트를 표시하는 방법에 대한 자세한 내용은 다른 곳(https://neuroimage.usc.edu/brainstorm/Tutorials/Epilepsy)에서 확인할 수 있습니다. - 브레인스톰에서 사용할 수 있는 OpenMEEG BEM(대칭 경계 요소 방법) 소프트웨어를 사용하여 3층(즉, 두피, 두개골 내부 및 외부 두개골) 기하학적 모델(그림 3B)로 정의된 사실적인 머리 모델을 계산합니다. MRI 볼륨을 소스 공간(공간 해상도가 5mm인 소스 포인트 그리드)으로 사용합니다.
참고: OpenMEEG BEM 소프트웨어는 대칭 경계 요소 방법을 사용하여 두피(즉, 공기-두피 인터페이스), 외부 두개골(즉, 두피-두개골 인터페이스) 및 내부 두개골(두개골-뇌 인터페이스)을 특징으로 하는 사실적인 전방 모델을 계산합니다. 대안 솔루션으로, 유한요소법(FEM)은 헤드 체적 도체의 현실적인 주제별 표현을 허용하기 때문에 순방향 문제를 해결하는 데 사용할 수 있습니다. 두부 조직 전도도 값은 종종 문헌에서 추정되며 피험자(50)의 연령에 따라 달라질 수 있습니다. FEM을 사용하여 순방향 모델을 풀려면 Brainstorm47,50,51에서 사용할 수 있는 DUNEuro FEM 소프트웨어를 사용하여 3개에서 최대 5개(즉, 백질, 회백질, 뇌척수액, 두개골 및 피부) 기하학적 모델로 정의된 사실적인 머리 모델을 계산합니다. FEM을 사용한 순방향 모델 추정에 대한 자세한 내용은 다른 곳(https://neuroimage.usc.edu/brainstorm/Tutorials/Duneuro)에서 확인할 수 있습니다. - MEG, EEG, 결합된 MEG 및 EEG 센서 어레이에서 개별적으로 제약되지 않은 ECD 방법을 사용하여 선택한 내부 스파이크의 기본 생성기를 국소화합니다. 이러한 쌍극자 소스의 위치를 파악하려면 빈 방 MEG 기록에서 잡음 공분산을 계산하거나 이를 항등 행렬로 설정하십시오.
참고: IED의 SNR이12로 낮은 경우 대체 접근 방식으로 유사한 전압 분포를 가진 평균 IED에서 소스 위치 파악을 수행하는 것을 고려하십시오. - 이전에 표시된 각 IED의 피크에서 Brainstorm 에서 사용할 수 있는 쌍극자 스캔 방법을 수행하여 전체 뇌 부피에서 가장 중요한 소스 쌍극자를 선택합니다. 적합도가 >60%인 소스 쌍극자만 선택하고 중심에서 15mm 떨어진 쌍극자의 수로 각 쌍극자에 대해 정의된 집집을 추정합니다(그림 3C).
참고: ECD 클러스터니스에 대한 자세한 내용은52에서 확인할 수 있습니다.
- SOZ의 매핑
- FreeSurfer46의 대뇌 피질 재구성 프로세스를 사용하여 피험자의 MRI에서 3D 피질 표면을 생성합니다.
- Brainstorm47에서 재구성된 해부학을 가져와 대뇌 피질 재건 결과를 시각화합니다. 가져온 MRI에서 피사체 좌표계를 정의하는 기준점을 설정합니다.
- 브레인스톰에서 동시 MEG 및 HD-EEG 신호(ictal 이벤트 포함)를 가져오고 MRI 등록 프로세스를 사용하여 MEG 및 EEG 센서를 MRI에 등록하여 디지털화된 기준점에 대한 정렬을 조정합니다. 필요한 경우 EEG 센서를 피질 표면에 투영합니다.
참고: 피험자가 녹음 중에 발작을 일으킨 경우, 다시view 녹음 중에 기록한 메모를 확인하여 ictal 사건이 어느 세션에서 녹음되었는지 평가하십시오. - MEG 및 HD-EEG 동시 녹화를 열고 원시 데이터를 육안으로 검사하여 불량 채널을 제거합니다. 브레인스톰47 에서 사용할 수 있는 SSP 아티팩트 수정 기술을 적용하여 기록에서 생물학적 아티팩트(예: 심장 박동, 눈 깜박임)를 거부합니다.
- 동시 MEG 및 HD-EEG 데이터에 노치(전력선 간섭에 따라 50 또는 60Hz) 및 대역 통과(1-70Hz) 필터를 적용합니다.
- 녹음 노트에 따르면 발작의 시작과 종료(명시된 경우)를 식별하고 이러한 이벤트를 신호에 표시하여 ictal epileptiform disations를 포함하는 데이터의 올바른 부분을 식별합니다. 발작 시작의 예는 각각 MEG 및 HD-EEG에 대한 그림 4 에 표시되어 있습니다.
참고: 피험자가 MEG 획득 중 발작을 일으키면 의료진은 즉시 피험자를 돕고 응급 치료를 제공해야 합니다. 따라서, ictal 이벤트가 있는 이러한 데이터 부분의 지속 시간은 짧을 수 있습니다. - 페이지당 10초의 표준 디스플레이 설정을 사용하여 MEG 및 EEG의 ictal 이벤트 동안 발생하는 각 간질 방전(예: 반복적인 스파이크, 날카로운 파도 또는 스파이크-웨이브 복합체)의 음의 피크를 표시합니다. 각 피크 마킹 전에 MEG 및 EEG에 대한 지형 필드와 전위 맵을 각각 확인합니다(그림 4A).
참고: 발작은 발병이 시작되는 위치에 따라 전신 발작 또는 국소 발작으로 분류됩니다. 간질 증후군에 따라 다르지만 발작은 빈도, 진폭 및 형태가 다를 수 있는 반복적인 전기 방전을 특징으로 하는 최소 10초의 현상입니다. - 브레인스톰에서 사용할 수 있는 OpenMEEG BEM 소프트웨어를 사용하여 MEG 및 EEG 센서에 대한 3층(즉, 두피, 내부 두개골 및 외부 두개골)의 사실적인 머리 모델을 계산합니다. MRI 볼륨을 소스 공간(공간 해상도가 5mm인 소스 포인트 그리드)으로 사용합니다.
참고: FEM을 사용하여 순방향 모델을 풀려면 Brainstorm 47,50,51에서 사용할 수 있는 DUNEuro FEM 소프트웨어를 사용하여 3층에서 최대 5층(즉, 백질, 회백질, 뇌척수액, 두개골 및 피부) 기하학적 모델로 정의된 사실적인 머리 모델을 계산합니다. FEM을 사용한 순방향 모델 추정에 대한 자세한 내용은 다른 곳(https://neuroimage.usc.edu/brainstorm/Tutorials/Duneuro)에서 확인할 수 있습니다. - MEG, EEG, 결합된 MEG 및 EEG 센서 어레이에서 개별적으로 제약되지 않은 ECD 방법을 사용하여 선택한 ictal 방전의 기본 발생기를 국소화합니다. 이러한 쌍극자 소스의 위치를 파악하려면 빈 방 MEG 기록에서 잡음 공분산을 계산하거나 이를 항등 행렬로 설정하십시오.
- 이전에 표시된 각 ictal 파형의 피크에서 Brainstorm 에서 사용할 수 있는 쌍극자 스캔 방법을 수행하여 전체 뇌 부피에서 가장 중요한 소스 쌍극자를 선택합니다. 적합도가 >60%인 소스 쌍극자만 선택하고 클러스터니스를 추정합니다(각 쌍극자 중심에서 쌍극자까지의 거리는 15mm로 설정)52.
- 웅변 피질의 매핑
- 시각 운동 작업 중과 청각 및 체성 감각 자극 중에 기록된 신호를 사용하여 앞에서 설명한 4.2.1-4.2.3 단계를 수행합니다.
- 동시 MEG 및 HD-EEG 기록을 열고 원시 데이터를 육안으로 검사하여 불량 채널을 제거합니다. 이와 별도로 각 세션에 대해 브레인스톰47 에서 사용할 수 있는 SSP 아티팩트 수정 기술을 적용하여 녹음에서 생물학적 아티팩트(예: 심장 박동, 눈 깜박임)를 거부합니다. 또한 추가 분석에 사용할 수 없는 아티팩트로 오염된 모든 데이터 세그먼트를 삭제하거나 "잘못된 간격"으로 표시합니다.
- 동시 MEG 및 HD-EEG 데이터에 노치(전력선 간섭에 따라 50 또는 60Hz) 및 대역 통과(1-100Hz) 필터를 적용합니다.
- 운동 피질을 매핑하기 위해 FDI 및 APB 전극에서 기록된 EMG 신호를 열고 FDI 쌍 전극의 기준선과 다른 근육 활성화의 첫 번째 피크를 선택하여 피험자가 수행한 두드리기 이벤트를 오른손과 왼손에 별도로 수동으로 표시합니다. Brainstorm47을 사용하여 각 세션에 대해 이 단계를 개별적으로 수행합니다.
참고: 브레인스톰에서만 시각화를 위해 필터 탭을 사용하고 탭하는 동안 EMG 활동의 피크를 올바르게 표시하는 데 도움이 되는 주파수 범위(예: 고역 통과: 30Hz, 저역 통과: 300Hz, 노치: 60Hz)를 선택합니다. 이벤트의 이름은 세션 간에 동일해야 합니다. 예를 들어, 피험자가 오른쪽 손가락(또는 왼쪽 손가락)으로 탭할 때 발생하는 이벤트는 "Tap_right"(또는 "Tap_left")로 명명될 수 있습니다. 이 단계를 통해 모든 세션에서 발생한 동일한 유형의 이벤트에 대해 고유한 분석을 수행할 수 있습니다. - 각 세션에서 다음 매개변수를 선택하여 아티팩트가 없는 세그먼트에서 발생하는 이벤트를 가져옵니다: 시각적 자극: 자극 시작 전 [-200; 0] ms의 기준선을 포함한 [-200; +500] ms 시간 창; 탭핑 이벤트: [-1500; +1000]ms 시간 창, 시각적 자극 시작 전 [-1500; -1000]ms의 기준선을 포함합니다. 변조된 짹짹 소리: 자극 시작 전 [-500; 0] ms의 기준선을 포함한 [-500; +1000] ms 시간 창; 촉각 자극: 자극 시작 전 [-100; 0]ms의 기준선을 포함한 [-100; +500]ms 시간 창.
- 모든 세션에서 특정 작업의 이벤트를 가져오면 평균 참조 몽타주를 적용하여 EEG 데이터의 SNR을 늘리고 자극 전체의 평균을 추정하여 이벤트 유발 필드와 전위를 얻습니다. 운동 작업(예: 두드리기) 및 촉각 자극의 경우 이 마지막 단계는 각각 오른손과 왼손에 대해 수행됩니다.
참고: 그림 5, 그림 6, 그림 7 및 그림 8의 패널 A와 B는 MEG 및 EEG에 대한 시각, 운동, 청각 및 체성 감각 유발 반응의 예를 보여줍니다. 특정 작업에 대한 총 자극 수는 완료된 세션의 수에 따라 엄격하게 달라집니다. 모터 작업의 경우 이 숫자는 올바르게 수행된 태핑 작업에 따라 달라집니다. - 시각, 운동, 청각 또는 체성 감각 유발 필드 및 전위에 대해 Brainstorm에서 사용할 수 있는 OpenMEEG BEM 소프트웨어를 사용하여 MEG 및 EEG 센서에 대한 3층(즉, 두피, 내부 두개골 및 외부 두개골)의 사실적인 머리 모델을 계산합니다. 3D 피질 표면을 소스 공간으로 사용합니다.
참고: FEM을 사용하여 순방향 모델을 풀려면 Brainstorm 47,50,51에서 사용할 수 있는 DUNEuro FEM 소프트웨어를 사용하여 3층에서 최대 5층(즉, 백질, 회백질, 뇌척수액, 두개골 및 피부) 기하학적 모델로 정의된 사실적인 머리 모델을 계산합니다. FEM을 사용한 순방향 모델 추정에 대한 자세한 내용은 다른 곳(https://neuroimage.usc.edu/brainstorm/Tutorials/Duneuro)에서 확인할 수 있습니다. - 각 이벤트 유발 필드와 전위에 대해 MEG, EEG 및 결합된 MEG 및 EEG 센서 어레이에 대해 Brainstorm 도구 상자에 구현된 dSPM을 사용하여 평균 이벤트에 대한 피질 소스를 계산합니다. 각 작업에 특정한 사전 자극 기준선 기간을 사용하여 노이즈 공분산 행렬을 설정합니다(4.3.5단계 참조).
- 작업에 따라 아틀라스를 사용하거나 해당 위치에서 가상 센서(즉, 관심 영역, ROI)의 재구성을 통해 정의할 수 있는 관련 웅변 뇌 영역[일차 시각 피질(V1), 일차 운동 피질(M1), 일차 청각 피질(A1) 또는 일차 체성 감각 피질(S1)]에서 관찰된 최대 피질 소스를 추출합니다(그림 5C, 그림 6C, 그림 7C 및 그림 8C).
- 선형 스케일(주파수 범위: 1:1:100Hz)을 사용하여 관련된 웅변적인 뇌 영역(V1, M1, A1 또는 S1)에서 이벤트 유발 필드 및 잠재적 소스에 대해 Morlet 웨이블릿 시간-주파수 분해를 수행합니다.
주의: 자극 시작에 시간-및 위상-고정되는 유발된 진동을 추정하기 위해, MEG/EEG 신호는 처음에 이벤트에 대해 평균화된 후 시간-주파수 분석(53,54)의 대상이 된다. - Brainstorm에서 사용할 수 있는 이벤트 관련 섭동 방법을 사용하여 대뇌 피질 소스 맵의 표준화를 수행하여 각 이벤트(그림 5D, 그림 6D, 그림 7D 및 그림 8D)에 대해 개별적으로 기준선(4.3.5단계 참조)을 기준으로 정규화합니다.
참고: 이벤트 관련 섭동을 사용한 소스 맵의 표준화는 기준선에 대한 평균과의 편차를 백분율로 추정하는 시간-주파수 전력 맵에 대한 정규화 측정입니다. 이 표준화 프로세스에 대한 자세한 내용은 다른 곳(https://neuroimage.usc.edu/brainstorm/Tutorials/TimeFrequency#Normalized_time-frequency_maps)에서 확인할 수 있습니다.
- 유효성 검사
- 경막하 그리드 및/또는 깊이 전극의 이식을 통해 수술 외 iEEG 기록을 획득합니다. 두개내 전극의 수, 유형 및 배치는 수술 전 평가의 비침습적 진단 검사에서 얻은 정보의 합계에서 생성된 임상 가설을 기반으로 다학제 뇌전증 팀에 의해 결정됩니다.
참고: 수술 전 평가의 일환으로 수술 외 iEEG는 1,024Hz 샘플링 속도를 사용하여 디지털 EEG 시스템을 통해 며칠에 걸쳐 기록됩니다. - 각 피험자에 대해 사용할 수 있는 임상 정보를 기반으로 전문 간질 전문의가 정의한 SOZ를 식별합니다.
참고: SOZ는 임상적으로 정의된 ictal 발병 전 또는 동시에 발생할 수 있는 배경 활동과 다른 첫 번째 명백한 ictal 전기 방전을 보여주는 뇌 영역으로 정의됩니다. 이 ictal 전기 방전에 관련된 모든 채널은 다른 뇌 영역에서 발생하는 발작을 포착하더라도 SOZ 접촉으로 간주됩니다. - iEEG에 기록된 ictal 이벤트 동안 각 두개내 전극에서 발생하는 각 간질 방전의 피크를 표시하고 이전에 4.1.7-4.1.10단계에서 설명한 대로 ECD 방법을 사용하여 이러한 ictal 이벤트에 대한 소스 국소화를 수행합니다.
- 소스 국소화 결과의 황금 표준으로 임상적으로 정의된 SOZ와 관련하여 iEEG 국소화 결과를 비교합니다.
- 경막하 그리드 및/또는 깊이 전극의 이식을 통해 수술 외 iEEG 기록을 획득합니다. 두개내 전극의 수, 유형 및 배치는 수술 전 평가의 비침습적 진단 검사에서 얻은 정보의 합계에서 생성된 임상 가설을 기반으로 다학제 뇌전증 팀에 의해 결정됩니다.
결과
DRE가 있는 소아 환자는 Jane and John Justin Institute for Mind Health, Cook Children's Health Care System(CCHCS)의 간질 클리닉에서 모집되었습니다. 여기에는 (i) 10세 여성, (ii) 13세 남성, (iii) 10세 여성의 대표 환자 3명의 데이터가 제시됩니다.
사례 1: 10세 된 한 여자아이가 3살 때부터 발작을 일으켜 입원했다. 환자는 8번의 ASM을 투여한 후에도 매일 발작을 일으켰습니다. 초기 발작은 눈 편차(불분명한 측면)와 행동 정지를 특징으로 했습니다. 나중에, 환자는 ictal pouting ( "chapeau de gendarme"신호), 머리가 왼쪽으로 편향 및 양측 긴장 팔 경직 (오른쪽 우세)을 특징으로하는 ~ 30 초의 발작을 매일 경험했습니다. 장기 비디오 뇌파 검사 결과 머리가 왼쪽으로 치우친 후 왼쪽 팔이 올라오는 비대칭 긴장성 발작이 두 차례 발견되었습니다. 잠자는 동안에도 세 번의 긴장성 발작이 관찰되었으며, 간헐적으로 눈을 뜨고, 위를 바라보고, 왼팔 또는 오른팔을 들어 올리는 전신 빠른 폴리스파이크와 느린 파동이 자주 발생했습니다. 이 폴리스파이크(polyspikes)와 슬로우 슬립 파(slow-sleep waves)는 주로 왼쪽 중간 측두엽에서 두드러졌다. 뇌 MRI에서 다음과 같은 다초점 이형성증이 발견되었습니다: (i) 좌측 두정엽(postcentral gyrus) transmantle sign이 있는 국소 피질 이형성증(FCD), (ii) 우측 두정후두 접합부 FCD, (iii) 좌측 측두극 FCD. 양전자 방출 단층촬영(PET)은 MRI 검사에서 신호 이상(즉, FCD)의 초점에 해당하는 좌측 두정엽, 좌측 측두엽 및 우측 두정후두 접합부에서 대사 저하를 보여주었습니다. 환자는 난치성 간질로 진단되었으며, chapeau의 고정 관념 기호학에 이어 강장제 팔 경직이 뒤따랐으며, 이는 근심 전두엽 또는 섬/측두엽 발병 가능성을 시사합니다. 광범위한 양측 stereo-EEG(sEEG) 탐색은 전두엽, cingulate, insular 및 이형성증 영역을 대상으로 하여 권장되었습니다. iEEG 모니터링 중에 환자는 "chaeau de gendarme"을 동반한 전형적인 발작을 일으킨 후 양측 전방 인공두에 걸쳐 최대로 미만성 EEG 발병을 특징으로 하는 오른쪽 또는 왼쪽 상지의 긴장 상승/굴곡이 뒤따랐습니다. 다초점 IED는 주로 좌측 전측두엽과 배외측 전두엽 피질에서 관찰되었으며, 이중에는 양측 인슐라(insula)가 포함되었다. iEEG 기록에 대해 수행된 ESI는 좌측 및 우측 배외측 전두엽 피질과 전방 인슐라에서 임상적으로 양측으로 정의된 SOZ의 위치를 확인했습니다.
수술 전 평가의 일환으로 동시 MEG 및 HD-EEG 데이터에 대한 소스 위치 파악을 수행했습니다. MEG 및 HD-EEG 기록은 양쪽 전두측두엽 영역에서 빈번한 IED를 나타냈다. 도 3a 는 MEG 및 HD-EEG 데이터 모두에 대한 IED의 대표적인 예를 보여줍니다. 지형 필드와 두 양식의 잠재적 매핑은 오른쪽 전두측두엽 영역에 가능한 기본 출처를 나타냈습니다. ESI는 우측 및 좌측 전두측두엽 및 두정엽 영역을 덮는 흩어져 있는 쌍극자 군집을 나타냈습니다. MSI는 우측 인슐라 근처에 위치한 우측 전두측두엽(right frontotemporal lobe)에 쌍극자의 국소 클러스터를 보여주었습니다. EMSI는 임상적 관찰을 확인한 iEEG 골드 스탠다드에 따라 수행된 ESI에 따라 양측 전두측두엽 영역에서 쌍극자의 초점 클러스터를 표시했습니다(그림 3C). EMSI를 통해 추정된 이러한 쌍극자는 iEEG 정의 SOZ와의 평균 거리를 9.81mm(중앙값: 11.18, 표준: 2.37)로 보여주었습니다.
사례 2: 난치성 간질을 앓고 있는 13세 소년이 9세 때부터 발작을 일으켜 입원했다. 발작은 전조와 함께 시작되어 때때로 의식이 보존되고 머리가 왼쪽으로 국소 클론화되는 좌측 머리/눈 편향이 뒤따르며 ~30초 동안 지속되며 일주일에 여러 번 발생했습니다. 처방된 ASM 중 어느 것도 발작 통제에 성공하지 못했습니다. 장기 비디오 EEG에서 우리는 중간 측두엽, 전두측두엽, 측두엽 및 중심 피질을 포함하는 우측 반구에서 우측 후측두엽 스파이크와 빈번한 스파이크파 방출을 관찰했습니다. 환자는 행동 변화, 왼쪽 팔을 뻗을 때 머리/눈이 왼쪽으로 치우치고, 때때로 왼쪽 팔의 간대 활동을 특징으로 하는 6번의 전기 임상 발작과 이차적인 양측 경련 활동을 동반한 3번의 발작을 겪었습니다. 최대 발병은 우측 전두측두엽에서 발생했으며 우측 전두측두엽에서 진화했습니다. 뇌 MRI는 우측 대뇌 반구(perisylvian 우세)의 피질에 광범위한 기형이 있었고 우측 측심실의 진공 확장으로 우측 대뇌 반구에서 경미한 부피 손실이 발견되었습니다. 환자는 우반구에서 발병하는 난치성 간질로 진단되었으며, 미만성 피질 기형 부위의 측두엽 및 주위 발병을 선호했습니다. Stereo-EEG는 우측 측두엽, 주위 피질, 섬 피질 및 두정두엽 피질에 전극을 배치하여 침범 정도를 설명하기 위해 수행되었습니다. 우측 전두측두엽의 넓은 영역에서 최대 발병으로 iEEG 모니터링 중에 여러 전기임상 국소 발작 발작이 포착되었습니다. iEEG 데이터에 대해 수행된 ESI는 우측 측두엽(우측 중간 측두이랑 근처)과 주위 영역으로 구성된 보다 초점 영역에서 이러한 발작을 국소화했습니다.
수술 전 평가의 일환으로 MEG와 HD-EEG를 동시에 수행하여 환자는 두 번의 발작을 경험했는데, 하나는 디지털화 과정에서 나무 의자에 앉아 있을 때였고 다른 하나는 MEG와 HD-EEG 모두에서 발병을 볼 수 있는 실제 기록 중에 포착되었습니다(그림 4A). ictal 발병 시점의 지형 필드 및 전위 맵은 그림 4A와 같이 발작 발병의 기본 생성기가 오른쪽 중간 측두엽에 있을 수 있음을 나타냅니다. ictal 이벤트에 대한 소스 국소화는 ESI와 MSI에 대해 서로 다른 결과를 나타냈습니다: ESI는 우측 전두측두엽 및 편두엽 쪽으로 국소화된 쌍극자를 보인 반면, MSI는 주로 우측 측두엽에서 높은 군집을 가진 쌍극자를 보여주었고(그림 4B), 전두측두엽 피질에 추가로 흩어져 있는 쌍극자를 보여주었습니다. 이러한 솔루션을 결합함으로써 EMSI는 iEEG 골드 스탠다드에 대한 ESI와 일치하는 측두엽 내 ictal 발병의 국소화를 밝혔습니다(그림 4B). 특히, EMSI는 iEEG 모니터링에 의해 정의된 SOZ와의 평균 거리를 12.21mm(중앙값: 13.62, 표준: 2.37)로 국소화 결과를 제시했습니다.
사례 3: 국소 관련 특발성 간질을 앓고 있는 15세 여성이 13세부터 발작을 일으키기 시작했는데, 돌이켜 보면 8-9세에 반복적이고 정형화된 목 움직임으로 인해 틱으로 진단받았을 가능성이 있습니다. 환자는 잠시 머리가 왼쪽으로 기울어지다가 때때로 과잉 운동 행동(즉, 전신 긴장성 간대성 발작)을 동반한 국소 인지 장애 발작으로 진행되었으며 야간 경련 발작도 있었습니다. 여러 ASM을 투여했지만 완전한 발작 조절을 달성하지 못했습니다. 장기간의 비디오-EEG 모니터링 동안, 환자는 좌측 후측두엽에서 발병하는 2차 일반화를 동반한 국소 전기임상 발작, 머리를 왼쪽으로 기울이는 수많은 짧은 국소 운동 발작, 좌측 신관 피질에서 발병을 동반한 미묘한 전기적 발작을 겪었습니다. 뇌 MRI 검사에서 급성 두개내 이상은 발견되지 않았고 키아리 I 기형은 발견되지 않았다. 머리의 양전자 방출 단층 촬영-컴퓨터 단층 촬영(PET-CT) 검사에서 음성 결과가 나왔습니다. 이치탈 단일광자 방출 CT(SPECT), 동시 MEG 및 HD-EEG, 경추 X선, 두경부의 자기공명혈관조영술(MRA), 최종적으로 좌반구의 sEEG 탐색과 같은 추가 검사가 권장되었습니다.
평가의 일환으로 환자는 일차 시각, 운동, 청각 및 체성 감각 피질과 같은 웅변적인 뇌 영역을 매핑하기 위해 MEG 및 HD-EEG 동시 녹음에 참여했습니다. 처음에 환자는 시각 운동 작업을 수행한 후 청각 및 체성 감각 자극을 수행했습니다. 시각 자극에 대한 첫 번째 피질 반응은 MEG 및 HD-EEG 모두에 대한 자극 시작 후 ~ 70 ms에서 발생했습니다 (그림 5A). 그림 5B MEG 및 HD-EEG에 대한 시각적 자극에 관련된 피질 위치의 지형 필드와 잠재적 지도를 각각 보고합니다. HD-EEG의 경우, 후두부 뇌 영역을 덮고 있는 채널의 극성 변화가 관찰된 반면, MEG의 경우 동일한 영역에서 더 복잡한 필드 분포가 발견되었습니다(그림 5B). dSPM을 사용한 소스 국소화는 Desikan-Killiany 아틀라스의 다음 뇌 영역 내에서 이 시점에서 국소 피질 활동을 드러냈습니다: (i) MSI에 대한 cuneus; (ii) ESI에 대한 외측 후두엽 피질; (iii) EMSI에 대한 cuneus 및 lateral occipital cortex (그림 5C). 시각 피질 반응에 대한 시간-주파수 분석은 MSI(대략적인 범위: 30-50Hz), ESI(대략적인 범위: 40-50Hz) 및 EMSI(대략적인 범위: 30-50Hz)에 대한 감마 주파수 대역의 이벤트 관련 동기화(ERS)를 나타냈습니다(그림 5D). 운동 유발 반응의 경우, 운동 시작 동안 반대측 M1에서 뮤 리듬 활동의 억제가 관찰되었습니다(그림 6A). 안으로 그림 6B, 우리는 MEG 및 HD-EEG에 대한 운동 작업 중에 활성화된 뇌 영역의 지형 영역과 잠재적 지도를 각각 보고했습니다. MEG 필드 맵은 반대쪽 중추 뇌 영역에서 자기 유입 및 유출의 명확한 변화를 나타냈으며, 이는 반대쪽 M1(그림 6B). HD-EEG 전위 맵은 동일한 영역에서 초점 극성 변화를 보여주었으며, 전위는 자기장(그림 6B). 에 표시된 바와 같이 MSI, ESI 및 EMSI에 대한 Desikan-Killiany 아틀라스의 반대측 전중심 이랑에서 태핑 작업을 수행하는 동안 최대 소스 활성화의 피크가 관찰되었습니다. 그림 6C. 다가오는 두드리는 움직임에 대한 기대 동안 발생하는 운동 관련 피질 반응은 MSI (대략적인 범위 : 20-30 Hz) 및 EMSI (대략적인 범위 : 20-40 Hz)에 대한 베타 및 감마 대역의 ERS와 ESI (대략적인 범위 : 30-50 Hz)에 대한 감마 대역을 보여주었으며, 문헌에서는 다음과 같이 언급되었습니다. mu rhythm suppression (그림 6D).55,56 청각 자극에 대한 반응으로 청각 유발 필드와 전위는 각각 MEG 및 HD-EEG에 대한 자극 시작 전달 후 ~80ms 및 ~120ms에서 최대 양의 피크를 가졌습니다(그림 7A). 안으로 그림 7B, 우리는 MEG 및 HD-EEG에 대한 청각 자극에 관련된 대뇌 피질 위치의 지형 필드와 잠재적 지도를 각각 보고했습니다. MEG와 HD-EEG 모두에서 왼쪽 측두엽 뇌 영역을 덮고 있는 센서에서 명확하게 정의된 음극과 양극으로 명백한 극성 변화가 관찰되었습니다. 이러한 수직 자기장 및 전위 맵은 V1(그림 7B). 평균적인 청각 유발 필드 및 전위에 대한 소스 국소화를 수행한 결과, MSI, ESI 및 EMSI에 대한 Desikan-Killiany 아틀라스의 상측두이랑의 횡측두회와 후방부에서 각각 최대 피질 활성화가 관찰되었습니다(그림 7C). 청각 유발 반응의 시간-주파수 분석은 MSI(대략적인 범위: 40-60Hz) 및 EMSI(대략적인 범위: 35-50Hz)의 경우 감마 대역의 ERS와 ESI(그림 7D). 마지막으로, 우리는 MEG 및 HD-EEG에 대한 자극 시작 후 ~60 및 ~50 ms에서 촉각 자극에 대한 반응으로 첫 번째 피질 활동을 관찰했습니다(그림 8A). 안으로 그림 8B에서는 MEG와 HD-EEG에 대한 체성 감각 자극 중에 활성화되는 뇌 영역의 지형 필드와 잠재적 지도를 각각 보고했습니다. MEG 필드 맵은 반대쪽 두정 영역을 커버하는 센서에서 자속의 뚜렷한 변화와 함께 명확한 극성 변화를 나타낸 반면, HD-EEG 전위 맵은 음극보다 더 강한 양극으로 동일한 영역에서 극성의 덜 분명한 변화를 보여주었습니다. 이러한 수직 자기장 및 전위 맵은 S1의 초점 피질 발전기를 나타낼 수 있습니다. 평균 체성 감각 유발 반응에 대한 dSPM을 사용하여, 이 시점에서의 최대 피질 소스 활성은 각각 MSI, ESI 및 EMSI에 대한 Desikan-Killiany 아틀라스의 반대측 중심 후 이랑 내에서 관찰되었습니다(그림 8C). 촉각 자극에 반응하여 MSI(대략적인 범위: 15-40Hz) 및 EMSI(대략적인 범위: 20-40Hz)에 대한 베타 및 감마 주파수 대역의 ERS와 ESI의 감마 주파수 대역(대략적인 범위: 30-40Hz)(그림 8D)도 관찰되었다.
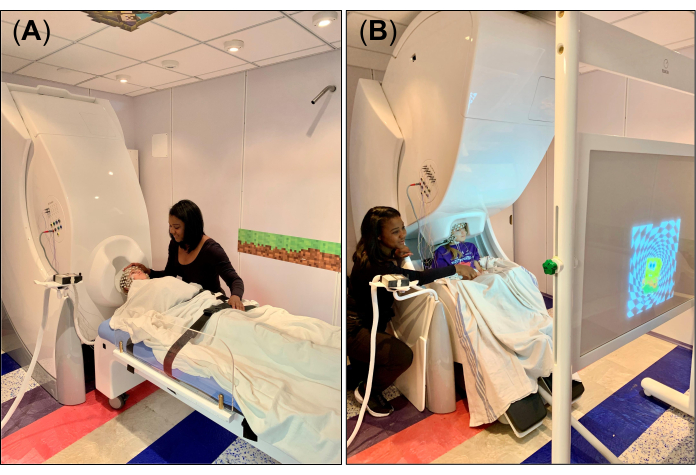
그림 1: CCHCS에서 동시 MEG 및 HD-EEG에 대한 실험 설정. (A) 비자성 MEG 호환 베드를 사용하여 휴지/절전 상태 기록을 위해 MEG의 갠트리가 앙와위 위치(90°, 수평 위치)로 설정된 HD-EEG(256개 채널) 및 MEG(306개 센서) 시스템. 기술자는 안전과 편안함을 보장하면서 녹음을 위해 피험자(9세 소녀)를 준비하고 있습니다. (B) HD-EEG 및 MEG 시스템은 비자성 MEG 호환 의자를 사용하여 앉은 자세에서 녹음하도록 설정됩니다. 기술자는 시각 운동 작업 중에 시각적 자극이 투사될 화면 앞에서 피사체의 올바른 위치를 보장하면서 녹화를 위해 피사체를 준비하고 있습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
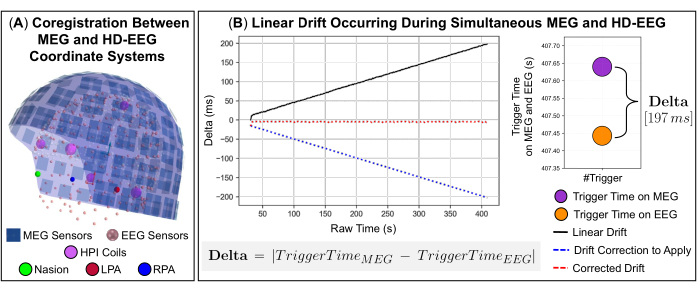
그림 2: 서로 다른 획득 시스템을 사용하여 동시 MEG 및 HD-EEG 기록의 데이터를 결합하는 기술적 측면. (A) 대표 피험자(9세 소녀)에 대한 MEG 및 HD-EEG 센서의 동일한 좌표계(피험자의 머리 좌표로 정의됨)로의 공간 정렬(공동 등록). 피사체의 머리 좌표는 다음과 같은 기준점으로 표시됩니다: nasion(녹색) 및 왼쪽/오른쪽 preauricular points(각각 빨간색 및 파란색). 306 MEG 센서(파란색) - 102 자력계 및 204 평면 그래디오미터 - 및 헤드 위치 표시기(HPI) 코일(자홍색)이 표시됩니다. 동일한 좌표계에 정렬되면 256개의 HD-EEG 채널도 표시됩니다(분홍색). (B) 왼쪽 패널: 대표 피험자(9세 소녀)에 대해 MEG와 HD-EEG 시스템 간에 발생하는 데이터 샘플의 선형 드리프트(즉, 델타, 검은색 선으로 표시). Delta는 동일한 트리거가 MEG 및 EEG 시스템 모두에 전송되고 시간이 지남에 따라 낮은(델타 = 0ms) 값에서 높은(델타 = 197ms) 값까지 지속적으로 증가하는 시간 간의 차이의 절대값으로 정의됩니다. 신호에 적용할 다항식 함수를 사용하여 추정된 선형 드리프트의 보정은 파란색 점선으로 표시됩니다. MEG와 EEG 시스템 간의 동기화된 시간을 나타내는 수정된 드리프트(시간 경과에 따른 델타 ~0ms)는 빨간색 점선으로 표시됩니다. 오른쪽 패널: MEG 및 EEG 시스템 모두에 전송된 마지막 트리거에 대해 추정된 시간 이동(델타 = 197ms)의 그래픽 표현이 표시됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
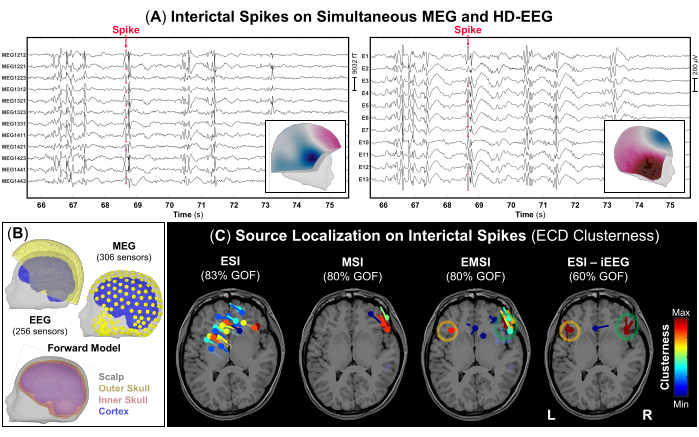
그림 3: MEG 및 HD-EEG 데이터의 간질 간질 방전(IED). (A) 잦은 IED가 있는 10세 여성(사례 1)의 MEG 및 HD-EEG 동시 기록(10초)의 시간 부분. 시각화를 위해 306개의 MEG 센서와 256개의 EEG 전극의 하위 그룹이 선택되었습니다. IED의 피크에서 지형 필드와 전위 맵은 각각 MEG 및 HD-EEG에 대한 내부 패널로 표시됩니다. (B) MEG 및 HD-EEG 센서(노란색)의 위치가 피험자의 3D 머리와 대뇌 피질(파란색) 표면에 함께 등록되어 있습니다. 피험자의 수술 전 MRI에서 재구성한 3개의 층[즉, 두피(회색), 외부 두개골(노란색), 내부 두개골(분홍색)]로 구성된 사실적 경계 요소법(BEM) 머리 모델. (C) 등가 전류 쌍극자(ECD)를 사용하여 IED에서 수행된 소스 국소화 클러스터니스 결과는 iEEG(골드 스탠다드)에서 ESI, MSI, EMSI 및 ESI에 대한 피험자의 수술 전 MRI에 표시됩니다(골드 스탠다드)52. 적합도가 >60%인 쌍극자 클러스터니스의 히트 맵은 낮은 값(파란색)에서 높은 값(빨간색)으로 표시됩니다. iEEG 데이터에서 수행된 ESI를 통해 정의된 발작 시작 영역은 황금 표준(주황색 및 녹색 원)으로 간주되었습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
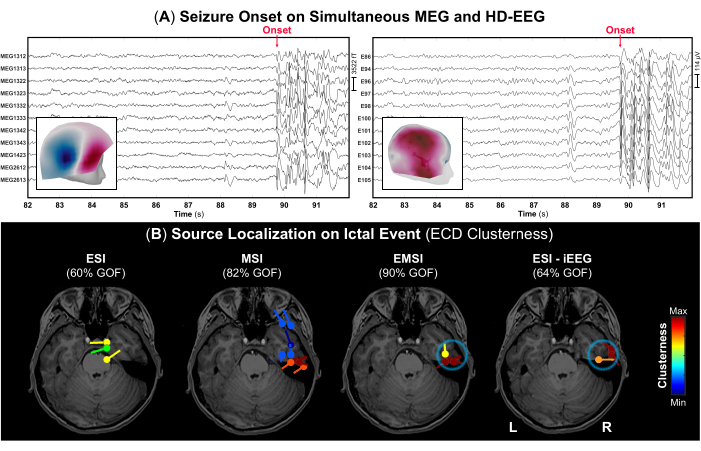
그림 4: MEG 및 HD-EEG 데이터에서 발작 시작. (A) 발작 시작(빨간색 화살표)과 13세 남성(사례 2)의 동시 MEG 및 HD-EEG 기록(10초)의 시간 부분. 시각화를 위해 306개의 MEG 센서와 256개의 EEG 전극의 하위 그룹이 선택되었습니다. ictal 시작 시 지형 필드와 전위 맵은 각각 MEG 및 HD-EEG에 대한 내부 패널로 표시됩니다. (B) 등가 전류 쌍극자(ECD) 방법을 사용하여 ictal 이벤트 시작 시 수행된 소스 국소화 클러스터니스 결과는 iEEG(골드 스탠다드)에서 ESI, MSI, EMSI 및 ESI에 대한 피험자의 수술 전 MRI에 표시됩니다(골드 스탠다드)52. 적합도가 >60%인 쌍극자 클러스터니스의 히트 맵은 낮은 값(파란색)에서 높은 값(빨간색)으로 표시됩니다. iEEG 데이터에서 수행된 ESI를 통해 정의된 발작 시작 영역은 황금 표준(파란색 원)으로 간주되었습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
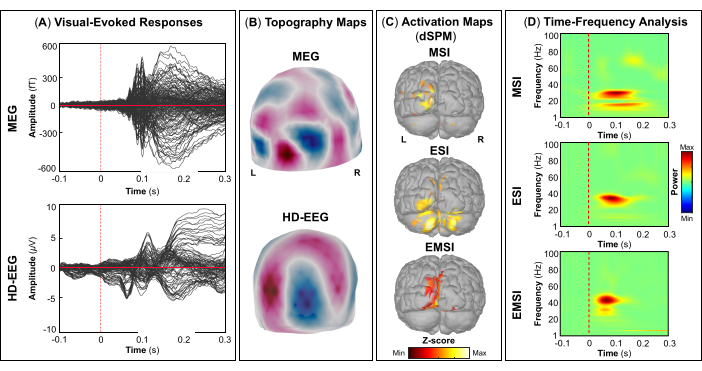
그림 5: MEG 및 HD-EEG 데이터의 시각 유발 필드 및 전위. (A) MEG(상단 패널) 및 HD-EEG(하단 패널)에 대한 15세 여성의 평균 시각적 유발 반응은 -100ms와 300ms 사이의 시간 간격에 대해 표시됩니다. (B) 주요 시각 피질의 지형 필드 및 전위 맵은 MEG 및 HD-EEG에 대해 표시됩니다. 각각. (C) MSI, ESI 및 EMSI에 대해 각각 dSPM(Dynamic Statistical Parametric Mapping) 방법을 사용하여 추정된 Desikan-Killiany 아틀라스(즉, cuneus 및 lateral occipital cortex)의 뇌 영역에서 대뇌 피질 활성화의 최대 진폭을 가진 소스 활성화 맵. 소스 활성화의 히트 맵(dSPM 정규화 z-점수)이 표시됩니다. (D) 1차 시각 피질에서 시각 유발 반응에 대한 Morlet 웨이블릿 시간-주파수 분해를 사용하여 얻은 시간-주파수 맵은 -100ms에서 300ms 시간 창에 대해 표시됩니다. 기준선 [-200; 0]ms에 대한 평균에서 정규화된 데이터의 편차를 기반으로 백분율로 표현된 시간-주파수 전력의 히트 맵이 표시됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
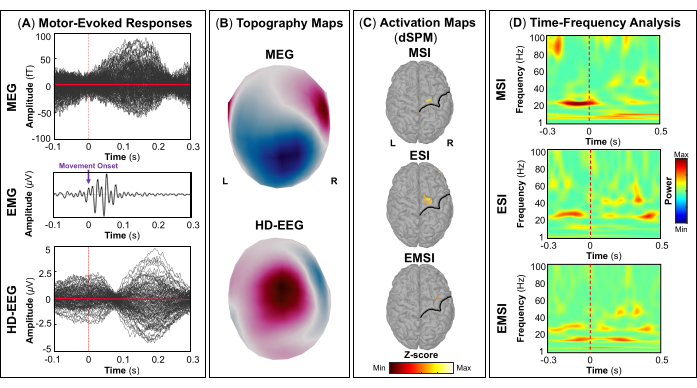
그림 6: MEG 및 HD-EEG 데이터의 모터 유발 필드 및 전위. (A) MEG(상단 패널) 및 HD-EEG(하단 패널)에 대한 15세 여성의 평균 모터 유발 응답은 -100ms에서 300ms 사이의 시간 간격으로 왼쪽 인덱스 태핑 작업에 대해 표시됩니다. 움직임 시작(보라색 화살표)이 있는 근전도(EMG) 신호(중간 패널)는 -100ms에서 300ms 사이의 시간 간격으로 표시됩니다. 신호는 주파수 대역 30-300Hz(노치 필터: 60Hz)에서 필터링됩니다. (B) 1차 운동 피질의 지형 필드와 전위 맵은 각각 MEG 및 HD-EEG에 대해 표시됩니다. (C) MSI, ESI 및 EMSI에 대해 각각 dSPM(Dynamic Statistical Parametric Mapping) 방법을 사용하여 추정된 Desikan-Killiany 아틀라스의 반대측 전중심 이랑에서 피질 활성화의 최대 진폭을 가진 소스 활성화 맵. 소스 활성화의 히트 맵(dSPM 정규화 z-점수)이 중앙 열구(검은색 선)와 함께 표시됩니다. (D) -300 ms - 500 ms 시간 창에 대한 일차 운동 피질의 모터 유발 응답에 대한 Morlet 웨이블릿 시간-주파수 분해를 사용하여 얻은 시간-주파수 맵. 기준선 [-1500; -1000]ms에 대한 평균에서 정규화된 데이터의 편차를 기반으로 백분율로 표현된 시간-주파수 전력의 히트 맵이 표시됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
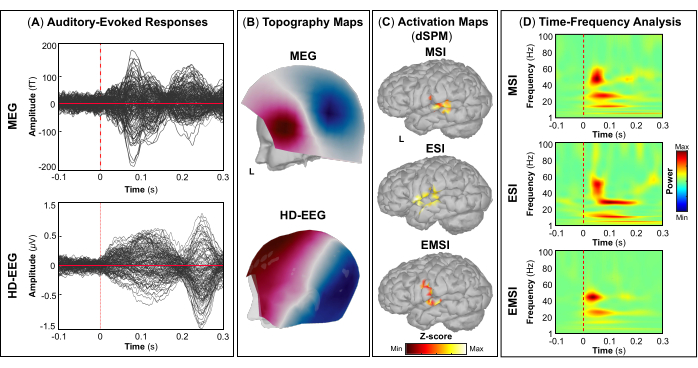
그림 7: MEG 및 HD-EEG 데이터의 청각 유발 필드 및 전위. (A) MEG(상단 패널) 및 HD-EEG(하단 패널)에 대한 15세 여성의 평균 청각 유발 반응은 -100ms와 300ms 사이의 시간 간격에 대해 표시됩니다. (B) MEG 및 HD-EEG에 대해 각각 일차 청각 피질의 지형 필드와 전위 지도가 표시됩니다. (C) MSI, ESI 및 EMSI에 대한 동적 통계적 매개변수 매핑(dSPM) 방법을 사용하여 각각 추정된 Desikan-Killiany 아틀라스의 상측두이랑의 횡측두회와 후측두회에서 피질 활성화의 최대 진폭을 가진 소스 활성화 맵. 소스 활성화의 히트 맵(dSPM 정규화 z-점수)이 표시됩니다. (D) -100 내지 300 ms 시간 창에 대한 일차 청각 피질에서의 청각 유발 반응에 대한 Morlet 웨이블릿 시간-주파수 분해를 사용하여 얻은 시간-주파수 맵. 기준선 [-500; 0]ms에 대한 평균에서 정규화된 데이터의 편차를 기반으로 백분율로 표현된 시간-주파수 전력의 히트 맵이 표시됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
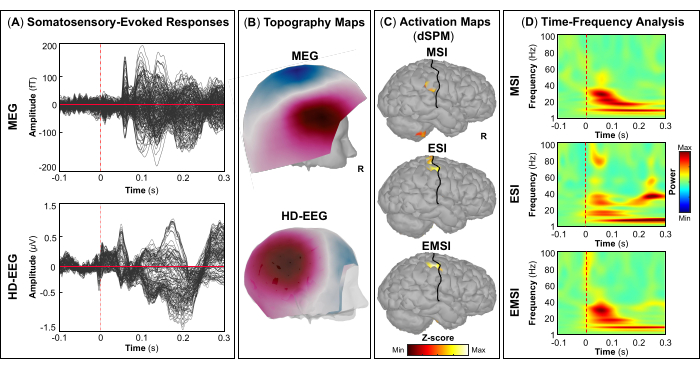
그림 8: MEG 및 HD-EEG 데이터의 체성 감각 유발 필드 및 전위. (A) MEG(상단 패널) 및 HD-EEG(하단 패널)에 대한 15세 여성의 평균 체성 감각 유발 반응은 -100에서 300ms 사이의 시간 간격에서 왼쪽 숫자의 자극에 대해 표시됩니다. (B) MEG 및 HD-EEG에 대해 일차 체성 감각 피질의 지형 필드 및 전위 지도가 표시됩니다. 각각. (C) MSI, ESI 및 EMSI에 대해 각각 dSPM(Dynamic Statistical Parametric Mapping) 방법을 사용하여 추정된 Desikan-Killiany 아틀라스의 반대측 후중심 이랑에서 피질 활성화의 최대 진폭을 가진 소스 활성화 맵. 소스 활성화의 히트 맵(dSPM 정규화 z-점수)이 중앙 열구(검은색 선)와 함께 표시됩니다. (D) -100 ms - 300 ms 시간 창에 대한 일차 체성 감각 피질의 체성 감각 유발 반응에 대한 Morlet 웨이블릿 시간-주파수 분해를 사용하여 얻은 시간-주파수 맵. 기준선 [-100; 0]ms에 대한 평균에서 정규화된 데이터의 편차를 기반으로 백분율로 표현된 시간-주파수 전력의 히트 맵이 표시됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
토론
본 연구에서는 DRE를 앓고 있는 소아의 휴식/수면, 과제 수행, 자극 수용 중 MEG와 HD-EEG를 동시에 기록하는 실험 설정을 설명하고, EMSI를 이용하여 자극 영역, SOZ, 웅변 뇌 영역을 국소화하기 위한 방법론적 틀을 제시한다. 또한 고유한 기능을 제공하는 서로 다른 상용 제품의 MEG 및 HD-EEG 데이터를 병합하기 위한 기술 권장 사항을 제공합니다. 우리는 간질 유발 및 웅변적인 뇌 영역의 국소화에서 EMSI의 임상적 유용성을 향상시키기 위해 세 가지 사례의 데이터를 제시합니다. 이 연구 결과는 EMSI 결과가 두 가지 방식 중 하나로 얻은 결과보다 우수하다는 것을 나타내며, 이는 결합된 솔루션에서 MEG 및 EEG 신호의 보완 특성의 부가적 가치와 데이터 기록에 사용되는 센서 수 증가(>550 센서) 때문일 수 있습니다. 특히, EMSI는 자극성 물질과 SOZ를 비침습적으로 국소화하여 iEEG 골드 스탠다드(iEEG gold standard)의 ESI로 일치하는 결과를 보였으며, 이는 임상적 관찰을 확인하였습니다.
제안된 방법론에는 다음과 같은 중요한 단계가 포함됩니다: (i) DRE가 있는 어린이로부터 시각, 운동, 청각 및 체성 감각 유발 필드 및 전위뿐만 아니라 전체 뇌 간 및 ICTAL 활동의 뇌를 포괄하는 센서(>550 센서)의 높은 공간 샘플링을 통한 동시 MEG 및 HD-EEG(즉, 높은 SNR) 기록의 고품질 획득(단계 3.1-3.2); (ii) 상이한 획득 시스템으로 기록된 MEG 및 HD-EEG 신호의 시간적 동기화 및 공간적 공동 정합(단계 3.12); (iii) 각각 ICTAL INTERICTAL ACTIVITY(단계 4.1.1-4.1.7), ICTAL 발병 ACTIVITY(단계 4.2.1-4.2.7) 및 이벤트 관련 응답(단계 4.3.1-4.3.6)을 포함하는 데이터 부분의 신중한 전처리 및 선택; (iv) 신뢰할 수 있는 소스 국소화 방법(예: 클러스터링 및 dSPM이 있는 ECD)을 사용하여 자극 영역, SOZ 및 웅변적인 뇌 관심 영역의 정확한 소스 국소화(각각 4.1.8-4.1.9, 4.2.8-4.2.9 및 4.3.7-4.3.9).
MEG 및 HD-EEG 동시 레코딩을 수행할 때 가장 중요한 단계는 두 수집 시스템이 기록한 데이터를 공간적으로(좌표 공간 간 정렬) 및 시간적으로(선형 클럭 드리프트 보정) 동기화하는 것입니다. 이러한 동기화는 MEG 및 HD-EEG 신호에서 동시에 발생하는 내부, ICTAL 및 시각/모터/청각/촉각 이벤트를 올바르게 식별하는 데 매우 중요합니다. 이러한 이벤트의 시점 선택에 있어서의 오류는 소스 국소화 결과에 영향을 미칠 수 있으며, 이러한 이벤트의 생성에 반드시 관여하지 않는 뇌 영역을 식별할 수 있습니다.
MEG 시스템은 MEG 및 EEG 측정을 동시에 수행하기 위해 제품에 통합된 호환 가능한 32, 64 및 128 채널 EEG 시스템을 제공하는 경우가 많습니다. 이러한 경우 공통 트리거 신호를 전송하여 데이터를 일시적으로 동기화할 필요가 없습니다. 마찬가지로, 대부분의 EEG 시스템은 오늘날 모든 MEG 시스템과 호환됩니다. 이러한 하드웨어의 발전에도 불구하고 수술 전 평가의 일환으로 MEG 및 HD-EEG 기록을 동시에 수행하는 간질 센터는 거의 없습니다. 여기에서 우리는 이러한 통합성을 활용하여 306채널 MEG 및 256채널 EEG 시스템을 결합하여 피험자의 머리를 덮고 있는 >550 센서로 뇌 활동을 동시에 기록했습니다. 현재까지 MEG, HD-EEG 및 iEEG 데이터의 고급 분석을 위한 소프트웨어(예: Brainstorm, CURRY, EEGLab, FieldTrip, MNE 또는 NUTMEG)는 거의 사용할 수 없습니다. 따라서 새로운 신경영상 분석 소프트웨어로 제안된 방법론을 검증하기 위한 향후 연구가 필요합니다. 마지막으로, MSI와 ESI를 고유한 솔루션(EMSI)으로 결합함으로써 데이터 분석의 계산 복잡성이 증가했습니다.
설명된 방법은 향후 연구에서 해결해야 할 몇 가지 제한 사항을 제시합니다. 두 대표 환자의 MEG 및 HD-EEG 데이터 모두에서 발생하는 IED를 수동으로 선택하면서 두 신호(MEG 또는 EEG) 중 하나에서만 발생하는 간질 스파이크는 무시했습니다. 스파이크의 수동 선택은 시간이 많이 걸리고 주관적인 접근 방식일 수 있으며, 지난 수십 년 동안 개발된 IED를 감지하기 위한 자동화된 접근 방식을 사용하여 단순화할 수 있습니다57,58,59. 그러나 각 IED에 대한 신중한 분석과 정교한 감지를 위해 항상 육안 검사가 권장됩니다. 또한 SOZ를 EZ의 근사치로 사용했습니다. 그러나 SOZ가 항상 수술 결과를 예측하는 것은 아닙니다60,61,62,63. 따라서 향후 연구에서는 수술 결과를 EZ를 보다 정확하게 묘사하기 위한 실측 자료로 사용할 수 있습니다13,14,15,16,17,19,20. 발작은 MEG와 EEG를 동시에 사용하여 성공적으로 포착할 수 있지만 적절한 소스 위치 파악 기술을 사용하여 국소화할 수 있습니다44,64, 임상실습에서 이러한 ICTAL 사건을 기록하는 것은 상대적으로 드물며, 특히 ASM의 외래 환자로부터 그렇습니다. 이는 주로 MEG 기록의 제한된 기간과 발작 중에 발생하는 과도한 신체 움직임(예: 환자의 머리가 듀어 밖으로 미끄러짐) 때문이며, 이로 인해 소스 위치 파악 결과에 심각한 영향을 미칠 수 있는 생물학적 인공물이 발생할 수 있습니다. 최근 리뷰에서 Stefan et al. 환자의 7%-24%에서 MEG 기록 중 발작이 발생했다고 보고했으며, 다른 연구에서 평균 기록 시간은 30분에서 최대 5.7시간이었습니다.65. CCMC에서는 89명 중 18명(20.2%)의 환자가 지난 ~2년 이내에 수행된 MEG 및 HD-EEG 동시 기록 중에 포착된 감염 사건을 경험했습니다. 그러나 18명 중 8명(44.4%)만이 분석에 성공했다. interictal MEG 기록이 정상 또는 불확정적인 소견을 보여주는 경우, ictal MEG 또는 HD-EEG를 사용하여 EZ를 높은 정밀도로 국소화할 수 있습니다. 그러나 이러한 녹음에 대한 기술 및 물류 요구 사항을 해결해야 합니다. 또한, EMSI를 통한 웅변적 피질 국소화에 대한 대표 데이터는 비침습적 fMRI 또는 수술 중 전기 피질 자극과 같은 이러한 기능적 뇌 영역의 국소화에 대한 황금 표준과 비교되지 않았습니다. 따라서 추가 연구를 통해 EMSI와 fMRI를 멀티모달 비침습적 이미징 도구에 통합하여 DRE가 있는 소아에서 이러한 웅변적인 뇌 영역의 국소화 정확도를 향상시킬 수 있습니다. 이 작업은 또한 언어 웅변 영역과 같은 다른 기능적 뇌 영역을 지역화하는 것으로 확장될 수 있습니다. DRE가 있는 환자의 수술 전 평가에서 수술 적합성을 결정하고, 외과적 절제 범위를 계획하고, 수술 후 영구적인 기능 결손을 예방하기 위해 언어 기능의 국소화가 매우 중요합니다66. 여러 비침습적 연구에 따르면 MEG를 사용한 언어 매핑은 종종 지배적인 언어 반구를 식별하기 위한 황금 표준으로 간주되는 침습적 Wada 테스트와 유사한 일치 결과를 제공할 수 있습니다67,68,69,70. 최근 연구에서는 다양한 기술(즉, 대뇌 피질 자극 매핑, 고감마 전기 피질 검사, fMRI 및 경두개 자기 자극)의 조합이 수술 전 언어 매핑을 위한 상호 확인적이고 보완적인 정보를 제공할 수 있는 다중 모드 접근 방식을 제안했습니다71. 이러한 장점에도 불구하고 나이로 인해 인지적, 지적, 언어 장벽이 있는 소아 환자에게는 언어 영역을 매핑하는 것이 여전히 어렵습니다. 따라서 가까운 장래에 더 많은 연령별 작업과 아동 친화적인 설정이 개발되어야 합니다. 이 연구에서는 임상 목적으로 인증되지 않은 소프트웨어를 사용하여 MEG 및 HD-EEG 데이터를 분석했습니다. 이러한 도구는 가치 있고 효과적인 것으로 입증되었지만, 임상적 사용을 위해 수술 전 평가 결과를 보고할 때 고려해야 하는 책임 문제를 수반합니다. 여기에서는 스폰지 기반 EEG 전극 시스템만 사용하여 HD-EEG 기록을 위한 절차를 설명합니다. 겔 기반 EEG 전극을 사용하는 대체 시스템은 임상 및 연구 환경 모두에서 널리 사용됩니다. 더 높은 SNR EEG 기록을 제공하지만 더 긴 준비 시간(~40-60분)이 필요하므로 소아과 사용에는 적합하지 않습니다. 대안적으로, 몇몇 실험실에서는 MEG 기록 중에 저밀도 겔 기반 EEG 시스템을 사용하는데, 이는 준비 시간(HD-EEG 시스템에 비해) 측면에서 유리하지만, 전체 두피를 덮는 전극의 수가 적기 때문에 공간 해상도가 현저히 낮습니다12,16,72,73.
현재 뇌전증 환자에서 간질 유발 뇌 영역의 국소화는 여전히 주로 iEEG 모니터링으로 이루어지고 있습니다. 더욱이, 웅변적인 뇌 영역의 정확한 국소화를 위한 방법론은 잘 정의되어 있지 않으며, 현재 MEG 실험실에서 사용되는 실험 설정은 소아 환자에게 적합하지 않으며, 이러한 목적으로 HD-EEG를 사용하는 것은 매우 제한적입니다. 이러한 부위의 정확한 위치 파악은 수술 전 평가를 용이하게 하고 절제 또는 iEEG 전극 배치를 위한 수술 계획을 강화할 수 있습니다. 지금까지 여러 연구에서 EZ 12,13,14,15,16,17,18,19 및 체성 감각 피질의 웅변 영역을 식별하기 위해 DRE 및 국소 간질 환자의 수술 전 평가 에서 ESI 또는 MSI의 기여도를 조사했습니다 41각각. MSI 또는 ESI를 단독으로 사용하는 것에 비해 EMSI를 사용하여 소스 현지화 결과와 결과 예측 성능이 더 우수하다는 연구는 거의 없다 13,31,42. 이러한 연구 결과에도 불구하고 MEG와 EEG의 기록은 거의 동시에 수행되지 않으며 MSI와 ESI는 전 세계적으로 소수의 간질 센터에서만 구현되고 있습니다. 우리가 아는 한, 이 연구는 MEG 및 HD-EEG 동시 데이터 수집 및 분석뿐만 아니라 소아 간질에서 EMSI를 수행하여 자극 영역, SOZ 및 웅변 뇌 영역, 즉 일차 시각, 운동, 청각 및 체성 감각 피질의 비침습적 식별을 위한 제안을 제공하는 첫 번째 연구입니다.
여기에서 DRE가 있는 두 환자(사례 1 및 2)의 동시 비침습적 데이터에서 감지된 간질 스파이크 및 ictal 이벤트에 대해 EMSI를 수행했으며 이전 연구42에 따라 SOZ에서 각각 ~9mm 및 ~12mm의 소스 국소화 오류를 달성했습니다. 인상적이게도, 이러한 방법은 임상 관찰에 의해 간질성 것으로 정확히 지적된 뇌 영역에 국한된 군집된 쌍극자를 사용하여 두개내 소견(즉, iEEG 데이터의 ESI)에 필적하는 국소화 정확도를 달성했습니다(그림 3C 및 그림 4B). DRE를 앓고 있는 세 번째 대표 환자(사례 3)의 비침습적 데이터를 사용하여 시각, 운동, 청각 및 체성 감각 유발 활동에 대한 EMSI를 수행하고 해당 웅변 뇌 영역(즉, 시각, 운동, 청각 및 체성 감각 피질)에서 두드러진 소스 활성화 패턴을 발견했습니다(그림 5C, 그림 6C, 그림 7C 및 그림 8C).
우리의 결과는 위치 파악 정확도를 향상시킬 수 있는 MEG 및 EEG 양식에서 캡처한 보완 정보를 융합하여 도출되었습니다. EEG는 모든 두개내 전류를 반영하는 것으로 잘 알려져 있는 반면, MEG는 대부분 접선 소스에 민감하고 뇌 심부 소스에는 눈이 멀어있습니다 29,74. 이 연구에서 볼 수 있듯이 MEG와 EEG를 결합하면 각 양식의 한계를 극복하고, 우수한 국소화 결과를 제공하며, ESI 또는 MSI를 단독으로 사용할 경우 놓칠 수 있는 간질 유발 및 웅변 뇌 영역을 식별할 수 있습니다. 또한, 수술 전 평가에서 fMRI를 받지 않은 환자에서 EMSI를 사용하여 웅변적인 뇌 영역을 매핑하기 위한 대안적인 비침습적 접근 방식을 제시합니다.
동시 MEG 및 EEG와 같은 비침습적 기술을 사용하여 간질 유발 및 웅변 뇌 영역의 국소화는 웅변 피질 영역을 보존하면서 EZ의 완전한 제거 또는 분리를 위해 DRE가 있는 어린이의 수술 전 평가 중 필수적인 단계입니다. 제안된 방법론은 수술 전 뇌전증 평가뿐만 아니라 일반적으로 발달하는 어린이와 건강한 성인 모두에서 건강한 뇌의 생리적 기능뿐만 아니라 간질 또는 기타 신경 장애와 관련된 형태학적 및 기능적 뇌 변화를 탐구하기 위한 인지 신경 과학에서의 적용을 지원하는 동시 MEG 및 EEG 데이터의 수집 및 분석에 대한 자세한 설명을 제공합니다. 간질 유발 뇌 네트워크를 조사하는 향후 연구에서는 동시 MEG 및 HD-EEG 데이터에서 EMSI를 사용하여 비침습적으로 추정한 네트워크 허브(즉, 고도로 연결된 뇌 영역)가 MSI 및/또는 ESI를 단독으로 사용하여 추정된 것보다 DRE가 있는 소아의 EZ를 더 정확하게 국소화할 수 있는지 여부를 평가할 수 있습니다 75,76,77. 또한, EMSI를 통해 추정된 스파이크 및 리플의 시공간 전파(즉, 고주파 진동, >80Hz)의 비침습적 매핑은 간질 활동 전파의 병태생리학적 메커니즘을 더 잘 이해하고 EZ78,79의 정확한 바이오마커인 이러한 전파의 발병 생성기를 비침습적으로 평가하는 데 도움이 될 수 있습니다. 제시된 프로토콜은 상이한 방향의 소스에 대한 MEG 및 EEG 센서 어레이의 민감도를 검사함으로써 MEG 및 EEG 시스템의 상보성을 추가로 조사하는 데 도움이 될 수 있습니다. 이러한 분석은 MEG 및 HD-EEG를 동시에 수행하면서 뇌의 전기생리학적 특성에 대한 통찰력을 제공할 수 있습니다.
공개
저자는 공개하지 않습니다.
감사의 말
이 연구는 미국 국립신경장애뇌졸중연구소(National Institute of Neurological Disorders and Stroke, R01NS104116; R01NS134944; 수석 연구원: Christos Papadelis).
자료
| Name | Company | Catalog Number | Comments |
| AIRSTIM unit | SD Instruments | N/A | The SDI AIRSTIM system is an alternative unconditioned stimulus to shock |
| Baby Shampoo | Johnson's | N/A | Baby Shampoo is as gentle to the eyes as pure water and is specially designed to gently cleanse baby’s delicate hair and scalp. |
| Control III disinfectant cleaning solution | Maril Products, Inc. | http://www.controlthree.com/ | Disinfectant and germicide solution formulated for hospitals |
| Elekta Neuromag | TRIUX | NM24132A | Comprehensive bioelectromagnetic measurement system characterized by 306-channel neuromagnetometer for functional brain studies |
| FASTRAK | Polhemus technology | NS-7806 | Using A/C electromagnetic technology, FASTRAK delivers accurate position and orientation data, with virtually no latency. With a single magnetic source, FASTRAK delivers data for up to four sensors. The source emits an electromagnetic field, sensors within the field of range are tracked in full 6DOF (6 Degrees-Of-Freedom). Setup is simple and intuitive, with no user calibration required. |
| Genuine Grass Reusable Cup EEG Electrodes | Natus Medical, Inc. | N/A | Each Genuine Grass EEG Electrode undergoes rigorous mechanical and electrical testing to assure long life for unsurpassed recording clarity and dependability. |
| Geodesic Sensor Net | Electrical Geodesics, Inc. | S-MAN-200-GSNR-001 | 32 to 256 electrodes to place on the human head to aquire dense-array electroencephalography data |
| GeoScan Sensor Digitization System | Electrical Geodesics, Inc. | 8100550-03 | Handheld Scanner and Software for 3D electrode position registration |
| Natus Xltek NeuroWorks | Natus Medical, Inc. | https://natus.com/ | The Natus NeuroWorks platform simplifies the process of collecting, monitoring and managing data for routine EEG testing, ambulatory EEG, long-term monitoring, ICU monitoring, and research studies. |
| Natus NeuroWorks EEG Software | Natus Medical, Inc. | https://natus.com/neuro/neuroworks-eeg-software/ | NeuroWorks EEG software simplifies the process of collecting, monitoring, trending and managing EEG testing data, allowing care providers to save time and focus on delivering the best care. |
| ROSA ONE Brain | Zimmer Biomet | https://www.zimmerbiomet.com/en/products-and-solutions/zb-edge/robotics/rosa-brain.html | ROSA ONE Brain is a robotic solution to assist surgeons in planning and performing complex neurosurgical procedures through a small drill hole in the skull. |
| Ten20 Conductive Paste | Weaver and company | N/A | Ten20 contains the right balance of adhesiveness and conductivity, enabling the electrodes to remain in place while allowing the transmittance of electrical signals. |
참고문헌
- Oldham, M. S., Horn, P. S., Tsevat, J., Standridge, S. Costs and clinical outcomes of epilepsy surgery in children with drug-resistant epilepsy. Pediatr Neurol. 53 (3), 216-220 (2015).
- Willie, J. T., et al. Real-time magnetic resonance-guided stereotactic laser amygdalohippocampotomy for mesial temporal lobe epilepsy. Neurosurgery. 74 (6), 569-584 (2014).
- Rosenow, F., Lüders, H. Presurgical evaluation of epilepsy. Brain. 124, Pt 9 1683-1700 (2001).
- Önal, Ç, et al. Complications of invasive subdural grid monitoring in children with epilepsy). J Neurosurg. 98 (5), 1017-1026 (2003).
- Hader, W. J., et al. Complications of epilepsy surgery-a systematic review of focal surgical resections and invasive EEG monitoring. Epilepsia. 54 (5), 840-847 (2013).
- Meng, Y., et al. Risk factors for surgical site infection after intracranial electroencephalography monitoring for epilepsy in the pediatric population. J Neurosurg Pediatr. 22 (1), 31-36 (2018).
- Jobst, B. C., et al. Intracranial EEG in the 21st Century. Epilepsy Curr. 20 (4), 180-188 (2020).
- Schwartz, E. S., et al. Magnetoencephalography for pediatric epilepsy: how we do it. AJNR Am J Neuroradiol. 29 (5), 832-837 (2008).
- Michel, C. M., et al. Electric source imaging of human brain functions. Brain Res Rev. 36 (2-3), 108-118 (2001).
- Michel, C. M., He, B. EEG source localization. Handb Clin Neurol. 160, 85-101 (2019).
- Michel, C. M., Brunet, D. EEG source imaging: A practical review of the analysis steps. Front Neurol. 10, 325(2019).
- Plummer, C., et al. Interictal and ictal source localization for epilepsy surgery using high-density EEG with MEG: a prospective long-term study. Brain. 142 (4), 932-951 (2019).
- Duez, L., et al. Electromagnetic source imaging in presurgical workup of patients with epilepsy: A prospective study. Neurology. 92 (6), e576-e586 (2019).
- Mouthaan, B. E., et al. Diagnostic accuracy of interictal source imaging in presurgical epilepsy evaluation: A systematic review from the E-PILEPSY consortium. Clin Neurophysiol. 130 (5), 845-855 (2019).
- Pellegrino, G., et al. Clinical yield of magnetoencephalography distributed source imaging in epilepsy: A comparison with equivalent current dipole method. Hum Brain Mapp. 39 (1), 218-231 (2018).
- Tamilia, E., et al. Assessing the localization accuracy and clinical utility of electric and magnetic source imaging in children with epilepsy. Clin Neurophysiol. 130 (4), 491-504 (2019).
- Coito, A., et al. Interictal epileptogenic zone localization in patients with focal epilepsy using electric source imaging and directed functional connectivity from low-density EEG. Epilepsia Open. 4 (2), 281-292 (2019).
- Singh, J., Ebersole, J. S., Brinkmann, B. H. From theory to practical fundamentals of electroencephalographic source imaging in localizing the epileptogenic zone. Epilepsia. 63 (10), 2476-2490 (2022).
- Brodbeck, V., et al. Electrical source imaging for presurgical focus localization in epilepsy patients with normal MRI. Epilepsia. 51 (4), 583-591 (2010).
- Santalucia, R., et al. Clinical added value of interictal automated electrical source imaging in the presurgical evaluation of MRI-negative epilepsy: A real-life experience in 29 consecutive patients. Epilepsy Behav. 143, 109229(2023).
- Schneider, F., et al. Magnetic source imaging in non-lesional neocortical epilepsy: additional value and comparison with ICEEG. Epilepsy Behav. 24 (2), 234-240 (2012).
- Hämäläinen, M., Hari, R., Ilmoniemi, R. J., Knuutila, J., Lounasmaa, O. V. Magnetoencephalography-theory, instrumentation, and applications to noninvasive studies of the working human brain. Rev Mod Phys. 65, 413-497 (1993).
- Baillet, S., Mosher, J. C., Leahy, R. M. Electromagnetic brain mapping. IEEE Signal Process Mag. 18 (6), 14-30 (2001).
- Fuchs, M., Kastner, J., Tech, R., Wagner, M., Gasca, F. MEG and EEG dipole clusters from extended cortical sources. Biomed Eng Lett. 7 (3), 185-191 (2017).
- Singh, S. P. Magnetoencephalography: Basic principles. Ann Indian Acad Neurol. 17, Suppl 1 S107-S112 (2014).
- Ahlfors, S. P., Han, J., Belliveau, J. W., Hämäläinen, M. S. Sensitivity of MEG and EEG to source orientation. Brain Topogr. 23, 227-232 (2010).
- Kim, H., Chung, C. K., Hwang, H. Magnetoencephalography in pediatric epilepsy. Korean J Pediatr. 56 (10), 431-438 (2013).
- Gorjan, D., Gramann, K., De Pauw, K., Marusic, U. Removal of movement-induced EEG artifacts: Current state of the art and guidelines. J Neural Eng. , (2022).
- Barkley, G. L., Baumgartner, C. MEG and EEG in epilepsy. J Clin Neurophysiol. 20 (3), 163-178 (2003).
- Ebersole, J. S., Ebersole, S. M. Combining MEG and EEG source modeling in epilepsy evaluations. J Clin Neurophysiol. 27 (6), 360-371 (2010).
- Yoshinaga, H., et al. Benefit of simultaneous recording of EEG and MEG in dipole localization. Epilepsia. 43 (8), 924-928 (2002).
- Baumgartner, C. Controversies in clinical neurophysiology. MEG is superior to EEG in the localization of interictal epileptiform activity: Con. Clin Neurophysiol. 115 (5), 1010-1020 (2004).
- Barkley, G. L. Controversies in neurophysiology. MEG is superior to EEG in localization of interictal epileptiform activity: Pro. Clin Neurophysiol. 115 (5), 1001-1009 (2004).
- Braeutigam, S. Magnetoencephalography: Fundamentals and established and emerging clinical applications in radiology. ISRN Radiol. 2013, 529463(2013).
- Papadelis, C., et al. Current and emerging potential for magnetoencephalography in pediatric epilepsy. J Pediatr Epilepsy. 2 (1), 73-85 (2013).
- Fiedler, P., Fonseca, C., Supriyanto, E., Zanow, F., Haueisen, J. A high-density 256-channel cap for dry electroencephalography. Hum Brain Mapp. 43 (4), 1295(2022).
- Sharon, D., Hämäläinen, M. S., Tootell, R. B. H., Halgren, E., Belliveau, J. W. The advantage of combining MEG and EEG: comparison to fMRI in focally-stimulated visual cortex. Neuroimage. 36 (4), 1225(2007).
- Pataraia, E., Lindinger, G., Deecke, L., Mayer, D., Baumgartner, C. Combined MEG/EEG analysis of the interictal spike complex in mesial temporal lobe epilepsy. Neuroimage. 24 (3), 607-614 (2005).
- Ahmed Mahmutoglu, M., Rupp, A., Baumgärtner, U. Simultaneous EEG/MEG yields complementary information of nociceptive evoked responses. Clin Neurophysiol. 143, 21-35 (2022).
- Aydin, Ü, et al. Combined EEG/MEG can outperform single modality EEG or MEG source reconstruction in presurgical epilepsy diagnosis. PLoS One. 10 (3), e0118753(2015).
- Bast, T., et al. Combined EEG and MEG analysis of early somatosensory evoked activity in children and adolescents with focal epilepsies. Clin Neurophysiol. 118 (8), 1721-1735 (2007).
- Chikara, R. K., et al. Electromagnetic source imaging predicts surgical outcome in children with focal cortical dysplasia. Clin Neurophysiol. 153, 88-101 (2023).
- Hari, R., et al. IFCN-endorsed practical guidelines for clinical magnetoencephalography (MEG). Clin Neurophysiol. 129 (8), 1720-1747 (2018).
- Bagić, A. I., Knowlton, R. C., Rose, D. F., Ebersole, J. S. American Clinical Magnetoencephalography Society Clinical Practice Guideline 1: Recording and analysis of spontaneous cerebral activity. J Clin Neurophysiol. 28 (4), 348-354 (2011).
- Papadelis, C., Chen, Y. H. Pediatric magnetoencephalography in clinical practice and research. Neuroimaging Clin N Am. 30 (2), 239-248 (2020).
- De Macedo Rodrigues, K., et al. A FreeSurfer-compliant consistent manual segmentation of infant brains spanning the 0-2 year age range. Front Hum Neurosci. 9, 21(2015).
- Tadel, F., Baillet, S., Mosher, J. C., Pantazis, D., Leahy, R. M. Brainstorm: A user-friendly application for MEG/EEG analysis. Comput Intell Neurosci. 2011, 879716(2011).
- Kane, N., et al. A revised glossary of terms most commonly used by clinical electroencephalographers and updated proposal for the report format of the EEG findings. Revision 2017. Clin Neurophysiol Pract. 2, 170-185 (2017).
- Lantz, G., et al. Propagation of interictal epileptiform activity can lead to erroneous source localizations: a 128-channel EEG mapping study. J Clin Neurophysiol. 20 (5), 311-319 (2003).
- Vorwerk, J., et al. A guideline for head volume conductor modeling in EEG and MEG. Neuroimage. 100, 590-607 (2014).
- Schrader, S., et al. DUNEuro-A software toolbox for forward modeling in bioelectromagnetism. PLoS One. 16 (6), e0252431(2021).
- Ntolkeras, G., et al. Presurgical accuracy of dipole clustering in MRI-negative pediatric patients with epilepsy: Validation against intracranial EEG and resection. Clin Neurophysiol. 141, 126-138 (2022).
- David, O., Kilner, J. M., Friston, K. J. Mechanisms of evoked and induced responses in MEG/EEG. Neuroimage. 31, 1580-1591 (2006).
- Pantev, C. Evoked and induced gamma-band activity of the human cortex. Brain Topogr. 7 (4), 321-330 (1995).
- Fox, N. A., et al. Assessing human mirror activity with EEG mu rhythm: A meta-analysis. Psychol Bull. 142 (3), 291-313 (2016).
- Genzer, S., Ong, D. C., Zaki, J., Perry, A. Mu rhythm suppression over sensorimotor regions is associated with greater empathic accuracy. Soc Cogn Affect Neurosci. 17 (9), 788-801 (2022).
- Janmohamed, M., et al. Moving the field forward: detection of epileptiform abnormalities on scalp electroencephalography using deep learning-clinical application perspectives. Brain Commun. 4 (5), 218(2022).
- Bagheri, E., Jin, J., Dauwels, J., Cash, S., Westover, M. B. A fast machine learning approach to facilitate the detection of interictal epileptiform discharges in the scalp electroencephalogram. J Neurosci Methods. 326, 108362(2019).
- Thomas, J., et al. Automated detection of interictal epileptiform discharges from scalp electroencephalograms by convolutional neural networks. Int J Neural Syst. 30 (11), 2050030(2020).
- Zijlmans, M., Zweiphenning, W., van Klink, N. Changing concepts in presurgical assessment for epilepsy surgery. Nat Rev Neurol. 15 (10), 594-606 (2019).
- Akiyama, T., et al. Focal resection of fast ripples on extraoperative intracranial EEG improves seizure outcome in pediatric epilepsy. Epilepsia. 52 (10), 1802-1811 (2011).
- Duncan, J. S., Winston, G. P., Koepp, M. J., Ourselin, S. Brain imaging in the assessment for epilepsy surgery. Lancet Neurol. 15 (4), 420(2016).
- Jacobs, J., et al. High-frequency electroencephalographic oscillations correlate with outcome of epilepsy surgery. Ann Neurol. 67 (2), 209-220 (2010).
- Ricci, L., et al. Virtual implantation using conventional scalp EEG delineates seizure onset and predicts surgical outcome in children with epilepsy. Clin Neurophysiol. 139, 49-57 (2022).
- Stefan, H., Rampp, S. Interictal and Ictal MEG in presurgical evaluation for epilepsy surgery. Acta Epileptologica. 2, 11(2020).
- Jahangiri, F. R., Chima, G. S., Pearson, M., Jackson, J., Siddiqui, A. A. Mapping of the language cortex. Cureus. 13 (5), e14960(2021).
- Merrifield, W. S., Simos, P. G., Papanicolaou, A. C., Philpott, L. M., Sutherling, W. W. Hemispheric language dominance in magnetoencephalography: sensitivity, specificity, and data reduction techniques. Epilepsy Behav. 10 (1), 120-128 (2007).
- Wheless, J. W., et al. Magnetoencephalography (MEG) and magnetic source imaging (MSI). Neurologist. 10 (3), 138-153 (2004).
- Breier, J. I., Simos, P. G., Zouridakis, G., Papanicolaou, A. C. Lateralization of activity associated with language function using magnetoencephalography: a reliability study. J Clin Neurophysiol. 17 (5), 503-510 (2000).
- Pataraia, E., Baumgartner, C., Lindinger, G., Deecke, L. Magnetoencephalography in presurgical epilepsy evaluation. Neurosurg Rev. 25 (3), 141-159 (2002).
- Babajani-Feremi, A., et al. Language mapping using high gamma electrocorticography, fMRI, and TMS versus electrocortical stimulation. Clin Neurophysiol. 127 (3), 1822-1836 (2016).
- Brodbeck, V., et al. Electroencephalographic source imaging: a prospective study of 152 operated epileptic patients. Brain. 134, Pt 10 2887-2897 (2011).
- Sohrabpour, A., et al. Effect of EEG electrode number on epileptic source localization in pediatric patients. Clin Neurophysiol. 126 (3), 472-480 (2015).
- Laohathai, C., et al. Practical fundamentals of clinical MEG interpretation in epilepsy. Front Neurol. 12, 722986(2021).
- Corona, L., et al. Mapping functional connectivity of epileptogenic networks through virtual implantation. Proceedings of the Annu Int Conf IEEE Eng Med Biol Soc. 2021, 408-411 (2021).
- Corona, L., et al. Non-invasive mapping of epileptogenic networks predicts surgical outcome. Brain. 146 (5), 1916-1931 (2023).
- Rijal, S., et al. Functional connectivity discriminates epileptogenic states and predicts surgical outcome in children with drug resistant epilepsy. Sci Rep. 13 (1), 9622(2023).
- Tamilia, E., et al. Noninvasive mapping of ripple onset predicts outcome in epilepsy surgery. Ann Neurol. 89 (5), 911-925 (2021).
- Matarrese, M. A. G., et al. Spike propagation mapping reveals effective connectivity and predicts surgical outcome in epilepsy. Brain. 146 (9), 3898-3912 (2023).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유