需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
扩大目标,脐血细胞毒性T淋巴细胞,巨细胞病毒,EB病毒,腺病毒
摘要
在这里,我们描述的第一个好生产质量管理规范(GMP)标准的方法从脐带血幼稚T细胞的来源主要是病毒特异性细胞毒性T淋巴细胞(CTL)。
摘要
干细胞移植后的病毒感染是最常见的死亡原因,尤其是在脐带血(CB)移植(CBT),CB不包含相当数量的病毒有经验的T细胞可以保护收件人感染。1 -我们和其他人表明,病毒特异性CTL产生的血清学阳性的捐助者,并注入到收件人的安全和保护。5-8然而,直到最近,病毒特异性T细胞不能产生脐带血,可能是由于病毒特异性记忆T细胞的缺乏。
为了更好地模仿体内吸幼稚T细胞的条件,我们建立了一个方法,该方法使用CB来源的树突状细胞(DC)的腺病毒载体(Ad5f35pp65)含有的免疫CMV抗原病毒pp65转,因此驱动T细胞特异性对巨细胞病毒和腺病毒。在开始,我们利用这些马捕获区议会,以及CB来源的T细胞的细胞因子的存在下,IL-7,IL-12和IL-15。[10]在所述第二刺激我们使用EBV-转化的B细胞,或EBV-LCL,同时表达潜在的和裂解EB病毒抗原。 ad5f35pp65转导的EBV-LCL是用于刺激的T细胞中的IL-15的存在,在第二次刺激。后续的刺激使用Ad5f35pp65转导的EBV-LCL和IL-2。
从50×10 6 CB单核细胞中,我们能够产生向上的150×10 6病毒特异性T细胞,裂解抗原脉冲的目标和释放细胞因子响应于抗原刺激11将这些细胞在GMP兼容的方式制造,使用仅分馏脐带血单元分数的20%,并已被翻译供临床使用。
研究方案
1。单核细胞分离(0天)
- 插入秒杀到出口的20%部分的脐带血阴鲁尔适配器,连接注射器和清除血液中。解冻血液转移到20毫升温热在50ml离心管中的RPMI。用5毫升的RPMI冲洗脐血袋和转移到相同的离心管中。
- 离心细胞以400×g进行10分钟。吸出上清液。
- 在20毫升的温暖的RPMI重悬细胞。到在50ml离心管中的15毫升淋巴制剂层细胞。离心40分钟@ 400×克。
- 含有单核细胞的收获的接口,并在20毫升的RPMI清洗。离心10分钟@ 450×克。
- 吸液上清液,并在20毫升的RPMI清洗。计数细胞和旋转5分钟@ 400×克。
- 吸液上清液和重悬细胞,在5×10 6个细胞/ mL的Cellgenix:直流介质(无血清)。为EBV-LCL代的取出1毫升,放入15毫升CEntrifuge管。
2。树突状细胞生成(第0天)
- 板2毫升的细胞(已经在5×10 6细胞/ mL的直流媒体)成一个6孔板每孔。发表在1-2个小时的孵化器。
- 1-2小时后,洗掉非贴壁细胞,用PBS洗涤3-4次。收集非粘附细胞,并冷冻。加入2毫升/ DC含1000 U / mL的IL-4和GM-CSF 800 U / mL的。
- DC启动后3-4天,补充IL-4,加入100μL/孔含终浓度为1000U/mL IL-4和800 U / mL的GM-CSF和GM-CSF。
- 5-6天收获DC刮以及用移液管。计数的大细胞,离心5分钟@ 400×克。吸液媒体和重悬DC在2×10 6细胞/ mL的直流媒体。加入0.5 mL /孔24孔培养板。
- 转导DC使用Ad5f35pp65的MOI为每个单元10传染性单位矢量。添加vector到24孔板的各孔中。孵育细胞1.5小时。 1.5小时后,加入1.5毫升/ DC媒体含1000 U / mL的IL-4,800 U / mL的GM-CSF,10 ng / mL的TNF-α,1μg/ mL的PGE-1,100毫微克/毫升IL-6,和10 ng / mL的IL-1β。这些细胞因子成熟的区议会。
3。 EBV-LCL(从第0天开始)的生成
- 含有5×10 6单核细胞的离心管。添加200μL浓EBV B95.8上清液和完整的媒体的1.8毫升的(RPMI + 10%FBS + 2mM的L-谷氨酰胺)含环孢霉素(1微克/毫升)。
- 等分试样100μL的细胞分为10个孔的96孔板中,分为5口井和200μL。添加100μL完整的媒体+环孢素的孔中只有100μL的细胞。填写剩余的井用无菌水。
- 饲料LCL每周和扩大从96孔板,24孔板后1〜2周。一个星期后,转移到T25烧瓶,并在随后的一星期转移到一个T75烧瓶中。在这个阶段,我们建议您冻结等分LCL。它通常需要1个月,以产生足够数量的LCL。
4。 CTL启动 - 7天开始后的区议会
- 嘉实区议会和30 Gy的照射。洗4 x和计数。 :重悬直流在T细胞的介质,含人血清(45%RPMI,45%CLICK,10%人血清,2mM L-谷氨酰胺)@ 1×10 5个区议会/毫升。
- 解冻从步骤2.2的非粘附细胞。洗涤细胞,并计数。重悬在2×10 6在含有人血清的T细胞介质的非贴壁细胞/ mL。加入10纳克/毫升的IL-7和IL-12,和5 ng / mL的IL-15。添加1毫升的细胞在24孔板上每孔。每孔加入1 mL的DC。填充空的24孔板的孔中,用无菌水。
- 后7天,饲料和/或T细胞起始分裂细胞与T细胞的介质,含有人血清。
- T细胞后9-12天开始,冻结的T细胞,直到LCL准备。
- ØNCE LCL已经扩大,在T75烧瓶中传代,转导LCL 5分钟@ 400×g下离心。加入到细胞沉淀的载体在100传染性单位每个细胞的MOI。孵育1.5小时。 1.5小时后,重新悬浮在完整的媒体在5×10 5 LCL /毫升,并在24孔板中,每孔加入2毫升12
- 术后第2天,收获LCL在40 Gy的照射。洗4 x和计数。重悬LCL在T细胞介质中含有2.5×10 5细胞/ mL的人血清。加入1 mL的LCL的24孔培养板每孔。此外,添加到的Grex40的培养装置,以及5 ng / mL的IL-15的5×10 6个 LCL 13
- 收获的T细胞。离心机@ 400×g离心5分钟,吸出上清液,并重新悬浮在含有1×10 6个 T细胞/ mL的人血清的T细胞介质。加入5 ng / mL的IL-15,并加入1毫升/孔的T细胞(总数为1×10 6个 T细胞),已经在24孔板上的LCL。在的Grex40,带来介质的总体积达30毫升。
- 每天3-4刺激后,如果细胞是汇合,然后将它们分割(板)1:1,并添加新鲜培养基中含50 U / mL的IL-2。如果他们不汇合,然后简单地吸½媒体和更换含50 U / mL的IL-2。在的Grex40,吸一半的媒体,更换新鲜的培养基,并添加50 U / mL的IL-2。
- 在第7天,重复在步骤4.6,但使用的IL-2的刺激的天,IL-15的。
5。代表性的成果
按照GMP标准FDA批准的制造协议的示意图, 如图1所示。这个过程需要50天左右。典型的产生病毒特异性T细胞扩大预先存在的记忆T细胞,然而,脐血缺乏病毒经验丰富的T细胞,因此,我们需要素幼稚T细胞的体外方法。要做到这一点,我们使用的树突状细胞,以及细胞因子IL-7,IL-12和IL-15,必要产生病毒特异性。
经过3刺激,收率 应该超过100×10 6个细胞。如果有足够的细胞是不可用时,可以进行额外的刺激,直到所需的号码的CTLs可用。这些细胞的大部分应该是CD3 +,CD4 +和CD8 + T细胞的混合物。应该有小于15%的NK细胞(CD3-/CD56 +)且小于1%CD19 + B细胞( 图2)。
扩大的CTL识别的抗原病毒pp65从巨细胞病毒,六邻体和聚氯从腺病毒,以及众多的EBV抗原表达于EBV-LCL。测试时,酶联免疫斑点法,CTL分泌IFN-?响应于比不相干抗原( 图3)的这些抗原。
,CTL还应该裂解抗原肽脉冲目标这样的PHA爆炸。在51 Cr释放试验,CTL裂解LCL,CMVpp65脉冲和腺病毒六邻体和/或聚氯脉冲的目标,但不是脉冲与目标不相关肽( 图4)。
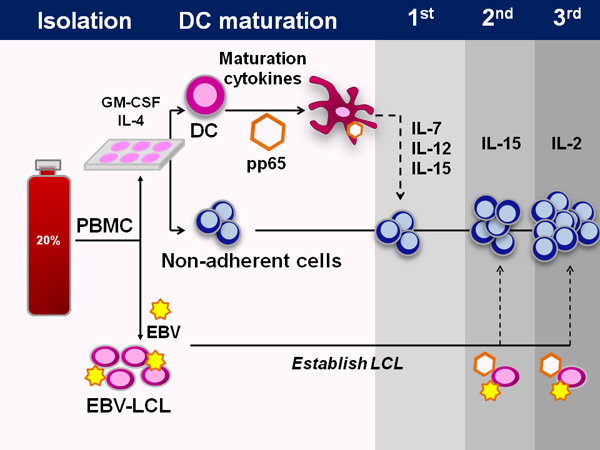
图1。生成多病毒特异性CTL从脐带血 。示意图显示CTL制造的全过程,从脐带血。首先,脐带血单核细胞分离出20%的馏分的分馏脐血单元。散货代保存中的5×10 6个细胞的异常,然后,所有的细胞铺板在树突状细胞的介质为1-2小时,在该点的非粘附细胞的收获和冻结。的DC,然后输入DC媒体中IL-4和GM-CSF。经过5天的文化,是成熟的DC和巨细胞病毒抗原的免疫细胞病毒pp65的腺病毒载体转导的。发起,这些DC的非贴壁细胞,以及细胞因子IL-7,IL-12的结合,和IL-15。在随后的刺激,使用相同的腺病毒载体转导EBV-LCL,被用作抗原呈递细胞。 IL-15是用于在第二次刺激和其后的IL-2。
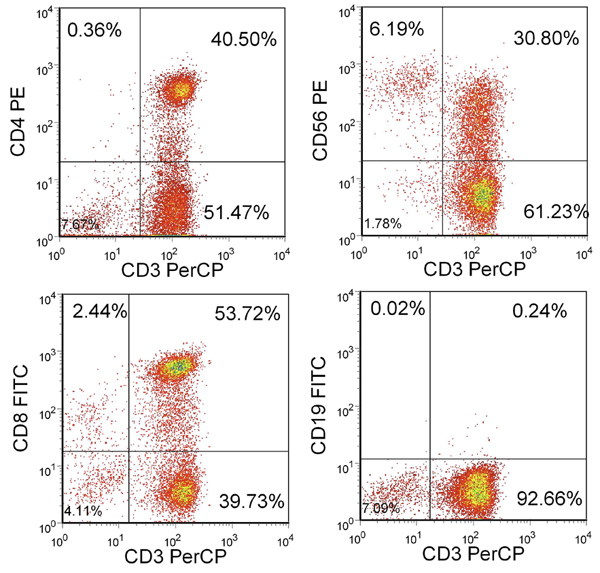
图2。产生的T细胞表型 。所示出的是活细胞的百分比,在淋巴细胞门控。 CTL是CD3 +,CD4 +或CD8 +,但主要CD3-/CD56-和CD19-。
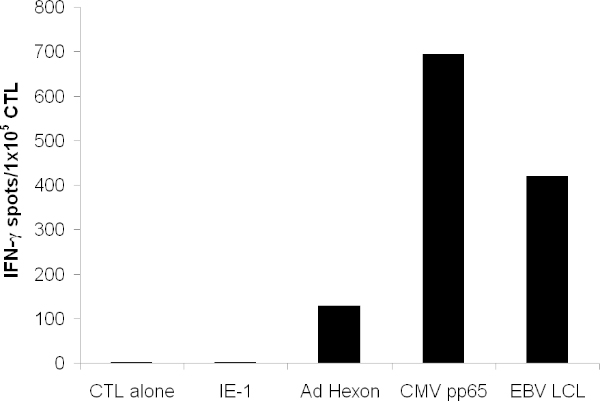
图3的T细胞的功能 。由IFN-γELISPOT的T细胞特异性进行了测试。脉冲跨越整个六邻体蛋白,聚氯,病毒pp65的重叠肽,T细胞和不相关的抗原IE-1。 CTL单独表示单独的媒体。自体LCL照射,并添加1×10 5 /孔。显示的是的平均斑点形成细胞C指望。2-15的三个孔。
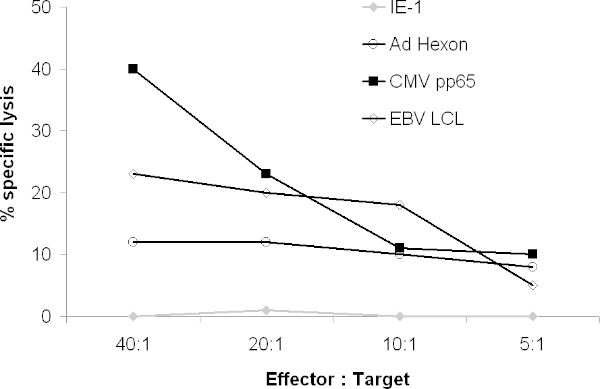
图4的CTL的细胞溶解活性 。所得的CTL裂解表达病毒抗原的目标的能力进行了测试中的51 Cr的检测。,跨越整个抗原或51 Cr-标记的自体LCL与CTL共培养的重叠肽脉冲的51 Cr-标记的自体的PHA爆炸。 4小时后,γ释放γ计数器上计数。
Access restricted. Please log in or start a trial to view this content.
讨论
目的是在控制病毒感染后,CBT目前的战略是有效的,但他们都与显著的毒性,价格昂贵,并且不授予长期保护,对以后的感染。事实上,一些抗病毒药物的使用可能会限制病毒特异性T细胞,否则将保护的膨胀。14另一种选择是来自供体的病毒特异性T细胞的输注。我们和其他人表明,这种T细胞是安全,有效和符合成本效益的。15日至17日在这里,我们表明,这种方法也可以扩展...
Access restricted. Please log in or start a trial to view this content.
披露声明
作者有没有透露。
致谢
这项工作得到了一个丹·邓肯的合作研究资助(CMB和EJS),美国国家心脏,肺,和血液研究所(US4HL081007),白血病和淋巴瘤协会临床研究学者奖(CMB),美国国家癌症研究所(RO1 CA06150816 EJS)。
Access restricted. Please log in or start a trial to view this content.
材料
| Name | Company | Catalog Number | Comments |
| 试剂名称 | 公司 | 目录编号 | |
| RPMI 1640 | Invitrogen公司 | 21870-076 | |
| DC媒体 | CellGenix | 20801-0500 | |
| EHAA(点击的中等) | Irvine Scientific公司 | 9195 | |
| 人血清 | 双子座生物制品 | 100-110 | |
| 透气性Cultureware 18 | 威尔逊狼 | 80040S | |
| IL-2的 | 凯龙(TCH药剂) | ||
| IL-12的 | NCI / CTEP的 | ||
| IL-15的 | CellGenix | 1013-050 | |
| IL-7的 | R&D | AFL207 | |
| IL-1β | R&D | AFL201 | |
| IL-6的 | 细胞Genix | 1004-050 | |
| GM-CSF | TCH药剂 | ||
| IL-4的 | R&D | AFL204 | |
| TNF-α的 | R&D | AFL210 | |
| Ad5f35pp65 | BCM CAGT载体生产设施 | ||
| 等离子传输带阴Luer适配器 | “联合国宪章”医疗 | 89-550-66J | |
| 淋巴制剂 | 奈科明 | 1114550 |
参考文献
- Kennedy-Nasser, A. A. Comparable outcome of alternative donor and matched sibling donor hematopoietic stem cell transplant for children with acute lymphoblastic leukemia in first or second remission using alemtuzumab in a myeloablative conditioning regimen. Biol. Blood Marrow Transplant. 14, 1245-1245 (2008).
- Hanley, P. J. Improving clinical outcomes using adoptively transferred immune cells from umbilical cord blood. Cytotherapy. 12, 713(2010).
- Szabolcs, P., Cairo, M. S. Unrelated umbilical cord blood transplantation and immune reconstitution. Semin. Hematol. 47, 22(2010).
- Canto, E., Rodriguez-Sanchez, J. L., Vidal, S. Distinctive response of naive lymphocytes from cord blood to primary activation via TCR. J. Leukoc. Biol. 74, 998-998 (2003).
- Leen, A. M. Monoculture-derived T lymphocytes specific for multiple viruses expand and produce clinically relevant effects in immunocompromised individuals. Nat. Med. 12, 1160-1160 (2006).
- Riddell, S. R. Restoration of viral immunity in immunodeficient humans by the adoptive transfer of T cell clones. Science. 257, 238(1992).
- O'Reilly, R. J. Adoptive transfer of antigen-specific T-cells of donor type for immunotherapy of viral infections following allogeneic hematopoietic cell transplants. Immunol. Res. 38, 237-237 (2007).
- Peggs, K. S. Adoptive cellular therapy for early cytomegalovirus infection after allogeneic stem-cell transplantation with virus-specific T-cell lines. Lancet. 362, 1375-1375 (2003).
- Sili, U. Large-scale expansion of dendritic cell-primed polyclonal human cytotoxic T-lymphocyte lines using lymphoblastoid cell lines for adoptive immunotherapy. J. Immunother. 26, 241(2003).
- Bollard, C. M. Good manufacturing practice-grade cytotoxic T lymphocytes specific for latent membrane proteins (LMP)-1 and LMP2 for patients with Epstein-Barr virus-associated lymphoma. Cytotherapy. 13, 518(2011).
- Hanley, P. J. Functionally active virus-specific T cells that target CMV, adenovirus, and EBV can be expanded from naive T-cell populations in cord blood and will target a range of viral epitopes. Blood. 114, 1958(1958).
- Hanley, P. J. Expansion of T cells targeting multiple antigens of cytomegalovirus, Epstein-Barr virus and adenovirus to provide broad antiviral specificity after stem cell transplantation. Cytotherapy. , (2011).
- Gerdemann, U. Generation of Multivirus-specific T Cells to Prevent/treat Viral Infections after Allogeneic Hematopoietic Stem Cell Transplant. J. Vis. Exp. (51), e2736(2011).
- Mori, T., Kato, J. Cytomegalovirus infection/disease after hematopoietic stem cell transplantation. Int. J. Hematol. 91, 588(2010).
- Einsele, H. Infusion of cytomegalovirus (CMV)-specific T cells for the treatment of CMV infection not responding to antiviral chemotherapy. Blood. 99, 3916(2002).
- Bao, L. Expansion of cytomegalovirus pp65 and IE-1 specific cytotoxic T lymphocytes for cytomegalovirus-specific immunotherapy following allogeneic stem cell transplantation. Biol. Blood Marrow Transplant. 14, 1156(2008).
- Shpall, E. J., Bollard, C. M., Brunstein, C. Novel cord blood transplant therapies. Biol. Blood Marrow Transplant. 17, Suppl 1. S39-S45 (2011).
- Vera, J. F. Accelerated production of antigen-specific T cells for preclinical and clinical applications using gas-permeable rapid expansion cultureware (G-Rex. J. Immunother. 33, 305(2010).
Access restricted. Please log in or start a trial to view this content.
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。