Method Article
简单重症监护研究中重复临床检查和重症监护超声检查的观察性研究方案
摘要
结构化方案对于为危重患者的研究问题提供答案是必要的。简单重症监护研究 (SICS) 为危重患者的重复测量提供了基础设施,包括临床检查、生化分析和超声检查。SICS 项目有特定的重点,但结构对其他调查是灵活的。
摘要
通过临床检查、生化分析和重症监护超声检查 (CCUS) 相结合对危重患者进行纵向评估,可以在早期发现干预的不良事件,例如液体超负荷。简单重症监护研究 (SICS) 是一条专注于临床变量组合的预后和诊断价值的研究线。
SICS-I 特别关注使用急性入院后 24 小时内获得的临床变量来预测心输出量 (CO) 和死亡率。其续集 SICS-II 侧重于 ICU 入住期间的重复评估。由训练有素的研究人员在入院后 3 小时内进行第一次临床检查,包括体格检查和有根据的猜测。第二次临床检查在入院后 24 小时内进行,包括身体检查和有根据的猜测、生化分析和心脏、肺、下腔静脉 (IVC) 和肾脏的 CCUS 评估。该评估在入院后第 3 天和第 5 天重复。CCUS 图像由独立专家验证,所有数据都注册在在线安全数据库中。90 天的随访包括根据患者的病历和市级人员登记处登记并发症和生存状态。SICS-II 的主要关注点是静脉充血与器官功能障碍之间的关联。
发布本协议的目的是提供有关这项正在进行的前瞻性观察队列研究的结构和方法的详细信息,以允许回答多个研究问题。阐明了危重患者联合临床检查和 CCUS 评估的数据收集设计。SICS-II 对其他中心开放,也可以接受可以用我们的数据回答的其他研究问题。
引言
重症监护病房 (ICU) 收治的患者病情最危重,合并症和多病发生率高,与入院诊断无关。因此,ICU 是调查共病和多病症、它们对患者预后的负面影响以及危重病如何导致导致更多多病症的并发症的场所。深入了解这个异质性的患者群体,对每个患者进行详细检查是最重要的。
简单重症监护研究 (SICS) 研究线旨在评估由医学专家协调的专门学生研究人员团队收集的 ICU 患者临床、血流动力学和生化变量的综合选择的预后和诊断价值。SICS-I 的主要目标之一是研究与重症监护超声检查 (CCUS) 测量的心输出量 (CO) 定义的休克最相关的临床检查结果的组合1。SICS-II 使用 SICS-I 的结构,但增加了重复的临床检查、生化分析和 CCUS。SICS-II 的主要重点是量化静脉充血并确定可能导致其发展的变量。重复测量提供有关患者病程的动态信息。研究表明,危重患者存在液体超负荷,液体超负荷与新的发病率有关。因此,我们专注于这些患者的静脉充血。此外,几项研究表明过量输液可能产生的负面影响 2,3,4,5,6。液体超负荷可被视为静脉充血或静脉液超负荷,这可能通过中心静脉压 (CVP) 升高或外周水肿来观察到。中心静脉系统压力升高可能导致器官灌注减少,继而出现器官衰竭,但静脉充血尚无确切定义。
先前的研究表明与过量液体给药相关的负面影响使用静脉充血的单一替代测量,例如 CVP、IVC 塌陷性、液体平衡和/或外周水肿 7,8,9,10。据我们所知,SICS-II 是第一项对多个器官进行重复 CCUS 的研究,并结合临床检查结果来评估 ICU 患者的血流动力学状态。关注这种多器官超声检查技术很重要,因为器官衰竭或器官功能减退总是影响整个血流动力学系统。我们预计 SICS-II 中反复检查的数据将有助于揭示静脉充血的病理生理学和后果。因此,这可能有助于改善对有静脉充血风险的危重患者的早期识别,并指导液体给药的优化。此外,可以探讨静脉充血与短期和长期器官衰竭之间的关联。最后,SICS-II 协议的成功实施将证明,与专门的学生研究人员团队一起进行大型前瞻性研究是可行的,并且可以产生高质量的数据来调查临床问题。
在这里,展示了对 ICU 患者进行全面临床检查以测量静脉充血的程序。SICS-II 的简明协议于 clinicaltrials.gov11 日发布。在第一次初步临床检查后,最多进行 3 次额外的临床检查、生化分析和 CCUS。体格检查包括反映外周灌注/微循环的变量,例如毛细血管再充盈时间 (CRT) 或斑点,以及宏循环的变量,例如血压、心率和尿量。此外,还记录了标准的护理实验室值(例如乳 酸、pH 值)。随后,进行心脏、肺、IVC 和肾脏的 CCUS 以获取灌注信息。进一步的方法将在我们的统计分析计划中详细说明,就像在 SICS-I12 中所做的那样。
根据 2018 年 5 月 14 日至 2018 年 8 月 15 日期间纳入的 138 名患者,重复测量该结构内的广泛临床变量似乎是可行的。我们还表明独立验证是可行的。SICS-II 体现了一种有价值的方法,使研究人员能够准确记录感兴趣变量的变化,因此可以作为进行研究的指南,以反映日常实践中观察到的患者病情进展。SICS-II 研究每天由 2-3 名学生研究人员组成的团队随时进行,并有一名高级主管随时待命。这些学生研究人员接受过进行体格检查和 CCUS 的培训。他们执行以下协议的所有步骤,并负责在工作时间和周末接收患者。此外,一个由约 30 名学生组成的更大的 ICU 学生团队参加晚班和夜班,对新患者进行初步临床检查(入院后 3 小时内)。 图 1 显示了研究方案的示意图摘要, 图 2 和图 3 显示了用于在收集时注册数据的病例报告表 (CRF)。
研究方案
本研究是根据赫尔辛基宣言(第 64 版,巴西 2013 年)的原则和涉及人类受试者的医学研究法案 (WMO)、良好临床实践指南和当地机构审查委员会(Medisch Ethische Toetsingscommissie;M18.228393)。
1. 患者入住 ICU 和筛查
注意: 对于筛选,全天更新包含最少患者数据的数字列表,并登记包含和排除。筛选列表存储在安全的医院电子系统中,研究人员可以独家访问。为了保护患者隐私,列表的所有物理副本都会在一天结束时销毁。纳入标准是:急性和计划外入院;和 18 岁以上的患者。
- 筛选所有新入院的患者管理系统,并检查患者是否符合纳入标准。
- 立即排除再入院、选择性入院、18 岁以下的患者以及无法给予知情同意的患者。
注意: 我们还排除了非创伤性神经系统入院原因的患者,因为我们在 SICS-I 中建立了多个患者组,其中该组血流动力学稳定,ICU 入院主要涉及神经系统治疗1。 - 将可能的包含添加到持续更新的患者列表中。使用此列表根据入院/纳入时间每天计划新的和重复的测量。
2. 临床检查 1
注意: 对入院后 3 小时内符合纳入标准的所有患者进行第一次临床检查。如果患者在白班入院,则由学生研究人员进行此检查。对于在夜班或夜班入院的患者,第一次临床检查由 ICU 学生团队的一名成员进行,数据由学生研究人员在第二天处理和最终确定。有关第一次临床检查方案的完整描述,请参见 clinicaltrials.gov13。如果可能的话,在床边,询问患者当时是否同意进行临床检查。稍后获得书面知情同意书:有关说明,请参阅步骤 1.2 和步骤 7。
- 体检
- 首先确保患者遵守所需的安全/隔离规则:按照标准医院程序用 70% 的酒精消毒双手和手腕,并在接触患者时使用非无菌手套和塑料围裙或其他预防措施,例如隔离衣。
- 自我介绍,如果患者没有镇静、意识清醒且身体状况不佳,请征得患者允许进行检查。向患者解释正在做什么。
注意: 在入住 ICU 期间或出院到病房后的后期阶段,需要患者本人或近亲(如果患者不能)提供正式知情同意。步骤 7 中对此进行了更详细的描述。 - 从床边监护仪记录血流动力学变量心率、呼吸频率、收缩压 (SBP)、舒张压 (DBP)、平均动脉压 (MAP) 和中心静脉压 (CVP)。
- 记录血氧饱和度 (SpO2) 以及患者是否接受无创呼吸支持或机械通气。如果是这样,请记录呼气末正压 (PEEP) 和吸入 O2 分数 (FiO2)。
- 通过在皮肤上按压 10 秒并松开,然后计算直到完全再灌注的秒数来确定膝关节和胸骨的再灌注。
- 通过用手触诊四肢来确定主观皮肤温度,并估计它们是冷的还是热的。
- 从监测仪记录膀胱温度,监测仪显示由连接到留置导尿管的传感器测得的温度。
- 通过在脚背中间放置一个额外的温度传感器并将其连接到显示器,确定足背的皮肤温度。测量后,将气囊温度传感器重新连接到显示器。
- 如果可观察到,请使用 Ait-Oufella 膝关节量表14 对斑驳的程度进行评分。
- 登记患者是否接受镇静剂,如果是,则记录哪种药物、什么泵速和剂量。
- 确定并登记患者的格拉斯哥昏迷量表 (GCS)15。
- 根据有根据的猜测和临床检查的结果,估计患者的住院生存率、6 个月的生存率和返回原居地的能力16,17。也向护士和医生询问他们的估计值,并在 CRF 上登记所有估计值。
3. 临床检查 2
注意: 第二次临床检查在入院后 24 小时内进行,包括 CCUS 测量。这项检查始终由受过 CCUS 培训的学生研究人员进行,而不是由 ICU 学生团队的成员进行。此外,在符合纳入标准并接受临床检查 1 但后来显示仅患有神经系统疾病(例如, 非创伤性蛛网膜下腔出血)的患者中,不进行包括 CCUS 在内的重复测量,这些最终被排除在外。
- 获得知情同意。
注意:根据格罗宁根大学医学中心 (UMCG) 的观察测量规定,自 2016 年 1 月 1 日起,临床检查期间收集的超声图像可以在未经明确同意的情况下使用。然而,SICS-II 研究的政策是尽早寻求患者的知情同意,同时坚持尽量减少对患者的"压力"的原则,增加共同决策,并给患者足够的时间考虑参与。由于大多数患者无法在 ICU 住院早期提供同意,因此通常会获得"延迟"同意。相反,如果他们能够在检查之前或之后提供或拒绝同意,则不会执行这些同意,或者分别删除所有已获得的数据。- 在开始检查之前,通过确定他们的 GCS 分数来确定患者是否警觉/有意识并能够与学生研究人员互动。向有能力的患者提供有关将要进行的检查的说明,并留下一封他们必须签署的标准化书面信。
- 如果无法征询患者的同意(由于意识障碍、心智能力受限等),请每天监测他们的 GCS 评分,如果可以联系到家庭成员,请考虑获得家人的同意(如步骤 7.1 所述)。
- 按照临床检查 1 中描述的步骤进行体格检查。
- 进行心脏和肺部的 CCUS。
注意: 当在 材料表、用于胸骨旁长轴视图 (PLAX) 的心脏换能器,以及用于心尖四腔和五腔视图(AP4CH、AP5CH)的心脏相控阵换能器。对于其他超声系统,用户应查阅其特定设备的作手册。- 打开机器。注册患者的匿名研究 ID,开始新的检查,然后等待自动 2D 成像模式显示在屏幕上。
- 如果患者穿衣服,请解开他们的病袍扣子,露出胸部。如有必要,放置新的心电图 (ECG) 贴纸并将它们连接到超声机。
- 将心电图电缆从机器连接到患者的床边监护仪。等待它稳定并在 CRF 中记录 ECG 测量的心率。
- 如果可能,将患者稍微旋转左侧。这提高了心脏和肾脏成像的质量。
注意: 技术注意事项: 在开始检查之前,单击"配置"按钮,并将图像设置设置为五个心周期,深度为 10-15 cm,图像宽度为 65°,频率为 1.7/3.4 MHz。 - 在超声换能器上放置足量的超声凝胶,并将换能器放在胸骨左侧外侧,第 3 和第 5 肋间隙之间,以获得 2D 模式下的 PLAX 视图。根据需要调整深度以记录左心室流出道测量的图像并保存图像。
注意: 左心室的最大宽度应在二尖瓣最大打开时可见。不应看到瓣膜的肌肉。在将换能器放在患者的胸部之前,警告他们凝胶很冷,可能会感到不舒服,并且他们会感到一些压力(尤其是在记录左心室流出道 (LVOT) 的图像时胸骨周围)。请注意,对于肋骨折的患者,应避开某些部位,因为这可能会让患者感到不舒服。 - 在 2D 模式下,将深度调整到 15-20 厘米,并将换能器放在心尖上,尾部到左乳晕。获得 AP4CH 视图,所有四个腔室都清晰可见。保存图像。
- 滚动轨迹球,使光标位于三尖瓣和右心室壁之间的边界上,以获得三尖瓣环平面收缩偏移 (TAPSE)。按下 M 模式 按钮可获得正确的图像,并在看到定义的窦性波时保存。保存图像。
- 将光标放在带有轨迹球的三尖瓣上。减小图像的宽度以增加每秒的帧数,这是 RV S 质量所必需的。先按 TVI 按钮,然后按 PW 按钮,以获取 RV S 的正确图像并保存。
- 从 AP4CH 视图中,向上倾斜换能器(即将其压 平)以获得 AP5CH 视图并在屏幕上显示主动脉根部。保存图像。
- 将光标放在主动脉瓣的正上方,然后按下 PW 按钮以获得 LVOT 脉搏波多普勒。将光标放在测量 LVOT 直径的同一位置。以最高质量保存图像(清晰的多普勒波边界,内部为空,与逆行或二尖瓣血流明显区分)。这些稍后将用于计算速度时间积分 (VTI),然后计算 CO。
注意: 每次测量始终尝试至少获得三个流波。如果心律不齐,至少应保留 5 次波次。 - 使用相同的相控阵心脏换能器进行肺部超声检查,并将设置更改为 3.7 MHz 的频率,深度更改为 15 cm,并且仅在 2 个心脏周期内记录图像。根据 BLUE 协议 18,将传感器放置在 6 个不同的位置,传感器的灯光位于12 点钟位置。确保始终以相同的顺序获取图像,以避免在以后查看图像时产生混淆。
- 通过将换能器放置在两侧第 2 和第 3 肋骨的肋间隙上,获得肺部的前锁骨中部视图。保存每一侧的图像。
- 通过将换能器向下放置 2 至 3 根肋骨,获得肺部的下前锁骨中视图。保存每一侧的图像。
- 通过将换能器置于患者的腋窝下,获得肺部的中轴视图。保存每一侧的图像。
- 心脏和肺部成像完成后,擦去患者胸部多余的凝胶。
- 进行 IVC 和肾脏的 CCUS。
- 单击 Probe 按钮并使用轨迹球将有源探头更改为凸/曲线阵列(腹部)传感器,用于 IVC 和肾脏检查。对于两次测量,传感器的光(可用于定位)应位于 12 点钟位置。
- 使用 2D 模式并设置为 10-20 cm 的深度和 2.5/5.0 MHz 的频率,将换能器放在剑突正下方,并将其向患者右侧移动约 2 cm。IVC 应该变得可见。保存图像。
- 使用轨迹球将光标放在 IVC 上壁的正上方和管腔外,然后按下 M 模式 按钮。保存图像。
- 对于肾脏超声,从 2D 模式开始,将设置调整到 10-15 厘米的深度和 2.2/4.4 MHz 的频率。将换能器放在胸腔的背侧和尾侧。在图像中获取所选的肾脏中心并保存它。
注意: 确保将换能器尽可能放在背侧,以过滤掉肝组织和肠袢。为了可靠地测量肾脏长度,肾脏的边界应该清晰可见,并且中央窦复合体(肾脏的回声更强的中心)和皮层之间的距离在整个图像中应该相似。 - 按下 Color 按钮可获取肾脏的彩色多普勒图像并确定肾血管系统中的血流。将光标放在肾脏中心皮髓交界处的任何动脉上,使用轨迹球可以清楚地看到多普勒血流。
- 调整光标角度并按下 PW 按钮。如有必要,在 Active Mode 中调整信号幅度和对比度。保存图像。
- 确定是否还有足够的静脉信号(即, 在 y 轴的负半部分可见血流),这是以后测量所必需的。如果没有,请重复步骤 3.4.5 并将光标放在中间皮髓交界处的静脉上,那里可以看到静脉血流。保存图像。
- 所有成像完成后,断开所有电缆,擦去患者和换能器上多余的凝胶,给患者穿扎或覆盖,并使用超声认可的消毒湿巾清洁换能器。
4. 临床检查 3 和 4
注意: 如果患者仍在 ICU 中(即没有死亡或转移到病房), 则在入院后第 3 天和第 5 天进行第三和第四次临床检查。
- 体检
- 按照临床检查 1 中描述的步骤进行体格检查。
- 心脏和肺部的 CCUS
- 根据步骤 3.3 对心脏和肺部进行超声检查。由于它是静态测量,因此只需获得一次 LVOT,因此不必记录在临床检查 3 和 4 中。
- IVC 和肾脏的 CCUS
- 根据步骤 3.4 对 IVC 和肾脏进行超声检查。由于它是静态测量,因此只需获得一次肾长,因此不必在临床检查 3 和 4 中记录。
5. 超声检查的测量和分析
注意: 每次检查后,都会使用临床检查期间保存的图像来测量所需的变量。测量值记录在 CRF 上并转录到在线临床患者数据管理系统。除了稍后将用于验证的原始图像外,还应保存执行测量且可见的图像。
- LVOT 测量
- 单击 Probe 按钮选择心脏换能器以开始测量。
- 使用步骤 3.3.5 中保存的图像,当阀门完全打开时暂停图像。
- 单击 Measure 按钮,然后选择右侧菜单上的 Cardiac-Dimension-LVOT 选项,开始测量。
- 光标出现后,在舒张末期,在主动脉瓣底部选择两个点,从内边缘到内边缘,在管腔的每一侧各一个。保存图像。
注意: LVOT 测量必须在 CO 测量之前完成并保存,以便机器可以自动确定。
- 一氧化碳测量
- 使用步骤 3.3.10 中保存的图像,追踪左心室输出量。将水平扫描调整为 100 cm/s。
- 选择三个形状良好的空心波,这些波具有与心电图对齐的清晰边界。单击 Measure 按钮并使用轨迹球选择 Cardiac-Aortic-LVOT Trace 选项。
- 追踪波形线,从基线开始和结束,超声机会自动计算 CO。对三个波形重复此作并保存此图像。
注意: 如果心律不规则,记录五个波的平均 CO 值。
- 塔普斯
- 使用步骤 3.3.7 中保存的 M 模式图像,单击 Measure 按钮,然后使用轨迹球选择右侧菜单上的 Cardiac-Dimension-TAPSE 选项。
- 首先将光标放在定义明确的窦性波的最低点上,然后放在最高点上。两者之间的差异 (TAPSE) 应显示在屏幕的左上角。分三个窦性波进行此作,并取三个 TAPSE 测量值的平均值。保存图像。
- 右心室收缩偏移 (RV S')
- 使用步骤 3.3.8 中保存的图像,单击 卡尺 按钮并将光标放在定义明确的曲线的最高峰上。分三条曲线执行此作并取平均值。保存图像。
- Kerley B 线伪影评估
注意: 代表正常肺表面的水平 A 线可用于检测 B 线的参考。这些起源于胸膜,与 A 线相比是高回声的。- 调整图像的对比度和/或增益。B 线并不总是在保存的图像中立即可见。
- 确定并注册获得的六张图像中每张图像的 Kerley B 线数量。由于 B 线的数量没有保存在机器中,因此必须立即在 CRF 上注册(介于 0 和 5 之间)。
- IVC 直径和塌陷性
- 单击 Probe 按钮选择腹部传感器以开始测量。
- 使用步骤 3.4.2 中保存的 2D 图像,单击 卡尺 按钮并测量 IVC 两壁之间的距离,距离其进入右心房的位置 2 厘米。这是 IVC 直径,请保存此图片。
- 使用步骤 3.4.3 中保存的 M 模式图像,单击 卡尺 按钮并测量 IVC 呼气和吸气直径。保存此图像。
注意: IVC 的呼气直径和吸气直径分别是 M 型图像中看到的最大和最小直径。
- 肾脏长度和血流量
- 使用步骤 3.4.4 中保存的 2D 图像,单击 卡尺 按钮并绘制从尾部到肾皮层颅端的最长线。这是以厘米为单位的肾脏长度,请在 CRF 中登记此发现。保存此图像。
- 使用步骤 3.4.6 中保存的多普勒图像,分析基线以下看到的静脉血流线为连续、单相或双相。在 CRF 中注册结果。
- 使用步骤 3.4.6 中保存的图像,单击 测量 按钮并使用轨迹球选择右侧菜单上的 腹部-肾脏-PS/ED/RI 选项。
- 将光标放在 y 轴正半部分脉动流波的峰值和最低点上。
注意: 如果存储了连续的脉动血流波,G6 机器可以使用以下公式自动计算多普勒肾阻力指数 (RRI):RRI =(峰值收缩速度 - 舒张末期速度)/峰值收缩速度。将图像与超声机的测量值一起保存在屏幕上。 - 使用步骤 3.4.6 或 3.4.7 中保存的图像,单击 卡尺 按钮,然后将光标放在峰值最大流速上,然后放在最低点(即舒张末期 )的最大流速上19。测量后保存图像。
注意: 静脉阻抗指数 (VII) 的计算公式为:VII =(峰值收缩速度 — 舒张末期速度)/ 峰值收缩速度20,21。在单相血流的情况下,VII 没有记录,因为只有一个峰是可见的,没有舒张期和收缩期是可区分的。
6. 超声图像的数据注册、存储和验证
注意: 如图 1 所示,数据配准在每次临床检查后进行。下面描述了将从电子健康记录中检索到的测量、临床检查和生化信息(表 2)获得的数据输入研究对象的匿名在线文件的过程。
- 访问在线安全的患者管理系统,并打开最近纳入的患者的档案。登记血气分析值、一般血清变量、血清肾变量和 24 小时尿液分析。 表 2 列出了获得的所有变量及其作说明。
- 验证心脏 CCUS 图像。
注意: 此验证由心血管成像核心实验室的独立专家根据 EACVI 指南22 完成。评估学生研究人员获得的图像质量并重复执行的测量,以确保尺寸测量和速度分布跟踪的质量要求。- 在舒张末期进行 LVOT 测量,如主动脉瓣下方的 ECG 信号所示。
- 在 AP5CH 视图中跟踪从 LVOT 获取的 PW 信号,以获得左心室每搏输出量和左心室 CO。
- 验证 IVC 和肾脏的所有图像和测量值。这应由经验丰富的独立腹部放射科医生进行。如果在临床检查期间无法获得所需的图像,可以请独立的腹部放射科医生进行 CCUS,在这种情况下,无需进行进一步验证。
7. 患者随访
- 登记知情同意书
- 如果在任何临床检查期间或临床检查方案完成后获得患者或家属同意,但患者仍被收治入院,请在患者数据管理系统中登记并上传手写签署的同意书。
- 如果同意被拒绝,请在患者数据管理系统中登记此内容以及未获得同意的原因,并通知研究协调员,研究协调员将删除所有患者数据。
- 死亡率数据
- 对于在入院期间死亡的患者,请直接从电子病历和相关死因中登记死亡率。
- 对于没有院内死亡率的患者,请从荷兰的市政登记处获取死亡率数据,该登记处每 90 天更新一次。
结果
这些代表性结果的目的是说明该协议的可行性。
病人
在 2018 年 5 月 14 日至 2018 年 8 月 15 日期间,共有 663 名患者入住 ICU。其中,208 名患者符合纳入条件(排除原因如图 4 所示)。49 名患者被排除在外,因为正在进行的复苏工作无法进行 CCUS。7 例患者拒绝参加 (无知情同意),4 例患者无法进行 CCUS,例如,由于机械通气的俯卧位或真空辅助闭合大伤口,导致 138 例纳入患者有数据进行分析。
CCUS 验证和图像质量
计划对心脏影像学进行广泛的验证。肾脏超声验证已启动。到目前为止,验证了 21 名患者 (15%) 的图像。在 18 例患者 (86%) 中,图像质量足够。列出了所有不赞成图像的原因,并返回给进行超声检查的研究人员以反馈。记录进行超声检查的研究人员的姓名,以便能够使用类内相关系数 (ICC) 评估观察者之间和观察者内的变异性。精确的统计方法将在我们的统计分析计划中描述,就像在 SICS-I12 中所做的那样。
示例案例:患者 X,中年女性
患者 X 在被发现意识障碍和低血压后入院。所有获得的测量值均如 表 1 所示。所有变量均在规定的时间内获得,没有丢失数据,说明了该协议的可能可行性。入院后 3 小时内进行第一次临床检查。在这次检查中,患者被镇静、插管并需要血管加压药治疗。10 小时后进行第二次临床检查,输注 700 mL 液体后显示生命体征稳定。血管加压药减少。CCUS 和生化分析显示心脏、 IVC 和肾功能正常 (图 5 、 图 6 和 图 7)。在 T3,两天后,停用血管加压药,但累积正液体平衡上升至 6 L,伴有 CO 升高、IVC 增宽和肾灌注减少,血清肌酐升高反映了肾灌注和功能减少。在 T4,入院后 5 天,体液平衡和血清肌酐进一步升高,患者出现 3 期 AKI。患者在入院后 2 天因来源不明的多器官衰竭死亡。
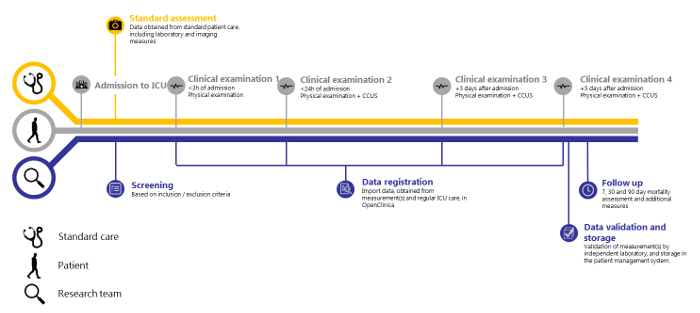
图 1:SICS-II 研究概述。 SICS-II 研究的时间表,从患者入院到重症监护室到数据登记的最后一步。 请单击此处查看此图的较大版本。

图 2:用于临床检查的病例报告表 (CRF) 1. CRF 由 ICU 团队的学生或学生研究人员在进行第一次临床检查时填写。 请单击此处查看此图的较大版本。

图 3:临床检查 2、3 和 4 的病例报告表 (CRF)。 CRF 由 ICU 团队的学生或学生研究人员在进行第二次、第三和第四次临床检查时填写。 请单击此处查看此图的较大版本。
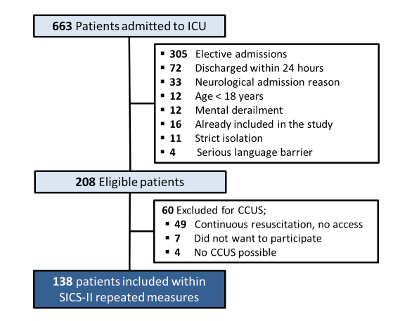
图 4:SICS-II 患者纳入和排除图表。 描述截至 2018 年 8 月 15 日的 SICS-II 研究中患者纳入和排除标准的流程图。 请单击此处查看此图的较大版本。
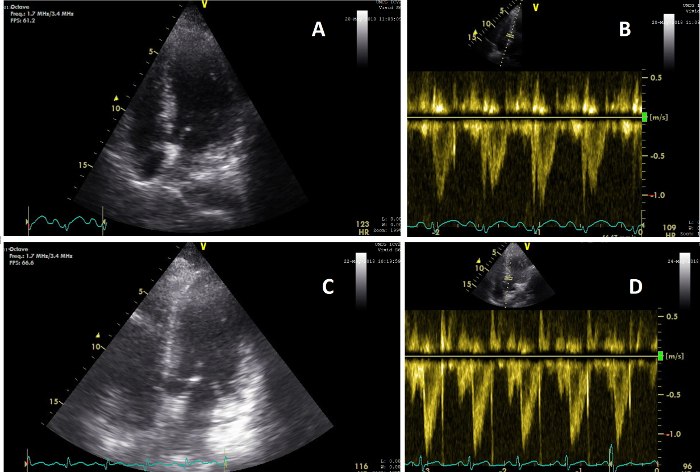
图 5:显示心脏功能变化的根尖视图。 (A) 临床检查期间进行的 CCUS 期间 AP4CH 视图上的心脏图像 2 (T=2);(B) T=2 时的心脏 VTI 脉搏波信号图像,显示 CO 为 5.6 L/min;(C) 临床检查期间进行 CCUS 期间 AP5CH 视图上的心脏图像 3 (T=3);(D) T=3 时的心脏 VTI 脉搏波信号图像,显示 CO 为 8.3 L/min。 请单击此处查看此图的较大版本。
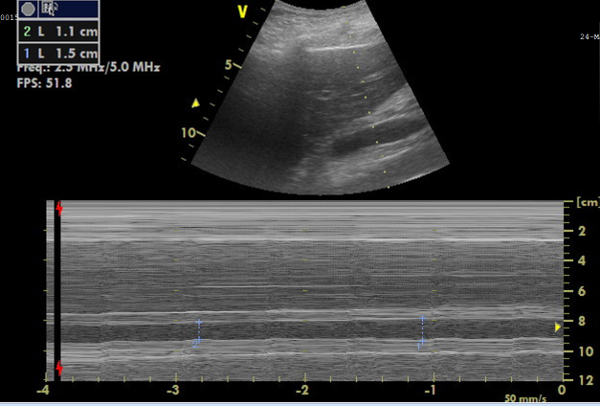
图 6:用于直径测量的下腔静脉 (IVC) 的 M 型图像。 顶部是实时显示 IVC 的图像,下面是代表 IVC 直径变化的 M 型图像,从中可以计算出塌陷性。 请单击此处查看此图的较大版本。
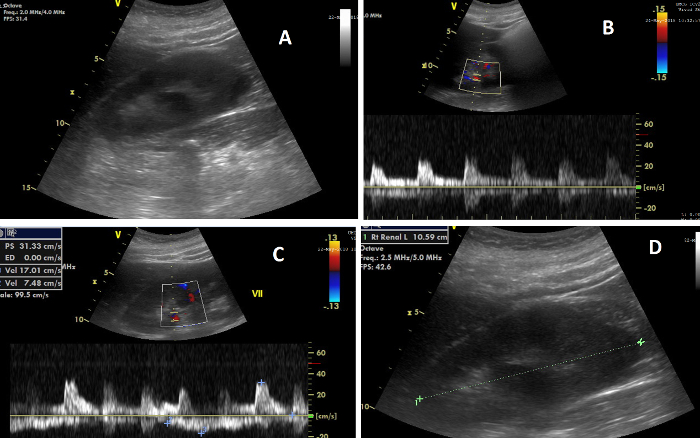
图 7:肾脏超声检查的各种要素。 (A) CCUS 期间右肾的图像;(B) 图像,顶部显示肾动脉中的多普勒血流,下方显示计算肾阻力指数的流波;(C) 顶部显示肾静脉中的多普勒血流的图像,下面是计算静脉阻抗指数的流波;(D) 说明肾长度测量的图像。 请单击此处查看此图的较大版本。
| 变量 | T1 第 1 天,00:38 | T2 型 第 1 天,10:53 | T3 第 3 天,10:14 | T4 系列 第 5 天,10:20 |
| 心率 (bpm) | 110 | 124 | 122 | 98 |
| 呼吸频率(每分钟呼吸次数) | 24 | 15 | 26 | 12 |
| 收缩压 (mmhg) | 100 | 115 | 130 | 118 |
| 舒张压 (mmhg) | 61 | 69 | 66 | 65 |
| 平均动脉压 (mmhg) | 73 | 80 | 84 | 81 |
| 累积体液平衡 (mL) | 0 | 704 | 7272 | 12338 |
| 机械通气 | PEEP 5,FiO2 40% | PEEP 5,FiO2 40% | PEEP 5,FiO2 30% | PEEP 5,FiO2 30% |
| CRT 胸骨(秒) | 1.5 | 2 | 4 | 3 |
| 中心温度 (◦ C) | 37.6 | 37.5 | 38.0 | 37.4 |
| 前一小时的尿量 (mL) | 117 | 60 | 0 | 10 |
| 服用正性肌力药 | 去 甲 肾上腺素 0.1 毫克/毫升 3.0 毫升/小时 | 去 甲 肾上腺素 0.1 毫克/毫升 1.0 毫升/小时 | 没有 | 没有 |
| 服用镇静剂 | 异丙酚 20 毫克/毫升 5.0 毫升/小时 | 没有 | 没有 | 没有 |
| APACHE IV 评分 | 92 | 88 | 87 | 90 |
| SOFA 评分 | 8 | 8 | 5 | 8 |
| LVOT (厘米) | 不适用 | 2.4 | 2.4 | 2.4 |
| 心输出量 (L/min) | 不适用 | 5.6 | 8.34 | 9.89 |
| TAPSE (毫米) | 不适用 | 25 | 26 | 21 |
| RV S' (厘米/秒) | 不适用 | 14 | 15 | 12 |
| IVC 吸气直径 (cm) | 不适用 | 1.14 | 1.24 | 1.10 |
| IVC 呼气直径 (cm) | 不适用 | 1.27 | 1.38 | 1.50 |
| Kerley B 线(总计) | 不适用 | 6 | 2 | 4 |
| 肾长 (cm) | 不适用 | 10.59 | 不适用 | 不适用 |
| 肾内静脉血流模式 | 不适用 | 连续的 | 连续的 | 连续的 |
| 多普勒肾 RI | 不适用 | 0.61 | 0.75 | 0.70 |
| 七 | 不适用 | 0.33 | 0.56 | 0.68 |
表 1:随机 SICS-II 患者。 患者 X,中年女性,被发现意识障碍后入住 ICU。缩写:bpm = 每分钟心跳次数,CRT = 毛细血管再充盈时间,LVOT = 左心室流出道,TAPSE = 三尖瓣环平面收缩偏移,RV S' = 右心室收缩偏移,IVC = 下腔静脉,RRI = 肾阻力指数,VII = 静脉阻抗指数,N.A. = 不适用。
| 变量 | 单位 | 源 | 获取地点 |
| 授乳 | 毫摩尔/升 | 动脉血气分析 | 从标准护理开始,每次临床检查都尽可能接近,最大差异 12 小时 |
| 氯化物 | 毫摩尔/升 | 动脉血气分析 | 从标准护理开始,每次临床检查都尽可能接近,最大差异 12 小时 |
| 酸碱度 | 动脉血气分析 | 从标准护理开始,每次临床检查都尽可能接近,最大 12 ho 差异 | |
| PCO2 | 千帕斯卡 | 动脉血气分析 | 从标准护理开始,每次临床检查都尽可能接近,最大差异 12 小时 |
| PaO2 (二氧化硅) | 千帕斯卡 | 动脉血气分析 | 从标准护理开始,每次临床检查都尽可能接近,最大差异 12 小时 |
| HCO3- | 毫摩尔/升 | 动脉血气分析 | 从标准护理开始,每次临床检查都尽可能接近,最大差异 12 小时 |
| 血红蛋白 | 毫摩尔/升 | 动脉血气分析 | 从标准护理开始,每次临床检查都尽可能接近,最大差异 12 小时 |
| 白 | 10 x 10-9/升 | 血清分析 | 从标准护理开始,每次临床检查都尽可能接近,最大差异 12 小时 |
| 长链细胞 | 10 x 10-9/升 | 血清分析 | 从标准护理开始,每次临床检查都尽可能接近,最大差异 12 小时 |
| HS 肌钙蛋白 | 纳克/升 | 血清分析 | 从标准护理开始,每次临床检查都尽可能接近,最大差异 12 小时 |
| ASAT | 单位 / L | 血清分析 | 从标准护理开始,每次临床检查都尽可能接近,最大差异 12 小时 |
| 阿拉特 | 单位 / L | 血清分析 | 从标准护理开始,每次临床检查都尽可能接近,最大差异 12 小时 |
| 总胆红素 | uoml/L | 血清分析 | 从标准护理开始,每次临床检查都尽可能接近,最大差异 12 小时 |
| 肌酸酐 | umol/L | 血清分析 | 从 ICU 入院开始的所有测量 |
| 尿量 | 毫升 | 24 小时的尿液收集 | 从 ICU 入院开始的所有测量 |
| 肌酸酐 | 毫摩尔/24 小时 | 尿液分析 | 从 ICU 入院开始的所有测量 |
表 2:获得的生化变量列表。 此处列出了研究期间收集的所有患者生化变量。
讨论
所有检查都需要根据方案进行。只有根据预先指定的定义进行体格检查才有价值23.应根据方案收集实验室值以获得所有值。如步骤 3.3 所述,清晰、可解释的 CCUS 图像是回答本研究研究问题的关键。如果获得图像质量较差的图像,则无法执行步骤 5 中描述的测量和分析,并且重复测量的目的将失效。采取了三种重要措施来最大限度地降低获得低质量图像的风险。首先,在我们的研究中执行 CCUS 的学生研究人员由经验丰富的心脏病专家重症监护医师培训。文献表明,短期培训计划非常适合获得 CCUS24 的基本能力。其次,学生研究人员在前 20 次考试期间由一名高级学生研究人员监督,因此他们可能会收到实际反馈。最后,所有获得的心脏和肾脏图像将分别由心脏成像核心实验室的独立专家和经验丰富的腹部放射科医生重新评估和验证,以确保数据可靠。
为了保证图像质量,研究人员还需要注意其他方面。有时需要重新涂抹超声凝胶或重新定位探头,使其更好地与患者皮肤接触,以确保最佳图像质量。花足够的时间来获得最佳图像也很重要,如果有疑问,应在完成临床检查之前咨询高级研究人员,即监督心脏病专家-重症监护医师或核心实验室技术人员。通过执行图 1 中显示的协议化步骤,确保对所有超声图像的持续评估和验证。此外,学生研究人员和专家经常交换反馈,从而可以轻松快速地实施协议更改,以进一步提高图像和测量的质量。这种频繁的验证使系统错误易于检测,因此可以相应地调整未来学生研究人员的 CCUS 培训。此外,向所有团队成员开放的月度会议允许对协议进行全面评估和(如有必要)修改。
全天候进行患者筛查和纳入是成功实施本研究的另一个关键因素。这只能通过拥有一支专门的学生研究人员团队、一个庞大的学生团队提供支持以及与 ICU 护理人员的良好协调来实现。这种协调是通过护理人员和研究人员之间定期的低风险接触来实现的,以优化与标准护理的合作。
该协议的一个局限性是,成功进行 CCUS 取决于放置探头的预先指定位置的可访问性。在 SICS-I 期间,已经表明,当患者需要阻碍理论上最佳超声心动图窗口的引流管、纱布或伤口敷料时,不能进行心脏CCUS1。此外, 通过 IVC 测量所需的经胸超声心动图获得适当肋下窗口的可能性先前已被证明在一般 ICU 人群中可能受到限制25。该协议在不同时间点进行不同检查所需的 24/7 可用性也是一个潜在的限制,因为一些中心可能缺乏这样做的能力。即使在像 UMCG 这样的大型学术医院,确保这也导致了研究开始的延迟。超声测量的另一个固有限制是测量结果的观察者间差异。为了保证 24/7 全天候纳入患者,一名研究人员不可能对所有纳入的患者进行所有临床检查。本研究旨在让同一研究人员对同一患者进行所有超声测量,以最大限度地减少个体层面的变异性,但对于整个队列,观察者间的变异性仍然是一个问题。
多个器官的超声成像是一种快速、安全、有效的结构,用于可视化器官灌注和功能。这是所有医疗专业人员都应该能够使用的便捷工具,对于基于简单、标准化方案的测量,通常应该提供可靠的测量结果。
此外,大多数评估超声检查,尤其是超声心动图使用的观察性研究,本质上是回顾性的,或者仅包括少数患者。26 该协议允许对未选择的危重患者队列进行 24/7 结构化筛选,其中可以定义感兴趣的亚群,从而允许同时调查多个研究问题。
此外,尽管众所周知,重症监护中的临床变量是高度动态的并且相互影响,但大多数研究仅调查了特定器官的单一超声测量的附加价值27,28。这是第一个专注于重复测量、全身超声和静脉充血的方案。我们预计 SICS-II 将更准确地反映患者在 ICU 入住期间的血流动力学状态。
SICS 中使用的当前结构可以应用于大量设置,目前正在研究添加其他元素。它的优势在于基础研究线和适应性线的结合,其中新变量可以很容易地添加到 CRF 中,以便研究新的研究问题。这种适应性的一个例子是通过变形成像(即短期劳损 )在特定患者子集的常规方案中增加了广泛的脑室壁评估。
此外,患者纳入目前仅在 ICU 中进行,现在错过了部分患者的护理轨迹。ICU 患者通常首先被送入急诊科 (ED),并在 ICU 出院后留在普通医院病房。因此,SICS 旨在通过在急诊室到达时纳入患者,并从初始入院开始登记干预措施和血流动力学功能,从而在早期阶段纳入患者。此外,在 ICU 出院到普通病房后进行 CCUS 的计划也在进行中,以便可以在每个预定义的研究时间对所有患者进行测量。另一个重要方面是该协议对其他中心的可扩展性:它的简单性允许中心轻松适应,这些中心可以自己开始纳入。
最后,结构化 CCUS 方案的开发和成功实施也可能产生临床影响。尽管仅用于研究目的,但它可以在拟议的短期培训期后由医生用于临床 CCUS。然后评估促进对(没有经验的)医生进行 CCUS 培训是否会减少额外的诊断测试会很有趣。
披露声明
作者没有什么可披露的。
致谢
我们要感谢 SICS-I 研究组的所有成员,他们参与了 SICS-I 并参加了有关当前协议的头脑风暴会议。我们还要感谢重症监护科研究局及其协调员的支持;W. Dieperink 博士和 M. Onrust。此外,我们要感谢 ICU 学生团队和学生研究人员,他们迄今为止在结构上将患者纳入 SICS-II;JA de Bruin,BE库宁,K. Selles 博士。
材料
| Name | Company | Catalog Number | Comments |
| Ultrasound machine | GE Healthcare | 0144VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound machine | GE Healthcare | 3507VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound machine | GE Healthcare | 0630VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound gel | Parker | 01-08 | Aquasonic 100 ultrasound transmission gel |
| Temperature probe | DeRoyal | 81-010400EU | Skin Temperature Sensor |
参考文献
- Hiemstra, B., et al. Clinical examination, critical care ultrasonography and outcomes in the critically ill: cohort profile of the Simple Intensive Care Studies-I. BMJ open. 7 (9), 017170(2017).
- Lee, J., et al. Association between fluid balance and survival in critically ill patients. Journal of Internal Medicine. 277 (4), 468-477 (2015).
- Perner, A., et al. Fluid management in acute kidney injury. Intensive Care Medicine. 43 (6), 807-815 (2017).
- Balakumar, V., et al. Both Positive and Negative Fluid Balance May Be Associated With Reduced Long-Term Survival in the Critically Ill. Critical care medicine. 45 (8), 749-757 (2017).
- Hjortrup, P. B., et al. Restricting volumes of resuscitation fluid in adults with septic shock after initial management: the CLASSIC randomised, parallel-group, multicentre feasibility trial. Intensive Care Medicine. 42 (11), 1695-1705 (2016).
- Prowle, J. R., Kirwan, C. J., Bellomo, R. Fluid management for the prevention and attenuation of acute kidney injury. Nature reviews. Nephrology. 10 (1), 37-47 (2014).
- Gambardella, I., et al. Congestive kidney failure in cardiac surgery: the relationship between central venous pressure and acute kidney injury. Interactive CardioVascular and Thoracic Surgery. 23 (5), 800-805 (2016).
- Chen, K. P., et al. Peripheral Edema, Central Venous Pressure, and Risk of AKI in Critical Illness. Clinical journal of the American Society of Nephrology : CJASN. 11 (4), 602-608 (2016).
- Song, J., et al. Value of the combination of renal resistance index and central venous pressure in the early prediction of sepsis-induced acute kidney injury. Journal of critical care. 45, 204-208 (2018).
- Zhang, L., Chen, Z., Diao, Y., Yang, Y., Fu, P. Associations of fluid overload with mortality and kidney recovery in patients with acute kidney injury: A systematic review and meta-analysis. Journal of Critical Care. 30 (4), (2015).
- Simple Intensive Care Studies II - Full Text View. ClinicalTrials.gov. , Available from: https://clinicaltrials.gov/ct2/show/NCT03577405? term=simple+intensive+care+studies (2018).
- Wetterslev, J. Statistical analysis plan Simple Intensive Care Studies-I DETAILED STATISTICAL ANALYSIS PLAN (SAP) 1. Administrative information 1.1. Title, registration, versions and revisions. ClinicalTrials.gov. , Available from: https://clinicaltrials.gov/ProvidedDocs/24/NCT02912624/SAP_000.pdf (2018).
- van der Horst, I. C. C. Simple Observational Critical Care Studies - Full Text View - ClinicalTrials.gov. ClinicalTrials.gov. , Available from: https://clinicaltrials.gov/ct2/show/NCT03553069 (2018).
- Ait-Oufella, H., et al. Alteration of skin perfusion in mottling area during septic shock. Annals of Intensive Care. 3 (1), 31(2013).
- Teasdale, G., Jennett, B. Assessment of Coma and Impaired Consciousness: A Practical Scale. The Lancet. 304 (7872), 81-84 (1974).
- Detsky, M. E., et al. Discriminative Accuracy of Physician and Nurse Predictions for Survival and Functional Outcomes 6 Months After an ICU Admission. JAMA. 317 (21), 2187(2017).
- Lipson, A. R., Miano, S. J., Daly, B. J., Douglas, S. L. The Accuracy of Nurses' Predictions for Clinical Outcomes in the Chronically Critically Ill. Research & reviews. Journal of nursing and health sciences. 3 (2), 35-38 (2017).
- Lichtenstein, D. A. BLUE-protocol and FALLS-protocol: two applications of lung ultrasound in the critically ill. Chest. 147 (6), 1659-1670 (2015).
- Tang, W. H. W., Kitai, T. Intrarenal Venous Flow: A Window Into the Congestive Kidney Failure Phenotype of Heart Failure. JACC: Heart Failure. 4 (8), 683-686 (2016).
- Jeong, S. H., Jung, D. C., Kim, S. H., Kim, S. H. Renal venous doppler ultrasonography in normal subjects and patients with diabetic nephropathy: Value of venous impedance index measurements. Journal of Clinical Ultrasound. 39 (9), 512-518 (2011).
- Iida, N., et al. Clinical Implications of Intrarenal Hemodynamic Evaluation by Doppler Ultrasonography in Heart Failure. JACC: Heart Failure. 4 (8), 674-682 (2016).
- Lang, R. M., et al. Recommendations for Cardiac Chamber Quantification by Echocardiography in Adults: An Update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. European Heart Journal - Cardiovascular Imaging. 16 (3), 233-271 (2015).
- Hiemstra, B., Eck, R. J., Keus, F., van der Horst, I. C. C. Clinical examination for diagnosing circulatory shock. Current opinion in critical care. 23 (4), 293-301 (2017).
- Vignon, P., et al. Basic critical care echocardiography: validation of a curriculum dedicated to noncardiologist residents. Critical care medicine. 39 (4), 636-642 (2011).
- Jensen, M. B., Sloth, E., Larsen, K. M., Schmidt, M. B. Transthoracic echocardiography for cardiopulmonary monitoring in intensive care. European journal of anaesthesiology. 21 (9), 700-707 (2004).
- Koster, G., van der Horst, I. C. C. Critical care ultrasonography in circulatory shock. Current opinion in critical care. 23 (4), 326-333 (2017).
- Haitsma Mulier, J. L. G., et al. Renal resistive index as an early predictor and discriminator of acute kidney injury in critically ill patients; A prospective observational cohort study. PloS one. 13 (6), 0197967(2018).
- Micek, S. T., et al. Fluid balance and cardiac function in septic shock as predictors of hospital mortality. Critical care. 17 (5), London, England. 246(2013).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。