Method Article
簡易集中治療研究における反復臨床検査およびクリティカルケア超音波検査のための観察研究プロトコル
要約
構造化されたプロトコルは、重篤な患者の研究課題に対する答えを提供するために必要です。Simple Intensive Care Studies(SICS)は、臨床検査、生化学分析、超音波検査など、重症患者における反復測定のためのインフラストラクチャを提供します。SICSプロジェクトには特定の焦点がありますが、構造は他の調査に対して柔軟です。
要約
臨床検査、生化学分析、救命救急超音波検査(CCUS)の組み合わせによる重症患者の縦断的評価は、体液過負荷などの介入の有害事象を早期に検出する可能性があります。Simple Intensive Care Studies(SICS)は、臨床変数の組み合わせの予後的および診断的価値に焦点を当てた研究ラインです。
SICS-I は、急性期入院後 24 時間以内に得られた臨床変数を使用して、心拍出量 (CO) と死亡率を予測することに特に焦点を当てました。その続編であるSICS-IIは、ICU入室時に繰り返し評価を行うことに焦点を当てています。訓練を受けた研究者による最初の臨床検査は、入院後3時間以内に行われ、身体検査と教育を受けた推測で構成されています。2回目の臨床検査は入院後24時間以内に行われ、身体検査と教育を受けた推測、生化学分析、心臓、肺、下大静脈(IVC)、腎臓のCCUS評価が含まれます。この評価は、入院後 3 日目と 5 日目に繰り返されます。CCUS画像は独立した専門家によって検証され、すべてのデータはオンラインの安全なデータベースに登録されます。90日目のフォローアップには、患者のカルテと市町村の人名簿による合併症と生存状態の登録が含まれます。SICS-IIの主な焦点は、静脈うっ血と臓器機能障害との関連です。
このプロトコルを公開する目的は、この進行中の前向き観察コホート研究の構造と方法の詳細を提供することであり、複数の研究の質問に答えることができます。重症患者における臨床検査とCCUS評価を組み合わせたデータ収集の設計が説明されています。SICS-IIは、他のセンターが参加できるように開放されており、私たちのデータで答えることができる他の研究課題にも開放されています。
概要
集中治療室(ICU)に入院した患者は、入院診断に関係なく、併存疾患および多疾患の発生率が高い最も重篤な疾患です。したがって、ICUは、併存疾患と多疾患、それらが患者の転帰に与える悪影響、および重篤な疾患が追加の多疾患に寄与する合併症をどのように引き起こすかを調査するための環境です。この不均一な患者グループで洞察を得ることは、個々の患者の詳細な検査が最も興味深いものです。
Simple Intensive Care Studies(SICS)研究ラインは、医療専門家がコーディネートした学生研究者の専任チームによって収集されたICU患者の臨床的、血行動態的、生化学的変数の包括的な選択の予後および診断的価値を評価することを目的として設計されています。SICS-Iの主な目的の1つは、クリティカルケア超音波検査(CCUS)1で測定された心拍出量(CO)によって定義されるショックに最も関連する臨床検査所見の組み合わせを調査することです。SICS-IIは、SICS-Iの構造を踏襲しつつも、臨床検査、生化学分析、CCUSを繰り返し追加しています。SICS-IIの主な焦点は、静脈うっ血を定量化し、その発症に寄与する可能性のある変数を特定することです。測定を繰り返すことで、患者の病気の経過に関する動的な情報が得られます。研究によると、重症患者には体液過剰が存在し、体液過剰は新たな罹患率と関連していることが示されています。したがって、これらの患者の静脈うっ血に焦点を当てます。さらに、いくつかの研究は、過剰な水分投与の可能性のある悪影響を示唆しています2,3,4,5,6。体液過負荷は、静脈うっ血または静脈体液過負荷として認識され、中心静脈圧(CVP)または末梢浮腫の増加によって観察される場合があります。中心静脈系の圧力上昇は、臓器灌流の減少とそれに続く臓器不全の一因となる可能性がありますが、静脈うっ血の正確な定義は存在しません。
過剰な体液投与に関連する悪影響を示唆した以前の研究では、CVP、IVCの虚脱性、体液バランス、および/または末梢浮腫などの静脈うっ血の単一の代理測定が使用されていました7,8,9,10。私たちの知る限り、SICS-IIは、ICU患者の血行動態を評価するために、臨床検査の結果と組み合わせて複数の臓器の反復CCUSを実施した最初の研究です。臓器不全や臓器機能の低下は常に血行動態システム全体に影響を与えるため、この多臓器超音波検査技術に焦点を当てることが重要です。SICS-IIで繰り返しの検査で得られたデータから、静脈うっ血の病態や影響の解明に役立つと期待しています。したがって、これは、静脈うっ血のリスクがある重篤な患者の早期特定を改善し、輸液投与の最適化を導くのに役立つ可能性があります。さらに、静脈うっ血と短期および長期の臓器不全との関連を探ることができます。最後に、SICS-IIプロトコルが成功裏に実施されれば、専任の学生研究者チームによる大規模な前向き研究の実施が可能であり、臨床問題を調査するための質の高いデータが得られることが明らかになります。
ここでは、静脈うっ血の測定を目的としてICU患者の包括的な臨床検査を行う手順を示します。SICS-IIの簡潔な議定書がclinicaltrials.gov 11日に発表されました。初回の初回臨床検査後、最大3回の追加臨床検査、生化学解析、CCUSを実施します。身体検査は、毛細血管補充時間(CRT)やまだらなどの末梢灌流/微小循環を反映する変数と、血圧、心拍数、尿量などの大循環の変数で構成されます。また、標準治療の検査値(乳酸、pHなど) も登録されています。その後、心臓、肺、IVC、腎臓のCCUSを実施して、灌流に関する情報を取得します。さらなる方法は、SICS-I12で行われたように、統計分析計画内で詳しく説明されます。
2018 年 5 月 14 日から 2018 年 8 月 15 日までの 138 人の患者に基づくと、この構造内の幅広い臨床変数の反復測定は実行可能であると思われます。また、独立した検証が実行可能であることも示します。SICS-IIは、研究者が関心のある変数の変化を正確に記録するための貴重な方法論を例示しており、日常診療で見られる患者の状態の進行を反映した研究を実施するためのガイドとして機能します。SICS-IIの研究は、常に2〜3人の学生研究者のチームによって毎日実施され、上級監督者が待機しています。これらの学生研究者は、身体検査とCCUSの実施について訓練を受けています。彼らは、次のプロトコルのすべてのステップを実行し、勤務時間中と週末の両方で患者を含める責任があります。また、約30名のICU学生チームが夜間・夜勤に参加し、新規患者の初診(入院後3時間以内)を実施しています。 図1 は試験プロトコルの概略概要を示し、 図2 と図3 は収集時にデータを登録するために使用される症例報告書(CRF)を示しています。
プロトコル
この研究は、ヘルシンキ宣言(第64版、ブラジル2013年)の原則に従って実施され、ヒトを対象とする医学研究法(WMO)、Good Clinical Practiceのガイドライン、および地元の施設審査委員会(Medisch Ethische Toetsingscommissie;M18.228393)。
1. ICUへの入院とスクリーニング
手記: スクリーニングでは、最小限の患者データを含むデジタルリストが終日更新され、包含と除外が登録されます。スクリーニングリストは、研究者専用の安全な病院の電子システムに保存されます。患者のプライバシーを保護するため、リストのすべての物理的なコピーは一日の終わりに破棄されます。選択基準は次のとおりです:急性および計画外の入院;18歳以上の患者。
- すべての新規入院について患者管理システムをスクリーニングし、患者が選択基準を満たしているかどうかを確認します。
- 再入院、選択的入院、18歳未満の患者、およびインフォームドコンセントを提供できない患者を直ちに除外します。
手記: また、SICS-Iでは複数の患者グループを設立しており、このグループは血行動態が安定しており、ICUへの入院は主に神経学的治療に関係しているため、非外傷神経学的入院理由のある患者も除外しています1。 - 継続的に更新される患者リストに、可能なインクルージョンを追加します。このリストを使用して、入院/登録の時間に基づいて、毎日新しい測定と繰り返し測定を計画します。
2. 臨床検査1
手記: 最初の臨床検査は、入院後3時間以内に選択基準を満たすすべての患者で実施されます。この検査は、患者が日勤中に入院した場合、学生研究者によって行われます。夜間や夜勤で入院した患者さんに対しては、この初回臨床検査はICUの学生チームの一員が行い、翌日には学生研究者がデータを処理して確定します。最初の臨床検査のプロトコルの完全な説明については、clinicaltrials.gov13を参照してください。ベッドサイドでは、可能であれば、その瞬間に臨床検査に同意するかどうかを患者さんに尋ねます。書面によるインフォームドコンセントは後で取得されます:手順についてはステップ1.2を、ステップ7を参照してください。
- 健康診断
- まず、患者に必要な安全/隔離ルールを確保することから始めます:標準的な病院の手順に従って手と手首を70%アルコールで消毒し、非滅菌手袋とプラスチック製のエプロンを使用するか、患者との接触時には隔離ガウンなどの追加の予防策を使用します。
- 自己紹介をし、患者が鎮静剤を投与されておらず、意識があり、適切でない場合は、検査を行う許可を求めてください。患者に何が行われているのかを説明します。
手記: 正式なインフォームドコンセントは、ICU入院中または病棟への退院後の段階で、患者自身または患者ができない場合は近親者から求められます。これについては、ステップ 7 で詳しく説明します。 - 血行動態変数の心拍数、呼吸数、収縮期血圧 (SBP)、拡張期血圧 (DBP)、平均動脈圧 (MAP)、および中心静脈圧 (CVP) をベッドサイド モニターから登録します。
- 酸素飽和度 (SpO2) と、患者が非侵襲的な呼吸サポートを受けているか、機械的に換気されているかを登録します。その場合は、呼気終末陽圧(PEEP)と吸気O2 の割合(FiO2)を登録します。
- 膝と胸骨の再灌流を決定するには、皮膚を10秒間押して離し、完全な再灌流までの秒数を数えます。
- 四肢を手で触診して主観的な皮膚温度を決定し、それらが冷たいか暖かいかを推定します。
- モニターから膀胱温度を記録し、留置尿道カテーテルに取り付けられたセンサーで測定した体温を表示します。
- 足の背の中央に追加の温度センサーを配置し、モニターに接続して、足の背側の皮膚温度を決定します。この測定後、膀胱温度センサーをモニターに再接続します。
- Ait-Oufella膝スケール14を使用して、観察可能な場合はまだらの程度を採点します。
- 患者が鎮静剤を投与されているかどうか、また、投与されている場合は、どの薬剤を、どのポンプ速度で、どの投与量で投与しているかを登録します。
- 患者のグラスゴー昏睡スケール (GCS) を決定して登録します15。
- 患者の病院での生存率、6か月の生存率、および知識に基づいた推測とこの臨床検査の結果に基づいて元の住居に戻る能力を推定します16,17。看護師と医師にも見積もりを依頼し、すべての見積もりをCRFに登録します。
3. 臨床検査2
手記: 2回目の臨床検査は入院後24時間以内に実施され、CCUS測定が含まれます。この審査は、常にCCUSの訓練を受けた学生研究者が実施し、ICUの学生チームのメンバーによって行われるものではありません。また、選択基準を満たし、臨床検査1を受けたが、 後にもっぱら神経疾患(非外傷性くも膜下出血)であることが示された患者では、CCUSを含む反復測定は行われず、最終的には除外されます。
- インフォームドコンセントを取得します。
注: フローニンゲン大学医療センター (UMCG) の観察測定に関する規則に基づき、2016 年 1月 1 日 により、臨床検査中に収集された超音波画像は、明示的な同意なしに使用できます。しかし、SICS-II試験では、患者からのインフォームドコンセントをできるだけ早期に求めると同時に、患者への「ストレス」を最小化し、意思決定の共有を増やし、患者が参加を検討するための十分な時間を与えるという原則を支持する方針です。ほとんどの患者はICU滞在の早い段階で同意を提供できないため、通常は「遅延」同意が得られます。逆に、審査の前後に同意を提供または拒否できる場合は、それぞれ実施しないか、すでに取得したデータをすべて削除します。- 検査を開始する前に、患者が警戒心/意識があり、GCSスコアを決定することにより、学生研究者と関わることができるかどうかを判断します。有能な患者に実施する検査に関する説明を提供し、彼らが署名しなければならない標準化された書面による手紙を残します。
- 患者が同意のために相談できない場合 (意識障害、精神的能力の制限など)、GCS スコアを毎日監視し、家族が連絡可能な場合は家族の同意を得ることを検討してください (ステップ 7.1 で説明)。
- 臨床検査1の手順に従って身体検査を行います。
- 心臓と肺のCCUSを実行します。
手記: このプロトコルは、超音波装置を 資料表、胸骨傍長軸図(PLAX)用の心臓トランスデューサー、および頂端4および5チャンバービュー(AP4CH、AP5CH)用の心臓フェーズドアレイトランスデューサー。その他の超音波システムについては、ユーザーは特定のデバイスの操作マニュアルを参照する必要があります。- マシンの電源を入れます。患者の匿名のスタディIDを登録し、新しい検査を開始し、自動2Dイメージングモードが画面に表示されるのを待ちます。
- 患者が服を着ている場合は、ガウンのボタンを外して胸を露出させます。新しい心電図(ECG)ステッカーを貼り、必要に応じて超音波装置に接続します。
- マシンからのECGケーブルを患者のベッドサイドモニターに接続します。安定するのを待ち、ECGで測定した心拍数をCRFに登録します。
- 可能であれば、患者を左側に少し回転させて配置します。.これにより、心臓と腎臓の両方の画像検査の品質が向上します。
手記: 技術的な考慮事項: 検査を開始する前に、[ 設定 ] ボタンをクリックし、画像設定を 5 心周期、深さ 10–15 cm、画像幅 65°、周波数 1.7/3.4 MHz に設定します。[ プローブ ] ボタンをクリックして、正しいプローブが選択されているかどうかを確認します。 - 超音波トランスデューサーに十分な量の超音波ゲルを置き、トランスデューサーを胸骨の外側左側、3番目と5番目の肋間腔の間に置き、2DモードでPLAXビューを取得します。必要に応じて深さを調整して、左心室流出路測定用の画像を記録し、画像を保存します。
手記: 左心室の最大幅は、僧帽弁の最大開口部で見えるはずです。バルブの筋肉が見えないようにする必要があります。トランスデューサーを患者の胸部に置く前に、ゲルが冷たくて不快に感じる可能性があること、およびある程度の圧力を感じることを警告します(特に左心室流出路(LVOT)の画像を記録するときは胸骨の周囲)。肋骨骨折のある患者では、患者にとって不快である可能性があるため、一部の場所は避けるべきであることに注意してください)。 - 2Dモードでは、深さを15〜20 cmに調整し、トランスデューサーを心臓の頂点、尾側から左乳輪の上に置きます。AP4CHのビューが得られ、4つのチャンバーすべてが明確に視覚化されています。画像を保存します。
- カーソルが三尖弁と右心室壁の境界にあるようにトラックボールを転がして、三尖弁環状平面収縮期エクスカーション (TAPSE) を取得します。 M-Mode ボタンを押して正しい画像を取得し、定義された洞波が見られたら保存します。画像を保存します。
- カーソルをトラックボールのある三尖弁の上に置きます。画像の幅を狭くして、RV S の品質に必要な 1 秒あたりのフレーム数を増やします。最初に TVI ボタンを押し、次に PW ボタンを押して、RV S'の正しい画像を取得して保存します。
- AP4CHビューから、トランスデューサーを上に傾ける(つまり、 平らにする)とAP5CHビューを取得し、大動脈基部を画面上に表示します。画像を保存します。
- カーソルを大動脈弁の真上に置き、 PW ボタンを押してLVOTパルス波ドップラーを取得します。LVOTの直径が測定されたのとまったく同じ場所にカーソルを置きます。画像を最高品質で保存します(シャープなドップラー波の境界、内側が中空で、逆行性または僧帽弁の流れと区別できます)。これらは、後で速度時間積分 (VTI) の計算に使用され、その後の CO の計算に使用されます。
手記: すべての測定で少なくとも3つの流れの波を得るように常に試みてください。不規則なリズムの場合は、少なくとも5つの波を保存する必要があります。 - 同じフェーズドアレイ心臓トランスデューサーを使用して肺超音波検査に進み、設定を周波数3.7 MHz、深さ15 cmに変更し、2回の心周期中にのみ画像を記録します。トランスデューサーを6つの異なる場所に配置し、トランスデューサーの光をBLUEプロトコル18に従って12時に置きます。後で画像を表示するときに混乱を避けるために、常に同じ順序で画像を取得してください。
- 両側の第2肋骨と第3肋骨の肋間腔にトランスデューサーを配置することにより、肺の優れた前鎖骨中央部のビューを取得します。各面の画像を保存します。
- トランスデューサーを2〜3本の肋骨の下に配置することにより、肺の眼前鎖骨中央部の図を取得します。各面の画像を保存します。
- トランスデューサーを患者の脇の下に置くことにより、肺の中軸図を取得します。各面の画像を保存します。
- 心臓と肺の画像診断が完了したら、患者の胸部から余分なゲルを拭き取ります。
- IVCと腎臓のCCUSを実行します。
- プローブボタンをクリックし、トラックボールを使用して、アクティブプローブをIVCおよび腎臓検査用の凸型/曲線アレイ(腹部)トランスデューサーに変更します。探触子の光は、方位のために使用することもできますが、どちらの測定でも12時の位置にある必要があります。
- 2Dモードを使用し、深さ10〜20 cm、周波数を2.5 / 5.0 MHzに設定して、トランスデューサーを剣状突起のすぐ下に置き、患者の右側に約2cm変位させます。IVCが表示されます。画像を保存します。
- カーソルをIVCの上壁のすぐ上、トラックボールを使用してルーメンの外側に置き、 Mモード ボタンを押します。画像を保存します。
- 腎超音波検査では、2Dモードから始めて、設定を深さ10〜15 cm、周波数2.2/4.4 MHzに調整します。トランスデューサーを胸郭の背側と尾側に配置します。選択した腎臓を画像の中心に取得し、保存します。
手記: トランスデューサーをできるだけ背側に配置して、肝臓組織と腸ループをろ過してください。腎臓の長さを確実に測定するには、腎臓の境界がはっきりと見える必要があり、中央洞複合体(腎臓のよりエコー源性のある中心)と皮質の間の距離は、画像全体で類似している必要があります。 - カラーボタンを押すと、腎臓のカラードップラー画像が得られ、腎臓血管系の流れがわかります。トラックボールを使用してドップラーの流れがはっきりと見える腎臓の中心にある皮質髄質接合部にある動脈にカーソルを置きます。
- カーソルの角度を調整し、 PW ボタンを押します。必要に応じて、 アクティブモードで 信号の振幅とコントラストを調整します。画像を保存します。
- また、後の測定に必要な十分な静脈信号(つまり、 y軸の負の半分に見える流れ)があるかどうかを判断します。そうでない場合は、手順3.4.5を繰り返し、静脈の流れが見える中央の皮質髄質接合部の静脈にカーソルを置きます。画像を保存します。
- すべてのイメージングが完了したら、すべてのケーブルを切断し、患者とトランスデューサーから余分なゲルを拭き取り、患者をドレスアップまたはカバーし、超音波承認の消毒ワイプでトランスデューサーを清掃します。
4. 臨床検査3・4
手記: 3回目と4回目の臨床検査は、患者がまだICUにいる場合(つまり、死亡や病棟への移動が行われていない場合 )は、入院後3日目と5日目に行われます。
- 健康診断
- 臨床検査1の手順に従って身体検査を実施します。
- 心臓と肺のCCUS
- ステップ3.3に従って、心臓と肺の超音波検査を実施します。LVOTは静的な測定であるため、臨床検査3および4に記録する必要がないため、一度だけ取得してください。
- IVCと腎臓のCCUS
- ステップ3.4に従って、IVCと腎臓の超音波検査を実施します。腎臓の長さは静的な測定値であるため、臨床検査3および4で記録する必要はありません。
5. 超音波検査の測定と分析
手記: 臨床検査中に保存された画像は、各検査後に目的の変数を測定するために使用されます。測定値はCRFに登録され、オンラインの臨床患者データ管理システムに転記されます。測定が実行され、表示される画像も、後で検証に使用される元の画像に加えて保存する必要があります。
- LVOT測定
- プローブ ボタンをクリックして心臓 トランスデューサーを選択し、測定を開始します。
- 手順3.3.5で保存した画像を使用して、バルブが完全に開いたときに画像を一時停止します。
- [ 測定 ]ボタンをクリックし、右側のメニューで [Cardiac-Dimension-LVOT ]オプションを選択して、測定を開始します。
- カーソルが表示されたら、拡張期末期に、大動脈弁の基部にある2つの点(内腔の両側に1つずつ、内縁から内縁まで)を選択します。画像を保存します。
注意: LVOT測定は、CO測定の前に実行して保存する必要があります。これにより、機械が自動的に決定できます。
- CO測定
- ステップ3.3.10で保存した画像を使用して、左心室出力をトレースします。水平スイープを100 cm / sに調整します。
- ECGと整列する明確な境界線を持つ3つの整形の中空の波を選択します。 「測定 」ボタンをクリックし、トラックボールを使用して 「心臓-大動脈-LVOTトレース 」オプションを選択します。
- ベースラインで開始および終了する波形ラインをトレースすると、超音波装置が自動的にCOを計算します。これを3つの波に対して繰り返して、この画像を保存します。
手記: 不規則なリズムの場合は、5つの波で得られた平均CO値を記録します。
- タプセ
- 手順3.3.7で保存したMモード画像を使用して、[ 測定 ]ボタンをクリックし、トラックボールを使用して右側のメニューで Cardiac-Dimension-TAPSE オプションを選択します。
- 最初に明確に定義された洞波の最低点にカーソルを置き、次に最高点にカーソルを置きます。2 つの違い (TAPSE) は、画面の左上隅に表示されます。これを3つの正弦波で行い、3つのTAPSE測定値の平均を取ります。画像を保存します。
- 右心室収縮期エクスカーション (RV S')
- ステップ3.3.8で保存した画像を使用して、[ キャリパー ]ボタンをクリックし、明確に定義された曲線の最高ピークにカーソルを置きます。これを3つの曲線で行い、平均を取ります。画像を保存します。
- Kerley Bラインアーティファクト評価
注: 正常な肺表面を表す水平のAラインは、Bラインの検出の参照に使用できます。これらは胸膜から発生し、Aラインに比べて高エコーです。- 画像のコントラストやゲインを調整します。Bラインは、保存された画像に常にすぐに表示されるとは限りません。
- 取得した6つの画像のそれぞれについて、Kerley Bラインの数を決定して登録します。Bラインの数はマシンに保存されないため、すぐにCRF(0〜5)に登録する必要があります。
- IVCの直径と折りたたみ性
- プローブ ボタンをクリックして腹部 トランスデューサーを選択し、測定を開始します。
- ステップ3.4.2で保存した2D画像を使用して、 キャリパー ボタンをクリックし、IVCの2つの壁の間の距離を、IVCが右アトリウムに入る位置から2cmで測定します。これがIVCの直径で、この画像を保存してください。
- ステップ3.4.3で保存したMモード画像を使用して、 キャリパー ボタンをクリックし、IVC呼気径と吸気径を測定します。この画像を保存します。
手記: IVCの呼気径と吸気径は、それぞれMモード画像で見られる最大径と最小径です。
- 腎臓の長さと血流
- ステップ3.4.4で保存した2D画像を使用して、 キャリパー ボタンをクリックし、腎皮質の尾側から頭蓋端まで伸びる最長の線を引きます。これは腎臓の長さ(cm)で、この所見をCRFに登録します。この画像を保存します。
- ステップ3.4.6で保存したドップラー画像を使用して、ベースラインの下に連続、単相、または二相として見られる静脈流線を分析します。結果を CRF に登録します。
- 手順3.4.6で保存した画像を使用して、[ 測定 ]ボタンをクリックし、トラックボールを使用して、右側のメニューで 腹部-腎臓-PS / ED/RI オプションを選択します。
- カーソルをピークと、y軸の正の半分にある脈動性流波の最低点に置きます。
手記: G6マシンは、連続的な脈動流波が保存されている場合、RRI =(ピーク収縮期速度-拡張期末速度)/ピーク収縮期速度の式を使用して、ドップラー腎抵抗指数(RRI)を自動的に計算できます。超音波装置からの測定値を画面に保存します。 - ステップ3.4.6または3.4.7で保存した画像を使用して、 キャリパー ボタンをクリックし、カーソルを最初にピーク最大流速の上に置きます、次に天下(つまり、 拡張末期)の最大流速の上に置きます19。測定後、画像を保存します。
手記: 静脈インピーダンス指数 (VII) は、VII = (ピーク収縮期速度 — 拡張期末速度) / ピーク収縮期速度20,21 から計算されます。単相流の場合、1つのピークしか見えず、拡張期と収縮期を区別できないため、VIIは登録されません。
6. 超音波画像のデータ登録、保存、検証
手記:図1に示すように、データ登録は各臨床検査の後に行われます。以下では、電子カルテから取得した測定、臨床検査、生化学情報(表2)から得られたデータを、被験者の匿名化されたオンラインファイルに入力する手順について説明します。
- オンラインで保護された患者管理システムにアクセスし、最近含まれた患者の書類を開きます。血液ガス分析値、一般血清変数、血清腎変数、および 24 時間尿分析を登録します。取得されるすべての変数のリストとその手順を 表 2 に示します。
- 心臓の CCUS 画像を検証します。
注: この検証は、EACVI ガイドライン22 に従って、Cardiovascular Imaging Core Laboratory の独立した専門家によって行われます。学生研究者によって得られた画像の品質が評価され、実行された測定が繰り返されて、寸法測定と速度プロファイルのトレースに必要な品質が確保されます。- 大動脈弁のすぐ下にあるECG信号に見られるように、拡張期末でLVOT測定を実行します。
- LVOTから取得したPW信号をAP5CHビューで追跡し、左心室一回拍出量と左心室COを取得します。
- IVCと腎臓のすべての画像と測定値を検証します。これは、独立した経験豊富な腹部放射線科医が行う必要があります。臨床検査中に目的の画像を取得するのに問題がある場合は、独立した腹部放射線科医にCCUSを依頼することができますが、その場合、それ以上の検証は行われません。
7. 患者様のフォローアップ
- インフォームドコンセントの登録
- 臨床検査中または臨床検査プロトコルの終了後に患者または家族の同意が得られても、患者がまだ入院している場合は、これを患者データ管理システムに登録し、手書きの同意書をアップロードしてください。
- 同意が拒否された場合は、同意が得られなかった理由とともに患者データ管理システムに登録し、研究コーディネーターに通知し、すべての患者データを削除します。
- 死亡率データ
- 入院中に死亡した患者については、電子患者記録と関連する死因から直接死亡率を登録します。
- 院内死亡のない患者については、90日ごとに更新されるオランダの市町村登録簿から死亡率データを取得します。
結果
これらの代表的な結果の目的は、プロトコールの実現可能性を示すことです。
患者
合計で、663人の患者が2018年5月14日から2018年8月15日の間にICUに入院しました。これらのうち、208人の患者が組み入れの対象となりました(除外の理由は 図4に示されています)。蘇生努力が進行中のため、CCUSを実施する可能性がなかったため、49人の患者が除外されました。7人の患者が参加を拒否し(インフォームドコンセントなし)、4人の患者では、例えば、人工呼吸器のための腹臥位や大きな創傷の真空補助閉鎖のためにCCUSが不可能であったため、138人の患者が分析のためのデータを持つことになった。
CCUS検証と画質
心臓画像の広範な検証が計画されています。腎超音波検査の検証が開始されました。これまでに、21人の患者(15%)の画像が検証されました。18人の患者(86%)で、画像は十分な品質で現れました。画像が不承認となったすべての理由をリストアップし、超音波検査を行った研究者にフィードバックするために返送しました。超音波検査を行った研究者の名前は、クラス内相関係数 (ICC) を使用して観察者間および観察者内の変動性を評価できるように記録されています。正確な統計手法は、SICS-I12で行われたように、統計分析計画で説明されます。
例:患者X、中年女性
患者Xは、意識障害と低血圧で発見された後に入院しました。得られたすべての測定値を 表1に示します。すべての変数は、データを失うことなく設定された必要な時間内に取得されており、このプロトコルの可能な実現可能性を示しています。入院後3時間以内に最初の臨床検査が行われました。この検査中、患者は鎮静剤を投与され、挿管され、昇圧剤治療が必要でした。2回目の臨床検査は10時間後に実施され、700mLの輸液後に安定したバイタルが示されました。昇圧剤は減少しました。CCUSおよび生化学的分析では、心臓、IVC、腎機能は正常であることが示されました(図5、 図6 、 図7)。2日後のT3では、昇圧剤は停止されましたが、累積正の体液バランスは6リットルに上昇し、COの増加、IVCの拡大、腎灌流の低下、および血清クレアチニンの増加に反映された機能の低下を伴いました。入院から5日後のT4では、体液バランスと血清クレアチニンがさらに上昇し、ステージ3のAKIを発症しました。患者は2日後、入院後7日で原因不明の多臓器不全により死亡した。
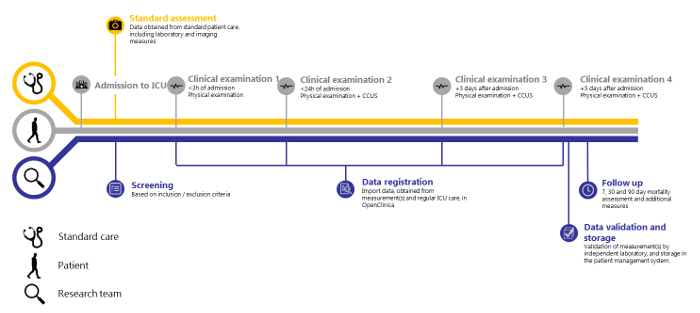
図1:SICS-II試験の概要。 集中治療室への患者入院からデータ登録の最終ステップまでのSICS-II研究のタイムライン。 この図の拡大版を表示するには、ここをクリックしてください。

図2:臨床検査用症例報告書(CRF)1. CRFは、ICUチームの学生または学生研究者が最初の臨床検査を実施する際に記入します。 この図の拡大版を表示するには、ここをクリックしてください。

図3:臨床検査2、3、4の症例報告書(CRF)。 CRFは、ICUチームの学生または学生研究者が第2回、第3回、第4回の臨床検査を実施する際に記入します。 この図の拡大版を表示するには、ここをクリックしてください。
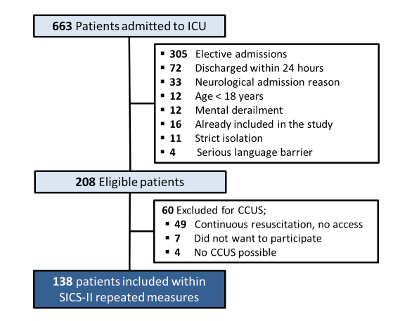
図4:SICS-II患者の包含および除外チャート。 2018年8月15日までのSICS-II研究における患者の包含と除外の基準を説明するフローチャート。 この図の拡大版を表示するには、ここをクリックしてください。
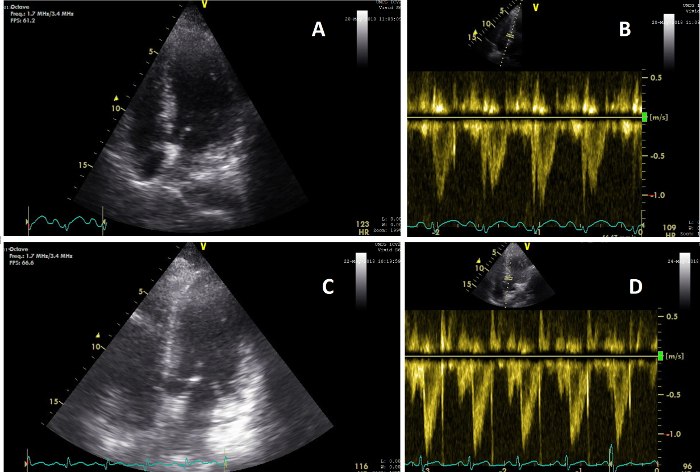
図5:心機能の変化を示す頂端図。 (A)臨床検査2中に実施されたCCUS中のAP4CHビュー上の心臓の画像(T = 2)。(B)T=2上の心臓VTIパルス波信号の画像で、COが5.6 L / minであることを示しています。(C)臨床検査中に実施されたCCUS中のAP5CHビュー上の心臓の画像3(T=3;(D)T=3上の心臓VTIパルス波信号の画像、8.3L/minのCOを示しています 。この図の拡大版を見るには、ここをクリックしてください。
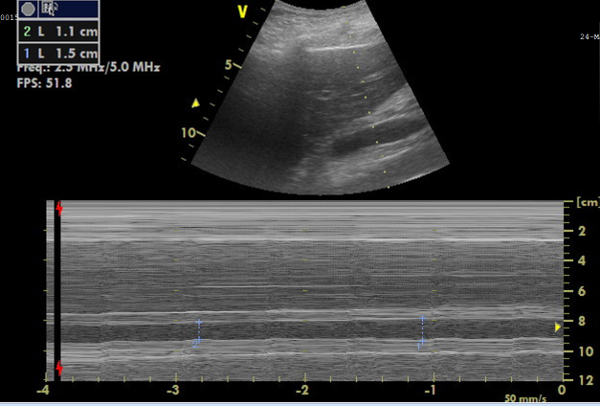
図6:直径測定のための下大静脈(IVC)のMモード画像。 上面にIVCをリアルタイムに表示した画像、下面にはIVCの直径変化を表すMモード画像があり、そこから折り畳み可能性を計算できます。 この図の拡大版を表示するには、ここをクリックしてください。
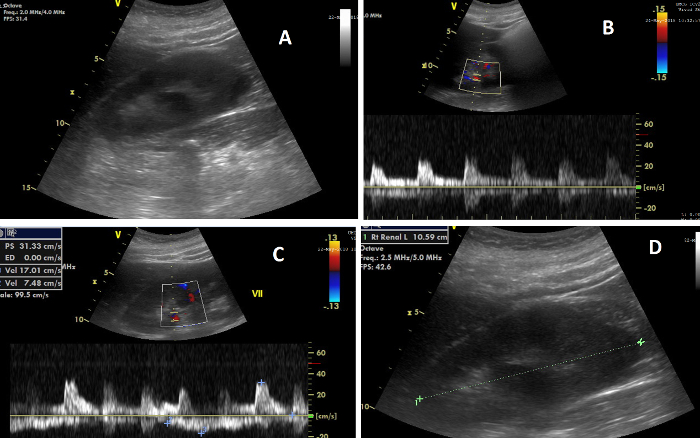
図7:腎超音波検査のさまざまな要素。 (A)CCUS中の右腎臓の画像。(B)上部に腎動脈内のドップラー流量を示す画像、および下に、腎抵抗指数が計算される流量波を示す画像。(C)上部に腎静脈内のドップラー流量を示す画像、下部に静脈インピーダンス指数が計算される流量波を示す画像。(D)腎臓の長さの測定を示す画像。 この図の拡大版を表示するには、ここをクリックしてください。
| 変数 | T1 1日目 00:38 | T2 1日目 10:53 | T3 3日目 10:14 | T4 5日目 10:20 |
| 心拍数(bpm) | 110 | 124 | 122 | 98 |
| 呼吸数(1分あたりの呼吸数) | 24 | 15 | 26 | 12 |
| 収縮期血圧 (mmhg) | 100 | 115 | 130 | 118 |
| 拡張期血圧(mmhg) | 61 | 69 | 66 | 65 |
| 平均動脈圧(mmhg) | 73 | 80 | 84 | 81 |
| 累積体液バランス(mL) | 0 | 704 | 7272 | 12338 |
| 人工呼吸 | PEEP 5、FiO2 40% | PEEP 5、FiO2 40% | PEEP 5、FiO2 30% | PEEP 5、FiO2 30% |
| CRT胸骨(秒) | 1.5 | 2 | 4 | 3 |
| 中心温度(◦ C) | 37.6 | 37.5 | 38.0 | 37.4 |
| 前1時間の尿量(mL) | 117 | 60 | 0 | 10 |
| 投与された変力剤 | ノルアドレナリン 0.1 mg / ml 3.0ミリリットル/時 | ノルアドレナリン 0.1 mg / ml 1.0ミリリットル/時 | 何一つ | 何一つ |
| 鎮静剤を投与しました。 | プロポフォール 20 mg / mlの 5.0ミリリットル/時 | 何一つ | 何一つ | 何一つ |
| APACHE IVスコア | 92 | 88 | 87 | 90 |
| SOFAスコア | 8 | 8 | 5 | 8 |
| LVOT(cm) | N.A. | 2.4 | 2.4 | 2.4 |
| 心拍出量(L / min) | N.A. | 5.6 | 8.34 | 9.89 |
| タプセ (mm) | N.A. | 25 | 26 | 21 |
| RV S' (cm/s) | N.A. | 14 | 15 | 12 |
| IVC吸気径(cm) | N.A. | 1.14 | 1.24 | 1.10 |
| IVC呼気径(cm) | N.A. | 1.27 | 1.38 | 1.50 |
| カーリーBライン(合計) | N.A. | 6 | 2 | 4 |
| 腎臓の長さ(cm) | N.A. | 10.59 | N.A. | N.A. |
| 腎内静脈流パターン | N.A. | 蟬 | 蟬 | 蟬 |
| ドップラー腎RI | N.A. | 0.61 | 0.75 | 0.70 |
| VII | N.A. | 0.33 | 0.56 | 0.68 |
表1:無作為のSICS-II患者。 患者X、意識障害でICUに入院した中年女性。略語:bpm =ビート/分、CRT =毛細血管補充時間、LVOT =左心室流出路、TAPSE =三尖弁環状平面収縮期エクスカーション、RV S' =右心室収縮期エクスカーション、IVC =下大静脈、RRI =腎抵抗指数、VII =静脈インピーダンス指数、NA =該当なし。
| 変数 | 単位 | 源 | 取得場所 |
| 乳酸 | mmol/L | 動脈血ガス分析 | 標準治療から、各臨床検査に限りなく近づき、最大12時間の差 |
| 塩化 | mmol/L | 動脈血ガス分析 | 標準治療から、各臨床検査に限りなく近づき、最大12時間の差 |
| pHの | 動脈血ガス分析 | 標準治療から、各臨床検査にも限りなく近づき、最大12ホ差 | |
| PCO2 (英語) | kPaの | 動脈血ガス分析 | 標準治療から、各臨床検査に限りなく近づき、最大12時間の差 |
| PaO2 | kPaの | 動脈血ガス分析 | 標準治療から、各臨床検査に限りなく近づき、最大12時間の差 |
| HCOの3- | mmol/L | 動脈血ガス分析 | 標準治療から、各臨床検査に限りなく近づき、最大12時間の差 |
| ヘモグロビン | mmol/L | 動脈血ガス分析 | 標準治療から、各臨床検査に限りなく近づき、最大12時間の差 |
| 白血球 | 10 x 10-9 / L | 血清分析 | 標準治療から、各臨床検査に限りなく近づき、最大12時間の差 |
| 血小板 | 10 x 10-9 / L | 血清分析 | 標準治療から、各臨床検査に限りなく近づき、最大12時間の差 |
| HSトロポニン | ng/L | 血清分析 | 標準治療から、各臨床検査に限りなく近づき、最大12時間の差 |
| アサット | U/L | 血清分析 | 標準治療から、各臨床検査に限りなく近づき、最大12時間の差 |
| アラット | U/L | 血清分析 | 標準治療から、各臨床検査に限りなく近づき、最大12時間の差 |
| 総ビリルビン | uoml/L | 血清分析 | 標準治療から、各臨床検査に限りなく近づき、最大12時間の差 |
| クレアチニン | ウモール/L | 血清分析 | ICU入室開始からのすべての測定値 |
| 尿量 | ミリリットル | 24時間の尿収集 | ICU入室開始からのすべての測定値 |
| クレアチニン | MMOL/24時間 | 尿分析 | ICU入室開始からのすべての測定値 |
表2:得られた生化学的変数のリスト。 研究中に収集されたすべての患者の生化学的変数がここにリストされています。
ディスカッション
すべての検査は、プロトコルに従って実施する必要があります。身体検査は、事前に指定された定義23に従って実施された場合にのみ価値があります。実験室の値は、すべての値を取得するためにプロトコルに従って収集する必要があります。明確で解釈可能なCCUS画像は、ステップ3.3で説明したように、この研究の研究課題に答えるための鍵となります。低品質の画像が得られると、ステップ 5 で説明した測定と解析を実行できなくなり、繰り返し測定の目的が期限切れになります。低品質の画像を取得するリスクを最小限に抑えるために、3つの重要な対策が講じられています。まず、私たちの研究でCCUSを実施する学生研究者は、経験豊富な心臓専門医集中治療医によって訓練されています。文献によると、CCUS24の基本的な能力を習得するには、短期のトレーニングプログラムが適しています。次に、学生研究者は、最初の20回の試験で上級の学生研究者によって監督されるため、実践的なフィードバックを受け取ることができます。最後に、取得したすべての心臓および腎臓の画像は、データの信頼性を確保するために、Cardiac Imaging Core Laboratory の独立した専門家と経験豊富な腹部放射線科医によってそれぞれ再評価および検証されます。
画質を確保するために、研究者は他の側面にも注意を払う必要があります。最適な画質を確保するためには、超音波ゲルを再塗布したり、プローブの位置を変えたりして、患者の皮膚に接触しやすくすることが必要になる場合があります。また、最適な画像を取得するために十分な時間をかけることも重要であり、疑問がある場合は、臨床検査が完了する前に、主任研究者、つまり指導する循環器専門医集中治療医またはコアラボテクニストに相談する必要があります。すべての超音波画像の継続的な評価と検証は、図1に示されているプロトコル化された手順を実施することで保証されます。さらに、学生研究者や専門家が頻繁にフィードバックを交換するため、プロトコルの変更を迅速に実装して、画像や測定の品質をさらに向上させることが容易になります。この頻繁な検証により、系統的エラーを簡単に検出できるため、将来の学生研究者向けのCCUSトレーニングをそれに応じて適応させることができます。さらに、すべてのチームメンバーが参加できる月例会議では、プロトコルの徹底的な評価と(必要に応じて)修正が可能です。
患者のスクリーニングとインクルージョンのための24時間の可用性は、この研究を成功させるためのもう一つの重要な要素です。これは、学生・研究者の専任チーム、サポートを提供する大規模な学生チーム、そしてICUの介護者との良好な調整によってのみ達成されます。この調整は、介護者と研究者の間で、標準治療との協力を最適化するための可能な改善について定期的に低利害関係で連絡を取ることによって行われます。
このプロトコルの制限は、CCUSを正常に実施できるかどうかは、プローブが配置される事前に指定された位置へのアクセス性に依存することです。SICS-Iでは、患者がドレーン、ガーゼ、または創傷被覆材を必要とする場合、理論的に最適な心エコー検査ウィンドウ1を阻害する場合、心臓CCUSを実行できないことがすでに示されました。さらに、IVC測定に必要な経胸壁心エコー検査 を介して 適切な肋骨下窓を取得する可能性は、一般的なICU集団25では潜在的に制限されていることが以前に示されています。このプロトコルで異なる時点で異なる検査を実施するために必要な24時間年中無休の可用性も、一部のセンターがそうする能力を欠いている可能性があるため、潜在的な制限です。UMCGのような大規模な学術病院でも、これを確保することが研究開始の遅れにつながっています。超音波検査測定に固有の別の制限は、測定値の観察者間の変動性です。患者の包含が24時間週7日保証されるためには、1人の研究者がすべての包含された患者のすべての臨床検査を実施することは不可能です。この研究は、同じ研究者が 1 人の同じ患者ですべての超音波測定を実施して、個人レベルでのばらつきを最小限に抑えることを目的としていますが、コホート全体では、観察者間のばらつきが依然として問題です。
複数の臓器の超音波イメージングは、臓器の灌流と機能を視覚化するための迅速、安全、かつ効果的な構造になります。これは、すべての医療専門家が使用できる便利なツールであり、シンプルで標準化されたプロトコルに基づく少数の測定が一般的に信頼性の高い測定を提供するはずです。
さらに、超音波検査、特に心エコー検査の使用を評価するほとんどの観察研究は、本質的に遡及的であるか、少数の患者のみを対象としている。26 このプロトコルは、重篤な患者の選択されていないコホートの構造的な24/7スクリーニングを可能にし、そのうちの関心のある亜集団を定義することができるため、複数の研究課題を同時に調査することができます。
さらに、救命救急における臨床変数は非常に動的であり、相互に影響し合うことが知られているにもかかわらず、ほとんどの研究では、特定の臓器の単一超音波測定の相加的価値のみが調査されています27,28。これは、反復測定、全身超音波検査、静脈うっ血に焦点を当てた最初のプロトコルです。SICS-IIは、ICU入室時の患者の血行動態をより正確に反映することを期待しています。
SICSで現在使用されている構造は、多数の設定に適用でき、他の要素の追加も現在検討中です。その強みは、基礎研究ラインと、新しい変数をCRFに簡単に追加して新しい研究課題を調査できる適応ラインの組み合わせにあります。この適応性の一例は、変形画像による広範な心室壁評価、すなわち、 短期間のひずみを、特定の患者のサブセットにおける通常のプロトコルに追加することです。
さらに、患者のインクルージョンは現在、ICUでのみ行われており、患者のケアの軌跡の一部が失われています。ICUの患者さんは、まず救急科(ED)に入院し、ICU退院後も通常の病棟に滞在することが多いです。したがって、SICSは、EDの到着時に患者を含め、最初の入院以降の介入と血行動態機能を登録することにより、早期の段階の患者を含めることを目指しています。さらに、ICU退院後に通常の病棟にCCUSを実施する計画も進行中であり、事前に定義された研究時間ごとにすべての患者を測定できます。もう一つの重要な側面は、プロトコルが他のセンターに拡張可能であることです:そのシンプルさは、自分自身でインクルージョンを開始することができるセンターによる容易な適応を可能にします。
最後に、構造化されたCCUSプロトコルの開発と成功裏の実装は、臨床的な影響ももたらす可能性があります。研究目的のみに使用されていますが、提案された短いトレーニング期間の後、医師による臨床CCUSに実装される可能性があります。次に、(経験の浅い)医師にCCUSトレーニングを促進することで、追加の診断テストが減少するかどうかを評価することは興味深いでしょう。
開示事項
著者は何も開示していません。
謝辞
SICS-Iに関与し、現在のプロトコルに関するブレインストーミングセッションに参加したSICS-Studyグループのすべてのメンバーに感謝します。また、クリティカルケア部門のリサーチビューローとそのコーディネーターの支援に感謝します。W.ディーペリンク博士とM.オンラスト。また、これまでSICS-IIに患者を構造的に含めてくださったICU学生チームと学生研究者の方々に感謝します。JAデブルーイン、BEキューニング、博士K.セルズ。
資料
| Name | Company | Catalog Number | Comments |
| Ultrasound machine | GE Healthcare | 0144VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound machine | GE Healthcare | 3507VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound machine | GE Healthcare | 0630VS6 | Ultrasound machine, GE Vivid S6 |
| Ultrasound gel | Parker | 01-08 | Aquasonic 100 ultrasound transmission gel |
| Temperature probe | DeRoyal | 81-010400EU | Skin Temperature Sensor |
参考文献
- Hiemstra, B., et al. Clinical examination, critical care ultrasonography and outcomes in the critically ill: cohort profile of the Simple Intensive Care Studies-I. BMJ open. 7 (9), 017170(2017).
- Lee, J., et al. Association between fluid balance and survival in critically ill patients. Journal of Internal Medicine. 277 (4), 468-477 (2015).
- Perner, A., et al. Fluid management in acute kidney injury. Intensive Care Medicine. 43 (6), 807-815 (2017).
- Balakumar, V., et al. Both Positive and Negative Fluid Balance May Be Associated With Reduced Long-Term Survival in the Critically Ill. Critical care medicine. 45 (8), 749-757 (2017).
- Hjortrup, P. B., et al. Restricting volumes of resuscitation fluid in adults with septic shock after initial management: the CLASSIC randomised, parallel-group, multicentre feasibility trial. Intensive Care Medicine. 42 (11), 1695-1705 (2016).
- Prowle, J. R., Kirwan, C. J., Bellomo, R. Fluid management for the prevention and attenuation of acute kidney injury. Nature reviews. Nephrology. 10 (1), 37-47 (2014).
- Gambardella, I., et al. Congestive kidney failure in cardiac surgery: the relationship between central venous pressure and acute kidney injury. Interactive CardioVascular and Thoracic Surgery. 23 (5), 800-805 (2016).
- Chen, K. P., et al. Peripheral Edema, Central Venous Pressure, and Risk of AKI in Critical Illness. Clinical journal of the American Society of Nephrology : CJASN. 11 (4), 602-608 (2016).
- Song, J., et al. Value of the combination of renal resistance index and central venous pressure in the early prediction of sepsis-induced acute kidney injury. Journal of critical care. 45, 204-208 (2018).
- Zhang, L., Chen, Z., Diao, Y., Yang, Y., Fu, P. Associations of fluid overload with mortality and kidney recovery in patients with acute kidney injury: A systematic review and meta-analysis. Journal of Critical Care. 30 (4), (2015).
- Simple Intensive Care Studies II - Full Text View. ClinicalTrials.gov. , Available from: https://clinicaltrials.gov/ct2/show/NCT03577405? term=simple+intensive+care+studies (2018).
- Wetterslev, J. Statistical analysis plan Simple Intensive Care Studies-I DETAILED STATISTICAL ANALYSIS PLAN (SAP) 1. Administrative information 1.1. Title, registration, versions and revisions. ClinicalTrials.gov. , Available from: https://clinicaltrials.gov/ProvidedDocs/24/NCT02912624/SAP_000.pdf (2018).
- van der Horst, I. C. C. Simple Observational Critical Care Studies - Full Text View - ClinicalTrials.gov. ClinicalTrials.gov. , Available from: https://clinicaltrials.gov/ct2/show/NCT03553069 (2018).
- Ait-Oufella, H., et al. Alteration of skin perfusion in mottling area during septic shock. Annals of Intensive Care. 3 (1), 31(2013).
- Teasdale, G., Jennett, B. Assessment of Coma and Impaired Consciousness: A Practical Scale. The Lancet. 304 (7872), 81-84 (1974).
- Detsky, M. E., et al. Discriminative Accuracy of Physician and Nurse Predictions for Survival and Functional Outcomes 6 Months After an ICU Admission. JAMA. 317 (21), 2187(2017).
- Lipson, A. R., Miano, S. J., Daly, B. J., Douglas, S. L. The Accuracy of Nurses' Predictions for Clinical Outcomes in the Chronically Critically Ill. Research & reviews. Journal of nursing and health sciences. 3 (2), 35-38 (2017).
- Lichtenstein, D. A. BLUE-protocol and FALLS-protocol: two applications of lung ultrasound in the critically ill. Chest. 147 (6), 1659-1670 (2015).
- Tang, W. H. W., Kitai, T. Intrarenal Venous Flow: A Window Into the Congestive Kidney Failure Phenotype of Heart Failure. JACC: Heart Failure. 4 (8), 683-686 (2016).
- Jeong, S. H., Jung, D. C., Kim, S. H., Kim, S. H. Renal venous doppler ultrasonography in normal subjects and patients with diabetic nephropathy: Value of venous impedance index measurements. Journal of Clinical Ultrasound. 39 (9), 512-518 (2011).
- Iida, N., et al. Clinical Implications of Intrarenal Hemodynamic Evaluation by Doppler Ultrasonography in Heart Failure. JACC: Heart Failure. 4 (8), 674-682 (2016).
- Lang, R. M., et al. Recommendations for Cardiac Chamber Quantification by Echocardiography in Adults: An Update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. European Heart Journal - Cardiovascular Imaging. 16 (3), 233-271 (2015).
- Hiemstra, B., Eck, R. J., Keus, F., van der Horst, I. C. C. Clinical examination for diagnosing circulatory shock. Current opinion in critical care. 23 (4), 293-301 (2017).
- Vignon, P., et al. Basic critical care echocardiography: validation of a curriculum dedicated to noncardiologist residents. Critical care medicine. 39 (4), 636-642 (2011).
- Jensen, M. B., Sloth, E., Larsen, K. M., Schmidt, M. B. Transthoracic echocardiography for cardiopulmonary monitoring in intensive care. European journal of anaesthesiology. 21 (9), 700-707 (2004).
- Koster, G., van der Horst, I. C. C. Critical care ultrasonography in circulatory shock. Current opinion in critical care. 23 (4), 326-333 (2017).
- Haitsma Mulier, J. L. G., et al. Renal resistive index as an early predictor and discriminator of acute kidney injury in critically ill patients; A prospective observational cohort study. PloS one. 13 (6), 0197967(2018).
- Micek, S. T., et al. Fluid balance and cardiac function in septic shock as predictors of hospital mortality. Critical care. 17 (5), London, England. 246(2013).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved