Method Article
冠状动脉疾病无创即时检测的信号采集、评分解释和经济性
摘要
介绍了获取冠状动脉疾病 (CAD) 测试生理信号的方法。提出了一种方法来解释有关测试阳性和阴性的 CAD 分数,包括每个分数的粒度。在当前护理标准的背景下讨论了该测试的经济性。
摘要
冠状动脉疾病 (CAD) (POC-CAD) 的即时无创检测之前已经开发和验证。该测试需要同时采集正交电压梯度 (OVG) 和光电容积脉搏波信号,这是本文描述的主要方法。获得生物电信号 OVG 需要在患者胸部准备好的皮肤上放置电极(布置类似于 Frank 导线配置,包括六个双极电极和一个参考电极)和手指上的血流动力学传感器(使用标准传输方式)。信号被上传到基于云的系统,从信号中提取工程特征并提供给机器学习算法以产生 CAD 分数。然后,医生必须在患者 CAD 的验前概率的背景下解释 CAD 评分的值,从而得出 CAD 的验后概率。这种解释可以在测试阳性和测试阴性的层面上进行,也可以在更精细的粒度层面上进行;此处根据似然比提出了每种方法。使用验后概率,医生必须确定治疗患者的适当下一步;使用几个场景来说明此过程。只有在经济上可行的情况下,测试采用才可行;讨论了将测试集成到 CAD 诊断流程中以及由此为医疗保健系统节省的成本。经济模型表明,可以通过防止延误治疗来节省医疗保健系统的成本,如果不加以解决,将导致疾病进展,需要更先进(和昂贵)的护理。
引言
缺血性心脏病 (IHD) 目前是全球主要死亡原因1。冠状动脉疾病 (CAD) 是 IHD 的解剖学前体,其特征是冠状动脉内存在显著病变。在解剖学上,可以通过左主动脉至少 70% 或 50% 的闭塞来定义意义2。也可以通过测量病变对血流的影响,根据病变的功能影响来定义显著性。具体来说,血流储备分数 (FFR) 和瞬时血流储备 (iFR) 评估病变引起的血流变化,在 FFR < 0.80 或 iFR < 0.89 时,病变被定义为显着的2。确认存在严重 CAD 的金标准是通过左心导管插入术 (LHC) 进行有创冠状动脉造影 (ICA)。严重的 CAD 需要通过放置支架或冠状动脉旁路移植术进行血运重建,从而减轻心肌缺血和相应的心绞痛症状并稳定斑块(在支架置入术的情况下)。
目前的 CAD 无创检测通常需要辐射暴露、应激和造影剂注射(对肾脏有影响)1。最常用的诊断测试是心肌灌注成像 (MPI),也称为单光子发射计算机断层扫描 (SPECT) 和冠状动脉计算机断层扫描血管造影 (CCTA)。SPECT 涉及注射放射性同位素以跟踪休息和压力(运动或药物)期间的灌注。CCTA 使用多张 X 线对冠状动脉进行成像。正电子发射断层扫描 (PET) 和心脏磁共振成像 (CMR) 有时也用于 CAD 检测1。所有这些方式都需要对设备进行大量资本投资,需要训练有素的人员进行测试,在某些情况下,还需要医用同位素的可用性。由于这些要求,这些方式通常不广泛可用,尤其是在农村地区,这会导致患者护理的延误并增加相关风险。
因此,目标是设计一种无创的 CAD 即时检测 (POC-CAD):CorVista 系统3。该系统是 FDA 批准的功能显著性 CAD 测试,性能与 CCTA4 相当。该测试可以在没有患者压力的情况下使用,也不需要对设备或专业人员进行资本投资。它非常适合在通常无法使用当前成像技术的农村和资源受限的环境中使用。
POC-CAD 的开发3 和验证4 之前已经发布过。简而言之,POC-CAD 首先使用 Capture 设备同时采集正交电压梯度和光电容积脉记图信号,如协议步骤 1 中所述。正交电压梯度是使用类似于 Frank 导联配置5 的导联放置获得的生物电信号,包括六个双极电极和一个连接到躯干的参比电极。光电容积脉搏波图是使用标准传输方式获得的,其中红光和红外光通过指尖传输并撞击传感器6。获取信号后,它会自动上传到基于云的系统,从信号中提取工程特征并提供给机器学习算法,以产生 CAD 分数,该分数显示在 Web 门户中。在协议步骤 2 和 3 中,描述了解释测试返回的 CAD 分数的方法。具体来说,已发布的数据或与医生相关的其他来源可用于在患者接受测试之前估计 CAD 的可能性。似然比可以根据检验性能计算,并用于使用二进制测试结果(步骤 2)或更精细的 CAD 分数值(步骤 3)将 CAD 的概率从验前更新到验后。最后,讨论了 POC-CAD 的经济性建模与当前护理标准相比。
研究方案
该研究得到了西方机构审查委员会的批准,并根据赫尔辛基宣言进行。获得所有受试者的书面知情同意书以进行参与。简而言之,要被纳入,受试者必须年满 18 岁且有心血管症状但没有已知的冠状动脉疾病并计划接受 ICA 或 CCTA。排除标准包括既往心肌梗死病史、既往冠状动脉旁路移植术和既往心脏瓣膜置换术等。完整的研究纳入和排除标准可以在 clinicaltrials.gov 的国家临床试验 (NCT) 编号 NCT03864081下找到。所使用的设备和软件列在 材料表中。
1. 信号采集
- 通过剃掉电极部位的任何毛发来准备皮肤。用肥皂和水清洁,并在需要时使用干净干燥的纱布或不含酒精的湿巾,确保皮肤上没有残留物。
- 将引线连接到电极并按照 表 1 放置它们。
注意:电极质量可能会影响信号质量;建议使用 Diagnostic Quality 或 High-Performance 电极。 - 将血流动力学(光电容积脉搏波,PPG)传感器放在受试者的手指上,确保手指尽可能远离传感器,传感器电缆位于手的顶部。
- 除非伤口或其他临床相关原因阻止其使用,否则请使用食指。建议患者在放置传感器后不要移动传感器。
- 将患者平躺在舒适的休息位置。确保 PPG 传感器电缆和电极电缆不重叠。
- 如果需要,使用缓冲垫(例如,卷起的毯子或毛巾以及枕头),以防止患者直接压迫背部的蓝色电极。
- 为了限制信号噪声并最大限度地提高信号质量,请尽可能关闭所有电子设备(显示器、电视、手机等)或将它们移出房间。关掉房间的灯。
- 输入患者信息并确认正确性:患者的名字、患者的姓氏、出生时的性别、身高(英寸)、体重(磅)、出生日期和病历号(全部必填,可以按任何顺序输入)。
- 确保患者感到舒适,并提醒他们保持安静(例如,采集期间不要说话)。
- 将设备放在平坦的表面上,并确认在应用程序中的位置。按 Start 开始信号采集。
- 监控设备中是否有任何错误消息,如果出现这些消息,请按照屏幕上的说明解决它们。
- 信号采集完成后,需要 3 分 35 秒,设备会自动将数据传输到云端进行信号质量评估。让患者保持与设备的连接,直到确认通过信号质量。
- 从患者身上拆下电极并取下 PPG 传感器。
- 访问门户以查看测试结果(将在信号上传到云端后约 10 分钟可用)。
表 1:潜在客户位置。 描述应放置七个电极中每个电极的解剖位置。 请点击此处下载此表格。
2. 解释给定检测阳性 与 的测试结果。检测阴性
- 确定患者患病的验前概率(例如,使用欧洲心脏病学会 (ESC) 指南7)。
- 通过将 CAD 分数与 0 进行比较来确定患者的测试是阳性还是阴性:如果大于或等于零,则患者的结果是阳性,如果小于零,则结果为阴性。
- 从报告中读取 CAD 评分值,并将其与报告底部显示的验证队列中阴性和阳性患者的分布进行比较。
- 计算灵敏度和特异性8,然后使用方程 1 和方程 29 计算似然比 (LR)。
注意:显示了一个工作示例,假设测试灵敏度为 88%(使用 ICA 阳性受试者计算,这是唯一的疾病受试者组)和特异性为 51%(使用 CCTA 阴性的受试者以 94% 的权重和 ICA 阴性的受试者以 6% 的权重计算,以代表总体人群通过 PROMISE 研究10)。
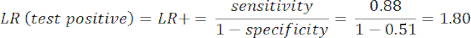 (方程 1)
(方程 1)
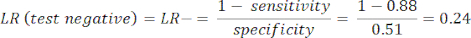 (方程 2)
(方程 2) - 根据以下公式 3-511 计算患者的验后概率,其中 LR+ 用于阳性检测,LR- 用于阴性检测:
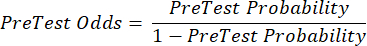 (方程 3)
(方程 3)
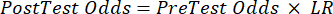 (方程 4)
(方程 4)
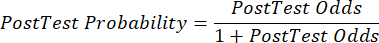 (方程 5)
(方程 5) - 根据 CAD 的更新概率,根据测试结果,确定适当的患者护理下一步(例如,使用表 2 中所示的 ESC 指南7 建议)。
表 2:按 CAD 概率划分的 ESC 指南。 对于 CAD 的 4 个概率水平,欧洲心脏病学会指南用于对该概率的适当解释,包括下一次测试(如有必要)。 请点击此处下载此表格。
3. 更精细地解释给出的测试结果
- 通过考虑在用于验证测试的总体中观察到的 CAD 分数范围,特别是将测试阳性和测试阴性范围内的三分位数(三个箱中的受试者数量相等)划分为三分位数,如 表 3 所示。
注意:为简化计算,该分析排除了导管插入术阴性受试者的 6% 贡献,纳入其不会显着改变结果。 - 在检测阴性范围内的每个三分位数中,计算真阴性 (TN) 的数量,即真正没有患病的受试者,以及假阴性 (FN) 的数量,即真正患有疾病的受试者。
- 应用以下公式 6-811 来确定每个测试阴性三分位数的 LR-(来自负三分位数的 LR+ 无关紧要)。
注意:这些方程式假设 tertile 的性能概况代表计算性能统计数据的完整测试阴性范围(需要校正因子 3,对应于 tertiles 的数量,以达到相对于测试阳性的原始测试阴性频率)。
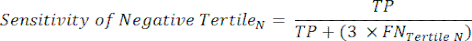 (方程 6)
(方程 6)
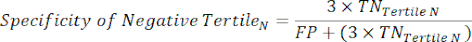 (方程 7)
(方程 7)
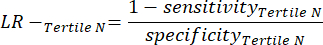 (方程 8)
(方程 8)
- 应用以下公式 6-811 来确定每个测试阴性三分位数的 LR-(来自负三分位数的 LR+ 无关紧要)。
- 在检测阳性范围内的每个三分位数中,计算真阳性 (TP) 的数量,即真正患有疾病的受试者,以及假阳性 (FP) 的数量,即真正没有疾病的受试者。
- 应用方程 9-11 来确定每个检测呈阳性的三分位数的 LR+(来自阳性三分位数的 LR- 无关紧要)11。
注意:这些方程式假设 tertile 的性能概况代表用于计算性能统计数据的完整测试阳性范围(需要 3 的校正因子,对应于 tertiles 的数量,以达到相对于测试负性的原始测试阳性频率)。
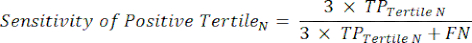 (方程 9)
(方程 9)
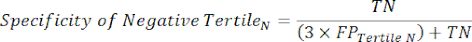 (方程 10)
(方程 10)
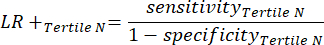 (方程 11)
(方程 11)
- 应用方程 9-11 来确定每个检测呈阳性的三分位数的 LR+(来自阳性三分位数的 LR- 无关紧要)11。
- 确定患者的 CAD 评分位于哪三分之一,并给出 表 3 中的 LRs,根据步骤 2 中所示的程序计算验后概率。
注:正如预期的那样,LR- 值会随着负 CAD 分数的增加而降低,而 LR+ 值会随着 CAD 分数的正数增加而增加,这意味着更负的 CAD 分数会更有效地降低验前概率,而更正的 CAD 分数会更有效地增加验前概率。 - 作为执行步骤 2.4-3.4 中列出的计算的替代方法,使用 表 4 使用患者的 CAD 评分7 将验前概率转换为验后概率。
表 3:似然比。 对于 test-positive 和 test-negative 中的三个分数范围,分别是相应的正似然比和负似然比。 请点击此处下载此表格。
表 4:前测到测后概率映射。 对于 10 个水平的验前概率,相应的验后概率在三个负三分位数中的每一个和每个正三分位数中给出 CAD 分数。绿色对应于 <15% 的疾病概率(ESC 指南指出可以排除 CAD);黄色对应于 15%-65% 的疾病概率(ESC 指南指出,基于影像学的无创检测是 首选);橙色对应于 66%-85% 的疾病概率(ESC 指南指出 应进行基于影像学的无创检测);红色对应于 >85% 的疾病概率(ESC 指南指出可以判定 CAD)。有关进一步的指导信息,请参阅 表 2 。请注意,CAD 分数为 0 被视为检测阳性。 请点击此处下载此表格。
结果
图 1 中可以看到一个示例信号,图 2 中报告了一个示例信号,就像使用该测试的医生一样。以下是几个患者案例,以证明该方法在解释 CAD 评分的重要性中的应用。
案例 1
一名 67 岁男性主诉静息时胸痛、手臂放射性疼痛以及出汗和恶心的症状。根据 ESC 指南7,他的年龄、性别和症状与 84% 的初始疾病概率一致。ESC 指南建议,此类患者需要无创检查以诊断 CAD,从而保证转诊至心导管插入术和任何必要的干预(表2)。进行 POC-CAD,返回 CAD 评分为 0.32,这是一个检测阳性结果,属于阳性 CAD 评分的最高三分位数,LR+ 为 2.888(表 3)。因此,患者的验后概率为 94%,根据 ESC 指南(表 2),可以安全地假设患者患有 CAD,有创心导管插入术是适当的行动方案。
案例 2
一名 39 岁女性在休息时出现胸痛,放射至左侧和右侧。根据 ESC 指南7,她的年龄、性别和症状与 28% 的初始疾病概率一致,并且指南建议非侵入性测试将是更可取的下一步,以更好地了解 CAD 的可能性。然而,指南还指出,对于年轻患者(例如这位 39 岁的女性),医生应注意辐射暴露,这对于进行 SPECT 等需要注射放射性同位素的测试是必要的。这种测试的另一种选择是 CCTA,但这需要许多 X 射线。因此,POC-CAD 是一个合乎逻辑的选择,因为它不需要辐射。进行了测试,返回值 -0.12,在负范围的第一个三分位数的范围内,LR- 为 0.129(表 3)。由此产生的验后概率为 4%,降至根据 ESC 指南可以安全排除 CAD 的水平,无需对 CAD 进行进一步测试。
案例 3
一名 74 岁女性因非心绞痛性胸痛和呼吸困难前来就诊。根据 ESC 指南7,她的年龄、性别和症状与 24% 的初始疾病概率一致,并且指南建议非侵入性测试是更可取的下一步,以更好地了解 CAD 的可能性。患者不愿从她接受治疗的农村诊所前往所有检测方式(PET、SPECT、CCTA、CMR)可用的大城市中心,因此医生提供了 POC-CAD。CAD 评分为 0.07,落入正范围的第一分位数,LR+ 为 1.446,导致验后概率为 33%。根据阳性结果和疾病可能性的增加,患者同意前往该市进行 PET 扫描。PET 也提示疾病,LR+ 为 6.0412,并增加了 PET 后 33% 至 75%。
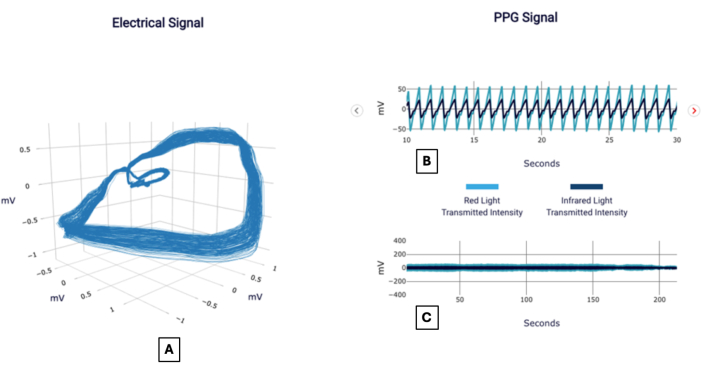
图 1:示例信号。 示例 POC-CAD 报告显示了正交电压梯度的可视化,也称为电信号 (A) 和集中在 20 秒间隔 (B) 和完整持续时间 (C) 上的光电容积脉搏波信号。 请单击此处查看此图的较大版本。
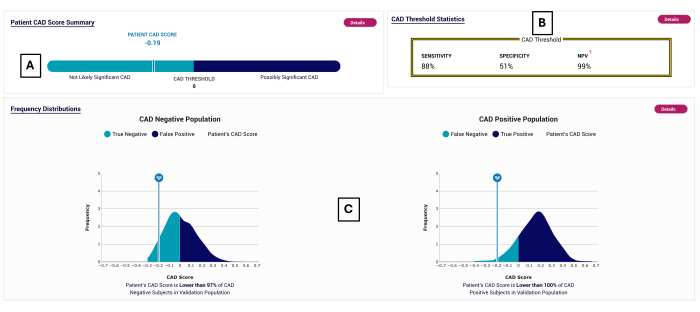
图 2:CAD 报告示例。 示例 POC-CAD 报告,显示 CAD 分数为 -0.19 (A),属于检测阴性范围 (<0)。测试性能如 (B) 所示。显示了在 (C) 中验证了 POC-CAD 的受试者的 CAD 分数分布。 请单击此处查看此图的较大版本。
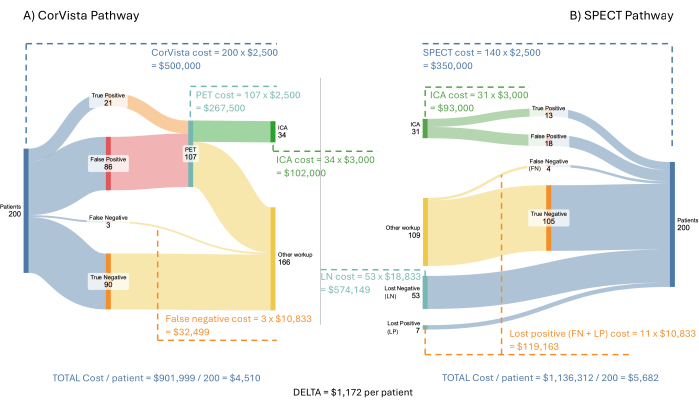
图 3:成本经济模型流程。 假设 200 名患者的传入人群通过 POC-CAD>PET 通路 (A) 和 SPECT 通路 (B) 运行。显示了每个途径的每个分支的医疗保健系统的成本,以及实施 POC-CAD>PET 途径时每位患者的平均节省。 请单击此处查看此图的较大版本。
讨论
本节的主要重点是测试的经济性;但是,首先讨论 CAD 验前概率评估的各个方面是有用的。如协议步骤 2 和 3 中所述,CAD 验前概率的估计是将 CAD 分数置于上下文中并确定 CAD 验后概率的关键步骤。我们使用了 ESC 2013 指南,该指南根据三个特征确定 CAD 的可能性:性别、年龄和症状(在典型心绞痛、非典型和非心绞痛组中)7。然而,重要的是要注意,医生在选择任何定量或定性方法时可能会应用他们的临床判断。此外,还有其他已发布的定量方法可用于此类估计,包括 Diamond-Forrester13,它需要与 ESC 2013 相同的输入特征。更全面的变体也已发表,例如扩展了14 Diamond-Forrester 的女性雌激素状态(以补偿更年期的年龄变化,以及任何子宫切除术),以及糖尿病、高血压、高脂血症、吸烟、冠心病家族史和肥胖。但是,请注意,某些方法可能将 CAD 定义为 50% 管腔狭窄,而 70% 代表当前的 ACC 指南(左主干除外为 50%)。
POC-CAD 的经济性以及测试如何与护理路径相互作用是确定测试是否真正适合临床使用的关键特征。对于冠状动脉疾病的诊断,最常用的测试是 MPI,通常称为核应力测试或 SPECT。截至 2019 年,大约 85% 的15 加元评估中使用了 MPI。据估计,美国每年进行 7-800 万例 SPECT-MPI 研究16。在大约 5% 的患者病例中,CCTA 用于诊断 CAD。CCTA 被认为在排除重大 CAD 方面具有卓越的诊断性能。另外两种成像方式,PET 和心脏 MRI,构成了其余评估的大部分。对于所有这些测试,都需要一台成像相机和一个合格的团队来运行和解释测试。这种相机是昂贵的资本设备。因此,这些测试通常仅限于城市医疗保健机构的可用性,因为城市医疗保健机构有足够的数量来证明初始费用和运营成本的合理性。
2021 年,美国心脏病学会 (ACC) 发布了针对无已知 CAD 或既往检查以及 CAD 2,17 中等风险患者的指南,其中 MPI 和 CCTA 都被认为是一线诊断选择。与 CCTA 和 MPI 相比,POC-CAD 可用于任何护理点环境,例如医生办公室、重症监护医院、部落护理中心和三级护理中心,而不是像 CCTA 和 MPI 那样仅限于那些拥有昂贵成像设备的中心和作它们所需的团队。
通常,一线检查后疑似 CAD 的患者将被转诊进行 ICA;如前所述,这被认为是 CAD 的金标准诊断。ICA 是由侵入性心脏病学专家在门诊医院进行的一种侵入性手术。
最近对一家大型高等教育中心的放射学检查预约出席率的研究显示,由于取消或未出现,患者没有参加 24% 的预定预约18。研究的放射学方式包括 CAD 诊断。该研究中报告的数字与与医疗保健系统财务官的讨论一致,后者假设未出现率为 20%。此外,在与乡村医生的多次讨论中,可能需要大量的旅行时间才能到达测试,高达 50% 的患者可能不会继续预约和参加预约。在下面的模型中,保守地对于农村市场,假设为 30%(即 70% 参加预约)。
对下游检测的诊断率有直接影响,因为有大量患者没有进行推荐的检测。假设有和没有严重冠状动脉疾病的个体的发病率是一致的,那么在转诊人群中检测病情的敏感性将是预期敏感性的 70%。据报道,在 SPECT 的情况下,检测具有功能意义的 CAD 的灵敏度为 73%,有效灵敏度仅为 53% (= 0.7 x 73%)12,即,在转诊人群中,几乎有一半的具有功能意义的 CAD 患者会被漏诊。这些错过的患者不会给医疗保健系统带来零成本。具有功能意义的 CAD 阳性患者可能会在以后就诊,并且由于疾病进展而产生大量额外费用。例如,如果患者随后到急诊科就诊,则有急性冠脉综合征体征的患者的平均就诊费用为 30,000 美元19。
此外,即使对于那些没有严重 CAD 的患者,如果他们不遵循医生的转诊进行影像学检查,他们也不太可能返回该医生那里,因此,确定其他可能导致他们症状的原因的机会有限。就潜在疾病的进展而言,这对患者和医疗保健系统来说也可能代价高昂。例如,已证明心力衰竭的诊断延迟每年会使该患者的治疗费用增加 8,000 美元20。
这里介绍的成本经济模型旨在捕捉这些影响,将 POC-CAD 用作重要 CAD 的一线测试与使用 SPECT 的场景进行比较。由于 POC-CAD 是一种排除测试,因此预计假阳性结果的数量会比 SPECT 多。期望检测的所有阳性结果都会进入 ICA 是不合理的。在许多情况下,最好采用第二次测试。在分析具有功能意义的 CAD 的各种无创测试的规则输入和排除性能时,Knuuti 等人建议在 CCTA 之后进行功能测试,例如 SPECT12。然而,这又存在无法识别相对较大比例的阳性患者的风险。更好的功能测试是心脏 PET,其敏感性为 89%,特异性为 85%12。心脏 PET 在美国的使用越来越多,目前最常由心脏病专家开具处方,并且已经比 CCTA15,21 更频繁地使用。在此模型中,假设 PET 的阳性结果继续进行 ICA。由于 PET 的敏感性与 POC-CAD 的敏感性相似,因此假设传入 PET 群体中的所有阳性都被 PET 正确分类为阳性。在使用 SPECT 作为一线检测的模型中,假设阳性患者会继续进行 ICA。假设传入患病率为 12%,则 ICA 的正检出率为 41%,接近 PROMISE 研究中观察到的阳性检出率 10。
图 3 描述了模型和结果,使用了 200 名有心血管疾病症状的假设新来人群。假设 SPECT、PET 和 POC-CAD 均按相同的费率报销:每次检测 2,500 USD。ICA 假设报销为 3,000 美元。ICA 期间或之后的任何治疗费用不包括在模型中,因为这超出了模型所代表的诊断途径。丢失的阴性患者和丢失的阳性患者的成本更难估计。鉴于这些患者被定义为没有按照医生的指示进行影像学检查,因此假设他们与医疗保健系统的下一次互动是因心血管疾病症状到急诊科就诊。在一项对具有此类症状的急诊科表现的研究中,Pope 等人确定 17% 符合急性心肌缺血的标准,6% 患有稳定型心绞痛,21% 患有非缺血性心脏问题,56% 患有非心脏问题22。O'Sullivan 等人计算出在急诊科初次就诊的费用为非致命性心肌缺血 34,200 美元,无冠状动脉血运重建心绞痛 17,300 美元23。仅使用初次就诊的费用是一种保守的方法,因为事件产生的急性期(3 年)费用要高得多,分别为 73,300 美元和 36,000 美元。使用 United Healthcare 2,988 报告的信息,53% 的胸痛就诊费用估计为 2,988 美元,但没有发现由此产生的心脏问题。最后,对于 21% 患有非缺血性心脏病的人,费用估计为 2,988 美元,加上因延迟治疗心脏病而造成的增量费用。如上所述,对于心力衰竭患者,延迟诊断的年度增量成本计算为 8,00020 美元。因此,假设这些患者中的大多数患有心力衰竭或肺动脉高压,并且两者的延迟治疗费用相似,则 21% 的费用为 10,988 美元。同样,仅使用一年的增量成本是一种保守的方法,因为这实际上适用于随后的每一年。总体而言,模型中使用的这些成本的加权平均值为 10833 USD。
成本经济模型表明,总而言之,由于延迟治疗导致疾病进展需要更高级护理的成本,每位患者可能为医疗保健系统平均节省 1,172 美元。此外,采用该途径将使 ICA 的产量提高到 62%,而目前在 SPECT 途径中观察到和建模的产量为 41%。
如果外推到美国每年 225 万名出现心血管疾病症状的农村患者,实施 POC-CAD 作为严重 CAD 的一线检测的总潜在节省约为 26.4 亿美元。如上所述,这些节省的很大一部分是由于比 SPECT 具有更高的敏感性和更高的诊断率而不会漏诊具有功能意义的 CAD 患者。此外,ICA 可实现更高的产量是一个关键优势,因为与 SPECT 途径相比,在 POC-CAD>PET 途径下进行的 ICA 更多。ICA 的更高产量将有利于患者,他们目前经常对阴性 ICA 结果感到沮丧25、介入心脏病专家和医疗保健系统。
对这种模型的一个可能的反对意见是,每个人都应该直接被推荐给 PET,而不是先使用 POC-CAD 测试。这种方法,尤其是在考虑到农村人口时,可能充满了目前在所有影像学检查中观察到的相同问题——失访。如果保持对模型的相同假设,PET 的有效检出率将只有 62% (= 0.7 x 89%),因此仍然遗漏了该人群中许多真正阳性的患者。相反,据观察,POC-CAD 检测呈阳性可以鼓励患者跟进转诊以进行后续诊断测试(例如 ICA),因此,预计这不会成为 POC-CAD>PET 通路的问题。人们可能还会争辩说,SPECT 是主要途径,因此最有可能是 POC-CAD 之后在实践中使用的测试。在这种情况下,所得 POC-CAD>SPECT 通路的节省将略高于上述水平,但 ICA 的有效检出率将略低 (58%),因为流中将额外漏诊 3 名阳性患者(假阴性),共 200 名。
总之,POC-CAD 为诊断途径提供了一个有前途的补充。该测试的主要优点是它可以在护理点使用,无需使用辐射、压力或造影剂,但提供与 CCTA 相当的结果,以排除具有功能意义的 CAD26。此外,在同一次就诊中即可获得结果,使医生无需安排再次就诊即可与患者讨论下一步的护理步骤。由于该测试可以在护理点进行,并且结果可快速获得,因此 POC-CAD 解决了观察到的失访的重大问题,尤其是在农村地区,约占美国人口的四分之一。鉴于测试的稳健排除特征,阴性结果,医生可以快速探索患者症状的其他解释。当对由此导致的患者诊断延迟的成本进行建模时,使用 POC-CAD 作为一线测试将为患者、医生和付款人提供显着优势。此外,现有的成像方式不会看到体积的显着增加或减少,这是许多成像中心关心的问题。通过更及时地诊断和治疗患者的病情,可以节省成本。
披露声明
T.B.、N.N.、F.F.、H.G.、C.B.、S.R. 和 I.S. 是 Analytics for Life 的员工。
有关 CorVista CAD 评分解释的方法代表了基于已验证总体子集的当前假设,需要进一步验证。请参阅产品使用说明。
致谢
作者要感谢 Dubberly Design Office(旧金山)的 Cody Wackerman 和 Hugh Dubberly 在可视化 图 3 所示路径方面的帮助。
材料
| Name | Company | Catalog Number | Comments |
| CorVista CAD | CorVista | n/a | System comprising signal acquisition, cloud processing, and delivery of a report containing the CAD Score via a web portal |
| Electrodes | Various (see comments) | Diagnostic quality or high performance electrodes are recommended. For example: Conmed ClearTrace 1700-007 Skintact FS-TB1 Vermed A10005 |
参考文献
- World Health Organization. The top 10 causes of death [Internet]. 2020 [cited 2024 Jun 27]. , Available from: https://www.who.int/news-room/fact-sheets/detail/the-top-10-causes-of-death (2020).
- Lawton, J. S., et al. 2021 ACC/AHA/SCAI guideline for coronary artery revascularization: A report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol. 79 (2), e21-e129 (2022).
- Burton, T., et al. Development of a non-invasive machine-learned point-of-care rule-out test for coronary artery disease. Diagnostics. 14 (7), 719(2024).
- Stuckey, T. D., et al. Clinical validation of a machine-learned, point-of-care system to IDENTIFY functionally significant coronary artery disease. Diagnostics. 14 (10), 987(2024).
- Frank, E. An accurate, clinically practical system for spatial vectorcardiography. Circulation. 13 (5), 737-749 (1956).
- Park, J., Seok, H. S., Kim, S. S., Shin, H. Photoplethysmogram analysis and applications: An integrative review. Front Physiol. 12, 808451(2022).
- Montalescot, G., et al. 2013 ESC guidelines on the management of stable coronary artery disease: the Task Force on the management of stable coronary artery disease of the European Society of Cardiology. Eur Heart J. 34 (38), 2949-3003 (2013).
- Baratloo, A., Hosseini, M., Negida, A., El Ashal, G. Part 1: Simple definition and calculation of accuracy, sensitivity and specificity. Emergency. 3 (2), 48-49 (2015).
- Ranganathan, P., Aggarwal, R. Understanding the properties of diagnostic tests-Part 2: Likelihood ratios. Perspect Clin Res. 9 (2), 99-102 (2018).
- Douglas, P. S., et al. Outcomes of anatomical versus functional testing for coronary artery disease. New Eng J Med. 372 (14), 1291-1300 (2015).
- Safari, S., Baratloo, A., Elfil, M., Negida, A. Evidence based emergency medicine; part 4: Pre-test and post-test probabilities and Fagan's nomogram. Emergency. 4 (1), 48(2016).
- Knuuti, J., et al. The performance of non-invasive tests to rule-in and rule-out significant coronary artery stenosis in patients with stable angina: a meta-analysis focused on post-test disease probability. Eur Heart J. 39 (35), 3322-3330 (2018).
- Diamond, G. A., Forrester, J. S. Analysis of probability as an aid in the clinical diagnosis of coronary-artery disease. New Eng J Med. 300 (24), 1350-1358 (1979).
- Morise, A. P. Comparison of the Diamond-Forrester method and a new score to estimate the pre-test probability of coronary disease before exercise testing. Am Heart J. 138 (4), 740-745 (1999).
- Pelletier-Galarneau, M., Vandenbroucke, E., Lu, M., Li, O. Characteristics and key differences between patient populations receiving imaging modalities for coronary artery disease diagnosis in the US. BMC Cardiovasc Disord. 23 (1), 251(2023).
- Li, J., et al. Factors that impact a patient's experience when undergoing single-photon emission computed tomography myocardial perfusion imaging (SPECT-MPI) in the US: A survey of patients, imaging center staff, and physicians. J Nuclear Cardiol. 28 (4), 1507-1518 (2021).
- Lawton, J. S., et al. 2021 ACC/AHA/SCAI guideline for coronary artery revascularization: A report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol. 79, e21-e129 (2022).
- Aijaz, A., et al. Sociodemographic factors associated with outpatient radiology no-shows versus cancellations. Acad Radiol. S1076 - 6332 (24), 00228-00229 (2024).
- Cowper, P. A., et al. Acute and 1-year hospitalization costs for acute myocardial infarction treated with percutaneous coronary intervention: Results From the TRANSLATE-ACS registry. J Am Heart Assoc. 16 (8), 8(2019).
- Thomas, A., et al. Forgone medical care associated with increased health care costs among the U.S. heart failure population. JACC Heart Fail. 9 (10), 710-719 (2021).
- Reeves, R. A., Halpern, E. J., Rao, V. M. Cardiac imaging trends from 2010 to 2019 in the Medicare population. Radiol Cardiothorac Imaging. 3 (5), (2021).
- Pope, J. H., et al. Missed diagnoses of acute cardiac ischemia in the Emergency Department. New Eng J Med. 342 (16), 1163-1170 (2000).
- OʼSullivan, A. K., et al. Cost estimation of cardiovascular disease events in the US. Pharmacoeconomics. 29 (8), 693-704 (2011).
- Corso, A. Emergency visit cost with and without insurance in 2024. Mira. , https://www.talktomira.com/post/how-much-does-an-er-visit-cost (2024).
- Patel, M. R. Low diagnostic yield of elective coronary angiography. New Eng J Med. 362 (10), 886-895 (2010).
- Browning, S. CorVista System 510(k) Summary (K232686). , U.S. Food and Drug Administration. Retrieved from https://www.accessdata.fda.gov/cdrh_docs/pdf23/K232686.pdf (2024).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。