Method Article
冠動脈疾患に対する非侵襲的ポイントオブケアテストの信号取得、スコア解釈、および経済学
要約
冠動脈疾患(CAD)検査の生理学的シグナルを取得する方法論が提示されます。テストの陽性性と否定性に関するCADスコアを、それぞれの粒度を含めて解釈する方法が提案されています。テストの経済性は、現在の標準治療の文脈で議論されています。
要約
冠動脈疾患 (CAD) (POC-CAD) のポイントオブケア非侵襲的検査は、以前に開発され、検証されています。このテストでは、直交電圧勾配(OVG)信号と光電式容積脈波信号の同時取得が必要であり、これがこのホワイトペーパーで説明する主要な方法論です。生体電位信号であるOVGの取得には、患者の胸部の準備された皮膚に電極を配置する必要があります(フランクリード構成と同様に配置され、6つのバイポーラ電極と参照電極を含む)および指の血行動態センサー(標準的な伝送モダリティを使用)。信号はクラウドベースのシステムにアップロードされ、そこで設計された特徴が信号から抽出され、機械学習アルゴリズムに供給されてCADスコアが生成されます。その後、医師は、患者の検査前のCADの確率のコンテキストでCADスコアの値を解釈する必要があり、その結果、検査後のCADの確率が得られます。この解釈は、テストの陽性率とテストの陰性のレベルで、またはより詳細なレベルの粒度で実行できます。ここでは、それぞれの方法論を尤度比に基づいて提案します。検査後の確率を使用して、医師は患者の治療における適切な次のステップを決定しなければなりません。このプロセスを説明するために、いくつかのシナリオが使用されます。テストの採用は、経済的に実行可能な場合にのみ実現可能です。また、このテストをCAD診断フローに統合し、その結果として医療システムにもたらすコスト削減について説明します。この経済モデルは、治療の遅延を防ぐことで医療システムのコスト削減を達成できることを示しています。治療の遅延は、対処せずに放置すると、より高度な(そして高価な)ケアを必要とする疾患の進行につながります。
概要
虚血性心疾患(IHD)は、現在、世界の主要な死因です1。冠動脈疾患 (CAD) は、IHD の解剖学的前駆体であり、冠状動脈内に重大な病変が存在することを特徴としています。有意性は、左主動脈2における少なくとも70%または50%の閉塞によって解剖学的に定義することができる。有意性は、血流への影響を測定することにより、病変の機能的影響に基づいて定義することもできます。具体的には、フラクショナル フロー リザーブ (FFR) と瞬時フロー リザーブ (iFR) は、病変によって引き起こされるフローの変化を評価し、病変は FFR < 0.80 または iFR < 0.892 で有意であると定義されます。重要なCADの存在を確認するためのゴールドスタンダードは、左心カテーテル法(LHC)による侵襲性冠動脈造影法(ICA)です。重要なCADは、ステントまたは冠状動脈バイパス移植による血行再建術を保証し、心筋虚血および対応する狭心症症状を緩和し、プラークを安定させます(ステント留置術の場合)。
現在のCADの非侵襲的試験では、放射線被曝、ストレス、造影剤注入(腎臓への影響を伴う)が必要になることがよくあります1。最も一般的に使用される診断テストは、心筋灌流イメージング(MPI)(単一光子放出型コンピューター断層撮影法(SPECT)とも呼ばれる)と冠動脈コンピューター断層撮影血管造影法(CCTA)です。SPECTは、休息時やストレス時(運動中または薬物中)の灌流を追跡するために、放射性同位元素を注入するものです。CCTAは、複数のX線を使用して冠状動脈を画像化します。CADテストには、陽電子放出断層撮影法(PET)や心臓磁気共鳴画像法(CMR)も時折使用されます1。これらすべてのモダリティには、機器への多額の設備投資、テストを実施するための訓練を受けた人員、場合によっては医療用アイソトープの利用可能性が必要です。これらの要件により、これらのモダリティは、特に地方の環境では広く利用できないことが多く、患者のケアの遅延を引き起こし、関連するリスクをエスカレートさせます。
そこで、CAD(POC-CAD)用の非侵襲的なポイントオブケア検査、CorVistaシステム3を設計することが目標でした。このシステムは、機能的に重要なCADのFDA認可試験であり、CCTA4に匹敵する性能を備えています。この検査は、患者のストレスなく、機器や専門スタッフへの設備投資を必要とせずに使用できます。これは、現在のイメージング技術にアクセスできないことが多い農村部やリソースに制約のある環境での使用に最適です。
POC-CADの開発3 と検証4 は以前に公開されています。簡単に言うと、POC-CADは、プロトコルステップ1で説明したように、キャプチャデバイスを使用して直交電圧勾配信号と光電式容積脈波信号を同時に取得することから始まります。直交電圧勾配は、Frankリード構成5と同様のリード配置を使用して取得された生体電位信号であり、6つのバイポーラ電極と胴体に取り付けられた参照電極で構成されます。フォトプレチスモグラムは、赤色光と赤外光が指先を透過し、センサー6に当たる標準的な透過モダリティを使用して取得されます。信号が集録されると、クラウドベースのシステムに自動的にアップロードされ、そこでエンジニアリングされた特徴が信号から抽出され、機械学習アルゴリズムに供給されてCADスコアが生成され、Webポータルに表示されます。プロトコルのステップ2と3では、テストによって返されたCADスコアを解釈する方法が説明されています。具体的には、公開されたデータまたは医師に関連する他の情報源のいずれかを使用して、患者が検査を受ける前にCADの確率を推定できます。尤度比は、テストのパフォーマンスから計算し、バイナリテスト結果(ステップ2)またはCADスコアのより詳細な値(ステップ3)を使用して、テスト前からテスト後へのCADの確率を更新するために使用できます。最後に、現在の標準治療と比較したPOC-CADの経済性のモデリングについて説明します。
プロトコル
この研究は、Western Institutional Review Boardによって承認され、ヘルシンキ宣言に従って実施されました。参加のために、すべての被験者から書面によるインフォームドコンセントが得られました。簡単に言えば、含まれるには、被験者は心血管症状のある 18 歳以上である必要がありますが、冠状動脈疾患は知られておらず、ICA または CCTA を受ける予定である必要があります。除外基準には、心筋梗塞の既往歴、冠動脈バイパス移植術、心臓弁置換術の既往歴などが含まれていました。完全な研究の選択基準と除外基準は、clinicaltrials.gov のNational Clinical Trial(NCT)番号NCT03864081に記載されています。使用した機器とソフトウェアは 、資料表に記載されています。
1. 信号取得
- 電極部位の毛を削って肌を整えます。石鹸と水で洗浄し、必要に応じて清潔で乾燥したガーゼまたはノンアルコールワイプを使用して、皮膚に残留物が残っていないことを確認します。
- リード線を電極に接続し、 表1に従って配置します。
注意: 電極の品質は信号の品質に影響を与える可能性があります。診断品質または高性能の電極を使用することをお勧めします。 - 血行動態(光電式容積脈波、PPG)センサーを被験者の指に置き、指がセンサーのできるだけ奥まで来るようにし、センサーケーブルを手の上部に沿って配置します。
- 人差し指は、傷やその他の臨床的に関連する理由により使用が妨げられない限り、使用してください。.センサーを置いたら動かさないように患者にアドバイスしてください。
- 患者を仰向けに平らに置き、快適な安静姿勢にします。PPGセンサーケーブルと電極ケーブルが重ならないようにしてください。
- 必要に応じてクッション(例:丸めた毛布やタオル、枕と一緒に)を使用して、患者が背中の青色電極に直接圧力をかけないようにします。
- 信号ノイズを制限し、信号品質を最大化するには、可能な限り、すべての電子機器(モニター、テレビ、携帯電話など)の電源を切るか、部屋から取り外してください。部屋の照明を消します。
- 患者情報を入力し、正確性を確認します:患者の名、患者の姓、出生時の性別、身長(インチ)、体重(ポンド)、生年月日、医療記録番号(すべて必須、任意の順序で入力可能)。
- 患者が快適であることを確認し、じっと静かにするように促します(例:取得中は話さないでください)。
- デバイスを平らな面に置き、アプリケーションへの配置を確認します。 Start を押して、信号集録を開始します。
- デバイスでエラーメッセージがないか監視し、表示された場合は、画面の指示に従って解決します。
- 信号収集が完了した後、3分35秒かかりますが、デバイスは信号品質評価のためにデータを自動的にクラウドに送信します。通過信号の品質が確認されるまで、患者をデバイスに取り付けたままにします。
- 電極を患者から取り外し、PPGセンサーを取り外します。
- ポータルにアクセスして、テスト結果を表示します(信号がクラウドにアップロードされてから約10分後に利用可能になります)。
表 1: リードの配置。 7つの電極のそれぞれを配置する解剖学的位置の説明。 この表をダウンロードするには、ここをクリックしてください。
2.テスト結果が陽性 対 の場合の検査結果の解釈。テスト陰性
- 患者の検査前の疾患の確率を判断します(たとえば、欧州心臓病学会(ESC)ガイドライン7を使用)。
- CADスコアを0と比較して、患者の検査が陽性か陰性かを判断します:ゼロ以上の場合、患者の結果は検査陽性、またはゼロ未満の場合は結果は検査陰性です。
- レポートからCADスコア値を読み取り、レポートの下部に示されている検証コホートの陰性患者と陽性患者の分布と比較します。
- 感度と特異度8を計算し、次に式1と式29を使用して尤度比(LR)を計算します。
注: テスト感度が 88% (疾患を持つ被験者の唯一のグループである ICA からの陽性の被験者を使用して計算) であり、特異度が 51% (CCTA から陰性の被験者を 94% の重みで、ICA から陰性の被験者を 6% の重みで使用して計算し、PROMISE 研究10 を通じて全人口を表すために) が実際の例を示しています。
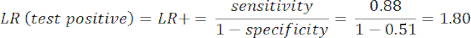 (式 1)
(式 1)
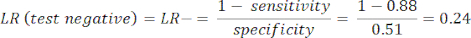 (式 2)
(式 2) - 次の式 3-511 (陽性の場合は LR+ が使用され、陰性の場合は LR- が使用されます) を前提として、患者の検査後の確率を計算します。
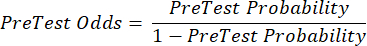 (式3)
(式3)
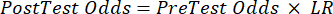 (式4)
(式4)
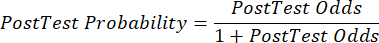 (式5)
(式5) - CADの更新された確率で、テストの結果を考慮して、患者ケアの適切な次のステップを決定します(たとえば、表2に示すESCガイドライン7の推奨事項を使用します)。
表2:CADの確率によるESCガイドライン。 CADの確率の4つのレベルについて、欧州心臓病学会のガイドラインは、次のテスト(必要な場合)を含め、その確率の適切な解釈を目的としています。 この表をダウンロードするには、ここをクリックしてください。
3. より詳細な粒度で与えられたテスト結果の解釈
- 表3に示すように、テストの検証に使用された母集団で観察されたCADスコアの範囲、特にテスト陽性とテスト陰性の範囲で三分位数(3つのビンに等しい数の被験者)への分割を考慮して、テスト陽性とテスト陰性の結果の粒度を上げます。
注: 計算を簡単にするために、カテーテル法から陰性の被験者の 6% の寄与はこの分析から除外され、それを含めても結果は大きく変わりません。 - テスト陰性範囲の各三分位数内で、真に病気にかかっていない被験者である True Negative (TN) の数と、本当に病気にかかっている被験者である False Negative (FN) の数を計算します。
- 次の式6-811 を適用して、各テスト陰性の三分位数(陰性の三分位数からのLR+は関係ありません)のLR-を決定します。
注:この方程式は、三分位数のパフォーマンスプロファイルがパフォーマンス統計を計算するための完全なテスト陰性範囲を表すことを前提としています(テスト陽性率に関して元のテスト陰性度を達成するためには、三分位数に対応する3の補正係数が必要です)。
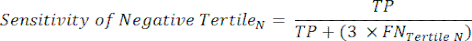 (式6)
(式6)
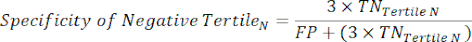 (式7)
(式7)
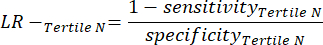 (式8)
(式8)
- 次の式6-811 を適用して、各テスト陰性の三分位数(陰性の三分位数からのLR+は関係ありません)のLR-を決定します。
- テスト陽性範囲の各三分位数内で、真陽性(TP)の数(本当に病気にかかっている被験者)と偽陽性(FP)の数(本当に病気にかかっていない被験者)を計算します。
- 式9-11を適用して、各テスト陽性の三分位数(LR-は正の三分位数から関連性がない)11のLR+を決定します。
注:この式は、パフォーマンス統計を計算するために、三分位数のパフォーマンスプロファイルがテスト陽性の全範囲を表すことを前提としています(テストの陰性度に関して元のテスト陽性の頻度を達成するためには、三分数に対応する3の補正係数が必要です)。
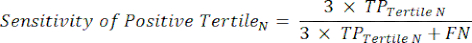 (式9)
(式9)
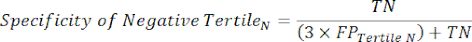 (等価10)
(等価10)
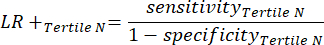 (EQN 11)
(EQN 11)
- 式9-11を適用して、各テスト陽性の三分位数(LR-は正の三分位数から関連性がない)11のLR+を決定します。
- 患者のCADスコアがどの三分位数内にあるかを決定し、 表3のLRを考慮して、ステップ2で示した手順を前提としたテスト後の確率を計算します。
注:予想通り、LR-値はCADスコアが負の値が多いほど減少し、LR+値はCADスコアが正の値が多いほど増加します。つまり、CADスコアが負の値が多いほどテスト前の確率が効果的に減少し、CADスコアが正の値が多いほどテスト前の確率が効果的に増加します。 - ステップ2.4〜3.4にリストされている計算を実行する代わりに、 表4 を使用して、患者のCADスコア7を使用してテスト前の確率をテスト後の確率に変換します。
表3:尤度比。 テスト陽性とテスト陰性内のスコアの 3 つの範囲について、それぞれ対応する正の尤度比と負の尤度比。 この表をダウンロードするには、ここをクリックしてください。
表 4: テスト前とテスト後の確率マッピング。 10 レベルのテスト前確率について、対応するテスト後確率には、3 つの負の三分位数と正の三分位数のそれぞれで CAD スコアが与えられます。緑色の着色は<15%の疾患確率に対応します(ESCガイドラインではCADを除外できると記載されています)。黄色の着色は、15%〜65%の疾患確率に対応します(ESCガイドラインでは、画像ベースの非侵襲的検査が 望ましいと述べています)。オレンジは66%〜85%の疾患確率に対応します(ESCガイドラインでは、画像ベースの非侵襲的検査 を実施する必要があると述べています)。赤は>85%の疾患確率に対応します(ESCガイドラインではCADを除外できるとされています)。ガイドラインの詳細については、 表 2 を参照してください。CAD スコア 0 はテスト陽性と見なされることに注意してください。 この表をダウンロードするには、ここをクリックしてください。
結果
信号の例を 図 1 に示し、 図 2 にレポートを示します。これは、テストを使用する医師に見えるようになっています。以下は、CADスコアの重要性を解釈する際の方法論の適用を示すために提供されているいくつかの患者のケースです。
ケース1
67歳の男性は、安静時の胸痛、放射状の腕の痛み、発汗、吐き気の症状を訴えました。ESCガイドライン7に基づくと、彼の年齢、性別、および症状は、84%の初期疾患確率と一致しています。ESCガイドラインは、そのような患者がCADの診断を下すために非侵襲的検査を必要とし、心臓カテーテル検査への紹介と必要な介入を正当化することを示唆しています(表2)。POC-CADを実行したところ、0.32のCADスコアが返されましたが、これはテスト陽性の結果であり、陽性のCADスコアの最高三位数に分類され、LR+は2.888でした(表3)。したがって、患者の検査後の確率は 94% であり、ESC ガイドライン (表 2) によれば、患者は安全に CAD を持っていると想定でき、侵襲的な心臓カテーテル検査が適切な行動方針です。
ケース2
39歳の女性は、安静時に胸痛を呈し、左側と右側の両方に放射状に広がっています。ESCガイドライン7に基づくと、彼女の年齢、性別、および症状は、疾患の初期確率である28%と一致しており、ガイドラインは、CADの確率をより深く理解するための次のステップとして、非侵襲的検査が望ましいことを示唆しています。しかし、ガイドラインでは、若い患者(この39歳の女性など)では、医師は放射線被曝を意識すべきであり、これはSPECTのような検査を行うために必要な放射線被曝であり、放射性同位元素の注射が必要であるとも述べられています。このような検査の別のオプションはCCTAですが、これには多くのX線が必要です。したがって、POC-CADは放射線を必要としないため、論理的な選択です。テストが実行され、負の範囲の最初の三分位数の範囲内で -0.12 の値が返され、LR- は 0.129 でした (表 3)。結果として得られるテスト後の確率は4%で、ESCガイドラインに従ってCADを安全に除外できるレベルまで低下し、CADに対して追加のテストは必要ありません。
ケース3
74歳の女性が非狭心症性胸痛と呼吸困難を呈しています。ESCガイドライン7に基づくと、彼女の年齢、性別、および症状は、疾患の初期確率である24%と一致しており、ガイドラインは、CADの確率をより深く理解するための次のステップとして、非侵襲的検査が望ましいことを示唆している。患者は、治療を受けている地方の診療所から、すべての検査方法(PET、SPECT、CCTA、CMR)が利用可能な大都市の中心部に移動することを躊躇しているため、医師はPOC-CADを提供しています。CADスコアは0.07で、LR+が1.446で正の範囲の最初の三分位数に収まり、テスト後の確率は33%になります。陽性の結果と病気の可能性の増加に基づいて、患者はPETスキャンのために市内に旅行することに同意します。PETはまた、LR+が6.0412で、PET後の33%から75%を増加させる疾患を示していました。
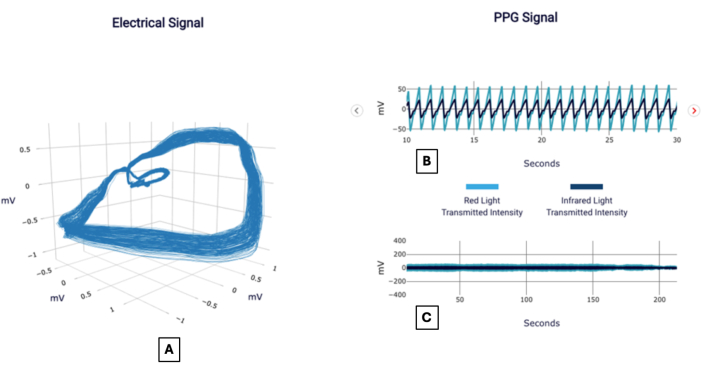
図1:信号の例。 電気信号(A)とも呼ばれる直交電圧勾配と、20秒間隔(B)と全持続時間(C)に焦点を当てた光電式容積脈波信号の視覚化を示す模範的なPOC-CADレポート。 この図の拡大版を表示するには、ここをクリックしてください。
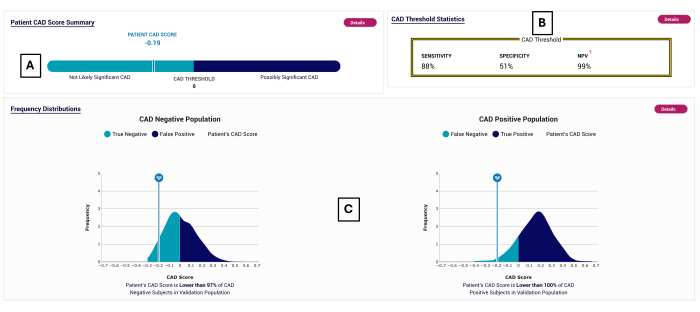
図2:CADレポートの例。 模範的なPOC-CADレポートで、CADスコアが-0.19(A)で、テスト陰性の範囲(<0)に収まっています。テスト性能を(B)に示します。(C)でPOC-CADを検証した被験者について、CADスコアの分布を表示します。 この図の拡大版を表示するには、ここをクリックしてください。
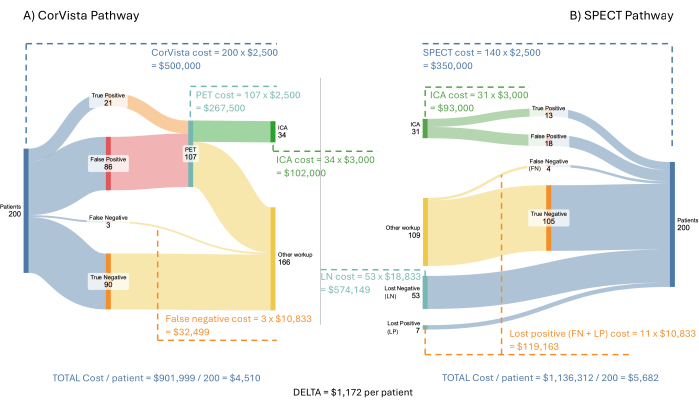
図3:コスト経済モデルの流れ。 200人の患者からなる架空の患者集団が、POC-CAD>PET経路(A)とSPECT経路(B)を介して実行されます。医療システムへのコストは、各経路の各分岐ごとに示されており、POC-CAD>PET経路が実装された場合の患者一人当たりの平均節約額も示されています。 この図の拡大版を表示するには、ここをクリックしてください。
ディスカッション
このセクションの主な焦点は、テストの経済性です。ただし、最初にCADの事前テスト確率の評価の側面について説明することは有用です。プロトコルのステップ2および3で説明したように、CADのテスト前の確率の推定は、CADスコアをコンテキスト化し、CADのテスト後の確率を決定するための重要なステップです。ESC 2013 ガイドラインでは、性別、年齢、症状 (定型狭心症、非定型性、非狭心症のグループ内) の 3 つの特性に基づいて CAD の確率を決定しました7。ただし、医師は定量的または定性的方法の選択に臨床的判断を適用する可能性があることに注意することが重要です。さらに、ESC 2013と同じ入力特性を必要とするDiamond-Forrester13など、このような推定に利用できる他の公開された定量的方法があります。より包括的なバリエーションは、女性のためのエストロゲンの状態を持つ14 ダイヤモンドフォレスターを拡張するなど、(更年期障害の年齢変動を補うためだけでなく、任意の子宮摘出術)、糖尿病、高血圧、高脂血症、喫煙、冠状動脈疾患の家族歴、および肥満。ただし、一部の方法論では、CAD を 50% の内腔狭窄と定義しているのに対し、70% は現在の ACC ガイドラインを表していることに注意してください (左主動脈の 50% を除く)。
POC-CADの経済性と、検査がケアパスとどのように相互作用するかは、検査が本当に臨床使用に適しているかどうかを判断する上で重要な特性を表しています。CADの診断に最も頻繁に使用されるテストはMPIであり、多くの場合、核負荷テストまたはSPECTとして知られています。2019年現在、CAD15の評価の約85%でMPIが使用されています。米国では、年間推定700万〜800万件のSPECT-MPI研究が実施されています16。患者の症例の約5%で、CCTAはCADの診断に使用されており、CCTAは重要なCADを除外する優れた診断性能を持っていると認識されています。他の 2 つの画像診断法である PET と心臓 MRI が、残りの評価の大部分を占めています。これらすべてのテストでは、イメージングカメラと資格のあるチームがテストを実行して解釈する必要があります。このようなカメラは高価な資本設備です。その結果、これらの検査は、初期費用と運用コストの両方を正当化するのに十分な量がある都市部の医療現場に限られることがよくあります。
2021年、米国心臓病学会(ACC)は、CADまたは以前の検査が知られておらず、リスクが中程度でCAD2,17の患者向けのガイドラインを発表しました。このガイドラインでは、MPIとCCTAの両方が最前線の診断オプションとして認識されていました。CCTAやMPIとは対照的に、POC-CADは、CCTAやMPIのように高価な画像機器を備えたセンターとその運用に必要なチームに限定されるのではなく、診療所、救命救急病院、部族医療センター、三次医療センターなど、あらゆるポイントオブケア環境で使用できます。
通常、最前線の検査後にCADが疑われる患者はICAに紹介されます。ICAは、侵襲的な心臓病専門医が外来病院で行う侵襲的な処置です。
大規模な高等教育センターでの放射線検査の予約出席率に関する最近の研究では、予定された予約の24%がキャンセルまたは無断キャンセルのために患者が出席しなかったことが示されました18。研究された放射線モダリティには、CAD診断が含まれていました。この調査で報告された数字は、医療システムの財務責任者との話し合いと一致しており、財務責任者はノーショー率を20%と想定しています。さらに、検査を受けるためにかなりの移動時間が必要になる可能性のある地方の医師との複数の話し合いでは、最大50%の患者が予約と予約の両方に対応しない可能性があります。次のモデルでは、控えめに農村市場の場合、これは30%(つまり、70%が予約に出席する)と想定されます。
かなりの数の患者が推奨検査に進まない場合、ダウンストリーム検査の診断歩留まりに直接影響します。重大な冠状動脈疾患のある個人とない個人間でレートが一貫していると仮定すると、紹介された集団全体で状態を検出する感度は、予想される感度の 70% になります。機能的に重要なCADを検出するための感度が73%と報告されているSPECTの場合、有効な感度はわずか53%(= 0.7 x 73%)12であり、つまり、紹介された集団の臨床的に重要なCADを持つ患者のほぼ半数が見逃されます。これらの見逃された患者は、医療システムにゼロの費用がかかるわけではありません。機能的に重要なCADを持つ陽性患者は、後で診察を受ける可能性が高く、疾患の進行により大幅な追加費用が発生します。例えば、患者がその後救急科に来院した場合、急性冠症候群の徴候を有する患者の訪問の平均費用は30,000ドルと計算されている19。
さらに、重大なCADを持たない患者であっても、医師の紹介に従って画像診断を行わないと、その医師に戻る可能性が低くなり、他に症状の原因が何であるかを判断する機会が限られています。これは、基礎疾患の進行という点で、患者と医療システムの両方にとってもコストがかかる可能性があります。たとえば、心不全の診断が遅れると、その患者の治療費に年間8,000ドルの増加が生じることが示されています20。
ここで紹介するコスト経済モデルは、POC-CADを重要なCADの最前線テストとして使用するシナリオとSPECTを使用するシナリオを比較し、これらの影響を捉えることを目的としています。POC-CADは除外テストであるため、SPECTよりも多くの誤検出結果が予想されます。この検査で陽性反応が出た人全員がICAに送られると期待するのは不合理です。多くの場合、2回目のテストを採用するのが理想的です。機能的に重要なCADのさまざまな非侵襲的テストのルールインおよびルールアウトパフォーマンスを分析する場合、Knuutiらは、CCTAに続いてSPECT12などの機能テストを行うことを推奨しています。しかし、これもまた、陽性患者の比較的大きな割合を特定できないリスクを冒しています。より優れた機能検査は、感度が89%、特異度が85%の心臓PETです12。心臓PETは米国でますます使用されており、現在、心臓専門医によって最も頻繁に処方されており、すでにCCTA15,21よりも頻繁に使用されています。このモデルでは、PETからの陽性はICAに進むと仮定されます。PETの感度はPOC-CADの感度と似ているため、流入するPET母集団のすべての陽性はPETによって陽性として正しく分類されていると想定されます。SPECTを最前線の検査とするモデルでは、陽性者がICAに進むと仮定します。入ってくる有病率を 12% と仮定すると、ICA での収率は 41% となり、これは PROMISE 研究10 で観察されたものに近いです。
図3 は、心血管疾患の症状を持つ200人の患者からなる架空の流入集団を使用したモデルと結果を示しています。SPECT、PET、POC-CADは、それぞれ同じレート(テストあたり2,500ドル)で払い戻されると想定されています。ICAは3,000ドルで払い戻されると想定されています。ICA中またはその後の治療の費用は、モデルが表す診断経路を超えているため、モデルには含まれていません。ロストネガティブ患者とロストポジティブ患者のコストは、見積もりがより困難です。これらの患者が医師の指示に従わずに画像検査を進めたと定義されることを考えると、医療システムとの次の相互作用は、心血管疾患の症状を訴えて救急科を受診することであると想定されます。このような症状を伴う救急科のプレゼンテーションの研究では、Popeらは、17%が急性心虚血の基準を満たし、6%が安定狭心症、21%が非虚血性心疾患、56%が非心臓疾患であると判断しました22。救急科での最初のプレゼンテーションの費用は、O'Sullivanらによって、非致死性心筋虚血で34,200ドル、冠動脈血行再建術を伴わない狭心症で17,300ドルと計算されています23。最初のプレゼンテーションでの費用のみを使用することは、イベントに発生する急性期(3年)の費用がそれぞれ73,300ドルと36,000ドルと大幅に高いため、保守的なアプローチです。United Healthcare24が報告した情報によると、胸痛による訪問の53%で、心臓の問題は特定されていないため、救急外来の受診費用は2,988ドルと見積もられています。最後に、非虚血性心臓の問題を抱える21%の場合、費用は2,988ドルと見積もられており、さらに心臓病の治療の遅れによる増分費用が加算されています。上記のように、心不全の患者の場合、診断の遅延による年間増分コストは8,000ドルと計算されています20。したがって、21%の費用は10,988ドルと想定されており、これらの患者の大多数が心不全または肺高血圧症のいずれかを患っており、両方に対して同様の遅延治療費用がかかると仮定しています。繰り返しになりますが、1年間の増分コストのみを使用することは、実際にはその後の各年に適用されるため、保守的なアプローチです。全体として、モデルで使用されているこれらのコストの加重平均は 10,833 ドルです。
コスト経済モデルは、要約すると、治療の遅延によるコストにより、より高度なケアを必要とする疾患の進行につながるため、患者1人あたり平均1,172ドルの医療システムへの潜在的な節約を示しています。さらに、この経路を採用すると、ICAでの収量は、SPECT経路で現在観察およびモデル化されている41%と比較して、62%に増加します。
米国で年間225万人の心血管疾患の症状を呈する農村人口に外挿すると、POC-CADを重要なCADの最前線のテストとして実装することによる潜在的な節約総額は約26億4,000万ドルになります。前述したように、これらの節約の大部分は、SPECTよりも高い感度と高い診断収率により、機能的に重要なCADの患者を見逃さないことに由来します。さらに、POC-CAD>PET経路ではSPECT経路よりも多くのICAが実行されるため、ICAでより高い収率を達成できることは重要な利点です。ICAでの歩留まりが高いことは、現在ICAの陰性結果25に不満を感じていることが多い患者、インターベンショナル心臓専門医、および医療システムにとって有益です。
このモデルに対する反論の1つは、最初にPOC-CADテストを使用するのではなく、すべての人を直接PETに紹介すべきだということです。このアプローチは、特に農村部の人口を考慮すると、現在すべての画像検査で観察されているのと同じ問題、つまりフォローアップの損失という問題を伴う可能性があります。モデルについて同じ仮定が維持された場合、PETの実効収率はわずか62%(= 0.7 x 89%)であり、したがって、この集団の真に陽性の患者の多くを見逃しています。逆に、POC-CADによる検査が陽性であった場合、患者はその後の診断検査(ICAなど)への紹介をフォローアップするようになることが観察されており、したがって、これはPOC-CAD>PET経路の問題になるとは予想されていません。また、SPECTが主要な経路であり、したがって、POC-CADに続いて実際に使用されるテストである可能性が最も高いと主張する人もいるかもしれません。この場合、結果として得られる POC-CAD>SPECT 経路の節約は、上記のものよりもわずかに高くなりますが、ICA での実効収率はわずかに低くなります (58%) 。これは、フロー中に 200 人の見逃された陽性患者 (偽陰性) が追加で存在するためです。
結論として、POC-CADは診断経路に有望な追加を提供します。このテストの主な利点は、放射線、ストレス、またはコントラストを使用せずにポイントオブケアで使用できることですが、機能的に重要なCAD26を除外するためにCCTAと同等の結果が得られます。さらに、結果は同じ訪問内で利用できるため、医師は別の訪問をスケジュールすることなく、患者とケアの次のステップについて話し合うことができます。この検査はポイントオブケアで実施でき、結果はすぐに入手できるため、POC-CADは、特に米国人口の約4分の1を占める農村部で観察されたフォローアップの損失という重大な問題に対処します。検査の堅牢な除外プロファイルを考えると、結果が陰性の場合、医師は患者の症状に関する他の説明を迅速に調査できます。その結果として生じる患者の診断の遅延のコストをモデル化すると、POC-CADを最前線の検査として使用することは、患者、医師、および支払者に大きな利点をもたらします。さらに、既存のイメージングモダリティでは、多くのイメージングセンターにとって懸念事項であるボリュームの大幅な増加も減少も見られません。コスト削減は、患者の状態をよりタイムリーに診断し、治療することで実現されます。
開示事項
T.B.、N.N.、F.F.、H.G.、C.B.、S.R.、およびI.S.は、Analytics for Lifeの従業員です。
CorVista CADスコアの解釈に関する方法論は、検証された母集団のサブセットに基づく現在の仮定を表しており、さらなる検証が必要です。使用方法については、製品の説明書を参照してください。
謝辞
著者は、 図 3 に示されている経路の視覚化に協力してくれた Dubberly Design Office (サンフランシスコ) の Cody Wackerman 氏と Hugh Dubberly 氏に感謝します。
資料
| Name | Company | Catalog Number | Comments |
| CorVista CAD | CorVista | n/a | System comprising signal acquisition, cloud processing, and delivery of a report containing the CAD Score via a web portal |
| Electrodes | Various (see comments) | Diagnostic quality or high performance electrodes are recommended. For example: Conmed ClearTrace 1700-007 Skintact FS-TB1 Vermed A10005 |
参考文献
- World Health Organization. The top 10 causes of death [Internet]. 2020 [cited 2024 Jun 27]. , Available from: https://www.who.int/news-room/fact-sheets/detail/the-top-10-causes-of-death (2020).
- Lawton, J. S., et al. 2021 ACC/AHA/SCAI guideline for coronary artery revascularization: A report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol. 79 (2), e21-e129 (2022).
- Burton, T., et al. Development of a non-invasive machine-learned point-of-care rule-out test for coronary artery disease. Diagnostics. 14 (7), 719(2024).
- Stuckey, T. D., et al. Clinical validation of a machine-learned, point-of-care system to IDENTIFY functionally significant coronary artery disease. Diagnostics. 14 (10), 987(2024).
- Frank, E. An accurate, clinically practical system for spatial vectorcardiography. Circulation. 13 (5), 737-749 (1956).
- Park, J., Seok, H. S., Kim, S. S., Shin, H. Photoplethysmogram analysis and applications: An integrative review. Front Physiol. 12, 808451(2022).
- Montalescot, G., et al. 2013 ESC guidelines on the management of stable coronary artery disease: the Task Force on the management of stable coronary artery disease of the European Society of Cardiology. Eur Heart J. 34 (38), 2949-3003 (2013).
- Baratloo, A., Hosseini, M., Negida, A., El Ashal, G. Part 1: Simple definition and calculation of accuracy, sensitivity and specificity. Emergency. 3 (2), 48-49 (2015).
- Ranganathan, P., Aggarwal, R. Understanding the properties of diagnostic tests-Part 2: Likelihood ratios. Perspect Clin Res. 9 (2), 99-102 (2018).
- Douglas, P. S., et al. Outcomes of anatomical versus functional testing for coronary artery disease. New Eng J Med. 372 (14), 1291-1300 (2015).
- Safari, S., Baratloo, A., Elfil, M., Negida, A. Evidence based emergency medicine; part 4: Pre-test and post-test probabilities and Fagan's nomogram. Emergency. 4 (1), 48(2016).
- Knuuti, J., et al. The performance of non-invasive tests to rule-in and rule-out significant coronary artery stenosis in patients with stable angina: a meta-analysis focused on post-test disease probability. Eur Heart J. 39 (35), 3322-3330 (2018).
- Diamond, G. A., Forrester, J. S. Analysis of probability as an aid in the clinical diagnosis of coronary-artery disease. New Eng J Med. 300 (24), 1350-1358 (1979).
- Morise, A. P. Comparison of the Diamond-Forrester method and a new score to estimate the pre-test probability of coronary disease before exercise testing. Am Heart J. 138 (4), 740-745 (1999).
- Pelletier-Galarneau, M., Vandenbroucke, E., Lu, M., Li, O. Characteristics and key differences between patient populations receiving imaging modalities for coronary artery disease diagnosis in the US. BMC Cardiovasc Disord. 23 (1), 251(2023).
- Li, J., et al. Factors that impact a patient's experience when undergoing single-photon emission computed tomography myocardial perfusion imaging (SPECT-MPI) in the US: A survey of patients, imaging center staff, and physicians. J Nuclear Cardiol. 28 (4), 1507-1518 (2021).
- Lawton, J. S., et al. 2021 ACC/AHA/SCAI guideline for coronary artery revascularization: A report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol. 79, e21-e129 (2022).
- Aijaz, A., et al. Sociodemographic factors associated with outpatient radiology no-shows versus cancellations. Acad Radiol. S1076 - 6332 (24), 00228-00229 (2024).
- Cowper, P. A., et al. Acute and 1-year hospitalization costs for acute myocardial infarction treated with percutaneous coronary intervention: Results From the TRANSLATE-ACS registry. J Am Heart Assoc. 16 (8), 8(2019).
- Thomas, A., et al. Forgone medical care associated with increased health care costs among the U.S. heart failure population. JACC Heart Fail. 9 (10), 710-719 (2021).
- Reeves, R. A., Halpern, E. J., Rao, V. M. Cardiac imaging trends from 2010 to 2019 in the Medicare population. Radiol Cardiothorac Imaging. 3 (5), (2021).
- Pope, J. H., et al. Missed diagnoses of acute cardiac ischemia in the Emergency Department. New Eng J Med. 342 (16), 1163-1170 (2000).
- OʼSullivan, A. K., et al. Cost estimation of cardiovascular disease events in the US. Pharmacoeconomics. 29 (8), 693-704 (2011).
- Corso, A. Emergency visit cost with and without insurance in 2024. Mira. , https://www.talktomira.com/post/how-much-does-an-er-visit-cost (2024).
- Patel, M. R. Low diagnostic yield of elective coronary angiography. New Eng J Med. 362 (10), 886-895 (2010).
- Browning, S. CorVista System 510(k) Summary (K232686). , U.S. Food and Drug Administration. Retrieved from https://www.accessdata.fda.gov/cdrh_docs/pdf23/K232686.pdf (2024).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved