Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Speichel, Speicheldrüse, und Hämolymphe Abholung Ixodes scapularis Zecken
In diesem Artikel
Zusammenfassung
Die Sammlung von infizierten Zecke Hämolymphe, Speicheldrüsen, und Speichel ist wichtig, zu untersuchen, wie durch Zecken übertragene Erreger eine Krankheit verursachen. In diesem Protokoll haben wir demonstrieren, wie man Hämolymphe und Speicheldrüsen von der Fütterung sammeln Ixodes scapularis Nymphen. Wir zeigen auch, Speichel Sammlung von weiblichen I. scapularis Erwachsene.
Zusammenfassung
Zecken sind weltweit und plagen die Menschen mit vielen Zecken-übertragene Erkrankungen. Zecken sind Vektoren für Krankheitserreger, die Lyme-Borreliose und Frühsommer-Rückfallfieber (Borrelia spp.), Rocky Mountain Spotted Fever (Rickettsia rickettsii), Ehrlichiose (Ehrlichia chaffeensis und E. equi), Anaplasmose (Anaplasma phagocytophilum), Enzephalitis (tick-verursachen Meningo-Enzephalitis-Virus), Babesiose (Babesia spp.), Colorado Zeckenbissen (Coltivirus) und Tularämie (Francisella tularensis) 1-8. Um richtig in den Wirt übertragen werden diese Erreger unterschiedlich die Genexpression regulieren, interagieren mit Zecken-Proteine und wandern durch die Zecke 3,9-13. Zum Beispiel, passt sich die Lyme-Borreliose-Agent, Borrelia burgdorferi, durch differentiellen Genexpression zu dem Fest und Hungersnot Stadien der Zecke enzootischen Zyklus 14,15. Darüber hinaus verbraucht als ein Ixodes Zecken einBlutmehl Borrelia replizieren und wandern aus dem Mitteldarm in die Haemocoel, wohin sie wandern in die Speicheldrüsen und werden in den Wirt mit dem Speichel vertrieben 9,16-19 übertragen.
Wie eine Zecke führt der Host antwortet in der Regel mit einer starken hämostatischen und angeborene Immunantwort 11,13,20-22. Trotz dieser Wirtsreaktionen, I. scapularis kann für mehrere Tage zu ernähren, da Zecken Speichel enthält Proteine, die immunmodulatorische sind, lytische Mittel, Antikoagulanzien und fibrinolysins, die Zecke 3,11,20,21,23 Fütterung zu helfen. Die immunmodulatorischen Aktivitäten von Zeckenspeichel oder Speicheldrüsen-Extrakt (SGE) besessen zu erleichtern Übertragung, Vermehrung und Verbreitung von zahlreichen Zecken übertragenen Krankheitserregern 3,20,24-27. Um weiter zu verstehen, wie durch Zecken übertragene Erreger eine Krankheit verursachen es wichtig, aktiv zu sezieren Fütterung Zecken und sammeln Zeckenspeichel ist. Dieses Video demonstriert Protokoll Dissektion Techniken fürdie Sammlung von Hämolymphe und die Entfernung der Speicheldrüsen von der aktiven Zuführen I. scapularis Nymphen nach 48 und 72 Stunden nach der Platzierung der Maus. Wir zeigen auch, Speichel Kollektion von einer erwachsenen Frau I. scapularis tick.
Protokoll
1. Hämolymphe Sammlung der Präparation der Objektträger
(Movie 1)
- Vorsichtig entfernt aktiv Zuführen Zecken aus einem Tier und in 3% Wasserstoffperoxid topische für 5 Minuten und dann in 70% Ethanol für 10 Minuten an die Oberfläche zu sterilisieren.
- Mit einem Pap-Stift zeichnen Sie einen Kreis auf einem Silan beschichtete Objektträger und steckt die Zecke innerhalb der PAP PEN Kreis.
- Silan beschichtete Objektträger für die besten Einhaltung der Hämolymphe auf den Objektträger verwendet.
- Sehen Sie das Häkchen unter einem Binokular (1X Ziel, 10x Okular, 3,5 facher Vergrösserung).
- Drücken Sie vorsichtig auf der Zecke mit einer Pinzette zu Dorsum der Zecke die Beine spreizen und immobilisieren die Zecke.
Hinweis: Bei der Immobilisierung die Zecke nicht zu fest drücken, da dies die Punktion oder Mitteldarm der Zecke kann stören und verunreinigen das Hämolymphe.
- Amputieren der Zecke am Bein oder die Beine an the distale Gelenk mit einer feinen Spitze Einweg-Skalpell. Um die Infektiosität zu ermitteln via Hämolymphe nur ein Bein muss amputiert werden. Für Sammlung von Hämolymphe auf einer Folie mehrere Beine amputiert werden kann.
Hinweis: Schneiden Sie nicht das Bein zu nahe an den Körper, weil diese Mitteldarm Kontamination der Hämolymphe verursachen können.
- Nachdem das Bein oder die Beine abgeschnitten sind weiterhin üben Sie sanften Druck an der Zecke Dorsum für die Hämolymphe zur Sekretion aus den Beinen auf die Folie. Bewegen Sie das Häkchen um auf der Folie, um die Hämolymphe zu verbreiten.
2. Speicheldrüse Entfernung
(Filme 2 & 3)
- Spot 25 ul mehrere Pools von Phosphat-gepufferter Salzlösung (PBS) auf einen Objektträger und legen einen Haken in eine der PBS-Pools.
- Sehen Sie das Häkchen unter einem Binokular (1X Ziel, 10x Okular, 3,5 facher Vergrösserung).
- Stabilisieren Sie die Zecke mit feinen Spitzen forceps, indem Sie die Basis Capitulum (Mundwerkzeuge) oder den hinteren Teil der Zecke.
- Legen Sie die feinen Pinzetten in die hintere der Zecke und in Scheiben schneiden bis die Zecke ist Dorsum, um die Organe freizulegen. Falls gewünscht kann der Mitteldarm zu diesem Zeitpunkt entfernt werden und in ein frisches Pool von PBS auf einem Objektträger oder einem Mikrozentrifugenröhrchen mit PBS.
- Finden Sie das Paar Speicheldrüsen (Traube-wie Cluster) bilateral neben den Beinen der Zecke befinden. Wenn die Speicheldrüsen sind nicht unter die Zecke Trümmer bewegen Sie den wichtigsten Teil Tick, immer noch mit den Speicheldrüsen, in ein frisches Pool von PBS, um die Störung und Verlust der Speicheldrüsen reduzieren sichtbar.
Hinweis: Frühere in einer Fütterung sind die Speicheldrüsen schwieriger zu lokalisieren, weil sie nicht so weit entwickelt sind als im Vergleich zu einem späteren Zeitpunkt in der Fütterung.
- Entfernen Sie die Speicheldrüsen der Zecke aus mit feinen Pinzetten und in ein frisches Pool von PBS.
- With feinen Pinzetten übertragen Sie die Speicheldrüsen zu einem anderen sauberen 25 ul PBS-Pool, wiederholen Dieser Waschschritt 3-4 weitere Male, um alle externen Mikroorganismen und Zecken zu entfernen.
Hinweis: Waschen Sie die Speicheldrüse Cluster sanft, um den Verlust und die Störung der einzelnen Speicheldrüsen zu reduzieren.
- Platzieren Sie die Drüsen in einem sauberen Pool von PBS auf einem mit Silan beschichtete Folie oder in einem Mikrozentrifugenröhrchen mit PBS.
3. Speichelsammlung
(Movie 4)
- Entfernen Sie vorsichtig erwachsene weibliche Zecken aus dem Kaninchen oder anderen Host mit feinen Pinzetten, kurz bevor sie abfallen sich prall an, etwa 5-7 Tage nach der Befestigung.
- Beachten Sie die fast engorged Tick auf das eine Ende eines Objektträgers mit Tesafilm. Das Band sollte etwa platziert werden ¾ der Weg nach oben der Zecke Rücken in Richtung des Kopfes, so dass der Zecke Grundlage Capitulum (Mundwerkzeuge) ausgesetzt.
- Wo die Band den vorderen Rand der Zecken Dorsalfläche Pipette 5 ul 5% Pilocarpin-Lösung (in Methanol) erfüllt. Lassen Sie das Band, um das Pilocarpin über die Zecke Dorsum Docht, ohne dass das Pilocarpin in Kontakt mit der Zecke Grundlage Capitulum kommen.
- Bringen Sie ein Stück ungiftig Modelliermasse auf den Objektträger etwa einen Zoll von der Zecke Mundwerkzeuge.
- Mit feinen Pinzetten brechen Sie die Spitze eines beigezogenen Kapillarrohr 28 auf den gewünschten Durchmesser.
- Ansicht der Zecke Grundlage Capitulum unter einem Binokular.
- Sanften Sitz der Zecke Hypostom in die Kapillare gezogen so dass die oberen Palpen auf der Außenseite des Kapillarrohrs befinden.
- Drücken Sie die entgegengesetzten Ende des Kapillarrohrs in der Modelliermasse um das Kapillarrohr in Position zu halten.
- Stellen Sie das montierte salivating Zecke in einer dunklen Kammer mit hoher Luftfeuchtigkeit (z. B. ein Deckel Styroporbox mit nassen Brei gefüttert ER Handtücher). Drücken Sie den Träger so den Hypostom Punkten auf den Boden des Behälters, so dass die Schwerkraft beim Speichelprobe zu unterstützen.
- Stellen Sie den Behälter bei Raumtemperatur.
- Genau beobachten salivating Zecken für die erste Stunde, und sammeln Speichel, wie es durch Austreiben es aus der Kapillarröhrchen mit einer Pasteur-Pipette Glühbirne erzeugt wird. Nach der ersten Stunde, überprüfen Anhäufung jede Stunde für mindestens 4 Stunden. Weiter, um den Speichel, wie es erzeugt wird, zu sammeln.
Hinweis: Der Speichel Erwerb kann gestoppt werden, sobald genügend Speichel für die Prüfung durchgeführt wird, gesammelt werden.
- Wenn die Zecken sind nicht Speichelfluss oder wenn mehr Speichel benötigt wird, Speichelfluss kann gelegentlich mit der Kapillare eine Hypostom massieren induziert werden.
- Geben Sie 0,1 Volumina von Protease Inhibitor Cocktail auf die Speichel-und Speicher bei -80 ° C bis sie benötigt werden.
4. Repräsentative Ergebnisse
e_content "> Movie 1 veranschaulicht, wie eine nur teilweise eingezogenen I. scapularis Nymphe halten und die Beine amputieren, um Hämolymphe auf einen Objektträger zu sammeln. Sobald das Bein oder Beine amputiert werden eine klare Flüssigkeit abgesondert wird (Abbildung 1A und 1B). Wenn der Mitteldarm gebrochen wird die Hämolymphe erscheint trübe, wie es ist kommt aus dem amputierten Bein (e) (Abbildung 1C und 1D).Die Gewinnung von Speicheldrüsen nach der Nymphe hat sich für 48 oder 72 Stunden gefüttert wird in Filmen 2 und 3 gezeigt. Nachdem die Zecke punktiert wird es im Allgemeinen eine Menge Schutt (bestehend aus Luftröhre, Malpighischen Gefäße, Blut, Bindegewebe etc.) zu bewegen, um den Verlust oder die Störung der Speicheldrüsen der Zecke zu verhindern, um einen frischen Pool von PBS. 2A und 2B zeigen, wo die Speicheldrüsen befinden, nachdem die Nymphe aufgeschnittenen sind und 2C zeigt entfernt Speicheldrüse Cluster in einem Pool von PBS.
Speichelsammlung aus I festgelegt scapularis erwachsenen Weibchen i s in Film 4 und Abbildung 3 dargestellt. Ein Häkchen salivating in ein Kapillarrohr ist in Film 5 beobachtet. Diese Methode der Speichel-Auflistung verwendet, um den Speichelfluss anzuregen Pilocarpin und kann über 20 ul Speichel pro erwachsene weibliche Zecke liefern.
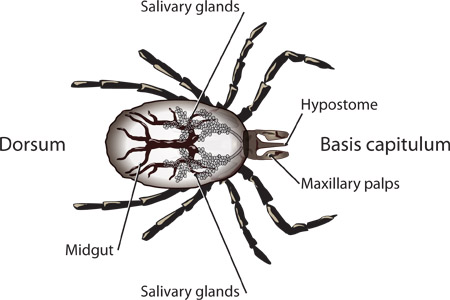
Abbildung 1. Markierten Strukturen einer I. scapularis Nymphe.
Movie 1. Ixodes scapularis Hämolymphe Sammlung. Hier klicken, um Film zu sehen .

Abbildung 2. Nicht kontaminierte (A & B) und verunreinigt (C & D) Hämolymphe exsudierenden von der Nymphe Bein.
Movie 2. Speicheldrüse Extraktion aus einem 48 Stunden gefüttert I. scapularis Nymphe.pload/3894/3894movie2.avi "> Klicken Sie hier, um Film zu sehen.
Movie 3. Speicheldrüse Extraktion aus einem 72 Stunden gefüttert I. scapularis Nymphe. Klicken Sie hier, um Film zu sehen .
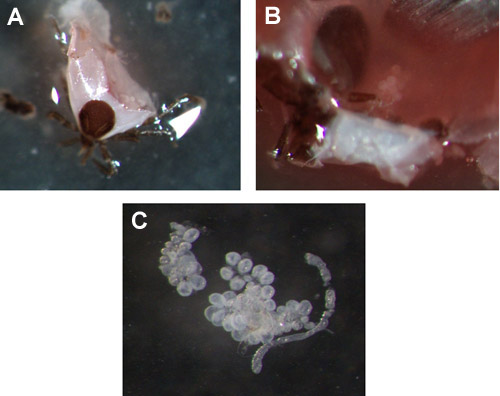
Abbildung 3. Ixodes scapularis Nymphe Speicheldrüsen. (A & B) Beispiele für Speicheldrüsen in 72 Stunden gefüttert Nymphe, vor der Extraktion. (C) entfernt Speicheldrüse Cluster.
Movie 4. Speichelsammlung up von einem erwachsenen I festgelegt scapularis weibliche Zecke. Klicken Sie hier, um Film zu sehen .

Abbildung 4. Speichelsammlung aus adulten I. scapularis weibliche tIcks. (A & B) Markieren auf einem Objektträger mit Hypostom in der ausgezogenen Ende des Kapillarröhrchens mit dem unpulled Ende des Kapillarrohrs durch Modelliermasse gehalten. (C & D) befeuchteten Kammer mit salivating erwachsenen I. scapularis weiblichen Zecken.
Movie 5. Ixodes scapularis weibliche Zecke salivating in ein Kapillarrohr. Klicken Sie hier, um Film zu sehen .
Diskussion
Die Sammlung von Zecken Hämolymphe, Speicheldrüsen, und Speichel ist in der Studie von Zecken übertragene Erreger Übertragung wichtig, Prävalenz, Verbreitung, Vermehrung und Persistenz sowohl in der Zecke und dem Host 6,11-13,20,23,29. Es gibt mehrere Möglichkeiten, um ein Häkchen 30,31 sezieren. Allerdings, wenn das Sammeln Speicheldrüsen ist es wichtig, die Zecke richtig, so dass die Speicheldrüsen nicht gebrochen oder verloren in der Zecke die Überreste zu sezieren. Sobald die Speichel...
Offenlegungen
Wir haben nichts zu offenbaren.
Danksagungen
Die Autoren möchten sich bei der Aufteilung des Vector-Borne Diseases Animal Resources Abteilung bedanken, speziell Andrea Peterson, Lisa Massoudi, Verna O'Brien, John Liddell und für ihre Pflege und Wartung der Mäuse und Kaninchen. Wir möchten auch an Amy Ullmann, Theresa Russell, und Barbara J. Johnson für ihre Beiträge zu diesem Manuskript danken. Schließlich möchten wir Alissa Eckert in das Amt des Associate Director für Kommunikation an der CDC anerkennen für die Herstellung der grafischen Darstellungen und Judy Lavelle zum Lenken alle Gesetzmäßigkeiten mit den Dreharbeiten zu dieser Handschrift verbunden.
Materialien
| Name | Company | Catalog Number | Comments |
| Reagens | Firma | Katalog-Nummer | |
| Wasserstoffperoxid | Fischer | H312-500 | |
| Ethanol | Acros | 61509-5000 | |
| PBS | Boston Bioproducts | BM-2205 | |
| Dumont feinen Pinzette (3C) | Fischer | NC9906085 | |
| Silan behandelten Objektträger | Bioworld | 42763007-1 | |
| Pap-pen | Bioworld | 21750008-1 | |
| Super-Frost Plus Objektträger | Fischer | 12-550-18 | |
| Pilocarpin | Sigma | P6503-5G | |
| Protease-Inhibitor-Cocktail | Sigma | P2714 | |
| Nr. 11 Einweg-Skalpell | Feder | 2975 # 11 | |
| Ungiftige Knetmasse | Fisher | S17307 | |
| Kapillarrohre | Chase Scientific Glass, inc. | 40A502 |
Referenzen
- Quach, K. A., Boctor, F. N., Elston, D. M. What's eating you? Hyalomma ticks. Cutis. 87, 165-167 (2011).
- Graham, J., Stockley, K., Goldman, R. D. Tick-borne illnesses: a CME update. Pediatr. Emerg. Care. 27, 141-147 (2011).
- Nuttall, P. A., Paesen, G. C., Lawrie, C. H., Wang, H. Vector-host interactions in disease transmission. J. Mol. Microbiol. Biotechnol. 2, 381-386 (2000).
- Estrada-Pena, A., Jongejan, F. Ticks feeding on humans: a review of records on human-biting Ixodoidea with special reference to pathogen transmission. Exp. Appl. Acarol. 23, 685-715 (1999).
- Nuttall, P. A. Pathogen-tick-host interactions: Borrelia burgdorferi and TBE virus. Zentralbl Bakteriol. 289, 492-505 (1999).
- Jones, L. D., Hodgson, E., Nuttall, P. A. Enhancement of virus transmission by tick salivary glands. J. Gen. Virol. 70, 1895-1898 (1989).
- Labuda, M., Nuttall, P. A. Tick-borne viruses. Parasitol. 129, 221-245 (2004).
- Socolovschi, C., Mediannikov, O., Raoult, D., Parola, P. Update on tick-borne bacterial diseases in Europe. Parasite. 16, 259-273 (2009).
- Zhang, L., et al. Molecular Interactions that Enable Movement of the Lyme Disease Agent from the Tick Gut into the Hemolymph. PLoS Pathog. 7, e1002079 (2011).
- Piesman, J., Schneider, B. S. Dynamic changes in Lyme disease spirochetes during transmission by nymphal ticks. Exp. Appl. Acarol. 28, 141-145 (2002).
- Brossard, M., Wikel, S. K. Tick immunobiology. Parasitol. , S161-S176 (2004).
- Machackova, M., Obornik, M., Kopecky, J. Effect of salivary gland extract from Ixodes ricinus ticks on the proliferation of Borrelia burgdorferi sensu stricto in vivo. Folia Parasitol. 53, 153-158 (2006).
- Nuttall, P. A., Labuda, M. Tick-host interactions: saliva-activated transmission. Parasitol. 129, 177-189 (2004).
- Anguita, J., Hedrick, M. N., Fikrig, E. Adaptation of Borrelia burgdorferi in the tick and the mammalian host. FEMS Microbiol. Rev. 27, 493-504 (2003).
- Hovius, J. W., van Dam, A. P., Fikrig, E. Tick-host-pathogen interactions in Lyme borreliosis. Trends Parasitol. 23, 434-438 (2007).
- Dunham-Ems, S. M., et al. Live imaging reveals a biphasic mode of dissemination of Borrelia burgdorferi within ticks. Journal Clin. Invest. 119, 3652-3665 (2009).
- Ribeiro, J. M., Mather, T. N., Piesman, J., Spielman, A. Dissemination and salivary delivery of Lyme disease spirochetes in vector ticks (Acari: Ixodidae). J. Med. Entomol. 24, 201-205 (1987).
- Piesman, J. Transmission of Lyme disease spirochetes (Borrelia burgdorferi. Exp. Appl. Acarol. 7, 71-80 (1989).
- De Silva, A. M., Fikrig, E. Growth and migration of Borrelia burgdorferi in Ixodes ticks during blood feeding. Am. J. Trop. Med. Hyg. 53, 397-404 (1995).
- Horka, H., Cerna-Kyckova, K., Skallova, A., Kopecky, J. Tick saliva affects both proliferation and distribution of Borrelia burgdorferi spirochetes in mouse organs and increases transmission of spirochetes to ticks. Int. J. Med. Microbiol. 299, 373-380 (2009).
- Brossard, M., Wikel, S. K. Immunology of interactions between ticks and hosts. Med. Vet. Entomol. 11, 270-276 (1997).
- Wikel, S. K. Tick modulation of host immunity: an important factor in pathogen transmission. Int. J. Parasitol. 29 (99), 851-859 (1999).
- Binnington, K. C., Kemp, D. H. Role of tick salivary glands in feeding and disease transmission. Adv. Parasitol. 18, 315-339 (1980).
- Guo, X., et al. Inhibition of neutrophil function by two tick salivary proteins. Infect. Immun. 77, 2320-2329 (2009).
- Montgomery, R. R., Lusitani, D., De Boisfleury Chevance, A., Malawista, S. E. Tick saliva reduces adherence and area of human neutrophils. Infect. Immun. 72, 2989-2994 (2004).
- Lima, C. M., et al. Differential infectivity of the Lyme disease spirochete Borrelia burgdorferi derived from Ixodes scapularis salivary glands and midgut. J. Med. Entomol. 42, 506-510 (2005).
- Severinova, J., et al. Co-inoculation of Borrelia afzelii with tick salivary gland extract influences distribution of immunocompetent cells in the skin and lymph nodes of mice. Folia Microbiol. 50, 457-463 (2005).
- Labuda, M., Jones, L. D., Williams, T., Nuttall, P. A. Enhancement of tick-borne encephalitis virus transmission by tick salivary gland extracts. Med. Vet. Entomol. 7, 193-196 (1993).
- Kariu, T., Coleman, A. S., Anderson, J. F., Pal, U. Methods for Rapid Transfer and Localization of Lyme Disease Pathogens Within the Tick Gut. J. Vis. Exp. (48), e2544 (2011).
- Edwards, K. T., Goddard, J., Varela-Stokes, A. S. Examination of the internal morphology of the Ixodid tick Amblyomma maculatum koch, (Acari:Ixodidae); a "How-to" pictorial dissection guide. Midsouth Entomologist. 2, 28-39 (2009).
- Ledin, K. E., et al. Borreliacidal activity of saliva of the tick Amblyomma americanum. Med. Vet. Entomol. 19, 90-95 (2005).
- Ribeiro, J. M., Zeidner, N. S., Ledin, K., Dolan, M. C., Mather, T. N. How much pilocarpine contaminates pilocarpine-induced tick saliva?. Med. Vet. Entomol. 18, 20-24 (2004).
- Barker, R. W., Burris, E., Sauer, J. R., Hair, J. A. Composition of tick oral secretions obtained by three different collection methods. J. Med. Entomol. 10, 198-201 (1973).
- Burgdorfer, W. Hemolymph test. A technique for detection of rickettsiae in ticks. Am. J. Trop. Med. Hyg. 19, 1010-1014 (1970).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten