Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
1,3,5-triphenylbenzol und Corannulene als Electron Receptors für Lithium solvatisierte Elektron-Lösungen
In diesem Artikel
Zusammenfassung
The authors report on conductivity studies carried out on lithium solvated electron solutions (LiSES) prepared using 1,3,5-triphenylbenzene (TPB) and corannulene as electron receptors.
Zusammenfassung
Die Autoren berichten über Leitfähigkeit Studien über Lithium solvatisierten Elektronen Lösungen (Lises) durchgeführt, hergestellt zwei Arten von polyzyklischen aromatischen Kohlenwasserstoffen (PAK) verwendet, nämlich 1,3,5-triphenylbenzol und Corannulen, als Elektronen-Rezeptoren. Die festen PAHs wurden zuerst in Tetrahydrofuran (THF) gelöst, um eine Lösung zu bilden. Metallisches Lithium wurde dann in diese PAH / THF-Lösungen aufgelöst entweder blau oder grünlich-blau-Lösungen zu liefern, die Farben, die das Vorhandensein von solvatisierten Elektronen sind. Leitfähigkeitsmessungen bei Umgebungstemperatur auf 1,3,5-Triphenylbenzol Basis Lises durchgeführt, bezeichnet mit Li x TPB (THF) 24,7 (x = 1, 2, 3, 4), zeigte eine Zunahme der Leitfähigkeit mit einer Zunahme von Li: PAH - Verhältnis von x = 1 bis 2. jedoch verringerte sich die Leitfähigkeit allmählich bei weiterem Erhöhen des Verhältnisses. Tatsächlich ist die Leitfähigkeit von Li x TPB (THF) 24,7 für x = 4 ist sogar niedriger als für x x Cor (THF) 247 (x = 1, 2, 3, 4, 5), lineare Beziehung zu negativen Steigungen zeigte ein metallisches Verhalten angibt , ähnlich wie Biphenyl und Naphthalin- Basis Lises.
Einleitung
Lithium solvatisierten Elektronen Lösungen (Lises) hergestellt unter Verwendung von einfachen zweikernigen polyaromatischen Kohlenwasserstoffen (PAH), wie Biphenyl und Naphthalin können potentiell als flüssige Anoden in Lithiumzellen refuelable 1-7 verwendet werden. In den Lises dienten diese einfachen PAH-Moleküle, wie die Elektronen Rezeptoren für solvatisierten Elektronen aus gelöstem metallischem Lithium.
Progressing aus diesen beiden Ringsystemen haben die Autoren da durch dann Leitfähigkeitsmessung Studien über Lises aus , die komplexer PAHs vorbereitet verwenden, beginnend mit der Gruppe von Cyclopenta-2,4-dienon Derivate 8. Diese PAKs sind größere PAKs (> zwei Benzolringe) und PAHs mit Substituenten in ihren aromatischen Ringen eingebaut. Ein größerer PAH-Molekül mit mehr als zwei Ringen wird erwartet, als entweder resultierende Biphenyl oder Naphthalin in Lises mit einer höheren Energiedichte damit mehr Lithiumatome pro Molekül PAH aufzunehmen. Das Ziel der EinfühSubstituenten in PAHs ing ist die PAH akzeptieren Elektronen leichter und stabiler geworden als Polyanionen in Lises zu machen.
Im Rahmen der laufenden Bemühungen Lises mit höherer Energiedichte zu entwickeln, dieses Papier auf die Charakterisierung von Lises aus Corannulen gemacht durch die Literaturverfahren 9 sowie 1,3,5-triphenylbenzol, synthetisiert TPB durch eine leicht modifizierte Literatur hergestellt berichten 10 . 1,3,5-Triphenylbenzol, wie in Figur 1 (1) gezeigt ist , kann mit zwei zusätzlichen Phenylringe an den Positionen 3 und 5 des selben Ring als Biphenylderivat klassifiziert werden. Da dieses Molekül vier Benzolringe hat, sollte es 4 Atome von Li pro Molekül Aufnahme, die und Naphthalin (<2,5 Mol-Äquivalente Lithium pro Molekül) mehr als für Biphenyl (in 0,5 M Lösung maximal 2,5 Mol-Äquivalente Li pro PAH) ist .
Corannulene ist ein Fünf-Ring PAH in eine Schüsselform angeordnet sind, wie in Abbildung 1 (2 gezeigt). Zabula et al. 11 haben die Durchführbarkeit des Auflösens metallisches Lithium in einer Lösung von Corannulen / Tetrahydrofuran (THF) zeigte eine Lösung mit fünf Li + -Ionen zwischen zwei stabilen Tetraanionen von Corannulen sandwichartig zu bilden.
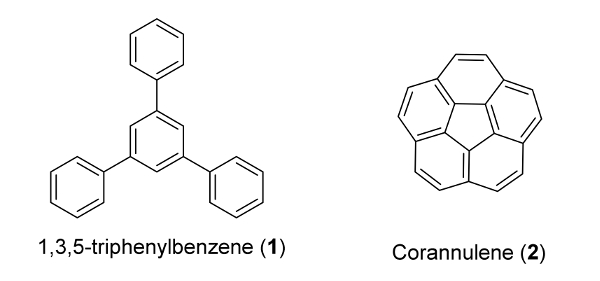
Abbildung 1: Die molekularen Strukturen von 1,3,5-Triphenylbenzol (1) und Corannulen (2) 1,3,5-Triphenylbenzol als biphenyl - Derivat mit zwei zusätzlichen Phenylringe an den Positionen 3 und 5 des gleichen Ring klassifiziert ist. . Corannulene ist ein Fünf-Ring PAH mit seinen fünf Benzolringen in eine Schüsselform angeordnet sind . Bitte hier klicken , um eine größere Version dieser Figur zu sehen.
Somit können sowohl 1,3,5-triphenylbenzol und Corannulen sind potentielle Kandidaten für eine hohe EnergieDichte Lises.
Protokoll
1. Herstellungsverfahren für 1,3,5-triphenylbenzol (1)
- Platzieren einer Mischung von Acetophenon (4,0 g, 33,3 mmol) und 100 ml absolutem Ethanol in einen Rundboden-Dreihals 250 ml Kolben, ausgestattet mit Magnetrührer, Rückflußkühler, Stickstoffeinlaß, einem Einleitungsrohr, Tropftrichter und Thermometer. Hinzufügen, Siliciumtetrachlorid (11,9 g, 8,0 ml, 70,2 mmol, 2,1 eq.) Zu dem Gemisch in einer Portion bei 0 ° C unter Stickstoff den Tropftrichter verwendet.
- Beobachten der Entwicklung von gasförmigem Chlorwasserstoff für 10 min. Dann rührt das Reaktionsgemisch bei 40 ° C für 20 Stunden.
- Abkühlen der Reaktionsmischung auf 23 ° C und gießen in 200 g Wasser mit Eis vermischt (1: 1 Massenverhältnis).
- Extrahieren der resultierenden Mischung mit Dichlormethan (2 x 100 ml) unter Verwendung eines Extraktionstrichter.
- Die vereinigten Extrakte werden einmal mit gesättigter NaCl - Lösung (100 ml) und trockne über 15 g wasserfreiem MgSO 4. Filtern Sie die Flüssigkeit Teil aus und dann konzentrieren unsing am Rotationsverdampfer.
- Reinige das Produkt durch Umkristallisation aus Ethanol (Auflösung in minimalen Menge Ethanol durch partielle Verdampfung des Lösungsmittels folgte, auf 6 ° C über Nacht gehalten, und schnelle Filtration) 2,2 g (Ausbeute 63%) von 1,3,5-Triphenylbenzol zu erhalten (1) als blaßgelbe Kristalle.
Note: 1 H-NMR (400 MHz, CDCl 3). Δ = 7.41 (m, 3H), 7,50 (m, 6H), 7,72 (d, 6H, J = 7,33 Hz), 7,80 (s, 3H) 13 C-NMR (400 MHz, CDCl 3): δ = 125.21, 127.39, 127.57, 128.88, 141.18, 142.38.
2. Lises Vorbereitet mit 1,3,5-triphenylbenzol
- Herstellung von 1,3,5-Triphenylbenzol Basis Lises
HINWEIS: 1,3,5-triphenylbenzol in diesem Papier verwendet wurde wie im oben beschriebenen Verfahren synthetisiert. Die 1,3,5-triphenylbenzol -basierte Lises durch Li bezeichnet x TPB (THF) 24,7 x zeigt die Li bezeichnet: PAH - Molverhältnis und TPB bezeichnet 1,3,5-triphenylbenzol. bereiten Lix TPB (THF) 24.7 innerhalb einer mit Argon gefüllten Handschuhbox bei Raumtemperatur über die folgenden Schritte:- Abmessen gut definierte Mengen von metallischem Li, THF und TPB separat innerhalb der Glovebox die Ziel molare Zusammensetzung von Li x TPB (THF) 24,7 für x = 1, 2, 3 und 4. Mit 41,6 mg, 83,3 mg zu erreichen, 124,9 mg, 166,6 mg von Li für x = 1, 2, 3 bzw. 4.
- Für jede der vier Lises Proben vorbereitet werden, innerhalb von vier separaten Glasflaschen in 12 ml THF 1,84 g TPB auflösen für jede Flasche 12 ml farblose Lösungen von TPB (THF) 24.7 zu bilden. Verwenden Sie ein 0,5 M 1,3,5-triphenylbenzol in allen Lösungen.
- Die abgewogene metallischen Li zu den vier Flaschen Folien und versiegeln Sie die Flaschen mit Parafilm.
- Rühren Sie die Mischung in jeder Flasche über Nacht ein glasbeschichteten Magnetrührer mit der vollständigen Auflösung von metallischem Li zu gewährleisten.
- Leitfähigkeitsmessungen
- Tragenaus alle Messungen Leitfähigkeit eine Standard-Leitfähigkeitszelle Sonde auf der Basis der Vier-Elektroden-Technik. Bringen Sie die Zelle Sonde zu einem Meter. Die Sonde hat eine sekundäre Funktion der Lösung, die Temperatur in der gleichen Zeit und zeigen beide Leitfähigkeit und Temperaturmessungen zu messen.
- Vor der Messungen zu kalibrieren das Messgerät 50 ml Standard 0,01 M wässrige KCl-Lösung durch die Leitfähigkeitssonde des Herstellers außerhalb der Glovebox zur Verfügung gestellt werden.
- Führen Sie alle Leitfähigkeitsmessungen für 1,3,5-triphenylbenzol-basierte Lises, Li x TPB (THF) 24,7 für x = 1, 2, 3, 4 in der Glovebox.
- Für jede dieser Lises, die Probe in einen kurzen Glaszylinder ausgießen und die Sonde in die Lösung eintauchen. Zeichnen Sie die Leitfähigkeitsmessung über einen Zeitraum von ein bis zwei Stunden, bis jede Probe wieder auf Umgebungstemperatur. Die Zeit für jede Probe genommen auf Umgebungstemperatur zurückkehren von ~ 1-2 Stunden. Die Sonde wkrank bleiben in der Probe für die gesamte Dauer der Leitfähigkeitsmessung eingetaucht.
3. Corannulene
- Herstellung von Corannulen-basierten Lises
. HINWEIS: Der Corannulen in diesem Papier verwendet wurde , an der School of Physical synthetisiert und mathematischen Wissenschaften, NTU ein mehrstufiges Literaturverfahren unter Verwendung von 9 Die Corannulen-basierten Lises durch Li bezeichnet x Cor (THF) 247 , wobei x bezeichnet die Li: PAH Molaren Verhältnis und Cor bezeichnet die Corannulen. Bereiten Li x Cor (THF) 247 innerhalb einer mit Argon gefüllten Handschuhbox bei Raumtemperatur über die folgenden Schritte:- Abmessen gut definierte Mengen von metallischem Li, THF und Cor separat innerhalb der Glovebox die Ziel molare Zusammensetzung zu erreichen von Li x Cor (THF) 247 für x = 1, 2, 3, 4 und 5. Mit 4,2 mg, 8,3 mg, 12,5 mg, 16,6 mg und 20,8 mg von Li für x = 1, 2, 3, 4 bzw. 5.
- Next, für jeden der fünf Lises Proben (x = 1, 2, 3, 4 und 5) hergestellt werden soll, 0,15 g Cor innerhalb fünf separaten Glasflaschen in 12 ml THF lösen sich 12 ml einer farblosen Lösung von Cor zu bilden (THF) 247 in jeder Flasche. Verwenden Sie eine Corannulen Konzentration von 0,05 M).
- Als nächstes fügen Sie die gewogen metallischen Li zu den fünf Flaschen Cor (THF) 247 und versiegeln Sie die Flaschen mit Parafilm - Folien.
- Rühren Sie die Mischung in jeder Flasche über Nacht ein glasbeschichteten Magnetrührer unter Verwendung der vollständigen Auflösung des metallischen Lithiums zu gewährleisten.
- Leitfähigkeitsmessungen
- Für Leitfähigkeit in Abhängigkeit von Temperaturmessungen, entfernen Sie jede der fünf Flaschen mit Li x Cor (THF) 247 für x = 1, 2, 3, 4 und 5 einzeln aus der Glovebox, wickeln Sie es mit einer zusätzlichen Schicht aus para-Film und tauchen innerhalb einer isolierten Styropor-Behälter mit Trockeneis gefüllt.
HINWEIS: Die Lises Proben kam nicht in Fortsetzungwirken entweder mit Feuchtigkeit oder Sauerstoff, während außerhalb der Glovebox, weil die Flaschen versiegelt wurden. - Kühlen Sie jede Flasche bis auf etwa 10 ° C durch jede Flasche für etwa 30 Minuten in dem Trockeneis eingetaucht zu halten, bevor sie wieder in die Glovebox für Leitfähigkeitsmessungen übertragen werden.
- Spülen Sie die Vorkammer des Glovebox mindestens 5-mal für jede Probe gekühlt, um sicherzustellen, dass keine Spuren von Kondenswasser die Flasche zurück in die Glovebox begleiten.
- Ähnlich der Art , in der Leitfähigkeit in Abhängigkeit von Temperaturmessungen für Naphthalin basierenden Lises Proben 1 gesammelt wurden, zu messen , die Leitfähigkeit des Li x Cor (THF) 247 (x = 1, 2, 3, 4, 5) über einen Zeitraum von ein bis 2 Stunden, bis jede Probe wieder auf Umgebungstemperatur. Die Sonde bleibt in der Probe für die gesamte Dauer der Leitfähigkeitsmessung eingetaucht.
- Für Leitfähigkeit in Abhängigkeit von Temperaturmessungen, entfernen Sie jede der fünf Flaschen mit Li x Cor (THF) 247 für x = 1, 2, 3, 4 und 5 einzeln aus der Glovebox, wickeln Sie es mit einer zusätzlichen Schicht aus para-Film und tauchen innerhalb einer isolierten Styropor-Behälter mit Trockeneis gefüllt.
Ergebnisse
Die Reaktion zwischen verschiedenen Mengen von Lithium und Mischungen von 1,3,5-triphenylbenzol mit THF gibt grünlichblau oder tiefblau gefärbte Lösungen , wie in Abbildung 2 dargestellt. Eine helle Farbe anzeigt , dass die jeweilige Probe von Lises eine geringe Konzentration an gelösten Elektronen hat. 1,3,5-Triphenylbenzol zeigt Erhöhung der Leitfähigkeit mit einer Zunahme von Li: PAH - Verhältnis von 1 bis 2 in 0,5 M THF - Lösung (Tabelle 1). Jedoch nimmt Leitfähigkeitswert ...
Diskussion
Für die 1,3,5-Triphenylbenzol Basis Lises, eine Probe mit einer hellen Farbe zeigt, dass es eine geringe Konzentration solvatisierter Elektronen aufweist. Li x TPB (THF) 24.7 (für x = 1, 2, 3, 4) , die ein Verhalten in seiner Leitfähigkeit in Abhängigkeit von x zeigt ähnlich zu für Lises aus Biphenyl und Naphthalin 1, 2 .Es ist eine anfängliche Erhöhung der Leitfähigkeit gesehen mit Erhöhung von Li: PAH - Verhältnis von 1 bis 2 und eine anschließende Abnahme der Leit...
Offenlegungen
Die Autoren haben nichts zu offenbaren.
Danksagungen
Die Autoren erkennen an Mitteln aus dem Singapur Ministerium für Bildung Tier-2-Forschungsfonds (Projekt MOE2013-T2-2-002) für dieses Projekt.
Materialien
| Name | Company | Catalog Number | Comments |
| Tetrahydrofuran Anhydrous, ≥99.9%, Inhibitor-free | Sigma Aldrich | 401757-100ML | |
| Lithium Foil | Alfa Aesar | 010769.14 | |
| Cond 3310 Conductivity Meter | WTW | Not Applicable | |
| 1,3,5-triphenylbenzene | Synthesized from acetophenone according to procedure described in literature | ||
| Silicon tetrachloride | Sigma Aldrich | 215120-100G | |
| acetophenone | TCI | A0061-500g | |
| Ethanol | Merck Millipore | 1.00983.2511 | |
| Corannulene | Synthesized by literature procedure |
Referenzen
- Tan, K. S., Yazami, R. Physical-Chemical and Electrochemical Studies of the Lithium Naphthalenide Anolyte. Electrochim Acta. 180, 629-635 (2015).
- Tan, K. S., Grimsdale, A. C., Yazami, R. Synthesis and Characterisation of Biphenyl-Based Lithium Solvated Electrons Solutions. J Phys Chem B. 116, 9056-9060 (2012).
- Rinaldi, A., Tan, K. S., Wijaya, O., Wang, Y., Yazami, R., Menictas, C., Skyllas-Kazacos, M., Lim, T. M., Hughes, S. Ch. 11. Advances in batteries for large- and medium-scale energy storage applications in power systems and electric vehicles. , (2014).
- Wang, Y., Tan, K. S., Yazami, R. . Materials Challenges In Alternative & Renewable Energy (MCARE 2014). , (2014).
- Yazami, R., Tan, K. S. . in 8th annual Li Battery Power. , (2012).
- Yazami, R. Hybrid Electrochemical Generator With A Soluble Anode. US patent. , (2010).
- Yazami, R., Tan, K. S. Liquid Metal Battery. US patent. , (2015).
- Lim, Z. B., et al. Synthesis and assessment of new cyclopenta-2,4-dienone derivatives for energy storage applications. Synthetic Met. 200, 85-90 (2015).
- Butterfield, A. M., Gilomen, B., Siegel, J. S. Kilogram-Scale Production of Corannulene. Org. Process Res. Dev. 16, 664-676 (2012).
- Elmorsy, S. S., Pelter, A., Smith, K. The direct production of tri- and hexa-substituted benzenes from ketones under mild conditions. Tetrahedron Lett. 32, 4175-4176 (1991).
- Zabula, A. V., Filatov, A. S., Spisak, S. N., Rogachev, A. Y., Petrukhina, M. A. A Main Group Metal Sandwich: Five Lithium Cations Jammed Between Two Corannulene Tetraanion Decks. Science. 333, 1008-1011 (2011).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten