Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
1,3,5-triphénylbenzène et corannulène comme Electron Receptors pour lithium solvatés Electron Solutions
Dans cet article
Résumé
The authors report on conductivity studies carried out on lithium solvated electron solutions (LiSES) prepared using 1,3,5-triphenylbenzene (TPB) and corannulene as electron receptors.
Résumé
Les auteurs rapportent des études de conductivité effectuées sur des solutions électroniques de lithium solvaté (Lises) préparés en utilisant deux types d'hydrocarbures aromatiques polycycliques (HAP), à savoir le 1,3,5-triphénylbenzène et corannulène, en tant que récepteurs d'électrons. HAP solides ont été d'abord dissous dans le tétrahydrofuranne (THF) pour former une solution. Le lithium métallique est ensuite dissous dans ces solutions HAP / de THF pour donner soit des solutions bleu ou bleu verdâtre, des couleurs qui indiquent la présence d'électrons solvatés. Les mesures de conductivité à température ambiante réalisée sur la base lises 1,3,5-triphénylbenzène, représenté par Li x TPB (THF) 24.7 (x = 1, 2, 3, 4), a montré une augmentation de la conductivité avec une augmentation de Li: HAP rapport de x = 1 à 2. Toutefois, la conductivité a diminué progressivement lorsqu'on augmente encore le rapport. En effet , la conductivité de Li x TPB (THF) , 24,7 pour x = 4 est encore plus faible que pour x x Co (THF) 247 (x = 1, 2, 3, 4, 5), ont montré une relation linéaire à pente négative, indiquant un comportement métallique semblable à biphényle et naphtalène- Lises base.
Introduction
Solutions d'électrons solvatés au lithium (de Lises) préparés en utilisant des hydrocarbures simples à deux anneaux aromatiques polycycliques (HAP) , tels que le biphényle et le naphtalène peuvent potentiellement être utilisés comme anodes liquides dans les cellules au lithium ravitaillée 1-7. Dans les lises, ces molécules de HAP simples servis que les récepteurs d'électrons pour les électrons solvatés de lithium métallique dissous.
Progresser à partir de ces systèmes à deux cycles, les auteurs ont depuis effectué des études de mesure de conductivité sur Lises qui sont préparés en utilisant des HAP plus complexes, en commençant par le groupe de dérivés cyclopenta-2,4-diénone 8. Ces HAP comprennent des HAP plus grandes (> deux anneaux de benzène) et des HAP avec des substituants incorporés dans leurs cycles aromatiques. Une molécule d'HTAP plus grande avec plus de deux cycles est prévu pour accueillir plus d'atomes de lithium par molécule de HAP que soit biphényle ou naphtalène, entraînant ainsi lises avec une densité d'énergie plus élevée. L'objectif de introduction des substituants en HAP est de rendre le PAH accepter des électrons plus facilement et devenir plus stable que polyanions dans Lises.
Dans le cadre des efforts continus pour développer Lises avec une densité d'énergie plus élevée, ce document fera rapport sur la caractérisation des Lises préparés à partir de corannulène faite par la procédure de la littérature 9 ainsi que le 1,3,5-triphénylbenzène, TPB synthétisé par une littérature légèrement modifiée 10 . 1,3,5-triphénylbenzène, comme représenté sur la figure 1 (1), peut être considéré comme un dérivé de biphényle avec deux noyaux phényle supplémentaires au niveau des positions 3 et 5 de la même bague. Etant donné que cette molécule possède quatre noyaux benzéniques, il faut absorption 4 atomes de Li par molécule, ce qui est plus que pour biphényle (maximum 2,5 équivalents molaires de Li par HAP dans 0,5 M de solution) et le naphtalène (<2,5 équivalents molaires de lithium par molécule) .
Corannulène est un cinq anneaux PAH disposés en forme de bol comme le montre la figure 1 (2). Zabula et al. , 11 ont démontré la faisabilité de la dissolution de lithium métallique dans une solution de corannulène / tétrahydrofuranne (THF) pour former une solution avec cinq ions Li + en sandwich entre deux tétra - anions stables corannulène.
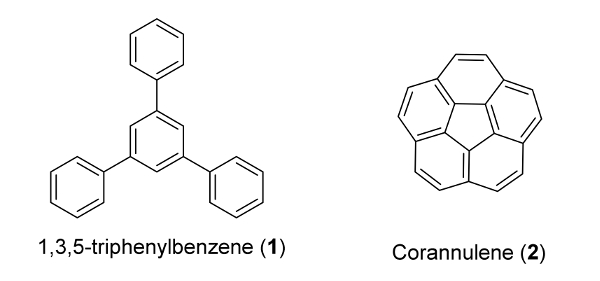
Figure 1: Les structures moléculaires de 1,3,5-triphénylbenzène (1) et corannulène (2) 1,3,5-triphénylbenzène est classé comme un dérivé de biphényle avec deux noyaux phényle supplémentaires aux positions 3 et 5 du même cycle. . Corannulène est un PAH cinq anneaux avec ses cinq anneaux de benzène disposés en forme de bol. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
Ainsi, à la fois 1,3,5-triphénylbenzène et corannulène sont des candidats potentiels pour haute énergieLises densité.
Protocole
1. Procédure Préparation de 1,3,5-triphénylbenzène (1)
- Placer un mélange de l'acétophénone (4,0 g, 33,3 mmol) et de 100 ml d'éthanol absolu dans un fond à trois cols de 250 ml ballon équipé d'un agitateur magnétique, d'un condenseur à reflux, d'une entrée d'azote, d'un bulleur, d'un thermomètre et d'une ampoule à brome. Ajouter du tétrachlorure de silicium (11,9 g, 8,0 ml, 70,2 mmol, 2,1 éq.) Au mélange en une portion à 0 ° C sous atmosphère d'azote en utilisant l'entonnoir à robinet.
- Observer l'évolution du chlorure d'hydrogène gazeux pendant 10 min. Incorporer ensuite le mélange réactionnel à 40 ° C pendant 20 heures.
- Refroidir le mélange réactionnel à 23 ° C et verser dans 200 g d'eau mélangée avec de la glace (1: 1 ratio de masse).
- On extrait le mélange résultant avec du dichlorométhane (2 x 100 ml) en utilisant un entonnoir d'extraction.
- Laver les extraits combinés une fois avec une solution saturée de NaCl (100 ml) et on sèche sur 15 g de MgSO4 anhydre. Filtrez la partie liquide hors tension, puis nous concentrering un évaporateur rotatif.
- On purifie le produit par recristallisation à partir d'éthanol (dissolution dans une quantité minimale d'éthanol, suivie d'une évaporation partielle du solvant, en gardant à 6 ° C pendant une nuit et une filtration rapide) pour obtenir 2,2 g (rendement 63%) de 1,3,5-triphénylbenzène (1) sous forme de cristaux jaune pâle.
Note: 1 H-RMN (400 MHz, CDCl 3):. Δ = 7,41 (m, 3H), 7,50 (m, 6H), 7,72 (d, 6H, J = 7.33Hz), 7,80 (s, 3H) 13 C-RMN (400 MHz, CDCl 3): δ = 125,21, 127,39, 127,57, 128,88, 141,18, 142,38.
2. Lises Préparé avec 1,3,5-triphénylbenzène
- Préparation du 1,3,5-triphénylbenzène à base lises
NOTE: 1,3,5-triphénylbenzène utilisé dans le présent document a été synthétisé conformément à la procédure décrite ci-dessus. Les Lises à base de 1,3,5-triphénylbenzène sont désignés par Li x TPB (THF) 24,7 x désigne le Li: rapport molaire PAH et TPB désigne 1,3,5-triphénylbenzène. Préparer Lix TPB (THF) à l' intérieur d' une boîte à gants 24.7 rempli d'argon à température ambiante par les étapes suivantes:- Mesurer des quantités bien définies d' éléments métalliques Li, le THF et le TPB séparément à l' intérieur de la boîte à gants pour obtenir la composition molaire cible de Li x TPB (THF) , 24,7 pour x = 1, 2, 3 et 4. Utilisation 41,6 mg, 83,3 mg, 124,9 mg, 166,6 mg de Li pour x = 1, 2, 3 et 4, respectivement.
- Pour chacun des quatre échantillons de lises à préparer, on dissout 1,84 g de TPB dans 12 ml de THF à l' intérieur de quatre bouteilles en verre séparées pour former 12 ml de solutions incolores de TPB (THF) 24.7 pour chaque bouteille. Utilisez un M 1,3,5-triphénylbenzène 0,5 dans toutes les solutions.
- Ajouter le métal pesé Li foils aux quatre bouteilles et sceller les bouteilles avec Parafilm.
- On agite le mélange pendant une nuit dans chaque bouteille à l'aide d'un agitateur magnétique revêtu de verre pour assurer la dissolution complète du Li métallique.
- Mesures de conductivité
- Portertoutes les mesures de conductivité en utilisant une sonde de conductivité de la cellule standard basée sur la technique à quatre électrodes. Attacher la sonde de la cellule à un mètre. La sonde a une fonction secondaire pour mesurer la température de la solution en même temps et afficher à la fois des mesures de conductivité et de température.
- Avant les mesures, étalonner l'appareil en utilisant 50 ml de solution standard 0,01 M KCl aqueuse fournies par le fabricant de la sonde de conductivité en dehors de la boîte à gants.
- Effectuer toutes les mesures de conductivité pour Lises à base de 1,3,5-triphénylbenzène, Li x TPB (THF) 24,7 pour x = 1, 2, 3, 4 à l' intérieur de la boîte à gants.
- Pour chacun de ces Lises, versez l'échantillon dans un cylindre de verre court et immerger la sonde dans la solution. Notez la mesure de la conductivité sur une période d'une à deux heures jusqu'à ce que chaque échantillon retourne à une température ambiante. Le temps pris pour chaque échantillon revenir à la température ambiante est d'environ 1-2 heures. La sonde wrestent mal immergé dans l'échantillon pendant toute la durée de la mesure de la conductivité.
3. corannulène
- Préparation de Lises base corannulène-
NOTE:. Le corannulène utilisé dans le présent document a été synthétisé à l'École des sciences physiques et mathématiques, NTU en utilisant un procédé de la littérature en plusieurs étapes 9 Les Lises basée corannulène-sont désignés par Li x Co (THF) 247 où x désigne la Li: molaire PAH rapport et Cor désigne le corannulène. Préparer Li x Co (THF) 247 l' intérieur d' une boîte à gants remplie d'argon à température ambiante via les étapes suivantes:- Mesurer des quantités bien définies d' éléments métalliques Li, THF et Co séparément à l' intérieur de la boîte à gants pour obtenir la composition cible molaire de Li x Co (THF) 247 pour x = 1, 2, 3, 4 et 5. Utilisation de 4,2 mg, 8,3 mg, 12,5 mg, 16,6 mg et 20,8 mg de Li pour x = 1, 2, 3, 4 et 5 respectivement.
- Next, pour chacune des cinq lises échantillons (x = 1, 2, 3, 4 et 5) d'être préparé, on dissout 0,15 g de Co dans 12 ml de THF à l' intérieur de cinq bouteilles de verre séparées pour former 12 ml d' une solution incolore de Cor (THF) 247 dans chaque bouteille. Utilisez une concentration de corannulène de 0,05 M).
- Ensuite, ajouter le métal pesé Li foils aux cinq bouteilles de Cor (THF) 247 et sceller les bouteilles avec Parafilm.
- On agite le mélange pendant une nuit dans chaque bouteille à l'aide d'un agitateur magnétique revêtu de verre pour assurer la dissolution complète du lithium métallique.
- Mesures de conductivité
- Pour la conductivité en fonction des mesures de température, retirer chacune des cinq bouteilles contenant Li x Co (THF) 247 pour x = 1, 2, 3, 4 et 5 individuellement à partir de la boîte à gants, l' envelopper avec une couche supplémentaire de para-film et de le plonger l'intérieur d'un conteneur en polystyrène isolé rempli de glace sèche.
NOTE: Les échantillons de Lises ne sont entrés en contagir soit avec l'humidité ou d'oxygène tout en dehors de la boîte à gants, car les bouteilles ont été scellées. - Refroidir chaque bouteille à environ 10 ° C en gardant chaque bouteille immergé dans la glace sèche pendant environ 30 minutes avant d'être transféré de nouveau dans la boîte à gants pour les mesures de conductivité.
- Purger l'antichambre de la boîte à gants au moins 5 fois pour chaque échantillon refroidi pour assurer qu'il n'y a pas de traces d'eau de condensation accompagnent la bouteille dans la boîte à gants.
- Semblable à la manière dont la conductivité en fonction des mesures de température ont été recueillies pour lises naphtaléniques échantillons 1, mesurer la conductivité du Li x Co (THF) 247 (x = 1, 2, 3, 4, 5) sur une période d'une à deux heures jusqu'à ce que chaque échantillon retourné à la température ambiante. La sonde reste immergée dans l'échantillon pendant toute la durée de la mesure de la conductivité.
- Pour la conductivité en fonction des mesures de température, retirer chacune des cinq bouteilles contenant Li x Co (THF) 247 pour x = 1, 2, 3, 4 et 5 individuellement à partir de la boîte à gants, l' envelopper avec une couche supplémentaire de para-film et de le plonger l'intérieur d'un conteneur en polystyrène isolé rempli de glace sèche.
Résultats
La réaction entre les différentes quantités de lithium et des mélanges de 1,3,5-triphénylbenzène avec du THF donne des solutions colorées en bleu ou bleu verdâtre profond , comme illustré sur la figure 2. Une couleur claire indique que l'échantillon particulier lises a une faible concentration en électrons solvatés. 1,3,5-triphénylbenzène montre augmentation de la conductivité avec une augmentation du rapport Li: HAP 1 à 2 dans une solution de THF 0,5 M (Tableau 1). ...
Discussion
Pour les lises à base de 1,3,5-triphénylbenzène, un échantillon avec une lumière de couleur montre qu'il a une faible concentration d'électrons solvatés. Li x TPB (THF) 24.7 (pour x = 1, 2, 3, 4) montre un comportement de sa conductivité par rapport à x semblable à celle observée pour les lises à base de biphényle et naphtalène 1, 2 .Il est une augmentation initiale de la conductivité avec augmentation du rapport Li: HPA 1-2 et une diminution subséquente ...
Déclarations de divulgation
Les auteurs n'ont rien à dévoiler.
Remerciements
Les auteurs reconnaissent le financement du ministère de l'Éducation du Fonds de recherche de niveau 2 Singapour (projet MOE2013-T2-2-002) pour ce projet.
matériels
| Name | Company | Catalog Number | Comments |
| Tetrahydrofuran Anhydrous, ≥99.9%, Inhibitor-free | Sigma Aldrich | 401757-100ML | |
| Lithium Foil | Alfa Aesar | 010769.14 | |
| Cond 3310 Conductivity Meter | WTW | Not Applicable | |
| 1,3,5-triphenylbenzene | Synthesized from acetophenone according to procedure described in literature | ||
| Silicon tetrachloride | Sigma Aldrich | 215120-100G | |
| acetophenone | TCI | A0061-500g | |
| Ethanol | Merck Millipore | 1.00983.2511 | |
| Corannulene | Synthesized by literature procedure |
Références
- Tan, K. S., Yazami, R. Physical-Chemical and Electrochemical Studies of the Lithium Naphthalenide Anolyte. Electrochim Acta. 180, 629-635 (2015).
- Tan, K. S., Grimsdale, A. C., Yazami, R. Synthesis and Characterisation of Biphenyl-Based Lithium Solvated Electrons Solutions. J Phys Chem B. 116, 9056-9060 (2012).
- Rinaldi, A., Tan, K. S., Wijaya, O., Wang, Y., Yazami, R., Menictas, C., Skyllas-Kazacos, M., Lim, T. M., Hughes, S. Ch. 11. Advances in batteries for large- and medium-scale energy storage applications in power systems and electric vehicles. , (2014).
- Wang, Y., Tan, K. S., Yazami, R. . Materials Challenges In Alternative & Renewable Energy (MCARE 2014). , (2014).
- Yazami, R., Tan, K. S. . in 8th annual Li Battery Power. , (2012).
- Yazami, R. Hybrid Electrochemical Generator With A Soluble Anode. US patent. , (2010).
- Yazami, R., Tan, K. S. Liquid Metal Battery. US patent. , (2015).
- Lim, Z. B., et al. Synthesis and assessment of new cyclopenta-2,4-dienone derivatives for energy storage applications. Synthetic Met. 200, 85-90 (2015).
- Butterfield, A. M., Gilomen, B., Siegel, J. S. Kilogram-Scale Production of Corannulene. Org. Process Res. Dev. 16, 664-676 (2012).
- Elmorsy, S. S., Pelter, A., Smith, K. The direct production of tri- and hexa-substituted benzenes from ketones under mild conditions. Tetrahedron Lett. 32, 4175-4176 (1991).
- Zabula, A. V., Filatov, A. S., Spisak, S. N., Rogachev, A. Y., Petrukhina, M. A. A Main Group Metal Sandwich: Five Lithium Cations Jammed Between Two Corannulene Tetraanion Decks. Science. 333, 1008-1011 (2011).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon