Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Herstellung von expandierten Chitinschäumen und deren Verwendung bei der Entfernung von bässrigem Kupfer
In diesem Artikel
Zusammenfassung
Diese Studie beschreibt eine Methode, um Chitin durch chemische Techniken, die keine spezielle Ausrüstung erfordern, zu einem Schaum zu erweitern.
Zusammenfassung
Chitin ist ein wenig genutztes, natürlich reichlich vorhandenes, mechanisch robustes und chemisch beständiges Biopolymer. Diese Eigenschaften sind in einem Adsorbens wünschenswert, aber Chitin fehlt die notwendige spezifische Oberfläche, und seine Modifikation erfordert spezielle Techniken und Ausrüstung. Hierin wird ein neuartiges chemisches Verfahren zur Ausdehnung von Chitinflocken, die aus Garnelenschalenabfällen gewonnen werden, zu Schäumen mit höherer Oberfläche beschrieben. Der Prozess beruht auf der Entwicklung vonH2-Gas aus der Reaktion von Wasser mit NaH, das in einem Chitingel eingeschlossen ist. Die Zubereitungsmethode erfordert keine spezielle Ausrüstung. Pulverröntgenbeugung undN2-Physisorption deuten darauf hin, dass die Kristallitgröße von 6,6 nm auf 4,4 nm abnimmt und die spezifische Oberfläche von 12,6 ± 2,1m2/gauf 73,9 ± 0,2m2/gzunimmt. Infrarotspektroskopie und thermogravimetrische Analysen zeigen jedoch, dass der Prozess die chemische Identität des Chitins nicht verändert. Die spezifische Cu-Adsorptionskapazität des expandierten Chitins erhöht sich proportional zur spezifischen Oberfläche von 13,8 ± 2,9 mg/g auf 73,1 ± 2,0 mg/g. Die Cu-Adsorptionskapazität als Oberflächendichte bleibt jedoch relativ konstant bei durchschnittlich 10,1 ±0,8 Atom/nm2 , was wiederum auf keine Veränderung der chemischen Identität des Chitins hindeutet. Diese Methode bietet die Möglichkeit, Chitin in ein Material mit höherer Oberfläche umzuwandeln, ohne seine wünschenswerten Eigenschaften zu beeinträchtigen. Obwohl der Chitinschaum hier als Adsorbens beschrieben wird, kann man ihn sich als Katalysatorträger, Wärmeisolator und Strukturmaterial vorstellen.
Einleitung
Chitin ist ein mechanisch robustes und chemisch inertes Biopolymer, das nach Cellulose in natürlicher Häufigkeit an zweiter Stellesteht 1. Es ist der Hauptbestandteil im Exoskelett von Arthropoden und in den Zellwänden von Pilzen und Hefen2. Chitin ist ähnlich wie Cellulose, jedoch mit einer Hydroxylgruppe jedes Monomers, die durch eine Acetylamingruppe ersetzt wird (Abbildung 1A, B). Dieser Unterschied erhöht die Festigkeit der Wasserstoffbindung zwischen benachbarten Polymerketten und verleiht Chitin seine charakteristische strukturelle Elastizität und chemische Inertheit2,3. Aufgrund seiner Eigenschaften und seines Reichtums hat Chitin ein erhebliches industrielles und akademisches Interesse geweckt. Es wurde als Gerüst für das Gewebewachstum4,5,6, als Komponente inVerbundwerkstoffen 7,8, 9,10,11und als Unterstützung für Adsorbentien und Katalysatoren11 , 12,13,14untersucht. Insbesondere seine chemische Stabilität macht Chitin attraktiv für Adsorptionsanwendungen, die Bedingungen beinhalten, die für gängige Adsorbentien unwirtlich sind14. Darüber hinaus macht die Fülle von Amingruppen Chitin zu einem wirksamen Adsorbens für Metallionen15. Die Protonierung der Amingruppen unter sauren Bedingungen reduziert jedoch die Metalladsorptionskapazität von Chitin16. Eine erfolgreiche Strategie besteht darin, Adsorptionsstellen einzuführen, die resistenter gegen Protonierungsind 17,18. Stattdessen wird hierin eine einfache Methode beschrieben, um die spezifische Oberfläche und damit die Anzahl der Adsorptionsstellen in Chitin zu erhöhen.
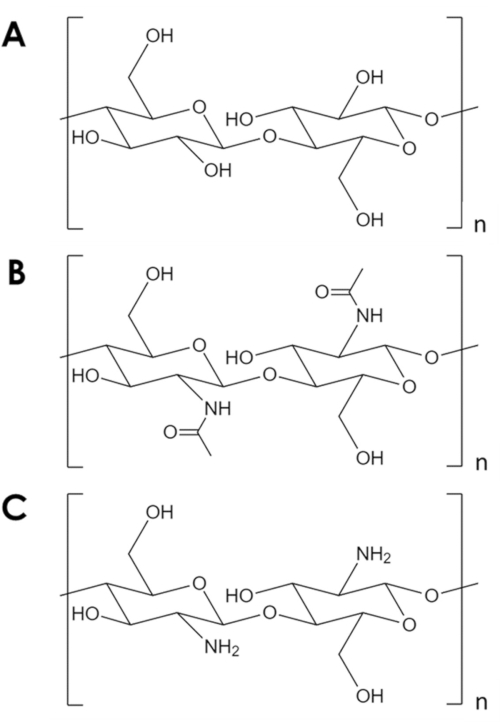
Abbildung 1. Chemische Struktur. A) Cellulose, (B) Chitin, (C) Chitosan. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Trotz seiner vielen möglichen Anwendungen wird Chitin nicht ausreichend genutzt. Die Chitinverarbeitung ist aufgrund seiner geringen Löslichkeit in den meisten Lösungsmitteln eine Herausforderung. Eine wesentliche Einschränkung seiner Verwendung in der Katalyse und Adsorption ist seine geringe spezifische Oberfläche. Während typische Kohlenstoff- und Metalloxidstützen spezifische Oberflächen in der Größenordnung 102-103 m2/g aufweisen, haben handelsübliche Chitinflocken Oberflächen in der Größenordnung von 10m2/g19,20,21. Es gibt Methoden, um Chitin zu Schäumen zu erweitern, aber sie beruhen ausnahmslos auf hohen Temperaturen und Drücken, starken Säuren und Basen oder speziellen Geräten, die eine signifikante Eintrittsbarriere darstellen5,21,22,23,24,25. Darüber hinaus neigen diese Methoden dazu, Chitin zu deacetylieren, um Chitosan zu bilden(Abbildung 1C)- ein löslicheres und reaktiveres Biopolymer5,25,26.
Hierin wird ein Verfahren beschrieben, um Chitin zu festen Schäumen zu erweitern, seine spezifische Oberfläche und Adsorptionskapazität zu erhöhen und seine chemische Integrität zu erhalten. Die Methode beruht auf der schnellen Entwicklung von Gas aus einem Chitingel und erfordert keine spezielle Ausrüstung. Die erhöhte Adsorptionskapazität des expandierten Chitins wird mit wässrigem Cu2+nachgewiesen - einer häufigen Verunreinigung im lokalen Grundwasser26.
| Einheit | Ordentliche Flocke | Gebackener Schaum | Lyophilisierten Schaum | |
| Kristallinität | % | 88 | 74 | 58 |
| Kristallgröße | Nm | 6.5 | 4.4 | 4.4 |
| Oberfläche | m2/g | 12.6 ± 2.1 | 43,1 ± 0,2 | 73,9 ± 0,2 |
| Cu Aufnahme | mg/g | 13,8 ± 2,9 | 48,6 ± 1,9 | 73,1 ± 2,0 |
| Cu Aufnahme | Atom/nm2 | 10,5 ± 2,8 | 10,7 ± 0,4 | 9,4 ± 0,3 |
Tabelle 1. Zusammenfassung der Materialeigenschaften. Chitinschäume haben eine geringere Kristallinität und Kristallgröße im Vergleich zu sauberen Chitinflocken. Die spezifische Oberfläche und Cu-Aufnahme der Chitinschäume sind jedoch proportional höher als die der reinen Chitinflocken.
Access restricted. Please log in or start a trial to view this content.
Protokoll
1. Herstellung von expandiertem Chitin
- Bereiten Sie eine 250 ml Lösung von 5 Gew.-% LiCl in Dimethylacetamid (DMAc) vor
ACHTUNG: Das Lösungsmittel DMAc ist ein brennbarer Reizstoff, der die Fruchtbarkeit schädigen und Geburtsfehler verursachen kann. Behandeln Sie DMAc in einem Abzug mit chemikalienbeständigen Handschuhen und Schutzbrillen, um den Kontakt mit Haut und Augen zu vermeiden.- 15 g LiCl und 285 g (268 ml) DMAc in einen 500 mL Erlenmeyerkolben mit 50 mm Polytetrafluorethylen (PTFE) auskleiden.
- Den Kolben mit einem Gummiseptum verschließen und auf eine Heizrührplatte legen. Legen Sie einen Temperaturfühler durch das Septum in die Mischung. Rühren Sie die Mischung bei 400 U / min und 80 ° C, bis sich das gesamte LiCl aufgelöst hat (~ 4 h)
- 1,0 g ofengetrocknete Chitinflocken in der LiCl/DMAc-Lösung zu einem Sol-Gel auflösen
- Mindestens 1,2 g Chitinflocken im Ofen bei 80°C 24 h trocknen.
- 1,0 g ofengetrocknete Chitinflocken und 250 mL 5 Gew.-% LiCl/DMAc-Lösung in einen 500 ml Rundkolben geben. Platzieren Sie einen 50 mm PTFE-ausgekleideten magnetischen Rührbalken.
- Den Kolben mit einem Gummiseptum verschließen und auf einen rührenden Wärmeblock legen. Stechen Sie das Septum mit einer Nadel durch und lassen Sie es, damit der Kolben entlüften kann. Den Block auf 80 °C erhitzen und die Mischung bei 400 U/min umrühren, bis sich das gesamte Chitin aufgelöst hat (24-48 h).
- Lassen Sie das resultierende Chitin Sol-Gel langsam auf Raumtemperatur abkühlen, während Sie weiter rühren (~ 1 h).
- Sobald Sie bei Raumtemperatur sind, stellen Sie den Kolben mit dem Chitin-Sol-Gel in ein Eisbad und rühren Sie weiter, bis sich seine Temperatur stabilisiert hat (~ 20 min).
- Bereiten Sie eine 100-ml-Aufschlämmung naH in DMAc vor.
ACHTUNG: NaH in Kontakt mit Wasser setzt brennbare Gase frei, die sich spontan entzünden können. Um den Kontakt mit feuchter Luft zu begrenzen, wird NaH in Mineralöl gelagert, das vor Gebrauch abgewaschen werden muss. Behandeln Sie mit Chemikalienschutzhandschuhen und Schutzbrillen vorsichtig in einem Abzug.- Entfernen Sie etwa 1 g NaH aus dem Mineralöllager und waschen Sie es dreimal mit 10 ml Hexanen.
- 100 ml DMAC in einen 250 ml Erlenmeyerkolben geben, dann 0,82 g des gewaschenen NaH hinzufügen und einen MIT PTFE ausgekleideten magnetischen Rührstab legen.
- Schwenken Sie die Mischung, um eine NaH/ DMAc-Aufschlämmung zu erzeugen.
HINWEIS: NaH löst sich nicht vollständig auf.
- Forme das Chitingel, indem du die gesamte NaH/DMAc-Aufschlämmung zum Chitin-Sol-Gel hinzufügst.
- Entkappen Sie das abgekühlte Sol-Gel und fügen Sie die gesamte NaH-Aufschlämmung unter kräftigem Rühren hinzu. Ersetzen Sie die Kappe und rühren Sie die Mischung bei 400 U / min für 72 h oder bis sich ein Gel im Kolben bildet.
- Formen Sie den Chitinschaum, indem Sie dem Chitingel Wasser hinzufügen.
- Nach der Bildung des Gels den Kolben abkappen und 100 ml deionisiertes (DI) Wasser hinzufügen.
HINWEIS: Es ist wichtig, diesen Schritt in einem Abzug durchzuführen, da der ProzessH2-Gas entwickelt.
- Nach der Bildung des Gels den Kolben abkappen und 100 ml deionisiertes (DI) Wasser hinzufügen.
- Isolieren und waschen Sie den Chitinschaum in Wasser und Methanol, um DMAc und Salze zu entfernen.
- Entfernen Sie den expandierten Chitinschaum aus dem Kolben und legen Sie ihn in eine Kristallisationsschale oder ein Becherglas, das groß genug ist, um ihn und 1000 ml DI-Wasser zu halten.
HINWEIS: Der Chitinschaum kommt nicht in einem Stück heraus und muss möglicherweise aufgebrochen werden. - Spülen Sie das isolierte Gel dreimal mit 500 ml DI-Wasser ab. Tränken Sie das Gel in 1000 ml DI-Wasser für 24 h, dann in 500 ml Methanol für 24 h und schließlich in 1000 ml DI-Wasser für 24 h wieder.
- Entfernen Sie den expandierten Chitinschaum aus der Wasserwäsche und lassen Sie ihn 24-48 h an der Luft trocknen.
- Entfernen Sie den expandierten Chitinschaum aus dem Kolben und legen Sie ihn in eine Kristallisationsschale oder ein Becherglas, das groß genug ist, um ihn und 1000 ml DI-Wasser zu halten.
- Trocknen Sie das gewaschene Chitingel zu einem festen Schaum und mahlen Sie es dann zu einem Pulver.
- Trocknen Sie das Gel im Ofen bei 85 °C für 48 h unter Umgebungsluft oder in einem Lyophilisator bei -43 °C und 0,024 mbar für 48 h.
- Mit Mörser und Stößel den trockenen Chitinschaum zu einem feinen Pulver mahlen.

Abbildung 2. Herstellung von expandiertem Chitinschaum. (A) Das anfängliche Chitin in LiCl/DMAc-Lösung. (B) Zugabe der NaH/DMAc-Aufschlämmung. (C) Der Chitinschaum nach Zugabe von Wasser. (D) Der Chitinschaum, wie er aus dem Reaktionskolben extrahiert wird. (E) Der Chitinschaum beim Waschen mit Wasser. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
2. Entwicklung der Adsorptionsisothermen
- Bereiten Sie 500 ml Stammlösungen von aq. Cu2+ (MW 63,5 g/mol) in konzentrationen 50 mg/L, 100 mg/L, 200 mg/L, 300 mg/L, 400 mg/L und 450 mg/L. Fügen Sie dazu 90 mg, 180 mg, 360 mg, 540 mg, 720 mg und 810 mg Cu(NO3) hinzu2· 2,5H2O (MW 232,6 g/mol) an jeweils sechs Behälter. Fügen Sie 500 ml 18 MΩ Wasser hinzu, verschließen Sie den Behälter und schütteln Sie, um die Feststoffe aufzulösen.
- Fügen Sie 50 mg Chitin zu 100 ml jeder Stammlösung hinzu, stellen Sie den pH-Wert auf 7 ein und lassen Sie ihn 48 Stunden lang ausgleichen.
- Übertragen Sie 100 ml jeder Stammlösung in einen 100-ml-Behälter, damit der Kopfraum minimal ist. Fügen Sie 50 mg gemahlenes Chitin in jeden Behälter hinzu und verschließen Sie sie dann.
- Behälter auf einen Orbitalschüttler legen und bei 60 U/min für 30 min schütteln. Nehmen Sie dann die Behälter vom Orbitalschüttler und stellen Sie den pH-Wert mit NH 4 HCO3oder HNO3 auf7 ein.
- Ersetzen Sie die Behälter wieder auf dem Orbitalschüttler und schütteln Sie sie bei 60 U / min und bei einer konstanten Temperatur für 48 h. Halten Sie das Labor bei 18 ± 2 °C.
- Messen Sie die Cu-Konzentration der ausgangsstoffmäßigen Lösungen und derjenigen, denen Chitin zugesetzt wurde. Verwenden Sie die kolorimetrische Bicinchoninat-Methode, ein Kolorimeter und vorgemessene Reagenzpakete27.
- Entfernen Sie die Behälter aus dem Orbitalschüttler, lassen Sie die Mischungen mindestens 30 Minuten ruhen und nehmen Sie dann ein 1 ml Aliquot mit einer Spritze, die mit einem 0,3 μm Glasmikrofaserfilter ausgestattet ist.
- Das Aliquot in einen 250 mL Behälter geben und mit 18 MΩ Wasser auf 100 mL verdünnen.
HINWEIS: Dieser Schritt ist aufgrund der niedrigen Decke der Erkennung von Cu (5 mg / L) durch die Bicinchoninat-Methode mit dem Kolorimeter notwendig. - 10 ml der verdünnten Probe in eine Küvette überführen. Legen Sie die Küvette in das Kolorimeter und nullen Sie das Instrument.
- Geben Sie eine Packung vorgemessenes Cu-Reagenz (Bicinchoninat-Methode) in die verdünnte Probe in der Küvette und warten Sie 45 s, bis die Chelatreaktion abgeschlossen ist. Lassen Sie die Lösung violett werden. Die Intensität der gebildeten Farbe ist proportional zur Cu-Konzentration.
- Legen Sie die Küvette wieder in das Kolorimeter und messen Sie die Cu-Konzentration der verdünnten Probe. Multiplizieren Sie die Konzentration der verdünnten Probe mit 100, um die Konzentration der Originalprobe zu erhalten.
- Extrahieren Sie die maximale Cu-Aufnahme aus den Adsorptionsisothermendaten.
- Berechnen Sie die Aufnahme jeder Probe für jede Gleichgewichts-Cu-Konzentration mit der Gleichung28:

- Zeichnen Sie die Adsorptionsaufnahme im Vergleich zur Gleichgewichtskonzentration der Proben auf, um eine Standard-Cu-Adsorptionsisotherme zu erzeugen.
- Zeichnen Sie das Verhältnis von Gleichgewichtskonzentration zu Aufnahme im Vergleich zur Gleichgewichtskonzentration auf, um die linearisierte Cu-Adsorptionsisotherme zu erzeugen.
HINWEIS: Das Diagramm sollte linear sein, und die Umkehrung der Steigung stellt die maximale Cu-Aufnahme dar.
- Berechnen Sie die Aufnahme jeder Probe für jede Gleichgewichts-Cu-Konzentration mit der Gleichung28:
Access restricted. Please log in or start a trial to view this content.
Ergebnisse
Expandiertes Chitin zeigt unabhängig von der Trocknungsmethode die gleiche Morphologie. Abbildung 3 zeigt Bilder von sauberen Chitinflocken (Abbildung 3A1), ofengetrocknetem expandiertem Chitin (Abbildung 3B1) und lyophilisiertem expandiertem Chitin (Abbildung 3C3). Während die ordentlichen Flocken das Aussehen von grobem Sand haben, hat der expandierte Chitinschaum das Aussehen eines Kerns aus g...
Access restricted. Please log in or start a trial to view this content.
Diskussion
Die vorgeschlagene Methode zur Herstellung von Chitinschaum ermöglicht die Herstellung solcher Schäume, ohne dass spezielle Geräte oder Techniken erforderlich sind. Die Herstellung des Chitinschaums beruht auf der Suspension von Natriumhydrid in einem Chitin-Sol-Gel. Der Kontakt mit Wasser aus der Atmosphäre induziert die Gelierung der Chitinmatrix und die Entwicklung von Wasserstoffgas durch Zersetzung des Natriumhydrids. Daher sind die kritischen Schritte der Zubereitung (1) die Bildung des Sol-Gels, (2) die Einfü...
Access restricted. Please log in or start a trial to view this content.
Offenlegungen
Die Autoren haben nichts preiszugeben.
Danksagungen
Die Forschung wurde vom Combat Capabilities Development Command Army Research Laboratory (Kooperationsvertragsnummer W911NF-15-2-0020) gesponsert. Alle Meinungen, Ergebnisse und Schlussfolgerungen oder Empfehlungen, die in diesem Material zum Ausdruck gebracht werden, sind die der Autoren und spiegeln nicht unbedingt die Ansichten des Army Research Lab wider.
Wir danken dem Center for Advanced Materials Processing (CAMP) an der Montana Technological University für die Verwendung einiger der für diese Studie erforderlichen Spezialausrüstungen. Wir danken auch Gary Wyss, Nancy Oyer, Rick LaDouceur, John Kirtley und Katherine Zodrow für die technische Unterstützung und hilfreiche Diskussionen.
Access restricted. Please log in or start a trial to view this content.
Materialien
| Name | Company | Catalog Number | Comments |
| Ammonium bicarbonate | Sigma-Aldrich | 9830 | NH4HCO3, ≥99.5 % |
| Chitin | Sigma-Aldrich | C7170 | Pandalus borealis, practical grade |
| Colorimeter | Hanna Instruments | HI83399-01 | Photometer for wastewater analysis |
| Copper High Range Checker | Hanna Instruments | HI702 | Bicinchoninate colorimetric titration |
| Copper nitrate hydrate | Sigma-Aldrich | 223395 | Cu(NO3)2 · 2.5 H2O, 98 % |
| Dimethylacetamide (DMAc) | Sigma-Aldrich | 271012 | Anhydrous, 99.8 % |
| IR Spectrophotometer | Thermo Nicolet | Nexus 670 | Fitted with an ATR cell |
| Lithium chloride | Sigma-Aldrich | 310468 | LiCl, ≥99 % |
| N2 Physisorption Apparatus | Micromeritics | Tristar II | |
| Nitric acid | BDH | BDH7208-1 | HNO3, 0.1 N |
| Scanning electron microscope | Zeiss LEO | 1430 VP | 15 kV, secondary electron detector, 29-31 mm working distance |
| Sodium hydride | Sigma-Aldrich | 223441 | NaH, packed in mineral oil, 90 % |
| Thermogravimetric analyzer | TA Instruments | Q500 | 100 ml/min N2, 10 °C/min to 800 °C |
| Water Purification System | Millipore | Milli-Q | Type A water (18 MΩ) |
| X-Ray Diffractometer | Rigaku | Ultima IV | Cu K-α radiation, 8.04 keV |
Referenzen
- Rinaudo, M. Chitin and chitosan: Properties and applications. Progress in Polymer Science. 31 (7), 603-632 (2006).
- Percot, A., Viton, C., Domard, A. Optimization of chitin extraction from shrimp shells. Biomacromolecules. 4 (1), 12-18 (2003).
- Austin, P. R. Chitin solvents and solubility parameters. Chitin, Chitosan, and Related Enzymes. , 227-237 (1984).
- Deepthi, S., Venkatesan, J., Kim, S. K., Bumgardner, J. D., Jayakumar, R. An overview of chitin or chitosan/nano ceramic composite scaffolds for bone tissue engineering. International Journal of Biological Macromolecules. 93, 1338-1353 (2016).
- Tao, F., et al. Applications of chitin and chitosan nanofibers in bone regenerative engineering. Carbohydrate Polymers. 230, 115658(2020).
- Zhao, L., et al. Regulation of the morphological and physical properties of a soft tissue scaffold by manipulating DD and DS of O-carboxymethyl chitin. ACS Applied Bio Materials. 3 (9), 6187-6195 (2020).
- Duan, Y., Freyburger, A., Kunz, W., Zollfrank, C. Cellulose and chitin composite materials from an ionic liquid and a green co-solvent. Carbohydrate Polymers. 192, 159-165 (2018).
- Kadokawa, J., Takegawa, A., Mine, S., Prasad, K. Preparation of chitin nanowhiskers using an ionic liquid and their composite materials with poly(vinyl alcohol). Carbohydrate Polymers. 84 (4), 1408-1412 (2011).
- Chen, Z., Wang, J., Qi, H. J., Wang, T., Naguib, H. E. Green and sustainable layered chitin-vitrimer composite with enhanced modulus, reprocessability, and smart actuator function. ACS Sustainable Chemistry and Engineering. 8 (40), 15168-15178 (2020).
- Zhang, Z., Lucia, L. A. Chitin-clay composite gels with enhanced thermal stability prepared in a green and facile approach. Journal of Materials Science. 56 (4), 3600-3611 (2021).
- Ahmed, M. J., Hameed, B. H., Hummadi, E. H. Review on recent progress in chitosan/chitin-carbonaceous material composites for the adsorption of water pollutants. Carbohydrate Polymers. 247, 116690(2020).
- Matsuoka, A., et al. Hydration of nitriles to amides by a chitin-supported ruthenium catalyst. RSC Advances. 5 (16), 12152-12160 (2015).
- Wang, Y., Li, Y., Liu, S., Li, B. Fabrication of chitin microspheres and their multipurpose application as catalyst support and adsorbent. Carbohydrate Polymers. 120, 53-59 (2015).
- Anastopoulos, I., Bhatnagar, A., Bikiaris, D., Kyzas, G. Chitin Adsorbents for Toxic Metals: A Review. International Journal of Molecular Sciences. 18 (1), 114(2017).
- Habiba, U., Afifi, A. M., Salleh, A., Ang, B. C. Chitosan/(polyvinyl alcohol)/zeolite electrospun composite nanofibrous membrane for adsorption of Cr6+, Fe3+ and Ni2+. Journal of Hazardous Materials. 322, 182-194 (2017).
- Kim, U. J., et al. Protein adsorption of dialdehyde cellulose-crosslinked chitosan with high amino group contents. Carbohydrate Polymers. 163, 34-42 (2017).
- He, Y., et al. Fabrication of PVA nanofibers grafted with octaamino-POSS and their application in heavy metal adsorption. Journal of Polymers and the Environment. , (2020).
- Tian, H., et al. Electrospinning of polyvinyl alcohol into crosslinked nanofibers: An approach to fabricate functional adsorbent for heavy metals. Journal of Hazardous Materials. 378, (2019).
- Meille, V. Review on methods to deposit catalysts on structured surfaces. Applied Catalysis A: General. 315, 1-17 (2006).
- Dotto, G. L., Cunha, J. M., Calgaro, C. O., Tanabe, E. H., Bertuol, D. A. Surface modification of chitin using ultrasound-assisted and supercritical CO2 technologies for cobalt adsorption. Journal of Hazardous Materials. 295, 29-36 (2015).
- Phongying, S., Aiba, S., Chirachanchai, S. Direct chitosan nanoscaffold formation via chitin whiskers. Polymer. 48 (1), 393-400 (2007).
- Tan, T. S., Chin, H. Y., Tsai, M. L., Liu, C. L. Structural alterations, pore generation, and deacetylation of α- and β-chitin submitted to steam explosion. Carbohydrate Polymers. 122, 321-328 (2015).
- Chang, F. S., Chin, H. Y., Tsai, M. L. Preparation of chitin with puffing pretreatment. Research on Chemical Intermediates. 44 (8), 4939-4955 (2018).
- Goodrich, J. D., Winter, W. T. α-Chitin Nanocrystals prepared from shrimp shells and their specific surface area measurement. Biomacromolecules. 8 (1), 252-257 (2007).
- Rolandi, M., Felts, J. Naturally sourced chitin foam. , US 2020/0239670 A1 (2020).
- McDermott, S., Hailer, M. K., Lead, J. R. Meconium identifies high levels of metals in newborns from a mining community in the U.S. Science of the Total Environment. 707, 135528(2020).
- Hach Handbook of Water Analysis. Copper, Bicinchoninate Method, Method 8506. Hach Handbook of Water Analysis. , (1979).
- Crittenden, J. C., Trusell, R. R., Hand, D. R., Howe, K. J., Tchbanoglous, G. Adsorption. MWH's Water Treatment. , 1117(2012).
- Focher, B., Beltrame, P. L., Naggi, A., Torri, G. Alkaline N-deacetylation of chitin enhanced by flash treatments. Reaction kinetics and structure modifications. Carbohydrate Polymers. 12 (4), 405-418 (1990).
- Scherrer, P. Determination of the size and the internal structure of colloidal particles by means of X-rays. News from the Society of Sciences in Göttingen, Mathematical- Physical Class. 2, 98-100 (1918).
- Brunauer, S., Emmett, P. H., Teller, E. Adsorption of gases in multimolecular layers. Journal of the American Chemical Society. 60 (2), 309-319 (1938).
- Sing, K. S. W. Adsorption methods for the characterization of porous materials. Advances in Colloid and Interface Science. 76-77, 3-11 (1998).
- Rouquerol, J., Llewellyn, P., Rouquerol, F. Is the bet equation applicable to microporous adsorbents. Studies in Surface Science and Catalysis. 160, 49-56 (2007).
- Vorokh, A. S. Scherrer formula: estimation of error in determining small nanoparticle size. Nanosystems: Physics, Chemistry, Mathematics. , 364-369 (2018).
- Labidi, A., Salaberria, A. M., Fernandes, S. C. M., Labidi, J., Abderrabba, M. Adsorption of copper on chitin-based materials: Kinetic and thermodynamic studies. Journal of the Taiwan Institute of Chemical Engineers. 65, 140-148 (2016).
- Tian, M., Zhao, T. Q., Chin, P. L., Liu, B. S., Cheung, A. S. -C. Methane and propane co-conversion study over zinc, molybdenum and gallium modified HZSM-5 catalysts using time-of-flight mass-spectrometry. Chemical Physics Letters. 592, 36-40 (2014).
Access restricted. Please log in or start a trial to view this content.
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten