Method Article
Intraoperative Beurteilung von Resektionsrändern bei Mundhöhlenkrebs: So geht's
In diesem Artikel
Zusammenfassung
Ziel dieses Protokolls ist es, einen klaren Überblick über die probengetriebene intraoperative Beurteilung von Resektionsrändern zu geben. Es wird empfohlen, dieses Protokoll umzusetzen, um die Patientenversorgung an anderen Instituten zu verbessern.
Zusammenfassung
Das Ziel der onkologischen Kopf-Hals-Chirurgie ist die vollständige Tumorresektion mit ausreichenden Resektionsrändern unter Beibehaltung der akzeptablen Funktion und des Aussehens. Für das Plattenepithelkarzinom der Mundhöhle (OCSCC) zeigten verschiedene Studien, dass nur 15% -26% aller Resektionen ausreichend sind. Ein Hauptgrund für die geringe Anzahl adäquater Resektionen ist der Mangel an Informationen während der Operation; der Margin-Status ist erst nach der abschließenden histopathologischen Beurteilung, Tage nach der Operation, verfügbar.
Die Chirurgen und Pathologen des Erasmus MC University Medical Center in Rotterdam begannen 2013 mit der Implementierung der probengesteuerten intraoperativen Bewertung der Resektionsränder (IOARM), die 2015 zum Behandlungsstandard wurde. Diese Methode ermöglicht es dem Chirurgen, eine unzureichende Resektion in eine adäquate Resektion umzuwandeln, indem er während der ersten Operation eine zusätzliche Resektion durchführt. Die intraoperative Beurteilung wird durch ein Umsiedlungsverfahren unterstützt, das eine genaue Identifizierung unzureichender Ränder (auf der Probe) im Wundbett ermöglicht.
Die Umsetzung dieses Protokolls führte zu einer Verbesserung der adäquaten Resektionen von 15%-40%. Das probengesteuerte IOARM ist jedoch nicht weit verbreitet, da das Brutto von frischem Gewebe für Pathologen kontraintuitiv ist. Es besteht die Befürchtung, dass das Auffüllen von frischem Gewebe die anatomische Orientierung, Form und Größe der Probe verschlechtert und daher die endgültige histopathologische Beurteilung beeinflusst. Diesen möglichen negativen Auswirkungen wird durch das beschriebene Protokoll entgegengewirkt. Hier wird das Protokoll für probengetriebenes IOARM detailliert vorgestellt, wie es am Institut durchgeführt wird.
Einleitung
Jedes Jahr werden weltweit rund 350.000 neue Patienten mit Krebs in der Mundhöhle diagnostiziert; 90% der Fälle sind Plattenepithelkarzinome1. Die Sterblichkeitsrate beträgt 175.000 weltweit pro Jahr und das 5-Jahres-Überleben beträgt 50% bis 64,8%1,2,3,4.
Die primäre Behandlung des Plattenepithelkarzinoms der Mundhöhle (OCSCC) ist dieOperation 5. Das Ziel der Operation ist die vollständige Entfernung des Tumors mit ausreichenden Margen, so das Royal College of Pathologists6. Ränder >5 mm (klar) werden als ausreichend angesehen, während Ränder von 0-5 mm als unzureichend angesehen werden.
Ausreichende Resektionsmargen führen zu einem höheren Überleben und einer Verringerung der lokalen Rezidivraten von OCSCC7,8,9. Tumorresektionen mit unzureichenden Margen führen zur Notwendigkeit einer adjuvanten Therapie (postoperative Strahlentherapie und/oder Chemotherapie). Dies bringt eine zusätzliche Belastung für den Patienten mit sich, erhöht die Morbidität und verringert die Lebensqualität10. Der Resektionsrand ist der einzige onkologische prognostische Faktor, den der Chirurg und Pathologe beeinflussen kann.
Jüngste Berichte haben gezeigt, dass ausreichende Resektionen nur in 15%-26% der Fälle erreicht werden7,8,11. Diese schlechten Ergebnisse werden durch die komplexe Anatomie der Mundhöhle und den Mangel an intraoperativer Führung verursacht. Während der Operation kann sich der Chirurg nur auf Inspektion, Palpation und präoperative Bildgebung verlassen.
Der endgültige Margin-Status folgt erst einige Tage nach der Operation. Tritt bei der abschließenden pathologischen Beurteilung ein unzureichender Spielraum auf, kommt eine zweite Operation in der Regel nicht in Frage, da die Wundbettrekonstruktion zu diesem Zeitpunkt in der Regel verheilt ist. Darüber hinaus ist eine zweite Operation meist nicht effektiv, da die Verlagerung der unzureichenden Marge im postoperativen Umfeld noch schwieriger ist.
Um den Mangel an intraoperativen Informationen über den Margenstatus zu beheben, wurde 2013 eine probengesteuerte intraoperative Bewertung der Resektionsmargen (IOARM) eingeführt9. Es wurde 2015 zum Standard der Versorgung im Institut. Hier wird die IOARM-Methode im Detail beschrieben, um Kollegen an anderen Instituten die Implementierung dieses Protokolls zu ermöglichen.
Protokoll
Diese Studie wurde von der institutionellen Medizinischen Ethikkommission genehmigt (MEC-2015-150).
HINWEIS: Alle Patienten- und Personalinformationen in den Abbildungen oder Beispielen sind fiktiv (d. H. XXXXX und JJJJ).
1. Vor der Operation
- Chirurgische Abteilung: Anfrage für IOARM während der Planung der Operation.
- Pathologieabteilung: Sicherstellen der Logistik / Ausrüstung (siehe Materialtabelle) und der Verfügbarkeit von Personal (Pathologe / Pathologie-Resident und Assistent).
2. Während der Operation
- Operationssaal (OP)
- Stellen Sie sicher, dass alle beteiligten Mitarbeiter mit dem Umzugsprotokoll12vertraut sind.
- Befolgen Sie das Umzugsprotokoll.
- Tauchen Sie die Tags mindestens 30 Minuten vor Beginn der Operation in Chlorhexidin ein.
- Platzieren Sie die Tags gepaart auf beiden Seiten der beabsichtigten Resektionslinie (sowohl oberflächlich als auch tief), so dass sich ein Tag auf der Resektionsprobe befindet und der andere an der entsprechenden Stelle im Wundbett verbleibt (Abbildung 1A), wie von Van Lanschot et al.12beschrieben.
- Schneiden Sie zwischen den einzelnen Tags aus.
- Entfernen Sie die Probe mit dem Tumor (ein Tag von jedem Paar verbleibt im Wundbett, Abbildung 1B).
- Füllen Sie das Pathologie-Antragsformular mit einem klaren Hinweis auf die anatomische Lage der Tags aus (z. B. Tag 1 = anterior, Tag 2 = superior).
- Notieren Sie die chirurgischen Eingriffsdefekte der Probe und ihre Position in Bezug auf die Tags auf dem Pathologie-Antragsformular.
HINWEIS: Verfahrensbedingte Defekte erzeugen falsche Resektionsoberflächen und können zu einer falschen Zuordnung unzureichender Ränder sowohl während des IOARM als auch während der endgültigen Pathologie führen. - Bringen Sie die Probe in die Pathologieabteilung.
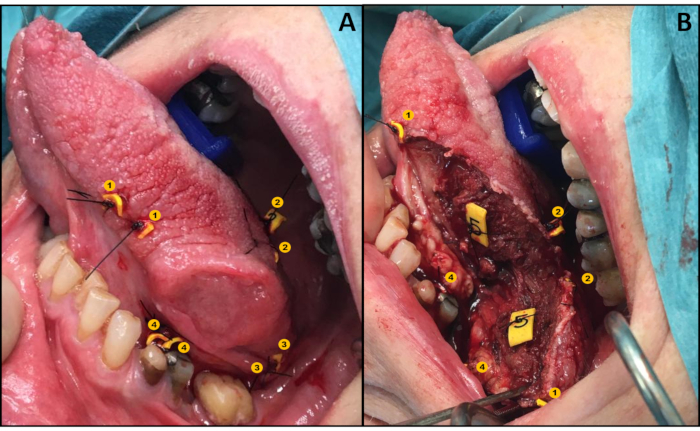
Abbildung 1: Veranschaulichung des Umsiedlungsprotokolls. (A) Paarweise Anbringung von Tags. (B) Wundbett und Probe beide mit einem Etikett jedes Paares. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
- IOARM - Grossing Raum (GR), Pathologie
- Spülen Sie die Probe mit Wasser ab und tupfen Sie sie vorsichtig mit Gaze oder Papier trocken.
HINWEIS: Registrieren Sie jeden nächsten Schritt mit Fotos und speichern Sie sie in der elektronischen Patientenakte (EPF). - Notieren Sie die allgemeinen Informationen (Datum, Patienten-ID, Pathologienummer, Chirurg, Pathologe, Art der verwendeten Probe und verwendete Tags) auf der anatomischen Vorlage.
- Geben Sie die Positionen der Tags auf der anatomischen Vorlage an (Abbildung 2).
- Legen Sie die Probe auf die anatomische Schablone.
- Spülen Sie die Probe mit Wasser ab und tupfen Sie sie vorsichtig mit Gaze oder Papier trocken.
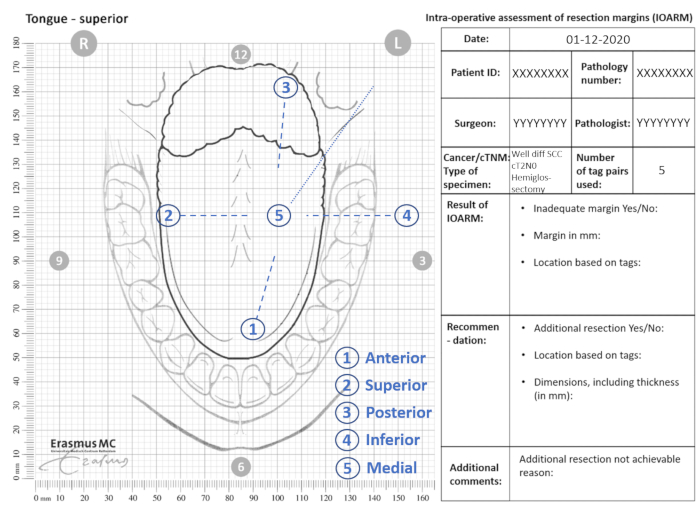
Abbildung 2: Beispiel einer anatomischen Vorlage für IOARM. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
- Färben Sie die Resektionsoberfläche gemäß dem Standardprotokoll ein (z. B. überlegenes Blau und minderwertiges Grün).
- Untersuchen Sie die Probe visuell und durch Palpation (Pathologe und Chirurg).
- Geben Sie die Position eines verdächtigen Bereichs (d. h. Rand <5 mm) auf der anatomischen Vorlage an und beziehen Sie ihn auf die nummerierten Tags (Abschnitt Ergebnis von IOARM, Abbildung 2).
- Führen Sie einen Schnitt senkrecht zur Resektionsfläche an der verdächtigen Stelle durch (Abbildung 3A). Je nach Größe der Probe und/oder verdächtigen Regionen einen oder mehrere Schnitte mit einem Abstand von ca. 5 mm vornehmen. Bei mehr als einem Schnitt nummerieren Sie die Schnitte als IOA1, IOA2 usw.
- Messen Sie die Ränder (d.h. den Abstand zwischen Resektionsfläche und Tumorgrenze) an den Gewebeschnitten (Abbildung 3B) und notieren Sie die genauen Werte in mm auf der anatomischen Schablone (Abschnitt Ergebnis von IOARM, Abbildung 3C).
HINWEIS: Wenn die Tumorgrenze makroskopisch nicht unterscheidbar ist (z. B. kann der Tumor nicht von umgebendem fibrotischem oder Speicheldrüsengewebe unterschieden werden), ist eine mikroskopische Analyse nach gefrorenem Schnitt indiziert.
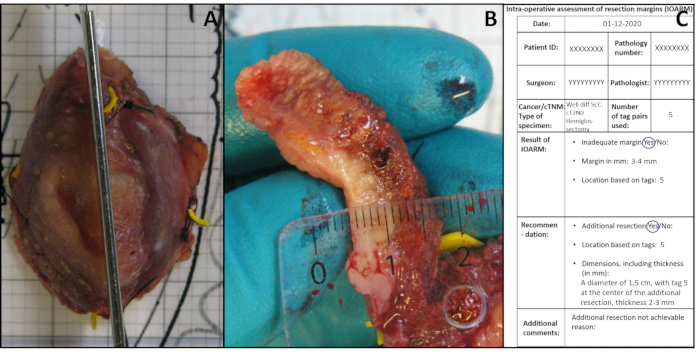
Abbildung 3: Illustration von IOARM. (A) Senkrechte Inzision, die nach Identifizierung verdächtiger Region durch Palpation durchgeführt wird. (B) Die Marge wird gemessen. (C) Das Ergebnis von IOARM und die Empfehlung werden aufgezeichnet. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
- Fahren Sie mit dem Abschluss des Vorgangs fort, Schritt 2.2.19. Wenn eine ausreichende Marge erkannt wird (d. h. eine zusätzliche Resektion ist nicht erforderlich).
- Geben Sie die genaue Position basierend auf den Tags an, wenn ein unzureichender Rand erkannt wird, und notieren Sie ihn in der Vorlage. Fahren Sie mit einer zusätzlichen Resektion fort, falls chirurgisch/technisch erreichbar, Schritt 2.2.13.
- Kommentieren Sie den Grund in der Vorlage, wenn eine zusätzliche Resektion nicht erreichbar ist (Abschnitt Zusätzliche Kommentare, Abbildung 2).
- Empfehlen Sie (Pathologe / Chirurg) die zusätzliche Resektion basierend auf dem genauen Ort und geben Sie die Dicke an, die erforderlich ist, um eine adäquate Resektion zu erreichen (Abbildung 3C).
HINWEIS: Wenn der unzureichende Rand einen positiven Rand betrifft, sollte für die zusätzliche Resektion eine Mindestdicke von 6 mm empfohlen werden. - Bewahren Sie (Pathologe) die Hauptresektionsprobe im Kühlschrank auf, bis die zusätzliche Resektion eingegangen ist.
- Verschieben (Chirurg) sie den Bereich der zusätzlichen Resektion in Bezug auf die Tags im Wundbett, basierend auf der Aufzeichnung von IOARM (Abbildung 3C).
- Führen Sie die zusätzliche Resektion durch.
- Senden Sie die zusätzliche Resektion an den GR.
- Überprüfen Sie (Pathologe) die Genauigkeit der zusätzlichen Resektion in Bezug auf ihre Position (basierend auf Tags) und ihre Größe.
HINWEIS: Die oben genannten Schritte gelten im Falle einer engen Marge. Bei einer positiven Marge ist ein IOARM der zusätzlichen Resektion notwendig (Pathologe). Der Chirurg wartet auf das Ergebnis des zweiten IOARM, bevor er die Operation abschließt. - Entfernen Sie (Chirurg) die verbleibenden Tags vom Wundbett und schließen Sie die Operation ab.
- Kopieren (Pathologe) alle Daten aus der anatomischen Vorlage in die EPF.
3. Nach IOARM - Grossing Room (GR), Pathologie
HINWEIS: Um die anatomische Ausrichtung und Form der Probe zu erhalten, werden die folgenden Schritte durchgeführt.
- Setzen Sie die Probe durch die korrekte Ausrichtung aller Gewebeschnitte (Querschnitte und polare Enden) basierend auf den Tags und den während IOARM aufgenommenen Fotos wieder zusammen.
HINWEIS: Querschnitte befinden sich in der Mitte der Probe und die polaren Enden sind die äußeren Teile der Probe. - Schneiden Sie die Korkstücke etwas größer als die Gewebeabschnitte.
- Legen Sie jeden Gewebeabschnitt auf ein Stück Kork.
- Zeichnen Sie mit einem Permanentmarker eine Linie auf den Korken um den Gewebeabschnitt und machen Sie ein Foto (Abbildung 4A).
- Legen Sie ein weiteres Stück Kork auf alle Gewebeabschnitte mit Ausnahme der polaren Enden (Abbildung 4B).
- Halten Sie den oberen und unteren Korken zusammen, mit dem Gewebeabschnitt dazwischen, indem Sie Stifte durch beide Korken neben dem Rand des Gewebeschnitts platzieren, jedoch nicht durch den Gewebeabschnitt (Abbildung 4B).

Abbildung 4: Illustration der Methode zur Erhaltung der anatomischen Ausrichtung und Form von Gewebeschnitten. (A) Gewebeschnitte werden auf ein Stück Kork mit einer auf dem Korken gezogenen Linie um den Gewebeabschnitt mit einem Permanentmarker gelegt. (B) Stifte werden schräg über die polaren Enden gelegt und ein weiteres Stück Kork wird über den Gewebeabschnitt gelegt. (C) Illustration einer wieder zusammengesetzten frischen Probe, die zusammen mit Stiften aufbewahrt wird, die die angrenzenden Korken durchstechen. (D) Illustration einer wieder zusammengesetzten festen Probe, die mit Stiften zusammengehalten wird, die benachbarte Korken durchstechen. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
- Platzieren Sie die polaren Enden auf einem separaten Stück Kork (Abbildung 4A).
- Halten Sie die polaren Enden am Korken befestigt, indem Sie schräg Stifte über das Gewebe legen und den Korken direkt neben dem Rand des Gewebes durchbohren (Abbildung 4B).
ACHTUNG: Durchstechen Sie die Probe nicht mit den Stiften. - Setzen Sie die gesamte Probe wieder zusammen: Setzen Sie alle Gewebeabschnitte einschließlich der polaren Enden in der richtigen anatomischen Ausrichtung zusammen.
- Halten Sie alle Gewebeabschnitte zusammen, indem Sie die benachbarten Korken durchstechen (Abbildung 4C).
- Positionieren Sie die Probe mit der richtigen Ausrichtung auf der anatomischen Schablone und machen Sie ein Foto.
- Legen Sie die Probe in Formaldehydlösung (Formalin 4%).
HINWEIS: Zur ordnungsgemäßen Fixierung können Papierstücke auf die Probe gelegt werden, um sie in Formalin zu versinken. - Machen Sie einen klaren und sichtbaren Warnhinweis auf dem Behälter mit der Probe (z. B. Vorsichtsnadeln/ -nadeln), um Unfälle zu vermeiden.
- Lagern Sie den Behälter mit der Probe zur weiteren Verarbeitung gemäß dem Standard-Pathologieprotokoll.
4. Grossing der fixierten Probe nach IOARM
HINWEIS: Nach der Formalinfixierung sollte die Probe vorzugsweise von dem Pathologen/Assistenzarzt/Assistenten, der das IOARM durchgeführt hat, grossisiert werden.
VORSICHT: Seien Sie vorsichtig mit den Nadeln/ Stiften, wenn Sie die Probe aus dem Behälter nehmen.
- Befolgen Sie das institutionelle Bruttoprotokoll.
HINWEIS: Ergreifen Sie zusätzliche Maßnahmen, um die korrekte Orientierung zu gewährleisten und den Vergleich des Margenstatus zwischen IOARM und der endgültigen pathologischen Bewertung zu erleichtern.- Konsultieren Sie die Bilder des IOARM.
- Nehmen Sie die Probe aus dem Behälter.
- Überprüfen Sie, ob alle Gewebeschnitte vorhanden sind.
- Positionieren Sie die Probe mit der richtigen Ausrichtung auf der anatomischen Schablone und machen Sie ein Foto (Abbildung 4D).
- Entfernen Sie die Stifte.
- Trennen Sie die einzelnen Gewebeabschnitte mit entsprechendem Kork.
- Machen Sie Fotos von jedem Gewebeschnitt mit den entsprechenden Korken und konzentrieren Sie sich dabei auf die Linien, die um den Gewebeschnitt gezeichnet wurden, um eine mögliche Schrumpfung des Gewebes nach der Fixierung zu beurteilen (Abbildung 5).

Bild 5: Illustration eines polaren Endes mit der dem Kork zugewandten Schnittfläche, die durch geneigte Stifte gegen den Kork gehalten wird. (A) Frisches Exemplar. (B) Nach der Fixierung. (C) Die Schnittfläche des polaren Endes ist nach der Fixierung flach. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
- Trennen Sie alle Gewebeschnitte systematisch vom Korken (z. B. von vorne nach hinten oder von links nach rechts).
- Gross die IOARM-Gewebeschnitte auf die Standard-Endgewebeschnitte (2-3 mm dick).
- Legen Sie alle endgültigen Gewebeschnitte in der richtigen anatomischen Ausrichtung (z. B. von anterior nach posterior) auf ein Papier auf dem Bruttotisch.
- Nummerieren Sie alle endgültigen Gewebeabschnitte nacheinander mit einem Permanentmarker auf dem Papier (Abbildung 6).
- Kommentieren Sie die Position von IOARM mit einem Permanentmarker (Abbildung 6).
- Machen Sie Fotos, einschließlich aller endgültigen Gewebeschnitte, und speichern Sie sie in der EPF (Abbildung 6).
- Wählen Sie die relevanten endgültigen Gewebeschnitte und IOARM-Abschnitte aus, die für die endgültige pathologische Beurteilung weiterverarbeitet werden sollen.

Abbildung 6: Grosse Probe mit der Position des IOARM markiert. Entsprechende Zahlen 1-5 beziehen sich auf Gewebeschnitte von links nach rechts. A-E entspricht Gewebeschnitten, die für die histopathologische Bewertung enthalten sind. Beachten Sie, dass das verbleibende Gewebestück, das durch gefrorene Sektion (FS) bewertet wurde, angezeigt ist, um einen direkten Vergleich mit dem permanenten HE-gefärbten Abschnitt zu ermöglichen. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
5. Die abschließende pathologische Bewertung - Auswirkungen von IOARM auf den endgültigen Margenstatus
- Folgen Sie dem lokalen standardisierten Protokoll. Das Protokoll, das hier befolgt wird, ist das PALGA (Pathologisch-Anatomisch Landelijk Geautomatiseerd Archief, das landesweite Netzwerk und Register der Histo- und Zytopathologie in den Niederlanden) nationale Kopf-Hals-Protokoll für den endgültigen standardisierten strukturierten Pathologiebericht.
HINWEIS: Dieses Protokoll basiert auf den aktuellen Standards des American Joint Committee on Cancer (AJCC), der Union for International Cancer Control (UICC) und der Weltgesundheitsorganisation (WHO).- Beurteilen Sie alle Ränder in Millimetern, einschließlich Schleimhaut, Submukosa und Knochen.
- Wenn ein unzureichender Rand gefunden wird, kommentieren Sie seine Ausdehnung (z. B. ist der submuköse Rand vorne 3,5 mm und erstreckt sich über eine Trajektorie von 6 mm).
- Beurteilen Sie das Vorhandensein von Dysplasie und ihren Grad für Schleimhautresektionsränder.
- Geben Sie den endgültigen Rand an, indem Sie die Abmessungen der zusätzlichen Resektion (falls durchgeführt) zu dem am Hauptmuster gemessenen Rand addieren.
- Notieren Sie die eindeutige Pathologienummer der zusätzlichen Resektion im Pathologiebericht der Hauptprobe (z. B. Ränder: vordere 6 mm, hintere 8 mm, überlegene 6 mm (einschließlich 3 mm der zusätzlichen Resektion, H20-2021), untere 7 mm, mediale 5,3 mm).
- Überprüfen Sie die während IOARM gefundenen Ränder.
- Kommentieren Sie das Ergebnis dieser Überprüfung (z. B. stimmen die während der intraoperativen Bewertung festgestellten NB-Margen mit den Margen überein, die auf der endgültigen Pathologie basieren).
HINWEIS: Die für IOARM benötigte Zeit sollte begrenzt sein, um den chirurgischen Arbeitsablauf nicht zu beeinträchtigen. Am Institut dauert das IOARM ca. 10 min. Der Chirurg und der Pathologe führen das IOARM gemeinsam durch. Für die Umzugsmethode (Platzieren der Tags während der Operation) wird eine zusätzliche Zeit von 5 min benötigt. Dies wird für jedes Institut je nach Logistik unterschiedlich sein.
Ergebnisse
Beispiel für IOARM, das zu einer adäquaten Resektion führt
Der Patient präsentiert sich mit einem cT2N0M0 SCC der linken Seite der Zunge ohne Anamnese. Der Patient wird einer von IOARM unterstützten Hemiglossektomie unterzogen. Das Exemplar wird inspiziert und palpiert; die Schleimhautränder werden als >5 mm gemessen. Ein Bereich in der submukösalen Resektionsfläche ist verdächtig für einen unzureichenden Rand, der sich um Tag 5 befindet. Der submuköse Rand beträgt bei Tag 5 3-4 mm. Alle Informationen werden auf der Vorlage aufgezeichnet und in die EPF kopiert (Abbildung 7A).
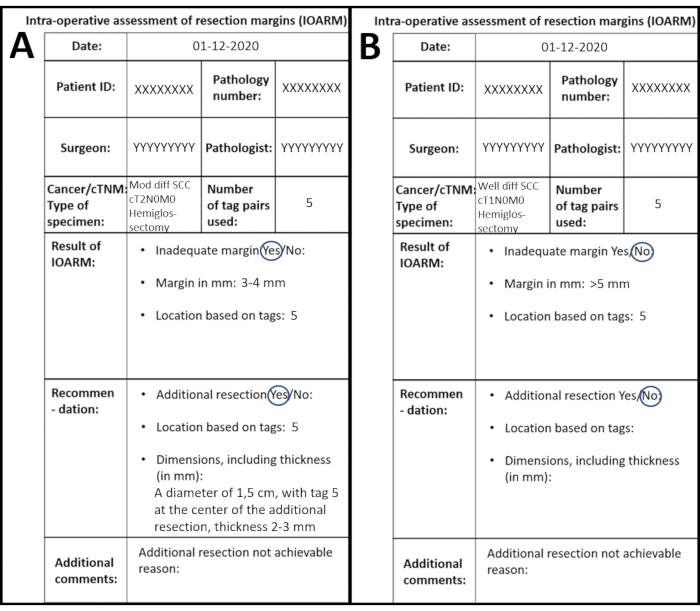
Abbildung 7: Beispiele für zwei verschiedene IOARMs, die auf der anatomischen Schablone aufgezeichnet wurden. (A) IOARM, was zu einer adäquaten Resektion führt. (B) IOARM führt nicht zu einer adäquaten Resektion. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Der Chirurg kehrt in den OP zurück und führt die zusätzliche Resektion durch. Der Pathologe überprüft die Genauigkeit und abmessungen, einschließlich der Dicke der zusätzlichen Resektion.
Der abschließende Pathologiebericht zeigt das Vorhandensein eines mäßig differenzierten pT2-Plattenepithelkarzinoms auf der linken Zungenseite. Der Tumordurchmesser beträgt 2,5 cm und die Invasionstiefe 6,0 mm. Das schlimmste Muster der Invasion (WPOI) ist Kategorie 3. Perineurale Invasion (PNI) ist nicht vorhanden und die lymphovaskuläre Invasion (LVI) ist vorhanden. Die minimalen Ränder (Schleimhaut und Submukosal) an der unteren, oberen, vorderen und hinteren Stelle betragen 5,8 mm (einschließlich zusätzlicher Resektion (PA-Nummer: XXXXX) von 3 mm Dicke), 6,2 mm (einschließlich zusätzlicher Resektion (PA-Nummer: XXXXX) von 3 mm Dicke), 5,2 mm bzw. 5,5 mm. IOARM steht in Übereinstimmung mit der endgültigen Pathologie.
| Ränder (mm) | |||
| Ort | Basierend auf IOARM | Nach zusätzlicher Resektion | Basierend auf der endgültigen Pathologie |
| Minderwertig | 3-4 | 6-7 | 5.8 |
| Überlegen | 3-4 | 6-7 | 6.2 |
| Anterior | >5 | 5.2 | |
| Hintern | >5 | 5.5 | |
Tabelle 1: Beispiel für Resektionsränder während IOARM, die zu einer adäquaten Resektion bei der endgültigen Pathologienach zusätzlicher Resektion führen.
Beispiel für IOARM, das nicht zu einer adäquaten Resektion führt
Der Patient präsentiert ein cT1N0M0 SCC der rechten Seite der Zunge ohne Anamnese. Der Patient wurde einer resektion unterzogen, die von IOARM unterstützt wurde. Der Chirurg bringt die Probe zum Pathologen in der Pathologieabteilung. Die Schleimhaut wird visuell inspiziert, und die Schleimhautränder werden mit einem transparenten Lineal gemessen, alle Schleimhautränder sind >5 mm. Die submukösen Ränder werden visuell inspiziert und palpiert und alle Ränder scheinen >5 mm zu sein. Ein verdächtiger Bereich befindet sich bei Tag 1 (vordere Resektionsfläche) und Tag 3 (posteriore Resektionsfläche). Ein Grossing-Messer wird senkrecht zur Resektionsfläche von vorne nach hinten platziert (Tag 1 bis Tag 3) und ein Schnitt wird gemacht. Der Pathologe misst den Rand am Querschnitt und die Ränder sind >5 mm. Alle Informationen werden auf der Vorlage aufgezeichnet und in die EPF kopiert (Abbildung 7B).
Der abschließende Pathologiebericht zeigt ein gut differenziertes pT1-Plattenepithelkarzinom auf der rechten Seite der Zunge. Der Durchmesser des Tumors beträgt 1, 8 cm und die Invasionstiefe beträgt 3,8 mm. Das schlimmste Invasionsmuster (WPOI) ist Kategorie 2. Perineurale Invasion (PNI), lymphovaskuläre Invasion (LVI) und Dysplasie sind nicht vorhanden. Die minimalen Ränder (Schleimhaut und Submukosal) an den unteren, oberen, vorderen und hinteren Stellen betragen 4,0 mm, 6,1 mm, 6,4 mm bzw. 7,8 mm. IOARM ist nicht in Übereinstimmung mit der endgültigen Pathologie, Margin Inferior wurde verpasst.
| Ränder (mm) | |||
| Ort | Basierend auf IOARM | Nach zusätzlicher Resektion | Basierend auf der endgültigen Pathologie |
| Minderwertig | >5 | Nicht empfohlen alle Ränder > 5mm | 4.0 |
| Überlegen | >5 | 6.1 | |
| Anterior | 6 | 6.4 | |
| Hintern | 8 | 7.8 | |
Tabelle 2: Beispiel für Resektionsränder während IOARM, die nicht zu einer adäquaten Resektion bei der endgültigen Pathologie führen.
Diskussion
Das Ziel der chirurgischen Behandlung von OCSCC-Patienten ist die vollständige Entfernung des Tumors mit ausreichenden Margen. Dies wird zu oft nicht erreicht, was dazu inspirierte, einen angepassten Ansatz für die orale Krebschirurgie mit Schwerpunkt auf der intraoperativen Beurteilung der Resektionsränder zu entwickeln. Abgesehen von den Resektionsrändern beeinflussen auch andere nachteilige Tumorfaktoren wie das Muster der Invasion, der perineuralen Invasion und der lymphovaskulären Invasion das lokale Rezidiv. Von allen unerwünschten Tumorfaktoren können Chirurgen und Pathologen jedoch nur die Resektionsränder7,8,11beeinflussen .
Die probengetriebene IOARM-Methode wurde 2013 implementiert; dies wurde schließlich durch den Nachweis gestützt, dass probengetriebenes IOARM dem defektgetriebenen IOARM7,13,14,15,16,17überlegen ist. Dies führte zu seiner Empfehlung des AJCC im Jahr 201718. Bemerkenswert ist, dass die probengetriebene IOARM-Methode 2015 zum Standard der Versorgung im Institut wurde. Von 2013 bis 2020 wurde der IOARM in 304 Fällen durchgeführt, mit einem steilen Anstieg gegenüber 2018.
Es ist wichtig zu erkennen, dass die Entwicklung und Implementierung einer IOARM-Methode viele Mitarbeiter (Pathologen / Chirurgen / Assistenten / Auszubildende / Forscher) umfasst, um sie zum Behandlungsstandard zu machen. Viele Fachleute waren während vieler Jahre an der Entwicklung dieses Protokolls beteiligt, was eigentlich die Stärke der Methode ist. Die Entwicklung dieser Methode begann 2013 und erreichte 2015 einen Konsens. Dies wurde auf der Grundlage der zweiwöchentlichen Treffen erreicht, in denen Gespräche über alle mit der Operation behandelten Patienten, einschließlich IOARM, stattfanden. Auf diese Weise war es möglich, das Verfahren zeitnah anzupassen und zu verfeinern. Darüber hinaus ermöglichten die zweiwöchentlichen Treffen eine prospektive Datenerhebung, die die Grundlage für die Leistungs- und Folgestudienbildet 9. Darüber hinaus stellte das Team in jedem Fall sicher, dass die endgültige Pathologie nicht durch IOARM beeinträchtigt wurde. Schließlich ist es wichtig zu erkennen, dass diese Art der Bewertung ein dynamischer Prozess ist und immer Veränderungen in Richtung Verbesserung erfahren wird.
Bei der probengetriebenen IOARM-Methode werden die Ränder durch Inspektion, Palpation und senkrechte Schnitte (Grossing) beurteilt. Dieser Ansatz ermöglicht eine möglichst genaue Schätzung der Margen in Millimetern und ermöglicht eine Rückmeldung darüber, ob eine zusätzliche Resektion erforderlich ist und wie die Abmessungen aussehen sollten. Kubik et al. beschrieben mehrere Gründe (z.B. zusätzliche Resektion an einer falschen Stelle, die falsche Ausrichtung der zusätzlichen Resektion, falsche Abmessungen der zusätzlichen Resektion) dafür, dass zusätzliche Resektionen unzureichend sind17. Das IOARM ist eine wertvolle Methode, aber nur, wenn es von einer möglichst genauen Umsiedlungsmethode mit unzureichenden Margen begleitet wird, damit der Chirurg eine adäquate zusätzliche Resektion durchführen kann. Die räumliche Beziehung zwischen der zusätzlichen Resektion und der Hauptprobe ist der Schlüsselfaktor. Daher wurde eine einfache, aber elegante Umsiedlungsmethode, wie in Abbildung 1 gezeigt, von Van Lanschot et al.12entwickelt und detailliert beschrieben. Diese Methode ermöglicht es dem Chirurgen, eine zusätzliche Resektion durchzuführen, die auf der Verlagerung des unzureichenden Randes basiert, der durch die Tags im Wundbett definiert ist. Zum Beispiel findet sich ein Rand von 2 mm zwischen den Tags 1-2-3, der Chirurg führt eine zusätzliche Resektion um die Tags 1-2-3 mit einer Dicke von 4 mm durch. Diese Umsiedlungsmethode wird durch die Ergebnisse von Smits et al.9als wirksam erwiesen.
Diese IOARM-Methode wird durch ein Eingefrorenschnittverfahren nur dann unterstützt, wenn der Tumor makroskopisch nicht vom umgebenden Gewebe (z.B. Gewebefibrose nach Strahlentherapie oder Narbenbildung nach vorangegangener Operation oder Speicheldrüsengewebe) unterschieden werden kann. Einige Institute verwenden einen anderen Ansatz, bei dem gefrorene Abschnitte aus der Probe aus allen Quadranten13,19entnommen werden. Diese Methode ermöglicht ein standardisierteres Protokoll. Die Vollständigkeit dieser Methode ist jedoch möglicherweise nicht immer effizient. Darüber hinaus werden mehrere eingefrorene Abschnitte benötigt, was kostspielig, zeitaufwendig und nicht für alle Institute zugänglich ist. Die beschriebene Methode ist effizienter, da die Region von Interesse vorausgewählt ist (d.h. Region mit verdächtig unzureichender Marge) und daher billiger, schneller und für jedes Institut verfügbar ist. Dies steht im Einklang mit früheren Erkenntnissen, dass die Analyse eingefrorener Abschnitte die Genauigkeit von probengesteuertem IOARM auf der Grundlage von Bruttowerten in den meisten Fällen nicht verbessert und nicht kosteneffizient ist20,21,22.
Laut Literatur >93% aller unzureichenden Ränder finden sich an den submukösen Resektionsrändern23. Das deckt sich mit den Erkenntnissen des Instituts. Schleimhautveränderungen mit hochgradiger Dysplasie/CIS sind während IOARM oft leicht zu erkennen, nur in wenigen Fällen wird ein eingefrorener Abschnitt empfohlen. Bisher wurden in der IOARM-Kohorte keine positiven Schleimhautränder in Bezug auf Krebs oder hochgradige Dysplasie/CIS festgestellt.
Obwohl das probengesteuerte IOARM die Rate adäquater Resektionen bei OCSCC-Patienten signifikant verbessert und folglich das Patientenergebnis7,9,22,21verbessert , hinkt seine breite Implementierung hinterher. Die Hauptursache dafür ist die Tatsache, dass das Brutto von frischem Gewebe für Pathologen kontraintuitiv ist. Die Pathologen befürchten, dass das Grobwerden von frischem Gewebe die anatomische Orientierung, Form und Größe der Probe verschlechtert und daher die endgültige histopathologische Beurteilung beeinflusst24,25. Die im Protokoll vorgeschriebenen Maßnahmen verhindern jedoch diese möglichen negativen Auswirkungen. Seit der Implementierung dieses Protokolls wurden die anatomische Ausrichtung, Form und Größe der Probe nie verändert, noch wurde die endgültige pathologische Beurteilung jemals beeinträchtigt (Manuskript in Vorbereitung).
Obwohl für die Durchführung von IOARM wenig zusätzliche Zeit erforderlich ist, ist es klar, dass es keine wirklichen Hindernisse für die Implementierung von IOARM gibt, aber es muss die Bereitschaft bestehen, eine Lernkurve zu durchlaufen, was das Einbringen von frischem Gewebe und die Identifizierung unzureichender Margen betrifft. Die wichtigste Voraussetzung ist ein engagiertes und kooperatives Team von Chirurgen und Pathologen. In dieser Studie wurde eine IOARM-Methode zur Kopf-Hals-Krebschirurgie beschrieben, die in jedem Institut und bei jeder anderen Krebsoperation problemlos eingesetzt werden kann. Dieses Protokoll verbessert signifikant die Rate adäquater Resektionen und reduziert gleichzeitig die Notwendigkeit einer postoperativen Strahlentherapie und verbessert das Patientenergebnis. Die probengesteuerte IOARM-Methode wird Chirurgen helfen, eine erstmalige richtige Operation zu erreichen, und die Patienten werden davon profitieren.
Offenlegungen
Die Autoren haben nichts preiszugeben.
Danksagungen
Wir danken Bas J. van Brakel und Roxanna Haak für ihre Hilfe bei der Durchführung von IOARM. Klara A. Bouman-Zevenbergen, Ian Overduin und Silvy L. Sabiran - Singoredjo für ihre Unterstützung und unterstützende Rolle bei der Sicherstellung von Logistik, Ausrüstung und Verfügbarkeit von Personal in der Pathologieabteilung.
Materialien
| Name | Company | Catalog Number | Comments |
| Anatomical templates | https://www.palga.nl/assets/uploads/Protocollen/HoofdHalstumoren.pdf | ||
| Anatomical tweezers | |||
| Brush | to apply the inc to the tissue | ||
| Bucket for formalin fixation | Size of the container depends on the size fo the tissue | ||
| Buffered formalin 4% | |||
| Camera | |||
| Computer | |||
| Cork | Thin plates of cork | ||
| Ethanol 70% | |||
| Examination gloves | |||
| Gauze or Paper | That wont leave particles on the specimen | ||
| Grossing knife 15cm | |||
| Grossing knife 30cm | |||
| Grossing tabel | |||
| Inc for tissue | 3 or more different colors | ||
| Labcoat | |||
| Long pins/Sewing pins | |||
| Paper | To place the tissue sections on during the grossing | ||
| Permanent markers | Different colors (black/blue/red/green) | ||
| Relocation tags | Premier Farnell Limited BV, Utrecht, The Netherlands | Numbered from 0-9, cut to a size of 5 mm x 7 mm x 2 mm | |
| Scalpel | |||
| Surgical tweezers | |||
| Sutures | Ethicon | Ethilon 3.0 | To suture in the tags |
| Tap water | |||
| Transparant ruler 30 cm | 2 rulers needed |
Referenzen
- Bray, F., et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: A Cancer Journal for Clinicians. 68 (6), 394-424 (2018).
- Sharma, S. M., Prasad, B. R., Pushparaj, S., Poojary, D. Accuracy of intraoperative frozensection in assessing margins in oral cancer resection. Journal of Maxillofacial and Oral Surgery. 8 (4), 357-361 (2009).
- vander Ploeg, T., Datema, F., Baatenburg de Jong, R., Steyerberg, E. W. Prediction of survival with alternative modeling techniques using pseudo values. PLoS One. 9 (6), 100234(2014).
- Chen, S. W., et al. Trends in clinical features and survival of oral cavity cancer: fifty years of experience with 3,362 consecutive cases from a single institution. Cancer Management and Research. 10, 4523-4535 (2018).
- Shah, J. P., Gil, Z. Current concepts in management of oral cancer--surgery. Oral Oncology. 45 (4-5), 394-401 (2009).
- Helliwell, T., Woolgar, J. Dataset for histopathology reporting of mucosal malignancies of the oral cavity. Royal College of Pathologists. , London, UK. (2013).
- Varvares, M. A., Poti, S., Kenyon, B., Christopher, K., Walker, R. J. Surgical margins and primary site resection in achieving local control in oral cancer resections. The Laryngoscope. 125 (10), 2298-2307 (2015).
- Smits, R. W., et al. Resection margins in oral cancer surgery: Room for improvement. Head & Neck. 38, Suppl 1 2197-2203 (2016).
- Smits, R. W. H., et al. Intraoperative assessment of the resection specimen facilitates achievement of adequate margins in oral carcinoma. Frontiers in Oncology. 10, 614593(2020).
- Lin, A. Radiation therapy for oral cavity and oropharyngeal cancers. Dental Clinics of North America. 62 (1), 99-109 (2018).
- Dik, E. A., et al. Resection of early oral squamous cell carcinoma with positive or close margins: relevance of adjuvant treatment in relation to local recurrence: margins of 3 mm as safe as 5 mm. Oral Oncology. 50 (6), 611-615 (2014).
- van Lanschot, C. G. F., et al. Relocation of inadequate resection margins in the wound bed during oral cavity oncological surgery: A feasibility study. Head & Neck. 41 (7), 2159-2166 (2019).
- Amit, M., et al. Improving the rate of negative margins after surgery for oral cavity squamous cell carcinoma: A prospective randomized controlled study. Head & Neck. 38, Suppl 1 1803-1809 (2016).
- Maxwell, J. H., et al. Early oral tongue squamous cell carcinoma: Sampling of margins from tumor bed and worse local control. JAMA Otolaryngology-- Head & Neck Surgery. 141 (12), 1104-1110 (2015).
- Hinni, M. L., Zarka, M. A., Hoxworth, J. M. Margin mapping in transoral surgery for head and neck cancer. Laryngoscope. 123 (5), 1190-1198 (2013).
- Kain, J. J., et al. Surgical margins in oral cavity squamous cell carcinoma: Current practices and future directions. Laryngoscope. 130 (1), 128-138 (2020).
- Kubik, M. W., et al. Intraoperative margin assessment in head and neck cancer: a case of misuse and abuse. Head and Neck Pathology. 14 (2), 291-302 (2020).
- Amin, M. B., et al. The Eighth edition AJCC cancer staging manual: Continuing to build a bridge from a population-based to a more "personalized" approach to cancer staging. CA: A Cancer Journal for Clinicians. 67 (2), 93-99 (2017).
- Gokavarapu, S., et al. Revision of margins under frozen section in oral cancer: a retrospective study of involved margins in pT1 and pT2 oral cancers. The British Journal of Oral & Maxillofacial Surgery. 53 (9), 875-879 (2015).
- Chaturvedi, P., et al. Gross examination by the surgeon as an alternative to frozen section for assessment of adequacy of surgical margin in head and neck squamous cell carcinoma. Head & Neck. 36 (4), 557-563 (2014).
- Mair, M., et al. Intraoperative gross examination vs frozen section for achievement of adequate margin in oral cancer surgery. Oral Surgery, Oral Medicine, Oral Pathology and Oral Radiology. 123 (5), 544-549 (2017).
- Datta, S., et al. Frozen section is not cost beneficial for the assessment of margins in oral cancer. Indian Journal of Cancer. 56 (1), 19-23 (2019).
- Woolgar, J. A., Triantafyllou, A. A histopathological appraisal of surgical margins in oral and oropharyngeal cancer resection specimens. Oral Oncology. 41 (10), 1034-1043 (2005).
- Umstattd, L. A., Mills, J. C., Critchlow, W. A., Renner, G. J., Zitsch, R. P. Shrinkage in oral squamous cell carcinoma: An analysis of tumor and margin measurements in vivo, post-resection, and post-formalin fixation. American Journal of Otolaryngology. 38 (6), 660-662 (2017).
- Pangare, T. B., et al. Effect of Formalin Fixation on Surgical Margins in Patients With Oral Squamous Cell Carcinoma. Journal of Oral Maxillofacial Surgery: Official Journal of the American Association of Oral and Maxillofacial Surgeons. 75 (6), 1293-1298 (2017).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten