Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Pipeline für die Planung und Durchführung von transkraniellen Ultraschall-Neuromodulationsexperimenten am Menschen
In diesem Artikel
Zusammenfassung
Die transkranielle Ultraschallstimulation (TUS) ist eine aufstrebende nicht-invasive Neuromodulationstechnik, die eine sorgfältige Planung von akustischen und thermischen Simulationen erfordert. Die Methodik beschreibt eine Bildverarbeitungs- und Ultraschallsimulationspipeline für eine effiziente, benutzerfreundliche und optimierte Planung von TUS-Experimenten am Menschen.
Zusammenfassung
Die transkranielle Ultraschallstimulation (TUS) ist eine aufstrebende nicht-invasive Neuromodulationstechnik, die in der Lage ist, sowohl kortikale als auch subkortikale Strukturen mit hoher Präzision zu manipulieren. Experimente mit Menschen erfordern eine sorgfältige Planung von akustischen und thermischen Simulationen. Diese Planung ist unerlässlich, um Knocheninterferenzen mit der Form und Flugbahn des Ultraschallstrahls zu berücksichtigen und sicherzustellen, dass die TUS-Parameter den Sicherheitsanforderungen entsprechen. Für die Schädelrekonstruktion und Simulationen werden T1- und T2-gewichtete Ultraschalluntersuchungen mit Nullzeitecho (ZTE) und Magnetresonanztomographie (MRT) mit einer isotropen Auflösung von 1 mm (alternativ Computertomographie-Röntgenaufnahmen (CT)) aufgenommen. Die Kartierung von Ziel und Trajektorie wird mit Hilfe einer Neuronavigationsplattform durchgeführt. SimNIBS wird für die anfängliche Segmentierung des Schädel-, Haut- und Gehirngewebes verwendet. Die Simulation von TUS wird mit dem BabelBrain-Tool übertragen, das den ZTE-Scan verwendet, um synthetische CT-Bilder des Schädels zu erstellen, die in akustische Eigenschaften umgewandelt werden sollen. Wir verwenden einen Phased-Array-Ultraschallwandler mit elektrischer Lenkung. Die Z-Lenkung wird so eingestellt, dass die Zieltiefe erreicht wird. Auch andere Aufnehmerkonfigurationen werden im Planungstool unterstützt. Thermische Simulationen werden durchgeführt, um sicherzustellen, dass die Anforderungen an Temperatur und mechanischen Index innerhalb der von der FDA empfohlenen akustischen Richtlinien für TUS bei menschlichen Probanden liegen. Während der TUS-Verabreichungssitzungen unterstützt ein mechanischer Arm die Bewegung des Schallkopfs an die gewünschte Stelle mithilfe eines rahmenlosen stereotaktischen Lokalisierungssystems.
Einleitung
Zu den häufig verwendeten nicht-invasiven Neurostimulationstechniken gehören die transkranielle Gleichstromstimulation (tDCS) und die transkranielle Magnetstimulation (TMS). Beide haben jedoch eine begrenzte Eindringtiefe und eine geringe Präzision 1,2. Im Gegensatz dazu ist der transkranielle Ultraschall (TUS) eine aufstrebende nicht-invasive Technik, die in der Lage ist, die neuronale Aktivität zu verstärken oder zu unterdrücken 3,4,5 und auf kortikale oder subkortikale Strukturen mit Millimetergenauigkeit abzuzielen 6,7. Tiermodelle mit Nagetieren 4,8,9, Kaninchen10, Schafen 5,11, Schweinen6 und nichtmenschlichen Primaten 7,12,13,14 haben die Wirksamkeit und Sicherheit von TUS gezeigt. Studien haben gezeigt, dass das Ansprechen verschiedener Gehirnregionen unter anderem Bewegungen der Gliedmaßen8 bei Ratten, somatosensorisch evozierte Potentiale (SSEPs) bei Schweinen6 und Veränderungen der visuomotorischen Aktivität12, der kognitiven und motivationalen Entscheidungsfindung bei nichtmenschlichen Primaten13 hervorrufen kann. Beim Menschen wurde beobachtet, dass TUS die motorisch evozierten Potentiale (MEPs) und die Leistung bei einer Reaktionszeitaufgabe verändert, wenn es auf den primären motorischen Kortex15,16 abzielt, und die Leistung bei einer taktilen Diskriminierungsaufgabe und SSEPs, wenn es auf den somatosensorischen Kortex17 und den sensorischen Thalamus18 abzielt. Histologische Analysen haben keine groben oder mikroskopischen strukturellen Veränderungen im Zusammenhang mit TUS bei Schweinen6, Schafen 5,11, Kaninchen10 und nichtmenschlichen Primaten14 ergeben, und es wurden keine Nebenwirkungen beobachtet, die sich signifikant von anderen nicht-invasiven Neurostimulationstechniken unterscheiden19.
TUS verwendet gepulsten, fokussierten Ultraschall mit geringer Intensität bei einer Frequenz zwischen 200 kHz und 700 kHz, um einen transienten neuromodulatorischen Effekt zu erzeugen. Die typische räumliche Spitzenpuls-Durchschnittsintensität (Isppa) in situ beträgt 10 W/cm2 oder weniger, wobei die berichteten Tastverhältnisse (Prozentsatz der Zeit, in der der Ultraschall eingeschaltet ist) bei Menschen 20,21,22,23,24 zwischen 0,5 % und 70 % liegen. Obwohl vorgeschlagen wurde, dass die Mechanismen der TUS-Neuromodulation hauptsächlich eine mechanische Bewegung der Lipidmembranen beinhalten, die zur Öffnung der Ionenkanäleführt 25,26,27, können mögliche thermische und Kavitationseffekte nicht ignoriert werden. Sie werden anhand mechanischer (MI) und thermischer (TI) Indizes bewertet. Der MI beschreibt die vorhergesagten kavitationsbedingten Bioeffekte, die bei TUS auftreten werden, während der TI den potentiellen Temperaturanstieg im Gewebe nach Ultraschallanwendung beschreibt28,29. Darüber hinaus führt eine Änderung der Frequenz und der Eingangsintensität auch dazu, dass sich die MI und TI ändern. Höhere Frequenzen haben eine bessere räumliche Auflösung und verringern die Wahrscheinlichkeit mechanischer Bioeffekte; Sie haben jedoch eine stärkere Absorption im Gewebe, was das Potenzial für einen Temperaturanstieg erhöht28. Alternativ erhöhen niedrigere Frequenzen bei gleicher Intensität den MI. In ähnlicher Weise führt eine Erhöhung der Intensität tendenziell zu einer Zunahme des Ausmaßes mechanischer und thermischer Bioeffekte30. Es ist daher zwingend erforderlich, dass vor den Experimenten für alle TUS-Parameter, die implementiert werden, eine sorgfältige Planung und Simulation durchgeführt wird.
Die Planung eines TUS-Experiments erfordert die Identifizierung des Ziels und der interessierenden Trajektorie sowie die Durchführung thermischer und akustischer Simulationen. Simulationen helfen dabei, mechanische Effekte zu optimieren und die thermischen Auswirkungen von TUS auf Gewebe abzuschwächen. Sie erfordern ein Verständnis der Vorhersage der Schädelerwärmung, der Druckamplitude des Ultraschalls im Brennpunkt, der fokalen Korrektur und anderer Erwärmungen innerhalb des Schädels und der Haut. Eine angemessene Simulation stellt sicher, dass der Schwerpunkt das gewünschte Ziel erreicht und die Sicherheitsparameter für den Ultraschalleinsatz eingehalten werden, die in den Sicherheitsrichtlinien zur biophysikalischen Sicherheit festgelegt sind, die vom International Transcranial Ultrasound Stimulation Safety and Standards Consortium (ITRUSST)31 empfohlen werden und auf den Empfehlungen der FDA und von Health Canada basieren. Neuere Studien haben auch einen auditiven Störeffekt hervorgehoben, der von TUS begleitet wird 32,33,34 bei Tieren und Menschen, wobei die TUS-Stimulation Hörbahnen im Gehirn aktivieren kann, um Reaktionen hervorzurufen 32,33,34. Die Durchtrennung der Hörnerven32, die Entfernung von Cochlea-Flüssigkeit32 oder die chemische Taubheit33 bei Nagetieren wurden eingesetzt, um diese Wirkungen bei Tieren zu verringern. Beim Menschen wurde die Verabreichung eines auditiven Tones über Kopfhörer verwendet, um auditive Geräusche effektiv von TUS zu maskieren, wobei die TUS-induzierte auditive Aktivität confoundy34 kontrolliert wurde. Dies unterstreicht die Notwendigkeit, den Hörrauschen unter Scheinstimulationsbedingungen zu kontrollieren, was in die Planung, das Design und die Implementierung des Protokolls einbezogen werden muss.
Hier stellen wir Ihnen eine Anleitung vor, wie Sie die Vorbereitung (Schritt 1, Schritt 2), die Planung (Schritt 3), die Simulationen (Schritt 4) und die TUS-Durchführung (Schritt 5), die für die Durchführung des TUS-Neuromodulationsexperiments am Menschen erforderlich sind, angemessen abschließen.
Protokoll
Alle Methoden, bei denen menschliche Probanden verwendet werden, wurden in Übereinstimmung mit dem Tri-Council Ethical Conduct for Research Involving Humans durchgeführt, und das Protokoll wurde vom Conjoint Health Research Ethics Board (CHREB) an der Universität Calgary genehmigt. Alle Probanden gaben vor der Teilnahme eine schriftliche Einverständniserklärung ab. Von den menschlichen Teilnehmern musste es sich um gesunde, rechtshändige Erwachsene im Alter zwischen 18 und 40 Jahren handeln, die bereit und in der Lage waren, eine Magnetresonanztomographie (MRT) durchzuführen. Zu den Ausschlusskriterien gehörten Anfälle in der Familienanamnese, Stimmungs- oder Herz-Kreislauf-Störungen, Ohrtraumata, Alkohol- oder Drogenabhängigkeit, Einnahme von verschreibungspflichtigen Medikamenten, Metallimplantate einschließlich eines Herzschrittmachers, Schwangerschaft, Herz-Kreislauf-Erkrankungen, neurologische oder psychiatrische Störungen in der Vorgeschichte, Unfähigkeit, mit dem Prüfarzt und dem Studienpersonal zu kommunizieren, sowie Geschäftsunfähigkeit oder eingeschränkte Geschäftsfähigkeit. Das im Folgenden beschriebene Protokoll folgt den Empfehlungen von ITRUSST zur standardisierten Berichterstattung von TUS-Studien35. Die Einzelheiten zu den Geräten, der Software und den erforderlichen Weblinks, die in dieser Studie verwendet wurden, sind in der Materialtabelle aufgeführt.
1. Hochauflösende Magnetresonanztomographie
- Stellen Sie sich den Teilnehmer mit einer 24-Kanal-Kopf-/Halsspule vor.
HINWEIS: Alternativ reicht die beste vor Ort erhältliche Kopf-/Halsspule aus, um eine anatomische MRT zu erhalten. - Erfassen Sie T1- und T2-gewichtete MRT-Bilder und Nullzeit-Echo-Sequenzen (ZTE) mit einer Auflösung von 1 mm.
HINWEIS: Es wird empfohlen, MRT-Bilder zu sammeln, ohne dass der Teilnehmer Over-Ear-Kopfhörer trägt, da dies die Bildrekonstruktion beeinträchtigen und spätere Planungs- und Umsetzungsschritte erschweren kann. Stattdessen wird empfohlen, dass der Teilnehmer zur MR-Sicherheit nur Gehörschutzstöpsel trägt.- Verwenden Sie für die T1-gewichtete Bildgebung eine 3D-Inversionswiederherstellungs-vorbereitete FSPGR-Sequenz (Fast Spoiled Gradient Echo) mit den folgenden Parametern: Repetitionszeit (TR) = 8,4 ms, Echozeit (TE) = 3,2 ms, Inversionszeit (TI) = 650 ms, Flip-Winkel von 10 Grad, ein Sichtfeld von 256 mm x 256 mm x 188 mm, Matrixgröße von 256 x 256 x 188 mm, GRAPPA (ARC)-Faktor von 2 in Richtung der Phasenkodierung und sagittal-schräge Orientierung zur Annäherung an die Ausrichtung mit AC-PC.
HINWEIS: Die Gesamtscanzeit beträgt 5 Minuten und 21 Sekunden. - Verwenden Sie für die T2-gewichtete Bildgebung ein 3D-Fast-Spin-Echo (FSE) mit den folgenden Parametern: TR = 3000 ms, TE = 60-90 ms, eine Echozuglänge von 130, ein Sichtfeld von 256 mm x 225 mm x 188 mm, eine Matrixgröße von 256 x 256 x 188 und eine sagittal-schräge Ausrichtung, die sich der Ausrichtung mit der AC-PC-Achse annähert. Ein GRAPPA (ARC)-Faktor von zwei wurde für die Phasenkodierung und die Schnittrichtung verwendet.
HINWEIS: Die Gesamtscanzeit beträgt 3 Minuten und 58 Sekunden. - Verwenden Sie für ZTE-Bilder einen isotropen 3D-ZTE-Scan mit den folgenden Einstellungen: TR = 698 ms, TE = 16 μs, Flip-Winkel von 1 Grad, Empfängerbandbreite von 62,5 kHz, Anzahl der Mittelwerte = 3,5, ein Sichtfeld von 256 mm x 256 mm x 256 mm, Matrixgröße von 256 x 256 x 256 mm.
HINWEIS: Die Gesamtscanzeit beträgt 5 min und 23 s.
HINWEIS: Die MRT-Bilder müssen fertiggestellt sein, bevor mit der TUS-Planung begonnen werden kann.
- Verwenden Sie für die T1-gewichtete Bildgebung eine 3D-Inversionswiederherstellungs-vorbereitete FSPGR-Sequenz (Fast Spoiled Gradient Echo) mit den folgenden Parametern: Repetitionszeit (TR) = 8,4 ms, Echozeit (TE) = 3,2 ms, Inversionszeit (TI) = 650 ms, Flip-Winkel von 10 Grad, ein Sichtfeld von 256 mm x 256 mm x 188 mm, Matrixgröße von 256 x 256 x 188 mm, GRAPPA (ARC)-Faktor von 2 in Richtung der Phasenkodierung und sagittal-schräge Orientierung zur Annäherung an die Ausrichtung mit AC-PC.
2. Vorverarbeitung von Teilnehmerbildern
- Konvertieren Sie T1-w-, T2-w- und ZTE DICOM-Scandateien von DICOM in das Nifti-Format mit dem Tool dcm2niix. Führen Sie in einem Terminalfenster Folgendes aus: dcm2niix .
HINWEIS: Das dcm2niix-Tool ist auf GitHub verfügbar (siehe Materialtabelle). Das BabelBrain-Tool registriert die Bilder der Teilnehmer mit, um Bilder zu berücksichtigen, die an verschiedenen Tagen aufgenommen wurden. Wenn T1-w-Bilder nicht isotrop sind, werden sie auf isotrope Voxel von 1 mm neu abgetastet. CT/ZTE-Bilder sind es jedoch nicht. Stattdessen werden die Masken für die Simulation auf die endgültige Auflösung in Bezug auf PPW neu abgetastet. Es sind keine zusätzlichen Schritte zur Mitregistrierung oder zum Abgleich erforderlich. - Führen Sie die Co-Registrierung und die Extraktion von Gewebemasken mit dem Charme-Tool von SimNIBS durch. Führen Sie in einem Terminalfenster Folgendes aus: charm --forceqform, wobei eine Zeichenfolge zur Identifizierung ist. An dieser Stelle kann die Versuchsplanung pausiert und zu einem anderen Zeitpunkt fortgesetzt werden.
HINWEIS: Die erstellten Dateien werden in einem Unterverzeichnis m2m gespeichert, das in späteren Planungsphasen verwendet wird. Die Vorverarbeitung von Bildern mit dem Charme-Werkzeug ist für die Gewebesegmentierung erforderlich, da dies für die Verwendung im BabelBrain-Werkzeug36 erforderlich ist.
3. Planung der Trajektorie
- Öffnen Sie Brainsight, klicken Sie auf Neues leeres Projekt und laden Sie das T1-w Nifti-Bild des Teilnehmers, das in Schritt 2.1 erstellt wurde.
HINWEIS: Wenn Sie eine Brainsight-Version vor v2.5.3 verwenden, kann entweder "Neues leeres Projekt" oder "Neues SimNIBS-Projekt" ausgewählt werden. Wenn Sie Brainsight v2.5.3 und höher verwenden, gibt es eine Integration zwischen Brainsight und BabelBrain und es wird dringend empfohlen, auf "Neues SimNIBS-Projekt" zu klicken. Beides reicht jedoch immer noch aus, um Planungsschritte abzuschließen. Für "Neues leeres Projekt" muss das T1-w-Bild geladen werden, während für "Neues SimNIBS-Projekt" eine MSH-Datei geladen werden muss, die das T1-w-Bild direkt lädt. Alle anderen Funktionalitäten und Schritte bleiben gleich. - Klicken Sie auf Overlays und dann auf Overlays konfigurieren , um ein Overlay zu erstellen und anzuzeigen. Klicken Sie auf Hinzufügen , um die Datei auszuwählen, die überlagert werden soll.
HINWEIS: Wenn das Ziel nicht auf einem T1-w-Bild visualisiert werden kann, muss es zuerst auf einem gemeinsam registrierten T2-w-Bild lokalisiert werden (daher sind die Koordinaten T1-w und T2-w identisch). Übertragen Sie dann die Koordinaten für nachfolgende Planungsschritte auf ein T1-w-Bild. Das Charm-Werkzeug in Schritt 2.2 erzeugt ein co-registriertes T2-w-Bild im Dateipfad m2m /T2_reg.nii.gz. - Schließen Sie den Abschnitt Overlays, klicken Sie auf die Registerkarte Ziele , gefolgt von Ziele konfigurieren. Klicken Sie auf die blaue Informationsschaltfläche, um die Deckkraft, die Farbe und den Schwellenwert des Overlays zu ändern und so einen Vergleich der Bilder zu ermöglichen.
HINWEIS: Dies kann durchgeführt werden, um co-registrierte Nifti-Bilder zu visualisieren, und sollte verwendet werden, um zu beobachten, wie sich die akustischen Simulationen mit dem Ziel überlagern. - Klicken Sie auf die Registerkarte Rekonstruktionen und dann auf das Dropdown-Menü Neue Rekonstruktion... . Klicken Sie auf Skin und dann im neuen Fenster auf Compute Skin . Wenn Sie fertig sind, klicken Sie auf die Schaltfläche "Schließen " in der oberen linken Ecke des Fensters.
- Klicken Sie auf der Registerkarte "Rekonstruktionen" auf das Dropdown-Menü Neue Rekonstruktion... und dann auf Full Brain Curvilinear.
- Passen Sie jedes Feld auf den sagittalen (Abbildung 1A), koronalen (Abbildung 1B) und transversalen (Abbildung 1C) Bildern an, indem Sie die Ränder des grünen Feldes so ziehen, dass die Linien das Gehirn eng umgeben (Abbildung 1).
- Scrollen Sie durch alle Schnitte, um sicherzustellen, dass sich keine Ränder des Gewebes überlappen. Klicken Sie auf Krummlinig berechnen und stellen Sie die Schältiefe auf 4 mm ein (Abbildung 1D).
HINWEIS: Die vollständige Krümmung des Gehirns bietet eine 3D-Rekonstruktion des Kortex, die geschält werden kann, um verschiedene Tiefen zu beobachten. Es ermöglicht die genaue und konsistente Platzierung einer TMS-Spule über dem Gehirn, um die interessierende Region zu lokalisieren.
- Klicken Sie in Brainsight auf die Registerkarte Orientierungspunkte , gefolgt von Sehenswürdigkeiten konfigurieren.
- Platzieren Sie das Fadenkreuz (Cursor) auf der Spitze der Nase und beschriften Sie im Feld "Name:" den Orientierungspunkt mit "Nase" (Abbildung 2A). Platzieren Sie das Fadenkreuz zwischen den Augen oberhalb des Nasenrückens und beschriften Sie den Orientierungspunkt mit "Nasion" (Abbildung 2A).
- Platzieren Sie das Fadenkreuz auf dem linken Ohr und beschriften Sie den Orientierungspunkt mit "L-Ohr" (Abbildung 2B). Platzieren Sie das Fadenkreuz auf dem rechten Ohr und beschriften Sie den Orientierungspunkt mit "R-Ohr" (Abbildung 2C).
- Klicken Sie auf die Registerkarte Ziele und verwenden Sie das Fadenkreuz (Cursor), um das gewünschte Ziel zu lokalisieren.
- Platzieren Sie das Fadenkreuz (Cursor) an der Position des gewünschten Ziels und verwenden Sie die Winkelumschalter auf der rechten Seite des Bildschirms, um den Flugbahnwinkel einzustellen.
- Sobald das gewünschte Ziel und die gewünschte Trajektorie ausgewählt sind, klicken Sie auf das Dropdown-Menü Neu und wählen Sie Trajectory. Benennen Sie das Ziel, indem Sie es in das Textfeld neben "Name:" eingeben.
- Exportieren Sie das Ziel, indem Sie auf Exportieren... klicken und speichern Sie es im entsprechenden Betreffordner. Nachdem die Datei gespeichert wurde, kann die Planung pausiert und das Experiment später neu gestartet werden.
HINWEIS: Das Ziel wird in den nachfolgenden Schritten verwendet, um thermische und akustische Simulationen durchzuführen.
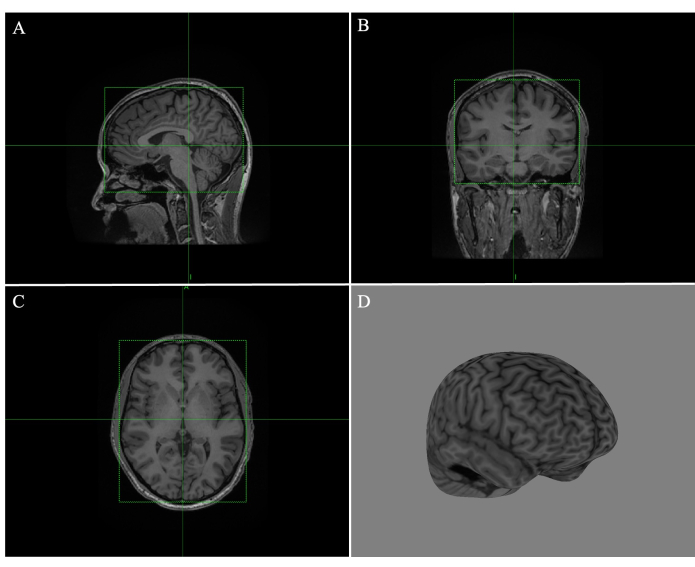
Abbildung 1: Erstellen einer vollständigen Gehirnkrümmung in Brainsight. (A) Box angepasst an den Rand des sagittalen MRT-Bildes. (B) Box, die an den Rand des koronalen MRT-Bildes angepasst ist. (C) Box, die an den Rand des transversalen MRT-Bildes angepasst ist. (D) Krümmungsrekonstruktion des gesamten Gehirns mit einer Schältiefe von 4 mm. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
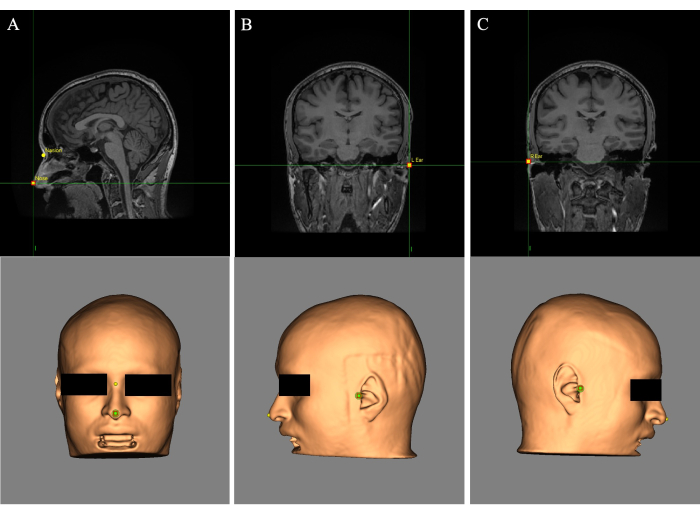
Abbildung 2: Orientierungspunkte auf der Hautrekonstruktion und dem MRT-Bild. (A) Platzierung der Orientierungspunkte an Nase und Nase. (B) Platzierung des Orientierungspunkts am linken Ohr. (C) Platzierung des Orientierungspunkts am rechten Ohr. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
4. Simulationen mit BabelBrain
HINWEIS: Details zur Simulation mit BabelBrain finden Sie im BabelBrain-Handbuch: https://proteusmrighifu.github.io/BabelBrain/index.html.
- Öffnen Sie BabelBrain und wählen Sie die benötigten Dateien für akustische und thermische Simulationen aus.
HINWEIS: In dieser Einreichung wird ein Phased-Array-Wandler verwendet; Andere Schallköpfe sind jedoch vollständig mit dieser Planungssoftware kompatibel. Dieses Programm kann Simulationen für Single-, CTX_500-, H-317-, H-246- und Wandler durchführen. Bei der folgenden Methode wird der H-317 als ausgewählter Schallkopf verwendet.- Wählen Sie die txt-Datei aus, die zuvor in Schritt 3.7.3 aus Brainsight exportiert wurde, indem Sie auf Trajektorie auswählen... klicken und die entsprechende Teilnehmerdatei auswählen. Klicken Sie auf SimNIBS auswählen... , um die in Schritt 2 erstellte SimNIBS-Datei (m2m_folder Namen) auszuwählen. Klicken Sie auf T1W... auswählen und wählen Sie das in Schritt 2.1 erzeugte T1-w-Bild aus, das zuvor für die Ziel- und Trajektorienkartierung verwendet wurde.
- Wählen Sie in der Dropdown-Liste neben der Beschriftung "CT verwenden?" die Option "Echte CT " aus, wenn Sie einen CT-Scan verwenden, "ZTE ", wenn Sie einen ZTE-Scan verwenden, oder "NEIN ", wenn Sie eine vereinfachte Maske verwenden, die mit dem Charm-Werkzeug generiert wurde, wenn nur T1- und T2-w-Bilder verfügbar sind. Wenn Sie ein CT- oder ZTE-Bild verwenden, klicken Sie auf das Dropdown-Menü Correg.? und dann auf CT zu MR. Klicken Sie auf Auswählen und wählen Sie das entsprechende Bild aus der entsprechenden Teilnehmerdatei aus.
- Klicken Sie auf "Thermisches Profil auswählen ..." und wählen Sie die thermische Profildatei aus, die die Beschallungsparameter des Experiments in Bezug auf Dauer ein, Dauer aus und Einschaltdauer beschreibt.
HINWEIS: Details können im Handbuch von BabelBrain eingesehen werden: https://proteusmrighifu.github.io/BabelBrain/index.html. Beispiele für Profile finden Sie unter https://github.com/ProteusMRIgHIFU/BabelBrain/tree/main/Profiles. - Klicken Sie auf das Dropdown-Menü neben "Schallkopf" und wählen Sie den Wandler aus, der zum Experimentieren verwendet wird. Klicken Sie auf das Dropdown-Menü neben "Computing-Backend" und wählen Sie das Computing-Backend des Computers aus, auf dem die Simulationen ausgeführt werden. Sobald Sie alle Informationen eingegeben haben, klicken Sie auf WEITER , um den Rest der Simulationen abzuschließen.
- Unterschritt A: Maske berechnen.
- Wählen Sie die Ultraschallfrequenz des Schallkopfs und den entsprechenden Punkt pro Wellenlänge (PPW) aus.
HINWEIS: 6 ppw sind für die meisten Szenarien ausreichend. - Lassen Sie den normalisierten ZTE-Bereich und die Hounsfield-Einheiten (HU) unverändert.
HINWEIS: Wenn Sie einen echten CT verwenden, wird nur der HU-Schwellenwert angezeigt. Wenn kein ZTE- oder CT-Scan bereitgestellt wird, fehlt dieser Eintrag. - Klicken Sie auf Planungsmaske berechnen. Überprüfen Sie das Bild und stellen Sie sicher, dass die Grenzen für Haut, Schädel und Gehirn genau erkannt wurden.
HINWEIS: Wenn Unstimmigkeiten vorhanden sind, passen Sie den normalisierten ZTE-Bereich und/oder den HU-Schwellenwert an.
- Wählen Sie die Ultraschallfrequenz des Schallkopfs und den entsprechenden Punkt pro Wellenlänge (PPW) aus.
- Teilschritt B: Akustische Simulation. Klicken Sie auf die Registerkarte Schritt 2 - Ac Sim, um sie zu öffnen.
HINWEIS: Diese Registerkarte sieht je nach ausgewähltem Schallkopf unterschiedlich aus. Was folgt, ist spezifisch für den H-317-Schallkopf.- Passen Sie den Abstand vom zu fokussierenden Kegel an, um den Abstand von der Oberfläche des Kegels zum Ziel widerzuspiegeln, indem Sie den entsprechenden Abstand eingeben.
HINWEIS: Dies wird durch den physikalischen Kegel vorgegeben, der in Experimenten verwendet werden soll. - Führen Sie die Simulation aus, indem Sie auf die Schaltfläche Felder berechnen klicken.
- Passen Sie den Wert für die Z-Lenkung (mm) so an, dass sich das Fadenkreuz (das Ziel anzeigt) in der Mitte des Fokuspunkts befindet (Abbildung 3). Drücken Sie die Pfeile nach oben oder unten oder geben Sie den gewünschten Wert manuell ein und klicken Sie dann auf Felder berechnen.
HINWEIS: Positive Werte lenken den Brennfleck tiefer in das Gehirn, während negative Werte dazu führen, dass sich der Brennpunkt oberflächlich bewegt. - Stellen Sie die mechanische X/Y-Empfindlichkeit ein, wenn sich der Brennfleck lateral zum gewünschten Ziel befindet. Lassen Sie Z mechanisch unverändert. Klicken Sie auf Felder berechnen.
HINWEIS: Die mechanische Z-Geschwindigkeit wird in Abhängigkeit vom Abstand vom Kegel in 4.3.1 neu berechnet. Falls es erforderlich ist, die Z-Lenkung, die mechanische X/Y-Lenkung oder die maximale Tiefe über das Ziel hinaus nach Abschluss einer Berechnung anzupassen, müssen die akustischen Simulationsdateien neu berechnet werden. Klicken Sie auf Felder berechnen und wählen Sie Ja , um neu zu berechnen. Wählen Sie Nein aus, um die vorhandenen Dateien erneut zu laden.
- Passen Sie den Abstand vom zu fokussierenden Kegel an, um den Abstand von der Oberfläche des Kegels zum Ziel widerzuspiegeln, indem Sie den entsprechenden Abstand eingeben.
- Teilschritt C: Thermische Simulation. Klicken Sie auf die Registerkarte Step 3 - Thermal Sim und dann auf Calculate Thermal Fields. Bewertung der mechanischen und thermischen Simulationen (Abbildung 4), um sicherzustellen, dass sie den akustischen Richtlinien bei menschlichen Probanden entsprechen, wie sie von ITRUSST31 empfohlen werden (Mechanischer Index (MI) im Weichgewebe ≤1,9; thermischer Anstieg ≤2 °C, thermische Dosis ≤0,25 CEM43, Expositionszeit begrenzt auf 80 min für 1,5 < kranialer thermischer Index (TIC) ≤ 2,0, 40 min für 2,0 < TIC ≤ 2,5, 10 min für 2,5 < TIC ≤ 3.0, 160 s für 3.0 < TIC ≤ 4.0, 40 s für 4.0 < TIC ≤ 5.0 und 10 s für 5.0 < TIC ≤ 6.0).
HINWEIS: BabelBrain löst die Biowärmeübertragungsgleichung, um den Temperaturanstieg36 zu schätzen. In seltenen Fällen können abnormale Hochtemperaturvoxel auftreten, in diesem Fall sollten MRT-Bilder analysiert werden, wenn anatomische Merkmale den ungewöhnlichen Temperaturanstieg erklären könnten.- Passen Sie denI sppa an, indem Sie auf die Pfeile nach oben oder unten neben dem Feld Isppa (W/cm 2) klicken oder manuell einen Wert über 0,1 eingeben, um zu beobachten, wie sich die Parameter mit unterschiedlichen Intensitäten ändern.
HINWEIS: Eine Zusammenfassung aller Intensitäten, Temperaturänderungen und mechanischen Indizes kann als Referenz als CSV-Datei exportiert werden. Die Software berechnet die erforderliche Intensität unter Wasserbedingungen (Isppa in Wasser), die angewendet werden muss, um die gewünschte Intensität vor Ort zu erreichen. - Klicken Sie auf die Schaltflächen MTB, MTS und MTC im unteren Bereich der Benutzeroberfläche, um die Scheibe mit der höchsten Temperatur im Gehirn, in der Haut und im Schädel anzuzeigen. Nachdem der Schritt der thermischen Simulation abgeschlossen ist, sind die Simulationen abgeschlossen.
HINWEIS: Dateien werden automatisch am selben Speicherort wie das T1-w-Bild gespeichert.
HINWEIS: Akustische Dateien mit einer Endung <... FullElasticSolution_Sub_NORM.nii.gz> können in Brainsight geladen werden, um die Überlagerung des akustischen Feldes im T1-Raum zu visualisieren. Es wird Dateien für reine Wasserbedingungen (mit dem Infix "Water" im Dateinamen) und Dateien für Gewebe-Zustände (kein Infix im Dateinamen) geben. Befolgen Sie die Schritte im Hinweis nach Schritt 3.1, um ein Overlay hinzuzufügen. Nach dem Schritt der thermischen Simulation sind die Simulationen abgeschlossen, und das Experiment kann bis zur TUS-Liefersitzung pausiert werden.
- Passen Sie denI sppa an, indem Sie auf die Pfeile nach oben oder unten neben dem Feld Isppa (W/cm 2) klicken oder manuell einen Wert über 0,1 eingeben, um zu beobachten, wie sich die Parameter mit unterschiedlichen Intensitäten ändern.
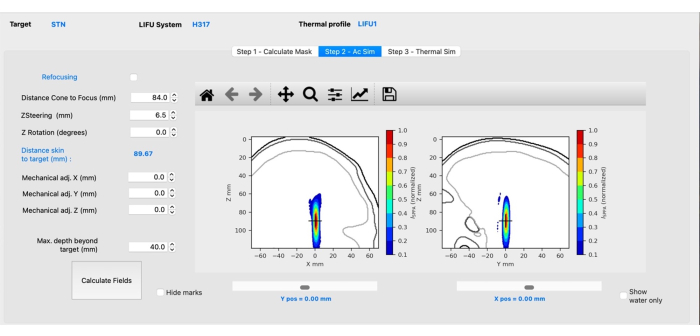
Abbildung 3: Akustische Simulation mit BabelBrain. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
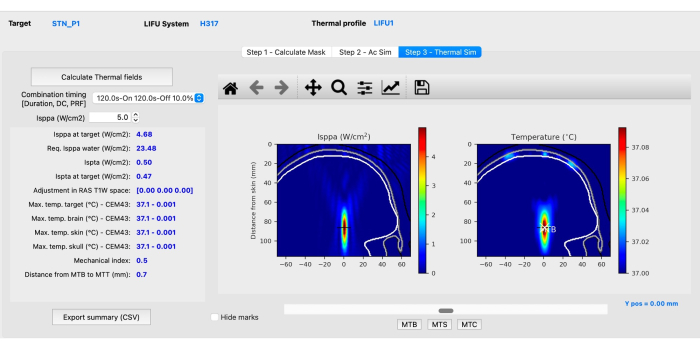
Abbildung 4: Thermische Simulation mit BabelBrain. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
5. TUS-Liefersitzung
- Öffnen Sie Brainsight und klicken Sie auf Vorhandenes Projekt öffnen. Wählen Sie die Brainsight-Datei aus, die während der Trajektorien- und Zielzuordnung erstellt und gespeichert wurde.
- Klicken Sie auf Sitzungen , um eine neue Experimentiersitzung zu starten. Klicken Sie auf das Dropdown-Menü und wählen Sie Neu und dann Online-Sitzung aus. Klicken Sie auf den Namen des Ziels , gefolgt von Hinzufügen und Weiter , um das Ziel zur Experimentsitzung hinzuzufügen und mit dem Experimentierfenster fortzufahren.
HINWEIS: Wenn die TUS-Lieferung mit einem anderen Computer durchgeführt wird als dem, der für die Planung verwendet wurde, muss für Brainsight das entsprechende T1-w-Bild ausgewählt werden. In diesem Fall wird ein neues Fenster geöffnet, in dem Sie aufgefordert werden, das zugehörige T1-w-Teilnehmerbild aus der Teilnehmerdatei auszuwählen. - Klicken Sie auf Fenster und Werkzeugkalibrierung und wählen Sie die zu verwendenden Werkzeuge aus, gefolgt von Neu kalibrieren.
HINWEIS: Dieser Schritt muss für den Wandler und alle anderen während der Versuchssitzung verwendeten Werkzeuge, wie z. B. eine TMS-Spule, durchgeführt werden.- Befestigen Sie den großen Spulentracker und den Kalibrierblock am Wandler. Stellen Sie sicher, dass die Kamera die Passermarken auf beiden Tools sehen kann. Klicken Sie auf Kalibrierungs-Countdown starten , um die Kalibrierung neu zu kalibrieren.
HINWEIS: Durch das Speichern der Kalibrierung wird sichergestellt, dass sie für den Experimenttag gleich bleibt. Wenn dies nicht der Fall ist und sich der Computer ausschaltet, muss das Gerät neu kalibriert werden.
- Befestigen Sie den großen Spulentracker und den Kalibrierblock am Wandler. Stellen Sie sicher, dass die Kamera die Passermarken auf beiden Tools sehen kann. Klicken Sie auf Kalibrierungs-Countdown starten , um die Kalibrierung neu zu kalibrieren.
- Richten Sie den Schallkopf entsprechend den Einstellverfahren für Experimente ein. Entfernen Sie den Tracker am Geber, bevor Sie ihn aufstellen, damit er nicht beschädigt wird.
HINWEIS: Der beschriebene Aufbau gilt für den Geber H-317 mit einem kundenspezifischen Koppelkonus.- Montieren Sie den Konus nach Bedarf und platzieren Sie die Schallkopffolie zwischen dem Konus und der Endkappe. Befestigen Sie den Kupplungskegel mit Schrauben, Unterlegscheiben und Muttern am Flansch des Wandlers und stellen Sie sicher, dass alle fest sitzen, damit keine Lecks auftreten.
- Füllen Sie den Wandler mit entionisiertem Wasser und befestigen Sie die Schläuche von der Pumpe an den Wandler, indem Sie den Schlauch mit der Bezeichnung "IN" mit "OUT" und den "OUT" mit "IN" verbinden. Verstopfen Sie das Wasserloch, während Sie "DRAIN" an der Pumpe drücken, um den Druck zu entlasten.
- Drehen Sie den Wandler auf den Kopf, um die Luftblasen auf der Folie zu isolieren, und drehen Sie ihn dann nach oben, sodass sie durch das Wandlerrohr mit der Bezeichnung "OUT" austreten können. Wiederholen Sie dies, bis alle sichtbaren Luftblasen entfernt sind. Stellen Sie den Wandler so ein, dass das "OUT"-Rohr nach vorne und am höchsten Punkt abgewinkelt ist, und lassen Sie die Pumpe 30 Minuten lang laufen.
- Drehen Sie den Wandler auf den Kopf, um sicherzustellen, dass alle Luftblasen entfernt wurden. Wenn noch welche übrig sind, isolieren Sie die Luftblasen auf der Folie und drehen Sie den Wandler wie zuvor, um sicherzustellen, dass sie durch das "OUT"-Rohr austreten. Wiederholen Sie den Vorgang, bis alle Blasen entfernt wurden.
- Schalten Sie die Pumpe aus, lösen Sie die Schläuche und verriegeln Sie den Wandler auf Neutralstellung. Befestigen Sie den Tracker wieder an dem Geber und fahren Sie mit der Einrichtung der Teilnehmer fort.
- Befestigen Sie den Probanden-Tracker entweder mit einer Brille, einem Stirnband über den Ohren und Augenbrauen (Abbildung 5) oder dem leichten Klebetracker am Kopf des Teilnehmers. Stellen Sie sicher, dass die Passermarken so ausgerichtet sind, dass sie für die Kamera sichtbar sind und nicht vom Geber blockiert oder getroffen werden, wenn er sich auf ihn zubewegt oder seine endgültige Position erreicht hat.
- Platzieren Sie die Kamera vor dem Teilnehmer, sodass sie den Motiv-Tracker und den Zeiger sehen kann.
HINWEIS: Wenn sie nicht sichtbar sind, leuchtet die Anzeige unten links auf dem Bildschirm rot. Dies kann auch überprüft werden, indem Sie die Registerkarte "Polaris" in Brainsight aufrufen.
- Platzieren Sie die Kamera vor dem Teilnehmer, sodass sie den Motiv-Tracker und den Zeiger sehen kann.
- Klicken Sie in Brainsight auf die Registerkarte Registrierung . Platzieren Sie den Zeiger auf alle vier Orientierungspunkte, die in Schritt 3.6 festgelegt wurden, stabilisieren Sie ihn mit beiden Händen und klicken Sie dann auf Sample & Go To Next Landmark.
HINWEIS: Es ist wichtig, dass das Stirnband oder die Brille eng am Kopf des Teilnehmers anliegt und dass sich der Motiv-Tracker nicht bewegt. Führen Sie in diesem Fall die Registrierung erneut durch. Wenn die Passermarken gedreht werden müssen, um die Bewegung des Schallkopfs nach Abschluss der Registrierung zu ermöglichen, wiederholen Sie die Registrierung. - Klicken Sie auf die Registerkarte Validierung , um die Teilnehmerregistrierung zu validieren. Platzieren Sie den Zeiger leicht an verschiedenen Positionen entlang der Kopfhaut und stellen Sie sicher, dass alle Spitzen weniger als 3 mm groß sind.
HINWEIS: Kommerzielle Neuronavigationssysteme, die für TMS entwickelt wurden, werden für TUS-Experimente am Menschen verwendet. Ein Translationsfehler von 3 mm ist für die Kalibrierung von Handschallköpfen37 akzeptabel, da er mit der Zielgenauigkeit38, 39 und anderen Neuronavigationssystemen40 übereinstimmt. Der Wert von 3 mm ist in die Neuronavigationssoftware Brainsight eingebettet.- Wenn Punkte größer als 3 mm sind, klicken Sie auf die Schaltfläche Hinzufügen , um zusätzliche Orientierungspunkte für bis zu maximal drei Punkte hinzuzufügen. Wenn mehr als drei Punkte erforderlich sind, um eine konsistente Validierung unter 3 mm zu erreichen, wiederholen Sie die Registrierung.
HINWEIS: Um den Erfolg der Registrierung zu verbessern, wird empfohlen, MRT-Bilder zu sammeln, ohne dass der Teilnehmer Over-Ear-Kopfhörer trägt, da dies die Bildrekonstruktion beeinträchtigen und die Registrierung erschweren kann. Achten Sie darauf, dass der Zeiger so nah wie möglich an der Landmarke platziert wird, bevor Sie auf Sample & Go To Next Landmark klicken, und stellen Sie sicher, dass der Zeiger mit beiden Händen stabilisiert wird. Die Validierung bietet die Gewissheit, dass der Durchschnitt aller Punkte entlang der Kopfhautoberfläche unter dem Schwellenwert liegt. Fahren Sie nicht fort, bis alle zufälligen Stellen auf der Kopfhaut unter dem Schwellenwert von 3 mm liegen.
- Wenn Punkte größer als 3 mm sind, klicken Sie auf die Schaltfläche Hinzufügen , um zusätzliche Orientierungspunkte für bis zu maximal drei Punkte hinzuzufügen. Wenn mehr als drei Punkte erforderlich sind, um eine konsistente Validierung unter 3 mm zu erreichen, wiederholen Sie die Registrierung.
- Sichern Sie den Kopf des Teilnehmers mit der Kinnstütze und dem Stabilisator, die auf dem Hinterkopf platziert sind, um Bewegungen zu verhindern (Abbildung 5). Stellen Sie sicher, dass sie für die Dauer des Experiments bequem auf dem Stuhl sitzen.
- Klicken Sie auf Ausführen. Verwenden Sie den mechanischen Arm, um den Wandler über dem Zielobjekt entlang der ausgewählten Flugbahn zu positionieren.
HINWEIS: Stellen Sie sicher, dass Sie üben und sich damit vertraut machen, wie sich die Komponenten des mechanischen Arms bewegen, um das Ziel zu erreichen. Der Erfolg bei der Positionierung des mechanischen Arms beruht darauf, dass man die Beweglichkeit des Arms versteht und weiß, wie er sich um die Kopfausrichtung bewegt, da dies stark von der Position des Ziels abhängt.- Verwenden Sie das Fadenkreuz am Bullseye-Fenster, um die richtige Positionierung und den richtigen Winkel zu erreichen (Abbildung 6). Richten Sie beide Kreise (translatorisch und rotierend) so aus, dass sie auf dem Fadenkreuz positioniert sind, und beziehen Sie sich zur Überprüfung auf den Genauigkeitsmesswert.
- Teilen Sie das Haar des Probanden entlang seines natürlichen Teils und kämmen Sie das Ultraschallgel ein, um sicherzustellen, dass keine Lufteinschlüsse im Haar vorhanden sind. Wenn eine große Fläche gekoppelt werden muss, tragen Sie Ultraschallgel auf die Schallkopffolie auf. Füllen Sie die verbleibenden Lufteinschlüsse mit einer Spritze mit zusätzlichem Ultraschallgel.
- Senken Sie den Wandler auf die entsprechende Höhe ab, indem Sie beobachten, wann sich das Fadenkreuz in der Mitte des Kastens befindet, der das Ziel umgibt (Abbildung 6). Dies zeigt an, wann die entsprechende Zieltiefe erreicht ist.
- Ein maßgeschneidertes Python-Skript verwendet die Ergebnisse der Simulationen in Schritt 4, um die Einheit mit 128 Verstärkern zu programmieren und Ton über Kopfhörer (https://github.com/ProteusMRIgHIFU/TUSApp) zu erzeugen. Wenn ein Online- und/oder Doppelblindexperiment durchgeführt wird, stellen Sie sicher, dass der Maskierungston über Kopfhörer34, 41 abgespielt wird, oder erhöhen Sie das Ein- und Ausschalten des Stimulus über die Burst-Dauer42, 43, 44 als Methoden zur Verringerung potenzieller auditiver Störeffekte.
HINWEIS: Wenn Sie in diesem Schritt ein handelsübliches Gerät verwenden, z. B. einen CTX-500-Wandler, schreiben Sie die Intensität vor, die unter Wasserbedingungen simuliert wurde, zusammen mit anderen Parametern (PRF, Dauer, Einschaltdauer). Der H-317-Schallkopf verwendet ein spezielles Skript, um den Schallkopf auszuführen. Daher wird dieser Schritt in der vorliegenden Stellungnahme nicht berücksichtigt.- Generieren Sie das Maskierungsaudio in MATLAB, das nach dem Start der TUS-Bereitstellung abgespielt werden soll. Der Klang während der Scheinstimulation kombiniert eine kontinuierliche Sündenwelle bei 250 kHz, eine Rechteckwelle mit einer Burstfrequenz von 100 Hz, die bei 48 kHz abgetastet wird, mit zufälligem Rauschen, um den vom Wandler erzeugten Klang genau zu replizieren. Während der TUS wird nur zufälliges Rauschen über den Kopfhörer abgespielt, da der vom Schallwandler abgegebene Ton auch vom Probanden gehört wird.
- Entfernen Sie nach Abschluss der TUS-Verabreichung den Schallkopf, das Gel und den Tracker vom Kopf des Teilnehmers, bevor Sie alle nachfolgenden experimentellen Verfahren durchführen.
- Um das TUS-Gerät zu reinigen, entfernen Sie den Tracker vom Geber, um Schäden zu vermeiden. Zerlegen Sie den Wandler, indem Sie den Stopfen an der Oberseite entfernen und auf den Kopf stellen, um das Wasser abzulassen. Entfernen Sie den Kupplungskegel und zerlegen Sie ihn, damit die Teile an der Luft trocknen können.
- Stellen Sie den Schallkopf wieder in den Leerlauf und stellen Sie sicher, dass alle Armkomponenten im 90°-Winkel verriegelt sind, um ihn bis zur nächsten TUS-Versuchssitzung zu lagern.

Abbildung 5: Fiducials, die für die Neuronavigation verwendet werden sollen. Brille (links) und Stirnband (rechts) mit Passermarken zur Motivverfolgung. Der Kopf des Probanden wird mit einer Kinnstütze und einem Stabilisator hinter dem Kopf gesichert. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
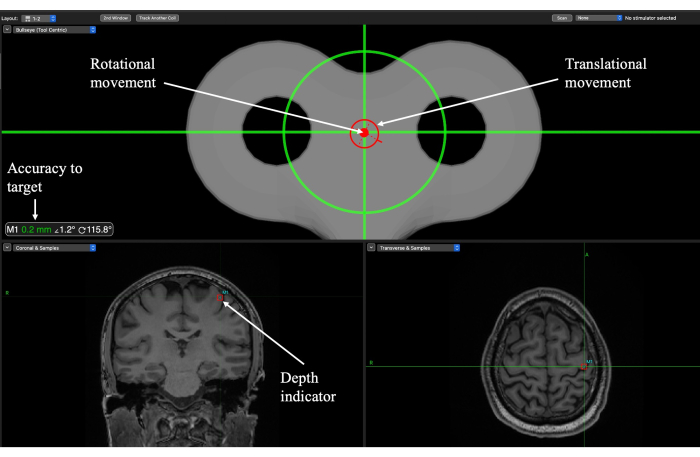
Abbildung 6: Brainsight Neuronavigationsbildschirm für die Ziellokalisierung während der TUS-Verabreichungssitzung für ein primäres Ziel des motorischen Kortex (M1). Rotations- und Translationsindikatoren leiten den Experimentator an, wo er den Schallkopf über der Kopfhaut positionieren muss und wann der Flugbahnwinkel erreicht ist. Die Genauigkeit zum Ziel gibt an, wie nah die Translations- und Rotationsorientierung am Ziel liegt, und sollte zur Feinabstimmung der Bewegung verwendet werden. Der Tiefenanzeiger zeigt die Tiefe des Brennflecks an und sollte verwendet werden, um den Schallkopf auf die entsprechende Höhe abzusenken. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Ergebnisse
Abbildung 7 zeigt vergleichende Sitzungsproben aus einer unserer Studien42 mit zwei unterschiedlichen Teilnehmern, die spezifische Ultraschallparameter verwendeten (Grundfrequenz von 250 kHz, Beschallungsdauer von 120 s, eine Impulswiederholfrequenz (PRF) von 100 Hz, ein Tastverhältnis von 10 % und eineI SPPA von 5 W/cm²). In dieser Studie wurden T1-, T2-w- und ZTE-MRT-Scans mit einer isotropen Auflösung von 1 mm von neurologisch gesunden Probanden erhal...
Diskussion
Bei dieser Methode werden fachspezifische Simulationen durchgeführt, um mögliche thermische und mechanische Effekte, die sich aus der TUS-Anwendung auf das Gehirn ergeben, vorherzusagen und zu bewerten. Die Datensätze zwischen den Teilnehmern müssen getrennt und sorgfältig dokumentiert werden, da die Verwendung eines falschen Scans oder einer falschen Datei zu ungenauen Simulationen führt. Wenn zahlreiche Teilnehmerscans gesammelt werden und die Planung gemeinsam durchgeführt wird, ist es wichtig, auf eine korrekt...
Offenlegungen
Die Autoren haben keine Interessenkonflikte anzugeben.
Danksagungen
Diese Arbeit wurde teilweise durch einen Discovery Grant des Natural Sciences and Engineering Research Council of Canada, das INNOVAIT-Programm, den Cumming Medical Research Fund, die Canada Foundation for Innovation (Project 36703), den Hotchkiss Brain Institute CAPRI Grant und die Parkinson Association of Alberta Funding unterstützt. GBP bedankt sich für die Unterstützung durch die Canadian Institutes for Health Research (FDN-143290) und das Campus Alberta Innovates Chair Program.
Materialien
| Name | Company | Catalog Number | Comments |
| 128-channel amplifier unit | Image Guided Therapy | This unit drives the H-317 transducer | |
| 24-channel head coil | General Electric | ||
| 3D printer | Raise3D | Pro2 | Filament thickness of 1.75mm. |
| 3T MRI scanner | General Electric | Discovery 750 HD | MR Console version DV26.0_R05_2008 |
| BabelBrain | Samuel Pichardo (University of Calgary) | Version 0.3.0 | Accessible at https://github.com/ProteusMRIgHIFU/BabelBrain. Executes thermal and acoustic simulations. |
| Blender | Blender Foundation | Version 3.4.1 | Accessible at https://www.blender.org. Blender is called automatically by BabelBrain. |
| Brainsight | Rogue Research | Version 2.5.2 | Used for target identification, trajectory planning, and execution of TUS delivery sessions. |
| Chair and chin/head holder | Rogue Research | To be used during TUS delivery session to ensure stability of participant’s head for optimized targeting. | |
| Custom-made coupling cone | University of Calgary team | 3D printed cone in acrylonitrile butadiene styrene (ABS), only required for H-317 transducer. | |
| dcm2niix | Chris Rorden (University of South Carolina) | Version 1.0.20220720 | Accessible at https://github.com/rordenlab/dcm2niix/releases. Used for pre-processing subject MR images. |
| Fiducials and headband or glasses | Brainsight, Rogue Research | ST-1325 (subject tracker), LCT-583 (large coil tracker) | Headband or glasses can be interchangeably used. |
| Headphones | Beats | Fit Pro True Wireless Earbuds | Wireless Bluetooth earbuds with disposable tips. |
| MacBookPro | Apple | M2 Max, 16”, 64GB RAM | Computer for completing trajectory planning and simulations |
| SimNIBS | Axel Thielscher (Technical University of Denmark) | Version 4.0.0 | Accessible at https://simnibs.github.io/simnibs/build/html.index.html |
| Syringe(s) | 10 mL, 60 mL | Used to add additional ultrasound gel to fill air pockets. | |
| Transducer | Sonicconcepts | H-317 | Other supported transducers include CTX_500 (NeuroFUS, Sonicconcepts), Single element, H-246 (Sonicconcepts), and Bsonix (Brainsonix) |
| Transducer film | Sonicconcepts | Polyurethane membrane | Interface between transducer and the subject |
| Ultrasound gel | Wavelength | Clear Ultrasound Gel | Coupling medium. |
| Windows Laptop | Acer | Aspire A717-71G, Intel Core i7-7700HQ, 16 GB RAM | System used to control 128-channel amplifier and generate sound through the headphones |
Referenzen
- Baek, H., Pahk, K. J., Kim, H. A review of low-intensity focused ultrasound for neuromodulation. Biomed Eng Lett. 7 (2), 135-142 (2017).
- Rezayat, E., Toostani, I. G. A review on brain stimulation using low intensity focused ultrasound. Basic Clin Neurosci. 7 (3), 187-194 (2016).
- Dell'Italia, J., Sanguinetti, J. L., Monti, M. M., Bystritsky, A., Reggente, N. Current state of potential mechanisms supporting low intensity focused ultrasound for neuromodulation. Front Hum Neurosci. 16, 872639 (2022).
- Kim, H., et al. Suppression of EEG visual-evoked potentials in rats through neuromodulatory focused ultrasound. Neuroreport. 26 (4), 211-215 (2015).
- Yoon, K., et al. Effects of sonication parameters on transcranial focused ultrasound brain stimulation in an ovine model. PLoS One. 14 (10), e0224311 (2019).
- Dallapiazza, R. F., et al. Non-invasive neuromodulation and thalamic mapping with low-intensity focused ultrasound. J Neurosurg. 128 (3), 875-884 (2018).
- Folloni, D., et al. Manipulation of subcortical and deep cortical activity in the primate brain using transcranial focused ultrasound stimulation. Neuron. 101 (6), 1109-1116 (2019).
- Gulick, D. W., Li, T., Kleim, J. A., Towe, B. C. Comparison of electrical and ultrasound neurostimulation in rat motor cortex. Ultrasound Med Biol. 43 (12), 2824-2833 (2017).
- King, R. L., Brown, J. R., Newsome, W. T., Pauly, K. B. Effective parameters for ultrasound-induced in vivo neurostimulation. Ultrasound Med Biol. 39 (2), 312-331 (2013).
- Yoo, S. S., et al. Focused ultrasound modulates region-specific brain activity. Neuroimage. 56 (3), 1267-1275 (2011).
- Kim, H. C., et al. Transcranial focused ultrasound modulates cortical and thalamic motor activity in awake sheep. Sci Rep. 11 (1), 19274 (2021).
- Deffieux, T., et al. Low-intensity focused ultrasound modulates monkey visuomotor behavior. Curr Biol. 23 (23), 2430-2433 (2013).
- Munoz, F., et al. Long term study of motivational and cognitive effects of low-intensity focused ultrasound neuromodulation in the dorsal striatum of nonhuman primates. Brain Stimul. 15 (2), 360-372 (2022).
- Verhagen, L., et al. Offline impact of transcranial focused ultrasound on cortical activation in primates. ELife. 8, e40541 (2019).
- Fomenko, A., et al. Systematic examination of low-intensity ultrasound parameters on human motor cortex excitability and behavior. ELife. 9, e54497 (2020).
- Legon, W., Bansal, P., Tyshynsky, R., Ai, L., Mueller, J. K. Transcranial focused ultrasound neuromodulation of the human primary motor cortex. Sci Rep. 8 (1), 10007 (2018).
- Legon, W., et al. Transcranial focused ultrasound modulates the activity of primary somatosensory cortex in humans. Nat Neurosci. 17 (2), 322-329 (2014).
- Legon, W., Ai, L., Bansal, P., Mueller, J. K. Neuromodulation with single-element transcranial focused ultrasound in human thalamus. Hum Brain Mapp. 39 (5), 1995-2006 (2018).
- Legon, W., et al. A retrospective qualitative report of symptoms and safety from transcranial focused ultrasound for neuromodulation in humans. Sci Rep. 10, 5573 (2020).
- Forster, A., et al. Investigating the role of the right inferior frontal gyrus in control perception: A double-blind cross-over study using ultrasonic neuromodulation. Neuropsychologia. 187, 108589 (2023).
- Forster, A., et al. Transcranial focused ultrasound modulates the emergence of learned helplessness via midline theta modification. J Affect Disord. 329, 273-284 (2023).
- Ziebell, P., et al. Inhibition of midfrontal theta with transcranial ultrasound explains greater approach versus withdrawal behavior in humans. Brain Stimul. 16 (5), 1278-1288 (2023).
- Kim, H. C., Lee, W., Weisholtz, D. S., Yoo, S. S. Transcranial focused ultrasound stimulation of cortical and thalamic somatosensory areas in human. PLoS One. 18 (7), e0288654 (2023).
- Kim, Y. G., et al. Neuromodulation using transcranial focused ultrasound on the bilateral medial prefrontal cortex. J Clin Med. 11 (13), 3809 (2022).
- Chu, Y. C., Lim, J., Chien, A., Chen, C. C., Wang, J. L. Activation of mechanosensitive ion channels by ultrasound. Ultrasound Med Biol. 48 (10), 1981-1994 (2022).
- Kubanek, J., et al. Ultrasound modulates ion channel currents. Sci Rep. 6 (1), 24170 (2016).
- Prieto, M. L., Firouzi, K., Khuri-Yakub, B. T., Maduke, M. Activation of Piezo1 but not NaV1.2 channels by ultrasound at 43 MHz. Ultrasound Med Biol. 44 (6), 1217-1232 (2018).
- Quarato, C. M. I., et al. A review on biological effects of ultrasounds: Key messages for clinicians. Diagnostics. 13 (5), 855 (2023).
- Nowicki, A. Safety of ultrasonic examinations; thermal and mechanical indices. Med Ultrason. 22 (2), 203 (2020).
- Miller, D. L., et al. Overview of therapeutic ultrasound applications and safety considerations. J Ultrasound Med. 31 (4), 623-634 (2012).
- Aubry, J. F., et al. ITRUSST consensus on biophysical safety for transcranial ultrasonic stimulation. arXiv preprint arXiv. , 2311.05359 (2023).
- Guo, H., et al. Ultrasound produces extensive brain activation via a cochlear pathway. Neuron. 98 (5), 1020-1030 (2018).
- Sato, T., Shapiro, M. G., Tsao, D. Y. Ultrasonic neuromodulation causes widespread cortical activation via an indirect auditory mechanism. Neuron. 98 (5), 1031-1041 (2018).
- Braun, V., Blackmore, J., Cleveland, R. O., Butler, C. R. Transcranial ultrasound stimulation in humans is associated with an auditory confound that can be effectively masked. Brain Stimul. 13 (6), 1527-1534 (2020).
- Martin, E., et al. ITRUSST consensus on standardised reporting for transcranial ultrasound stimulation. Brain Stimul. , S1935861X24000718 (2024).
- Pichardo, S. BabelBrain: An open-source application for prospective modeling of transcranial focused ultrasound for neuromodulation applications. IEEE Trans Ultrason Ferroelectr Freq Control. 70 (7), 587-599 (2023).
- Khoshnevisan, A., Allahabadi, N. S. Neuronavigation: Principles, clinical applications and potential pitfalls. Iran J Psychiatry. 7 (2), 97-103 (2012).
- Xu, L., et al. Characterization of the targeting accuracy of a neuronavigation-guided transcranial fus system in vitro, in vivo, and in silico. IEEE Trans Biomed Eng. 70 (5), 1528-1538 (2023).
- Kuehn, B., et al. Sensor-based neuronavigation: Evaluation of a large continuous patient population. Clin Neurol Neurosurg. 110 (10), 1012-1019 (2008).
- Ambrosini, E., et al. StimTrack: An open-source software for manual transcranial magnetic stimulation coil positioning. J Neurosci Methods. 293, 97-104 (2018).
- Kop, B. R., et al. Auditory confounds can drive online effects of transcranial ultrasonic stimulation in humans. eLife. , (2024).
- Zadeh, A. K., et al. The effect of transcranial ultrasound pulse repetition frequency on sustained inhibition in the human primary motor cortex: A double-blind, sham-controlled study. Brain Stimul. 17 (2), 476-484 (2024).
- Mohammadjavadi, M., et al. Elimination of peripheral auditory pathway activation does not affect motor responses from ultrasound neuromodulation. Brain Stimul. 12 (4), 901-910 (2019).
- Johnstone, A., et al. A range of pulses commonly used for human transcranial ultrasound stimulation are clearly audible. Brain Stimul. 14 (5), 1353-1355 (2021).
- Zeng, K., et al. Induction of human motor cortex plasticity by theta burst transcranial ultrasound stimulation. Ann Neurol. 91 (2), 238-252 (2022).
- Lee, W., et al. Image-guided transcranial focused ultrasound stimulates human primary somatosensory cortex. Sci Rep. 5, 8743 (2015).
- Ridding, M. C., Rothwell, J. C. Is there a future for therapeutic use of transcranial magnetic stimulation. Nat Rev Neurosci. 8 (7), 559-567 (2007).
- Nicolo, P., Ptak, R., Guggisberg, A. G. Variability of behavioural responses to transcranial magnetic stimulation: Origins and predictors. Neuropsychologia. 74, 137-144 (2015).
- Horvath, J. C., Carter, O., Forte, J. D. No significant effect of transcranial direct current stimulation (tDCS) found on simple motor reaction time comparing 15 different simulation protocols. Neuropsychologia. 91, 544-552 (2016).
- Horvath, J. C., Vogrin, S. J., Carter, O., Cook, M. J., Forte, J. D. Effects of a common transcranial direct current stimulation (tDCS) protocol on motor evoked potentials found to be highly variable within individuals over 9 testing sessions. Exp Brain Res. 234 (9), 2629-2642 (2016).
- Angla, C., Larrat, B., Gennisson, J., Chatillon, S. Transcranial ultrasound simulations: A review. Med Phys. 50 (2), 1051-1072 (2023).
- Miller, G. W., Eames, M., Snell, J., Aubry, J. Ultrashort echo-time MRI versus CT for skull aberration correction in MR-guided transcranial focused ultrasound: In vitro comparison on human calvaria. Med Phys. 42 (5), 2223-2233 (2015).
- Miscouridou, M., Pineda-Pardo, J. A., Stagg, C. J., Treeby, B. E., Stanziola, A. Classical and learned MR to pseudo-CT mappings for accurate transcranial ultrasound simulation. IEEE Trans Ultrason Ferroelectr Freq Control. 69 (10), 2896-2905 (2022).
- Pichardo, S., et al. A viscoelastic model for the prediction of transcranial ultrasound propagation: application for the estimation of shear acoustic properties in the human skull. Phys Med Biol. 62 (17), 6938-6962 (2017).
- Pichardo, S. . ProteusMRIgHIFU/BABELVISCOFDTD: Software Library for FDTD of viscoelastic equation using a staggered grid arrangement with support for GPU and CPU backends. , (2024).
- Aubry, J. F., et al. Benchmark problems for transcranial ultrasound simulation: Intercomparison of compressional wave models. J Acoust Soc Am. 152 (2), 1003-1019 (2022).
- Pinton, G., et al. Attenuation, scattering, and absorption of ultrasound in the skull bone: Absorption of ultrasound in the skull bone. Med Phys. 39 (1), 299-307 (2011).
- Chaplin, V., et al. On the accuracy of optically tracked transducers for image-guided transcranial ultrasound. Int J Comput Assist Radiol Surg. 14 (8), 1317-1327 (2019).
- Wu, S. Y., et al. Efficient blood-brain barrier opening in primates with neuronavigation-guided ultrasound and real-time acoustic mapping. Sci Rep. 8 (1), 7978 (2018).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten