Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Generación experimental de carcinoma asociada a los fibroblastos (CAF) a partir de fibroblastos humanos mamarios
En este artículo
Resumen
Carcinoma asociados fibroblastos (CAF), rica en miofibroblastos presentes en el estroma tumoral, juegan un papel importante en la conducción de la progresión del tumor. Hemos desarrollado un modelo de tumor coimplantation xengraft para generar experimentalmente CAF a partir de fibroblastos humanos mamarios. El protocolo describe cómo establecer miofibroblastos CAF que adquirir la capacidad de promover la génesis tumoral.
Resumen
Los carcinomas son los tejidos complejo compuesto por células neoplásicas y un compartimento no canceroso conocido como el "estroma". El estroma está formado por la matriz extracelular (MEC) y una variedad de células mesenquimales, incluyendo fibroblastos, miofibroblastos, células endoteliales, pericitos y leucocitos 1-3.
El estroma asociado al tumor es sensible a importantes señales paracrinas liberada por las células de carcinoma vecinos. Durante el proceso de la enfermedad, a menudo se convierte en el estroma poblada por carcinoma asociado a los fibroblastos (CAF), incluyendo un gran número de miofibroblastos. Estas células han sido previamente extraídos de diferentes tipos de carcinomas humanos para su cultivo in vitro. Una subpoblación de CAF se distingue a través de su regulación de la actina de músculo liso α-(α-SMA) la expresión de 4,5. Estas células son un sello de "fibroblastos activados" que comparten propiedades similares a miofibroblastos commonly observada en los tejidos dañados y fibrosis 6. La presencia de este subgrupo miofibroblástico CAF está muy relacionada con tumores malignos de alto grado y se asocia con mal pronóstico en los pacientes.
Muchos laboratorios, incluido el nuestro, han demostrado que la CAF, cuando se les inyectó células de carcinoma en ratones inmunodeficientes, son capaces de promover la génesis tumoral sustancial 7-10. CAF preparado a partir de pacientes con carcinoma, sin embargo, con frecuencia sufren senescencia durante la propagación de la cultura limitar la extensión de su uso a través de la experimentación en curso. Para superar esta dificultad, hemos desarrollado una nueva técnica para generar experimentalmente inmortalizado humanos líneas de células mamarias CAF (exp-CAF) a partir de fibroblastos humanos de mama, con un pecho coimplantation modelo de xenoinjerto tumoral.
Con el fin de generar exp-CAF, los padres fibroblastos de mama humano, procedente de los tejidos mamoplastia de reducción, fueron los primeros immortalised con hTERT, la subunidad catalítica de la telomerasa holoenzyme, y para expresar las buenas prácticas agrarias y un gen de resistencia a la puromicina. Estas células fueron coimplanted con células MCF-7 humanas de carcinoma de mama que expresan un oncogén ras activado (MCF-7-ras células) en un xenoinjerto de ratón. Después de un período de incubación in vivo, el primer inyectado fibroblastos humanos mamarios se extrajeron de los xenoinjertos de tumores en la base de su resistencia a la puromicina 11.
Hemos observado que el residente de fibroblastos humanos mamarios se han diferenciado, la adopción de un fenotipo tumoral miofibroblástico y adquirió propiedades que promueven durante el curso de la progresión del tumor. Es importante destacar que estas células, que se define como exp-CAF, imitan el fenotipo de promoción tumoral miofibroblástico de CAF aislado de los carcinomas de mama disecados de los pacientes. Nuestra xenoinjerto de tumor derivado de exp-CAF por lo tanto, proporcionar un modelo eficaz para estudiar la biología de la CAF en breas humanost carcinomas. El protocolo descrito también se puede extender para la generación y caracterización de diferentes poblaciones CAF derivados de otros tipos de carcinomas humanos.
Protocolo
1. Aislamiento de los principales cultivos fibroblastos humanos mamario normal
Los procedimientos experimentales para aislar los fibroblastos humanos primarios cultivados mamario normal se describen en la figura. 1A.
- Prepare el buffer de disociación celular, como se describió anteriormente 12: Dulbecco Modificado Medio Eagle (DMEM) con 10% de suero fetal bovino (FCS), penicilina-estreptomicina (200 unidades / ml), la colagenasa tipo I (1 mg / ml) y hialuronidasa ( 125 unidades / ml).
- Lavar el tejido del seno disecados de una mamoplastia de reducción (~ 0.5 gramos) varias veces en tampón fosfato salino (PBS). Picar el tejido en pequeños fragmentos (<1,5 mm 3) el uso de cuchillas de afeitar estéril.
- La transferencia de los fragmentos de tejido en un tubo cónico de 15 ml que contiene una cantidad adecuada de lo anterior disociación celular de amortiguación (10 ml por cada 0,5 gramo de tejido) y agitar durante 1 minuto a máxima velocidad.
- Digerir los fragmentos de tejido en el tampón de disociación celular fo 12-18 horas a 37 ° C con agitación lenta. * Tenga en cuenta que habrá todavía muchas piezas de fragmentos de tejido no se digiere queda en el tubo.
- Incubar el tubo durante 5 minutos a temperatura ambiente sin agitación. Transferir el resultado de células estromales enriquecido sobrenadante a un nuevo tubo cónico con una pipeta serológica de 5 ml.
- Centrifugar la fracción del estroma durante 5 minutos a 250 x g y resuspender el pellet de células en PBS. Se centrifuga de nuevo durante 5 minutos a 250 x g y resuspender el botón celular en DMEM suplementado con 10% FCS. Cultivar las células en DMEM con 10% FCS en una placa de Petri de 15 cm a 37 ° C y el dióxido de carbono al 5%.
- Se propagan las células hasta confluencia. Por lo general, se llevará a 8-10 días. Almacenar las células a -80 ° C con medio de congelación (10% dimetilsulfóxido y el 20% de FCS en DMEM). Prepare 5 viales congelados como un stock original. Descongelar un vial y expandir las células para preparar 5 viales de la población de secundaria que contienen fibroblastos pasajes de la población dentro de los 5duplicaciones (PD) para los experimentos posteriores. Estos procedimientos de selección clonal y minimizar el estrés cultural que pueden presentarse durante el cultivo de tejidos extendidos. * Tenga en cuenta que P1.1-7 también se puede utilizar para el aislamiento de los CAF de carcinomas de mama obtenida por una mastectomía 12.
2. Generación de buenas prácticas agrarias de etiquetado, puromicina resistente, inmortalizado fibroblastos humanos mamario normal
- Para inmortalizar la primaria fibroblastos humanos normales mamaria aislada en P1.7), introducir un retroviral pMIG (MSCV-IRES-GFP) 12 vector, expresando hTERT y las buenas prácticas agrarias. Cultivar las células durante 4-5 días y luego ordenar las buenas prácticas agrarias de células positivas mediante citometría de flujo.
- Introducir un retroviral pBabe-puro construcción que codifica un gen de resistencia a la puromicina fibroblastos inmortalizados GFP-etiquetados. Cultivar las células durante 5-7 días en presencia de puromicina (concentración final: 1 mg / ml) para aislar el GFP-positivo (GFP +), resistentes a la puromicina (puro R ) inmortalizado fibroblastos humanos mamarios.
- A continuación, para examinar si estos fibroblastos producen los virus activos, lo que puede conducir a la transferencia horizontal de genes que codifican las buenas prácticas agrarias y la resistencia a la puromicina, crecer 2.5x10 5 GFP + puro R inmortalizado fibroblastos humanos de mama en una placa de Petri de 6 cm por 2 días.
- Medio filtrante condicionada por estos fibroblastos utilizando un filtro de jeringa (tamaño de poro: 0,45 m) y agregarlo en 10T1 / 2 células de ratón fibroblastos de 12 horas en presencia de sulfato de protamina (5 mg / ml) que aumenta la eficiencia de la infección por el virus. El medio se cambió a 10% de FCS-DMEM de 2 días adicionales.
- Se examinan las células mediante un microscopio de fluorescencia. 10T1 / 2 células infectadas por el virus de la GFP se convertirá en GFP-positivas. También tratar las células con puromicina (1 mg / ml) durante 5-7 días y observar la placa en su caso puro R 10T1 / 2 células están presentes y forman colonias después del tratamiento puromicina.
- Tenga en cuenta que la transcripción de genes horizontalsfer por virus activo producido por la GFP los padres + puro R fibroblastos humanos mamarios pueden hacer las células que rodean murino y / o carcinoma de células GFP + R puro dentro de xenoinjertos de tumores. Esto puede dificultar el proceso de aislar el GFP inicialmente inyectado + puro R fibroblastos humanos mamaria de los xenoinjertos tumorales.
3a. La coinyección de los fibroblastos humanos mamaria con células de carcinoma de mama en un ratón inmunodeficiente
Los procedimientos experimentales para la generación de exp-CAF se ilustra en la figura. 1Ba.
- Mezcla de 1x10 6 células MCF-7-ras las células humanas de carcinoma de mama y 3x10 6 GFP + R puro, inmortalizado fibroblastos humanos mamarios generados en P2.2). Prepare las células en 400 l de medio de cultivo con 50% (v / v) Matrigel por inyección.
- Inyectar la mezcla de células por vía subcutánea en un ratón desnudo inmunodeficientes. Cuando los CAF son extraídos de forma independiente a partir de diferentestumores, implantes cada mezcla en los flancos derecho e izquierdo de varios ratones.
3b. La inyección de fibroblastos humanos de mama en un ratón inmunodeficiente
- Para generar los fibroblastos de control contra la exp-CAF, preparar 3x10 6 GFP + puro R inmortalizado fibroblastos humanos mamarios generados en P2.2 en 400 l de medio de cultivo con 50% (v / v) Matrigel por inyección (Fig. 1Bb). No mezcle los fibroblastos con las células de carcinoma.
- Implante de los fibroblastos preparado en P3b.1 en sitios subcutáneos de ratones desnudos.
* Tenga en cuenta que los fibroblastos inoculados se forma el tejido fibroblástico del tumor, pero no debajo de la piel.
4a. La disección de xenoinjertos de tumores
- Eutanasia del ratón alberga un subcutánea de mama humano xenoinjertos de cáncer 42 días después de la implantación (Fig. 1Ba). * Nota que cuando las células de carcinoma y / o fibroblastos son coimplanted, Los fibroblastos pueden necesitar ser incubadas durante más de 42 días dentro de los xenoinjertos tumorales para iniciar su fenotipo miofibroblastos.
- Cosecha del xenoinjerto tumoral en el flanco del ratón mediante disección roma con pinzas y tijeras. Sumergir el tejido del tumor en PBS.
4b. La disección de xenoinjerto de fibroblastos
- La eutanasia a los ratones que albergan el xenoinjerto de fibroblastos 42 días después de la implantación (Fig. 1Bb).
- Diseccionar el xenoinjerto de fibroblastos subcutáneos con pinzas y tijeras. Coloque el tejido fibroblástico en PBS. * Tenga en cuenta que un xenoinjerto de fibroblastos, que aparece como un tejido transparente pequeño, puede ser difícil de encontrar debajo de la piel.
5. Preparación de los principales cultivos de células de xenoinjertos
- Utilice un gabinete de bioseguridad estéril para disecar el tumor (~ 0.5 gramos) o tejido fibroblástico (~ 0,1 gramos). La transferencia de los tejidos extirpados en la parte superior de una cultura d 15 cmISH con 1 ml de PBS. Picar los tejidos en fragmentos de tejido pequeños (<1,5 mm 3) el uso de cuchillas de afeitar estéril. * Tenga en cuenta que si los xenoinjertos de fibroblastos pesa menos de 0,1 gramos, se recoge una xenoinjertos algunos adicionales de fibroblastos y mezclarlos entre sí para aumentar el número de células para el aislamiento.
- La transferencia de los fragmentos de tejido en un tubo cónico de 15 ml que contiene la celda de disociación de amortiguación (10 ml por cada 0,5 gramo de tejido) y agitar durante 1 minuto a máxima velocidad.
- Incubar la suspensión celular durante 3 horas a 37 ° C con agitación lenta continua.
6. El aislamiento de las células resistentes a la puromicina en la cultura
- Se centrifuga la suspensión celular disociada tanto de xenoinjerto de tumor o de fibroblastos durante 5 minutos a 250 x g y resuspender el botón celular en PBS. Se centrifuga de nuevo durante 5 minutos a 250 x g. Resuspender el pellet de células resultantes en el 10% FCS-DMEM. Cultivar las células en una placa de Petri de 15 cm en la presencia de puromicina (1 mg / ml) a 37 ° Cy el 5% de dióxido de carbono con el fin de eliminar las células carcinoma contaminantes y / o murino las células del estroma. Se propagan las células hasta confluencia (2-4 semanas). Almacenar las células a -80 ° C con medio de congelación. * Tenga en cuenta que el resultado puro células R, designado de 42 días de edad, exp-CAF1 (Fig. 1Ba) o el control de fibroblastos-1 en las células (Fig. 1Bb), son inmortales y positivo para las buenas prácticas agrarias. Se recomienda comprobar si estas células producen los virus activos con 10T1 / 2 células, como se describe en P2.3-6.
7a. El aislamiento de células CaF2 exp-en la cultura
Para potenciar aún más el fenotipo activado miofibroblástico de CAF, mezcla de los 42 días de edad CAF1 exp-células con células MCF-7-ras las células y se inyectan de nuevo por vía subcutánea en un ratón desnudo por períodos adicionales de 200 días. Diseccionar y disociar los xenoinjertos de tumores en una suspensión de un solo cultivo de células y las células en una placa de Petri de 15 cm con 10% FCS-DMEM en presencia de puromicina (1 mg / ml), como se indica en P60.1. Se propagan las células hasta confluencia (8-10 días). Almacenar las células a -80 ° C con medio de congelación. El resultado de puro R células se llaman 242 días de edad CaF2 exp-células (Fig. 1Ba).
7b. Extracción de control 2 de fibroblastos-células en cultivo
Para generar los fibroblastos de control contra la exp-CaF2 las células, se inyectan de 42 días de edad, el control de los fibroblastos-1 células por sí solas, sin células de carcinoma por vía subcutánea en un ratón desnudo, además, durante 200 días. Diseccionar y disociar el tejido fibroblástico en una suspensión de células individuales y la cultura de las células en una placa de Petri de 15 cm con 10% FCS-DMEM en presencia de puromicina (1 mg / ml) como se indica en P6.1. Se propagan las células hasta confluencia (3-4 semanas). Almacenar las células a -80 ° C con medio de congelación. El resultado de puro R se llaman las células de fibroblastos-2 de control de las células (Fig. 1Bb).
8. Los resultados representativos:
Control de los fibroblastos-2 y cel exp-CaF2ls, que han sido extraídos de xenoinjertos de tumores de mama, teñidas fuertemente positivo para los marcadores mesenquimales, incluyendo humanos específicos de vimentina, propil-4-hidroxilasa, 1A colágeno, fibronectina, S100A4, y la proteína de superficie de fibroblastos (Fig. 2A) 11, lo que indica humanos origen y la naturaleza mesenquimal de las células. En contraste, la citoqueratina, un marcador para las células epiteliales, no era una mancha en estos GFP + fibroblastos (Fig. 2B). Por lo tanto, estos hallazgos sugieren que la extrae CaF2 exp-2 y el control de fibroblastos-células tienen su origen en la de sus padres fibroblastos humanos mamarios se introdujo inicialmente en xenoinjertos de ratón.
Es importante destacar que una mayor proporción de CaF2 exp-células teñidas positiva para α-SMA y la glicoproteína de la matriz extracelular tenascina C 5, los cuales son marcadores de miofibroblastos en comparación con 42 días de edad, exp-CAF1 y el control de dos fibroblastos (Fig. . 2C, D) 11. Estos datos indican que FIBR residente de mama humanoprovincias evolución progresiva en miofibroblastos CAF en xenoinjertos de tumores.

Figura 1 Representación esquemática de aislamiento de los fibroblastos humanos mamarios. A) El tejido de la mamoplastia de reducción fue picada con hojas de afeitar estériles (P1.2) y se transfiere a un tubo cónico de 15 ml (P1.3). Los pequeños fragmentos de tejido fueron digeridas en la celda de la disociación de amortiguación (P1.4) y preparado para el cultivo in vitro (P1.5-7). Para inmortalizar los aislados primarios de fibroblastos humanos de mama, una pMIG retroviral (MSCV-IRES-GFP), vector, expresando hTERT y las buenas prácticas agrarias, se introdujo, y la GFP-con resultados positivos las células fueron ordenados mediante citometría de flujo (P2.1). Un retroviral pBabe-puro vector que codifica un gen de resistencia a la puromicina fue introducido en estas células. Tras el tratamiento puromicina, GFP-etiquetados (GFP +) resistentes a la puromicina (Puro R), immortalised de mama fibroblastos humanos fueron aislados (P2.2).
Ba) Para generar exp-CAF, GFP + puro R inmortalizado fibroblastos humanos coinjected mamaria con células MCF-7-ras células de carcinoma de mama por vía subcutánea en un ratón inmunodeficiente desnuda (P3a). El xenoinjerto de tumor fue resecado a los 42 días después de la implantación (P4a) y se disocia en una suspensión de una sola célula (P5). Estas células fueron cultivadas in vitro en presencia de puromicina para eliminar las células carcinoma de células de ratón y la contaminación del estroma (P6). El resultado resistentes a la puromicina células se denomina experimental generada CAF1 (exp-CAF1) las células. Estas células, resecado 42 días post-implantación, una vez más se mezclan con células MCF-7-ras y se implantaron subcutáneamente células en un ratón de acogida como antes (P7A). El tumor resultante se dejó crecer por períodos adicionales de 200 días, diseca, disociados, y se cultivan en presencia de puromicina. El aisladopuromicina resistentes a las células se denominan células CaF2 exp (242 días de edad).
Bb) Para aislar las células de control contra la exp-CAF, GFP + puro R inmortalizado fibroblastos humanos mamarios fueron inyectados por vía subcutánea en un ratón desnudo como cultivos puros sin MCF-7-ras células (P3b). El tejido fibroblástico, disecados 42 días post-implantación (P4B), se disocia en una sola célula suspensiones (P5) y las células resistentes a la puromicina, llamado control de fibroblastos-1 en las células, fueron aislados como se describió anteriormente (P6). Estos fibroblastos fueron una vez más implantados subcutáneamente en un ratón desnudo sin MCF-7-ras las células, además de 200 días (P7b). El tejido fibroblástico fue disecada, disociados, y se cultivan en presencia de puromicina. El aislado puromicina resistentes a las células fueron llamados fibroblastos-2 de control de las células (242 días de edad).
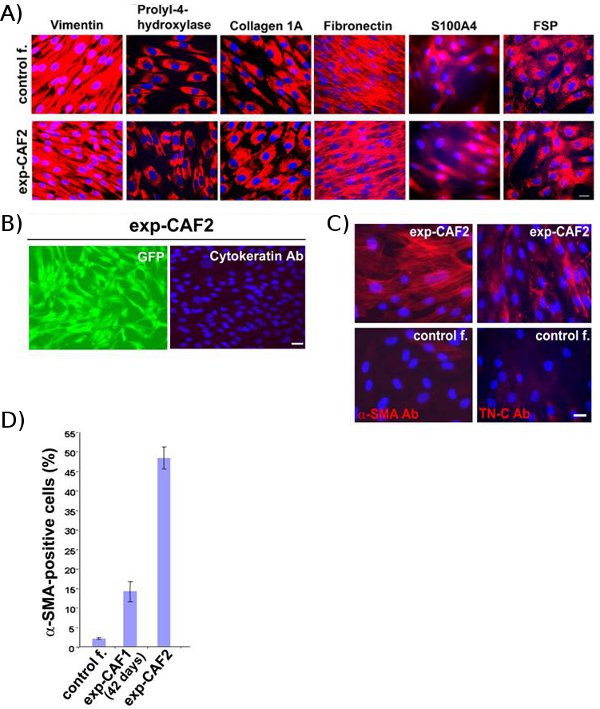
Figura 2 Exp-CAF y el control de los fibroblastos se originan en la de sus padres fibroblastos de mama humano. (A) los análisis de inmunofluorescencia de control de fibroblastos-2 (control de f.) y las células CaF2 exp. Los tipos de células tanto tinción positiva para marcadores mesenquimales (rojo), incluidos los humanos vimentina, prolil-4-hidroxilasa, 1A colágeno, fibronectina, S100A4, y proteína de la superficie de fibroblastos. (B) Por el contrario, pan-citoqueratina, un marcador para las células epiteliales , no se detecta en CaF2 exp-las células que expresan GFP (verde). Los núcleos celulares se tiñen con 4'-6-diamidino-2-phenylindole (DAPI) (azul). Barra de escala, de 50 micras (denominadas de Kojima et al. 11)
(C) Inmunofluorescencia de CaF2 exp las células y el control de dos fibroblastos (control f.) usando anticuerpos contra la α-SMA (rojo) o la tenascina C (TN-C) (rojo). Núcleos de las células se tiñeron con DAPI (azul). Barra de escala, de 50 micras. (D) 48% de CaF2 exp células tinción positiva para α-SMA, mientras que un4% de los 42 días de edad, exp-CAF1 y el 2,5% de la población de células de fibroblastos de control 2-son positivas para α-SMA. (Denominados de Kojima et al.11)
Discusión
La falta de marcadores específicos de la CAF y el nivel de heterogeneidad observada entre CAF hacer la caracterización de este tipo de células por sí un desafío. CAF estudiar in vitro también se ha visto obstaculizado por la complicación adicional de que estas células envejecen y dejan de proliferar en cultivo durante un largo período. Nuestro intento anterior para inmortalizar directamente CAF primario utilizando un retrovirus construir hTERT cDNA no tuvo éxito. Por lo tanto, a investigar más a fond...
Divulgaciones
No hay conflictos de interés declarado.
Agradecimientos
Agradecemos al Dr. Robert A. Weinberg (Whitehead Institute for Biomedical Research, Cambridge) por su generoso apoyo y supervisión de este trabajo y el Sr. Kieran Mellody (Universidad de Manchester, Manchester) para la edición crítica de este manuscrito. Este proyecto fue apoyado por la investigación del Reino Unido (CR-Reino Unido) el número de concesión C147/A6058 (AO)
Materiales
| Nombre del Material | Tipo | Empresa | Número de catálogo | Comentario |
| DMEM | Invitrogen | 61965-026 | ||
| Suero fetal bovino | GIBCO | 10270 | ||
| Penicilina-estreptomicina | Invitrogen | 15140-122 | ||
| Colagenasa tipo I | Sigma | C0130-1G | ||
| hialuronidasa | Sigma | H4272 | ||
| Vimentina (V9) de anticuerpos | Novocastra Laboratorios | NCL-L- VIM-V9 | ||
| Tenascina C (AC-8) de anticuerpos | un regalo de | |||
| α-SMA-Cy3 (1A4) de anticuerpos | Sigma | C6198 | ||
Prolil-4-hidroxilasa | Dako | M0877 | ||
| (5B5) de anticuerpos | ||||
| El colágeno tipo 1 1A anticuerpos | Sigma | HPA011795 | ||
| Pan-citoqueratina de anticuerpos | Sigma | C5992 | ||
| Anticuerpo de fibronectina | BD Biosciences | 610077 | ||
S100A4/FSP-1 (fibroblastos proteína-1 específicos) de anticuerpos | Dako | A5114 | ||
Fibroblastos proteína de la superficie (Clon 1B10) de anticuerpos | Abcam | ab11333 | ||
| MSCV-IRES-GFP construir | Solicitud a los autores de la | |||
| pBabe-puro construir | Compra de Addgene | |||
| Puromicina | Sigma | P8833 | ||
| DAPI | Sigma | D9564 | ||
| Tubo cónico de 15 ml | Corning | 430766 | ||
| Ratón desnudo | Taconic | NCRNU-F | Mujer desnuda NCR | |
| C3H/10T1/2 células | ATCC | CCL-226 |
Referencias
- Ronnov-Jessen, L., Bissell, M. J. Breast cancer by proxy: can the microenvironment be both the cause and consequence?. Trends Mol. Med. 15, 5-13 (2009).
- Mueller, M. M., Fusenig, N. E. Friends or foes - bipolar effects of the tumour stroma in cancer. Nat. Rev. Cancer. 4, 839-849 (2004).
- Bhowmick, N. A., Neilson, E. G., Moses, H. L. Stromal fibroblasts in cancer initiation and progression. Nature. 432, 332-337 (2004).
- Kalluri, R., Zeisberg, M. Fibroblasts in cancer. Nat. Rev. Cancer. 6, 392-401 (2006).
- De Wever, O. Tenascin-C and SF/HGF produced by myofibroblasts in vitro provide convergent pro-invasive signals to human colon cancer cells through RhoA and Rac. 18, 1016-1018 (2004).
- Serini, G., Gabbiani, G. Mechanisms of myofibroblast activity and phenotypic modulation. Exp. Cell. Res. 250, 273-283 (1999).
- Shimoda, M., Mellody, K. T., Orimo, A. Carcinoma-associated fibroblasts are a rate-limiting determinant for tumour progression. Semin. Cell. Dev. Biol. 21, 19-25 (2010).
- Pietras, K., Ostman, A. Hallmarks of cancer: interactions with the tumor stroma. Exp. Cell. Res. 316, 1324-1331 (2010).
- Polyak, K., Haviv, I., Campbell, I. G. Co-evolution of tumor cells and their microenvironment. Trends in Genetics. 25, 30-38 (2009).
- Franco, O. E., Shaw, A. K., Strand, D. W., Hayward, S. W. Cancer associated fibroblasts in cancer pathogenesis. Semin. Cell. Dev. Biol. 21, 33-39 (2010).
- Kojima, Y. Autocrine TGF-beta and stromal cell-derived factor-1 (SDF-1) signaling drives the evolution of tumor-promoting mammary stromal myofibroblasts. Proc. Natl. Acad. Sci. U. S. A. 107, 20009-20014 (2010).
- Orimo, A. Stromal fibroblasts present in invasive human breast carcinomas promote tumor growth and angiogenesis through elevated SDF-1/CXCL12 secretion. Cell. 121, 335-348 (2005).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados