Method Article
Test de activación de basófilos para la investigación de mecanismos IgE mediados de Hipersensibilidad a las Drogas
En este artículo
Resumen
Prueba de activación de basófilos es una potente herramienta para la detección de IgE-dependiente de las alergias In vitro. En este caso, un protocolo optimizado para la prueba de activación de basófilos se utiliza para investigar hipersensibilidad a la droga. Un método para la producción eficiente de proteínas covalentes drogas conjugados y su caracterización físico-química se describe.
Resumen
Las reacciones de hipersensibilidad contra los no-esteroides anti-inflamatorios no esteroideos (AINE) como propifenazona (PP) y diclofenaco (DF) se puede manifestar como Tipo I-reacciones alérgicas de tipo 1. En la práctica clínica, el diagnóstico de hipersensibilidad a la droga se lleva a cabo principalmente por la historia del paciente, como prueba de la piel no es fiable y las pruebas de provocación oral tiene riesgos que amenazan la vida para el paciente 2. Por lo tanto, la evidencia de un activo subyacente mediada por IgE mecanismo patógeno es difícil de obtener.
A continuación, presentamos un método in vitro basado en el uso de los basófilos humanos derivados de la droga hipersensibles pacientes que imita la reacción alérgica efectoras en vivo. Como los basófilos de pacientes alérgicos a las drogas llevan moléculas de IgE específica para el medicamento culpable, que se activan al entrecruzamiento de los receptores de IgE y la liberación alérgica moléculas efectoras. La activación de basófilos puede ser controlada por la determinación de la regulación al alza de la expresión de superficie CD63 por citometría de flujo 3.
En el caso de fármacos de bajo peso molecular, los conjugados están diseñados para permitir la reticulación IgE receptor en los basófilos. Como se muestra en la Figura 1, dos representantes de los AINE, PP y el DF, se unen covalentemente a la albúmina sérica humana (HSA) a través de un grupo carboxilo que reacciona con el grupo amino primario de los residuos de lisina. DF lleva un grupo carboxilo intrínseca y, por tanto, se puede utilizar directamente 4, mientras que uno que contiene un grupo carboxilo derivados del PP tuvo que ser organochemically sintetizado antes del estudio 1.
El grado de acoplamiento de los compuestos de bajo peso molecular de la molécula de proteína transportadora y su distribución espacial es importante para garantizar la reticulación de dos moléculas del receptor IgE. El protocolo aquí descrito se aplica de alto rendimiento-tamaño de cromatografía de exclusión (HPSEC) equipado con un índice de refracción secuencial (RI) y ultravioleta (UV) del sistema de detección para la determinación del grado de acoplamiento.
A medida que la metodología descrita se puede aplicar a otras drogas, la prueba de activación de basófilos (BAT) tiene el potencial de ser utilizado para la determinación de IgE-mediada por mecanismos de hipersensibilidad a la droga. En este sentido, determinar PP hipersensibilidad mediada por IgE y la hipersensibilidad DF como no-IgE-mediada por BAT.
Protocolo
1. Preparación de los conjugados de las drogas
- Disolver 10 mg DF en 1 ml de dH 2 O en un tubo de 1,5 ml de reacción. En el procedimiento aún más el uso 95 l de esta solución DF. Conjugar PP para disolver 30,4 mg HSA derivado de PP (304 g / mol) en 500 l 0,3 M de hidróxido sódico (NaOH).
- Añadir 430,6 l dH 2 O y 100 l 0,5 M 2 - (N-morfolino) etanosulfónico (MES) buffer de pH 6,5 a 95 l de disolución DF. Añadir 33,1 l dH 2 O y 140 l de 2 M de tampón MES pH 2,9 a la muestra de PP.
- Añadir 57,5 l de una solución recién preparada N-etil-N '- (3-dimetilaminopropil) clorhidrato de carbodiimida (EDC) solución madre disuelto en dH 2 O con una concentración de 100 mg / ml de la muestra DF, a 10 l solución EDC la muestra de PP. Vortex las muestras durante 1 minuto.
- Añadir 16,9 l de solución de HSA con una concentración de 118 mg / ml para cada muestra.
- Incubar las muestras durante 2 horas a temperatura ambiente con agitación a 300 revoluciones / min.
- Diálisis del DF y las muestras de PP 3 veces contra 2 litros de tampón fosfato salino (PBS) pH 7,4 durante varias horas cada uno. Realizar todos los pasos de diálisis a 4 ° C.
- Centrifugar la muestra 10 minutos a 14.000 xg y recoger el sobrenadante que contiene DF o PP conjugado con HSA.
- Compruebe sobrenadante de proteínas mediante la realización de un SDS-PAGE, utilizando geles de 12%. Carga de 12 mg de HSA conjugado en la ranura de un gel.
2. Determinar la tasa de acoplamiento de los conjugados de la droga (Figura 2)
- Para el análisis de la tasa de acoplamiento del DF y los conjugados de PP por utilizar una HPSEC sodio 100 mM fosfato pH 6,5 que contenía 150 mM NaCl y 0,05% de azida de sodio. Use un x 300 mm 7,8 TSK-Gel-G2000 columna SWXL.
- Realizar la detección de señales mediante el uso de una línea de acoplamiento de RI y el sistema detector de UV.
- Preparar una muestra de HSA estándar con una concentración de 1 mg / ml en dH 2 O. Para la calibración del detector de inyectar 50 l HSA solución estándar.
- Calcular la RI RI k constante y la UV UV constante k para el detector. Utilice el área de fórmulas RI RI = k * [(dn / dc) * c HSA (HSA)] y la zona UV UV = k * [(dA / dc) * c HSA (HSA)] con (dn / dc) = HSA 0,185 y (dA / dc) HSA = 0,518 5.
- Prepare DF y las normas derivadas de PP HPSEC que las cantidades de 5, 10 y 30 nmol de ambas normas pueden ser fácilmente inyectado.
- Calcular los valores medios de (dn / dc) y de drogas (DA / CC) de medicamentos para ambos estándares. Por DF, a (dn / dc) de 0,235 ± 0,010 y un (DA / CC) de 39,000 ± 0,493 se determinó. Para el PP, un (dn / dc) de 0.328 ± 0.016 y una de (QA / dc) 53,155 ± 2,464 se determinó.
- Inyectan drogas conjugados en HPSEC y determinar su RI y UV áreas de los picos.
- Calcular la concentración de DF, derivado de PP, y HSA por la solución de los RI dos ecuaciones k = área RI * [(dn / dc) * c drogas (medicamentos) + (dn / dc) * c HSA (HSA)] y la zona UV UV = k * [(dA / dc) * c drogas (medicamentos) + (dA / dc) * c HSA (HSA)] para las incógnitas.
3. MTD con conjugados de drogas
- Prepare siete copas de la citometría de flujo y la etiqueta de ellos en función de su contenido: el control de mancha, el control negativo, control positivo, y los conjugados de las drogas.
- Añadir 50 l de tampón de estimulación B-CCR-STB (Flow2 CAST, Bühlmann Laboratories, Schönenbuch, CH) en los viales reservados para el control de manchas y negativos. Como control positivo, use 50 l de una solución anti-FcεRI proporcionado por el kit CAST Flow2. Añadir la cantidad apropiada de solución de conjugado en los viales reservados para los conjugados de drogas mediante la creación de una serie de diluciones 1:10 de 0,02 -20 mg / ml DF conjugado y PP conjugado (concentraciones finales en un volumen de ensayo de 200 l). Estos experimentos de titulación se debe realizar para determinar la concentración de la activación de basófilos óptima para cada muestra.
- Añadir 100 l de amortiguación estimulación a cada tubo y la sangre de 50 pacientes l de EDTA conjunto. Mezclar las muestras con cuidado.
- Colocar 20 l Flow2 CAST reactivo de tinción con anticuerpos anti-CCR3 anticuerpos marcados con ficoeritrina (PE) y anti-CD63 anticuerpos marcados con isotiocianato de fluoresceína (FITC) a cada tubo y mezclar de nuevo. No pipetear los reactivos de tinción en la muestra sin mancha!
- Incubar las muestras durante 45 minutos en un baño de agua a 37 ° C.
- Detener la reacción en hielo durante 5 minutos.
- Lisis de los eritrocitos mediante la adición de 2,0 ml de reactivo CAST Flow2 lisis a cada vial y agitar suavemente. Incubar las muestras en la oscuridad durante 10 minutos a temperatura ambiente.
- Centrifugar las muestras durante 5 minutos a 500 xg y el sobrenadante decantar con precaución.
- Resuspender las células en 500 l de tampón de lavado Flow2 CAST y almacenar en hielo hasta que la citometría de flujo.
- Ajuste s del citómetro de flujo de voltajeCONFIGURACIÓN para dispersión frontal y lateral (FSC, SSC), mientras que la adquisición de la muestra sin teñir.
- Puerta de las células como los linfocitos previsto de la parcela SSC-FSC a la trama SSC-PE. Los basófilos son identificados por un PE-etiquetados anti-CCR3 anticuerpos como CCR3 hi he SSC y la puerta que en la trama FITC-PE. El anticuerpo anti-CD63 para detectar basófilos activados está marcado con FITC.
- Establecer el límite máximo de 2,5% de los basófilos como CD63 de alta en el control negativo. Una muestra se considera positiva para la activación de basófilos si basófilos> 5% son CD63 de alta y el índice de fluorescencia media (MFI) de la muestra dividida por la IMF del control negativo superior a 2 (Figura 3).
4. Los resultados representativos:
Este experimento evalúa las mejores técnicas disponibles como una herramienta útil para detectar IgE-dependiente de hipersensibilidad a la droga. Conjugados de los AINE se utilizan para la activación de basófilos. Por HPSEC con RI y detección UV estado de agregación, el grado de acoplamiento, y el rendimiento efectivo de los conjugados se determinan. Como muestra la Figura 4 muestra, el 43,5% de los conjugados DF quedó monomérica con un grado de acoplamiento de 5,0 DF / HSA. Para los agregados un grado de acoplamiento de 9,5 se determinó. El conjugado propifenazona se demostró que consisten en monómeros 68,5% con un grado de acoplamiento de 21,2. El grado de acoplamiento de los agregados fue de 27,9. En total, el grado de acoplamiento de los conjugados determina DF fue de 7,6 DF y de los conjugados de PP fue de 23,2.
MTD realiza con conjugados de las condiciones más favorables (concentración de los conjugados, el tiempo de estimulación) permite la investigación de IgE-dependiente de las reacciones de hipersensibilidad en los AINE. Como se muestra en la Figura 5, sólo el conjugado PP fue capaz de desencadenar la activación de basófilos visualizado por una regulación al alza en la expresión de superficie CD63: 20,6% de los basófilos se activan caracteriza por un registro de desplazamiento en la intensidad de la fluorescencia. La IMF aumentó en un factor de 4.9 de 386 (control negativo) del año 1893. Por el contrario, con el conjugado DF sólo el 3,1% de los basófilos se activan lo que estaba por debajo del 5% de corte. Asimismo, la IMF aumentó sólo en un factor 1.1 (límite de 2.0) de 197 (control negativo) a 210. La validez del ensayo está dada por (i) <5% de activación de basófilos en el control negativo, (ii) un registro de desplazamiento en la intensidad de la fluorescencia de una subpoblación de basófilos, y (iii)> 50% de basófilos activados (control positivo).
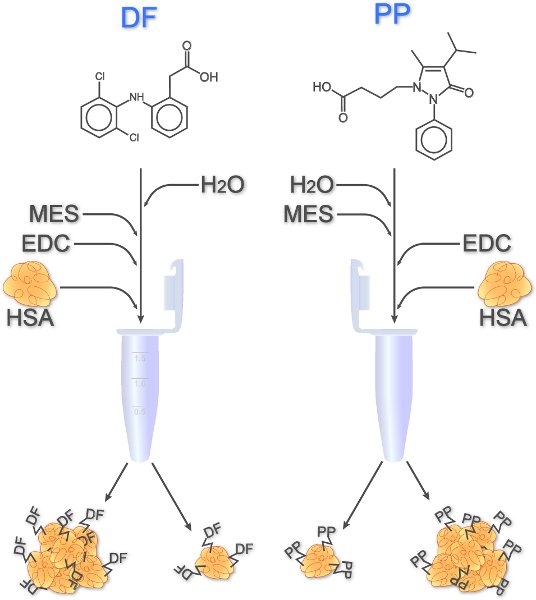
Figura 1. Acoplamiento de derivados DF y PP a la HSA. Después de disolver los medicamentos, agua, tampón MES, y EDC (reactivo de acoplamiento) se agregan. Las muestras se agitaron durante 1 minuto antes de HSA es una pipeta de las soluciones de drogas. Dentro de 2 horas con agitación a temperatura ambiente, las drogas se unen covalentemente a la HSA. Monómeros, así como los agregados puede dar lugar.

Figura 2. Cálculo de los grados de acoplamiento. En primer lugar, las constantes k RI y UV k se determinan. Por lo tanto, HSA estándar con concentración conocida se inyecta en el sistema HPSEC. (Dn / dc) y (DA / CC) de la HSA se dan los valores de 0,185 y 0,518, respectivamente 5. Las áreas de pico se utilizan para el cálculo de las constantes. En segundo lugar, para cada medicamento se inyecta tres normas para determinar las drogas y la concentración específica de RI y las áreas UV. Dado que la RI y las constantes k k UV son conocidos por los pasos anteriores, los derivados de las drogas específicas (dn / dc) y (dA / dc) se puede calcular. En tercer lugar, la droga-HSA conjugados se inyectan en HPSEC. El área del pico resultante se utiliza para calcular las concentraciones de la droga y HSA por pico por resolver las dos ecuaciones con dos incógnitas.
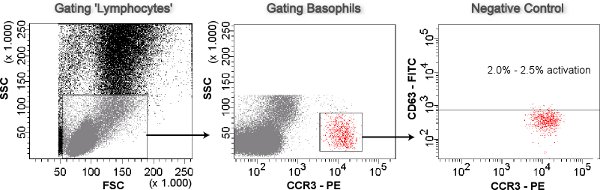
Figura 3. Gating basófilos. Las células como los linfocitos se predijo dispersión lateral cerrada frente a dispersión frontal (FSC-SSC parcela). Los basófilos son identificados como de alta CCR3 SSC Lo de los linfocitos cerrada (SSC-CCR3-PE parcela). Los basófilos son analizados para la activación (CD63 hi) en la trama CD63-FITC-CCR3-PE. El control negativo se utiliza para establecer el límite máximo de los basófilos 2,5% restante CD63 hi.
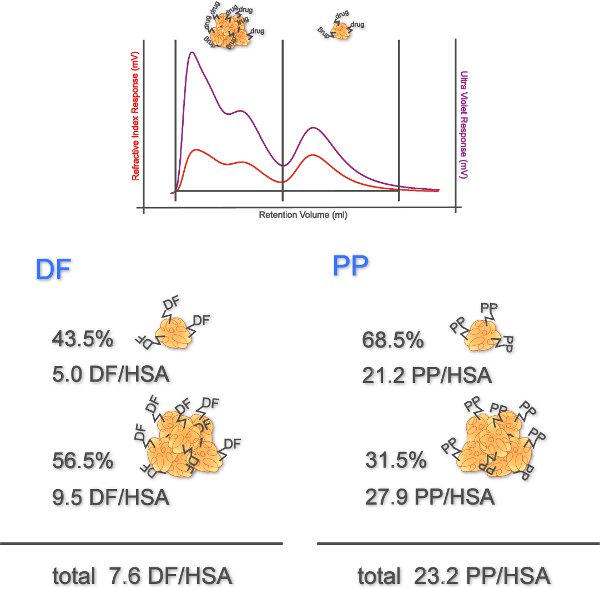
Figura 4. Decidido grados de acoplamiento de los conjugados de las drogas. RI y las señales de UV muestran dos picos que representan los agregados (eluyendo con un volumen de retención bajo) y monómeros (eluyendo con un volumen de retención de alta) de la droga-HSA conjugados. Porcentajes de monómeros y agregados (determinado a partir de señales IR) y sus grados de acoplamiento se representan (n = 1).
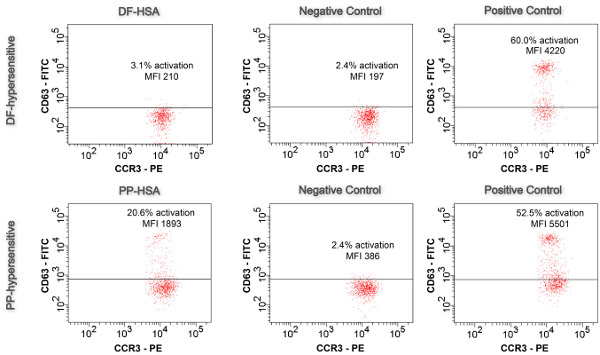
Figura 5. Basófilos Activatien la prueba. Resultados de la droga conjugada activado por las muestras, controles negativos y controles positivos se muestran en la CD63-FITC-CCR3-PE parcelas (n = 1).
Discusión
MTD es una bien establecida, aunque todavía no se utilizan habitualmente método para el diagnóstico de la enfermedad mediada por IgE alérgica 6,7. De hipersensibilidad a la droga, sin embargo, su aplicabilidad es comprometido como compuestos de bajo peso molecular no son capaces de entrecruzar los receptores de IgE, un requisito previo para la activación de basófilos 8. Por lo tanto, los medicamentos en investigación deben ser covalentemente a las proteínas de soporte adecuado (por ejemplo, HSA). Es importante destacar que el grado de acoplamiento (es decir, número de moléculas de fármaco por proteína transportadora), debe ser controlada para garantizar la actividad inmunológica (es decir, receptores de IgE entrecruzamiento) de los conjugados. En teoría, dos haptenos por molécula portadora debe ser suficiente para el receptor de IgE entrecruzamiento y un mínimo de cinco moléculas DF por HSA se ha demostrado para activar la liberación de mediadores en un ensayo basado en células 4. Ambos conjugados, PP-HSA y HSA-DF, se ha determinado que muestran un grado de acoplamiento suficientemente alta (HPSEC) y que se inmunológicamente activas haciendo que los reactivos adecuados para su uso en las mejores técnicas disponibles. Otro problema puede ser que los metabolitos de las drogas puede jugar un papel, como un metabolito de la droga en lugar de los padres puede causar la reacción de hipersensibilidad. En el caso del DF, esta posibilidad ha sido evaluada en detalle con anterioridad utilizando cinco Fase I los principales metabolitos, y una variante de conexión 4. Entre los factores importantes para el dominio de la técnica descrita son la calidad de la muestra de sangre (<12 horas desde la extracción de sangre, el número de basófilos detectado> 500) y la optimización de las condiciones de estimulación (tiempo, dosis). Además, las llamadas no respondedores que ni siquiera reaccionan con el control positivo (anticuerpo dirigido contra el receptor de IgE) tienen que ser identificados. Por lo tanto, los criterios de validación que incluye un anticuerpo anti-FcεRI como control positivo. Una ventaja importante del uso de conjugados de drogas es el hecho de que parece no tóxico en contraste con las drogas puras, como se muestra para DF-HSA conjugado por la co-estimulación con anti-FcεRI de anticuerpos en las mejores técnicas disponibles 4. Pura DF, por el contrario, muestra efectos citotóxicos a una concentración de 1,25 mg / ml causando problemas con la interpretación de las mejores técnicas disponibles 9. En general, las pruebas de citotoxicidad potencial es altamente recomendable para todos los conjugados de las drogas de nueva producción.
En este caso, hemos demostrado el potencial de la PP-HSA conjugado utilizado en las mejores técnicas disponibles para revelar hipersensibilidad mediada por IgE. Por el contrario, DF hipersensibilidad no está asociado con IgE demostrada por la falta de activación de basófilos en respuesta a DF-HSA conjugado. Es importante destacar que, en caso de duda respecto a un mecanismo mediado por IgE, conjugados tienen que ser evaluados para la actividad inmunológica de los sistemas de ensayo in vitro basados en células como se ha demostrado para DF 4.
Usando la configuración descrita de conjugar fármacos de bajo peso molecular de forma covalente a una proteína portadora moléculas adecuadas de una serie de reacciones de hipersensibilidad contra las drogas, incluidos los antibióticos, a otros AINEs, medios de contraste radiológico, relajantes musculares, anestésicos, etc puede ser investigado por una participación de un mediada por IgE mecanismo. Por lo tanto, las mejores técnicas disponibles pueden servir como una adición a los métodos existentes para el diagnóstico (pruebas cutáneas, pruebas de provocación oral).
Divulgaciones
No hay conflictos de interés declarado.
Agradecimientos
Este trabajo fue financiado por el Fondo Científico de Austria (FMF) conceder P18820-B13.
Ética declaración:
El estudio fue aprobado (PLUS_Ethik_090514) por el Comité Ético de Experimentación con seres humanos y / o animales en la Universidad de Salzburgo cumplir con los Declaraction Helsinki revisada en 1983 y todos los pacientes participantes dieron su consentimiento informado por escrito.
Materiales
| Name | Company | Catalog Number | Comments |
| Nombre del reactivo / dispositivo | Empresa | Número de catálogo | Comentarios |
|---|---|---|---|
| 2 - (N-morfolino) etanosulfónico | Sigma | M3671 | - |
| 7,8 x 300 mm TSK Gel -G2000SWXL columna | Tosoh Bioscience | 08540 | - |
| BD FACSCanto II | Becton Dickinson | 338962 | - |
| Centrífuga de sobremesa | Sigma | - | - |
| Diclofenac sal de sodio | Sigma | D6899 | - |
| EDTA Vacutainer | Becton Dickinson | 368589 | - |
| Flow2 CAST Kit | Bühlmann Laboratorios | FK-CCR | Kit efectiva CAST 14 de junio 2011 Flow2 ahora es de lanzamiento de flujo |
| HP1100 HPLC sistema | Hewlett Packard | - | - |
| Albúmina de suero humano | Sigma | A9511 | - |
| Centrífuga de laboratorio | Eppendorf | - | - |
| N-etil-N'-(3-dimetilaminopropil) carbodiimida clorhidrato (EDC) | Sigma | E6383 | - |
| PBS tabletas | AppliChem | A9199 | - |
| Propifenazona derivados | Departamento de Biología Molecular de la Universidad de Salzburgo, Austria | - | - |
| Agitador | Eppendorf | - | - |
| Azida de sodio | Sigma | S8032 | - |
| Cloruro de sodio (NaCl) | Sigma | S1679 | - |
| De bicarbonato sódico | Sigma | 90421C | - |
| Hidróxido de sodio | Sigma | S5881 | - |
| Fosfato de sodio | Sigma | 342483 | - |
| Matriz de detectores Triple | Viscotek | TDA302 | - |
| BioVortex personal V-1 más | Peqlab | 90-V-1 | - |
| Agua de baño 1012 | GFL | 1012 | - |
Referencias
- Himly, M. IgE-mediated immediate-type hypersensitivity to the pyrazolone drug propyphenazone. J Allergy Clin Immunol. 111, 882-888 (2003).
- Demoly, P., Pichler, W., Pirmohamed, M., Romano, A. Important questions in Allergy: 1--drug allergy/hypersensitivity. Allergy. 63, 616-619 (2008).
- Ebo, D. G., Hagendorens, M. M., Bridts, C. H., Schuerwegh, A. J., Clerck, L. S., Stevens, W. J. Flow cytometric analysis of in vitro activated basophils, specific IgE and skin tests in the diagnosis of pollen-associated food allergy. Cytometry Part B (Clinical Cytometry). 64B, (2005).
- Harrer, A. Diclofenac hypersensitivity: antibody responses to the parent drug and relevant metabolites. PLoS One. 5, e13707-e13707 (2010).
- Wen, J., Arakawa, T., Philo, J. S. Size-exclusion chromatography with on-line light-scattering, absorbance, and refractive index detectors for studying proteins and their interactions. Anal Biochem. 240, 155-166 (1996).
- De Weck, A. L., Sanz, M. L., Gamboa, P. M., Aberer, W., Bienvenu, J., Blanca, M., Demoly, P., Ebo, D. G., Mayorga, L., Monneret, G., Sainte Laudy, J. Diagnostic tests based on human basophils: more potentials and perspectives than pitfalls. II. Technical issues. J Investig Allergol Clin Immunol. 18, 143-155 (2008).
- Ebo, D. G. Flow-assisted allergy diagnosis: current applications and future perspectives. Allergy. 61, 1028-1039 (2006).
- Poulsen, L. K., Quan, S., Kragh, C., Platzer, M. H., Skov, P. S. The basophil granulocyte in allergic reactions: experimental models and their use for the identification of drugs with effects or side effects on basophils. Curr Med Chem - Anti-inflammatory & Anti-Allergy Agents. 3, 167-180 (2004).
- Sanz, M. L., Gamboa, P., de Weck, A. L. A new combined test with flowcytometric basophil activation and determination of sulfidoleukotrienes is useful for in vitro diagnosis of hypersensitivity to aspirin and other nonsteroidal anti-inflammatory drugs. Int Arch Allergy Immunol. 136, 58-72 (2005).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados