Method Article
L'attivazione dei basofili di prova per le Indagini di IgE-mediata Meccanismi di ipersensibilità a farmaci
In questo articolo
Riepilogo
Test di attivazione dei basofili è un potente strumento per la rilevazione di IgE-dipendente allergie In vitro. Qui, un protocollo ottimizzata per i test di attivazione dei basofili è utilizzato per indagare ipersensibilità a farmaci. Un metodo per la produzione efficiente di covalenti farmaco-proteina coniugati e la loro caratterizzazione fisico-chimica è descritta.
Abstract
Reazioni di ipersensibilità contro i non-steroidei anti-infiammatori non steroidei (FANS) come propyphenazone (PP) e diclofenac (DF) può manifestarsi come tipo I reazioni simil-allergiche 1. Nella pratica clinica, la diagnosi di ipersensibilità a farmaci è svolta prevalentemente dalla storia del paziente, come test cutaneo non è affidabile e test di provocazione orale porta pericolo di vita i rischi per il paziente 2. Quindi, le prove per un sottostante meccanismo patogenetico IgE-mediata è difficile da ottenere.
Qui, presentiamo un metodo in vitro basato sull'uso dei basofili umani derivati da pazienti con ipersensibilità al farmaco che imita la reazione allergica effettrici in vivo. Come basofili di farmaco pazienti allergici trasportare molecole di IgE specifiche per il farmaco colpevole, che si attivano al momento reticolazione recettore IgE e rilasciare le molecole effettrici allergiche. L'attivazione dei basofili può essere monitorato dalla determinazione della sovra-regolazione dell'espressione di CD63 superficie mediante citometria a flusso 3.
Nel caso di farmaci a basso peso molecolare, coniugati sono progettati per consentire reticolazione recettore IgE sui basofili. Come illustrato nella figura 1, due rappresentanti dei FANS, PP e DF, un legame covalente con albumina sierica umana (HSA) tramite un gruppo carbossilico reagisce con il gruppo amminico primario di residui di lisina. DF trasporta un gruppo carbossile intrinseca e, quindi, può essere utilizzato direttamente 4, mentre un gruppo carbossile contenenti derivati di PP doveva essere sintetizzato organochemically prima dello studio 1.
Il grado di accoppiamento dei composti a basso peso molecolare della molecola di proteina carrier e la loro distribuzione spaziale è importante per garantire la reticolazione di due molecole del recettore IgE. Il protocollo qui descritto si applica ad alte prestazioni di dimensioni cromatografia di esclusione (HPSEC) equipaggiato con un indice di rifrazione sequenziale (RI) e ultravioletti (UV), sistema di rilevamento per la determinazione del grado di accoppiamento.
Come la metodologia descritta può essere applicata per altri farmaci, il test di attivazione dei basofili (BAT) porta il potenziale per essere utilizzata per la determinazione di IgE-mediata meccanismi di ipersensibilità di droga. Qui, si determina come PP ipersensibilità IgE-mediata e ipersensibilità DF come non-IgE-mediata dalla BAT.
Protocollo
1. Preparazione di coniugati farmaco
- Sciogliere 10 mg DF in 1 ml di dH 2 O in una provetta da 1,5 ml di reazione. Nel procedere ulteriormente uso 95 ml di questa soluzione DF. A coniugare PP HSA sciogliere 30,4 mg di derivati PP (304 g / mol) in 500 microlitri 0,3 M di idrossido di sodio (NaOH).
- Aggiungi 430,6 microlitri dH 2 O e 100 l 0,5 M 2 - (N-morfolino) etano acido (MES) pH 6,5-95 l di DF sciolto. Aggiungi 33,1 microlitri dH 2 O e 140 ml di 2 M MES tampone pH 2,9 a campione PP.
- Aggiungere 57,5 ml di uno preparati al momento N-etil-N '- (3-dimetilamminopropil) carbodiimmide cloridrato (EDC) soluzione madre sciolto in dH 2 O con una concentrazione di 100 mg / ml al campione DF, o 10 ul di soluzione EDC per PP campione. Vortex i campioni per 1 minuto.
- Aggiungere 16,9 ml di soluzione di HSA con una concentrazione di 118 mg / ml per ogni campione.
- Incubare i campioni per 2 ore a temperatura ambiente agitando a 300 giri / min.
- Dializzare il DF e campioni di PP 3 volte contro le 2 litri di soluzione salina tampone fosfato (PBS) pH 7,4 per diverse ore ciascuno. Eseguire tutti i passaggi dialisi a 4 ° C.
- Centrifugare il campione 10 minuti a 14.000 xg e raccogliere il supernatante contenente DF o PP coniugato con HSA.
- Controllare surnatante per le proteine eseguendo un SDS-PAGE, utilizzando il 12% gel. Carico di circa 12 mg di HSA coniugato in uno slot gel.
2. Determinare il tasso di accoppiamento di coniugati farmaco (Figura 2)
- Per l'analisi del tasso di accoppiamento del DF e PP coniugati da HPSEC utilizzare una di sodio 100 mM tampone fosfato pH 6,5 contenente 150 mM di NaCl e sodio azide 0,05%. Utilizzare un 7,8 x 300 mm TSK-Gel-G2000 colonna SWXL.
- Eseguire il rilevamento dei segnali utilizzando un line-coupled RI e rivelatore sistema UV.
- Preparare un campione standard di HSA con una concentrazione di 1 mg / ml in DH 2 O. Per la calibrazione del rivelatore iniettare 50 microlitri HSA soluzione standard.
- Calcolare la costante k RI RI e UV UV costante k per il rivelatore. Utilizzare l'area formule RI RI = k * [(dn / dc) HSA * c (HSA)] e l'area UV UV = k * [(dA / dc) HSA * c (HSA)] con (dn / dc) HSA = 0,185 e (dA / dc) HSA = 0,518 5.
- Preparare DF e PP standard derivati HPSEC che ammonta 5, 10 e 30 nmol di entrambi gli standard possono essere facilmente iniettato.
- Calcolare i valori medi per (dn / dc), di droga e (dA / dc), farmaco per entrambi gli standard. Per DF, un (dn / dc) di 0,235 ± 0,010 e un (dA / dc) di 39,000 ± 0,493 è stato determinato. Per PP, una (dn / dc) di 0,328 ± 0,016 e un (dA / dc) di 53,155 ± 2,464 è stato determinato.
- Iniettare coniugati farmaco su HPSEC e determinare la loro RI e UV aree dei picchi.
- Calcolare la concentrazione di DF, derivati PP e HSA risolvendo l'area due equazioni RI RI = k * [(dn / dc) Farmaco * c (droga) + (dn / dc) HSA * c (HSA)] e UV zona UV = k * [(dA / dc) Farmaco * c (droga) + (dA / dc) HSA * c (HSA)] per le incognite.
3. BAT utilizzando coniugati farmaco
- Preparare sette coppe citometria a flusso e etichettarli a seconda del loro contenuto: controllo senza macchia, controllo negativo, controllo positivo, e coniugati droga.
- Pipettare 50 ml di B-CCR-STB buffer di stimolazione (FLOW2 CAST, Bühlmann Laboratories, Schönenbuch, CH) nel fiale riservato per il controllo senza macchia e negativo. Come controllo positivo, utilizzare 50 ml di un anti-FcεRI soluzione fornita dal kit FLOW2 CAST. Aggiungere la quantità appropriata della soluzione di coniugato alla fiale riservato ai coniugati farmaco creando una serie diluizione 1:10 da 0,02 -20 mg / ml DF coniugato e PP coniugato (concentrazioni finali in un volume dosaggio di 200 l). Questi esperimenti di titolazione devono essere eseguiti per determinare la concentrazione ottimale di attivazione dei basofili per ogni campione del paziente.
- Aggiungere 100 microlitri di buffer stimolo a ciascuna provetta con EDTA e sangue intero 50 microlitri del paziente. Mescolare accuratamente i campioni.
- Pipettare 20 l FLOW2 colorazione CAST reagente contenente anticorpi anti-CCR3 marcati con ficoeritrina (PE) e anti-CD63 anticorpi marcati con isotiocianato di fluorescina (FITC) per ciascuna provetta e mescolare nuovamente. Non pipettare colorazione del reagente nel campione senza macchia!
- Incubare i campioni per 45 minuti in un bagno d'acqua a 37 ° C.
- Fermare la reazione in ghiaccio per 5 minuti.
- Lisi degli eritrociti con l'aggiunta di 2,0 ml di reagente di lisi CAST FLOW2 ad ogni flacone e agitare delicatamente. Incubare i campioni al buio per 10 minuti a temperatura ambiente.
- Centrifugare i campioni per 5 minuti a 500 xg e decantare il surnatante con cura.
- Risospendere le cellule in 500 microlitri di buffer FLOW2 CAST lavare e conservare il ghiaccio fino citometria a flusso.
- S Regolare la tensione della citometria a flusso dimpostazioni per scatter in avanti e laterale (FSC, SSC) durante l'acquisizione del campione senza macchia.
- Porta le cellule come linfociti previsto dalla SSC-FSC complotto per la SSC-PE trama. Basofili sono identificati da un PE con etichetta anti-CCR3 anticorpi come CCR3 hi SSC lo e li porta nel FITC-PE trama. L'anticorpo anti-CD63 rilevazione basofili attivati è marcato con FITC.
- Impostare il cut-off ad un massimo del 2,5% dei basofili come CD63 hi nel controllo negativo. Un campione è considerato positivo per l'attivazione dei basofili se basofili> 5% sono CD63 hi e l'indice medio di fluorescenza (MFI) del campione divisa per la MFI del controllo negativo supera i 2 (Figura 3).
4. Rappresentante dei risultati:
Questo esperimento valuta BAT come uno strumento utile per rilevare IgE-dipendente ipersensibilità a farmaci. Coniugati proteina di FANS sono utilizzati per l'attivazione dei basofili. Da HPSEC con RI e rilevamento dello stato di aggregazione UV, il grado di accoppiamento, e la resa effettiva dei coniugati sono determinati. Come mostra la Figura 4 mostra, il 43,5% dei coniugati DF è rimasto monomerica con un grado di accoppiamento su 5,0 DF / HSA. Per gli aggregati un grado di accoppiamento di 9,5 è stata determinata. Il coniugato propyphenazone è stato dimostrato che consistono di monomeri 68,5% con un grado di accoppiamento di 21,2. Il grado di accoppiamento degli aggregati è stato 27,9. In totale, il grado di accoppiamento determinato di coniugati DF DF è stata di 7,6 e quello di coniugati PP era 23.2.
BAT eseguita con coniugati in condizioni ottimizzate (concentrazione di coniugati, il tempo di stimolazione) indagine ha permesso di IgE-dipendente reazioni di ipersensibilità FANS. Come mostrato nella Figura 5, solo il PP coniugato è stato in grado di innescare l'attivazione dei basofili visualizzati attraverso un up-regolazione dell'espressione di CD63 di superficie: 20,6% dei basofili sono stati attivati caratterizzati da un log-shift di intensità di fluorescenza. La IFM aumentato di un fattore pari a 4,9 da 386 (controllo negativo) al 1893. Al contrario, utilizzando il coniugato DF solo 3,1% dei basofili sono stati attivati, che era inferiore al 5% di cut-off. Anche la IFM è aumentato solo di un fattore 1,1 (limite 2,0) da 197 (controllo negativo) a 210. Validità del test è dato da (i) <5% di attivazione dei basofili nel controllo negativo, (ii) un log-spostamento di intensità di fluorescenza di una sottopopolazione basofili, e (iii)> 50% basofili attivati (controllo positivo).
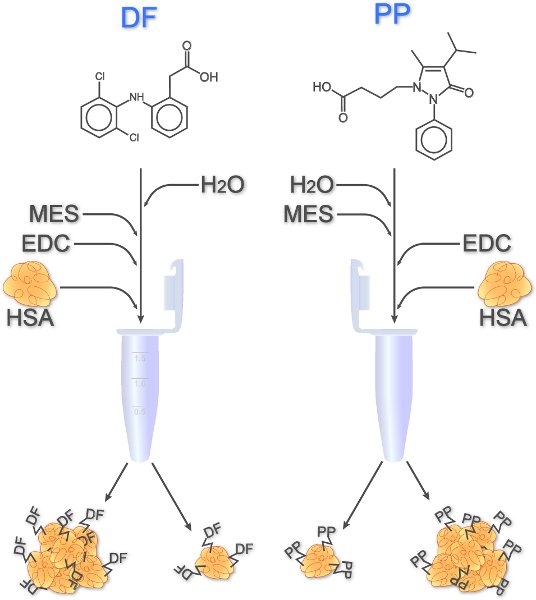
Figura 1. Accoppiamento di derivati DF e PP di HSA. Dopo aver sciolto le droghe, l'acqua, MES buffer e EDC (reagenti di accoppiamento) sono aggiunti. I campioni sono in agitazione per 1 minuto prima di HSA è pipettati alle soluzioni droga. Entro 2 ore agitazione a temperatura ambiente i farmaci si legano covalentemente alla HSA. Monomeri così come aggregati può causare.

Figura 2. Calcolo dei gradi di accoppiamento. In primo luogo, le costanti k RI e UV k sono determinati. Pertanto, HSA standard con concentrazione nota viene iniettato nel sistema HPSEC. (Dn / dc) e (dA / dc) di HSA sono riportati i valori di 0,185 e 0,518, rispettivamente 5. Le aree dei picchi sono utilizzati per calcolare le costanti. In secondo luogo, per ciascun farmaco viene iniettato tre standard per determinare droga e la concentrazione specifici per aree di RI e ai raggi UV. Dato che il RI k UV e le costanti k sono noti i passaggi precedenti, i derivati farmaco-specifici (dn / dc) e (dA / cc) può essere calcolato. In terzo luogo, droga HSA coniugati vengono iniettate nel HPSEC. Le aree dei picchi risultanti vengono utilizzati per calcolare le concentrazioni di farmaco e HSA al picco risolvendo le due equazioni con due incognite.
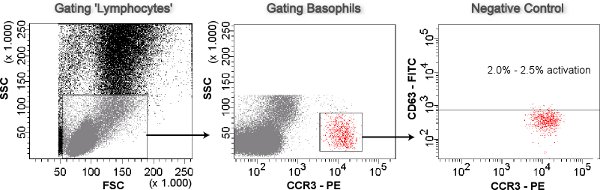
Figura 3. Gating basofili. Cellule come linfociti sono previsti side scatter gate contro forward scatter (SSC-plot FSC). I basofili sono identificati come CCR3 hi SSC lo dai linfociti gated (SSC-CCR3-PE trama). I basofili sono analizzati per l'attivazione (CD63 hi) nel CD63-FITC-CCR3-PE trama. Il controllo negativo viene utilizzato per impostare il cut-off del massimo basofili 2,5% rimanente CD63 hi.
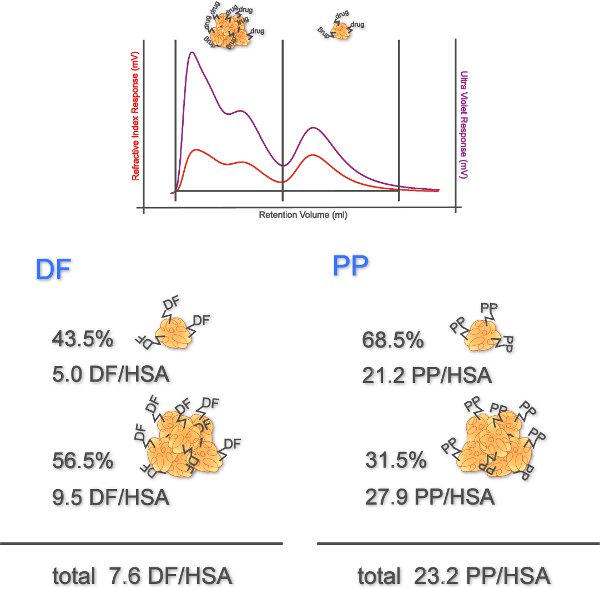
Figura 4. Gradi di accoppiamento determinato di coniugati farmaco. RI e segnali UV mostrano due picchi che rappresentano aggregati (eluizione a volume di ritenzione basso) e monomeri (eluizione a volume di ritenzione di altezza) di farmaco-HSA coniugati. Percentuali di monomeri e aggregati (determinata dai segnali RI) e le loro gradi di accoppiamento sono rappresentati (n = 1).
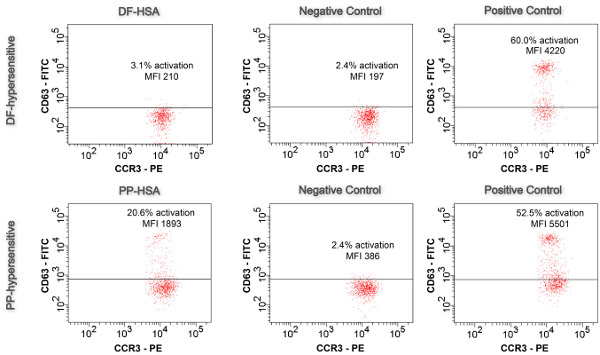
Figura 5. Basofili Activatiin prova. Risultati di farmaco coniugato attivato campioni, controlli negativi e controlli positivi sono mostrati in CD63-FITC-CCR3-PE trame (n = 1).
Discussione
BAT è una realtà consolidata anche se non ancora metodo utilizzato di routine per la diagnosi di IgE-mediata malattia allergica 6,7. Per ipersensibilità a farmaci, tuttavia, la sua applicabilità è compromessa come composti a basso peso molecolare non sono in grado di reticolazione recettori IgE, un prerequisito per l'attivazione dei basofili 8. Pertanto, i farmaci oggetto di indagine devono essere accoppiati in modo covalente alle proteine di trasporto idoneo (es. HSA). È importante sottolineare che il grado di accoppiamento (cioè il numero di molecole di farmaco per ogni proteina di trasporto) deve essere controllata per garantire attività immunologica (cioè recettore IgE cross-linking) delle coniugati. Teoricamente, due apteni per molecola vettore dovrebbe essere sufficiente per il recettore IgE cross-linking e un minimo di cinque molecole DF per HSA hanno dimostrato di innescare rilascio mediatore in un saggio basato su cellule 4. Entrambi i coniugati, PP-HSA e DF-HSA, sono stati determinati per visualizzare un grado di accoppiamento sufficientemente elevato (HPSEC) e di essere immunologicamente attive che li rende reattivi adatto per l'uso delle BAT. Un altro problema potrebbe essere che i metaboliti della droga può avere un ruolo, come un metabolita invece del farmaco può causare la reazione di ipersensibilità. In caso di DF, questa possibilità è stata valutata in dettaglio in precedenza utilizzando cinque Fase I principali metaboliti e una variante di collegamento 4. Fattori importanti per padroneggiare la tecnica descritta comprendono la qualità del campione di sangue (<12 ore dopo la raccolta del sangue, il numero dei basofili rilevato> 500) e l'ottimizzazione delle condizioni di stimolazione (tempo, dose). Inoltre, i cosiddetti non-responder che non hanno nemmeno reagire con il controllo positivo (anticorpo diretto contro il recettore IgE) devono essere identificati. Pertanto, i criteri di validazione devono includere un anti-FcεRI anticorpi come controllo positivo. Un importante vantaggio di usare coniugati farmaco è il fatto che appaiono non tossico in contrasto con la droga pura, come mostrato per DF-HSA coniugato dal co-stimolazione con anti-anticorpi in FcεRI BAT 4. DF puro, al contrario, mostra gli effetti citotossici ad una concentrazione di 1,25 mg / ml, causando problemi con l'interpretabilità delle BAT 9. Generalmente, i test di citotossicità potenziale è fortemente raccomandato per ogni coniugato di nuova produzione.
Qui, abbiamo dimostrato il potenziale di PP-HSA coniugato utilizzato in BAT per rivelare ipersensibilità IgE-mediata. Al contrario, DF ipersensibilità non è associato con livelli di IgE dimostrato dalla mancanza di attivazione dei basofili in risposta a DF-HSA coniugato. È importante sottolineare che, in caso di incertezza relativa ad un meccanismo IgE-mediata, coniugati devono essere valutati per l'attività immunologica da parte nei sistemi di dosaggio in vitro cell-based come è stato dimostrato per DF 4.
Utilizzando la configurazione descritta di coniugare i farmaci a basso peso molecolare covalente al vettore proteico adatto molecole una serie di reazioni di ipersensibilità contro la droga tra cui antibiotici, altri FANS, radiologico media, miorilassanti, anestetici, ecc possono essere indagato per un coinvolgimento di IgE-mediata meccanismo. Quindi, BAT può servire come aggiunta ai metodi esistenti per la diagnosi (test cutanei, test provocazione orale).
Divulgazioni
Nessun conflitto di interessi dichiarati.
Riconoscimenti
Questo lavoro è stato finanziato dal Fondo austriaco della scienza (FWF) concedere P18820-B13.
Etica dichiarazione:
Lo studio è stato approvato (PLUS_Ethik_090514) da parte del Comitato Etico per esperimenti che coinvolgono gli esseri umani e / o animali presso l'Università di Salisburgo conformi alle Declaraction di Helsinki modificata nel 1983 e tutti i pazienti partecipanti hanno dato il loro consenso informato scritto.
Materiali
| Name | Company | Catalog Number | Comments |
| Nome del reagente / dispositivo | Azienda | Numero di catalogo | Commenti |
|---|---|---|---|
| 2 - (N-Morpholino) etano acido | Sigma | M3671 | - |
| 7,8 x 300 mm TSK Gel -G2000SWXL colonna | Tosoh Bioscience | 08540 | - |
| BD FACSCanto II | Becton Dickinson | 338962 | - |
| Centrifuga da banco in alto | Sigma | - | - |
| Diclofenac sale sodico | Sigma | D6899 | - |
| EDTA-Vacutainer | Becton Dickinson | 368589 | - |
| FLOW2 CAST Kit | Bühlmann Laboratories | FK-CCR | Efficace CAST 14 Giugno 2011 FLOW2 kit è ora CAST di flusso |
| HP1100 sistema HPLC | Hewlett Packard | - | - |
| Albumina sierica umana | Sigma | A9511 | - |
| Laboratorio centrifuga | Eppendorf | - | - |
| N-etil-N'-(3-dimetilamminopropil) carbodiimmide cloridrato (EDC) | Sigma | E6383 | - |
| PBS compresse | Applichem | A9199 | - |
| Propyphenazone derivati | Dipartimento di Biologia Molecolare, Università di Salisburgo, Austria | - | - |
| Shaker | Eppendorf | - | - |
| Di sodio azide | Sigma | S8032 | - |
| Cloruro di sodio (NaCl) | Sigma | S1679 | - |
| Di sodio bicarbonato | Sigma | 90421C | - |
| Di sodio idrossido | Sigma | S5881 | - |
| Fosfato di sodio | Sigma | 342483 | - |
| Rivelatore a serie di triple | Viscotek | TDA302 | - |
| BioVortex personale V-1, più | Peqlab | 90-V-1 | - |
| Acqua del bagno 1012 | GFL | 1012 | - |
Riferimenti
- Himly, M. IgE-mediated immediate-type hypersensitivity to the pyrazolone drug propyphenazone. J Allergy Clin Immunol. 111, 882-888 (2003).
- Demoly, P., Pichler, W., Pirmohamed, M., Romano, A. Important questions in Allergy: 1--drug allergy/hypersensitivity. Allergy. 63, 616-619 (2008).
- Ebo, D. G., Hagendorens, M. M., Bridts, C. H., Schuerwegh, A. J., Clerck, L. S., Stevens, W. J. Flow cytometric analysis of in vitro activated basophils, specific IgE and skin tests in the diagnosis of pollen-associated food allergy. Cytometry Part B (Clinical Cytometry). 64B, (2005).
- Harrer, A. Diclofenac hypersensitivity: antibody responses to the parent drug and relevant metabolites. PLoS One. 5, e13707-e13707 (2010).
- Wen, J., Arakawa, T., Philo, J. S. Size-exclusion chromatography with on-line light-scattering, absorbance, and refractive index detectors for studying proteins and their interactions. Anal Biochem. 240, 155-166 (1996).
- De Weck, A. L., Sanz, M. L., Gamboa, P. M., Aberer, W., Bienvenu, J., Blanca, M., Demoly, P., Ebo, D. G., Mayorga, L., Monneret, G., Sainte Laudy, J. Diagnostic tests based on human basophils: more potentials and perspectives than pitfalls. II. Technical issues. J Investig Allergol Clin Immunol. 18, 143-155 (2008).
- Ebo, D. G. Flow-assisted allergy diagnosis: current applications and future perspectives. Allergy. 61, 1028-1039 (2006).
- Poulsen, L. K., Quan, S., Kragh, C., Platzer, M. H., Skov, P. S. The basophil granulocyte in allergic reactions: experimental models and their use for the identification of drugs with effects or side effects on basophils. Curr Med Chem - Anti-inflammatory & Anti-Allergy Agents. 3, 167-180 (2004).
- Sanz, M. L., Gamboa, P., de Weck, A. L. A new combined test with flowcytometric basophil activation and determination of sulfidoleukotrienes is useful for in vitro diagnosis of hypersensitivity to aspirin and other nonsteroidal anti-inflammatory drugs. Int Arch Allergy Immunol. 136, 58-72 (2005).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon