Method Article
Basophilenaktivierungstest für die Untersuchung von IgE-vermittelten Mechanismen in Drug Überempfindlichkeit
In diesem Artikel
Zusammenfassung
Basophilenaktivierungstest ist ein starkes Werkzeug für den Nachweis von IgE-abhängige Allergien In-vitro-. Hier ist ein optimiertes Protokoll für Basophilenaktivierungstest zur Arzneimittelüberempfindlichkeit untersuchen. Eine Methode für die effiziente Produktion von kovalenten Drogen-Protein-Konjugate und ihre physikalisch-chemischen Charakterisierung beschrieben wird.
Zusammenfassung
Überempfindlichkeitsreaktionen gegen nicht-steroidalen Antiphlogistika (NSAIDs) wie Propyphenazon (PP) und Diclofenac (DF) kann sich als Typ I-wie allergische Reaktionen 1. In der klinischen Praxis ist die Diagnose von Arzneimittelüberempfindlichkeit hauptsächlich durch Anamnese durchgeführt, wie Hauttests ist nicht zuverlässig und mündliche Provokationstestung trägt lebensbedrohliche Risiken für den Patienten 2. Daher ist ein Beweis für eine zugrunde liegende IgE-vermittelten Pathomechanismus schwer zu bekommen.
Hier präsentieren wir ein in vitro-Methode für die Verwendung von menschlichen Basophilen von Drogen-überempfindlichen Patienten, die allergische Reaktion Effektorzellen in vivo nachahmt abgeleitet werden. Als Basophilen von Drogen-allergischen Patienten IgE-Moleküle spezifisch für die Täter Drogen zu tragen, werden sie auf IgE-Rezeptor aktiviert Vernetzung und Freisetzung allergischer Effektormoleküle. Die Aktivierung von Basophilen kann durch die Bestimmung der Hochregulation von CD63 Oberflächenexpression mittels Durchflusszytometrie 3 überwacht werden.
Im Falle von niedermolekularen Medikamenten, sind Konjugate entwickelt, um IgE-Rezeptors Vernetzung auf Basophilen zu ermöglichen. Wie in Abbildung 1, zwei Vertretern der NSAIDs dargestellt, PP und DF, kovalent an humanes Serumalbumin (HSA) über eine Carboxylgruppe reagiert mit der primären Aminogruppe von Lysin-Reste gebunden. DF trägt eine intrinsische Carboxylgruppe und kann somit direkt 4 verwendet werden, während eine Carboxylgruppe enthaltende Derivat des PP musste organochemically vor der Studie 1 synthetisiert werden.
Die Kopplung Grad der niedermolekularen Verbindungen auf dem Protein-Träger-Molekül und ihrer räumlichen Verteilung ist wichtig, um die Vernetzung von zwei IgE-Rezeptor-Moleküle zu gewährleisten. Die hier beschriebene Protokoll gilt Hochleistungs-Größenausschlusschromatographie (HPSEC) mit einer sequentiellen Brechungsindex (RI) und Ultraviolett (UV)-Detektionssystem für die Bestimmung der Kopplungsgrad ausgestattet.
Da die beschriebene Methodik für andere Medikamente angewendet werden kann, trägt die Basophilenaktivierungstest (BAT) das Potenzial für die Bestimmung von IgE-vermittelten Mechanismen in Arzneimittelüberempfindlichkeit verwendet werden. Hier stellen wir fest, PP Hypersensibilität als IgE-vermittelten und DF Überempfindlichkeit wie BAT nicht IgE-vermittelt.
Protokoll
1. Herstellung von Wirkstoff-Konjugate
- Lösen Sie 10 mg DF in 1 ml dH 2 O in einem 1,5 ml Reaktionsgefäß. In die weitere Vorgehensweise verwenden 95 ul dieser DF-Lösung. Um Konjugat PP zu HSA auflösen 30,4 mg PP-Derivat (304 g / mol) in 500 ul 0,3 M Natronlauge (NaOH).
- Add 430,6 ul dH 2 O und 100 ul 0,5 M 2 - (N-Morpholino) ethansulfonsäure (MES)-Puffer pH 6,5 bis 95 mu l aufgelöst DF. Add 33,1 ul dH 2 O und 140 pl 2 M MES-Puffer pH 2,9 bis der PP-Probe.
- Add 57,5 ul einer frisch zubereiteten N-Ethyl-N '- (3-dimethylaminopropyl) carbodiimidhydrochlorid (EDC)-Stammlösung in dH 2 O mit einer Konzentration von 100 mg / ml, die DF Probe oder 10 ul EDC-Lösung aufgelöst der PP-Probe. Vortex die Proben für 1 Minute.
- Add 16,9 ul der HSA-Lösung mit einer Konzentration von 118 mg / ml zu jeder Probe.
- Inkubieren Sie die Proben für 2 Stunden bei Raumtemperatur unter Schütteln bei 300 U / min.
- Dialysieren die DF-und PP-Proben 3 mal gegen 2 l Phosphat-gepufferter Salzlösung (PBS) pH 7,4 für mehrere Stunden. Führen Sie alle Schritte Dialyse bei 4 ° C.
- Zentrifugieren Sie die Probe 10 Minuten bei 14.000 xg und den Überstand mit DF-oder PP-konjugierten HSA.
- Überprüfen Überstand für Proteine, die von der Durchführung einer SDS-PAGE mit 12% Gele. Legen Sie über 12 ug HSA-Konjugat in einem Gel-Steckplatz.
2. Bestimmen Kopplung von Arzneistoff-Konjugate (Abbildung 2)
- Für die Analyse der Kopplung von DF und PP-Konjugate von HPSEC mit einem 100 mM Natrium-Phosphat-Puffer pH 6,5, enthaltend 150 mM NaCl und 0,05% Natriumazid. Verwenden Sie einen 7,8 x 300 mm TSK-Gel-G2000 SWXL Spalte.
- Führen Erfassung von Signalen unter Verwendung eines Online-gekoppelten RI-und UV-Detektor-System.
- Bereiten Sie eine HSA-Standard-Probe mit einer Konzentration von 1 mg / ml in dH 2 O. Für Detektorkalibrierung Injektion von 50 ul HSA-Standard-Lösung.
- Berechnen Sie die RI k RI und UV k UV für den Detektor. Verwenden Sie die Formeln Bereich RI = k RI * [(dn / dc) HSA * c (HSA)] und Fläche UV = k UV * [(dA / dc) HSA * c (HSA)] mit (dn / dc) HSA = 0,185 und (dA / dc) HSA = 0,518 5.
- Bereiten DF-und PP-Derivat Standards für HPSEC, dass 5, 10 und 30 nmol Mengen beider Standards problemlos injiziert werden kann.
- Berechnen Sie die Mittelwerte für (dn / dc) Drogen-und (dA / dc) Medikament für beide Standards. Für DF, a (dn / dc) von 0,235 ± 0,010 und eine (dA / dc) von 39,000 ± 0,493 ermittelt wurde. Für PP, a (dn / dc) von 0,328 ± 0,016 und eine (dA / dc) von 53,155 ± 2,464 ermittelt wurde.
- Inject Arzneistoff-Konjugate auf HPSEC und bestimmen ihre RI-und UV-Peakflächen.
- Berechnen Sie die Konzentration von DF, PP-Derivat, und HSA durch die Lösung der beiden Gleichungen Bereich RI = k RI * [(dn / dc) Medikament * c (drug) + (dn / dc) HSA * c (HSA)] und Bereich UV = k UV * [(dA / dc) Medikament * c (drug) + (dA / dc) HSA * c (HSA)] für die Unbekannten.
3. BAT mit Arzneistoff-Konjugate
- Bereiten sieben Durchflusszytometrie Fläschchen und beschriften Sie sie je nach ihrem Inhalt: ungefärbte Kontrolle, Negativ-Kontrolle, positive Kontrolle und Arzneistoff-Konjugate.
- Je 50 ul der B-CCR-STB Stimulation-Puffer (Flow2 CAST, Bühlmann Laboratories, Schönenbuch, CH) in das Fläschchen für die ungefärbten und negative Kontrolle vorbehalten. Als positive Kontrolle, verwenden 50 ul einer anti-FcεRI Lösung durch die Flow2 CAST-Kit zur Verfügung gestellt. Fügen Sie die entsprechenden Mengen von Konjugat-Lösung, um die Fläschchen für die Arzneimittel-Konjugate durch die Schaffung einer 1:10 Verdünnungsreihe von 0,02 -20 pg / ml DF-Konjugat-und PP-Konjugat (Endkonzentrationen in einem Assay Volumen von 200 ul) vorbehalten. Diese Titration Experimente müssen durchgeführt werden, um die Konzentration der optimalen Basophilenaktivierung für jeden Patienten Probe zu bestimmen.
- 100 l Stimulation-Puffer in jedes Röhrchen und 50 ul Patienten EDTA-Vollblut. Mischen Sie die Proben vorsichtig.
- Je 20 ul Flow2 CAST Färbereagenz mit anti-CCR3 Antikörper mit Phycoerythrin (PE) und anti-CD63 Antikörper mit Fluorescein-Isothiocyanat (FITC) in jedes Röhrchen beschriftet und nochmals mischen. Nicht Pipette Färbereagenz in den ungefärbten Probe!
- Inkubieren Sie die Proben für 45 Minuten bei 37 ° C Wasserbad.
- Stop-Reaktion auf Eis für 5 Minuten.
- Lyse Erythrozyten durch Zugabe von 2,0 ml Flow2 CAST Lysereagenz in jedes Fläschchen und vortexen. Inkubieren Proben im Dunkeln für 10 Minuten bei Raumtemperatur.
- Centrifuge Proben für 5 Minuten bei 500 xg und sorgfältig dekantieren.
- Die Zellen in 500 ul Flow2 CAST Waschpuffer und speichere sie auf Eis, bis der Durchflusszytometrie.
- Passen Sie das Durchflusszytometer die Spannung sINSTELLUNGEN für Vorwärts-und Seitwärts-Streulicht (FSC, SSC), während dem Erwerb der ungefärbten Probe.
- Tor der Zellen vorhersagen, wie Lymphozyten aus dem SSC-Plot FSC auf die SSC-PE Grundstück. Basophile sind durch eine PE-markiertem anti-CCR3 Antikörper als CCR3 hallo SSC lo und Tor sie in die FITC-PE Grundstück identifiziert. Die anti-CD63 Antikörper erkennen aktivierten Basophilen ist mit FITC markiert.
- Stellen Sie die cut-off um maximal 2,5% der Basophilen als CD63 hallo in die Negativ-Kontrolle. Eine Probe gilt als positiv, wenn> 5% Basophile CD63 hallo und die mittlere Fluoreszenz (MFI) der Probe durch die MFI der negativen Kontrolle unterteilt übersteigt 2 (Abbildung 3) sind für Basophilenaktivierung.
4. Repräsentative Ergebnisse:
Dieses Experiment wertet BAT als ein nützliches Hilfsmittel, um IgE-abhängige Arzneimittelüberempfindlichkeit erkennen. Protein-Konjugate von NSAR sind für die Aktivierung von Basophilen verwendet. Durch HPSEC mit RI-und UV-Detektion Aggregatzustand, Kopplungsgrad und effektive Rendite der Konjugate ermittelt. Wie Abbildung 4 zeigt, blieb 43,5% der DF-Konjugate monomeren mit einem Kopplungsgrad von 5,0 DF / HSA. Für die Aggregate eine Kupplung Grad von 9,5 ermittelt wurde. Die Propyphenazon Konjugat wurde gezeigt, dass von 68,5% Monomeren mit einem Kopplungsgrad von 21,2 bestehen. Die Kopplung Grad der Aggregate betrug 27,9. Insgesamt war das bestimmt Kopplungsgrad der DF-Konjugate 7,6 DF und der PP-Konjugate betrug 23,2.
BAT mit Konjugaten unter optimierten Bedingungen (Konzentration der Konjugate, die Stimulation der Zeit) erlaubt Untersuchung von IgE-abhängige Reaktionen in NSAID Überempfindlichkeit durchgeführt. Wie in Abbildung 5 dargestellt, war nur der PP-Konjugat in der Lage, Auslöser Basophilenaktivierung visualisiert durch eine Hochregulation in CD63 Oberflächenexpression: 20,6% der Basophilen wurden aktiviert gekennzeichnet durch eine log-Verschiebung der Fluoreszenz-Intensität. Die MFI um den Faktor von 4,9 von 386 (negative Kontrolle), um 1893. Im Gegensatz dazu mit dem DF-Konjugat nur 3,1% der Basophilen wurden aktiviert, wurde die Schwelle von 5% cut-off. Auch die MFI erhöhte sich nur um den Faktor 1,1 (Grenzwert 2,0) von 197 (negative Kontrolle) auf 210. Assay Gültigkeit ist gegeben durch (i) <5% Basophilenaktivierung in die Negativ-Kontrolle, (ii) ein Protokoll-Verschiebung der Fluoreszenzintensität eines basophil Subpopulation, und (iii)> 50% aktivierten Basophilen (positive Kontrolle).
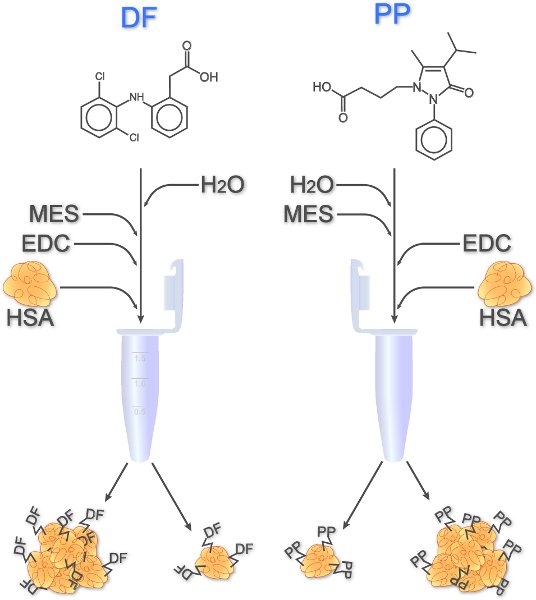
Abbildung 1. Kopplung von DF und PP-Derivat zu HSA. Nach dem Auflösen der Drogen-, Wasser-, MES-Puffer und EDC (Kupplungsreagenzes) zugegeben. Die Proben werden für 1 Minute gevortext, bevor HSA, um das Medikament Lösungen pipettiert wird. Innerhalb von 2 Stunden bei Raumtemperatur unter Schütteln die Medikamente kovalent an HSA. Monomere sowie Aggregate führen kann.

Abbildung 2. Berechnung der Kopplung Grad. Erstens sind die Konstanten k und k RI UV bestimmt. Daher ist HSA-Standard mit bekannter Konzentration in die HPSEC System injiziert. (Dn / dc) und (dA / dc) der HSA sind Werte von 0,185 und 0,518 gegeben, bzw. 5. Die Peakflächen sind für die Berechnung der Konstanten verwendet. Zweitens, für jedes Medikament drei Standards injiziert werden, um Drogen-und Konzentrations-spezifischen RI-und UV-Bereiche zu ermitteln. Da die k RI und UV k Konstanten aus den oben genannten Schritte bekannt sind, kann der Wirkstoff-spezifischen (dn / dc) und (dA / dc)-Derivate berechnet werden. Drittens, Drogen-HSA-Konjugate sind in HPSEC injiziert. Die daraus resultierenden Peakflächen werden verwendet, um die Konzentration der Drogen-und HSA pro Peak durch Lösen der zwei Gleichungen mit zwei Unbekannten zu berechnen.
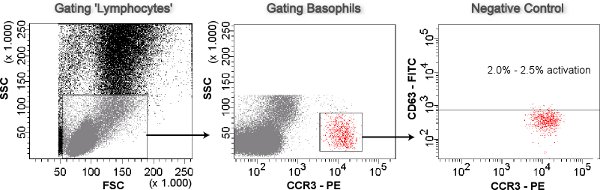
Abbildung 3. Basophil Gating. Cells prognostiziert, wie Lymphozyten gated side scatter gegenüber Vorwärtsstreuung (SSC-FSC Plot) werden. Die Basophilen sind CCR3 hallo SSC lo aus der gated-Lymphozyten (SSC-CCR3-PE Grundstück) identifiziert. Basophile sind für die Aktivierung (CD63 hallo) in den CD63-FITC-CCR3-PE Plot analysiert. Die negative Kontrolle wird verwendet, um den Cut-off von maximal 2,5% Basophile übrigen CD63 hallo gesetzt.
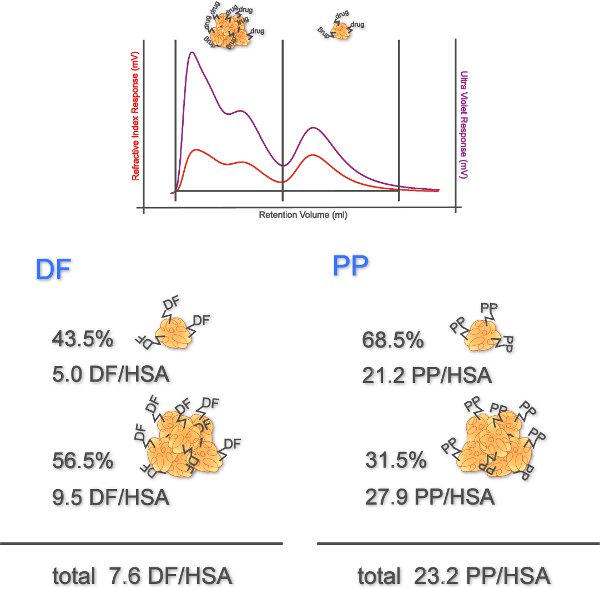
Abbildung 4. Entschlossen Kopplung Grad der Arzneimittel-Konjugate. RI-und UV-Signale zeigen zwei Peaks, welche Aggregate (Elution bei niedrigen Retentionsvolumen) und Monomere (Elution bei hohen Retentionsvolumen) von Drogen-HSA-Konjugate. Prozentuale Anteile der Monomere und Aggregate (ermittelt aus RI-Signale) und deren Kopplung Grad (n = 1) dargestellt.
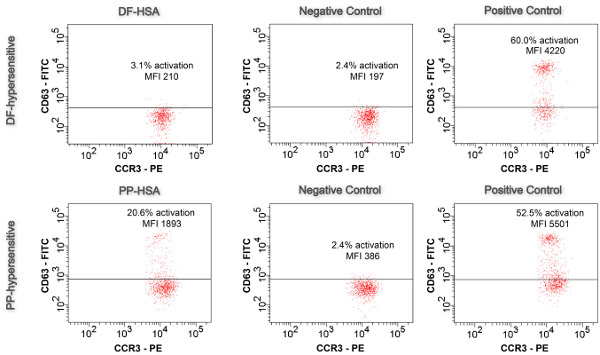
Abbildung 5. Basophil Activatizu testen. Die Ergebnisse der Drogen-Konjugat-aktivierten Proben, negativen Kontrollen und Positivkontrollen sind in CD63-FITC-CCR3-PE-Flächen (n = 1) dargestellt.
Diskussion
BAT ist eine gut etablierte, aber noch nicht routinemäßig Verfahren zur Diagnose von IgE-vermittelten allergischen Erkrankungen 6,7 verwendet. Für Arzneimittelüberempfindlichkeit jedoch ist seine Anwendbarkeit gefährdet als niedermolekulare Verbindungen nicht in der Lage sind zu vernetzen IgE-Rezeptoren, eine Voraussetzung für Basophilenaktivierung 8. Deshalb brauchen Drogen untersucht kovalent an geeigneten Carrier-Proteine (zB HSA) gekoppelt werden. Wichtig ist, muss die Kupplung Grad (dh die Zahl der Wirkstoff-Moleküle pro Trägerprotein) kontrolliert werden, um immunologische Aktivität zu gewährleisten (dh IgE-Rezeptors Vernetzung) der Konjugate werden. Theoretisch sollten zwei Haptene pro Trägermolekül ausreichend für IgE-Rezeptors Vernetzung und nur fünf DF-Molekülen pro HSA haben gezeigt, dass Mediatorfreisetzung in einem zellbasierten Assay 4 Trigger. Beide Konjugate, PP-HSA und DF-HSA, ermittelt worden sind, um eine ausreichend hohe Kopplungsgrad (HPSEC) anzuzeigen und zu immunologisch aktiven und eignen sich Reagenzien für den Einsatz in BAT. Ein weiteres Problem könnte sein, dass Drogenmetaboliten eine Rolle spielen, als Metabolit anstelle der Eltern Medikament kann die Überempfindlichkeit verursachen. Im Falle von DF, hat diese Möglichkeit im Detail zuvor mit fünf großen Phase-I-Metaboliten und eine Verknüpfung der Variante 4 bewertet worden. Wichtige Faktoren für die Bewältigung der beschriebenen Technik zählen Qualität der Blutprobe (<12 Stunden seit der Blutentnahme, die Anzahl der erkannten Basophilen> 500) und Optimierung der Stimulation (Zeit, Dosis). Darüber hinaus Non-Responder, die nicht einmal mit der positiven Kontrolle (Antikörper gegen den IgE-Rezeptor gerichtet sind) zu identifizieren, die zu reagieren sogenannten. Deshalb haben Validierungskriterien zu einer Anti-FcεRI Antikörper als positive Kontrolle beinhalten. Ein wichtiger Vorteil der Verwendung von Arzneistoff-Konjugate ist die Tatsache, dass sie ungiftig im Gegensatz zu reinen Drogen, wie für DF-HSA-Konjugat durch Co-Stimulation mit anti-FcεRI Antikörper in BAT 4 dargestellt erscheinen. Reine DF, dagegen zeigt zytotoxische Wirkung bei einer Konzentration von 1,25 mg / ml zu Problemen mit der Interpretierbarkeit der BAT 9. Im Allgemeinen ist das Testen für potentielle Zytotoxizität stark für jede neu produzierte Drogenkonjugat empfohlen.
Hier haben wir das Potenzial der PP-HSA-Konjugat in BAT verwendet werden, um IgE-vermittelte Überempfindlichkeit zeigen, dargestellt. Im Gegensatz dazu ist DF Überempfindlichkeit nicht mit IgE durch den Mangel an Basophilenaktivierung in Reaktion auf DF-HSA-Konjugat nachgewiesen verbunden. Wichtig ist, dass im Falle der Unsicherheit bezüglich einer IgE-vermittelten Mechanismus haben Konjugate für die immunologische Aktivität in vitro Zell-basierten Testsystemen untersucht, wie es für DF 4 gezeigt.
Mit dem beschriebenen Aufbau der Konjugation, niedermolekulare Wirkstoffe kovalent an geeigneten Protein-Träger-Molekülen eine Reihe von Überempfindlichkeitsreaktionen gegen Arzneimittel, einschließlich Antibiotika, andere NSAIDs, radiocontrast Medien, Muskelrelaxantien, Anästhetika, etc. können für eine Beteiligung einer IgE-vermittelten untersucht werden Mechanismus. Daher kann BAT als Ergänzung zu den bestehenden Verfahren für die Diagnose (Hauttest, orale Provokation Test) dienen.
Offenlegungen
Keine Interessenskonflikte erklärt.
Danksagungen
Diese Arbeit wurde vom österreichischen Wissenschaftsfonds (FWF) gewähren P18820-B13 gefördert.
Ethik-Anweisung:
Die Studie wurde genehmigt (PLUS_Ethik_090514) von der Ethikkommission für Versuche am Menschen und / oder Tiere an der Universität Salzburg die Einhaltung der Helsinki Declaraction als im Jahr 1983 überarbeitet und alle teilnehmenden Patienten gaben ihr schriftliches Einverständnis.
Materialien
| Name | Company | Catalog Number | Comments |
| Name des Reagenzes / device | Firma | Katalog-Nummer | Kommentare |
|---|---|---|---|
| 2 - (N-Morpholino) ethansulfonsäure | Sigma | M3671 | - |
| 7,8 x 300 mm TSK Gel -G2000SWXL Spalte | Tosoh Bioscience | 08540 | - |
| BD FACSCanto II | Becton Dickinson | 338962 | - |
| Tischzentrifuge | Sigma | - | - |
| Diclofenac-Natrium-Salz | Sigma | D6899 | - |
| EDTA-Vacutainer | Becton Dickinson | 368589 | - |
| Flow2 CAST Kit | Bühlmann Laboratories | FK-CCR | Effektive 14. Juni 2011 Flow2 CAST-Kit ist jetzt Durchfluss CAST |
| HP1100 HPLC-System | Hewlett Packard | - | - |
| Humanem Serumalbumin | Sigma | A9511 | - |
| Laborzentrifuge | Eppendorf | - | - |
| N-Ethyl-N'-(3-dimethylaminopropyl) carbodiimid Hydrochlorid (EDC) | Sigma | E6383 | - |
| PBS-Tabletten | AppliChem | A9199 | - |
| Propyphenazon derivative | Department of Molecular Biology, University of Salzburg, Österreich | - | - |
| Shaker | Eppendorf | - | - |
| Natriumazid | Sigma | S8032 | - |
| Natriumchlorid (NaCl) | Sigma | S1679 | - |
| Natriumhydrogencarbonat | Sigma | 90421C | - |
| Natronlauge | Sigma | S5881 | - |
| Natriumphosphat | Sigma | 342483 | - |
| Triple-Detektor-Array | Viscotek | TDA302 | - |
| Persönliche BioVortex V-1 plus | Peqlab | 90-V-1 | - |
| Wasserbad 1012 | GFL | 1012 | - |
Referenzen
- Himly, M. IgE-mediated immediate-type hypersensitivity to the pyrazolone drug propyphenazone. J Allergy Clin Immunol. 111, 882-888 (2003).
- Demoly, P., Pichler, W., Pirmohamed, M., Romano, A. Important questions in Allergy: 1--drug allergy/hypersensitivity. Allergy. 63, 616-619 (2008).
- Ebo, D. G., Hagendorens, M. M., Bridts, C. H., Schuerwegh, A. J., Clerck, L. S., Stevens, W. J. Flow cytometric analysis of in vitro activated basophils, specific IgE and skin tests in the diagnosis of pollen-associated food allergy. Cytometry Part B (Clinical Cytometry). 64B, (2005).
- Harrer, A. Diclofenac hypersensitivity: antibody responses to the parent drug and relevant metabolites. PLoS One. 5, e13707-e13707 (2010).
- Wen, J., Arakawa, T., Philo, J. S. Size-exclusion chromatography with on-line light-scattering, absorbance, and refractive index detectors for studying proteins and their interactions. Anal Biochem. 240, 155-166 (1996).
- De Weck, A. L., Sanz, M. L., Gamboa, P. M., Aberer, W., Bienvenu, J., Blanca, M., Demoly, P., Ebo, D. G., Mayorga, L., Monneret, G., Sainte Laudy, J. Diagnostic tests based on human basophils: more potentials and perspectives than pitfalls. II. Technical issues. J Investig Allergol Clin Immunol. 18, 143-155 (2008).
- Ebo, D. G. Flow-assisted allergy diagnosis: current applications and future perspectives. Allergy. 61, 1028-1039 (2006).
- Poulsen, L. K., Quan, S., Kragh, C., Platzer, M. H., Skov, P. S. The basophil granulocyte in allergic reactions: experimental models and their use for the identification of drugs with effects or side effects on basophils. Curr Med Chem - Anti-inflammatory & Anti-Allergy Agents. 3, 167-180 (2004).
- Sanz, M. L., Gamboa, P., de Weck, A. L. A new combined test with flowcytometric basophil activation and determination of sulfidoleukotrienes is useful for in vitro diagnosis of hypersensitivity to aspirin and other nonsteroidal anti-inflammatory drugs. Int Arch Allergy Immunol. 136, 58-72 (2005).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten