Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Electroforesis Capilar La separación del anticuerpo monoclonal isoformas El uso de un capilar Neutral
En este artículo
Resumen
Here, we present a comprehensive capillary zone electrophoresis protocol for the assessment of intrinsic physicochemical heterogeneity of monoclonal antibodies as a quality attribute.
Resumen
Biotherapeutic proteins, such as monoclonal antibodies (mAbs), are feasible alternatives for the treatment of chronic-degenerative diseases. The biological activity of these proteins depends on their physicochemical properties. The use of high-performance techniques like chromatography and capillary electrophoresis has been described for the analysis of physicochemical heterogeneity of mAbs. Nowadays, capillary zone electrophoresis (CZE) technique constitutes one of the most resolutive and sensitive assays for the analysis of biomolecules. Besides, the electro-driven separation in CZE is governed by extensive properties of matter and offers the advantage of analyzing proteins close to their native state. However, the successful implementation of this technique for routine analysis depends on the skills of the analyst at the critical steps during sample and system preparation. The purpose of this tutorial is to detail the steps to succeed in the CZE analysis of mAbs. Further, this protocol can be used for the development and improvement of skills of the personnel involved in protein analytical chemistry laboratories.
Introducción
Los anticuerpos monoclonales (mAb) son proteínas bioterapéuticos con creciente interés debido a su capacidad para actuar contra varias enfermedades crónicas y degenerativas 1. Al igual que otras biomoléculas, mAbs son propensos a someterse a varias modificaciones fisicoquímicas en todas las etapas de su ciclo de vida (es decir, desde la biosíntesis en el producto final). Tales modificaciones incluyen, pero no se limitan a: la desamidación, glicosilación, oxidación, ciclación, isomerización, la agregación y la escisión proteolítica 2. Por lo tanto, se necesitan técnicas analíticas capaces de resolver isoformas intrínsecas para supervisar mAbs heterogeneidad y la estabilidad con el fin de establecer las especificaciones de calidad.
La electroforesis capilar (CE) es una tecnología de separación de alto rendimiento realizado outinside de un tubo de sílice fundida estrecho (rango de micras) lleno de un electrolito de fondo (BGE). Tras la aplicación de un campo eléctrico (hasta 30,000 V), molécula cargadas migran hacia el electrodo con carga opuesta (es decir, la separación electro-driven). El uso de altas tensiones en CE permite análisis rápidos y aumento de la eficiencia, que son superiores a electroforesis en gel clásico. Electroforesis de zona capilar (CZE) es una técnica basada en la CE se utiliza rutinariamente en la industria biofarmacéutica para la evaluación de la calidad del producto 3-9. A diferencia de otros modos de CE (por ejemplo, electroforesis en gel capilar, isoeléctrico capilar de enfoque) o métodos basados en la cromatografía, CZE puede llevarse a cabo sin el uso de desnaturalizantes o interfaces en fase sólida, lo que permite el análisis de la heterogeneidad inherente de mAbs cerca de su estado nativo 10 . Separación CZE de isoformas de mAb se produce en el interior de un capilar de sílice fundida cubierto con un polímero hidrófilo (capilar neutro) y se basa en su movilidad electroforética diferente, que es gobernado por la carga, la masa, el tamaño y la forma (o volumen hidrodinámico) 11. restos de mAb se detectan cuandose movilizan y pasan a través de la ventana de detección, que es detectado por un detector de ultravioleta (UV) de la absorbancia a 214 nm 4.
La implementación exitosa de esta técnica analítica dependerá de la debida atención a los detalles antes y durante el experimento. Actuar de otra manera se incrementará el costo y el tiempo para llevar a cabo el análisis, en última instancia conduce a la insuficiencia constante y frustración.
A continuación, presentamos una guía paso a paso para llevar a cabo un análisis exitoso de mAb heterogeneidad mediante CZE través de la explicación detallada de la preparación de soluciones y muestras, la preparación del sistema de la CE, los métodos de instrumentos creados, la adquisición de datos, y el procesamiento. Para el propósito de este tutorial, un factor de necrosis antitumoral recombinante alfa totalmente humano (anti-TNF) mAb se utiliza como modelo de proteína; Sin embargo, este protocolo se puede personalizar fácilmente para el análisis de otras proteínas considerando breves modificaciones. UNdicionalmente, una serie de recomendaciones para mitigar los posibles problemas se proponen. Se invita al lector a seguir estrictamente el protocolo propuesto, como la probabilidad de tener éxito se incrementará.
Protocolo
1. Preparación de soluciones
- Preparar la solución de BGE.
- Preparar 100 ml de una solución compuesta de 0,05% (m / v) de celulosa hidroxi propil metil celulosa (HPMC), 200 mM ε-amino n-caproico (EACA) y acetato de litio 30 mM.
NOTA: Como HPMC es un polímero viscoelástico, verter el polvo en un vaso de precipitados de vidrio, añadir 80 ml de agua y, finalmente, añadir la barra de agitación. Continúe añadiendo los reactivos restantes como normalmente. Use gafas de seguridad al manipular acetato de litio, ya que puede causar irritación en los ojos. - Ajustar a pH 4,8 ± 0,1 con 50% (v / v) de ácido acético. Deje que la solución se estabilice durante 5 min y ajustar según sea necesario.
- Añadir agua para completar hasta un volumen final de 100 ml en matraz aforado.
- Filtrar a través de una membrana hidrófila con un tamaño de poro 0,2 micras.
- Almacenar a 2-8 ° C durante un máximo de 7 días.
- Preparar 100 ml de una solución compuesta de 0,05% (m / v) de celulosa hidroxi propil metil celulosa (HPMC), 200 mM ε-amino n-caproico (EACA) y acetato de litio 30 mM.
- Preparar el estándar interno.
- Preparar 1 mlde una solución compuesta de 1% (m / v) de histamina.
- Filtrar a través de una membrana hidrófila con un tamaño de poro 0,2 micras.
- Almacenar a 2-8 ° C durante un máximo de 1 día.
Preparación 2. Muestra
- Preparar 180 l de muestra mAb diluido con tampón Tris (tris 50 mM (hidroximetil) aminometano, pH 8,0) a una concentración final de 1 mg / ml.
- Añadir 20 l de 1% (m / v) de histamina.
- Mezclar y centrifugar a 1.000 xg durante 5 seg.
- Colocar un vial micro dentro de un vial universal.
- Transferir la muestra en el vial micro y tapar el vial universal. Dispensar la muestra hacia arriba con el fin de evitar la introducción de burbujas.
- Almacenar a 2-8 ° C durante un máximo de 1 día.
- Colocar el vial universal (con vial micro que contiene la solución de muestra) en la bandeja de entrada de muestra.
3. Preparación de Sistema CE.
- Limpieza del sistema de la CE.
NOTA: J Conductaes el procedimiento por lo menos una vez a la semana con el fin de evitar la fuga de corriente eléctrica derivada de la acumulación de polvo y escombros. Sin embargo, dependiendo de la aplicación (por ejemplo, el uso de un BGE con el aumento de la viscosidad o con alta concentración de sal, las muestras con un aumento de viscosidad) electrodos y palancas de apertura puede requerir ser limpiado más frecuentemente para evitar la contaminación cruzada y el arrastre de muestra.- Apague el interruptor de alimentación del instrumento CE y abrir la puerta principal.
- Limpiar la superficie de la cubierta de la muestra, la muestra que contiene el sistema (tampón de muestra y bandejas), cubierta del cartucho, la barra de sujeción, bloque de interfaz y los electrodos con un material no tejido humedecido en agua y limpie. Repita el procedimiento con una mezcla de etanol-humedecido limpie y seque antes de su uso.
- Enjuagar las palancas de apertura a fondo con agua. Limpiar su superficie con un trapo no tejido. Repita el procedimiento con una mezcla de etanol-humedecido limpie y seque antes de la instalación.
- Limpiar los dos extremos del cable de fibra óptica cuidadoly con un paño de microfibra humedecido en agua. Repita el procedimiento con un paño humedecido con etanol.
- El conjunto de cartucho.
- Retirar un nuevo capilar neutro (50 micras de diámetro interno) de su envoltorio.
- Pegue un extremo del tubo de protección capilar a la mesa de trabajo. Uncoil, enderezar y tire de la capilaridad hacia fuera del tubo.
- Stick un trozo de cinta o papel para la mesa de trabajo y añadir marcas de medición de la siguiente manera: longitud al detector (30 cm), ventana capilar (0,2 cm) y la longitud al extremo de salida (10 cm) (es decir, longitud 40,2 cm total 30,0 cm de longitud efectiva).
- Alinear la ventana capilar hasta la marca de medición de 0,2 cm en el documento de referencia. Fijar el capilar con cinta y marcar el capilar final: 2 mm fuera de las marcas de medición.
- Cortar la tapa de protección en el extremo de entrada capilar (el extremo más alejado de la ventana) en un solo movimiento lineal utilizando el borde a ras de la piedra de escisión.
- Sumergir el extremo capilar en un vial tapado universales lleno de agua a fin de evitar daños permanentes en el revestimiento interno capilar. Repita este procedimiento cada vez que el extremo capilar se expone al ambiente durante más de 1 min.
- Insertar el extremo de entrada capilar en el lado de salida del cartucho.
- Empujar y tirar del capilar a través del cartucho como sea necesario hasta que la ventana está centrada capilar a la ventana cartucho.
- Inserte la clavija del orificio (100 micras x 200 micras) en la ventana del cartucho.
NOTA: Confirme que la luz blanca pasa a través de la ventana cuando se expone a una fuente de luz blanca. Si la luz que pasa a través de tiene una apariencia de color marrón, realice los ajustes necesarios. - Insertar el capilar en el tubo de refrigerante preformada para una longitud total de 40,2 cm capilar (con la tuerca de la tubería pre-instalado, casquillo y la junta tórica en ambos extremos en ese orden).
- Empuje el capilar a través de la coolant tubo como sea necesario hasta que el capilar aparece en el otro lado de la tubería.
- Insertar el extremo del tubo de refrigerante en el lado de salida del cartucho y apretar la tuerca de la tubería.
- Insertar el extremo de entrada capilar en el lado de entrada del cartucho.
- Empuje y tire del capilar a través del cartucho según sea necesario hasta que el capilar aparece en el lado de entrada del cartucho.
- Insertar el extremo del tubo de refrigerante en el lado de entrada del cartucho y apretar la tuerca de la tubería.
- Cortar la tapa de protección en el extremo de salida capilar (el extremo más cercano de la ventana) en un solo movimiento lineal utilizando el borde a ras de la piedra de escisión.
- Inserte los clips de foca-retención sobre los extremos de los capilares y presione hasta que encaje en su posición. inspeccionar visualmente los extremos del capilar. Si no lo son, incluso, repita el procedimiento.
- Coloque la plantilla capilar de longitud en el borde de la mesa de trabajo.
- Coloque el cartucho hacia abajo against la plantilla capilar de longitud y alinear el capilar termina con las líneas de referencia en la plantilla. Si las marcas de medición capilar (véase 3.2.4) no se alinean con las líneas de referencia, realice los ajustes necesarios.
- Mantenga el capilar contra la plantilla capilar de longitud y corte ambos extremos del capilar utilizando el borde a ras de la escisión de piedra 2 mm por debajo de las líneas de referencia de la plantilla.
- inspeccionar visualmente el capilar termina con una lupa. Si extremos de los capilares no son lisas, bruñido utilizando la cara suave de la piedra de escisión.
- Inserte la junta tórica abertura en el orificio del tapón de apertura utilizando la herramienta de inserción junta tórica.
- Instalar viales tapados universales llenas de agua en la vaina del cartucho y el cartucho lugar en caso inmediatamente con extremos capilares insertados en viales. Para el almacenamiento a corto y largo plazo, mantener a 2-8 ° C.
- Preparación de bandejas de amortiguamiento.
- Llenar y colocar tapados universAL viales en la entrada de la memoria intermedia y bandejas de salida (Figura 1). posiciones de los viales de repetición en los carriles 2, 3, 4 y 5 de acuerdo con el número de muestras a analizar, la colocación de un carril por cada seis inyecciones de muestra.
NOTA: no mojar los tapones de los viales con el fin de evitar la fuga de corriente.
- Llenar y colocar tapados universAL viales en la entrada de la memoria intermedia y bandejas de salida (Figura 1). posiciones de los viales de repetición en los carriles 2, 3, 4 y 5 de acuerdo con el número de muestras a analizar, la colocación de un carril por cada seis inyecciones de muestra.
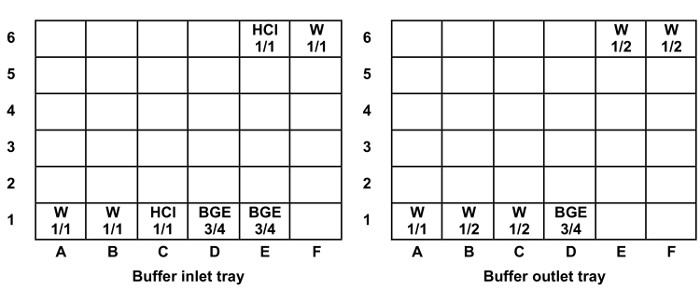
Figura 1: Posición y el nivel de llenado de viales universales en las bandejas de entrada y de salida de amortiguación. Llenar los niveles: 1/1 = 1.400 l, 3/4 = 1.300 l y 1/2 = 1000 l. Abreviaturas: W = agua, HCl = ácido clorhídrico 0,1 M. Haga clic aquí para ver una versión más grande de esta figura.
- Sistema de montaje de componentes del CE.
- Instalar el detector de UV.
- Instalar la palanca de aperturapresionando hacia arriba en el bloque de interfaz.
- Instalar el cable de fibra óptica. Inserte el extremo correspondiente a la barra de sujeción y, manteniendo ambos extremos, gire hacia la derecha. Conectar el otro extremo al detector UV.
NOTA: Maneje el cable de fibra óptica con cuidado durante este procedimiento, ya que podría causar la flexión de su fractura. - Coloque la muestra y las bandejas de amortiguamiento en el sistema de retención de la muestra y encajen en su posición.
- Coloque el cartucho capilar en el bloque de interfaz y, mientras presiona la barra de sujeción en ambos extremos, apretar los botones.
4. Métodos de configuración del instrumento
- Crear el acondicionamiento, el funcionamiento y los métodos de instrumentos de apagado de acuerdo con los siguientes parámetros y en la Tabla 1: Tensión, max: 30,0 kV; Actual, máxima: 300,0 mu; Cartucho de temperatura: 20.0 ° C; temperatura de almacenamiento de la muestra: 10,0 ° C; detector UV condiciones iniciales: Longitud de onda: 214 nm; Velocidad de datos: 4 Hz; Filtro: normal; anchura del pico (Puntos): 16-25; señal de absorbancia: Directo.
NOTA: velocidad de adquisición de datos se puede aumentar hasta 25 Hz con el fin de mejorar la cobertura de zonas de separación estrechos.
| programa de tiempo método acondicionado | |||||||
| Tiempo (min) | Evento | Valor | Duración | vial de entrada | vial de salida | Resumen | comentarios |
| - | Enjuague - Presión | 2068 mbar | 1.0 min | BI: C1 | BO: C1 | Adelante | HCl 0,1 M |
| - | Enjuague - Presión | 2068 mbar | 2.0 min | BI: B1 | BO: C1 | Adelante | Agua |
| - | Enjuague - Presión | 2068 mbar | 10,0 min | BI: E1 | BO: C1 | Adelante | BGE |
| 0.00 | Separada - Tensión | 15.0 KV | 10,0 min | BI: D1 | BO: D1 | 0,17 rampa Min, polaridad normal | Separar |
| 10.00 | Enjuague - Presión | 2758 mbar | 10,0 min | BI: E1 | BO: C1 | Adelante | BGE |
| 20.01 | Espere | - | 0.0 min | BI: A1 | BO: A1 | - | consejos de enjuague |
| Ejecución del programa de tiempo método | |||||||
| Tiempo (min) | Evento | Valor | Duración | vial de entrada | vial Outlet | Resumen | comentarios |
| - | Enjuague - Presión | 2068 mbar | 1.0 min | BI: C1 | BO: C1 | Adelante, Entrada / Salida inc vial 6 | HCl 0,1 M |
| - | Enjuague - Presión | 2068 mbar | 2.0 min | BI: B1 | BO: C1 | Adelante, Entrada / Salida inc 6 vial | Agua |
| - | Enjuague - Presión | 2068 mbar | 4,0 min | BI: E1 | BO: C1 | Adelante, Entrada / Salida inc vial 6 | BGE |
| - | Inyectar - Presión | 34 mbar | 20.0 seg | SI: A1 | BO: B1 | Anular, Adelante | inyección de la muestra |
| - | Espere | - | 0,4 min | BI: A1 | BO: A1 | Entrada / Salida inc vial 6 | consejos de lavado |
| 0 | Separada - Tensión | 15.0 KV | 30,0 min | BI: D1 | BO: D1 | 0,17 rampa mínima, polaridad normal, de entrada / salida inc vial 6 | La separación de la muestra |
| 0,5 | Cero automático | - | - | - | - | - | - |
| 30.01 | Deja de datos | - | - | - | - | - | - |
| 30.02 | Enjuague - Presión | 2068 mbar | 2.0 min | BI: B1 | BO: C1 | Adelante, Entrada / Salida inc vial 6 | Agua |
| 32.03 | Espere | - | 0.0 min | BI: A1 | BO: A1 | Entrada / Salida inc vial 6 | consejos de enjuague |
| 32.04 | Fin | - | - | - | - | - | Fin |
| programa de tiempo método shutdown | |||||||
| Tiempo (min) | Evento | Valor | Duración | vial de entrada | vial de salida | Resumen | comentarios |
| - | Enjuague - Presión | 2068 mbar | 1.0 min | BI: E6 | BO: E6 | Adelante | HCl 0,1 M |
| - | Enjuague - Presión | 2068 mbar | 6,0 min | BI: F6 | BO: F6 | Adelante | Agua |
| - | Lámpara - Off | - | - | - | - | - | - |
| - | Espere | - | 0.0 min | BI: A1 | BO: A1 | - | consejos de enjuague |
Tabla 1: acondicionado, correr y programas de tiempo de apagado.
5. Adquisición de Datos y Procesamiento
- Programar el conjunto de la muestra.
- Programar el capilar para el acondicionamiento usando el método acondicionado instrumento. Cuando el capilar se utiliza por primera vez, el programa de cuatro repeticiones; de lo contrario programar sólo dos repeticiones del método acondicionado.
- Programar las muestras a ser analizadas utilizando el método de funcionamiento del instrumento.
- Programar el capilar de almacenamiento mediante el método de apagado del instrumento y repita el procedimiento indicado en el apartado 3.2.22.
- Ejecutar el experimento.
- Exportar la electropherograms.
- Calcular el tiempo de migración y el contenido porcentual de, un principal básicond isoformas ácidas usando integración de la línea de caída vertical del perfil de electroferograma.
Resultados
La Figura 2 muestra el perfil de corriente eléctrica típica de un EACA 200 mM, acetato de litio 30 mM, pH 4,8 BGE con muestra de anti-TNFa mAb diluido con tampón de Tris (50 mM, pH 8,0). Como se puede observar, la corriente es estable durante todo el análisis y puede oscilar entre los valores de 30 a 35 mu. Figura 3 muestra el electroferograma CZE de una muestra en blanco en el que el pico detectado se corresponde con el patrón interno de histamina....
Discusión
En este tutorial, destacamos la importancia de las prácticas adecuadas cuando se realizan los análisis de CZE de anticuerpos monoclonales con el fin de aumentar la probabilidad de tener éxito. Sin embargo, cuando se utiliza CZE de forma rutinaria, los problemas surgen inevitablemente 12.
Para obtener los mejores resultados, es importante seguir las notas que se incluyeron durante todo el protocolo, ya que ayudarán al analista para superar y resolver problemas de pasos difícil...
Divulgaciones
The authors Carlos E. Espinosa-de la Garza, Rodolfo D. Salazar-Flores, Néstor O. Pérez, Luis F. Flores-Ortiz and Emilio Medina-Rivero are employees of Probiomed S.A. de C.V., which is developing, manufacturing and marketing biosimilar products. All authors are involved in the development of biosimilar products for Probiomed.
Agradecimientos
The authors thank Wiley for the granted permission to use the concepts of the following publication for this tutorial. Carlos E. Espinosa-de la Garza, Francisco C. Perdomo-Abúndez, Jesús Padilla-Calderón, Jaime M. Uribe-Wiechers, Néstor O. Pérez, Luis F. Flores-Ortiz, Emilio Medina-Rivero: Analysis of recombinant monoclonal antibodies by capillary zone electrophoresis. Electrophoresis. 2013. 34. 1133-1140. Copyright Wiley-VCH Verlag GmbH & Co. KGaA. This work was supported by CONACyT, Mexico, grant 230551.
Materiales
| Name | Company | Catalog Number | Comments |
| Glacial acetic acid | Tecsiquim | AT0035-7 | |
| ACS grade hydrochloric acid | J.T. Baker | 9535-05 | |
| Histamine dihydrochloride | Fluka | 53300 | |
| (Hydroxypropyl) methyl cellulose | Fluka | 09963 | |
| Lithium acetate | Sigma-Aldrich | 517992 | |
| 6-Aminocaproic acid | Sigma-Aldrich | A2504 | |
| eCAP Tris Buffer, 50.0 mM, pH 8 | Beckman Coulter | 477427 | |
| PA 800 Plus Pharmaceutical Analysis System | Beckman Coulter | A66528 | |
| eCAP Neutral capillary | Beckman Coulter | 477441 | |
| Vial, Micro, 200 µl | Beckman Coulter | 144709 | |
| Universal Vial Caps | Beckman Coulter | A62250 | |
| Universal Vials | Beckman Coulter | A62251 | |
| Cable, Optics, UV/Vis | Beckman Coulter | 144093 | |
| UV/Vis Detector Module | Beckman Coulter | 144733 | |
| Cartridge Assembly Kit, Blank | Beckman Coulter | 144738 |
Referencias
- Bruno, V., Battaglia, G., Nicoletti, F. The advent of monoclonal antibodies in the treatment of chronic autoimmune diseases. Neurol. Sci. 31, 283-288 (2011).
- Liu, H., Gaza-Bulseco, G., Faldu, D., Chumsae, C., Sun, J. Heterogeneity of monoclonal antibodies. J. Pharm. Sci. 97 (7), 2426-2447 (2008).
- Creamer, J. S., Oborny, N. J., Lunte, S. M. Recent advances in the analysis of therapeutic proteins by capillary and microchip electrophoresis. Anal. Methods. 6 (15), 5427-5449 (2014).
- Fekete, S., Guillarme, D., Sandra, P., Sandra, K. Chromatographic, Electrophoretic, and Mass Spectrometric Methods for the Analytical Characterization of Protein Biopharmaceuticals. Anal. Chem. 88 (1), 480-507 (2016).
- He, Y., et al. Analysis of identity, charge variants, and disulfide isomers of monoclonal antibodies with capillary zone electrophoresis in an uncoated capillary column. Anal. Chem. 82 (8), 3222-3230 (2010).
- He, Y., Isele, C., Hu, W., Ruesch, M. Rapid analysis of charge variants of monoclonal antibodies with capillary zone electrophoresis in dynamically coated fused-silica capillary. J. Sep. Sci. 34 (5), 548-555 (2011).
- Zhao, S. S., Chen, D. D. Y. Applications of capillary electrophoresis in characterizing recombinant protein therapeutics. Electrophoresis. 35 (1), 96-108 (2014).
- Štěpánová, S., Kašička, V. Determination of impurities and counterions of pharmaceuticals by capillary electromigration methods. J. Sep. Sci. 37 (15), 2039-2055 (2014).
- Štěpánová, S., Kašička, V. Recent applications of capillary electromigration methods to separation and analysis of proteins. Anal. Chim. Acta. 933, 23-42 (2016).
- Espinosa-de la Garza, C. E., et al. Analysis of recombinant monoclonal antibodies by capillary zone electrophoresis. Electrophoresis. 34 (8), 1133-1140 (2013).
- Staub, A., Guillarme, D., Schappler, J., Veuthey, J. L., Rudaz, S. Intact protein analysis in the biopharmaceutical field. J. Pharm. Biomed. Anal. 55 (4), 810-822 (2011).
- Altria, K. D., Altria, K. D. Troubleshooting. Methods in Molecular Biology, Vol 52. Capillary Electrophoresis Guidebook: Principles, Operation and Applications. , (1996).
- Ma, S., Nashabeh, W. Analysis of protein therapeutics by capillary electrophoresis. Chromatographia. 53 (5), 75-89 (2001).
- Jaccoulet, E., Smadja, C., Prognon, P., Taverna, M. Capillary electrophoresis for rapid identification of monoclonal antibodies for routine application in hospital. Electrophoresis. 36 (17), 2050-2056 (2015).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados