Method Article
Purificación de proteínas de histona H4, H3 y la cuantificación de las marcas acetilado histonas en las células y el tejido cerebral
En este artículo
Resumen
El propósito de este artículo es proporcionar a una guía completa y sistemática a la purificación eficiente de las histonas H3 y H4 y la cuantificación de residuos de histona acetilado.
Resumen
En todos los organismos eucariotas, la cromatina, la plantilla fisiológica de la información genética de todo, es esencial para la herencia. La cromatina está sujeta a una variedad de diversas modificaciones postraduccionales (PTMs) que en su mayoría ocurren en los términos aminos de las proteínas de la histona (es decir, la cola de la histona) y regulan la accesibilidad y el estado funcional del ADN subyacente. Colas de las histonas se extienden desde el núcleo del nucleosoma y están sujetos a la adición de grupos acetil de las histonas acetiltransferasas (HATs) y la eliminación de grupos acetil de las histonas deacetilasas (HDACs) durante el crecimiento celular y diferenciación. Patrones de acetilación específicos en residuos de lisina (K) en la cola de la histona determinan una homeostasis dinámica entre cromatina transcripcionalmente activa o transcripcionalmente reprimida (1) influyendo en la Asamblea de las histonas centrales y (2) reclutamiento sinérgico o proteínas asociadas a cromatina antagonistas del sitio de transcripción. El mecanismo regulador fundamental de la naturaleza compleja de la cola de la histona PTMs influye en la mayoría de los procesos con plantilla de cromatina y resulta en cambios en la maduración celular y la diferenciación en el desarrollo normal y patológico. El presente informe pretende proporcionar a novicios con un método eficiente para purificar proteínas de histona de núcleo de las células y el tejido cerebral y cuantificar confiablemente marcas de acetilación de las histonas H3 y H4.
Introducción
El término epigenética se refiere a cambios heredables en la actividad de los genes que se producen independientemente de los cambios en la secuencia de ADN1,2. Represión y transcripción genética se determinan por (1) la accesibilidad de la DNA cromosómica envuelta alrededor de un octámero de proteínas histonas de base (dos copias de cada uno de H2A, H2B, H3 y H4) y (2) la disponibilidad de factores de transcripción y las proteínas del andamio reclutó a promotor específico sitios3,4. Transcripción de genes está regulada por modificaciones mediada por enzima de sitios específicos de promotor de ADN y el PTMs histonas colas5,6,7. El termini N de las histonas H3 y H4 son entre las secuencias más altamente conservadas en los organismos eucariotas3, y sus modificaciones del posttranslational se han documentado extensivamente para desempeñar un papel central en la determinación de la estructura de la cromatina y función8,9. MPa en las colas de las histonas (es decir, acetilación, metilación, fosforilación y ubiquitinación) cambia el potencial de interacción de las colas, influyen en el estado estructural y plegamiento de la fibra de cromatina y por lo tanto, regula la accesibilidad del DNA y el proceso4,10,11,12. Grupos acetilo se agregan a y quitar residuos de K en la cola de las histonas por un sistema de interacción con las histonas epigenéticos las enzimas específicas, es decir, sombreros y HDACs, respectivamente13. Por ejemplo, la acetilación de la histona H4 en lisina 12 (H4K12ac) se ha demostrado previamente para activar la transcripción de genes relacionados con la adquisición y consolidación de memoria14. Además, varias líneas de evidencia sugieren que el control epigenético mediada por enzima de la transcripción del gene es un aspecto fundamental de salud celular crecimiento y diferenciación6,15. Alternancia en la regulación epigenética de la expresión de genes, modificaciones epigenéticas del ADN o por una mutación de las enzimas epigenéticas, se ha demostrado que altera en enfermedades humanas, donde el cambio en la actividad de un gen en particular es una de la patología (p. ej., cáncer)6,16,17. Así, la evaluación de los cambios en las histonas core PTMs está emergiendo como un objetivo de alto valor para las intervenciones terapéuticas potenciales. Sin embargo, determinar la abundancia, socios de interacción y roles específicos del PTMs histonas ha demostrado difícil18.
En el presente informe se describe una estrategia optimizada, de mediano rendimiento para purificar las histonas de la base de las células y los tejidos del cerebro en una sola fracción y un protocolo completo para la cuantificación de las histonas H3 y H4 MPa. De nota, aunque actualmente publicados basados en el ácido técnicas de purificación y las estrategias de detección basados en anticuerpos histonas se han adoptado ampliamente para la caracterización de las histonas, carecen de detalles descriptivos con respecto a los pasos críticos del procedimiento, así dificultando la extracción rápida y replicable de la histona y cuantificación. Por ejemplo, la transformación de célula del extracto y biopsias de tejido requiere de diferentes herramientas y tecnologías para la extracción exitosa. Además, el protocolo optimizado presentado en el manuscrito actual demuestra un enfoque práctico, medio de rendimiento. Las histonas Core se extraen como una fracción simple, pura, que permite la detección fiable del downstream anticuerpo-mediada PTM sin ninguna interferencia de impurezas. Además, en el manuscrito actual, los desafíos en cuanto a detección de histona debido a su pequeño peso molecular han sido burlados. Por lo general, la falta de compatibilidad entre protocolos de la electroforesis de gel, purificación y cuantificación impide que los científicos obtener resultados reproducibles y concluyentes. Aquí, se presenta un flujo de trabajo optimizado para purificar las histonas de la base de las células y tejidos y prepararlos para aguas abajo PTM análisis por western blot.
El protocolo actual permite la purificación de proteínas de las histonas del core conservando sus modificaciones del posttranslational nativos (por ejemplo, acetilación, metilación y fosforilación). La figura 1 muestra la línea de tiempo del Protocolo de purificación de las histonas.
Protocolo
Todos los ratones estaban alojados en un control de humedad y temperatura, acreditadas por AAALAC Animalario en la Facultad de Medicina Miller de la Universidad de Miami. Todos los experimentos fueron aprobados por la Universidad de Miami Miller School de medicina institucional Animal Care y el Comité uso (IACUC) y realizados según las especificaciones del NIH.
1. preparación del extracto de muestra
-
Células adherentes
- Células de la placa en platos de 10 cm en los medios de cultivo adecuados (1 x 106 a 1 x 109 células por plato para líneas celulares, como BV2, HEK-293 y SH-SY5Y, pero ~ 1 x 10 células de15 por plato para células primarias, como las neuronas corticales primarias). Asegurar que las células se distribuyen igualmente en toda la superficie de la placa y permiten a las células a crecer durante 48 h para llegar a la confluencia de ~ 100% (37 ° C, 5% CO2).
- Una vez que las células han alcanzado la confluencia deseada, suavemente Aspire los medios de cultivo y lavado las células 2 x con medios libres de suero precalentados bajo una campana de cultivo de tejidos.
- Aspire los medios libres de suero desde el plato y añadir 1 mL de tampón de extracción helada (0,4 M el ácido sulfúrico, 1 mM KCl, 1 mM MgCl2, 50 mM Tris-HCl [pH 8.0] y 1 x inhibidor de la proteasa cóctel) para cada plato.
- Use un raspador de plástico celular para recoger todas las células en el tampón de extracción (por raspado) y transferirlos a un 1.5 mL etiquetado tubo con una pipeta de 1000 μl. Pipetear las células arriba y abajo 3 x para facilitar la homogeneización.
- Cerrar todos los tubos y ponerlos inmediatamente en hielo.
-
Tejido cerebral
- Si se utiliza tejido congelado, coloque el tejido en un tubo de 1,5 mL prechilled y brevemente la descongele el hielo. Si se utiliza tejido fresco, proceder de inmediato a paso 1.2.2.
Nota: El protocolo actual describe procedimientos con cerebro de ratón congelado y las muestras de corteza prefrontal de ratón. - Homogeneizar el tejido utilizando un homogeneizador handheld de Dounce usando la cantidad apropiada de tampón de extracción y la cantidad recomendada de trazos (tabla 1). Para evitar la destrucción de cromatina excesiva, no exceda el número de trazos recomendadas.
- Con una solo canal 1.000 μl pipeta, transfiera el homogeneizado a un tubo de prechilled 1,5 mL. Cerrar todos los tubos y ponerlos inmediatamente en hielo.
- Si se utiliza tejido congelado, coloque el tejido en un tubo de 1,5 mL prechilled y brevemente la descongele el hielo. Si se utiliza tejido fresco, proceder de inmediato a paso 1.2.2.
2. preparación del extracto crudo de la histona
- Colocar los tubos de 1.5 mL que contienen las células o tejido suspendidas en tampón de extracción en una plataforma giratoria y gira a 15 rpm a 4 ° C para permitir la extracción de crudo histonas.
Nota: El tiempo de extracción puede variar para diferentes celulares y tipos de tejido y debe ser optimizado para cada procedimiento. El protocolo actual presenta los resultados obtenidos después de 15 min, 2 h y 24 h de la extracción (figura 2, figura 3, figura 4y figura 5). - Prechill la microcentrífuga a 4 ° C. Transcurrido el tiempo deseado de la extracción, centrifugar los tubos a máxima velocidad por 10 min a 4 ° C.
- Transferir el sobrenadante como las histonas crudas a un tubo de 1,5 mL nuevo, prechilled. Deseche los pellets.
- Guarde el sobrenadante a-80 ° C (la extracción se puede detener en este paso, vea "Paso de parada" en la figura 1) o proceder inmediatamente al siguiente paso.
- Neutralizar las histonas crudas con un volumen de 1/4 de 5 x buffer de neutralización (por ejemplo, Añadir 250 μl de 5 x buffer de neutralización a 1 mL de crudo histonas). Mezclar por pipeteo arriba y abajo x 6.
- Compruebe el pH de la mezcla con tiras de pH. Ajustar en consecuencia añadiendo más tampón de neutralización para llegar a un pH de 7.
- Evaluar la presencia de histonas y proteínas nonhistone en la histona cruda extracto como sigue (figura 2).
- Añadir 37.5 μl de la muestra a 12,5 μl de 4 x (Laemmli) tampón y desnaturalizar por 10 min a 99 º C.
- Cargar la muestra en un gel de SDS-PAGE y ejecutar el gel durante 1 h a 100 V.
- Teñir el gel durante la noche con la solución de tinción de R-250 azul brillante de Coomassie y desteñir durante tres lavados consecutivos (1 h/lavado) con la solución de extracción de R-250 azul brillante de Coomassie.
Nota: Las histonas crudas (figura 2) pueden compararse con las histonas eluídas y purificadas (es decir, entrada de columna [figura 5A]).
3. purificación de las histonas del Core
-
Spin columna equilibrado
- Añadir 500 μl de tampón de equilibrado a cada columna de giro se utiliza. No toque la membrana de la columna.
- Centrifugar a 4 ° C por 3 min a 800 x g. Deseche el flujo a través. Repetir 1 x.
-
Purificación de las histonas
- Añadir 500 μl de la muestra de interés en el paso 2.6 a la columna. Centrifugar a 4 ° C por 3 min a 800 x g. Recoge el flujo a través.
- Repita el paso anterior tantas veces como sea necesario para cargar toda la muestra a la columna. No llene demasiado la columna de vuelta.
- Combinar el flujo a través de cada paso de centrifugación para analizar la eficiencia del enlace de la columna (figura 3).
- Siga el paso 2.7 analizar la columna flujo a través.
-
Lavado de la columna
- Añadir 500 μl de la solución de lavado para cada columna. Centrifugar a 4 ° C por 3 min a 800 x g. Recoge el flujo colada (#1).
- Repita el paso 3.3.1 para un total de tres lavados. Recoger a través de flujo de lavado #2 y #3. La piscina no los columna consecutiva flujo lavados.
- Para evaluar eficacia de unión a histonas de la columna, analizar los lavados tres columna siguiendo el paso 2.7 (figura 4).
-
Elución de la histona
- Transfiera la columna a un nuevo tubo con 1,5 mL.
- Añada 50 μl del buffer de elución de las histonas. Centrifugar a 4 ° C por 3 min a 800 x g. Guardar el flujo que contienen histona las proteínas.
- Una elución adicional, repita el paso 3.4.2. No combinar el primeras y segundo paso eluidos como difieren en la pureza y la cantidad de histonas.
4. precipitación de las histonas del Core
- Añadir ácido perclórico (PCA) a las histonas purificadas a una concentración final de 4% PCA (por ejemplo, agregar 3 μl de 70% PCA a 50 μl de las histonas purificadas del paso 3.4.2.
- Centrífuga de 3 s para recoger todo el líquido residual de la pared del tubo. Mezclar mediante pipeteo arriba y abajo x 6.
- Colocar los tubos en un bastidor e incubar por 24 h a 4 ° C.
- Al día siguiente, prechill una microcentrífuga a 4 ° C y centrifugar las muestras durante 75 minutos a la velocidad máxima a 4 ° C.
- Una vez finalizada la centrifugación, una pequeña pelotilla blanca que contiene histonas precipitadas será visible en la parte inferior del tubo. No no agitar con vortex de la muestra.
- Cuidadosamente aspirar el sobrenadante y, sin perturbar el pellet, Añadir 500 μl de helada 4% PCA a la muestra.
- Centrifugar a 4 ° C por 10 min a velocidad máxima. Cuidadosamente aspirar el sobrenadante.
- Repita el paso 4,7 2 x.
- Sin perturbar el pellet, agregar 500 μl de acetona fría. Centrifugar a 4 ° C por 10 min a velocidad máxima. Cuidadosamente aspirar el sobrenadante.
- Repita el paso 4,9 2 x.
- Cuidadosamente aspirar el sobrenadante, dejar los tubos destapados y la muestra se seque en hielo durante 30 minutos comprobar si todos acetona residual se evapore.
- Dejar los tubos destapado y permitir que la muestra se seque a temperatura ambiente (RT) durante 5 minutos.
- Resuspender el pellet en 30 μl de agua estéril. No no la pipeta hacia arriba y hacia abajo. Flick el tubo suavemente con un dedo.
- Tapa todos los tubos y deje que las histonas reconstituir en hielo por 30-50 min, dependiendo del tamaño del pellet. Compruebe si el pellet se resuspendió.
- Tapa todos los tubos y deje que la pelotilla a suspender más a temperatura ambiente durante 5 minutos.
Nota: Esta solución (primera y segunda elución de paso 3.4.3) se constituye de las histonas purificadas y desaladas y puede utilizarse para el análisis adicional de la acetilación de la cuantificación y las histonas.
5. cuantificación de proteínas histonas eluídas
- Use un espectrofotómetro según protocolo del fabricante para cuantificar las proteínas histonas total obtenidas después de la elución final en paso 4.15. Medir la absorbancia a 230 nm. Anote el cociente A260/A280 de la contaminación de las muestras con ácidos nucleicos.
- Utilice la siguiente fórmula para calcular la concentración de las histonas (x):
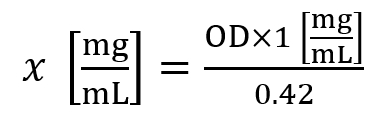
Aquí, el OD es la densidad óptica medida a A230 nm. - Una concentración de histona de ~1.5 mg/mL se considera un rendimiento promedio de líneas celulares, mientras que una concentración de histona de ~5.0 mg/mL se considera un rendimiento promedio de 30 mg de tejido.
6. Western Blot análisis
- Ajustar la histona purificada y eluída de paso 4.15 a ~ 10 μg de proteína histona/muestra.
- Añadir el volumen adecuado de agua y 4 x Laemmli tampón para ajustar los volúmenes de carga.
- Desnaturalizar las muestras durante 10 min a 99 º C. Enfriarlos en hielo. Centrífuga de 3 s para recoger todo el líquido residual y condensación de la pared del tubo.
- Cargar las muestras en un gel de SDS-PAGE y ejecutar el gel durante 1 h a 100 V.
- Para visualizar la proteína histona total, manchar el gel durante la noche con la solución de tinción de R-250 azul brillante de Coomassie y desteñir durante tres lavados consecutivos (1 h/lavado) con la solución de extracción de R-250 azul brillante de Coomassie.
Nota: La primera elución de proteínas histonas contiene histonas (figura 5A) de alta calidad mientras que la segunda elución contiene bajo ninguna niveles de histonas (figura 5B). - Para cuantificar el PTMs histonas, utilizar un sistema de transferencia (véase Tabla de materiales) para transferir la proteína histona del gel de SDS-PAGE (paso 6.4) sobre una membrana PVDF.
- Para armar el sándwich de transferencia, abra el cartucho del sistema de transferencia y coloque la pila de membrana PVDF (etiquetada como fondo +) en la parte inferior del cassette con la membrana hacia arriba. Rollo de membrana ligeramente con un rodillo de blot para quitar cualquier aire entre la pila y la membrana.
- Coloque el gel sobre la membrana de rollo el gel suavemente con un rodillo de blot para quitar cualquier aire entre la membrana y el gel y coloque la pila superior sobre el gel. Suavemente el rodillo otra vez Coloque la cubierta de cassette sobre el sándwich, presione firmemente hacia abajo y gire en sentido horario para trabar el nob.
- Inserte el casete en la ranura del sistema de transferencia. En la pantalla del aparato, seleccionar Protocolo de Turbo. Utilizar un protocolo de 3 min por un solo gel mini o un protocolo de 7 minutos para más de dos geles mini.
- Mancha la membrana con colorante Ponceau S por 5 min y visualizar las proteínas histonas total.
- Lavar en 1 x solución salina tamponada con Tris (TBS) con 0,1% Tween 20 para 2 h y el bloque en el 5% de leche para 1 h. incubar con el anticuerpo primario y secundario (durante la noche a 4 ° C o 1 h a temperatura ambiente, respectivamente) o según un protocolo previamente optimizado.
Nota: en el protocolo actual, H3K27 y anticuerpos contra acetilados histonas H4K12 (figura 6 y figura 7) (figura 8) fueron utilizados.
Resultados
Para ilustrar la evolución del Protocolo de purificación de las histonas y la composición de todas las fracciones analizadas, se evaluaron las histonas diferentes extractos de células microgliales humano BV2. Para demostrar la cuantificación de las histonas H3 y H4 PTMs (es decir, la acetilación), se utilizaron lisados de tejidos del cerebro.
BV2 células eran plateadas en 5 x 106 células por plato en platos de cultivo de tejidos tratados de 10 cm y permite crecer a confluencia para 48 h. luego se recolectaron las células y las histonas fueron lanzadas de la cromatina por una incubación en tampón de extracción que contiene 0,4 M ácido sulfúrico, 1 mM KCl, 1 mM MgCl2, 50 mM Tris-HCl (pH 8,0) y 1 x inhibidor de la proteasa. El tiempo de extracción, entre 15 min y 24 h, no afectó la composición de extractos de crudo histona por Coomassie azul brillante coloración (figura 2). Las histonas siguientes, crudas pasaron a través de las columnas de histona equilibrado y el flujo a través se analizaron. Eficiencia de la columna obligatorio está determinado por la ausencia de la proteína histona en el paso cuando se analizan por la coloración azul brillante de Coomassie. Se determinó la eficiencia de la columna obligatorio al 100% ya que hay ninguna proteína histona detectables presente en el análisis paso (figura 3). Todas las membranas con las histonas enlazadas luego se lavaron tres veces con tampón de lavado para eliminar las impurezas restantes, dejando las proteínas histonas sólo al gel de sílice. Determinamos que, para la extracción de todas las histonas veces (es decir, 15 min, 2 h y 24 h), el primer lavado de la membrana era el más importante eliminar contaminaciones nonhistone de las columnas, mientras que el segundo y tercer lavado no influyó en la pureza de la muestra. Así, dependiendo del tipo de muestra, los dos últimos lavados pueden omitirse. Tras la primera elución de la proteína histona de la columna (usando el tampón de elución que contiene NaCl 1mM y EDTA), histonas precipitadas durante la noche con 4% el ácido perclórico y luego peleteadas, lavadas y analizadas por el enriquecimiento de purificada histonas H3 y H4. Observamos 24 h de tiempo de extracción aumenta la cantidad de las histonas H3 y H4 en la fracción purificada en comparación a 15 min y 2 h de tiempo de extracción (figura 5A). La segunda elución de la columna no se tradujo en alta calidad o alta cantidad de histonas (figura 5B).
A continuación, utilizamos homogenados de tejido cerebral para cuantificar las histonas H3 y H4 MPa, es decir, acetilación. Tipo salvaje (C57BL6/J) ratones machos fueron administrados una amplia acción inhibidor de HDAC (tributirina) en una dosis de 5 g/kg por vía oral de 3 tejido d. entero-cerebro fue recogido el día 4 y las histonas crudas fueron extraídas según el protocolo descrito. Usando un desapareado t-test, se determinó que tributirina aumenta la acetilación de las histonas en el extracto crudo (t(6) = 6.184, P = 0,0004); sin embargo, las impurezas son detectadas en el extracto (las bandas de las histonas no están claramente definidas). Así, H4K12ac anticuerpo no tiene una alta especificidad (figura 6). Para evaluar la aplicabilidad del protocolo presentado a pequeñas secciones de tejido, recogimos la corteza prefrontal de transgénica triples la enfermedad de Alzheimer (3 x Tg-AD) ratones trataron diariamente con 10 mg/kg M344, una clase I e inhibidor de HDAC IIb, para cuatro meses. Precipitación y purificación de las histonas se realizó según el protocolo descrito en este documento. Con el purificado de las histonas H3 y H4 fracción, determinamos que M344 aumenta 2.4-fold H4K12 acetilación (t(6) = 13.03, P < 0.0001), con una alta especificidad del anticuerpo H4K12ac (figura 7). Asimismo, se observó un aumento en la acetilación de las histonas H3 en BV2 células en respuesta a otro inhibidor de HDAC, es decir, el inhibidor selectivo de la HDAC3, R.G.F.P.-966. 10 μm de R.G.F.P.-966 causas un aumento de aproximadamente doble de acetilación en histona H3K27 después de 24 h de tratamiento. Estudiante de desapareado t-prueba se usó para comparar las células versus tratadas de control.
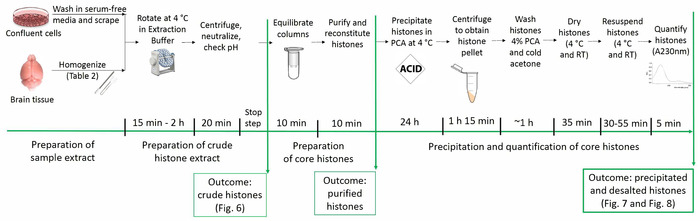
Figura 1: línea de tiempo del Protocolo de purificación de histona. Todos los pasos para el análisis de las histonas se muestran a continuación junto con el tiempo estimado necesario para cada paso. Figuras que representan el resultado de pasos determinados y presentado en el manuscrito figuran entre paréntesis. Haga clic aquí para ver una versión más grande de esta figura.
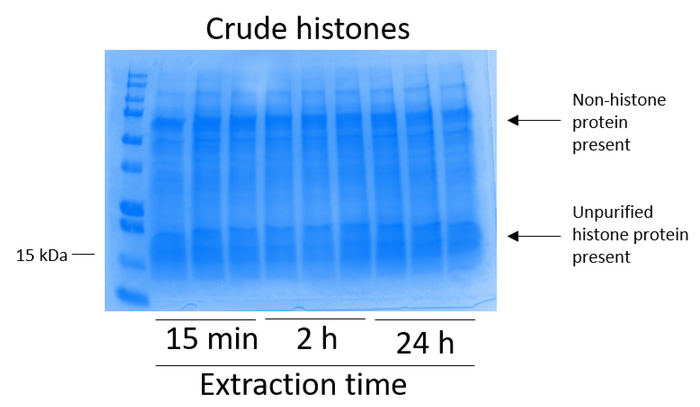
Figura 2: Representante gel teñido de azul brillante de Coomassie demostrando las histonas crudas extraídas de las células BV2. BV2 células fueron cultivadas durante 48 h antes de que comenzara el protocolo de extracción de las histonas. Las histonas crudas se extrajeron 15 min, 2 h y 24 h, con tres repeticiones para cada momento (esto ocurre también en la figura 3, figura 4y figura 5). Nonhistone e histona las proteínas están presentes en el extracto crudo de las histonas. Haga clic aquí para ver una versión más grande de esta figura.
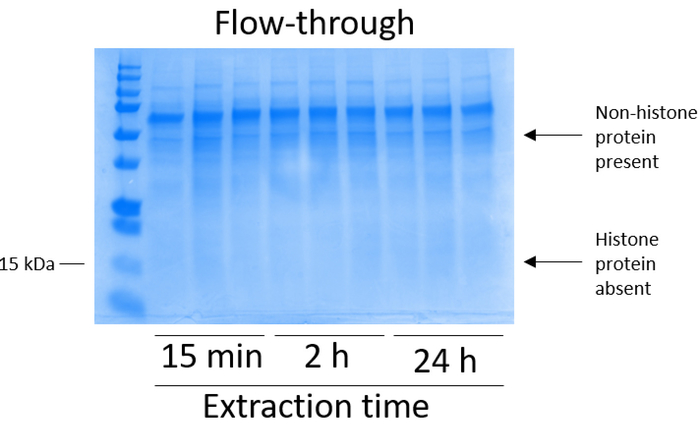
Figura 3: Representante gel teñido de azul brillante de Coomassie demostrando columna flujo siguientes histonas purificación pasos de células BV2. Después de histona crudo pasando por la columna de la Unión de las histonas, sólo nonhistone proteínas están presentes en el flujo a través. Las proteínas de las histonas están ausentes en esta fracción. Haga clic aquí para ver una versión más grande de esta figura.
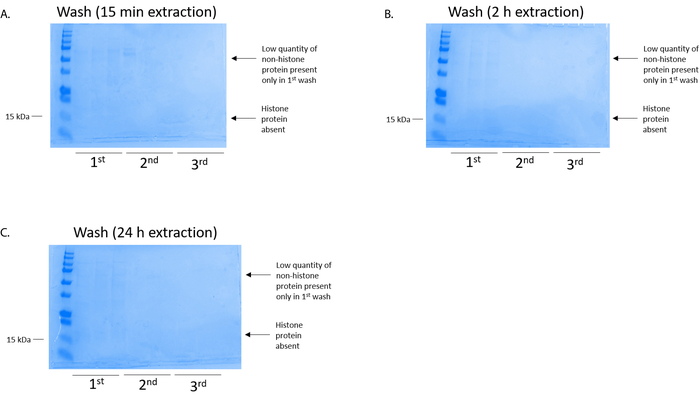
Figura 4: Representante gel teñido de azul brillante de Coomassie demostrando un lavado de columna tras un paso de purificación de la histona de las células BV2. Independientemente de los tiempos de extracción de las histonas, que fueron (A) 15 minutos, (B) 2 h, o (C) 24 h, bajas cantidades de proteínas nonhistone sólo estaban presentes en la columna de lavado de primera histonebinding. Proteínas histonas estuvieron ausentes en todos los lavados. Haga clic aquí para ver una versión más grande de esta figura.
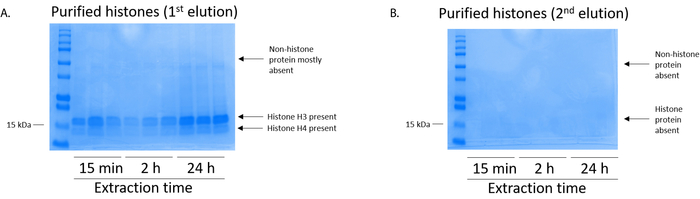
Figura 5: Representante gel teñido de azul brillante de Coomassie demostrando elutions después de un paso de purificación de la histona de las células BV2. (A) alta calidad purificada y desalado de las histonas H3 y H4 fueron detectados después de la primera elución de la columna de purificación de las histonas. Columna (B) la segunda elución de la purificación de la histona no dió una alta calidad o cantidad de las histonas H3 o H4. Haga clic aquí para ver una versión más grande de esta figura.
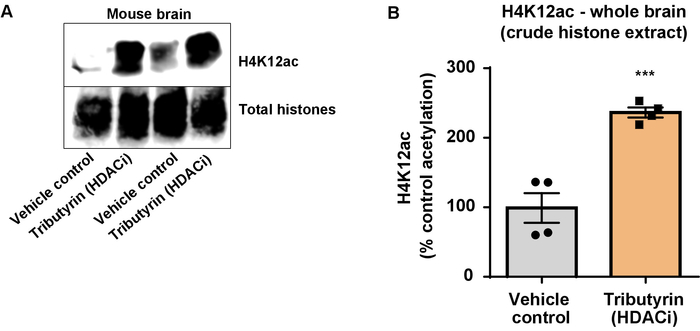
Figura 6: el actuar ampliamente HDAC inhibidor, tributirina, aumenta H4K12 la acetilación en todo el cerebro de los ratones de tipo salvaje. (A) este panel muestra un representante de western blot que representa un aumento de H4K12 la acetilación de la histona cruda extracto recogido de todo el cerebro de los ratones de tipo salvaje en respuesta a la HDAC ampliamente actuando el inhibidor, tributirina. (B) este panel muestra la cuantificación del incremento en H4K12 acetilación en vivo. Desapareado t-test se utilizó para comparar los grupos (t(6) = 6.076, P = 0.0005). Las barras representan la media ± el error estándar de la media (SEM). N = 8. P < 0.0001. Haga clic aquí para ver una versión más grande de esta figura.
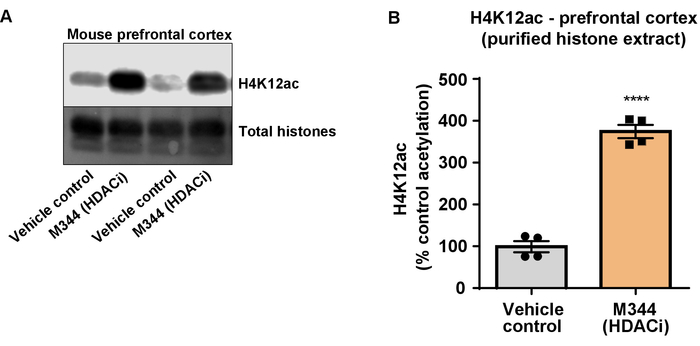
Figura 7: la clase I e inhibidor de HDAC IIb, M344, aumenta H4K12 la acetilación en la corteza prefrontal triple transgénica la enfermedad de Alzheimer (3 x Tg-AD) ratones. (A) este panel muestra un representante de western blot que representa un aumento de H4K12 de acetilación en el purificado e histona desalado extracto recogido de la corteza prefrontal de 3 x ratones Tg-anuncio en respuesta a la inhibición de la HDAC por M344. (B) este panel muestra la cuantificación del aumento de la acetilación de H4K12 en respuesta a M344 administrado en una dosis diaria de 10 mg/kg durante cuatro meses. Desapareado t-test se utilizó para comparar los grupos (t(6) = 13.30, P < 0.0001). Las barras representan la media ± SEM. N = 8. P < 0.00001. Haga clic aquí para ver una versión más grande de esta figura.
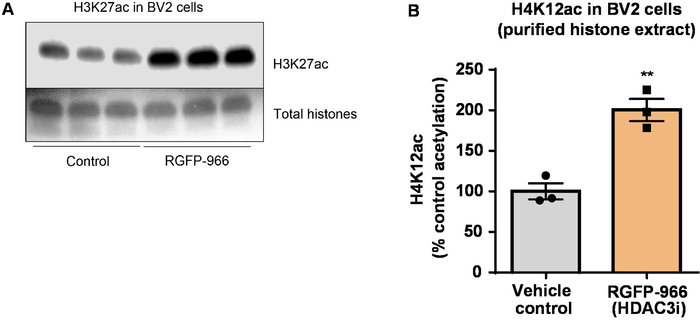
Figura 8: el inhibidor selectivo de la HDAC3, R.G.F.P.-966, aumenta H3K27 acetilación en las células microgliales BV2. (A) este panel muestra una mancha blanca /negra occidental representativa que representa un aumento de H3K27 acetilación en el extracto purificado y desalado histona recopilada de BV2 células en respuesta a la inhibición de la HDAC3 por R.G.F.P.-966. (B) R.G.F.P.-966 causa un aumento de aproximadamente doble de la acetilación de las histonas H3 y lisina (K) 27 después de 24 h de tratamiento. Desapareado t-prueba se usó para comparar las células versus tratadas de control (t(4) = 5.981, P = 0.002). Las barras representan la media ± SEM. N = 6. P < 0.01. Haga clic aquí para ver una versión más grande de esta figura.
| Tejido representativo (un hemisferio) * | Tejido medio peso (mg) | Tampón de extracción (mL) | Número de golpes |
| Cerebelo de ratón | 40 | 1 | 40 |
| Corteza frontal de ratón | 30 | 0.3 | 20 |
| Hipocampo de ratón | 27 | 0.3 | 18 |
| Corteza entorrinal de ratón | 19 | 0.3 | 17 |
| * Todos los experimentos fueron realizados en ratones macho adultos. | |||
| Edad media: 16 meses. Peso promedio: 30 gramos. | |||
Tabla 1: Condición optimizada para la homogeneización del tejido de cerebro.
Discusión
En el presente trabajo, hemos demostrado un método optimizado para purificar las proteínas de las histonas centrales y cuantificar las histonas H3 y H4 PTMs (por ejemplo, acetilación). El protocolo presentado es un flujo de trabajo integral que incorpora optimizado los procedimientos con respecto a las células y preparación de tejido de cerebro, elución purificación de histonas y la precipitación de histona detallada, crudo y cuantificación, que son seguidos por histona electroforesis y cuantificación de PTM de histona robusto. La gran cantidad de detalles proporcionados aquí permite una generación replicable de datos de alta calidad, a pesar de la necesidad de largas manipulaciones de las muestras de las histonas.
Muchos protocolos publicados actualmente requieren el uso de HPLC para aislar fracciones puras de las histonas H3 y H419. Aunque la HPLC es una técnica poderosa, su complejidad y bajo rendimiento disuaden a la mayoría de biólogos moleculares y nonexperts de su uso frecuente. De hecho, HPLC no está disponible en muchos laboratorios y personal altamente especializado es necesaria para operar el instrumento. HPLC es a menudo lentos, costosos y potencialmente peligrosos. Presentado aquí es una estrategia barata, de mediano rendimiento para lograr resultados de calidad similar que puentea HPLC. La estrategia divulgada también es más práctico y conveniente para el uso en casi cualquier laboratorio ya que utiliza un enfoque de columna de giro simple que no requiere de habilidades de operación instrumento especializado. Además, tetrámero de H3/H4 histona se extrae como sencillo, puro y abundante fracción, lo que permite una cuantificación fiable de PTMs conservados en cada una de las proteínas.
MPa es extremadamente sensibles a los cambios en el estrés oxidativo y cambios de pH20,21. Así, en contraste con métodos previamente publicados18, Divulgamos una estrategia eficiente de lavado las células en medios libres de suero para asegurar un mínimo disturbio metabólico de las células y para evitar la interferencia de la MPA nativa con componentes de suero. El actual protocolo no sólo evita el aislamiento de los núcleos tradicionales sino también ofrece tiempos óptimos para la lisis celular y el procedimiento de homogeneización de tejido exacto que permite la preservación de la envoltura nuclear, evitando la agregación nuclear. Aunque puede manipular el tiempo de extracción basado en el número de células, el tipo de célula utilizada, el tamaño del tejido, etc., lisis extendido no es deseable ya que podría conducir a la lisis de los núcleos y la liberación de ADN, haciendo la muestra difícil de manejar. Lo importante, múltiples puntos de comprobación en el protocolo existen para la validación de la purificación exitosa de la histona (p. ej., medidas 2.7 y 3.2.3). Esta estrategia también facilita la solución de problemas durante todo el procedimiento largo.
Otra característica importante y única del protocolo presentado es su compatibilidad total con herramientas de análisis de la mancha blanca /negra occidental río abajo y otros si así lo desean. Las proteínas de la histona se detectan en ~ 15 kDa13,22,23 y, semejantemente a otras proteínas de peso molecular pequeño, se ha demostrado difíciles detectar por técnicas immunoblotting estándar. El uso de un sistema de transferencia de alto rendimiento y alto rendimiento en combinación con geles de proteína óptima permite el mantenimiento de la proteína nativa confirmación (ausencia de SDS) y la actividad en ausencia de la SDS y la transferencia alta eficiencia de las proteínas de la histona de bajo peso molecular, asegurando así una cuantificación de PTM de histona confiable.
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Los autores expresan su agradecimiento al programa de investigación del Departamento de Florida de la salud Ed y Ethel Moore Alzheimer (becas 6AZ08 y 7AZ26), el NIH-NIAAA (grant 5R01AA023781-03) y la Asociación Americana del corazón (grant 17PRE33660831).
Materiales
| Name | Company | Catalog Number | Comments |
| 1.5 mL microcentrifuge tubes | ThermoFiser Scientific | 05-408-129 | or equivalent from other sources |
| Sterile water | Gibco | 15-230-204 | or equivalent from other sources |
| 70% perchloric acid | Sigma Aldrich | 311421 | or equivalent from other sources |
| 100% acetone | Sigma Aldrich | 270725 | or equivalent from other sources |
| pH-indicator strips, non-bleeding | Milliipore Sigma | 1095310001 | |
| 4x SDS sample buffer | BIO-RAD | 161-0747 | |
| Benchtop rotor | Cole-Parmer | UX-04397-34 | or equivalent from other sources |
| 1.5 mL tube rack | ThermoFiser Scientific | 05-541 | or equivalent from other sources |
| Histone purification mini kit | Active Motif | 40026 | spin columns included in the kit |
| Protease Inhibitor Cocktail | ThermoFiser Scientific | 78430 | or equivalent from other sources |
| Nanodrop instrument | ThermoFiser Scientific | ND-2000 | |
| Tissue culture dishes | VWR | 10062-880 | required for histone extraction from cultured cells |
| Tissue culute media | varies based on cell line used | varies based on cell line used | required for histone extraction from cultured cells |
| Low-serum media | ThermoFiser Scientific | 51985091 | required for histone extraction from cultured cells |
| Plastic cell scraper | Falcon | 353086 | required for histone extraction from cultured cells |
| SDS-PAGE gradient gel | BIO-RAD | 456-9035 | required for histone extraction from cultured cells |
| Coomassie Brilliant Blue R-250 Staining Solution | BIO-RAD | 1610436 | required for histone extraction from cultured cells |
| Coomassie Brilliant Blue R-250 Destaining Solution | BIO-RAD | 1610438 | required for histone extraction from cultured cells |
| Trans-Blot Turbo Mini PVDF Transfer Packs | BIO-RAD | 1704156 | required for histone extraction from cultured cells |
| Trans-Blot Turbo Transfer System | RIO-RAD | 1704150 | required for histone extraction from cultured cells |
| Ponceau S stain | CellSignalling | 59803S | required for histone extraction from cultured cells |
| Dounce homogenizer (size/cap sc 7mL) with a small size clearance | Kimble Chase | 885302-0007 | required for histone extraction from tissues |
| 100% bleach | Clorox | 68973 | required for histone extraction from tissues |
| H4K12ac antibody | Active Motif | 39166 | required for PTMs quantification via WB |
| H3K27ac antibody | Active Motif | 39134 | required for PTMs quantification via WB |
Referencias
- Holliday, R. Is there an Epigenetic Component in Long-term Memory?. Journal of Theoretical Biology. 200, 339-341 (1999).
- DeWoskin, V. A., Million, R. P. The epigenetics pipeline. Nature Reviews Drug Discovery. 12, 661-662 (2013).
- Eberharter, A., Becker, P. B. Histone acetylation: a switch between repressive and permissive chromatin. EMBO Reports. 3, 224-229 (2002).
- Grunstein, M. Histone acetylation in chromatin structure and transcription. Nature. 389, 349-352 (1997).
- Sartor, G. C., Powell, S. K., Brothers, S. P., Wahlestedt, C. Epigenetic Readers of Lysine Acetylation Regulate Cocaine-Induced Plasticity. The Journal of Neuroscience. 35, 15062-15072 (2015).
- Komatsu, N., et al. SAHA, a HDAC inhibitor, has profound anti-growth activity against non-small cell lung cancer cells. Oncology Reports. 15, 187-191 (2006).
- Bahari-Javan, S., Sananbenesi, F., Fischer, A. Histone-acetylation: a link between Alzheimer's disease and post-traumatic stress disorder. Frontiers in Neuroscience. 8, 160 (2014).
- Roh, T. -. Y., Cuddapah, S., Zhao, K. Active chromatin domains are defined by acetylation islands revealed by genome-wide mapping. Genes & Development. 19, 542-552 (2005).
- Mutskov, V., Felsenfeld, G. Silencing of transgene transcription precedes methylation of promoter DNA and histone H3 lysine 9. The EMBO Journal. 23, 138-149 (2004).
- Howe, L., Brown, C. E., Lechner, T., Workman, J. L. Histone acetyltransferase complexes and their link to transcription. Critical Reviews in Eukaryotic Gene Expression. 9, 231-243 (1999).
- Jenuwein, T., Allis, C. D. Translating the histone code. Science. 293, 1074-1080 (2001).
- Bowman, G. D., Poirier, M. G. Post-Translational Modifications of Histones That Influence Nucleosome Dynamics. Chemical Reviews. 115, 2274-2295 (2015).
- Volmar, C. -. H., Wahlestedt, C. Histone deacetylases (HDACs) and brain function. Neuroepigenetics. 1, 20-27 (2015).
- Plagg, B., Ehrlich, D., Kniewallner, K. M., Marksteiner, J., Humpel, C. Increased Acetylation of Histone H4 at Lysine 12 (H4K12) in Monocytes of Transgenic Alzheimer's Mice and in Human Patients. Current Alzheimer Research. 12, 752-760 (2015).
- Bhaskara, S., et al. Hdac3 is essential for the maintenance of chromatin structure and genome stability. Cancer Cell. 18, 436-447 (2010).
- Mottamal, M., Zheng, S., Huang, T. L., Wang, G. Histone Deacetylase Inhibitors in Clinical Studies as Templates for New Anticancer Agents. Molecules. 20, 3898-3941 (2015).
- Ramakrishnan, S., et al. HDAC 1 and 6 modulate cell invasion and migration in clear cell renal cell carcinoma. BMC Cancer. 16, 617 (2016).
- Wapenaar, H., Dekker, F. J. Histone acetyltransferases: challenges in targeting bi-substrate enzymes. Clinical Epigenetics. 8, 59 (2016).
- Klinker, H., Haas, C., Harrer, N., Becker, P. B., Mueller-Planitz, F. Rapid Purification of Recombinant Histones. PLoS ONE. 9, e104029 (2014).
- Chen, K., et al. Neurodegenerative Disease Proteinopathies Are Connected to Distinct Histone Post-translational Modification Landscapes. ACS Chemical Neuroscience. 9, 838-848 (2018).
- Simithy, J., Sidoli, S., Garcia, B. A. Integrating Proteomics and Targeted Metabolomics to Understand Global Changes in Histone Modifications. Proteomics. , (2018).
- Volmar, C. -. H., et al. An Epigenetic Approach for the Modulation of Amyloid Precursor Protein (APP) Processing and Improvement of Memory in Alzheimer's Disease. Neuropsychopharmacology: official publication of the American College of Neuropsychopharmacology. 40, S470 (2015).
- Volmar, C. -. H., et al. M344 promotes nonamyloidogenic amyloid precursor protein processing while normalizing Alzheimer’s disease genes and improving memory. Proceedings of the National Academy of Sciences. 114 (43), E9135-E9144 (2017).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados