Method Article
Identification des protéines d'interaction partenaires dans les cellules de mammifères à l'aide SILAC-immunoprécipitation quantitatives en protéomique
Dans cet article
Résumé
Expériences d'immunoprécipitation SILAC représentent un puissant moyen de découvrir de nouvelles interactions protéine: protéine. En permettant la quantification relative exacte de l'abondance de la protéine à la fois le contrôle et les échantillons de test, les interactions véritables peut être facilement distinguée de contaminants expérimentales, et les interactions de faible affinité préservée grâce à l'utilisation de conditions de tampon moins rigoureuses.
Résumé
Protéomique quantitative combinées avec purification immuno-affinité, SILAC immunoprécipitation, représentent un moyen puissant pour la découverte de nouvelles interactions protéine: protéine. En permettant la quantification relative exacte de l'abondance de la protéine à la fois le contrôle et les échantillons de test, les interactions véritables peuvent être aisément distinguées des contaminants expérimentales. Interactions de faible affinité peuvent être conservées grâce à l'utilisation de conditions de tampon moins rigoureuses et restent facilement identifiables. Ce protocole traite de l'étiquetage des cellules de culture de tissu avec des isotopes stables des acides aminés marqués, la transfection et l'immunoprécipitation d'une affinité marqué protéine d'intérêt, suivie de la préparation pour le dépôt d'une installation de spectrométrie de masse. Ce protocole traite ensuite comment analyser et interpréter les données renvoyées par le spectromètre de masse afin d'identifier les partenaires cellulaires interagissant avec une protéine d'intérêt. A titre d'exemple de cette technique est appliquée à identifier des protéines de liaison aux facteurs d'initiation de traduction eucaryotes: eIF4AI et eIF4AII.
Introduction
Une étape essentielle dans la compréhension de la fonction des protéines est l'identification de protéines interagissant pertinentes. Lorsque ces protéines sont inconnues, il ya un certain nombre de techniques disponibles, chacun avec leurs propres avantages et inconvénients. Il s'agit notamment du système de deux hybrides de levure, des essais déroulants utilisant la protéine recombinante, ainsi que la purification par affinité en tandem ou TAP-tagging 1, 2.
Une addition plus récente de ces techniques est la combinaison de la purification par affinité d'une protéine d'intérêt à partir d'une lignée cellulaire de mammifère approprié, suivie d'une spectrométrie de masse quantitative en utilisant un marquage isotopique stable d'acides aminés dans la culture cellulaire (SILAC) 3. Cela a des avantages sur la levure approche double-hybride en ce que la localisation cellulaire et les modifications post-traductionnelles sont pas perturbés, ainsi que des avantages plus traditionnelle TAP-tagging en ce qu'il s'agit d'une approche quantitative plutôt que qualitative permettant à l'utilisateur de readily distinguer non spécifiquement l'interaction des protéines et des contaminants, de facteurs de l'hôte qui se lient spécifiquement. En outre, comme un échantillon est généralement analysé ensemble, plutôt que de bandes de protéines individuels, des protéines d'intérêt ne sont pas masqués par la migration similaire des protéines sur un gel, pas plus qu'ils ne doivent généralement être présent à des concentrations suffisantes pour être visible après coloration, conduisant à augmentation du nombre de protéines identifiées confiance 4.
Pour illustrer cette technique, fusions GFP du facteur eucaryote d'initiation de traduction étroitement liée eIF4AI et eIF4AII qui part sur l'identité d'acides aminés de 90% ont été étudiés par la protéomique quantitative SILAC-immunoprécipitation. EIF4AI humain et II ont été clones dans pEGFP-C1 pour former une protéine de fusion où la GFP est fusionné à l'extrémité N-terminale de eIF4A. Pour éviter la nécessité de générer des lignées cellulaires stables transfection transitoire a été utilisé pour fournir ces constructions dans des cellules 293T en isotopes stables étiquetés.
Les cellules ont d'abord été marqué pendant deux semaines dans SILAC milieux de culture de cellules, suivie par la transfection d'ADN plasmidique codant pour une protéine d'intérêt. Les cellules ont ensuite été lysées, la concentration en protéines normalisées, et des quantités égales de lysat purifié par affinité sur agarose anti-GFP. Des quantités égales d'éluat sont ensuite combinés et soumis à une analyse LC-MS/MS. Les résultats de cette analyse sont ensuite traitées pour identifier les protéines de haute confiance: interactions de protéines (figure 1).
SILAC immunoprécipitation permet d'identifier non seulement les interactions directes, mais aussi faible affinité ou interactions indirectes avec des complexes de protéines 4. Grâce à ce système, eIF4AI et II immunoprécipitations permis l'identification reproductible et confiant du partenaire de liaison primaire eIF4G (isoformes I / II et III) 5, ainsi que les interactions indirectes avec eIF4E, et de nombreux composants du complexe eIF3.
Protocole
1. Production et repiquage des lignées cellulaires de SILAC marqué
Remarque: l'utilisation de la trypsine-EDTA doit être évité à tous les stades de passages et la préparation des échantillons expérimentaux pour l'analyse comme la trypsine peut contenir des acides aminés non étiquetés, ce qui conduirait à l'étiquetage incomplet des échantillons.
- Pour préparer une bouteille de milieux SILAC ajouter une aliquote d'une arginine convenablement SILAC marqué (84 mg / ml dans du PBS) et la lysine (146 mg / ml dans du PBS) pour une bouteille de Arg / Lys DMEM sans (contenant de 500 ml, 0,5 ml L-glutamine).
- Ensuite, ajouter 50 ml de FBS dialyse et 5 ml de pénicilline / streptomycine à la bouteille de 500 ml.
Note: Les cellules HEK 293T (ATCC) devraient être maintenus dans du milieu DMEM dépourvu arginine et la lysine et complété avec de la lumière (R0K0), moyen (R6K4) ou lourde (R10K8) acides aminés, de sérum fœtal bovin dialyse (10 kDa de coupure), et de la pénicilline / streptomycine. Les cellules doivent être maintenues dans les médias pour un minimum de 5 divisions cellulaires pour assurer complètel'étiquetage. Dans la plupart des cas, les cellules sont facilement étiquetés ≥ 2 semaines. - Pour diviser des cellules de passages, les cellules doivent être délogés de la monocouche en frappant le ballon. Les alternatives comprennent l'utilisation de racloirs ou de cellules en utilisant, un tampon de dissociation de cellules à base de PBS sans enzyme.
Remarque: Pour conserver les médias, les cellules doivent être repiquées dans des flacons T25 et le nombre de cellules plus grandes générées uniquement immédiatement avant l'expérience. - 24 heures avant la transfection de cellules, semences 3.5 x 10 6 cellules SILAC marqué dans un seul plat 10 cm 2 pour chaque condition expérimentale à l'étude.
2. Transfection de cellules marquées avec des constructions pEGFP-fusion
- Retirez le support de cellules et le remplacer par 9 ml de sans antibiotique SILAC DMEM (léger, moyen ou lourd) médias.
Remarque: Les antibiotiques ne doivent pas être ajoutées aux médias, car ils peuvent interférer avec l'efficacité de réactifs de transfection à base de liposomes. - Prepare un mélange de 10 pg du plasmide approprié (epEGFP-C1, pEGFP-eIF4A-I, pEGFP-eIF4A-II) dans 500 ul de sans antibiotique SILAC DMEM et le mélanger avec 500 ul de SILAC sans antibiotique du DMEM contenant 10 ul de réactif de transfection (par exemple, la lipofectamine 2000). Mélanger soigneusement la réaction par pipetage de haut en bas plusieurs fois.
- Faire incuber le mélange réactionnel à la température ambiante pendant 20 min, puis ajouter goutte à goutte à la monocouche cellulaire. Basculez la plaque doucement d'un côté à l'autre.
- Incuber les cellules transfectées à 37 ° C et 10% de CO2 pendant 24 heures.
Remarque: Si l'expression d'une protéine d'intérêt dans les résultats de toute toxicité apparente, alors il peut être nécessaire de réduire la quantité de plasmide transfecté et / ou la durée de la période d'expression subséquente.
3. Récolte Lysats de cellules
- Récupération des cellules de l'antenne dans le froid de la glace PBS en utilisant un grattoir cellulaire. Recueillir les cellules par centrifugation à 220 xg, 476; ° C pendant 5 min. Laver les cellules une autre 3x dans 10 ml de PBS glacé.
- Remettre en suspension le culot cellulaire dans 200 pi de tampon de lyse cellulaire (10 mM de TrisCl / pH 7,5, NaCl 150 mM, EDTA 0,5 mM, 0,5% de NP40) contenant fraîchement ajoutée cocktail d'inhibiteurs de protease III à une concentration de 1 x et RNase cocktail (facultatif) à 5 pi par ml.
Remarque: Pour les protéines avec de l'acide nucléique connue l'activité de liaison, il peut être nécessaire d'ajouter au lysat des nucléases avant la précipitation. Dans les cas où la nucléase est ajouté, les échantillons doivent être incubées sur de la glace pendant 30 minutes sur la glace, avec pipetage toutes les 10 min. L'extraction de l'acide nucléique total provenant d'une petite fraction de l'échantillon et l'analyse par électrophorèse sur gel d'agarose peut tester l'efficacité de la nucléase. - Centrifuger les échantillons à 13 000 xg, 4 ° C pendant 10 min conserver le surnageant comme le lysat cellulaire soluble.
- La concentration du lysat cellulaire doit être évaluée par dosage BCA selon les instructions du fabricant.
- Utiliser un tampon de lyse contenant un cocktail inhibiteur de protease III de normaliser la concentration de protéines dans un volume final de 500 ul.
- Ajuster le volume à 1 ml avec de l'addition de 500 ul de tampon de dilution (10 mM de TrisCl / pH 7,5, NaCl 150 mM, EDTA 0,5 mM) contenant un cocktail inhibiteur de protease III à une concentration finale de 1 x. Une aliquote de 50 ul de l'échantillon doit être conservé comme entrée de l'échantillon et du lysat conservé sur de la glace tout en préparant des perles anti-GFP (par exemple, GFP-trap).
Remarque: En règle générale les rendements varient entre 1-3,5 mg de protéine dans la finale 1 ml d'échantillon. Tandis que les tampons ci-dessus conviennent pour de nombreuses protéines d'intérêt, pour d'autres, il peut être nécessaire de modifier les composants du tampon afin d'assurer la protéine appât est solubilisé et à maintenir les interactions protéine-protéine. Modifications possibles comprennent l'agent tampon (phosphate, l'HEPES), la concentration de sel (150-500 mM), le choix d'un détergent, ou d'autres additifs.
4. Reliure à Anti-GPerles de PF
- Vortex brièvement la suspension de billes pour remettre en suspension les perles. En utilisant une pointe de pipette 200 pi de l'extrémité coupée, transférer 25 ul de billes par échantillon dans un nouveau tube.
Remarque: L'utilisateur doit préparer les perles pour une expérience de SILAC seul comme un mélange maître à minimiser la variation échantillon à échantillon. - Pour chaque 25 pi de billes en suspension, ajouter 20 volumes (1 500 pi par 75 pi) suspension de tampon de dilution, et centrifuger les perles à 2700 g pendant 5 min. Ensuite, laver les billes une nouvelle 2x dans 20 volumes de tampon de dilution.
- Ajouter 100 pi de tampon de dilution par 25 pi perle suspension. L'utilisation d'un embout de 200 ul avec l'extrémité coupée, transférer 85 pi de cette suspension remises en suspension à chacun des échantillons de SILAC marqué de l'étape 3.6.
- Incuber les échantillons avec des perles sur un rotateur à 4 ° C pendant 2 heures.
5. Laver, élution, et préparation des échantillons pour l'analyse MS
- Centrifuger les échantillons à 2700 xg, 46; C pendant 5 min. 50 pi du surnageant doivent être conservés que l'échantillon non lié, avec le reste du surnageant mis au rebut.
- 1 ml de tampon de dilution doit être ajouté à chaque tube pour remettre en suspension les billes et l'échantillon a été centrifugé à 2700 x g, 4 ° C pendant 5 min. Le surnageant doit être jetée. Cela devrait être effectué deux fois.
- Éluer des protéines à partir des billes par addition de 50 ul de tampon de charge SDS 2x, et en chauffant à 95 ° C pendant 10 min. Sédimenter les billes par centrifugation à 2700 g pendant 2 min à 4 ° C
- Conserver le surnageant dans des tubes prélubrifiés, où il peut être ensuite stocké à -80 ° C jusqu'à utilisation. Pour la soumission à une installation de spectrométrie de masse, mélanger les échantillons étiquetés 01:01:01 (par exemple, 10 pi de chaque) et soumettre l'échantillon mixte.
Remarque: À ce stade, les échantillons peuvent être testés par western blot, coloration à l'argent ou d'autres moyens pour tester l'interaction avec les partenaires de liaison connus / inconnus. Un exemple est donné sur la figureure 2, montrant la liaison spécifique d'un partenaire d'interaction connue - eIF4G par Western blot, et l'apparition de bandes de coloration d'argent présents dans des échantillons de pulldown une protéine d'intérêt, mais pas d'un échantillon témoin. - Soumettre l'échantillon pour analyse LC-MS/MS.
Remarque: une fois convaincu que la protéine marquée d'intérêt est avec succès des partenaires d'interaction, des volumes égaux de chaque échantillon étiqueté (léger, moyen et lourd) sont combinés et soumis à l'analyse LC-MS/MS obligatoire. Il est d'usage de présenter 30 pi total d'un échantillon IP pour l'analyse. Cela impliquerait mélangeant 10 ul d'échantillon Lumière marqué avec 10 pi d'échantillons lourds marqué moyennes marqué et 10 pi pour donner un total de 30 pi.
6 Analyse des données I:. Comprendre les résultats, et l'élimination des identifications faible confiance
Remarque: La liste des têtes de colonnes retournés par le logiciel du protéome Discoverer est donnée dans le tableau 1 Dif.logiciel de rentes (par exemple, MSQuant, MaxQuant) sera de retour différentes rubriques, cependant, seul un sous-ensemble de ceux-ci sont nécessaires pour l'analyse et ceux-ci sont communes aux différents logiciels. Les données doivent toujours inclure un numéro d'adhésion pour chaque protéine identifiée, le rapport de la comparaison de chaque rapport d'échantillonnage (lumière vs moyen, léger vs lourdes, moyennes vs lourde etc), le nombre de peptides uniques identifiés, et une certaine forme de taux de faux positifs ou d'une indication de confiance.
- Avant de passer aux données, d'abord copier les données brutes à une nouvelle feuille de calcul. De cette feuille de calcul supprimer toutes les colonnes sauf celles donnant le numéro d'accès, le nombre de peptides uniques, les ratios comparant des échantillons, le rapport de la variabilité, et la description de la protéine. Si réplique expériences ont été réalisées, elles doivent être combinés en un seul fichier Excel, avec l'expérience apparaissant sur un onglet séparé.
Remarque: Faible données de confiance comprend des protéines identifiées par seulement un seul peptide unique, et celles wici quantification n'était pas possible. - Utilisez 'sort' la fonction de Excelle pour trier les données par le nombre de peptides et supprimer les entrées pour des protéines qui n'ont pas plus d'un peptide. Puis trier par rapport et éliminer les protéines qui n'ont pas de rapports SILAC (protéines non quantifiés).
- Autre ratios de SILAC à un journal deux valeurs en utilisant la formule: '= log (rapport de SILAC, 2) », où« Ratio de SILAC »est remplacé par l'identifiant de cellule.
Remarque: en tant que rapport de SILAC élément de toutes les données pour des protéines qui montrent une diminution de l'abondance étant limité à des valeurs entre 0 et 1, il est habituel pour convertir un rapport de SILAC à un rapport log 2 de SILAC, car cela signifie que les protéines à la fois augmenté ou diminué en un échantillon est représenté sur une échelle logarithmique où 2 ou -2 représente une augmentation de 4 fois ou diminution de l'abondance, et 3 ou -3 une augmentation de 9 fois ou diminution de l'abondance respectivement. Suite à cette transformation, les données doivent s'adapter à une Garépartition USSIE centrée autour d'une rapport de 0 à SILAC log 2. Un exemple de ceci est donné dans la figure 3. - Créer de nouvelles colonnes dans le fichier Excel et calculer connecter deux ratios de SILAC pour tous les échantillons / colonnes simulées. Pour la conversion d'un rapport maquette / échantillon à un rapport échantillon / maquette, utiliser la formule: "= 1/ratio"
7 Analyse des données II:. Sélection Interactions élevés de confiance pour une étude plus approfondie
- Ouvrir Graphpad Prism, sélectionnez Nouveau> Tableau de données et graphique ... 'colonne' Sélectionnez dans la liste sur le côté gauche de la fenêtre, et sélectionner les données Entrée / Importer> Entrez les valeurs de répliques, empilés en colonnes options. Appuyez sur «Créer».
- Sélectionnez et copiez un échantillon / colonne de rapport Mock SILAC log 2 donnée de la feuille de calcul Excel dans le nouveau fichier Prism.
- Cliquez sur le menu déroulant le "Insérer" et sélectionnez "Nouveau analyse. Sous analyse de sélection de colonne "La distribution de fréquence. Garder les options par défaut cliquez sur 'OK'.
Remarque: Cette étape génère un histogramme illustrant le nombre de protéines identifiées dans un rapport donné. Cela devrait former une distribution gaussienne. - Dans le dossier "Résultats d'une nouvelle section« Histogramme »aura été généré. Sélectionnez la section de distribution de fréquences.
- Cliquez sur le menu déroulant le "Insérer" et sélectionnez Nouveau analyse> XY> non linéaire régression (ajustement de la courbe). Cliquez sur «distribution gaussienne» et cliquez sur OK.
Remarque: Cette étape correspond à une courbe aux données de distribution de fréquences générées à l'étape 7.3, ce qui donne des valeurs qui peuvent ensuite être utilisées pour calculer les seuils de signification. - Dans la fenêtre de résultat qui apparaît, la moyenne et l'écart type sont donnés. Générer un seuil en ajoutant 1,96 écarts-types de la moyenne.
Remarque: Les valeurs représentent la moyenne et les écarts-types de la gaussienne distribution, pas l'ensemble de données totale. 1,96 écarts-types mettraient un seuil à la limite de confiance de 95% (p ≤ 0,05). 2,58 SD donnerait 99%, et de 3,3 écart-type de 99,9%. Le seuil doit être déterminée individuellement pour chaque expérience de réplique car il peut varier.
8 Analyse des données III:. Fusion de datasets Replica
Remarque: Pour être confiant dans l'identification de partenaires d'interaction d'une expérience déroulant SILAC typique devrait idéalement être effectué trois fois, avec le milieu et les échantillons étiquetés lourds commuté pour l'une des répétitions pour contrôler tout effet des médias sur les résultats. Une protéine qui se présente comme l'interaction d'au moins deux des trois expériences, avec le «échantillon switched'-médias représentant idéalement un d'eux, est une interaction de confiance élevé.
- Revenir au fichier Excel, créer un nouvel onglet appelé «combinée». colonne Label A 'adhésion »et tous les numéros d'accès de chaque copie of les expériences individuelles dans cette colonne unique.
- Sélectionnez l'onglet «Données», puis l'option "supprimer les doublons".
- Créer des colonnes pour les rapports de SILAC, et le rapport de la variabilité de l'essai, ainsi que pour la colonne nom / description de protéine.
- Dans l'onglet Description, utiliser la formule de vlookup pour recueillir la description de chaque numéro d'accession. Faites glisser la formule dans la colonne à remplir dans la description de la protéine. La formule de vlookup est: "= vlookup (AccessionNo, WheretoLook, ColumnsAccross, False)", où: AccessionNo est $ aX x étant le numéro de ligne WheretoLook est l'onglet "Experiment Name '$ 2 $:.! $ Y $ Z où Y et Z sont la pièce en bas à droite de données sur la feuille de calcul référencé. ColumnsAccross est le nombre de colonnes en face de la num d'adhésionbre dans la colonne A une valeur de consigne se trouve.
Remarque: Par exemple, si le numéro d'accès est dans la colonne A, et les données d'intérêt se trouve dans la colonne E. La valeur ici serait 5 (colonne A compte pour 1). Comme le nombre d'adhésion ont été rassemblées à l'étape b, il est fort probable que vlookup ne sera pas obtenir tous les noms nécessaires à partir d'une expérience. Lorsqu'il retourne N / A, modifier la formule pour obtenir la description de chaque expérience à son tour jusqu'à ce que toutes les descriptions sont acquis. - Pour mettre en évidence l'interaction des protéines dans le jeu de données combinées, sélectionnez chaque colonne de rapport individuel et cliquez sur l'onglet Accueil, suivie par la mise en forme conditionnelle> Faits saillants cellules règles> Plus règles.
- Sélectionnez le style «classique». Format seules les cellules qui contiennent des «Valeur de la cellule», «supérieur ou égal à». Dans la zone, le type de la valeur de l'écart-type de 1,96, et cliquez sur 'OK'.
- Évaluer la variabilité de rapport pour chaque interaction positive. Si soustrayant le% vara responsabilité serait tomber un "hit" en dessous de la valeur de seuil, ce doit être traitée avec prudence.
Note: Ceci représente la façon cohérente les rapports individuels pour chaque peptide qui composent le ratio de SILAC de protéines sont un, et est exprimée en pourcentage. Lorsque le rapport de la variabilité est prise en compte et une protéine donne un rapport en SILAC-dessus du seuil, cette protéine représente un succès. Si le rapport variabilité donne une gamme qui est inférieur au seuil, le «hit» peut représenter un contaminant. - Répétez cette opération pour chacune des colonnes de résultats et à comparer entre les expériences. Protéines en surbrillance identifiés dans deux ou plusieurs expériences représentent une interaction de confiance élevé.
Remarque: Selon la base de données utilisée pour affecter des numéros d'adhésion de protéines, de différentes expériences une protéine peut avoir été identifié sous un autre, ou même plusieurs numéros d'adhésion. Il est important de vérifier afin de s'assurer que les protéines ne sont pas accidentellement omis.
Résultats
Dans une expérience SILAC déroulant typique, la grande majorité des protéines identifiées (> 90%) représentent des contaminants ainsi que des protéines de liaison non spécifique à la matrice d'affinité, ce qui est illustré sur la figure 2B, même si les protocoles de lavage de supprimer la majorité des contaminants cytoplasmiques tels que GAPDH (Figure 2A). Toutefois, la concentration des protéines de liaison non-spécifique en une distribution normale permet protéines qui se lient spécifiquement à une protéine d'intérêt doit être distinguée en tant que ceux-ci ont des ratios plus élevés échantillon / fictifs que l'arrière-plan. Alors que les contaminants devraient théoriquement se regrouper autour d'un rapport de 0 SILAC log 2, ce n'est pas nécessairement le cas, un exemple en est donné dans la figure 3. Raisons possibles pour cela inclure imparfait étiquetage SILAC de cellules, chargement volumes inégaux ou concentrations de lysat sur les perles anti-GFP, la perte accidentelle de perles pendant la purification ou inégal mélangetion d'échantillons à la fin de la procédure de purification 3. Toutefois, les données sont analysées en supposant fondée sur une norme seuil écart par rapport à la moyenne des contaminants normalement distribuées, des changements mineurs dans le centrage des données ne devraient pas affecter la qualité des résultats.
Lorsque l'on compare les différences dans les interactions protéiques entre les deux protéines apparentées, une situation similaire peut se produire où une protéine d'intérêt est produite à des niveaux plus élevés dans les cellules d'une seconde (soit en raison de la variation de l'efficacité de transfection, ou une propriété intrinsèque de la protéine ou de l'ARNm) . Une certaine variation dans l'expression (par exemple, figure 2A) peuvent être corrigées par l'analyse de la proportion de SILAC pour ces deux échantillons. Dans cet exemple, ce serait les échantillons GFP-eIF4AI et GFP-eIF4AII. En analysant le rapport 4AI/4AII SILAC comme indiqué à l'article 7, il est possible d'identifier les protéines dont la liaison varie considérablement entre les isoformes.
Sur la figure 4, une représentation des protéines de liaison à eIF4A identifiées dans l'une des répliques d'expériences réalisées est montré, illustrant la couverture du complexe du facteur d'initiation de ce protocole atteint. Les taux les plus élevés ont été généralement observées avec eIF4G, qui se lie directement à eIF4A, avec des ratios plus faibles pour eIF4E, qui se lie à eIF4G à un site en dehors du site de eIF4A contraignant. Ratios plus faibles ont été observés pour les membres du complexe eIF3. Cependant, cela illustre clairement que l'expérience satisfaisante identifié des partenaires de liaison à la fois directs et indirects de eIF4AI et II. Comme on pouvait s'y attendre de leur identité de séquence élevée 6, interactions protéine: protéine semblaient largement conservée entre les deux isoformes dans ce système expérimental 7, 8. Une sélection de certaines des protéines qui interagissent sont donnés dans le tableau 2, illustrant le format des données.| Titre de la colonne | Description |
| Accession | Affiche le numéro d'accès pour la séquence |
| Couverture | Proportion de la séquence de la protéine couverte par les peptides identifiés |
| ♯ PSM | Peptide correspondance spectrale |
| ♯ peptides | Nombre total de peptides uniques identifiés pour une protéine |
| ♯ AA | La longueur d'une protéine dans les acides aminés |
| MW (Da) | Le poids moléculaire d'une protéine dans Daltons. Exclut les modifications |
| calc. PI | Le point isoélectrique théorique d'une protéine |
| Score | Le score total d'une protéine (qui représente la somme de la indivscores peptidiques idual). Le score exact requis pour la signification varie selon les expériences. Une installation MS applique généralement un seuil de taux de fausse découverte de 5%. |
| Séquence | La séquence des acides aminés constituant la protéine |
| Rapport | L'intensité relative des peptides dans un échantillon marqué nommé, par rapport à un deuxième échantillon étiqueté |
| Ratio comte | Le nombre de rapports de peptides qui ont été utilisés pour calculer le ratio de protéine donnée |
| Ratio variabilité (%) | La variabilité des taux de peptides individuels utilisés pour calculer un rapport de la protéine donnée |
| Description | Le nom de la protéine |
Tableau 1. Des rubriques standard d'un rapport du protéome Discoverer de colonne.Alors que des informations utiles peuvent être tirés de l'ensemble de ces colonnes, ceux qui critiquent pour cette analyse sont présentés en caractères gras.
| Accession | Peptides | 4AI/Mock | 4AII/Mock | Nom | analyse de SILAC |
| A8K7F6 | 21 | 100 | 1 | eIF4AI | Protéine «d'appât» |
| Q14240 | 22 | 0,01 | 90,855 | eIF4AII | |
| G5E9S1 | 25 | 47,575 | 30.53 | eIF4GI | Protéines interagissant |
| Q59GJ0 | 5 | 11.778 | 10,619 | eIF4GII60; | |
| P06730 | 3 | 7.22 | 7.57 | eIF4E | |
| Q5T6W5 | 4 | 0,685 | 0,646 | hnRNPK | Contaminants non-liant spécifiquement |
| P62805 | 1 | 0,531 | 0,498 | Histone H4 | |
| H6VRG2 | 18 | - | - | Kératine-1 | Contaminants de l'environnement |
| P35527 | 11 | 0,01 | 0,01 | Kératine 1 cytosquelette 9 |
Tableau 2. Données typiques d'une expérience SILAC d'immunoprécipitation. Donner des exemples de données pour une protéine d'intérêt / appât (haute peptides, ratio élevé), protéines interagissant avec une protéine d'intérêt (hautes et basses peptides /, ratio élevé), la liaison non spécifique protéines (haut-bas pept /ides, le ratio tombe en dessous de seuil - dans cette expérience 0.96), et les contaminants environnementaux (souvent des peptides élevés, le ratio négatif / en dessous du seuil).

Figure 1. Plan expérimental. Tout d'abord les cellules sont cultivées dans un milieu dépourvu d'arginine et de lysine et substitués par isotope stable marqué arginine et la lysine pendant 2 semaines (1). (2) Les cellules sont ensemencées dans 10 cm 2 plats et transitoirement transfectées avec des plasmides codant la GFP (Mock) ou des protéines de fusion GFP (échantillons). (3) Les cellules sont lysées et les protéines de fusion GFP ou GFP sont immunoprécipitées à partir de lysats cellulaires. (4) Les échantillons sont combinés dans un rapport de 1:1 et soumis à une analyse LC-MS/MS. Les données sont ensuite analysées pour enlever faible ident de la protéine de confiancefications et pour sélectionner un niveau d'enrichissement de protéine correspondant à des protéines interagissant authentiques.
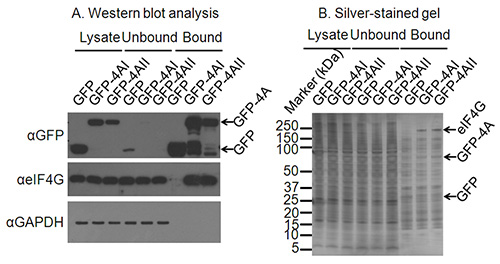
Figure 2. Confirmation conditions d'immunoprécipitation appropriés. A) Analyse par transfert de Western des lysats cellulaires, ainsi que les fractions non liées et liées de l'immuno-précipitation et immuno-précipitation confirme l'expression de la protéine d'intérêt. Un Western blot contre GAPDH confirme épuisement des protéines non-interaction et un transfert de Western en outre un partenaire d'interaction connue du eIF4A confirme le succès de l'immunoprécipitation des protéines de liaison à la protéine d'intérêt. B) Comparaison partenaires d'interaction d'une protéine d'intérêt ne sont pas connus, un gel coloré à l'argent peut confirmer l'immunoprécipitation des protéines interagissantes. Sur cette argent-tache bandes de gel ed pour GFP et GFP-eIF4AI/II sont claires, et une bande migrant à la taille correcte pour eIF4G est présent seulement dans les voies GFP-4AI/II-bound et pas dans la voie de contrôle de la GFP.

Figure 3. Des résultats représentatifs. Histogramme montrant la répartition des taux de protéines d'une répétition de (A) GFP-eIF4AI ou (B) GFP-eIF4AII déroulant. La coupure de 1,96 écart-type est marqué par une ligne pointillée. Protéines interagissant relevant pas de contaminants normalement distribués sont évidents de ~ 0,25 et 1 (A), et ~ 0.3-1.5 en (B).
les/ftp_upload/51656/51656fig4.jpg "/>
Figure 4. Identification des membres complexes eIF partir d'une seule réplique d'une expérience SILAC IP. Protéines en vert étaient la protéine d'intérêt utilisé pour le menu déroulant Interaction protéines sont ombrées de rouge à blanc selon la log 2 ratio de SILAC dans l'IP SILAC rouge étant la protéine la plus abondante dans l'analyse, et le blanc étant le seuil d'écart-type de 1,96. Protéines en gris n'ont pas été identifiés dans cette analyse.
Discussion
La stratégie déroulant SILAC décrit ici représente un moyen très sensibles et puissants de détection de nouvelle protéine: interactions entre protéines, et permet en outre la discrimination simple et rapide des modes de liaison entre les échantillons altérés étroitement liés d'intérêt. Dans cet exemple, cette technique a été utilisée pour étudier les interactions protéine: protéine des protéines eIF4AII eIF4AI et 6. À la connaissance de l'auteur, cette étude est la première dans la littérature exploiter l'utilitaire de protéomique de SILAC pour enquêter sur la interactome cellulaire de ces deux isoformes de eIF4A.
L'approche décrite ci-dessus utilise un GFP-tag et anti-GFP perles 9, 10 et donc des modifications peuvent être nécessaires pour permettre à cette approche doit être utilisé pour une protéine d'intérêt spécifique, par exemple si la balise est placée à l'extrémité N-ou C-terminale d'une protéine. Le cas échéant, des transferts Western possibles ou des tests fonctionnels devraientêtre effectuée pour détecter la liaison d'une protéine partenaire d'interaction connue. Si une protéine pas tolérer fusion avec une étiquette de la GFP, autre marquage ou stratégies déroulants ont été appliquées à pulldowns SILAC utilisant les deux autres balises (FLAG 11, biotine 12, STREP (données propres, non publié)), ou en utilisant des anticorps primaires contre une protéine d'où l'intérêt siRNA knockdown de la protéine cible fournit un échantillon de contrôle 13. Ces expériences ont été décrites ailleurs dans la littérature, mais en bref, l'étape 1 et les étapes 5.4-8 seraient appliquées comme ci-dessus, avec des étapes de 2 à 5,3 modifiés comme approprié pour le système d'expression / déroulant de choix en utilisant les entrées de protéines égalité comme décrit dans étapes 02.04 à 02.05. Comme les étapes de quantification permettent de protéines de liaison non spécifiques à être enlevés au niveau de l'analyse, il est recommandé d'omettre la pré-incubation avec des perles de contrôle, ou des lavages en sel élevées, afin de préserver la protéine de faible affinité: interactions de protéines avec une protéine d'intérêt . A ma nucléasey être inclus ou omis de ce protocole en fonction des spécificités d'une expérience particulière. Par exemple: que les protéines utilisées dans cette méthode sont hélicases d'ARN, RNase cocktail a été inclus dans le protocole pour éliminer les interactions indirectes médiées par l'ARN (étape 3.2). Dans certains cas toutefois, il pourrait être avantageux d'exécuter des expériences parallèles avec et sans nucléase pour identifier les interactions dépendantes d'acide nucléique.
Dans ce protocole, la commutation de «moyen» et échantillons «lourds» dans les expériences répétées est recommandé de contrôler les variations introduites par des différences dans les médias de SILAC ou la croissance des cellules. Un contrôle alternative implique la commutation séquentielle des trois (, 'moyen' «lumière», et «lourd») médias dans des répliques expériences. Tandis que cette approche est potentiellement plus strictes, il n'augmente la complexité de l'analyse, comme dans au moins une répétition, une protéine d'intérêt wmal être produite dans des cellules «légères» étiquetés et il est donc nécessaire de faire la distinction entre les protéines systématiquement identifiées dans les échantillons «légers» (contaminants environnementaux tels que les kératines), et ceux qui ne sont enrichies dans les échantillons «légers» quand il est lié à une protéine de intérêt.
Alors que l'utilisation des données de quantification permet de discrimination spécifique des interactions non-spécifiques grâce à l'utilisation d'un seuil, inévitablement des interactions authentiques peut être jeté. L'approche ci-dessus est une approche simple et rapide pour l'identification des interactions protéine: protéine qui peut être facilement tenté par des chercheurs qui n'ont aucune expérience précédente avec la spectrométrie de masse, ou l'analyse de grande protéine: protéine ensembles de données d'interaction. Pour la plupart des utilisations ce qui est plus que suffisant pour identifier de nouvelles protéines d'intérêt. D'autres modifications à cette approche pour aider à réduire cette perte de données sont décrits ailleurs dans la littérature et comprennent l'utilisation d'un prbibliothèque de fréquence où otein protéines contaminantes connu pour un ensemble spécifique de paramètres expérimentaux (lignée de cellules, la matrice de billes, des conditions de tampon) peut être exclu 10, 14. Toutefois, en fonction des paramètres expérimentaux particuliers, il peut être nécessaire d'exécuter un certain nombre d'expériences de contrôle pour générer un protéome de talon, ce qui peut donc augmenter à la fois le coût et la complexité de l'expérience. De plus amples informations sur cette technique est disponible sur le site de www.peptracker.co.uk 14.
Il convient également de noter que le protocole décrit ci-dessus consiste à mélanger des échantillons différemment marqués à la fin du processus d'immunoprécipitation (appelé un mélange Après purification - expérience de SILAC MAP). Ceci est fait comme interactions protéine: protéine se produisent à un équilibre donné 15. Il convient de noter que d'autres groupes ont combiné cette approche MAP SILAC décrite dans ce protocole avec incubation des échantillonsavant pulldown (Purification Après Mélange - SILAC PAM) pour différentes longueurs de temps (20 min à 2 h ont été utilisés dans la littérature) 15, 16. Sur la base de la rapidité avec laquelle un taux de protéine gouttes vers 01h01, il est possible d'étudier qualitativement et affinités de liaison pour définir des protéines comme les protéines qui interagissent stables ou dynamiques 15.
En résumé, pulldowns SILAC représentent un moyen très puissant pour identifier les protéines qui interagissent avec une protéine d'intérêt donné, dans un cadre physiologiquement pertinents. La technique peut être très facilement adapté à un certain nombre de stratégies de purification, ce qui permet son application à une protéine d'intérêt donné. La quantification des résultats simplifie grandement l'identification des interactions authentiques, et permet la détente de strictes conditions de tampon utilisés pour éliminer les liants non-spécifiques, et préserve ainsi les interactions de faible affinité. Comme jusqu'à trois échantillons peuvent être comparés en ce qui précèdestratégie, la technique a des atouts à comparer les différences claires dans la protéine de liaison entre les différentes isoformes de protéines, les protéines mutantes, ou l'effet des inhibiteurs pharmacologiques. Comme tranches de gel entiers sont analysés plutôt que des bandes individuelles que tache par Coomassie, le nombre de protéines identifiées au niveau de confiance élevé sont généralement plus élevés que ceux identifiés dans un TPS / TAP-déroulant standard, et expérimentateur biais dans la sélection des protéines d'intérêt est retiré. La technique compare donc très favorablement à d'autres techniques couramment utilisés dans l'identification de nouvelles protéines-interactions (levure 2-hybrides, la TPS / Son ou TAP Pulldowns).
Déclarations de divulgation
Les auteurs déclarent qu'ils n'ont aucun intérêt financier concurrents.
Remerciements
Ce travail a été soutenu par des subventions du Wellcome Trust et le BBSRC à IG. IG est un Wellcome Senior Fellow.
matériels
| Name | Company | Catalog Number | Comments |
| Dulbecco's Modified Eagle Medium (DMEM) | Dundee Cell Products | LM010 | DMEM lacking Arginine and Lysine. (and containing L-glutamine) |
| Dialysed FBS (10 kDa cutoff) 500 ml | Dundee Cell Products | DS1003 | |
| Arginine (R0) 25 g | Sigma-Aldrich | A8094 | Resuspend 0.5 g in 6 ml PBS, filter sterilize, and freeze in 0.5 ml aliquots (gives a 84 mg/ml stock) |
| Arginine (R6) 0.5 g | Cambridge Isotope Labs | CLM-2265 | Resuspend 0.5 g in 6 ml PBS, filter sterilize, and freeze in 0.5 ml aliquots (gives a 84 mg/ml stock) |
| Arginine (R10) 0.5 g | Cambridge Isotope Labs | CNLM-539 | Resuspend 0.5 g in 6 ml PBS, filter sterilize, and freeze in 0.5 ml aliquots (gives a 84 mg/ml stock) |
| Lysine (K0) 25 g | Sigma-Aldrich | L8662 | Resuspend 0.5 g in 3.5 ml PBS, filter sterilize, and freeze in 0.5 ml aliquots (gives a 146 mg/ml stock) |
| Lysine (K4) 0.5 g | Cambridge Isotope Labs | DLM-2640 | Resuspend 0.5 g in 3.5 ml PBS, filter sterilize, and freeze in 0.5 ml aliquots (gives a 146 mg/ml stock) |
| Lysine (K8) 0.5 g | Cambridge Isotope Labs | CNLM-291 | Resuspend 0.5 g in 3.5 ml PBS, filter sterilize, and freeze in 0.5 ml aliquots (gives a 146 mg/ml stock) |
| Penicillin/streptomycin, Liquid. 100 ml | Gibco | 15140-122 | |
| Lipofectamine 2000 transfection reagent | Invitrogen | 11668-027 | |
| GFP-trap Agarose (500 μl resin) | Chromotek | gta-20 | |
| 5x SDS Sample loading buffer | Fisher Scientific | PN39000 | The use of purchased rather than homemade sample buffer is recommended to minimize keratin contamination. |
| Protease inhibitor cocktail set III | Calbiochem | 539134 | |
| 1.7 ml prelubricated tubes | Costar | 3207 | |
| BCA protein assay kit (1 L) | Pierce | 23225 | |
| Tris (Trizma) | Sigma-Aldrich | T1503 | |
| Ethylenediaminetetraacetic acid (EDTA) | Sigma-Aldrich | E6758 | |
| Sodium chloride | Sigma-Aldrich | S3014 | |
| Rnase cocktail | Ambion | AM2286 | |
| NP-40 alternative | Millipore | 492016 |
Références
- Williamson, M. P., Sutcliffe, M. J. Protein-protein interactions. Biochem Soc Trans. 38, 875-878 (2010).
- Bailey, D., Urena, L., Thorne, L., Goodfellow, I. Identification of protein interacting partners using tandem affinity purification. J. Vis. Exp. (60), (2012).
- Trinkle-Mulcahy, L. Resolving protein interactions and complexes by affinity purification followed by label-based quantitative mass spectrometry. Proteomics. 12, 1623-1638 (2012).
- Emmott, E., et al. The cellular interactome of the coronavirus infectious bronchitis virus nucleocapsid protein and functional implications for virus biology. J Virol. 87, 9486-9500 (2013).
- Li, W., Belsham, G. J., Proud, C. G. Eukaryotic initiation factors 4A (eIF4A) and 4G (eIF4G) mutually interact in a 1:1 ratio in vivo. J Biol Chem. 276, 29111-29115 (2001).
- Nielsen, P. J., Trachsel, H. The mouse protein synthesis initiation factor 4A gene family includes two related functional genes which are differentially expressed. EMBO J. 7, 2097-2105 (1988).
- Galicia-Vazquez, G., Cencic, R., Robert, F., Agenor, A. Q., Pelletier, J. A cellular response linking eIF4AI activity to eIF4AII transcription. RNA. 18, 1373-1384 (2012).
- Zakowicz, H., et al. Mutational analysis of the DEAD-box RNA helicase eIF4AII characterizes its interaction with transformation suppressor Pdcd4 and eIF4GI. RNA. 11, 261-274 (2005).
- Rothbauer, U., et al. A versatile nanotrap for biochemical and functional studies with fluorescent fusion proteins. Mol Cell Proteomics. 7, 282-289 (2008).
- Trinkle-Mulcahy, L., et al. Identifying specific protein interaction partners using quantitative mass spectrometry and bead proteomes. J Cell Biol. 183, 223-239 (2008).
- Dobreva, I., Fielding, A., Foster, L. J., Dedhar, S. Mapping the integrin-linked kinase interactome using SILAC. J Proteome Res. 7, 1740-1749 (2008).
- Mittler, G., Butter, F., Mann, M. A SILAC-based DNA protein interaction screen that identifies candidate binding proteins to functional DNA elements. Genome research. 19, 284-293 (2009).
- Selbach, M., Mann, M. Protein interaction screening by quantitative immunoprecipitation combined with knockdown QUICK. Nat Methods. 3, 981-983 (2006).
- Boulon, S., et al. Establishment of a protein frequency library and its application in the reliable identification of specific protein interaction partners. Mol Cell Proteomics. 9, 861-879 (2010).
- Wang, X., Huang, L. Identifying dynamic interactors of protein complexes by quantitative mass spectrometry. Mol Cell Proteomics. 7, 46-57 (2008).
- Fang, L., et al. Characterization of the human COP9 signalosome complex using affinity purification and mass spectrometry. J Proteome Res. 7, 4914-4925 (2008).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon