Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Spectroscopie de résonance magnétique nucléaire à haute température et à haute pression in situ
Dans cet article
Résumé
Les structures moléculaires et la dynamique des solides, des liquides, des gaz et des mélanges sont d’un intérêt critique pour divers domaines scientifiques. La NMR MAS NMR in situ à haute température et à haute pression permet de détecter l’environnement chimique des constituants dans des systèmes en phase mixte dans des environnements chimiques étroitement contrôlés.
Résumé
La spectroscopie par résonance magnétique nucléaire (RMN) représente une technique importante pour comprendre la structure et les environnements de liaison des molécules. Il existe une volonté de caractériser les matériaux dans des conditions pertinentes au processus chimique d’intérêt. Pour remédier à cette situation, des méthodes mas NMR à haute température et à haute pression in situ ont été mises au point pour permettre l’observation d’interactions chimiques sur une gamme de pressions (sous vide à plusieurs centaines de barres) et de températures (bien en dessous de 0 °C à 250 °C). En outre, l’identité chimique des échantillons peut être composée de solides, de liquides, de gaz ou de mélanges des trois. La méthode intègre des rotors NMR tout-zirconia (porte-échantillon pour MAS NMR) qui peuvent être scellés à l’aide d’un bouchon fileté pour compresser un anneau O. Ce rotor présente une grande résistance chimique, la compatibilité de la température, faible fond NMR, et peut résister à des pressions élevées. Ces facteurs combinés lui permettent d’être utilisé dans un large éventail de combinaisons de systèmes, qui à leur tour permettent son utilisation dans divers domaines comme la séquestration du carbone, la catalyse, la science des matériaux, la géochimie et la biologie. La flexibilité de cette technique en fait une option attrayante pour les scientifiques de nombreuses disciplines.
Introduction
L’analyse spectroscopique des échantillons est un outil d’analyse utilisé pour obtenir des informations précieuses sur des matériaux d’intérêt tels que leur état chimique, leur structure ou leur réactivité. D’un point de vue simpliste, la résonance magnétique nucléaire (IRMN) est l’une de ces techniques qui utilise un fort champ magnétique pour manipuler l’état de rotation des noyaux atomiques afin de mieux comprendre l’environnement chimique des espèces d’intérêt. L’état de spin nucléaire se réfère à la direction relative du moment magnétique induite par le mouvement du noyau filature, une particule chargée positivement. En l’absence d’un champ magnétique, les spins nucléaires sont orientés au hasard mais en présence d’un champ magnétique, les spins nucléaires s’alignent préférentiellement avec le champ externe de l’aimant dans un état de spin à faible énergie. Ce fractionnement des états de spin en valeurs énergétiques discrètes est connu sous le nom d’effet Zeeman. La différence entre ces niveaux d’énergie (ΔE) est modélisée par l’équation 1 :
où h est la constante de Plank, B0 est la force du champ magnétique externe et γ est le rapport gyrommagnétique du noyau. L’environnement chimique de ces vrilles applique également de légères perturbations à ces niveaux d’énergie. Les ondes radio des fréquences correspondantes peuvent être utilisées pour exciter les noyaux, ce qui génère une magnétisation transversale due à des rotations gagnant en cohérence de phase à mesure que la magnétisation longitudinale (basée sur la population de spins dans des états parallèles et anti-parallèles) diminue. Comme les noyaux continuent de précéder sur l’axe du champ magnétique, le mouvement magnétique rotatif crée un champ magnétique qui tourne également et génère un champ électrique. Ce champ module les électrons dans la bobine de détection NMR, générant le signal NMR. De légères différences dans l’environnement chimique des noyaux de l’échantillon affectent les fréquences détectées dans la bobine.
L’analyse NMR des échantillons solides introduit des complexités introdues dans les fluides. Dans les fluides, les molécules dégringolent à des vitesses rapides, faisant la moyenne de l’environnement chimique spatialement autour des noyaux. Dans les échantillons solides, il n’y a pas d’effet de moyenne de ce genre, introduisant un environnement chimique dépendant de l’orientation et de larges lignes spectrales dans le signal NMR. Pour atténuer ces défis, une technique connue sous le nom de filature d’angle magique (MAS)est utilisée 1,2. Dans mas NMR, les échantillons sont rapidement tournés (plusieurs kilohertz) à un angle de 54.7356° par rapport au champ magnétique externe utilisant un mécanisme externe de filature pour adresser les interactions orientation-dépendantes (anisotropiques) de NMR. Ceci rétrécit sensiblement les dispositifs de NMR et améliore la résolution spectrale en faisant la moyenne des termes orientation-dépendants de l’anisotropie chimique de décalage, des interactions dipolar, et des interactions quadrupolar. Deux exceptions notables entravent les capacités de rétrécissement de la ligne de MAS NMR. Le premier est un fort couplage homonucléaire parfois présent dans 1H NMR qui nécessite des vitesses de rotation élevées (~70 kHz) à enlever. Toutefois, les températures significativement élevées des applications à haute température supprimeront considérablement l’interactionhomonucléaire de 1 H en donnant un mouvement thermique amélioré de sorte qu’un taux de rotation d’échantillon beaucoup réduit puisse être utilisé pour une résolution spectrale significativement améliorée. En outre, avec la technologie en constante évolution, rotors avec de plus petits diamètres peuvent maintenant être fabriqués pour atteindre des taux de rotation dépassant de loin 5 kHz, ce qui contribue à supprimer davantage les interactions dipolaires homonucléaires 1H. La deuxième exception est les interactions quadrupolar résiduelles de deuxième ordre pour les noyaux avec spin qui dépasse la moitié puisque seul le terme de premier ordre est éliminé à l’angle magique, laissant des lineshapes plus complexes qui ne peuvent être améliorées que par des champs magnétiques externes plus forts. Il convient de souligner que les techniques MQMAS 2D peuvent être facilement intégrées à la technologie actuelle afin qu’un véritable spectre isotropique de changement chimique puisse être obtenu de la même manière que les expériences MQMAS standard3.
MAS NMR a permis une caractérisation détaillée des matériaux solides, renforçant ainsi la qualité des observations. Toutefois, la nécessité de faire tourner les échantillons dans les rotors NMR (le titulaire de l’échantillon) à des taux élevés impose également des défis dans la conduite d’expériences à des températures élevées et des pressions qui peuvent être plus pertinentes aux conditions d’intérêt. Il peut parfois être souhaitable d’examiner les matériaux dans des conditions relativement dures pour les rotors NMR. Un certain nombre d’efforts ont permis d’adapter avec succès les technologies de NMR à l’état liquide pour effectuer des NMR4,5,6,7à haute température et à haute pression; toutefois, les bouchons de rotor commerciaux utilisés pour le MAS NMR à l’état solide peuvent être expulsés du rotor à haute pression, causant des dommages importants à l’équipement. De tels effets peuvent être aggravés par l’examen d’une réaction de décomposition qui augmente considérablement la pression dans le support de l’échantillon. En tant que tel, de nouvelles conceptions sont nécessaires pour mener efficacement et en toute sécurité des expériences in situ de NMR. Par exemple, le rotor doit respecter plusieurs qualités pour une utilisation efficace dans mas NMR, à savoir non magnétique, léger, durable, résistant à la température, matériau de fond à faible NMR, étanche, haute résistance et résistant aux produits chimiques. Les pressions que le rotor doit supporter sont assez grandes. Non seulement le rotor doit résister à la pression de l’échantillon contenu à l’intérieur (p. ex., gaz à haute pression), mais la rotation de l’appareil confère une force centrifuge qui a sa propre contribution à la pression totale du système8, PT, par équation 2 :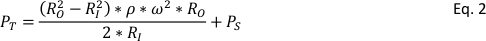
RI et RO sont le radii rotor intérieur et externe, respectivement, ω est la fréquence de rotation en radians par seconde, et P sest la pression de l’échantillon.
Un certain nombre de stratégies ont été élaborées pour répondre à cespréoccupations 9. Les premiers exemples ressemblaient à des tubes scellés parla flamme 10,11,12 ou des inserts en polymère13,14, qui étaient insuffisants pour un fonctionnement prolongé et contrôlé à des températures et des pressions élevées. Les itérations aux conceptions de rotor ont souffert des limitations de la température de fonctionnement maximale transmises par l’utilisation des réductions de volume d’époxy ou d’échantillon des insertionsen céramique 8,15,16. Une technologie récente réduit les coûts unitaires de production en utilisant de simples caractéristiques d’enclenchement dans un manchon de rotor commercial, mais offre relativement moins de contrôle sur les conditions avec lesquelles il peutfonctionner 17. La conception employée ci-dessus est un tout-zirconia, caverne-style manche rotor usiné avec un haut fileté18. Un bouchon est également fileté pour permettre un joint sécurisé. Le filetage inverse empêche la rotation de l’échantillon de desserrer le capuchon zirconia et un anneau O constitue les surfaces d’étanchéité. Cette conception du rotor est visible dans la figure 1 et des rotors et des instructions similaires pour les fabriquer ont été brevetés19. Une telle stratégie permet une résistance mécanique élevée, une résistance chimique et une tolérance à la température.
Ces conceptions conviennent aux températures et aux pressions d’au moins 250 °C et de 100 barres, limitées en température par la technologie de sonde NMR facilement disponible. Lorsqu’il est combiné avec de l’équipement spécialisé de préparation d’échantillons, il représente une technique vraiment puissante qui a été utilisée pour des applications de grande envergure comme la séquestration du carbone, la catalyse, le stockage de l’énergie et la biomédecine20. Un tel équipement comprend un moyen de prétratre les matériaux solides pour éliminer les espèces de surface indésirables telles que l’eau. Un four est souvent utilisé pour cette étape. Une boîte sèche est généralement utilisée pour charger les échantillons solides dans le rotor NMR. De là, le rotor est transféré dans un dispositif d’exposition qui permet au rotor d’être ouvert sous une atmosphère étroitement contrôlée pour charger un gaz ou un mélange désiré dans le rotor. Un tel dispositif est représenté dans la figure 2.
Protocole
Le protocole est divisé en quatre sections qui spécifient 1) la préparation de tout matériel solide utilisé dans le système ou l’activation ou le dégagement d’espèces adsorbées indésirables, 2) l’ajout de matériaux solides et liquides au rotor NMR, 3) l’ajout de gaz au rotor, et 4) la réalisation des expériences NMR dans le spectromètre. La procédure est représentative d’une séquence typique mais peut être modifiée pour répondre aux besoins spécifiques de l’expérience.
1. Prétraitement d’échantillons solides
- Pesez environ deux fois la masse de l’échantillon solide désiré pour l’expérience RMN (pour un rotor de 7,5 mm, ~250 mg) et placez l’échantillon solide dans un tube d’échantillon de quartz utilisé pour traiter les matériaux dans un système de four, en branchant le tube avec de la laine de quartz pour maintenir le matériau en place.
- Connectez les valves d’isolement au système de traitement des solides 1) ou 2) vide en plaçant le tube dans le four froid et en serrant les connexions.
- Apposer l’extrémité du tube de quartz (s) sur la valve d’isolation du gaz (s) en position ouverte.
- Commencez le traitement.
- Pour les systèmes d’écoulement :
- Apposer un thermocouple à l’extérieur du tube, le tenant en place avec un matériau résistant à la chaleur.
- Commencer le flux du gaz de traitement (p. ex., N2 à 100 sccm) pour dégager la surface solide ou activer le matériau.
- Alternativement, pour les systèmes de vide :
- Fermez la vanne d’isolement au système de vide et démarrez la pompe à vide.
- Lorsque le vide complet est établi, ouvrez très lentement la valve d’isolement pour appliquer le vide sur l’échantillon, en s’arrêtant périodiquement pour permettre au système d’équilibrer. Continuer jusqu’à ce que la vanne soit ouverte.
- Pour les systèmes d’écoulement :
- Allumez le contrôleur de four et réglez le programme de rampe de température à l’état désiré (p. ex., 300 °C pendant 4 heures à une vitesse de rampe de 5 °C/min).
- Démarrez le programme de température et laissez-le s’exécuter.
- Une fois terminé, laissez refroidir l’échantillon à une température réalisable.
- Éteignez le contrôleur de température et arrêtez le flux/vide.
- Scellez rapidement l’échantillon avec les vannes d’isolement pour maintenir l’environnement d’échantillonnage désiré.
- Déconnecter le tube de quartz du système de traitement et transférer les tubes et les valves fermées à l’antichambre d’une boîte à gants sèche purge n2.
- Videz et remplissez l’antichambre au moins 4 fois et transférez le tube à l’intérieur de la boîte à gants.
2. Chargement d’échantillons solides dans le rotor NMR
- Pesez le rotor NMR à haute pression et à haute température vide et propre avec le capuchon du rotor.
- Placez le rotor NMR dans le support pour maintenir la directionnalité.
- Placez l’entonnoir de l’échantillon dans l’alésage du rotor.
- Retirez la valve d’isolement du tube de l’échantillon et versez une petite quantité de matériau solide dans l’entonnoir.
- Appuyez sur la poudre dans l’entonnoir et dirigez-la légèrement vers le rotor avec la tige d’emballage si nécessaire.
- Répétez l’ajout échelonné de matériaux solides jusqu’à ce que la quantité désirée (p. ex., 1/2 rotor) soit atteinte.
- Pesez le rotor NMR (et le capuchon) avec l’échantillon à l’intérieur pour déterminer la quantité d’échantillon ajoutée.
- Si vous le souhaitez, dessinez une quantité spécifiée de n’importe quel échantillon liquide et injectez lentement le liquide au centre du rotor NMR à l’aide d’une micro seringue.
- Scellez le rotor en plaçant le bouchon sur le dessus et en le tournant dans le sens inverse des aiguilles d’une montre avec le rotor de capuchon pour engager l’anneau O entre le rotor et le capuchon. Notez qu’un nouvel anneau O peut être périodiquement nécessaire pour éviter les fuites, surtout si vous utilisez des mélanges chimiquement abrasifs ou de petits gaz tels que l’hydrogène.
- Pesez le rotor NMR pour déterminer la masse totale de l’échantillon ajouté.
3. Charger le rotor NMR avec les produits chimiques désirés aux conditions souhaitées
- Placez le rotor NMR scellé dans le stade du rotor, en vous assurant que la taille de l’insert de scène est compatible avec la taille du rotor et serrez l’écrou à la main pour le fixer en place. Notez que l’étanchéité du rotor dans le support dans cette étape déterminera l’étanchéité du joint de capuchon.
- Abaissez l’étage du rotor dans la partie inférieure du dispositif d’exposition à haute pression.
- Utilisez une clé Allen pour tourner l’une des vis à 90° pour fixer le stade du rotor dans le fond du dispositif d’exposition.
- Placez la partie supérieure du dispositif de chargement NMR dans et sur le dessus de la section inférieure, en alignant le capuchon NMR vers le haut de la tête de bouchon du rotor NMR pour s’assurer qu’il est engagé.
- Placez les 2 pinces sur le dessus de la lèvre où les sections supérieure et inférieure du dispositif d’exposition se rencontrent et verrouiller en place.
- Serrer les 6 boulons sur le dessus de la partie supérieure du dispositif d’exposition pour engager la surface d’étanchéité entre les sections supérieure et inférieure.
- Connectez la partie supérieure du dispositif d’exposition NMR à l’entrée et aux prises de la conduite de gaz.
- Connectez le thermocouple sur la partie supérieure du dispositif d’exposition NMR au capteur de température.
- Si vous le souhaitez, enveloppez le ruban chauffant autour des conduites de gaz et des sections supérieures du dispositif d’exposition pour permettre le chauffage avec le contrôleur respectif. Une plaque chaude peut également être engagée.
- S’assurer que la sortie de la chambre d’exposition est ouverte et que la vanne de gaz source est fermée, allumez la pompe à vide pour retirer l’air du dispositif d’exposition et des lignes associées.
- Purgez les lignes avec le gaz désiré ou inerte, en faisant du vélo entre le vide et la pression atmosphérique à trois reprises pour s’assurer que les lignes sont dégagées de l’air.
- Préparer la composition de gaz désirée soit à partir de 1) un système de livraison à haute pression ou 2) un système d’écoulement pour introduire des vapeurs à une pression spécifiée.
- Pour la préparation d’échantillons à haute pression ou sous vide :
- Fermez la prise de gaz du dispositif d’exposition et réglez les vannes de collecteur de gaz pour contourner la ligne d’injection liquide.
- Réglez la pression désirée sur la pompe à seringues haute pression du système de livraison à haute pression.
- Ouvrez les vannes de source de gaz sur la pompe à seringues haute pression et exécutez le programme fixé sur la pompe, en surveillant la pression réelle à l’intérieur du dispositif d’exposition.
- Lorsque la pression désirée est atteinte à l’intérieur du dispositif d’exposition, arrêtez la pompe à seringues et fermez les vannes de gaz source.
- Ouvrez le rotor NMR en tournant dans le sens des aiguilles d’une montre le mécanisme de vis externe, qui est couplé au bit intérieur du bouchon NMR.
- Laissez le gaz de la pression désirée pénétrer dans le rotor NMR et équilibrer.
- Reseal le rotor NMR en tournant le mécanisme de vis externe dans le sens inverse des aiguilles d’une montre. Une fenêtre d’observation aidera à déterminer quand le rotor est fermé.
- Dépressuriser lentement le système en ouvrant la vanne de sortie de gaz du dispositif d’exposition.
- Pour la préparation d’échantillons de gaz ou de vapeur :
- Assurez-vous que la prise de gaz du dispositif d’exposition est ouverte pour éviter la sur-pression.
- Réglez le débit de gaz désiré sur le contrôleur de débit de masse et commencez le flux de gaz.
- Connectez la ligne d’alimentation liquide de la pompe à seringues liquide au collecteur de gaz.
- Réglez les vannes de collecteur de gaz pour permettre le flux vers la ligne d’injection liquide.
- Réglez le débit liquide sur la pompe à seringues liquide pour obtenir la pression de vapeur désirée et commencer l’injection liquide.
- Ouvrez le rotor NMR en tournant dans le sens des aiguilles d’une montre le mécanisme de vis externe qui est couplé au bit intérieur de bouchon NMR.
- Permettre au système d’équilibrer aux pressions de gaz souhaitées à l’intérieur du rotor NMR et de reseal le rotor NMR en tournant le mécanisme de vis externe dans le sens inverse des aiguilles d’une montre. Une fenêtre d’observation aidera à déterminer quand le rotor est fermé.
- Arrêtez l’injection de la pompe à seringues liquides et configurez les vannes pour contourner la ligne d’injection liquide, déconnectant la pompe du système.
- Arrêtez le gaz qui coule.
- Pour la préparation d’échantillons à haute pression ou sous vide :
- Purgez le système avec un gaz inerte pour éliminer les gaz potentiellement toxiques ou inflammables.
- Arrêtez tout chauffage et laissez refroidir le système.
- Déconnectez tout ruban chauffant et le thermocouple.
- Déconnecter les conduites d’entrée et de gaz de sortie.
- Desserrez les 6 boulons sur le dessus du dispositif d’exposition pour compromettre le joint.
- Déballez les 2 sections de serrage et retirez-les du dispositif d’exposition.
- Soulevez soigneusement la partie supérieure vers le haut et hors de la section inférieure.
- Utilisez une clé Allen pour desserrer le stade du rotor et l’élaborer avec la tige filetée.
- Desserrez l’écrou sur le stade du rotor et retirez le rotor du composant de l’appareil.
- Pesez le rotor pour vous assurer que les quantités de gaz souhaitées sont présentes.
4. Mener l’expérience MAS NMR
- Placez le rotor NMR dans la bobine NMR sur la sonde NMR.
- Soulevez la sonde dans l’alésage de l’aimant et verrouillez-la en place.
- Lancez la filature d’échantillon à l’aide de la boîte de commande MAS et ajustez-vous au taux de rotation du rotor désiré.
- Utilisez l’ordinateur pour commencer la séquence de réglage/match sur le canal désiré.
- Ajustez les réglages/correspondance de la sonde pour optimiser l’électronique de la sonde.
- Quittez la séquence de réglage/match sur l’ordinateur et configurez les paramètres expérimentaux souhaités (p. ex., séquence d’impulsions, tableau d’expériences, température, etc.).
- Recueillir les données MAS NMR.
Résultats
La sortie du spectromètre NMR prend la forme d’une désintégration d’induction libre (FID) qui est le signal de domaine du temps des vrilles excitées comme ils se détendent vers l’équilibre thermodynamique. Un tel FID ressemble à la figure 3. Lorsque Fourier est passé du domaine du temps au domaine de fréquence (fréquence à PPM par équation 3, où la fréquence absolue de différence et une référence est divisée par la fréquence du transporteur du spectromètre NMR), il ...
Discussion
La méthode d’effectuer des mesures spectroscopiques MAS NMR décrites ci-après représente l’état de l’art pour effectuer à haute température, haute pression MAS NMR. Ces méthodes permettent d’observer les interactions se produisant dans des atmosphères sous vide jusqu’à plusieurs centaines de barres et de basses températures (bien en dessous de 0 °C à 250 °C) d’une manière fiable et reproductible. La capacité de sonder des systèmes contenant des mélanges de solides, de liquides et de gaz dans...
Déclarations de divulgation
Les auteurs déclarent les intérêts financiers concurrents suivants. J.Z.H et ses collègues détiennent un brevet sur la conception du rotor (US9151813B2). J.Z.H., N.R.J., et coll. ont déposé une demande de brevet provisoire sur le dispositif d’exposition.
Remerciements
L’examen des applications catalyseurs a été appuyé par le Département de l’énergie des États-Unis, l’Office of Science, l’Office of Basic Energy Sciences, la Division of Chemical Sciences, Biosciences et Geosciences Catalysis Program dans le cadre du contrat DE-AC05-RL01830 et FWP-47319. L’examen des demandes biomédicales a été appuyé par le National Institute of Health, National Institute of Environmental Health Sciences, dans le cadre de la subvention R21ES029778. Des expériences ont été menées à l’EMSL (grille.436923.9), un bureau du DOE of Science User Facility parrainé par le Bureau de la recherche biologique et environnementale et situé au Pacific Northwest National Laboratory (PNNL). PNNL est un laboratoire national multi-programmes exploité par Battelle pour le département américain de l’Énergie sous contrat DE-AC05-RL01830 et FWP-47319.
matériels
| Name | Company | Catalog Number | Comments |
| 1) Preparation of Solids Samples | |||
| Gas maniforld | |||
| Gas Mass Flow Controllers | |||
| Vacuum Pump | |||
| Tube Furnace | |||
| Temperature Controller | |||
| Thermocouple | |||
| Quartz Tube | |||
| Isolation Valves | |||
| Quartz Wool | |||
| 2) Loading solid samples into the rotor | |||
| Dry glove box | |||
| High-temperature, high-pressure NMR rotor | |||
| Sample funnel | |||
| Sample packing rod | |||
| Rotor holder | |||
| Analytical Balance | |||
| Microsyringe | |||
| Rotor cap bit | |||
| 3) Addition of gases to the rotor | |||
| NMR loading chamber | |||
| Rotor stage and appropriately sized inserts | |||
| Vacuum Pump | |||
| Gas maniforld | |||
| Gas Mass Flow Controllers | |||
| Vacuum Pump | |||
| Heating Tape | |||
| Temperature Controller | |||
| Thermocouple | |||
| Allen wrench | |||
| Threaded rod | |||
| Wrenchs | |||
| Pressure Gauge | |||
| High-pressure syringe pump | |||
| Liquid syringe pump | |||
| 4) Conducting the NMR experiments | |||
| MAS NMR probe | |||
| NMR spectrometer | |||
| Computer to control the spectrometer |
Références
- Andrew, E. R., Bradbury, A., Eades, R. G. Nuclear Magnetic Resonance Spectra from a Crystal rotated at High Speed. Nature. 182 (4650), 1659 (1958).
- Lowe, I. J. Free Induction Decays of Rotating Solids. Physical Review Letters. 2 (7), 285-287 (1959).
- Frydman, L., Grant, D. M., Harris, R. K. Fundamentals of Multiple-Quantum Magic-Angle Spinning NMR on Half-Integer Quadrupolar Nuclei. Encyclopedia of Nuclear Magnetic Resonance. 9, 262-274 (2002).
- Khodov, I., Dyshin, A., Efimov, S., Ivlev, D., Kiselev, M. High-pressure NMR spectroscopy in studies of the conformational composition of small molecules in supercritical carbon dioxide. Journal of Molecular Liquids. 309, (2020).
- Kolbe, F. High-Pressure in situ 129Xe NMR Spectroscopy: Insights into Switching Mechanisms of Flexible Metal-Organic Frameworks Isoreticular to DUT-49. Chemistry of Materials. 31 (16), 6193-6201 (2019).
- Ochoa, G., et al. (2) H and (139) La NMR Spectroscopy in Aqueous Solutions at Geochemical Pressures. Angewandte Chemie International Edition. 54 (51), 15444-15447 (2015).
- Hoffmann, H. C., et al. High-pressure in situ 129Xe NMR spectroscopy and computer simulations of breathing transitions in the metal-organic framework Ni2(2,6-ndc)2(dabco) (DUT-8(Ni)). Journal of the American Chemical Society. 133 (22), 8681-8690 (2011).
- Turcu, R. V. F., et al. Rotor design for high pressure magic angle spinning nuclear magnetic resonance. Journal of Magnetic Resonance. 226, 64-69 (2013).
- Jaegers, N. R., Hu, M. Y., Hoyt, D. W., Wang, Y., Hu, J. Z. Development and Application of In situ High-Temperature, High-Pressure Magic Angle Spinning NMR. Modern Magnetic Resonance. , 1-19 (2017).
- Miyoshi, T., Takegoshi, K., Terao, T. 13C High-Pressure CPMAS NMR Characterization of the Molecular Motion of Polystyrene Plasticized by CO2 Gas. Macromolecules. 30 (21), 6582-6585 (1997).
- Miyoshi, T., Takegoshi, K., Terao, T. 129Xe n.m.r. study of free volume and phase separation of the polystyrene/poly(vinyl methyl ether) blend. Polymer. 38 (21), 5475-5480 (1997).
- Miyoshi, T., Takegoshi, K., Terao, T. Effects of Xe Gas on Segmental Motion in a Polymer Blend As Studied by 13C and 129Xe High-Pressure MAS NMR. Macromolecules. 35 (1), 151-154 (2002).
- Yonker, C. R., Linehan, J. C. The use of supercritical fluids as solvents for NMR spectroscopy. Progress in Nuclear Magnetic Resonance Spectroscopy. 47 (1), 95-109 (2005).
- Deuchande, T., Breton, O., Haedelt, J., Hughes, E. Design and performance of a high pressure insert for use in a standard magic angle spinning NMR probe. Journal of Magnetic Resonance. 183 (2), 178-182 (2006).
- Hoyt, D. W., et al. High-pressure magic angle spinning nuclear magnetic resonance. Journal of Magnetic Resonance. 212 (2), 378-385 (2011).
- Vjunov, A., et al. Following Solid-Acid-Catalyzed Reactions by MAS NMR Spectroscopy in Liquid Phase-Zeolite-Catalyzed Conversion of Cyclohexanol in Water. Angewandte Chemie International Edition. 53 (2), 479-482 (2014).
- Chamas, A., et al. High temperature/pressure MAS-NMR for the study of dynamic processes in mixed phase systems. Magnetic Resonance Imaging. 56, 37-44 (2019).
- Hu, J. Z., et al. Sealed rotors for in situ high temperature high pressure MAS NMR. ChemComm. 51 (70), 13458-13461 (2015).
- Hu, J. Z., Hu, M. Y., Townsend, M. R., Lercher, J. A., Peden, C. H. High-pressure, high-temperature magic angle spinning nuclear magnetic resonance devices and processes for making and using same. US patent. , (2015).
- Jaegers, N. R., Mueller, K. T., Wang, Y., Hu, J. Z. Variable Temperature and Pressure Operando MAS NMR for Catalysis Science and Related Materials. Accounts of Chemical Research. 53 (3), 611-619 (2020).
- Dagle, V., et al. Single-step Conversion of Ethanol to n-butenes over Ag-ZrO2/SiO2 catalysts. ACS Catalysis. 10 (18), 10602-10613 (2020).
- Jaegers, N. R., Wang, Y., Hu, J. Z. Thermal perturbation of NMR properties in small polar and non-polar molecules. Scientific Reports UK. 10 (1), 6097 (2020).
- Jaegers, N. R. . Applications of In situ Magnetic Resonance Spectroscopy for Structural Analysis of Oxide-supported Catalysts. , (2019).
- Mehta, H. S., et al. A novel high-temperature MAS probe with optimized temperature gradient across sample rotor for in-situ monitoring of high-temperature high-pressure chemical reactions. Solid State Nuclear Magnetic Resonance. 102, 31-35 (2019).
- Hu, J. Z., et al. A large sample volume magic angle spinning nuclear magnetic resonance probe for in situ investigations with constant flow of reactants. Physical Chemistry Chemical Physics. 14 (7), 2137-2143 (2012).
- Jiang, Y., et al. In situ MAS NMR-UV/Vis investigation of H-SAPO-34 catalysts partially coked in the methanol-to-olefin conversion under continuous-flow conditions and of their regeneration. Microporous and Mesoporous Materials. 105 (1-2), 132-139 (2007).
- Xu, S., Zhang, W., Liu, X., Han, X., Bao, X. Enhanced In situ Continuous-Flow MAS NMR for Reaction Kinetics in the Nanocages. Journal of the American Chemical Society. 131 (38), 13722-13727 (2009).
- Graham, T. R., et al. In situ Al-27 NMR Spectroscopy of Aluminate in Sodium Hydroxide Solutions above and below Saturation with Respect to Gibbsite. Inorganic Chemistry. 57 (19), 11864-11873 (2018).
- Zhang, X., et al. Boehmite and Gibbsite Nanoplates for the Synthesis of Advanced Alumina Products. ACS Applied Nano Materials. 1 (12), 7115-7128 (2018).
- Zhang, X., et al. Transformation of Gibbsite to Boehmite in Caustic Aqueous Solution at Hydrothermal Conditions. Crystal Growth & Design. 19 (10), 5557-5567 (2019).
- Hu, J. Z., Jaegers, N. R., Hu, M. Y., Mueller, K. T. In situ and ex situ NMR for battery research. Journal of Physics: Condensed Matter. 30 (46), (2018).
- Hu, J. Z., et al. Adsorption and Thermal Decomposition of Electrolytes on Nanometer Magnesium Oxide: An in situ C-13 MAS NMR Study. ACS Applied Materials & Interfaces. 11 (42), 38689-38696 (2019).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon