É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Espectroscopia de ressonância magnética nuclear de alta temperatura e alta pressão no situ Magic Angle Spinning Nuclear Resonance
Neste Artigo
Resumo
As estruturas moleculares e a dinâmica de sólidos, líquidos, gases e misturas são de interesse crítico para diversos campos científicos. A NMR mas de alta temperatura e alta pressão permite a detecção do ambiente químico dos constituintes em sistemas de fases mistas em ambientes químicos fortemente controlados.
Resumo
A espectroscopia de ressonância magnética nuclear (NMR) representa uma técnica importante para entender a estrutura e os ambientes de ligação das moléculas. Existe um impulso para caracterizar materiais em condições relevantes para o processo químico de interesse. Para lidar com isso, in situ métodos mas nMR de alta temperatura e alta pressão foram desenvolvidos para permitir a observação de interações químicas sobre uma gama de pressões (vácuo para várias centenas de barras) e temperaturas (bem abaixo de 0 °C a 250 °C). Além disso, a identidade química das amostras pode ser composta por sólidos, líquidos e gases ou misturas dos três. O método incorpora rotores de NMR all-zirconia (porta-amostras para MAS NMR) que podem ser selados usando uma tampa roscada para comprimir um anel O. Este rotor exibe grande resistência química, compatibilidade de temperatura, baixo fundo NMR, e pode suportar altas pressões. Esses fatores combinados permitem que ele seja utilizado em uma ampla gama de combinações de sistemas, que por sua vez permitem seu uso em diversos campos como sequestro de carbono, catálise, ciência material, geoquímica e biologia. A flexibilidade dessa técnica torna-a uma opção atraente para cientistas de inúmeras disciplinas.
Introdução
A análise espectroscópica das amostras é uma ferramenta analítica usada para obter informações valiosas sobre materiais de interesse, como seu estado químico, estrutura ou reatividade. Em uma visão simplista, a ressonância magnética nuclear (RMN) é uma dessas técnicas que utiliza um forte campo magnético para manipular o estado de rotação dos núcleos atômicos para entender melhor o ambiente químico das espécies de interesse. O estado de rotação nuclear refere-se à direção relativa do momento magnético induzida pelo movimento do núcleo giratório, uma partícula positivamente carregada. Na ausência de um campo magnético, os giros nucleares são orientados aleatoriamente, mas na presença de um campo magnético, os giros nucleares se alinham preferencialmente com o campo externo do ímã em um estado de rotação de baixa energia. Esta divisão de estados de spin para valores de energia discretos é conhecida como o efeito Zeeman. A diferença entre esses níveis de energia (ΔE) é modelada pela Equação 1:
onde h é constante de Plank, B0 é a força do campo magnético externo e γ é a razão gyrommagnética do núcleo. O ambiente químico desses giros também aplica pequenas perturbações a esses níveis de energia. Ondas de rádio de frequências correspondentes podem ser usadas para excitar os núcleos, o que gera uma magnetização transversal devido a giros ganhando coerência de fase à medida que a magnetização longitudinal (baseada na população de giros em estados paralelos e anti-paralelos) é diminuída. À medida que os núcleos continuam precessing sobre o eixo do campo magnético, o movimento magnético rotativo cria um campo magnético que também está girando e gerando um campo elétrico. Este campo modula os elétrons na bobina de detecção de NMR, gerando o sinal NMR. Pequenas diferenças no ambiente químico dos núcleos na amostra afetam as frequências detectadas na bobina.
A análise de RMN de amostras sólidas introduz complexidades não encontradas em fluidos. Nos fluidos, as moléculas caem a taxas rápidas, em média o ambiente químico espacialmente ao redor dos núcleos. Em amostras sólidas, não ocorre tal efeito de média, introduzindo um ambiente químico dependente da orientação e linhas espectrais amplas no sinal NMR. Para mitigar esses desafios, uma técnica conhecida como fiação de ângulo mágico (MAS) é empregada1,2. Em MAS NMR, as amostras são rapidamente giradas (vários kilohertz) em um ângulo de 54,7356° em relação ao campo magnético externo usando um mecanismo de fiação externo para abordar as interações dependentes de orientação (anisotropic) da RN. Isso reduz substancialmente as características da RMN e melhora a resolução espectral, analisando os termos dependentes da orientação da anisotropia de mudança química, interações dipolares e interações quadruplicares. Duas exceções notáveis dificultam as habilidades de estreitamento da linha do MAS NMR. O primeiro é um forte acoplamento homonuclear às vezes presente em 1H NMR que requer altas velocidades de giro (~70 kHz) para remover. No entanto, as temperaturas significativamente elevadas das aplicações de alta temperatura suprimirão muito a interação homonuclear de 1H, transmitindo movimento térmico aprimorado de forma que uma taxa de rotação amostral muito reduzida possa ser utilizada para uma resolução espectral significativamente melhorada. Além disso, com a tecnologia em constante evolução, rotores com diâmetros menores agora podem ser fabricados para alcançar taxas de fiação muito superiores a 5 kHz, o que ajuda a suprimir ainda mais as interações dipolares homonucleares de 1H. A segunda exceção são as interações quadrupolares residuais de segunda ordem para núcleos com spin que excedem metade, uma vez que apenas o termo da primeira ordem é eliminado no ângulo mágico, deixando formas de linha mais complexas que só podem ser melhoradas por campos magnéticos externos mais fortes. Deve-se ressaltar que as técnicas 2D MQMAS podem ser prontamente incorporadas à tecnologia atual para que um verdadeiro espectro de mudança química isotropica possa ser obtido de forma semelhante aos experimentos padrão de MQMAS3.
A MAS NMR possibilitou a caracterização detalhada de materiais sólidos, fortalecendo a qualidade das observações. No entanto, a necessidade de girar as amostras em rotores de RMN (o portador da amostra) a altas taxas também impõe desafios na realização de experimentos a temperaturas elevadas e pressões que podem ser mais relevantes para as condições de interesse. Pode, às vezes, ser desejável examinar materiais em condições relativamente duras para rotores de RMN. Uma série de esforços adaptaram com sucesso tecnologias de RMN de estado líquido para conduzir NMR4,5,6,7; no entanto, as tampas comerciais do rotor usadas para o MAS NMR de estado sólido podem ser expelidas do rotor em altas pressões, causando danos significativos ao equipamento. Tais efeitos podem ser agravados através do exame de uma reação de decomposição que aumenta muito a pressão no suporte da amostra. Como tal, novos projetos são necessários para realizar de forma eficaz e segura experimentos in situ NMR. Por exemplo, o rotor deve aderir a várias qualidades para uso eficaz em MAS NMR, ou seja, não magnético, leve, durável, resistente à temperatura, material de fundo NMR baixo, vedado, de alta resistência e resistente químico. As pressões que o rotor deve suportar são bastante grandes. Não só o rotor deve suportar a pressão da amostra contida (por exemplo, gás de alta pressão), a rotação do dispositivo transmite força centrífuga que tem sua própria contribuição para a pressão total do sistema8, PT, pela equação 2: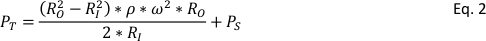
RI e RO são os raios do rotor interno e externo, respectivamente, ω é a frequência rotacional em radianos por segundo, e P s é a pressãoamostral.
Uma série de estratégias foram desenvolvidas para enfrentar essas preocupações9. Os primeiros exemplos se assemelhavam aos tubos selados por chamas10,11,12 ou inserções de polímeros13,14, que eram insuficientes para operação estendida e controlada a temperaturas e pressões elevadas. As iterações aos desenhos do rotor sofreram limitações na temperatura máxima de operação transmitida pelo uso de reduções de volume de epóxi ou amostra das pastilhas8,15,16. Uma tecnologia recente reduz os custos de produção unitária empregando recursos simples de snap-in em uma manga de rotor comercial, mas oferece relativamente menos controle sobre as condições com as quais pode operar17. O design aqui empregado é uma manga de rotor no estilo caverna, moída com um top18roscado. Uma tampa também é roscada para permitir um selo seguro. A rosca reversa impede que a rotação da amostra afrouxe a tampa da zircônia e um anel O constitua as superfícies de vedação. Este design do rotor é visível na Figura 1 e rotores e instruções semelhantes para fazê-los foram patenteados19. Tal estratégia permite alta resistência mecânica, resistência química e tolerância à temperatura.
Estes desenhos são adequados para temperaturas e pressões de pelo menos 250 °C e 100 bar, limitados em temperatura pela tecnologia de sonda NMR prontamente disponível. Quando combinado com equipamentos especializados de preparação de amostras, representa uma técnica verdadeiramente poderosa que tem sido empregada para aplicações de longo alcance como sequestro de carbono, catálise, armazenamento de energia e biomedicina20. Tais equipamentos incluem uma maneira de pré-tratamento dos materiais sólidos para remover espécies superficiais indesejadas, como a água. Uma fornalha é frequentemente empregada para esta etapa. Uma caixa seca é normalmente usada para carregar as amostras sólidas no rotor NMR. A partir daí, o rotor é transferido para um dispositivo de exposição que permite que o rotor seja aberto sob uma atmosfera bem controlada para carregar um gás ou mistura desejado no rotor. Tal dispositivo é retratado na Figura 2.
Protocolo
O protocolo é dividido em quatro seções que especificam 1) a preparação de quaisquer materiais sólidos que estão sendo utilizados no sistema ou ativação ou compensação de espécies adsorvidas indesejadas, 2) adição dos materiais sólidos e líquidos ao rotor NMR, 3) adição de gases ao rotor e 4) conduzindo os experimentos de RMN no espectrômetro. O procedimento é representativo de uma sequência típica, mas pode ser modificado para atender às necessidades específicas do experimento.
1. Pré-tratamento de amostras sólidas
- Pesar aproximadamente o dobro da massa da amostra sólida desejada para o experimento NMR (para um rotor de 7,5 mm, ~250 mg) e colocar a amostra sólida em um tubo de amostra de quartzo usado para tratar materiais em um sistema de forno, conectando o tubo com lã de quartzo para manter o material no lugar.
- Conecte as válvulas de isolamento ao tratamento de sólidos 1) fluxo ou 2) sistema de vácuo colocando o tubo no forno frio e apertando as conexões.
- Fixar as extremidades do tubo de quartzo na válvula de isolamento de gás na posição aberta.
- Comece o tratamento.
- Para sistemas de fluxo:
- Fixar um termopar na parte externa do tubo, segurando-o no lugar com um material resistente ao calor.
- Inicie o fluxo do gás de tratamento (por exemplo, N2 a 100 sccm) para limpar a superfície sólida ou ativar o material.
- Alternativamente, para sistemas de vácuo:
- Feche a válvula de isolamento para o sistema de vácuo e inicie a bomba de vácuo.
- Quando o vácuo completo é estabelecido, muito lentamente abra a válvula de isolamento para aplicar vácuo à amostra, parando periodicamente para permitir que o sistema se equilibre. Continue até que a válvula esteja aberta.
- Para sistemas de fluxo:
- Ligue o controlador do forno e defina o programa de rampa de temperatura para a condição desejada (por exemplo, 300 °C durante 4 horas a uma velocidade de rampa de 5 °C/min).
- Inicie o programa de temperatura e deixe-o funcionar.
- Quando concluída, deixe a amostra esfriar a uma temperatura viável.
- Desligue o controlador de temperatura e pare o fluxo/vácuo.
- Veda rapidamente a amostra com as válvulas de isolamento para manter o ambiente amostral desejado.
- Desconecte o tubo de quartzo do sistema de tratamento e transfira os tubos e as válvulas fechadas para a antecâmara de uma caixa de luvas seca, N2- purgada.
- Esvazie e rechee a antecâmara pelo menos 4 vezes e transfira o tubo dentro do porta-luvas.
2. Carregar amostras sólidas no rotor NMR
- Pesar o rotor NMR de alta pressão e alta pressão vazio e limpo com a tampa do rotor.
- Coloque o rotor NMR no suporte para manter a direcionalidade.
- Coloque o funil de amostra no furo do rotor.
- Remova a válvula de isolamento do tubo de amostra e despeje uma pequena quantidade de material sólido no funil.
- Bata o pó no funil e direcione-o levemente para dentro do rotor com a haste de embalagem, conforme necessário.
- Repita a adição stepwise de material sólido até que a quantidade desejada (por exemplo, rotor de 1/2) seja alcançada.
- Pesar o rotor NMR (e a tampa) com a amostra dentro para determinar a quantidade de amostra adicionada.
- Se desejar, elasenhe uma quantidade especificada de qualquer amostra líquida e injete lentamente o líquido no centro do rotor NMR com uma micro seringa.
- Sele o rotor colocando a tampa na parte superior e virando-a no sentido anti-horário com a tampa do rotor para engatar o anel O entre o rotor e a tampa. Observe que um novo anel O pode ser periodicamente necessário para evitar vazamentos, especialmente se usar misturas quimicamente abrasivas ou pequenos gases, como hidrogênio.
- Pesar o rotor NMR para determinar a massa total da amostra adicionada.
3. Carregar o rotor NMR com os produtos químicos desejados nas condições desejadas
- Coloque o rotor NMR selado no estágio do rotor, garantindo que o tamanho da inserção do palco seja compatível com o tamanho do rotor e aperte a porca manualmente para fixá-la no lugar. Note que o aperto do rotor no suporte nesta etapa determinará o aperto do selo da tampa.
- Abaixe o estágio do rotor na parte inferior do dispositivo de exposição de alta pressão.
- Use uma chave Allen para girar um dos parafusos 90° para fixar o estágio do rotor na parte inferior do dispositivo de exposição.
- Coloque a seção superior do dispositivo de carregamento NMR dentro e na parte superior da seção inferior, alinhando a tampa NMR na parte superior da tampa do rotor NMR para garantir que ele esteja ligado.
- Coloque os 2 grampos sobre a parte superior do lábio onde as seções superior e inferior do dispositivo de exposição se encontram e travam-nas no lugar.
- Aperte os 6 parafusos na parte superior do dispositivo de exposição para acionar a superfície de vedação entre as seções superior e inferior.
- Conecte a seção superior do dispositivo de exposição NMR à entrada e saídas da linha de gás.
- Conecte o termopar na parte superior do dispositivo de exposição NMR ao sensor de temperatura.
- Se desejar, enrole a fita de aquecimento ao redor das linhas de gás e das seções superiores do dispositivo de exposição para permitir o aquecimento com o respectivo controlador. Uma placa quente também pode ser engatilhada.
- Garantindo que a saída da câmara de exposição esteja aberta e a válvula de gás de origem esteja fechada, ligue a bomba de vácuo para remover o ar do dispositivo de exposição e das linhas associadas.
- Purgue as linhas com o gás desejado ou um inerte, pedalando entre vácuo e pressão atmosférica três vezes para garantir que as linhas sejam limpas do ar.
- Prepare a composição de gás desejada a partir de 1) um sistema de entrega de alta pressão ou 2) um sistema de fluxo para introduzir vapores a uma pressão especificada.
- Para preparação de amostras de alta pressão ou vácuo:
- Feche a saída de gás do dispositivo de exposição e ajuste as válvulas de coletor de gás para contornar a linha de injeção líquida.
- Coloque a pressão desejada na bomba de seringa de alta pressão do sistema de entrega de alta pressão.
- Abra as válvulas de fonte de gás na bomba de seringa de alta pressão e execute o conjunto do programa na bomba, monitorando a pressão real dentro do dispositivo de exposição.
- Quando a pressão desejada for alcançada dentro do dispositivo de exposição, pare a bomba de seringa e feche as válvulas de gás de origem.
- Abra o rotor NMR girando no sentido horário do mecanismo externo do parafuso, que é acoplado à tampa interior da NMR.
- Deixe o gás da pressão desejada entrar no rotor NMR e equilibrar.
- Resealar o rotor NMR girando o mecanismo externo do parafuso no sentido anti-horário. Uma janela de visualização ajudará a determinar quando o rotor está fechado.
- Despressurize lentamente o sistema abrindo a válvula de saída de gás do dispositivo de exposição.
- Para a preparação de amostras de gás ou vapor fluindo:
- Certifique-se de que a saída de gás do dispositivo de exposição está aberta para evitar a pressão excessiva.
- Defina a vazão de gás desejada no controlador de fluxo de massa e inicie o fluxo de gás.
- Conecte a linha de alimentação líquida da bomba de seringa líquida ao coletor de gás.
- Ajuste as válvulas de coletor de gás para permitir o fluxo para a linha de injeção líquida.
- Defina a taxa de fluxo líquido na bomba de seringa líquida para alcançar a pressão de vapor desejada e inicie a injeção líquida.
- Abra o rotor NMR girando no sentido horário o mecanismo externo do parafuso que é acoplado à tampa interior da NMR.
- Permita que o sistema se equilibre às pressões de gás desejadas dentro do rotor NMR e resseque o rotor NMR girando o mecanismo externo do parafuso no sentido anti-horário. Uma janela de visualização ajudará a determinar quando o rotor está fechado.
- Pare a injeção da bomba de seringa líquida e configure as válvulas para contornar a linha de injeção líquida, desconectando a bomba do sistema.
- Pare o gás que flui.
- Para preparação de amostras de alta pressão ou vácuo:
- Purgue o sistema com um gás inerte para remover quaisquer gases potencialmente tóxicos ou inflamáveis.
- Pare com qualquer aquecimento e deixe o sistema esfriar.
- Desconecte qualquer fita de aquecimento e o termopar.
- Desconecte as linhas de gás de entrada e saída.
- Solte os 6 parafusos na parte superior do dispositivo de exposição para comprometer o selo.
- Desprese as 2 seções de fixação e remova-as do dispositivo de exposição.
- Levante cuidadosamente a parte superior para cima e para fora da seção inferior.
- Use uma chave Allen para afrouxar o estágio do rotor e desenhá-lo com a haste roscada.
- Solte a porca no estágio do rotor e remova o rotor do componente do dispositivo.
- Pesar o rotor para garantir que as quantidades de gás desejadas estejam presentes.
4. Realização do experimento MAS NMR
- Coloque o rotor NMR na bobina NMR na sonda NMR.
- Levante a sonda no furo do ímã e bloqueie-a no lugar.
- Inicie a fiação da amostra usando a caixa de controle MAS e ajuste-se à taxa de rotação do rotor desejada.
- Use o computador para iniciar a sequência de sintonia/correspondência no canal desejado.
- Ajuste as configurações de ajuste/correspondência na sonda para otimizar a eletrônica da sonda.
- Saia da sequência de sintonia/correspondência no computador e configure os parâmetros experimentais desejados (por exemplo, sequência de pulso, matriz de experimento, temperatura, etc.).
- Colete os dados do MAS NMR.
Resultados
A saída do espectrômetro NMR assume a forma de uma decadência de indução livre (FID), que é o sinal de domínio de tempo das rodadas animadas à medida que relaxam de volta ao equilíbrio termodinâmico. Tal FID se assemelha à Figura 3. Quando Fourier se transformou do domínio temporal para o domínio de frequência (frequência para PPM pela Equação 3, pela qual a frequência absoluta e uma referência é dividida pela frequência portadora do espectrômetro NMR), representa o esp...
Discussão
O método de realização de medições espectroscópicas mas nmrescópicas aqui delineadas representa o estado da arte para a realização de NMR mas de alta temperatura e alta pressão. Tais métodos permitem a observação de interações ocorridas em atmosferas de vácuo até várias centenas de barras e de baixas temperaturas (bem abaixo de 0 °C a 250 °C) de forma confiável e reprodutível. A capacidade de sondar sistemas contendo misturas de sólidos, líquidos e gases em ambientes químicos flexíveis permite u...
Divulgações
Os autores declaram os seguintes interesses financeiros concorrentes. J.Z.H e colegas possuem uma patente sobre o design do rotor (US9151813B2). J.Z.H., N.R.J., et al. registraram um pedido de patente provisória no dispositivo de exposição.
Agradecimentos
A revisão das aplicações catalisadoras foi apoiada pelo Departamento de Energia dos EUA, Escritório de Ciência, Escritório de Ciências Básicas de Energia, Divisão de Ciências Químicas, Biociências e Programa de Catalise de Geociências sob contrato DE-AC05-RL01830 e FWP-47319. A revisão das aplicações biomédicas foi apoiada pelo Instituto Nacional de Saúde, Instituto Nacional de Ciências da Saúde Ambiental sob subvenção R21ES029778. Os experimentos foram realizados na EMSL (grid.436923.9), uma Instalação de Usuários do DoE Office of Science patrocinada pelo Escritório de Pesquisa Biológica e Ambiental e localizada no Pacific Northwest National Laboratory (PNNL). PNNL é um laboratório nacional multi-programa operado pela Battelle para o Departamento de Energia dos EUA sob contrato DE-AC05-RL01830 e FWP-47319.
Materiais
| Name | Company | Catalog Number | Comments |
| 1) Preparation of Solids Samples | |||
| Gas maniforld | |||
| Gas Mass Flow Controllers | |||
| Vacuum Pump | |||
| Tube Furnace | |||
| Temperature Controller | |||
| Thermocouple | |||
| Quartz Tube | |||
| Isolation Valves | |||
| Quartz Wool | |||
| 2) Loading solid samples into the rotor | |||
| Dry glove box | |||
| High-temperature, high-pressure NMR rotor | |||
| Sample funnel | |||
| Sample packing rod | |||
| Rotor holder | |||
| Analytical Balance | |||
| Microsyringe | |||
| Rotor cap bit | |||
| 3) Addition of gases to the rotor | |||
| NMR loading chamber | |||
| Rotor stage and appropriately sized inserts | |||
| Vacuum Pump | |||
| Gas maniforld | |||
| Gas Mass Flow Controllers | |||
| Vacuum Pump | |||
| Heating Tape | |||
| Temperature Controller | |||
| Thermocouple | |||
| Allen wrench | |||
| Threaded rod | |||
| Wrenchs | |||
| Pressure Gauge | |||
| High-pressure syringe pump | |||
| Liquid syringe pump | |||
| 4) Conducting the NMR experiments | |||
| MAS NMR probe | |||
| NMR spectrometer | |||
| Computer to control the spectrometer |
Referências
- Andrew, E. R., Bradbury, A., Eades, R. G. Nuclear Magnetic Resonance Spectra from a Crystal rotated at High Speed. Nature. 182 (4650), 1659 (1958).
- Lowe, I. J. Free Induction Decays of Rotating Solids. Physical Review Letters. 2 (7), 285-287 (1959).
- Frydman, L., Grant, D. M., Harris, R. K. Fundamentals of Multiple-Quantum Magic-Angle Spinning NMR on Half-Integer Quadrupolar Nuclei. Encyclopedia of Nuclear Magnetic Resonance. 9, 262-274 (2002).
- Khodov, I., Dyshin, A., Efimov, S., Ivlev, D., Kiselev, M. High-pressure NMR spectroscopy in studies of the conformational composition of small molecules in supercritical carbon dioxide. Journal of Molecular Liquids. 309, (2020).
- Kolbe, F. High-Pressure in situ 129Xe NMR Spectroscopy: Insights into Switching Mechanisms of Flexible Metal-Organic Frameworks Isoreticular to DUT-49. Chemistry of Materials. 31 (16), 6193-6201 (2019).
- Ochoa, G., et al. (2) H and (139) La NMR Spectroscopy in Aqueous Solutions at Geochemical Pressures. Angewandte Chemie International Edition. 54 (51), 15444-15447 (2015).
- Hoffmann, H. C., et al. High-pressure in situ 129Xe NMR spectroscopy and computer simulations of breathing transitions in the metal-organic framework Ni2(2,6-ndc)2(dabco) (DUT-8(Ni)). Journal of the American Chemical Society. 133 (22), 8681-8690 (2011).
- Turcu, R. V. F., et al. Rotor design for high pressure magic angle spinning nuclear magnetic resonance. Journal of Magnetic Resonance. 226, 64-69 (2013).
- Jaegers, N. R., Hu, M. Y., Hoyt, D. W., Wang, Y., Hu, J. Z. Development and Application of In situ High-Temperature, High-Pressure Magic Angle Spinning NMR. Modern Magnetic Resonance. , 1-19 (2017).
- Miyoshi, T., Takegoshi, K., Terao, T. 13C High-Pressure CPMAS NMR Characterization of the Molecular Motion of Polystyrene Plasticized by CO2 Gas. Macromolecules. 30 (21), 6582-6585 (1997).
- Miyoshi, T., Takegoshi, K., Terao, T. 129Xe n.m.r. study of free volume and phase separation of the polystyrene/poly(vinyl methyl ether) blend. Polymer. 38 (21), 5475-5480 (1997).
- Miyoshi, T., Takegoshi, K., Terao, T. Effects of Xe Gas on Segmental Motion in a Polymer Blend As Studied by 13C and 129Xe High-Pressure MAS NMR. Macromolecules. 35 (1), 151-154 (2002).
- Yonker, C. R., Linehan, J. C. The use of supercritical fluids as solvents for NMR spectroscopy. Progress in Nuclear Magnetic Resonance Spectroscopy. 47 (1), 95-109 (2005).
- Deuchande, T., Breton, O., Haedelt, J., Hughes, E. Design and performance of a high pressure insert for use in a standard magic angle spinning NMR probe. Journal of Magnetic Resonance. 183 (2), 178-182 (2006).
- Hoyt, D. W., et al. High-pressure magic angle spinning nuclear magnetic resonance. Journal of Magnetic Resonance. 212 (2), 378-385 (2011).
- Vjunov, A., et al. Following Solid-Acid-Catalyzed Reactions by MAS NMR Spectroscopy in Liquid Phase-Zeolite-Catalyzed Conversion of Cyclohexanol in Water. Angewandte Chemie International Edition. 53 (2), 479-482 (2014).
- Chamas, A., et al. High temperature/pressure MAS-NMR for the study of dynamic processes in mixed phase systems. Magnetic Resonance Imaging. 56, 37-44 (2019).
- Hu, J. Z., et al. Sealed rotors for in situ high temperature high pressure MAS NMR. ChemComm. 51 (70), 13458-13461 (2015).
- Hu, J. Z., Hu, M. Y., Townsend, M. R., Lercher, J. A., Peden, C. H. High-pressure, high-temperature magic angle spinning nuclear magnetic resonance devices and processes for making and using same. US patent. , (2015).
- Jaegers, N. R., Mueller, K. T., Wang, Y., Hu, J. Z. Variable Temperature and Pressure Operando MAS NMR for Catalysis Science and Related Materials. Accounts of Chemical Research. 53 (3), 611-619 (2020).
- Dagle, V., et al. Single-step Conversion of Ethanol to n-butenes over Ag-ZrO2/SiO2 catalysts. ACS Catalysis. 10 (18), 10602-10613 (2020).
- Jaegers, N. R., Wang, Y., Hu, J. Z. Thermal perturbation of NMR properties in small polar and non-polar molecules. Scientific Reports UK. 10 (1), 6097 (2020).
- Jaegers, N. R. . Applications of In situ Magnetic Resonance Spectroscopy for Structural Analysis of Oxide-supported Catalysts. , (2019).
- Mehta, H. S., et al. A novel high-temperature MAS probe with optimized temperature gradient across sample rotor for in-situ monitoring of high-temperature high-pressure chemical reactions. Solid State Nuclear Magnetic Resonance. 102, 31-35 (2019).
- Hu, J. Z., et al. A large sample volume magic angle spinning nuclear magnetic resonance probe for in situ investigations with constant flow of reactants. Physical Chemistry Chemical Physics. 14 (7), 2137-2143 (2012).
- Jiang, Y., et al. In situ MAS NMR-UV/Vis investigation of H-SAPO-34 catalysts partially coked in the methanol-to-olefin conversion under continuous-flow conditions and of their regeneration. Microporous and Mesoporous Materials. 105 (1-2), 132-139 (2007).
- Xu, S., Zhang, W., Liu, X., Han, X., Bao, X. Enhanced In situ Continuous-Flow MAS NMR for Reaction Kinetics in the Nanocages. Journal of the American Chemical Society. 131 (38), 13722-13727 (2009).
- Graham, T. R., et al. In situ Al-27 NMR Spectroscopy of Aluminate in Sodium Hydroxide Solutions above and below Saturation with Respect to Gibbsite. Inorganic Chemistry. 57 (19), 11864-11873 (2018).
- Zhang, X., et al. Boehmite and Gibbsite Nanoplates for the Synthesis of Advanced Alumina Products. ACS Applied Nano Materials. 1 (12), 7115-7128 (2018).
- Zhang, X., et al. Transformation of Gibbsite to Boehmite in Caustic Aqueous Solution at Hydrothermal Conditions. Crystal Growth & Design. 19 (10), 5557-5567 (2019).
- Hu, J. Z., Jaegers, N. R., Hu, M. Y., Mueller, K. T. In situ and ex situ NMR for battery research. Journal of Physics: Condensed Matter. 30 (46), (2018).
- Hu, J. Z., et al. Adsorption and Thermal Decomposition of Electrolytes on Nanometer Magnesium Oxide: An in situ C-13 MAS NMR Study. ACS Applied Materials & Interfaces. 11 (42), 38689-38696 (2019).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados