È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Spettroscopia di risonanza magnetica nucleare rotante ad alta temperatura e alta pressione in situ
In questo articolo
Riepilogo
Le strutture molecolari e la dinamica di solidi, liquidi, gas e miscele sono di interesse critico per diversi campi scientifici. MAS NMR MAS ad alta temperatura e alta pressione in situ consente di rilevare l'ambiente chimico dei costituenti in sistemi a fase mista in ambienti chimici strettamente controllati.
Abstract
La spettroscopia a risonanza magnetica nucleare (NMR) rappresenta una tecnica importante per comprendere la struttura e gli ambienti di legame delle molecole. Esiste un'unità per caratterizzare i materiali in condizioni rilevanti per il processo chimico di interesse. Per affrontare questo problema, sono stati sviluppati metodi MAS NMR ad alta pressione ad alta temperatura in situ per consentire l'osservazione delle interazioni chimiche su una gamma di pressioni (vuoto a diverse centinaia di bar) e temperature (ben al di sotto di 0 °C a 250 °C). Inoltre, l'identità chimica dei campioni può essere costituita da solidi, liquidi e gas o miscele dei tre. Il metodo incorpora rotori NMR all-zirconia (portacampioni per MAS NMR) che possono essere sigillati utilizzando un tappo filettato per comprimere un O-ring. Questo rotore presenta una grande resistenza chimica, compatibilità di temperatura, basso background NMR e può resistere ad alte pressioni. Questi fattori combinati consentono di utilizzarlo in una vasta gamma di combinazioni di sistemi, che a loro volta ne consentono l'uso in diversi campi come sequestro del carbonio, catalisi, scienza dei materiali, geochimica e biologia. La flessibilità di questa tecnica lo rende un'opzione attraente per gli scienziati di numerose discipline.
Introduzione
L'analisi spettroscopica dei campioni è uno strumento analitico utilizzato per ottenere preziose informazioni su materiali di interesse come il loro stato chimico, struttura o reattività. In una visione semplicistica, la risonanza magnetica nucleare (NMR) è una di queste tecnologie che utilizza un forte campo magnetico per manipolare lo stato di spin dei nuclei atomici per comprendere meglio l'ambiente chimico delle specie di interesse. Lo stato di spin nucleare si riferisce alla direzione relativa del momento magnetico indotta dal moto del nucleo rotante, una particella carica positivamente. In assenza di un campo magnetico, gli spin nucleari sono orientati casualmente ma in presenza di un campo magnetico, i giri nucleari si allineano preferenzialmente con il campo esterno del magnete in uno stato di spin a bassa energia. Questa divisione degli stati di spin in valori energetici discreti è nota come effetto Zeeman. La differenza tra questi livelli di energia (ΔE) è modellata dall'equazione 1:
dove h è la costante di Plank, B0 è la forza del campo magnetico esterno e γ è il rapporto giromagnetico del nucleo. L'ambiente chimico di questi spin applica anche lievi perturbazioni a questi livelli di energia. Le onde radio delle frequenze corrispondenti possono essere usate per eccitare i nuclei, che generano una magnetizzazione trasversale a causa degli spin che guadagnano coerenza di fase poiché la magnetizzazione longitudinale (basata sulla popolazione di giri in stati paralleli e anti-paralleli) è diminuita. Mentre i nuclei continuano a precessione attorno all'asse del campo magnetico, il movimento magnetico rotante crea un campo magnetico che ruota e genera anche un campo elettrico. Questo campo modula gli elettroni nella bobina di rilevamento NMR, generando il segnale NMR. Lievi differenze nell'ambiente chimico dei nuclei nel campione influenzano le frequenze rilevate nella bobina.
L'analisi NMR di campioni solidi introduce complessità non trovate nei fluidi. Nei fluidi, le molecole cadono a velocità elevate, calcolando la media dell'ambiente chimico spazialmente attorno ai nuclei. Nei campioni solidi, tale effetto medio non si verifica, introducendo un ambiente chimico dipendente dall'orientamento e ampie linee spettrali nel segnale NMR. Per mitigare queste sfide, viene utilizzata una tecnica nota come rotazione dell'angolo magico (MAS)1,2. Nel MAS NMR, i campioni vengono rapidamente ruotati (diversi kilohertz) con un angolo di 54,7356° rispetto al campo magnetico esterno utilizzando un meccanismo di rotazione esterno per affrontare le interazioni anisotropiche (anisotropiche) dell'NMR. Questo restringe sostanzialmente le caratteristiche nmr e migliora la risoluzione spettrale calcolando la media dei termini dipendenti dall'orientamento dell'anisotropia dello spostamento chimico, delle interazioni dipolari e delle interazioni quadrupolari. Due eccezioni degne di nota ostacolano le capacità di restringimento della linea di MAS NMR. Il primo è un forte accoppiamento omonucleare a volte presente in 1NMR H che richiede alte velocità di rotazione (~ 70 kHz) per rimuovere. Tuttavia, le temperature significativamente elevate delle applicazioni ad alta temperatura sopprimono notevolmente l'interazione omonucleare 1H impartendo un movimento termico migliorato in modo tale che una velocità di rotazione del campione molto ridotta possa essere utilizzata per una risoluzione spettrale significativamente migliorata. Inoltre, con la tecnologia in continua evoluzione, i rotori con diametri più piccoli possono ora essere fabbricati per raggiungere velocità di rotazione di gran lunga superiori a 5 kHz, il che aiuta a sopprimere ulteriormente le interazionidipolari omonucleari da 1 H. La seconda eccezione sono le interazioni quadrupolari residue di secondo ordine per i nuclei con spin che superano la metà poiché solo il termine del primo ordine viene eliminato con l'angolo magico, lasciando forme di linea più complesse che possono essere migliorate solo da campi magnetici esterni più forti. Va sottolineato che le tecniche MQMAS 2D possono essere prontamente incorporate nella tecnologia attuale in modo che un vero spettro di spostamento chimico isotropo possa essere ottenuto in modo simile agli esperimenti MQMAS standard3.
MAS NMR ha permesso una caratterizzazione dettagliata dei materiali solidi, rafforzando la qualità delle osservazioni. Tuttavia, la necessità di ruotare i campioni nei rotori NMR (il detentore del campione) a tassi elevati impone anche sfide nello svolgimento di esperimenti a temperature e pressioni elevate che possono essere più rilevanti per le condizioni di interesse. A volte può essere auspicabile esaminare i materiali in condizioni relativamente difficili per i rotori NMR. Una serie di sforzi hanno adattato con successo le tecnologie NMR allo stato liquido per condurre NMR4,5, 6,7adalta temperaturaead alta pressione; tuttavia, i tappi del rotore commerciali utilizzati per il MAS NMR allo stato solido possono essere espulsi dal rotore ad alte pressioni, causando danni significativi all'apparecchiatura. Tali effetti possono essere aggravati esaminando una reazione di decomposizione che aumenta notevolmente la pressione nel detentore del campione. Pertanto, sono necessari nuovi progetti per condurre in modo efficace e sicuro esperimenti NMR in situ. Ad esempio, il rotore deve aderire a diverse qualità per un uso efficace in MAS NMR, vale a dire non magnetico, leggero, resistente, resistente alla temperatura, materiale di fondo NMR basso, sigillabile, ad alta resistenza e resistente alle sostanze chimiche. Le pressioni che il rotore deve sopportare sono piuttosto grandi. Non solo il rotore deve sopportare la pressione del campione contenuto all'interno (ad esempio, gas ad alta pressione), ma la rotazione del dispositivo conferisce forza centrifuga che ha il suo contributo alla pressione totale delsistema 8, PT, dall'equazione 2: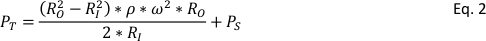
RI e RO sono i raggi del rotore interno ed esterno, rispettivamente, ω è la frequenza di rotazione nei radianti al secondo, e P sè la pressione del campione.
Sono state sviluppate diverse strategie per affrontare tali preoccupazioni9. I primi esempi assomigliavano a tubisigillati a fiamma 10,11,12 o inserti polimerici13,14,che erano insufficienti per un funzionamento esteso e controllato finemente a temperature e pressioni elevate. Le iterazioni ai progetti del rotore hanno sofferto di limitazioni nella temperatura massima di esercizio impartita dall'uso di riduzioni del volume epossidico o del campione dagliinserti ceramici 8,15,16. Una tecnologia recente riduce i costi di produzione unitari utilizzando semplici caratteristiche snap-in in un manicotto del rotore commerciale, ma offre un controllo relativamente minore sulle condizioni con cuipuò operare 17. Il design utilizzato nel presente documento è un manicotto del rotore in stile caverna all-zirconia fresato con una top18 filettata. Un cappuccio è anche filettato per consentire una tenuta sicura. La filettatura inversa impedisce alla rotazione del campione di allentare il tappo di zirconia e un O-ring costituisce le superfici di tenuta. Questo design del rotore è visibile nella figura 1 e rotori e istruzioni simili per farli sono stati brevettati19. Tale strategia consente un'elevata resistenza meccanica, resistenza chimica e tolleranza alla temperatura.
Questi progetti sono adatti per temperature e pressioni di almeno 250 °C e 100 bar, limitate in temperatura dalla tecnologia della sonda NMR prontamente disponibile. Se combinato con attrezzature specializzate per la preparazione dei campioni, rappresenta una tecnica davvero potente che è stata utilizzata per applicazioni di vasta portata come sequestro del carbonio, catalisi, accumulo di energia e biomedicina20. Tali attrezzature includono un modo per pretrattare i materiali solidi per rimuovere specie superficiali indesiderate come l'acqua. Per questo passaggio viene spesso utilizzato un forno. Una scatola asciutta viene in genere utilizzata per caricare i campioni solidi nel rotore NMR. Da lì, il rotore viene trasferito in un dispositivo di esposizione che consente al rotore di essere aperto sotto un'atmosfera strettamente controllata per caricare un gas o una miscela desiderati nel rotore. Tale dispositivo è raffigurato nella figura 2.
Protocollo
Il protocollo è diviso in quattro sezioni che specificano 1) la preparazione di tutti i materiali solidi utilizzati nel sistema o l'attivazione o lo sgombero di specie adsorbenti indesiderate, 2) l'aggiunta dei materiali solidi e liquidi al rotore NMR, 3) l'aggiunta di gas al rotore e 4) la conduzione degli esperimenti NMR nello spettrometro. La procedura è rappresentativa di una sequenza tipica, ma può essere modificata per adattarsi alle esigenze specifiche dell'esperimento.
1. Pretrattare campioni solidi
- Pesare circa il doppio della massa del campione solido desiderato per l'esperimento NMR (per un rotore da 7,5 mm, ~250 mg) e posizionare il campione solido in un tubo campione di quarzo utilizzato per il trattamento dei materiali in un sistema di forno, collegando il tubo con la lana di quarzo per mantenere il materiale in posizione.
- Collegare le valvole di isolamento al trattamento dei solidi 1) flusso o 2) sistema di vuoto posizionando il tubo nel forno freddo e stringendo i collegamenti.
- Apporre le estremità del tubo di quarzo sulle valvole di isolamento del gas in posizione aperta.
- Inizia il trattamento.
- Per i sistemi di flusso:
- Apporre una termocopia all'esterno del tubo, tenendola in posizione con un materiale resistente al calore.
- Iniziare il flusso del gas di trattamento (ad esempio, N2 a 100 sccm) per cancellare la superficie solida o attivare il materiale.
- In alternativa, per i sistemi sottovuoto:
- Chiudere la valvola di isolamento al sistema di vuoto e avviare la pompa per vuoto.
- Quando viene stabilito il vuoto completo, aprire molto lentamente la valvola di isolamento per applicare il vuoto al campione, fermandosi periodicamente per consentire al sistema di equilibrare. Continuare fino a quando la valvola non è aperta.
- Per i sistemi di flusso:
- Accendere il regolatore del forno e impostare il programma di rampa di temperatura sulla condizione desiderata (ad esempio, 300 °C per 4 ore a una velocità di rampa di 5 °C/min).
- Avviare il programma di temperatura e lasciarlo funzionare.
- Una volta completato, lasciare raffreddare il campione a una temperatura lavorabile.
- Spegnere il regolatore di temperatura e arrestare il flusso/vuoto.
- Sigillare rapidamente il campione con le valvole di isolamento per mantenere l'ambiente campione desiderato.
- Scollegare il tubo di quarzo dal sistema di trattamento e trasferire i tubi e le valvole chiuse nell'anticamera di una scatolaportaoggettiasciutta e epurata N 2.
- Svuotare e riempire l'anticamera almeno 4 volte e trasferire il tubo all'interno della scatola del guanto.
2. Caricamento di campioni solidi nel rotore NMR
- Pesare il rotore NMR ad alta pressione e ad alta temperatura vuoto e pulito con il tappo del rotore.
- Posizionare il rotore NMR nel supporto per mantenere la direzionalità.
- Posizionare l'imbuto campione nel foro del rotore.
- Rimuovere le valvole di isolamento dal tubo campione e versare una piccola quantità di materiale solido nell'imbuto.
- Toccare la polvere nell'imbuto e dirigerla leggermente nel rotore con l'asta di imballaggio, se necessario.
- Ripetere l'aggiunta graduale di materiale solido fino a raggiungere la quantità desiderata (ad esempio, 1/2 rotore).
- Pesare il rotore NMR (e il tappo) con il campione all'interno per determinare la quantità di campione aggiunto.
- Se lo si desidera, redigere una quantità specificata di qualsiasi campione liquido e iniettare lentamente il liquido al centro del rotore NMR con una micro siringa.
- Sigillare il rotore posizionando il tappo sulla parte superiore e ruotandolo in senso antiorario con il bit del tappo del rotore per innestare l'O-ring tra il rotore e il cappuccio. Si noti che un nuovo O-ring può essere periodicamente necessario per evitare perdite, specialmente se si utilizzano miscele chimicamente abrasive o piccoli gas come l'idrogeno.
- Pesare il rotore NMR per determinare la massa totale del campione aggiunto.
3. Ricaricare il rotore NMR con le sostanze chimiche desiderate alle condizioni desiderate
- Posizionare il rotore NMR sigillato nello stadio del rotore, assicurando che le dimensioni dell'inserto dello stadio siano compatibili con le dimensioni del rotore, e stringere il dado a mano per fissarlo in posizione. Si noti che la tenuta del rotore nel supporto in questo passaggio determinerà la tenuta della guarnizione del cappuccio.
- Abbassare lo stadio del rotore nella sezione inferiore del dispositivo di esposizione ad alta pressione.
- Utilizzare una chiave inglese Allen per ruotare una delle viti di 90° per fissare lo stadio del rotore nella parte inferiore del dispositivo di esposizione.
- Posizionare la sezione superiore del dispositivo di caricamento NMR in e sopra la sezione inferiore, allineando il bit del tappo NMR alla parte superiore della testa del tappo del rotore NMR per assicurarsi che sia inserito.
- Posizionare i 2 morsetti sopra la parte superiore del labbro in cui le sezioni superiore e inferiore del dispositivo di esposizione si incontrano e agganciarle in posizione.
- Stringere i 6 bulloni nella parte superiore della sezione superiore del dispositivo di esposizione per innestare la superficie di tenuta tra le sezioni superiore e inferiore.
- Collegare la sezione superiore del dispositivo di esposizione NMR all'ingresso e alle uscite della linea del gas.
- Collegare la termocopia sulla sezione superiore del dispositivo di esposizione NMR al sensore di temperatura.
- Se lo si desidera, avvolgere il nastro riscaldante intorno alle linee del gas e alle sezioni superiori del dispositivo di esposizione per consentire il riscaldamento con il rispettivo controller. Una piastra calda può anche essere impegnata.
- Assicurandosi che l'uscita della camera di esposizione sia aperta e che la valvola del gas sorgente sia chiusa, accendere la pompa del vuoto per rimuovere l'aria dal dispositivo di esposizione e dalle linee associate.
- Eliminare le linee con il gas desiderato o inerte, pedalando tre volte tra vuoto e pressione atmosferica per garantire che le linee siano liberate dall'aria.
- Preparare la composizione del gas desiderata da 1) un sistema di erogazione ad alta pressione o 2) un sistema di flusso per introdurre vapori a una pressione specificata.
- Per la preparazione di campioni ad alta pressione o sottovuoto:
- Chiudere l'uscita del gas del dispositivo di esposizione e impostare le valvole del collettore di gas per bypassare la linea di iniezione del liquido.
- Impostare la pressione desiderata sulla pompa siringa ad alta pressione del sistema di erogazione ad alta pressione.
- Aprire le valvole della fonte di gas sulla pompa della siringa ad alta pressione ed eseguire il programma impostato sulla pompa, monitorando la pressione reale all'interno del dispositivo di esposizione.
- Quando la pressione desiderata si ottiene all'interno del dispositivo di esposizione, arrestare la pompa della siringa e chiudere le valvole del gas sorgente.
- Aprire il rotore NMR ruotando in senso orario il meccanismo a vite esterno, che è accoppiato al bit interno del tappo NMR.
- Lasciare entrare il gas della pressione desiderata nel rotore NMR ed equilibrare.
- Ripiego il rotore NMR ruotando il meccanismo a vite esterno in senso antiorario. Una finestra di visualizzazione aiuterà a determinare quando il rotore è chiuso.
- Deprimere lentamente il sistema aprendo la valvola di uscita del gas del dispositivo di esposizione.
- Per la preparazione del campione di gas o vapore che scorre:
- Assicurarsi che l'uscita del gas del dispositivo di esposizione sia aperta per evitare una pressione eccessiva.
- Impostare la portata del gas desiderata sul regolatore di flusso di massa e iniziare il flusso di gas.
- Collegare la linea di alimentazione del liquido dalla pompa della siringa liquida al collettore di gas.
- Impostare le valvole del collettore di gas per consentire il flusso alla linea di iniezione del liquido.
- Impostare la portata del liquido sulla pompa della siringa liquida per ottenere la pressione di vapore desiderata e iniziare l'iniezione di liquido.
- Aprire il rotore NMR ruotando in senso orario il meccanismo a vite esterno accoppiato al bit interno del tappo NMR.
- Consentire al sistema di equilibrare le pressioni del gas desiderate all'interno del rotore NMR e di rigillare il rotore NMR ruotando il meccanismo a vite esterno in senso antiorario. Una finestra di visualizzazione aiuterà a determinare quando il rotore è chiuso.
- Interrompere l'iniezione della pompa della siringa liquida e configurare le valvole per bypassare la linea di iniezione del liquido, scollegando la pompa dal sistema.
- Fermare il gas che scorre.
- Per la preparazione di campioni ad alta pressione o sottovuoto:
- Spurgare il sistema con un gas inerte per rimuovere eventuali gas potenzialmente tossici o infiammabili.
- Interrompere qualsiasi riscaldamento e lasciare raffreddare l'impianto.
- Scollegare il nastro riscaldante e la termoscopia.
- Scollegare le linee del gas di ingresso e di uscita.
- Allentare i 6 bulloni sulla parte superiore del dispositivo di esposizione per compromettere la tenuta.
- Sganciare le 2 sezioni di bloccaggio e rimuoverle dal dispositivo di esposizione.
- Sollevare con cura la sezione superiore su e fuori dalla sezione inferiore.
- Utilizzare una chiave inglese Allen per allentare lo stadio del rotore e disegnarlo con l'asta filettata.
- Allentare il dado sullo stadio del rotore e rimuovere il rotore dal componente del dispositivo.
- Pesare il rotore per assicurarsi che siano presenti le quantità di gas desiderate.
4. Condurre l'esperimento MAS NMR
- Posizionare il rotore NMR nella bobina NMR sulla sonda NMR.
- Sollevare la sonda nel foro del magnete e bloccarla in posizione.
- Avviare la rotazione del campione utilizzando la casella di controllo MAS e regolare la velocità di rotazione del rotore desiderata.
- Utilizzare il computer per iniziare la sequenza di sintonizzazione/corrispondenza sul canale desiderato.
- Regolare le impostazioni di sintonizzazione/corrispondenza sulla sonda per ottimizzare l'elettronica della sonda.
- Uscire dalla sequenza di sintonizzazione/corrispondenza sul computer e impostare i parametri sperimentali desiderati (ad esempio, sequenza di impulsi, array di esperimenti, temperatura, ecc.).
- Raccogliere i dati MAS NMR.
Risultati
L'uscita dallo spettrometro NMR assume la forma di un decadimento a induzione libera (FID) che è il segnale del dominio del tempo dagli spin eccitati mentre si rilassano verso l'equilibrio termodinamico. Tale FID assomiglia alla figura 3. Quando Fourier si trasforma dal dominio del tempo al dominio della frequenza (frequenza a PPM dall'equazione 3, per cui la differenza frequenza assoluta e un riferimento sono divisi per la frequenza portante dello spettrometro NMR), rappresenta lo spettro ...
Discussione
Il metodo di conduzione delle misurazioni spettroscopiche MAS NMR descritte nel presente documento rappresenta lo stato dell'arte per condurre MAS NMR ad alta temperatura e alta pressione. Tali metodi consentono l'osservazione di interazioni che si verificano in atmosfere sottovuoto fino a diverse centinaia di bar e da basse temperature (ben al di sotto di 0 °C a 250 °C) in modo affidabile e riproducibile. La capacità di sondare sistemi contenenti miscele di solidi, liquidi e gas in ambienti chimici flessibili consent...
Divulgazioni
Gli autori dichiarano i seguenti interessi finanziari concorrenti. J.Z.H e colleghi detengono un brevetto sul design del rotore (US9151813B2). J.Z.H., N.R.J., et al.
Riconoscimenti
La revisione delle applicazioni catalizzatori è stata supportata dal Dipartimento dell'Energia degli Stati Uniti, dall'Office of Science, dall'Office of Basic Energy Sciences, dalla Division of Chemical Sciences, Biosciences, and Geosciences Catalysis Program con contratto DE-AC05-RL01830 e FWP-47319. La revisione delle applicazioni biomediche è stata sostenuta dal National Institute of Health, National Institute of Environmental Health Sciences nell'ambito della sovvenzione R21ES029778. Gli esperimenti sono stati condotti presso l'EMSL (grid.436923.9), un DOE Office of Science User Facility sponsorizzato dall'Office of Biological and Environmental Research e situato presso il Pacific Northwest National Laboratory (PNNL). PNNL è un laboratorio nazionale multi-programma gestito da Battelle per il Dipartimento dell'Energia degli Stati Uniti con contratto DE-AC05-RL01830 e FWP-47319.
Materiali
| Name | Company | Catalog Number | Comments |
| 1) Preparation of Solids Samples | |||
| Gas maniforld | |||
| Gas Mass Flow Controllers | |||
| Vacuum Pump | |||
| Tube Furnace | |||
| Temperature Controller | |||
| Thermocouple | |||
| Quartz Tube | |||
| Isolation Valves | |||
| Quartz Wool | |||
| 2) Loading solid samples into the rotor | |||
| Dry glove box | |||
| High-temperature, high-pressure NMR rotor | |||
| Sample funnel | |||
| Sample packing rod | |||
| Rotor holder | |||
| Analytical Balance | |||
| Microsyringe | |||
| Rotor cap bit | |||
| 3) Addition of gases to the rotor | |||
| NMR loading chamber | |||
| Rotor stage and appropriately sized inserts | |||
| Vacuum Pump | |||
| Gas maniforld | |||
| Gas Mass Flow Controllers | |||
| Vacuum Pump | |||
| Heating Tape | |||
| Temperature Controller | |||
| Thermocouple | |||
| Allen wrench | |||
| Threaded rod | |||
| Wrenchs | |||
| Pressure Gauge | |||
| High-pressure syringe pump | |||
| Liquid syringe pump | |||
| 4) Conducting the NMR experiments | |||
| MAS NMR probe | |||
| NMR spectrometer | |||
| Computer to control the spectrometer |
Riferimenti
- Andrew, E. R., Bradbury, A., Eades, R. G. Nuclear Magnetic Resonance Spectra from a Crystal rotated at High Speed. Nature. 182 (4650), 1659 (1958).
- Lowe, I. J. Free Induction Decays of Rotating Solids. Physical Review Letters. 2 (7), 285-287 (1959).
- Frydman, L., Grant, D. M., Harris, R. K. Fundamentals of Multiple-Quantum Magic-Angle Spinning NMR on Half-Integer Quadrupolar Nuclei. Encyclopedia of Nuclear Magnetic Resonance. 9, 262-274 (2002).
- Khodov, I., Dyshin, A., Efimov, S., Ivlev, D., Kiselev, M. High-pressure NMR spectroscopy in studies of the conformational composition of small molecules in supercritical carbon dioxide. Journal of Molecular Liquids. 309, (2020).
- Kolbe, F. High-Pressure in situ 129Xe NMR Spectroscopy: Insights into Switching Mechanisms of Flexible Metal-Organic Frameworks Isoreticular to DUT-49. Chemistry of Materials. 31 (16), 6193-6201 (2019).
- Ochoa, G., et al. (2) H and (139) La NMR Spectroscopy in Aqueous Solutions at Geochemical Pressures. Angewandte Chemie International Edition. 54 (51), 15444-15447 (2015).
- Hoffmann, H. C., et al. High-pressure in situ 129Xe NMR spectroscopy and computer simulations of breathing transitions in the metal-organic framework Ni2(2,6-ndc)2(dabco) (DUT-8(Ni)). Journal of the American Chemical Society. 133 (22), 8681-8690 (2011).
- Turcu, R. V. F., et al. Rotor design for high pressure magic angle spinning nuclear magnetic resonance. Journal of Magnetic Resonance. 226, 64-69 (2013).
- Jaegers, N. R., Hu, M. Y., Hoyt, D. W., Wang, Y., Hu, J. Z. Development and Application of In situ High-Temperature, High-Pressure Magic Angle Spinning NMR. Modern Magnetic Resonance. , 1-19 (2017).
- Miyoshi, T., Takegoshi, K., Terao, T. 13C High-Pressure CPMAS NMR Characterization of the Molecular Motion of Polystyrene Plasticized by CO2 Gas. Macromolecules. 30 (21), 6582-6585 (1997).
- Miyoshi, T., Takegoshi, K., Terao, T. 129Xe n.m.r. study of free volume and phase separation of the polystyrene/poly(vinyl methyl ether) blend. Polymer. 38 (21), 5475-5480 (1997).
- Miyoshi, T., Takegoshi, K., Terao, T. Effects of Xe Gas on Segmental Motion in a Polymer Blend As Studied by 13C and 129Xe High-Pressure MAS NMR. Macromolecules. 35 (1), 151-154 (2002).
- Yonker, C. R., Linehan, J. C. The use of supercritical fluids as solvents for NMR spectroscopy. Progress in Nuclear Magnetic Resonance Spectroscopy. 47 (1), 95-109 (2005).
- Deuchande, T., Breton, O., Haedelt, J., Hughes, E. Design and performance of a high pressure insert for use in a standard magic angle spinning NMR probe. Journal of Magnetic Resonance. 183 (2), 178-182 (2006).
- Hoyt, D. W., et al. High-pressure magic angle spinning nuclear magnetic resonance. Journal of Magnetic Resonance. 212 (2), 378-385 (2011).
- Vjunov, A., et al. Following Solid-Acid-Catalyzed Reactions by MAS NMR Spectroscopy in Liquid Phase-Zeolite-Catalyzed Conversion of Cyclohexanol in Water. Angewandte Chemie International Edition. 53 (2), 479-482 (2014).
- Chamas, A., et al. High temperature/pressure MAS-NMR for the study of dynamic processes in mixed phase systems. Magnetic Resonance Imaging. 56, 37-44 (2019).
- Hu, J. Z., et al. Sealed rotors for in situ high temperature high pressure MAS NMR. ChemComm. 51 (70), 13458-13461 (2015).
- Hu, J. Z., Hu, M. Y., Townsend, M. R., Lercher, J. A., Peden, C. H. High-pressure, high-temperature magic angle spinning nuclear magnetic resonance devices and processes for making and using same. US patent. , (2015).
- Jaegers, N. R., Mueller, K. T., Wang, Y., Hu, J. Z. Variable Temperature and Pressure Operando MAS NMR for Catalysis Science and Related Materials. Accounts of Chemical Research. 53 (3), 611-619 (2020).
- Dagle, V., et al. Single-step Conversion of Ethanol to n-butenes over Ag-ZrO2/SiO2 catalysts. ACS Catalysis. 10 (18), 10602-10613 (2020).
- Jaegers, N. R., Wang, Y., Hu, J. Z. Thermal perturbation of NMR properties in small polar and non-polar molecules. Scientific Reports UK. 10 (1), 6097 (2020).
- Jaegers, N. R. . Applications of In situ Magnetic Resonance Spectroscopy for Structural Analysis of Oxide-supported Catalysts. , (2019).
- Mehta, H. S., et al. A novel high-temperature MAS probe with optimized temperature gradient across sample rotor for in-situ monitoring of high-temperature high-pressure chemical reactions. Solid State Nuclear Magnetic Resonance. 102, 31-35 (2019).
- Hu, J. Z., et al. A large sample volume magic angle spinning nuclear magnetic resonance probe for in situ investigations with constant flow of reactants. Physical Chemistry Chemical Physics. 14 (7), 2137-2143 (2012).
- Jiang, Y., et al. In situ MAS NMR-UV/Vis investigation of H-SAPO-34 catalysts partially coked in the methanol-to-olefin conversion under continuous-flow conditions and of their regeneration. Microporous and Mesoporous Materials. 105 (1-2), 132-139 (2007).
- Xu, S., Zhang, W., Liu, X., Han, X., Bao, X. Enhanced In situ Continuous-Flow MAS NMR for Reaction Kinetics in the Nanocages. Journal of the American Chemical Society. 131 (38), 13722-13727 (2009).
- Graham, T. R., et al. In situ Al-27 NMR Spectroscopy of Aluminate in Sodium Hydroxide Solutions above and below Saturation with Respect to Gibbsite. Inorganic Chemistry. 57 (19), 11864-11873 (2018).
- Zhang, X., et al. Boehmite and Gibbsite Nanoplates for the Synthesis of Advanced Alumina Products. ACS Applied Nano Materials. 1 (12), 7115-7128 (2018).
- Zhang, X., et al. Transformation of Gibbsite to Boehmite in Caustic Aqueous Solution at Hydrothermal Conditions. Crystal Growth & Design. 19 (10), 5557-5567 (2019).
- Hu, J. Z., Jaegers, N. R., Hu, M. Y., Mueller, K. T. In situ and ex situ NMR for battery research. Journal of Physics: Condensed Matter. 30 (46), (2018).
- Hu, J. Z., et al. Adsorption and Thermal Decomposition of Electrolytes on Nanometer Magnesium Oxide: An in situ C-13 MAS NMR Study. ACS Applied Materials & Interfaces. 11 (42), 38689-38696 (2019).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon