Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Membranes échangeuses d’ions pour la fabrication d’un dispositif d’électrodialyse inverse
Dans cet article
Résumé
Nous démontrons la fabrication d’un dispositif d’électrodialyse inverse utilisant une membrane échangeuse de cations (CEM) et une membrane échangeuse d’anions (AEM) pour la production d’énergie.
Résumé
L’électrodialyse inverse (RED) est un moyen efficace de générer de l’énergie en mélangeant deux concentrations de sel différentes dans l’eau à l’aide de membranes échangeuses de cations (CEM) et de membranes échangeuses d’anions (AEM). La pile RED est composée d’un arrangement alternatif de la membrane échangeuse de cations et de la membrane échangeuse d’anions. Le dispositif RED agit comme un candidat potentiel pour répondre à la demande universelle pour les futures crises énergétiques. Ici, dans cet article, nous démontrons une procédure pour fabriquer un dispositif d’électrodialyse inverse à l’aide de CEM et d’AEM à l’échelle du laboratoire pour la production d’énergie. La zone active de la membrane échangeuse d’ions est de 49 cm2. Dans cet article, nous fournissons une procédure étape par étape pour synthétiser la membrane, suivie de l’assemblage de la pile et de la mesure de puissance. Les conditions de mesure et le calcul de la puissance nette de sortie ont également été expliqués. En outre, nous décrivons les paramètres fondamentaux qui sont pris en considération pour obtenir un résultat fiable. Nous fournissons également un paramètre théorique qui affecte les performances cellulaires globales relatives à la membrane et à la solution d’alimentation. En bref, cette expérience décrit comment assembler et mesurer des cellules ROUGES sur la même plate-forme. Il contient également le principe de fonctionnement et le calcul utilisés pour estimer la puissance nette de sortie de la pile RED à l’aide des membranes CEM et AEM.
Introduction
La récupération d’énergie à partir des ressources naturelles est une méthode économique respectueuse de l’environnement, rendant ainsi notre planète verte et propre. Plusieurs procédés ont été proposés jusqu’à présent pour extraire de l’énergie, mais l’électrodialyse inverse (RED) a un potentiel énorme pour surmonter le problème de la crise énergétique1. La production d’énergie à partir de l’électrodialyse inverse est une percée technologique pour la décarbonisation de l’énergie mondiale. Comme son nom l’indique, RED est un processus inverse, où le compartiment de la cellule alternative est rempli de la solution saline hautement concentrée et de la solution saline faiblement concentrée2. Le potentiel chimique généré par la différence de concentration en sel à travers les membranes échangeuses d’ions, recueilli à partir des électrodes à l’extrémité du compartiment.
Depuis l’an 2000, de nombreux articles de recherche ont été publiés, donnant un aperçu de la RED théoriquement et expérimentalement3,4. Des études systématiques sur les conditions de fonctionnement et des études de fiabilité dans des conditions de stress ont amélioré l’architecture de la pile et amélioré les performances globales des cellules. Plusieurs groupes de recherche ont détourné leur attention vers l’application hybride de RED, tels que RED avec procédé de dessalement5,RED avec énergie solaire6,RED avec procédé d’osmose inverse (RO)5,RED avec la pile à combustible microbienne7,et RED avec le procédé de refroidissement radiatif8. Comme mentionné précédemment, il y a beaucoup de place dans la mise en œuvre de l’application hybride de RED pour résoudre le problème de l’énergie et de l’eau propre.
Plusieurs méthodes ont été adoptées pour améliorer les performances de la cellule ROUGE et la capacité d’échange d’ions de la membrane. L’adaptation des membranes échangeuses de cations avec différents typesd’ions en utilisant le groupe acide sulfonique (-SO3 H), le groupe acide phosphonique (-PO3H2) et le groupe acide carboxylique (-COOH) est l’un des moyens efficaces de modifier les propriétés physico-chimiques de la membrane. Les membranes échangeuses d’anions sont adaptées aux groupes ammonium ( 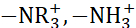 )9. La conductivité ionique élevée de l’AEM et du CEM sans détériorer la résistance mécanique de la membrane est le paramètre essentiel pour choisir une membrane appropriée pour l’application du dispositif. La membrane robuste dans des conditions de contrainte fournit une stabilité mécanique à la membrane et améliore la durabilité de l’appareil. Ici, une combinaison unique de poly sulfoné autonome haute performance (éther éther cétone) (sPEEK) en tant que membranes échangeuses de cations avec FAA-3 comme membranes échangeuses d’anions est utilisée dans l’application RED. La figure 1 montre l’organigramme de la procédure expérimentale.
)9. La conductivité ionique élevée de l’AEM et du CEM sans détériorer la résistance mécanique de la membrane est le paramètre essentiel pour choisir une membrane appropriée pour l’application du dispositif. La membrane robuste dans des conditions de contrainte fournit une stabilité mécanique à la membrane et améliore la durabilité de l’appareil. Ici, une combinaison unique de poly sulfoné autonome haute performance (éther éther cétone) (sPEEK) en tant que membranes échangeuses de cations avec FAA-3 comme membranes échangeuses d’anions est utilisée dans l’application RED. La figure 1 montre l’organigramme de la procédure expérimentale.
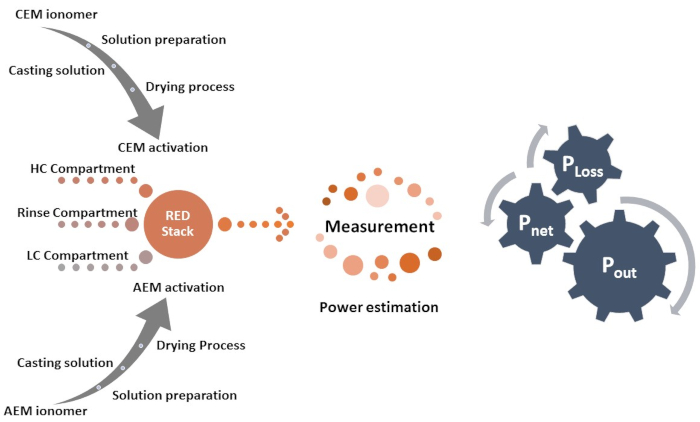
Figure 1: Tableau des procédures. L’organigramme présente la procédure adoptée pour la préparation de la membrane échangeuse d’ions suivie du processus de mesure de l’électrodialyse inverse. Veuillez cliquer ici pour voir une version plus grande de cette figure.
Protocole
1. Exigence expérimentale
- Achetez un polymère ionomère échangeur d’ions, une fibre polymère E-550 sulfonée-PEEK pour préparer le CEM et FAA-3 pour préparer AEM. Assurez-vous que tous les polymères ionomères sont entreposés dans un environnement propre, sec et exempt de poussière avant utilisation.
- Utiliser des solvants de haute pureté (>99%), y compris la N-méthyl-2-pyrrolidone avec un poids moléculaire de 99,13 g mol-1 et N, le N-diméthylacétamide de poids moléculaire 87,12, pour préparer une solution d’ionomère homogène. S’assurer que tous les produits chimiques et solvants de qualité analytique sont utilisés pour la préparation de la membrane telle qu’elle a été reçue sans autre purification.
- Après le processus d’activation des membranes, plongez immédiatement toutes les membranes dans une solution de NaCl 0,5 M pour de meilleures performances. Après activation des deux membranes, le séchage n’est pas nécessaire. De l’eau avec résistivité est de 18,2 MΩ à température ambiante a été utilisée tout au long de la synthèse de la membrane.
- Caractériser les propriétés de la membrane à l’aide d’une membrane sèche. La description détaillée des techniques de caractérisation et de leurs propriétés physicochimiques telles que la capacité d’échange d’ions, la conductivité ionique, l’épaisseur, l’analyse thermique et la morphologie de surface, est telle que présentée dans les littératures10,11.
- Utilisez un outil pour façonner la membrane pour CEM et AEM à la taille de la pile RED avec une zone active de 49 cm2,comme illustré à la figure 2.
- Pour la fabrication de la pile RED, faites une autre disposition CEM et AEM, séparées par une entretoise et un joint; une image réelle de la pile RED de travail est présentée à la figure 3a,et son schéma schématique de chaque couche est illustré à la figure 3b.
- Tout d’abord, placez la plaque PMMA face à l’électrode à l’envers; maintenant, placez le joint en caoutchouc et l’entretoise dessus, puis placez le CEM. Après cela, placez le joint en silicone avec l’entretoise sur le CEM, puis placez l’AEM dessus. De même, ajoutez le joint en silicium et l’entretoise sur le dessus d’AEM suivis de CEM. Maintenant, placez la plaque PMMA d’extrémité, le joint en caoutchouc et l’entretoise suivis d’un serrage à l’aide de boulons à vis et à écrou.
- Après avoir assemblé la pile RED, vérifiez la libre circulation de la concentration élevée (HC), de la faible concentration (LC) et rincez les solutions une par une. Tout flux transversal ou fuite doit être éliminé avant la mesure.
- Avant la mesure du courant et de la tension, surveillez le débit des solutions salines et la lecture du manomètre et assurez-vous qu’il est stabilisé. Assurez-vous que toutes les connexions sont à l’endroit exact avant le début de la mesure. Évitez de toucher la pile RED et ses tubes de connexion pendant que la mesure est en cours d’exécution.
NOTA : Les solutions HC et LC s’écoulent de leurs compartiments pour se jeter à travers une pompe péristaltique, un manomètre et une cheminée ROUGE, respectivement. - Utilisez la méthode galvanostat pour la mesure du courant et de la tension, l’instrument de compteur source connecté à la pile RED par des clips crocodile.

Figure 2: Taille et forme de la membrane, du joint et de l’entretoise préparés pour la fabrication de l’électrodialyse inverse. (a) joint extérieur en silicone, (b) espacement extérieur et entretoise intérieure, (c) joint intérieur en silicone, (d) membrane échangeuse de cations, (e) membrane échangeuse d’anions et (f) joint et assemblage membrane. Veuillez cliquer ici pour voir une version plus grande de cette figure.
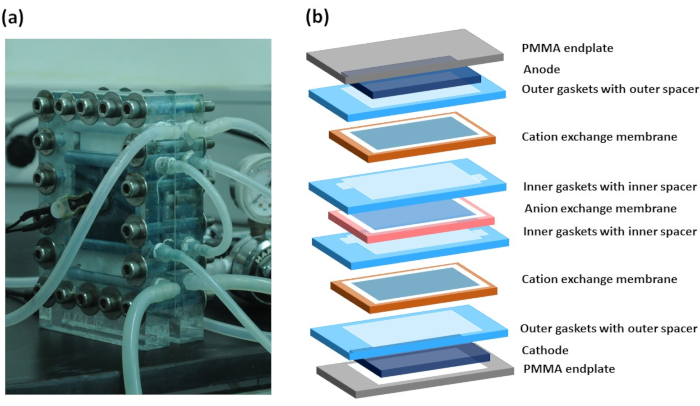
Figure 3: Pile d’électrodialyse inverse. (a)configuration de la cheminée d’électrodialyse inverse avec tubes de connexion, et(b)illustration schématique de différentes couches, y compris les plaques d’extrémité PMMA, électrodes, joint, entretoise, CEM et AEM. Veuillez cliquer ici pour voir une version plus grande de cette figure.
2. Préparation de membrane échangeuse d’ions
REMARQUE: La quantité de matériau précurseur a été optimisée pour obtenir une membrane de 18 cm de diamètre et d’une épaisseur d’environ 50 μm.
-
Membrane échangeuse de cations
- Prendre 5% en poids de fibres sulfonées-PEEK dans une fiole inférieure ronde de 250 mL et dissoudre les fibres dans du Diméthylacétamide (DMAc) comme solvant ayant un poids moléculaire de 87,12 g mol-1. Agiter le ballon pendant 10 min afin que tous les polymères ionomères se déposent.
- Placer une barre magnétique dans le ballon, puis maintenir le mélange dans le bain d’huile de silicium, puis agiter vigoureusement à 500 tr/min pendant 24 h à 80 °C pour obtenir une solution homogène.
- Filtrer la solution de PEEK sulfoné à travers un filtre de polytétrafluoroéthylène (PTFE) de 0,45 μm de la taille des pores.
- Après cela, versez la solution filtrée sur un plat circulaire en verre d’un diamètre de 18 cm. Assurez-vous que toutes les bulles d’air sont éliminées à l’aide d’un ventilateur d’air avant de placer la boîte de Petri dans le four.
- Placer la boîte de Petri à l’intérieur d’un four pour dessécher la solution à 90 °C pendant 24 h, ce qui donne une membrane autoportante d’environ 50 μm d’épaisseur. Faites ceci pour extraire la membrane autoportante: Pour décoller la membrane de la boîte de Petri, remplissez la boîte de Pétri avec de l’eau distillée tiède (~ 60 ° C) et laissez-la reposer pendant 10 minutes intactes. La membrane autoportante sortira automatiquement.
- Pour l’activation de la membrane, immerger la membrane autoportante préparée dansunesolution aqueuse d’acide sulfurique 1 M (H2SO4), soit 98,08 g, dans 1 L d’eau distillée, et incuber pendant 2 h à 80 °C.
REMARQUE: Cette étape assurera l’élimination des particules étrangères et d’autres produits chimiques tels que les solvants qui réditeront la possibilité d’encrassement de la membrane. - Laver la membrane trempée avec 1 L d’eau distillée pendant 10 min, au moins trois fois à température ambiante.
- Membrane échangeuse d’anions
- Dissoudre la solution d’ionomère FAA-3 10 % en poids dans un solvant de N-méthyl-2-pyrrolidone (NMP).
- Conserver la solution pour l’agitation à température ambiante pendant 2 h à ~500 tr/min.
- Après cela, filtrez la solution à l’aide du maillage avec une taille de pores de 100 μm.
- Verser ~30 mL de solution filtrée dans une boîte de Pétri circulaire en verre d’un diamètre de 18 cm. Assurez-vous que toutes les bulles d’air ont été enlevées à l’aide d’un ventilateur d’air avant de placer la boîte de Petri en verre dans le four. Le séchage se déroule à 100 °C pendant 24 h.
- Pour obtenir une membrane autoportante, versez de l’eau distillée chaude dans la boîte de Petri en verre et conservez-la pendant au moins 10 min. Maintenant, décollez les membranes et placez dans 1 litre de solution d’hydroxyde de sodium (NaOH) (concentration 1M et poids moléculaire 40 g mol-1)pendant 2 h.
- Ensuite, lavez soigneusement la membrane avec 1 L d’eau distillée pendant 10 min, au moins trois fois dans des conditions ambiantes.
REMARQUE: Toutes les membranes préparées ont été stockées dans la solution de NaCl 0,5 M pendant la nuit avant de l’utiliser dans la pile RED. De sorte que la conductivité de la membrane est améliorée et peut atteindre des performances de sortie stabilisées lors de la mesure de la pile RED. Le tableau 1 décrit les propriétés de la membrane10,11.
| Spécification | Unité | MEC | AEM |
| Degré de gonflement | % | 5±1 | 1±0,5 |
| Densité de charge ou capacité d’échange d’ions | meq/g | 1.8 | ~1,6 |
| Propriétés mécaniques (Résistance à la traction) | Mpa | >40 | 40-50 |
| Allongement à casser | % | ~42 | 30-50 |
| Module jeune (MPa) | 1500±100 | 1000-1500 | |
| Conductivité à température ambiante | S/cm | ~0,03 | ~0,025 |
| Permselectivité | % | 98-99 | 94-96 |
| Épaisseur | μm | 50±2 | 50±3 |
| Solvant | - | Diméthylacétamide (N-Diméthylacétamide) | N-méthyl-2-pyrrolidone (NMP) |
Tableau 1 : Propriétés des membranes. Résumé des propriétés de la membrane échangeuse de cations et d’échange d’anions.
3. Fabrication de l’électrodialyse inverse
-
Assemblage de la pile RED
- Préparer une solution modèle en utilisant du NaCl 0,6 M pour les milieux à forte concentration (HC) et du NaCl à 0,01 M pour les compartiments à faible concentration (CL)12.
REMARQUE: Ici, l’eau de rivière est considérée comme une solution saline à faible concentration, et l’eau de mer est représentée comme une solution saline à forte concentration. - Préparer 5 L de solution à haute concentration et à faible concentration dans un grand récipient connecté aux tubes. Maintenir les solutions sous agitation dans les conditions ambiantes (température ambiante) pendant au moins 2 h avant de les utiliser dans la pile RED.
- Préparer le mélange de NaCl 0,05M de [Fe(CN)6]-3/[Fe(CN)6]-4 et 0,3 M dans de l’eau de 500 mL comme solution de rinçage pour le ROUGE.
- Connectez les trois récipients de solution avec la pile RED à l’aide de tubes en caoutchouc à travers la pompe péristaltique et les manomètres. Utiliser le tube de la taille L/S 16 pour la solution de rinçage, et utiliser le tube de la taille L/S 25 pour la solution HC et LC.
- Pour faire une pile RED, prenez deux plaques d’extrémité composées de polyméthacrylate de méthyle (PMMA). Connectez les deux plaques d’extrémité horizontalement face à face avec des écrous, des boulons et des rondelles à l’aide d’une force de 25 Nm à l’aide d’un pilote de clé numérique. L’épaisseur des plaques d’extrémité en PMMA de 3 cm, et le trajet des canaux d’écoulement ont été conçus en plaques pour HC, LC, et solution de rinçage par un foreur2.
- Placez deux électrodes en treillis en titane métallique (Ti) enduit d’un mélange d’Iridium (Ir) et de ruthénium (Ru) dans un rapport de 1:1 et placez-les à l’extrémité des plaques pmma. Les deux électrodes d’extrémité sont connectées avec le clip crocodile du compteur source.
REMARQUE: Les deux plaques d’extrémité PMMA sont équipées d’électrodes en maille, les deux électrodes ont été superposées avec une entretoise de forme carrée et la plaque d’extrémité PMMA recouverte d’un joint en caoutchouc orienté vers l’intérieur. Après cela, CEM et AEM sont placés alternativement, séparés par un joint et une entretoise en silicone, comme le montre la figure 3. - Installez des joints en silicium, des entretoises en polymère et des membranes échangeuses d’ions (CEM et AEM) couche par couche, comme le présentent les diagrammes schématiques figure 4 et figure 5. Assurez-vous que la zone active des électrodes, les deux membranes, l’entretoise extérieure et intérieure, le joint extérieur et intérieur est de 7 x 7 = 49 cm2.
- Passer des solutions à forte concentration et à faible concentration des compartiments respectifs par des pompes péristaltiques, comme indiqué dans le diagramme schématique de la figure 4.
- Faire circuler la solution de rinçage dans les compartiments de l’électrode externe et de la membrane en mode de recirculation à l’aide de pompes péristaltiques. Le débit utilisé pour la solution de rinçage est de 50 mL min-1.
- Le débit fixe est utilisé pour analyser les performances de chaque membrane. Dans cette expérience, nous avons utilisé 100 mL min-1 à travers une pompe péristaltique.
- Préparer une solution modèle en utilisant du NaCl 0,6 M pour les milieux à forte concentration (HC) et du NaCl à 0,01 M pour les compartiments à faible concentration (CL)12.
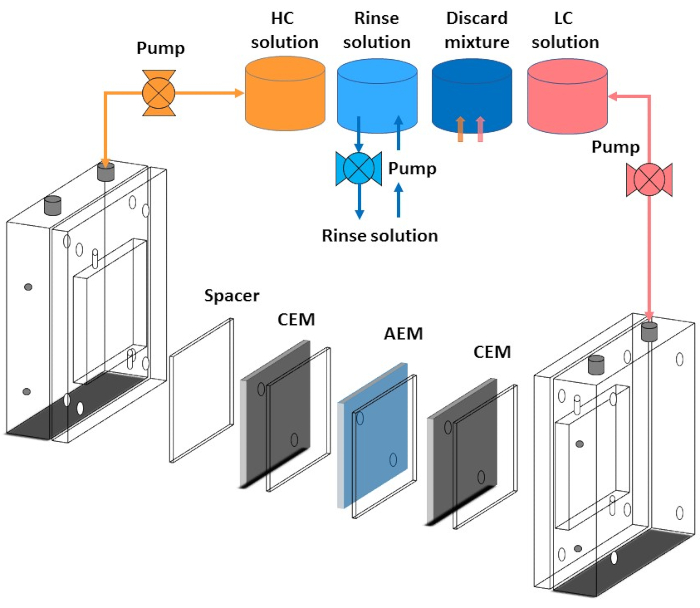
Figure 4: Représentation schématique de la connexion du tube avec cheminée d’électrodialyse inverse. Connexion de l’électrodialyse inverse avec des pompes péristaltiques, un récipient en solution à haute concentration, un récipient en solution à faible concentration, un récipient pour solution de rinçage et un récipient pour solution de rejet. Il montre également l’alignement de l’entretoise avec une membrane échangeuse d’anions (AEM) et une membrane échangeuse de cations (CEM). Veuillez cliquer ici pour voir une version plus grande de cette figure.
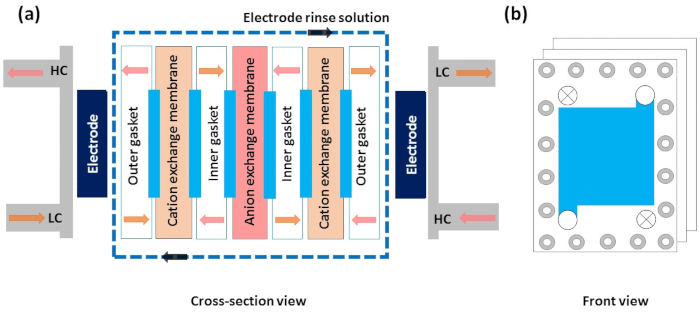
Figure 5: Schéma de principe des différentes couches dans la configuration de l’électrodialyse inverse. (a)La vue en coupe d’une illustration schématique de l’électrodialyse inverse montre la direction d’écoulement de la solution à haute concentration, de la solution à faible concentration et de la solution de rinçage d’électrode. Autres composants tels que les électrodes, les joints extérieurs et intérieurs, les entretoises externes et intérieures, la membrane échangeuse de cations et la membrane échangeuse d’anions. b)Vue de face de la cheminée, qui montre la direction d’écoulement d’une solution. Veuillez cliquer ici pour voir une version plus grande de cette figure.
4. Mesure de l’électrodialyse inverse
-
Calcul de puissance
- Laissez la concentration élevée, la faible concentration et la solution de rinçage traverser la pile au moins pendant 5 min. Mesurer les performances de sortie RED par un compteur source, qui est relié aux deux électrodes de la pile RED13.
- Calculez les caractéristiques courant-tension de la pile RED en termes de densité de puissance à l’aide de la méthode galvanostat.
REMARQUE: Dans la méthode galvanostat, un courant constant est appliqué à travers les électrodes et mesure le courant résultant. Le courant résultant est le courant généré en raison de la réaction électrochimique dans la cheminée. La mesure est effectuée sous une tension statique de 0,05 V avec un courant de balayage fixe de 10 mA. - La densité de puissance maximale de la pile RED est mesurée à l’aide de l’équation suivante 1.
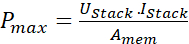 (1)
(1)
Ici, Pmax est la densité de puissance maximale de la pile RED (Wm-2),lapile U est la tension (V) produite par la membrane dans la pile, Istack est le courant enregistré (A), et Amem est la zone active des membranes(m2).
Résultats
Puissance nette
Les globules ROUGES génèrent généralement de l’énergie électrique à partir du gradient de salinité de la solution saline, c’est-à-dire le mouvement des ions dans la direction opposée à travers la membrane. Pour assembler correctement la pile RED, il faut aligner soigneusement toutes les couches, y compris les électrodes, les joints, les membranes et les entretoises de la pile, comme le montre le diagramme schématique de la figure 4 et de l...
Discussion
Le principe de fonctionnement du RED est principalement dominé par les propriétés physicochimiques de la membrane, qui est un élément crucial du système RED, comme illustré à la figure 3. Ici, nous décrivons les caractéristiques fondamentales de la membrane pour fournir un système RED haute performance. La perméabilité spécifique des ions de la membrane lui fait passer un type d’ions à travers leur nanocanal polymère. Comme son nom l’indique, le CEM peut passer le cation ...
Déclarations de divulgation
Les auteurs ne déclarent aucun conflit d’intérêts.
Remerciements
Ce travail a été soutenu par la subvention de la National Research Foundation of Korea (NRF) financée par le gouvernement coréen (MEST) (No. NRF-2017R1A2A2A05001329). Les auteurs du manuscrit sont reconnaissants à l’Université Sogang de Séoul (République de Corée).
matériels
| Name | Company | Catalog Number | Comments |
| AEM based membrane | Fumion | P1810-194 | Ionomer |
| CEM based membrane | Fumion | E550 | Ionomer |
| Digital torque wrench | Torqueworld | WP2-030-09000251 | wrench |
| Labview software | Natiaonal Instrument | - | Software |
| Laptop | LG | - | PC |
| Magnetic stirrer | Lab Companion | - | MS-17BB |
| N, N-Dimethylacetamide | Sigma aldrich | 271012 | Chemical |
| N-Methyl-2- pyrrolidone | Daejung | 872-50-4 | Chemical |
| Peristaltic pump | EMS tech Inc | - | EMP 2000W |
| Potassium hexacyanoferrate(II) trihydrate | Sigma aldrich | P3289 | Chemical |
| Potassium hexacyanoferrate(III) | Sigma aldrich | 244023 | Chemical |
| Pressure Gauge | Swagelok | - | Guage |
| Reverse electrodialysis setup | fabricated in lab | - | Device |
| RO system pure water | KOTITI | - | Water |
| Rotary evaporator | Hitachi | YEFO-KTPM | Induction motor |
| Sodium Chloride | Sigma aldrich | S9888 | Chemical |
| Sodium Hydroxide | Merk | 1310-73-2 | Chemical |
| Source meter | Keithley | - | 2410 |
| Spacer | Nitex, SEFAR | 06-250/34 | Spacer |
| Sulfuric acid | Daejung | 7664-93-9 | Chemical |
| Tube | Masterflex tube | 96410-25 | Rubber tube |
Références
- Dlugolecki, P., Gambier, A., Nijmeijer, K., Wessling, M. Practical potential of reverse electrodialysis as process for sustainable energy generation. Environmental Science & Technology. 43, 6888-6894 (2009).
- Kim, D., Kwon, K., Kim, D. H., Li, L. . Energy Generation Using Reverse Electrodialysis: Principles, Implementation, and Applications. , (2019).
- Mei, Y., Tang, C. Y. Recent developments and future perspectives of reverse electrodialysis technology: A review. Desalination. 425, 156-174 (2018).
- Yip, N. Y., Brogioli, D., Hamelers, H. V. M., Nijmeijer, K. Salinity gradients for sustainable energy: primer, progress, and prospects. Environmental Science & Technology. 50, 12072-12094 (2016).
- Li, W., et al. A novel hybrid process of reverse electrodialysis and reverse osmosis for low energy seawater desalination and brine management. Applied Energy. 104, 592-602 (2013).
- Brauns, E. Salinity gradient power by reverse electrodialysis: effect of model parameters on electrical power output. Desalination. 237, 378-391 (2009).
- Cusick, R. D., Kim, Y., Logan, B. E. Energy capture from thermolytic solutions in microbial reverse-electrodialysis cells. Science. 335, 1474-1477 (2012).
- Kim, D. H., Park, B. H., Kwon, K., Li, L., Kim, D. Modeling of power generation with thermolytic reverse electrodialysis for low-grade waste heat recovery. Applied Energy. 189, 201-210 (2017).
- Hong, J. G., et al. Potential ion exchange membranes and system performance in reverse electrodialysis for power generation: A review. Journal of Membrane Science. 486, 71-88 (2015).
- Choi, S. -. Y., et al. Controlling fuel crossover in open electrochemical cells by tuning the water nanochannel for power generation. ACS Sustainable Chemistry & Engineering. 8, 8613-8623 (2020).
- Shah, S. A., et al. Modified single-wall carbon nanotube for reducing fouling in perfluorinated membrane-based reverse electrodialysis. International Journal of Hydrogen Energy. 45, 30703-30719 (2020).
- Kwon, K., Han, J., Park, B. H., Shin, Y., Kim, D. Brine recovery using reverse electrodialysis in membrane-based desalination processes. Desalination. 362, 1-10 (2015).
- Kwon, K., Park, B. H., Kim, D. H., Kim, D. Parametric study of reverse electrodialysis using ammonium bicarbonate solution for low-grade waste heat recovery. Energy Conversion and Management. 103, 104-110 (2015).
- Hatzell, M. C., Ivanov, I., Cusick, R. D., Zhu, X., Logan, B. E. Comparison of hydrogen production and electrical power generation for energy capture in closed-loop ammonium bicarbonate reverse electrodialysis systems. Physical Chemistry Chemical Physics. 16, 1632-1638 (2014).
- Zhu, X. P., He, W. H., Logan, B. E. Reducing pumping energy by using different flow rates of high and low concentration solutions in reverse electrodialysis cells. Journal of Membrane Science. 486, 215-221 (2015).
- Vermaas, D. A., Saakes, M., Nijmeijer, K. Doubled power density from salinity gradients at reduced intermembrane distance. Environmental Science & Technology. 45, 7089-7095 (2011).
- Veerman, J., Saakes, M., Metz, S. J., Harmsen, G. J. Reverse electrodialysis: Performance of a stack with 50 cells on the mixing of sea and river water. Journal of Membrane Science. 327, 136-144 (2009).
- Veerman, J., Saakes, M., Metz, S. J., Harmsen, G. J. Electrical power from sea and river water by reverse electrodialysis: a first step from the laboratory to a real power plant. Environmental Science & Technology. 44, 9207-9212 (2010).
- Batchelor, C. K., Batchelor, G. K. . An Introduction to Fluid Dynamics. , (2000).
- Schock, G., Miquel, A. Mass transfer and pressure loss in spiral wound modules. Desalination. 64, 339-352 (1987).
- Da Costa, A. R., Fane, A. G., Wiley, D. E. Spacer characterization and pressure drop modelling in spacer-filled channels for ultrafiltration. Journal of Membrane Science. 87, 79-98 (1994).
- Vermaas, D. A., Veerman, J., Saakes, M., Nijmeijer, K. Influence of multivalent ions on renewable energy generation in reverse electrodialysis. Energy & Environmental Science. 7, 1434-1445 (2014).
- Vermaas, D. A., Saakes, M., Nijmeijer, K. Enhanced mixing in the diffusive boundary layer for energy generation in reverse electrodialysis. Journal of Membrane Science. 453, 312-319 (2014).
- Moreno, J., Grasman, S., van Engelen, R., Nijmeijer, K. Upscaling reverse electrodialysis. Environmental Science & Technology. 52, 10856-10863 (2018).
- Sarkar, S., SenGupta, A. K., Prakash, P. The donnan membrane principle: opportunities for sustainable engineered processes and materials. Environmental Science & Technology. 44, 1161-1166 (2010).
- Kim, H. -. K., et al. High power density of reverse electrodialysis with pore-filling ion exchange membranes and a high-open-area spacer. Journal of Materials Chemistry A. 3, 16302-16306 (2015).
- Długołęcki, P., Nymeijer, K., Metz, S., Wessling, M. Current status of ion exchange membranes for power generation from salinity gradients. Journal of Membrane Science. 319, 214-222 (2008).
- Geise, G. M., Curtis, A. J., Hatzell, M. C., Hickner, M. A., Logan, B. E. Salt concentration differences alter membrane resistance in reverse electrodialysis stacks. Environmental Science & Technology Letters. 1, 36-39 (2014).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon