Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
La production hépatique de glucose, l’uréagénèse et la lipolyse quantifiées à l’aide du modèle de foie de souris perfusé
Dans cet article
Résumé
Nous présentons ici une méthode robuste de perfusion in situ du foie de souris pour étudier la régulation aiguë et directe du métabolisme hépatique sans perturber l’architecture hépatique mais en l’absence de facteurs extra-hépatiques.
Résumé
Le foie a de nombreuses fonctions, y compris le métabolisme des nutriments. Contrairement à d’autres modèles in vitro et in vivo de recherche hépatique, le foie perfusé isolé permet d’étudier la biologie et le métabolisme hépatique dans l’ensemble du foie avec une architecture hépatique intacte, séparée de l’influence de facteurs extra-hépatiques. Les perfusions hépatiques ont été développées à l’origine pour les rats, mais la méthode a également été adaptée aux souris. Nous décrivons ici un protocole de perfusion in situ du foie de souris. Le foie est perfusé antérograde à travers la veine porte avec un tampon bicarbonaté oxygéné de Krebs-Henseleit, et la sortie est recueillie à partir de la veine cave inférieure suprahépatique avec serrage de la veine cave inférieure infrahépatique pour fermer le circuit. À l’aide de cette méthode, les effets hépatiques directs d’un composé d’essai peuvent être évalués avec une résolution temporelle détaillée. La fonction hépatique et la viabilité sont stables pendant au moins 3 h, ce qui permet d’inclure des contrôles internes dans la même expérience. Les possibilités expérimentales à l’aide de ce modèle sont nombreuses et peuvent permettre de mieux comprendre la physiologie du foie et les maladies du foie.
Introduction
Le foie est un organe essentiel du métabolisme. Il joue un rôle clé dans le contrôle de l’équilibre énergétique de l’ensemble du corps en régulant le métabolisme du glucose, des lipides et des acides aminés. L’augmentation des maladies du foie dans le monde est en train de devenir un fardeau majeur pour la santé mondiale, et davantage de connaissances sont nécessaires sur la physiopathologie et ses conséquences sur les fonctions hépatiques.
Divers modèles in vitro ont été développés pour la recherche sur le foie afin de compléter les études in vivo. Les hépatocytes primaires isolés et cultivés chez les rongeurs et les humains sont largement utilisés. Les cellules non parenchymateuses peuvent être séparées des hépatocytes par centrifugation différentielle et par gradient, et la co-culture de différents types de cellules est utile pour étudier la diaphonie intercellulaire1. Bien que les hépatocytes humains primaires soient considérés comme l’étalon-or pour tester la toxicité des médicaments, plusieurs études ont montré que les hépatocytes se dédifférencient rapidement dans la culture tissulaire, ce qui entraîne une perte des fonctions hépatiques 2,3,4. La culture d’hépatocytes dans un système sphéroïde 3D améliore la dédifférenciation, est plus stable et semble imiter le foie in vivo à un degré plus élevé que les systèmes de culture 2D traditionnels5. Les tranches de foie découpées avec précision sont un autre modèle in vitro bien établi qui maintient l’architecture tissulaire intacte et contient les cellules non parenchymateuses présentes dans le foie6. Les modèles in vitro plus avancés comprennent le foie sur puce7 et les organoïdes hépatiques8. Cependant, avec toutes ces approches, il y a une perte d’intégrité structurelle et de dynamique de l’écoulement, y compris l’écoulement vectoriel de la veine porte-hépatique, ce qui a probablement un impact sur la généralisabilité.
Le foie de rat isolé a été décrit pour la première fois par Claude Bernard en 18559, et est toujours utilisé dans divers domaines scientifiques pour l’étude de la biologie, de la toxicologie et de la physiopathologie du foie. Les avantages du foie perfusé par rapport aux modèles in vitro mentionnés ci-dessus comprennent le maintien de l’architecture hépatique, du flux vasculaire, de la polarité et de la zonation des hépatocytes, ainsi que des interactions entre les hépatocytes et les cellules non parenchymateuses. Par rapport aux études in vivo, le foie perfusé permet d’étudier le métabolisme hépatique de manière isolée en évitant les facteurs extra-hépatiques transportés par le sang et avec un contrôle complet des conditions expérimentales. Plusieurs modifications ont été apportées pour améliorer le modèle de perfusion hépatique de rat au cours des années10,11,12,13. Bien que des souris aient été utilisées pour des études isolées sur le foie perfusé, moins de littérature est disponible. Nous présentons ici une méthode de perfusion in situ du foie de souris par canulation de la veine porte et de la veine cave suprahépatique inférieure afin d’étudier les réponses métaboliques aiguës et directes aux substrats métaboliques et aux hormones telles que mesurées dans l’effluent veineux hépatique du foie de souris en temps réel.
Access restricted. Please log in or start a trial to view this content.
Protocole
Toutes les expériences sur les animaux ont été menées avec l’autorisation de l’Inspection danoise de l’expérimentation animale, du ministère de l’Environnement et de l’Alimentation du Danemark (permis 2018-15-0201-01397) et du comité d’éthique local conformément à la directive européenne 2010/63/UE, aux National Institutes of Health (publication n° 85-3) et conformément aux directives de la législation danoise régissant l’expérimentation animale (1987). Il s’agit d’une procédure terminale, et la cause du décès est l’exsanguination et la perforation du diaphragme sous anesthésie profonde.
1. Animaux de laboratoire
- Procurez-vous des souris de la variété, de l’âge et du sexe souhaités. Cette étude a utilisé des souris mâles C57BL/6JRj âgées de 11 à 16 semaines. Abritez jusqu’à 5 souris mâles ou 8 souris femelles par cage avec un accès ad libitum à la nourriture et à l’eau et maintenez un cycle lumière-obscurité de 12 h/12 h avec des lumières allumées de 6 h à 18 h.
2. Préparations préopératoires
- Faire un tampon de perfusion hépatique.
- Tampon de Krebs-Henseleit. Mélanger et dissoudre 118 mmol/L de NaCl, 4,7 mmol/L de KCl, 1,2 mmol/L de MgSO 4 et 1,2 mmol/L de KH 2 PO4 en dH 2 O. Dissoudre 1,25 mmol/L de CaCl2dans un bécher séparé et ajouter le tampon.
- Dissoudre 25 mmol/L de NaHCO3 et ajouter lentement au tampon tout en remuant. Stockez le tampon à 4 degrés. Le tampon est stable pendant au moins 1 mois.
REMARQUE : Des précipitations peuvent se produire si le CaCl2 et le NaHCO3 ne sont pas dissous individuellement avant d’être ajoutés.
- Filtrez le tampon de perfusion à travers un filtre de 2 μm et ajustez le pH à 7,5 à l’aide de HCl.
REMARQUE : Cette étape doit être effectuée le jour de l’expérience, car le pH augmente avec le temps, même lorsqu’il est stocké dans des flacons fermés. - Préparer les composés d’essai à une concentration plus élevée que la concentration finale souhaitée (p. ex., concentration 20x lorsqu’ils sont perfusés à un débit de 0,175 mL/min à l’aide d’une pompe à bras de poing) dans un tampon de perfusion Krebs-Henseleit filtré et dont le pH est ajusté. S’il y a lieu, diluer les composés d’essai dans un tampon de perfusion Krebs-Henseleit additionné de 1 % de BSA comme support (pour éviter l’adhérence aux tubes et à la verrerie, ce qui est essentiel pour tous les peptides), filtrés à travers un filtre de taille appropriée.
3. Fonctionnement et perfusion
REMARQUE : Une illustration de la configuration de perfusion utilisée dans cette étude est fournie à la figure 1.
- Gazer le tampon de perfusion (95 % d’O 2, 5 % de CO2) pendant au moins 30 min pour fournir suffisamment d’oxygène au foie et maintenir le pH correct dès le début de l’opération (le système tampon de bicarbonate atteindra un pH de 7,4 sous gazage continu, voir la figure supplémentaire 1).
- Anesthésier une souris en lui administrant de la kétamine (90 mg/kg) et de la xylazine (10 mg/kg) par injection intrapéritonéale.
- Placez la souris en décubitus dorsal sur une table d’opération chauffée et confirmez l’absence de réflexes en réponse au pincement des orteils. Vaporisez de l’éthanol à 70 % pour empêcher les cheveux de coller aux ciseaux. La fixation de la souris sur la surface chaude permet d’augmenter la stabilité pour les procédures suivantes.
- Faites une incision avec des ciseaux à la base de l’abdomen et coupez vers le haut jusqu’à la cage thoracique des deux côtés pour exposer la cavité abdominale. Déplacez les intestins vers la droite à l’aide d’un coton-tige, en exposant la veine porte.
- Placez deux ligatures sous la veine porte à l’aide d’une pince courbe et préparez un nœud lâche pour chaque ligature.
- Insérez un cathéter de 0,7 mm dans la veine porte. Lorsqu’il est perforé, retirez l’aiguille du cathéter et guidez le cathéter dans la veine jusqu’à ce que l’extrémité du cathéter soit proche du foie, comme illustré à la figure 2. Le sang s’écoule dans le cathéter.
- Serrez les ligatures. Si le cathéter n’est pas rempli de sang, remplissez-le avec un tampon de perfusion pour éviter l’introduction d’une bulle d’air.
- Fixez le tube de perfusion et initiez la perfusion du foie avec le tampon bicarbonaté de Krebs-Henseleit à 37 °C en démarrant la pompe à rouleaux à un débit de perfusion de 0,8 mL/min. Le foie pâlit en quelques secondes.
- Coupez la cage thoracique et le diaphragme à l’aide de ciseaux. À ce stade, l’animal est euthanasié. Placez une ligature sous la veine cave inférieure suprahépatique à l’aide d’une pince à pointe fine. Placez un stylo, une gaze roulée ou un autre objet jetable sous le dos de la souris pour rendre la veine plus accessible.
- Insérez un cathéter dans la veine cave inférieure suprahépatique via l’oreillette droite du cœur. Une fois perforé, retirez l’aiguille du cathéter et guidez le cathéter dans la veine jusqu’à ce que l’extrémité du cathéter soit proche du foie. Le tampon de sang et de perfusion s’épuise immédiatement.
- Serrez la ligature et fixez un tube pour la collecte des effluents de perfusion. Fixez tous les tubes avec du ruban adhésif imperméable (ruban adhésif élégant ou similaire).
- Utilisez un adaptateur de pince vasculaire pour placer une pince vasculaire sur la veine cave infrahépatique immédiatement au-dessus de la veine rénale droite afin d’éviter le mélange (Figure 2).
- Augmentez le débit de perfusion à 3,5 mL/min et démarrez une minuterie. Lancez l’enregistrement de la pression. Une perfusion réussie se traduit généralement par une pression de ~10 mm/Hg.
- Couvrez le foie d’un drap stérile imbibé de solution saline et ajoutez du sérum physiologique pendant l’expérience pour éviter qu’il ne se dessèche.
- Recueillir l’effluent de perfusion pendant 1 min et mesurer le volume. Le volume doit être d’environ 3,5 ml/min. Le mélange de sang n’est pas attendu à ce stade et le cœur ne pompe plus.
- Attendez une période d’équilibration de 30 min avant de commencer l’expérience.
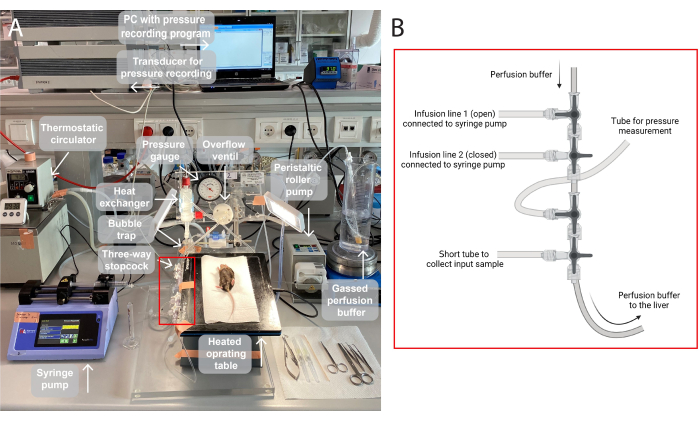
Figure 1 : Illustration de la configuration de la perfusion. (A)La table d’opération est surélevée sur un trépied et chauffée à 37 °C. Le tampon de perfusion est gazé (95 % d’O 2, 5 % de CO2), pompé via une pompe péristaltique à rouleaux et chauffé dans l’échangeur de chaleur avec un piège à bulles intégré. Le système se compose en outre d’un manomètre et d’une pompe à broche pour le réglage de la pression de perfusion. La pression de perfusion est enregistrée en continu et visualisée via un transducteur sur un PC, un programme d’enregistrement de la pression. (B) La boîte rouge capture les connexions des robinets d’arrêt à trois voies. Le premier robinet d’arrêt à trois voies est ouvert pour la perfusion d’un composé d’essai via un pousse-seringue, et le second est fermé. Le troisième est ouvert pour les mesures de pression en continu. Le quatrième robinet d’arrêt peut être utilisé pour prélever des échantillons d’entrée, par exemple pour l’analyse des gaz à travers le foie perfusé. Les connecteurs peuvent être modifiés selon les besoins pour des expériences spécifiques nécessitant plus ou moins de lignes de perfusion. Veuillez cliquer ici pour voir une version agrandie de cette figure.
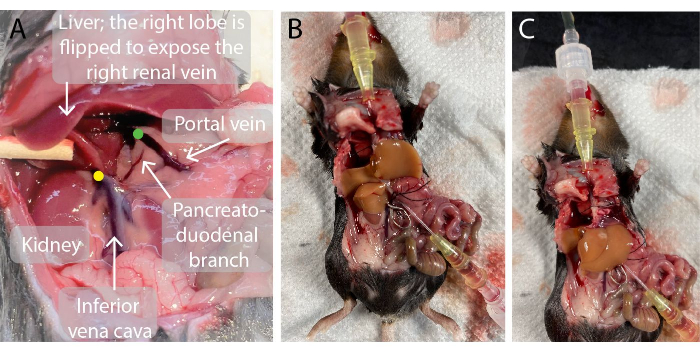
Figure 2 : Photos de la cavité abdominale de la souris avant et pendant la perfusion hépatique. (A)Le point vert indique l’emplacement de l’extrémité du cathéter de la veine porte. Il est important que l’extrémité du cathéter soit positionnée juste en dessous du point de ramification de la veine porte dans les veines portes hépatiques gauche et droite, mais au-dessus de la branche pancréato-duodénale pour éviter les fuites. Le point jaune indique l’emplacement correct de la pince vasculaire sur la veine cave inférieure infrahépatique entre la veine rénale droite et le foie pour éviter le reflux du sang dans le foie perfusé. (B, C) Un foie de souris perfusé avec les deux cathéters insérés dans la veine porte (B) et la veine cave inférieure suprahépatique (C) et la pince vasculaire sur la veine cave inférieure infrahépatique (B). Veuillez cliquer ici pour voir une version agrandie de cette figure.
4. Expérimentez
- Commencez l’expérience en prélevant les premiers échantillons de référence à l’aide d’un collecteur de fractions à la fin de la période d’équilibration. Prélevez des échantillons à l’intervalle de temps souhaité et placez-les immédiatement sur de la glace.
- Vérifiez régulièrement le piège à bulles et remplissez-le de tampon de perfusion lorsqu’il est presque vide.
- Prélever un échantillon du tampon à l’aide d’un robinet d’arrêt à trois voies immédiatement avant qu’il n’entre dans l’organe et du cathéter collecteur inséré dans la veine cave inférieure (après qu’il ait été perfusé dans le foie).
- Mesurez les échantillons à l’aide d’un analyseur de gaz du sang pour confirmer que l’organe est métaboliquement actif (indiqué par une augmentation de la pression partielle de CO2 et une diminution du pH).
- Répétez les étapes 4.3 à 4.4 à la fin de l’expérience pour évaluer la viabilité tout au long de l’expérience (figure supplémentaire 2).
REMARQUE : La diminution de la pression partielle d’oxygène ne fournit pas une mesure fiable de la respiration en raison des pertes d’oxygène des tuyaux, de l’organe, etc. - Après 15 minutes de perfusion initiale, commencer la première stimulation en perfusant une substance d’essai à travers un robinet d’arrêt à trois voies au débit désiré à l’aide d’un pousse-seringue (p. ex., concentration de 20 fois la substance d’essai lorsqu’elle est perfusée à un débit de 0,175 mL/min à l’aide d’une pompe à bras de poing). Vous pouvez également remplacer le tampon de référence par un nouveau tampon (oxygéné et chauffé) contenant le composé d’essai dans la concentration finale.
- Arrêtez la stimulation et prélevez des échantillons de base pendant 20 à 30 minutes avant de commencer la deuxième stimulation.
- À la fin de l’expérience, infusez un témoin positif approprié pendant 5 à 10 minutes.
- Après l’expérience, exciser le foie perfusé et le peser pour normaliser le débit au poids du foie. Congeler le foie dans de l’azote liquide pour mesurer la teneur en protéines afin de normaliser la production par rapport à la teneur en protéines.
5. Mesures biochimiques
- Quantifier la concentration de la molécule d’intérêt à l’aide de dosages appropriés pour les mesures dans le tampon de perfusion (tests colorimétriques ou ELISA internes ou disponibles dans le commerce). Le tampon est compatible avec la plupart des techniques basées sur les omiques telles que la métabolomique et la protéomique.
NOTE : Dans cette étude, l’urée a été mesurée sur la base d’un test colorimétrique décrit précédemment14. Le glucose et les acides gras non estérifiés ont été quantifiés à l’aide de trousses disponibles dans le commerce.
6. Analyse des données
- Présentez les données dans des graphiques XY montrant la sortie de sécrétion au fil du temps.
NOTE : L’une des vertus du système de perfusion in vitro est qu’il est possible d’exprimer les données sous forme de débit réel (concentration × débit, par exemple μmol/min) au lieu de la concentration mesurée dans le débit (mmol/L) comme dans les études in vivo . Envisagez de normaliser la sortie en fonction du poids du foie lorsque vous comparez différents modèles murins ou de la teneur totale en protéines (mesurée par BCA) lorsque vous comparez des souris témoins à des modèles de souris souffrant d’obésité ou de maladies du foie, où une augmentation du poids du foie peut être due à une augmentation de la teneur en graisse. - Présenter les données récapitulatives sous forme de points individuels par animal représentant la production moyenne ou totale au cours de la ligne de base et sur une période de stimulation (généralement de 15 à 30 minutes) ou la production incrémentielle en utilisant la ligne de base précédente pour chaque période de stimulation en fonction de la conception de l’étude.
- Analysez les données à l’aide d’un test t apparié (deux groupes) ou d’une ANOVA à un facteur avec des stimulations répétées (plus de deux groupes) avec un test post-hoc approprié pour les tests multiples.
Access restricted. Please log in or start a trial to view this content.
Résultats
Une base de référence stable est nécessaire pour déterminer si un stimulus ou un substrat conduit à la libération de la molécule d’intérêt. La figure 3A montre un exemple d’expérience réussie. La production d’urée dans le foie perfusé est mesurée à des intervalles de 2 minutes et indiquée sous forme de moyenne ± MEB. Les périodes de référence précédant chacune des deux périodes de stimulation sont stables. La production moyenne d?...
Access restricted. Please log in or start a trial to view this content.
Discussion
Le foie de souris perfusé isolé est un outil de recherche puissant pour l’étude de la dynamique et des mécanismes moléculaires du métabolisme hépatique. La possibilité de prélever des échantillons minute par minute permet d’évaluer en détail l’effet direct d’un composé d’essai sur le foie. Par rapport aux études in vivo, le foie perfusé permet d’étudier le métabolisme hépatique de manière isolée en évitant les facteurs extra-hépatiques transportés par le sang et avec une maîtr...
Access restricted. Please log in or start a trial to view this content.
Déclarations de divulgation
Les auteurs ne déclarent aucun conflit d’intérêts en rapport avec cet article.
Remerciements
Les études et Nicolai J. Wewer Albrechtsen ont été financées par la Novo Nordisk Foundation Excellence Emerging Investigator Grant - Endocrinology and Metabolism (demande no. NNF19OC0055001), le prix Future Leader de la Fondation européenne pour l’étude du diabète (NNF21SA0072746) et le Fonds de recherche indépendant du Danemark, Sapere Aude (1052-00003B). Le Centre de recherche sur les protéines de la Fondation Novo Nordisk est soutenu financièrement par la Fondation Novo Nordisk (accord de subvention NNF14CC0001). La figure 1B a été créée avec biorender.com. Nous remercions le Dr Rune E. Kuhre (Novo Nordisk A/S) pour ses discussions fructueuses sur le foie de souris perfusé.
Access restricted. Please log in or start a trial to view this content.
matériels
| Name | Company | Catalog Number | Comments |
| 3-way stopcock | BD | 394601 | |
| Altromin breeding diet | Altromin Spezialfutter | 1319 | |
| Calcium chloride dihydrate (CaCl2·2H2O) | Sigma | C8106 | |
| Catheters (0.7 mm) | BD | 381812 | |
| Filter paper (pore size 2.0 µm) | Millipore | AP2029325 | |
| Glucose kit | QuantiChromTM | DIGL-100 | Low concentration protocol |
| Ketamine | MSD Animal Health | 511485 | 90 mg/kg |
| Ligature (black sterile silk) | Agnthos | 14739 | |
| Magnesium sulfate (MgSO4) | Sigma | 230391 | |
| Non-esterified fatty acids kit | Fujifilm Wako Chemicals | NEFA-HR(2) | |
| Operating table, heated on tripod stand, type 873 | Harvard Bioscience, Inc. | 733776 | |
| Potassium chloride (KCl) | Sigma | P9541 | |
| Potassium dihydrogen phosphate(KH2PO4) | Merck | 1.04877 | |
| Roller Pump, with four channels | Harvard Bioscience, Inc. | 730100 | |
| Sleek tape | Mediq danmark | 4001910 | |
| Sodium bicarbonate (NaHCO3) | Sigma | S5761 | |
| Sodium chloride (NaCl) | Sigma | S1679 | |
| Thermostatic Circulator | Harvard Bioscience, Inc. | 730125 | Bath Volume 3 L, 230 V/50 Hz |
| Tubing | Tygon | E3603 | Inner diameter 1.59 mm, outer diameter 3.18 mm |
| Universal perfusion system | Harvard Bioscience, Inc. | 732316 | Basic unit uniper UP-100, type 834 |
| Vamin | Fresenius Kabi | B05ABA01 | Mixed amino acids |
| Vessel clamp adaptor | Deutsche Biomedical | DBC1002 | |
| Vessel clamps | Deutsche Biomedical | DBC1005 | |
| Windkessel | Harvard Bioscience, Inc. | 732068 | |
| Xylazine | Rompun Vet | 530701 | 10 mg/kg |
Références
- Bale, S. S., Geerts, S., Jindal, R., Yarmush, M. L. Isolation and co-culture of rat parenchymal and non-parenchymal liver cells to evaluate cellular interactions and response. Scientific Reports. 6, 25329(2016).
- Lauschke, V. M., et al. Massive rearrangements of cellular MicroRNA signatures are key drivers of hepatocyte dedifferentiation. Hepatology. 64 (5), 1743-1756 (2016).
- Seirup, M., et al. Rapid changes in chromatin structure during dedifferentiation of primary hepatocytes in vitro. Genomics. 114 (3), 110330(2022).
- Gupta, R., et al. Comparing in vitro human liver models to in vivo human liver using RNA-Seq. Archive of Toxicology. 95 (2), 573-589 (2021).
- Bell, C. C., et al. Characterization of primary human hepatocyte spheroids as a model system for drug-induced liver injury, liver function, and disease. Scientific Reports. 6, 25187(2016).
- Dewyse, L., Reynaert, H., van Grunsven, L. A. Best practices and progress in precision-cut liver slice cultures. International Journal of Molecular Sciences. 22 (13), 7137(2021).
- Li, X., George, S. M., Vernetti, L., Gough, A. H., Taylor, D. L. A glass-based, continuously zonated and vascularized human liver acinus microphysiological system (vLAMPS) designed for experimental modeling of diseases and ADME/TOX. Lab on a Chip. 18 (17), 2614-2631 (2018).
- Broutier, L., et al. Culture and establishment of self-renewing human and mouse adult liver and pancreas 3D organoids and their genetic manipulation. Nature Protocols. 11 (9), 1724-1743 (2016).
- Bartošek, I., Guaitani, A., Miller, L. L. Isolated Liver Perfusion and its Applications. , Raven Press. New York. (1973).
- Gores, G. J., Kost, L. J., LaRusso, N. F. The isolated perfused rat liver: conceptual and practical considerations. Hepatology. 6 (3), 511-517 (1986).
- Mischinger, H. J., et al. An improved technique for isolated perfusion of rat livers and an evaluation of perfusates. Journal of Surgical Research. 53 (2), 158-165 (1992).
- Vairetti, M., et al. Correlation between the liver temperature employed during machine perfusion and reperfusion damage: role of Ca2. Liver Transplantation. 14 (4), 494-503 (2008).
- Ferrigno, A., Richelmi, P., Vairetti, M. Troubleshooting and improving the mouse and rat isolated perfused liver preparation. Journal of Pharmacological and Toxicological Methods. 67 (2), 107-114 (2013).
- Zawada, R. J. X., Kwan, P., Olszewski, K. L., Llinas, M., Huang, S. -G. Quantitative determination of urea concentrations in cell culture medium. Biochemistry and Cell Biology. 87 (3), 541-544 (2009).
Access restricted. Please log in or start a trial to view this content.
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon