Réaliser des réactions en dessous de la température ambiante
Vue d'ensemble
Source : Laboratoire de Dr. Dana Lashley - College of William and Mary
Démonstration par : Matt Smith
Lorsque les nouvelles obligations sont formées au cours d’une réaction chimique, il faut que les espèces impliquées (atomes ou molécules) sont très proches et se heurtent dans l’autre. Les collisions entre ces espèces sont plus fréquente et plus efficace plus la vitesse à laquelle ces molécules sont déplacent. Une règle largement utilisée, qui a ses racines dans la Arrhenius équation1, stipule que l’élévation de la température de 10 K sera environ le double du taux de réaction, et élévation de la température de 20 K va quadrupler le taux :
(1)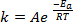
L’équation (1) se trouve souvent dans sa forme logarithmique :
(2)
où k est la vitesse de la réaction chimique, A est le facteur de fréquence (relatif à la fréquence des collisions moléculaires), Eun est l’énergie d’activation nécessaire pour la réaction, R est la constante des gaz parfaits et T est la température à laquelle se déroule la réaction.
Une température plus élevée signifie donc qu'une réaction est effectue beaucoup plus rapidement. Néanmoins, dans certains cas, il est souhaitable de réaliser des réactions à basse température, en dépit de l’abaissement effet sur la vitesse de la réaction. Quelques scénarios sont à cet égard précisés plus loin.
Quand il est utile d’exécuter une réaction sous la température ambiante, chimistes utilisent bains de refroidissement pour maintenir une certaine température ou température ambiante. Les réactions sont refroidies à la température désirée en plaçant le ballon à réaction à l’intérieur d’un bain de refroidissement approprié. Les réactifs de la réaction jamais entrent en contact direct avec les produits chimiques dans le bain de refroidissement. Le bain de refroidissement peut consister en un seul composant cryogénique (refroidissement) (par exemple, glace, neige carbonique ou l’azote liquide) ou peut-être un mélange de la composante cryogénique avec un certain solvant et/ou un sel additif. Le but du solvant est de transférer efficacement la température de l’agent de refroidissement dans le ballon de réaction et l’additif vise à abaisser le point de congélation du mélange (ou bien appuyez sur). (Notez qu’il est possible pour une substance à la fois un solvant et additif).
Procédure
Installation de salle de bain de refroidissement
Pour une configuration générale, préparer le bain de refroidissement de choix tel que décrit ci-dessous et plonger le ballon à réaction dans le bain (Figure 1). Ne remplissez pas le bateau de bain complètement, mais laisser assez d’espace pour permettre l’immersion du ballon à réaction.
Remarque : si la réaction est l’humidité sensible, soyez très prudent lors de l’ajout de réactifs à
Applications et Résumé
Quand est-il utile d’exécuter une réaction à une basse température ?
Afin de répondre à cette question nous laisse enquêter sur quatre différentes applications :
Application 1. Parfois, les réactions sont trop vigoureux et exothermique et le mélange réactionnel doit être refroidi afin d’éviter les fuites et la montée en raison de l’exploitation du gaz en pression. Une réaction fortement exothermique peut également devenir un...
References
- Gordon, A. J., Ford, R. A. The Chemist's Companion - A Handbook of Practical Data, Techniques, and References. Chapter 11 (1973) ISBN: 978-0-471-31590-2.
- Rondeau, R. E. Slush baths. J. Chem. Eng. Data. 11, 124 (1966)
Passer à...
Vidéos de cette collection:

Now Playing
Réaliser des réactions en dessous de la température ambiante
Organic Chemistry
70.7K Vues

Introduction à la catalyse
Organic Chemistry
34.5K Vues

Montage d'un chauffage à reflux
Organic Chemistry
167.9K Vues

Transfert de solvants via une rampe à vide (ligne Schlenk)
Organic Chemistry
41.7K Vues

Dégazage des liquides par la technique "cycle geler-pomper-dégeler"
Organic Chemistry
56.3K Vues

Préparation de réactifs anhydres et équipement
Organic Chemistry
79.4K Vues

Purification des composés par recristallisation
Organic Chemistry
709.4K Vues

Séparation des mélanges par précipitation
Organic Chemistry
157.8K Vues

Extraction solide-liquide
Organic Chemistry
238.0K Vues

Utilisation d'un évaporateur rotatif (ou Rotovap) pour éliminer un solvant
Organic Chemistry
212.9K Vues

Distillation fractionnée
Organic Chemistry
334.7K Vues

Préparation de cristaux pour analyse par diffraction des rayons X
Organic Chemistry
32.4K Vues

Performing 1D Thin Layer Chromatography
Organic Chemistry
289.9K Vues

Chromatographie sur colonne
Organic Chemistry
360.5K Vues

Spectroscopie à résonance magnétique nucléaire (RMN)
Organic Chemistry
248.4K Vues
