Realizar reacciones por debajo de la temperatura ambiente
Visión general
Fuente: Laboratorio del Dr. Dana Lashley - College of William and Mary
Demostración: Matt Smith
Cuando se forman nuevos enlaces en el curso de una reacción química, se requiere que las especies involucradas (átomos o moléculas) en las proximidades y chocan en uno otro. Las colisiones entre estas especies son más frecuente y eficaces cuanto mayor sea la velocidad en que estas moléculas son móviles. Una ampliamente utilizada por regla general, que tiene sus raíces en el Arrhenius ecuación1, los Estados que aumento de la temperatura de 10 K aproximadamente doble de la tasa de una reacción, y aumento de la temperatura de 20 K se cuadruplicará la velocidad:
(1)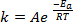
Ecuación (1) se encuentra a menudo en su forma logarítmica:
(2)
donde k es la tasa de la reacción química, es el factor de frecuencia (relativa a la frecuencia de las colisiones moleculares) , Ea es la energía de activación requerida para la reacción, R es la constante de gas ideal y T es la temperatura a la cual la reacción lleva a cabo.
Por lo tanto, una temperatura más alta significa que una reacción se termina mucho más rápido. Sin embargo, en algunos casos es deseable llevar a cabo reacciones a bajas temperaturas, a pesar del efecto de disminución en la velocidad de la reacción. Unos escenarios en este sentido se elaboran en más abajo.
Cuando es útil ejecutar una reacción debajo de temperatura ambiente, químicos utilizan baños de enfriamiento para mantener una determinada temperatura o rango de temperatura. Reacciones se enfrían a una temperatura deseada colocando el matraz de reacción dentro de un baño de enfriamiento apropiado. Los reactivos en la reacción no entre nunca en contacto directo con los productos químicos en el baño de enfriamiento. El baño que se refresca puede consistir en un solo componente (enfriamiento) criogénico (como hielo, hielo seco o nitrógeno líquido) o puede ser una mezcla del componente criogénico con un determinado solvente o una añadido sal. El propósito del solvente es transferir con eficacia temperatura del agente refrigerante al matraz de reacción, y el propósito del aditivo es menor (o apretar) el punto de congelación de la mezcla. (Tenga en cuenta que es posible que una sustancia solvente y aditivo).
Procedimiento
Instalación de baño de enfriamiento
Para una puesta a punto general, preparar el baño que se refresca de elección como se describe a continuación y sumerja el matraz de reacción en la bañera (figura 1). No llenar completamente el recipiente del baño, pero deje suficiente espacio para permitir la inmersión del matraz de reacción.
Nota: Si la reacción es humedad sensible, tenga mucho cuidado al agregar los reactivos en el matraz o cua
Aplicación y resumen
¿Cuándo es útil ejecutar una reacción a baja temperatura?
Para responder a esta pregunta nos dejó investigar cuatro aplicaciones diferentes:
Aplicación de 1. A veces las reacciones son demasiado vigorosas y exotérmica y la mezcla de reacción se debe enfriar para evitar que se derrame y acumulación debido al desarrollo de gas de la presión. Una reacción fuertemente exotérmica puede también convertirse en un peligro para la seguridad com...
Referencias
- Gordon, A. J., Ford, R. A. The Chemist's Companion - A Handbook of Practical Data, Techniques, and References. Chapter 11 (1973) ISBN: 978-0-471-31590-2.
- Rondeau, R. E. Slush baths. J. Chem. Eng. Data. 11, 124 (1966)
Saltar a...
Vídeos de esta colección:

Now Playing
Realizar reacciones por debajo de la temperatura ambiente
Organic Chemistry
70.7K Vistas

Introducción a la catálisis
Organic Chemistry
34.5K Vistas

Montaje de un sistema de reflujo para reacciones químicas calientes
Organic Chemistry
167.5K Vistas

Líneas de Schlenk para transferencia de disolventes
Organic Chemistry
41.6K Vistas

Desgasificación de líquidos con ciclos de congelación-bomba-descongelación
Organic Chemistry
56.1K Vistas

Preparación de equipos y reactivos anhidros
Organic Chemistry
79.4K Vistas

Purificación de compuestos por recristalización
Organic Chemistry
708.7K Vistas

Separación de mezclas por precipitación
Organic Chemistry
157.8K Vistas

Extracción sólido-líquida
Organic Chemistry
237.8K Vistas

Evaporación rotatoria para eliminar solventes
Organic Chemistry
212.9K Vistas

Destilación fraccionada
Organic Chemistry
334.5K Vistas

Crecimiento de cristales para el análisis de difracción de rayos x
Organic Chemistry
32.4K Vistas

Performing 1D Thin Layer Chromatography
Organic Chemistry
289.8K Vistas

Cromatografía en columna
Organic Chemistry
360.2K Vistas

Espectroscopia de resonancia magnética nuclear (RMN)
Organic Chemistry
247.9K Vistas
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados
