Synthèse d'un complexe de cobalt(II) porteur d'oxygène
Vue d'ensemble
Source : Deepika Das, Tamara M. Powers, département de chimie, Texas A & M University
Chimie bioinorganique est le domaine d’étude qui se penche sur le rôle que jouent les métaux en biologie. Environ la moitié de toutes les protéines contiennent des métaux, et on estime que jusqu'à un tiers de toutes les protéines dépendent métalliques actives sites fonctionnent. Les protéines qui comportent des métaux, appelés métalloprotéines, jouent un rôle vital dans une variété de fonctions cellulaires qui sont nécessaires à la vie. Métalloprotéines ont intrigué et inspiré des chimistes inorganiques synthétiques pendant des décennies, et de nombreux groupes de recherche ont consacré leurs programmes à la modélisation de la chimie des sites actifs contenant des métaux en protéines grâce à l’étude des composés de coordination.
Le transport d’O2 est un processus vital pour les organismes vivants. O2-métalloprotéines de transport sont chargées de la liaison, transporter, et libérant de l’oxygène, qui peut être ensuite utilisé pour les processus vitaux tels que la respiration. Le complexe de coordination du cobalt oxyphorique, [N,N'-bis(salicylaldehyde)ethylenediimino]cobalt(II) [Co(salen)]2 a été largement étudiée afin de comprendre comment métalliques complexes réversiblement lier O2 . 1
Dans cette expérience, nous synthétiser [Co(salen)]2 et étudier sa réaction réversible avec O2 en présence de diméthylsulfoxyde (DMSO). Tout d’abord, nous va quantifier la quantité d’O2 consommées lors de l’exposition [Co(salen)]2 de DMSO. Nous avons ensuite visuellement observera la libération d’O2 par le [Co(salen)]2- O2 adduit en exposant le solide à CHCl3.
Procédure
1. synthèse des inactifs [Co(salen)]2
- Charger un ballon à fond rond 250 mL 3-cou avec 120 mL de 95 % EtOH et 2,20 g (0,192 mL, mol 0,018) du salicylaldéhyde.
- Monter le cou de centre avec un condensateur connecté au N2. Monter les deux autres cols avec un septum en caoutchouc et d’un entonnoir de plus muni d’un septum en caoutchouc.
- Agiter la réaction dans un bain-marie et chauffer la solution à reflux (80 ° C).
- Ajouter l’éthylène diamine (0,52 g, mL 0,58, mo
Résultats
Caractérisation des inactifs [Co(salen)]2:
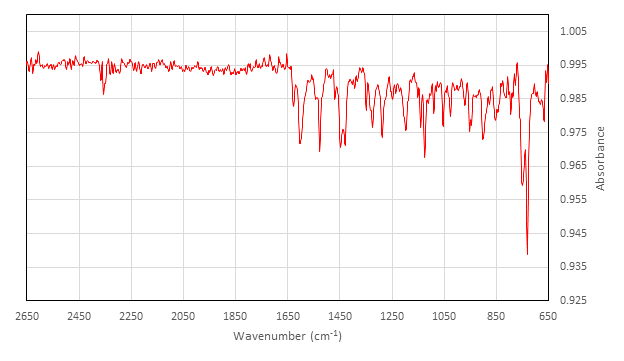
IR (cm-1) recueillies sur l’attachement de la RTA : 2357 (w), 1626 1602 (w), (m), 1542 (w), 1528 (m), 1454 1448 (w), (m), 1429 (m), 1348 (w), 1327 1323 (w), (m), 1288 (m), 1248 (w), 1236 (w), 1197 (m), 1140 (m), 1124 (m), 1089 1053 (w), (m), 1026 (w) , 970 (w), 952 (w), 947 (w), 902 (m), 878 (w), 845 (w), 813 (w), 794 (w), 75...
Applications et Résumé
Dans cette vidéo, nous explique les différentes façons que l’oxygène diatomique peut coordonner à métal ou plusieurs centres. Nous avons synthétisé les oxyphorique cobalt complexes [Co(salen)]2 et étudié sa liaison réversible avec O2. Nous avons démontré expérimentalement qu’inactif [Co(salen)]2 se lie réversiblement O2 et formes une de 2:1 Co:O2 adduit en présence de DMSO.
Tous les vertébrés reposent sur l’hémoglo...
Passer à...
Vidéos de cette collection:

Now Playing
Synthèse d'un complexe de cobalt(II) porteur d'oxygène
Inorganic Chemistry
51.8K Vues

Synthèse d'un métallocène de Ti(III) avec une ligne Schlenk
Inorganic Chemistry
31.6K Vues

Boîte à gants et capteurs d'impuretés
Inorganic Chemistry
18.7K Vues

Purification du Ferrocène par sublimation
Inorganic Chemistry
54.7K Vues

La méthode Evans
Inorganic Chemistry
68.7K Vues

Diffraction par rayons X : cristal vs poudre
Inorganic Chemistry
105.1K Vues

Spectroscopie par résonance paramagnétique électronique (RPE)
Inorganic Chemistry
25.6K Vues

Spectroscopie Mössbauer
Inorganic Chemistry
22.0K Vues

Interaction des acides et bases de Lewis au sein du complexe Ph3P-BH3
Inorganic Chemistry
39.0K Vues

Structure du ferrocène
Inorganic Chemistry
79.8K Vues

Application de la théorie des groupes à la spectroscopie IR
Inorganic Chemistry
45.9K Vues

Théorie de l’orbital moléculaire (OM)
Inorganic Chemistry
35.5K Vues

Quadruples clusters métalliques
Inorganic Chemistry
15.3K Vues

Capteurs solaires teintés
Inorganic Chemistry
16.0K Vues

Initiation photochimique des réactions de polymérisation radicalaire
Inorganic Chemistry
17.1K Vues
