Mesures électrochimiques d'un catalyseur sur support à l'aide d'un potentiostat / galvanostat
Vue d'ensemble
Source : Laboratoire de Dr. Yuriy Román, Massachusetts Institute of Technology
Un potentiostat/galvanostat (souvent dénommée simplement un potentiostat) est un instrument qui mesure actuelle à un potentiel appliqué (opération potentiostatique) ou des mesures potentielles à un courant appliqué (opération galvanostatique) (Figure 1). C’est l’instrument le plus couramment utilisé dans la caractérisation électrochimique des matériaux de l’anode et la cathode pour piles à combustible, électrolyseurs, batteries et supercapacités.
Classiquement, ces matériaux d’anode et la cathode est interfacé avec un potentiostat via une cellule électrochimique de trois électrodes. Les fils des électrodes de la potentiostat sont connectés à l’électrode de référence, la contre-électrode (souvent appelé l’électrode auxiliaire) et l’électrode de travail (qui contient le matériel de test d’intérêt). La cellule électrochimique est ensuite remplie avec une solution d’électrolyte de force ionique élevée, telle qu’une solution acide, alcaline ou sel. Les médias pour cette solution de force ionique élevée sont généralement aqueuse ; Toutefois, pour les applications nécessitant plus d’exploitation windows potentiels cellulaires, tels que des batteries et supercapacités, non aqueux, est souvent utilisé. Les médias de la cellule sont dégazé avec un gaz inerte (pour éviter les réactions secondaires indésirables) ou avec un gaz d’essai (si l’essai la réaction implique un gaz dans l’une des électrodes).
Alternativement, un pont salin ou une membrane sert à maintenir le contact ionique si les deux demi de cellules doivent être mesurées en différents électrolytes. Dans électrocatalyse hétérogène, ce type de cellule « deux compartiments » est souvent utilisé si la molécule de test à l’électrode de travail est également réactive à la contre-électrode. Cela arrive fréquemment que la contre-électrode généralement employée est de platine, qui est un catalyseur très actif de nombreuses réactions. Ici, les cellules dans un compartiment unique est utilisés, où tous les trois électrodes sont dans le même support.
Cette vidéo vous expliquera le processus de polissage d’une électrode de travail, préparer une encre de catalyseur, fixation de l’encre de catalyseur sur l’électrode de travail, préparer la cellule électrochimique et effectuer ensuite des mesures électrochimiques. Les mesures effectuées comprennent : voltampérométrie cyclique (CV), voltamétrie à balayage linéaire (LSV), chronopotentiométrie (CP) et la chronoampérométrie (CA).
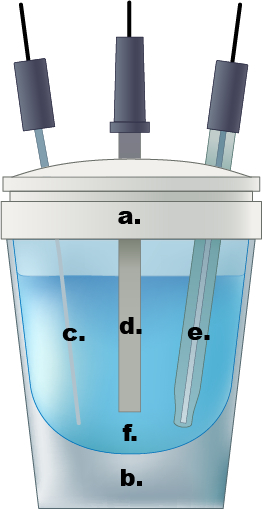
Figure 1. Un exemple d’une cellule électrochimique de compartiment unique. bouchon Teflon a.), b.) verre cellulaire, c.) PT fils contre-électrode, d.) électrode de travail, e.) Électrode de référence Ag/AgCl, f.) 0,5 solution d’électrolyte de l’acide sulfurique aqueux M.
Procédure
1. catalyseur encre et préparation de l’électrode de travail
Consignes de sécurité : Métaux pris en charge sur le noir de carbone peuvent être aspirés dans une enceinte de hood ou équilibre de fumée jusqu'à ce qu’il soit sous forme de suspension que ces poudres sont des dangers de l’inhalation.
- À l’aide d’une balance ci-joint, peser 5 à 10 mg de catalyseur métal/noir de carbone et ajouter un flacon en verre avec un bouchon.
- À l’aide d’une micropipette, di
Résultats
Cette procédure se traduira en chiffres contenant des parcelles du courant mesuré vs potentiel pour chacun des quatre techniques. Par convention de CV et LSV, les parcelles seront également produits dans le courant mesuré vs potentiel malgré la réalité que ce sont des techniques transitoires que mesurent le courants par rapport à la dérivée temporelle du potentiel.
Applications et Résumé
CV, LSV, CP et CA sont des techniques indispensables pour déterminer l’efficacité de nouveaux matériaux d’électrode pour les piles à combustible, électrolyseurs, batteries et supercapacités ainsi que pour développer les domaines tels que l’oxydation partielle sélective ou la réduction des produits chimiques. Ces méthodes permettent de déterminer les experiences de réactions sur les matériaux d’électrodes différentes par rapport à leur potentiel d’équilibre thermodynamique. Ces méthodes permet...
Passer à...
Vidéos de cette collection:

Now Playing
Mesures électrochimiques d'un catalyseur sur support à l'aide d'un potentiostat / galvanostat
Analytical Chemistry
51.4K Vues

Préparation des échantillons pour analyse
Analytical Chemistry
84.8K Vues

Étalon interne
Analytical Chemistry
204.9K Vues

Méthode de l'addition standard
Analytical Chemistry
320.3K Vues

Courbes d'étalonnage
Analytical Chemistry
797.3K Vues

Spectroscopie ultraviolet-visible (UV-Vis)
Analytical Chemistry
624.0K Vues

La spectroscopie Raman pour l'analyse chimique
Analytical Chemistry
51.2K Vues

Spectrométrie de fluorescence des rayons X
Analytical Chemistry
25.4K Vues

Chromatographie en phase gazeuse (CG) couplée à un détecteur à ionisation de flamme
Analytical Chemistry
282.2K Vues

La chromatographie en phase liquide à haute performance (CLHP)
Analytical Chemistry
384.9K Vues

Chromatographie par échange d'ions
Analytical Chemistry
264.7K Vues

Électrophorèse capillaire (EC)
Analytical Chemistry
94.0K Vues

Introduction à la spectrométrie de masse
Analytical Chemistry
112.3K Vues

Microscopie électronique à balayage (MEB)
Analytical Chemistry
87.3K Vues

Voltammétrie cyclique
Analytical Chemistry
125.4K Vues