A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
כרוני לטווח ארוך
In This Article
Summary
אנו מתארים את השיטה אגר חרוזים להקים זיהום מתמשך לטווח ארוך כרוני Pseudomonas aeruginosa בדרכי אוויר במודל העכבר.
Abstract
מודל עכבר של זיהום דרכי הנשימה הכרונית הוא נכס מרכזי בסיסטיק פיברוזיס מחקר (CF), אם כי יש מספר חששות לגבי המודל עצמו. שלבים מוקדמים של דלקת וזיהום נחקרו בהרחבה על ידי שימוש במודל העכבר אגר חרוזים Pseudomonas aeruginosa, בעוד שרק כמה דיווחים התמקדו בזיהום הכרוני לטווח הארוך בגוף חי. האתגר העיקרי לזיהום כרוני לטווח ארוך נותר נטל החיידקים הנמוך על ידי פ ' aeruginosa ואחוז הנמוך של שבועות עכברים נגועים לאחר אתגר, המציין כי תאי חיידקיים נמחקים בהדרגה על ידי המארח.
מאמר זה מציג שיטה להשגת זיהום כרוני לטווח ארוך יעיל בעכברים. שיטה זו מבוססת על ההטבעה של פ זני aeruginosa קליניים באגרו חרוזים במבחנה, ואחריו החדרת intratracheal בעכברי C57Bl/6NCrl. דלקת ריאות דו צדדית קשורה sevקריאה פסקי מדידים eral כולל ירידה במשקל, תמותה, זיהום כרוני, ותגובה דלקתית. פ זן קליני aeruginosa RP73 הועדף על זן המעבדה התייחסות PAO1 שכן היא גרמה לתמותה נמוכה יחסית, נגעים חמורים יותר, וזיהום כרוני גבוה יותר. פ קולוניזציה aeruginosa יכולה להתמיד בריאה במשך למעלה משלושה חודשים. הפתולוגיה ריאות Murine דומה לזו של חולי CF עם מחלת ריאות כרונית מתקדמת.
מודל עכברי זה מחקה באופן קרוב ביותר את מהלך המחלה האנושית ויכול לשמש הן ללימודים בפתוגנזה ולהערכת טיפולים חדשים.
Introduction
סיסטיק פיברוזיס (CF) הוא מחלה גנטית הנגרמת על ידי מוטציות ברגולטור המוליכות הטרנסממברני סיסטיק פיברוזיס גן (CFTR). גן זה מקודד לערוץ כלוריד הביע על הממברנה של רוב תאי האפיתל. הרס bronchiectasis, סתימת הריר וparenchymal נגרמים בעיקר על ידי זיהומי Pseudomonas aeruginosa בהדרגה לגרום למחלת ריאות קשה ותמותה ברוב של חולי CF 1. פתוגנזה CF הבנה ופיתוח נוסף של טיפולים חדשניים מסתמכים על מודל חיה עם תכונות אופייניות של CF. כמה עכברים, מהונדסים גנטי לגן CFTR, כבר נוצרו, אבל מגבלות ביכולתם של מינים אלה לשחזר מחלת ריאות כמו CF וכמה חריגות איבר אחרות ראו בחולי CF תועדו 2 באופן נרחב.
התפתחות הזיהום היא אחד האתגרים העיקריים במודל החיה CF. CL הספרותמוקדם מצביע על כך שזיהום כרוני שנמשך יותר מפעם אחת בחודש יכול להיות מושגת רק אם עכברים מחוסן עם חיידקים מוטבעים בסוכן משתק כגון אגר, agarose, או אלגינט אצות 3-5. סוכנים לשתק אלה מספקים את תנאי microaerobic / אנאירובי המאפשרים לחיידקים לגדול בצורה של microcolonies, בדומה לצמיחה בליחה של חולי CF 6. מודל זה של זיהום כרוני מוביל להתמדה של החיידקים לריאות וגורמות לדלקת בדרכי הנשימה ונזק 7. עם זאת, בהתאם לשיטה, זן החיידקים והמינון מחוסן לריאות, את האחוז של עכברים נגועים כרוניים ועומס החיידקים התאושש בתוך הריאות בנקודות זמן שונות יכולים להיות שונה במידה ניכרת. בפרט, האתגר העיקרי לזיהום כרוני לטווח ארוך נותר נטל החיידקים הנמוך על ידי פ ' aeruginosa ואחוז הנמוך של שבועות עכברים נגועים לאחר אתגר, המציין thaתאי חיידקיים לא נמחקים בהדרגה על ידי המארח. על ידי בחירת פ זן קליני aeruginosa RP73 מתוך אוסף של CF מבודד 8 השגנו הצלחת תמותה נמוכה, נגעים חמורים יותר, ואחוז הגבוה של זיהום כרוני עם מטען יציב חיידקים עד חודש בעכברי C57Bl/6NCrl.
מאמר זה מפרט את המתודולוגיה להטבעת פ aeruginosa בחרוזים אגר, אנחנו נגועים בעכברים על ידי החדרת intratracheal, מדדנו את עומס החיידקים וציטוקינים בריאות, אספנו נוזל BAL וביצעו בדיקה היסטולוגית. בסך הכל, בפרוטוקול זה יסייע לחוקרים בהתמודדות עם שאלות חשובות ביסודו על 8,9 פתוגנזה ובדיקת טיפולים חדשניים נגד פ זיהום כרוני aeruginosa 10,11.
Protocol
1. חיידקים מתכוננים לזיהום כרוני (שלושה ויומיים לפני מאוס אתגר)
- בחר את פ המתאים זן aeruginosa להיבדק.
- לחסן loopful של פ aeruginosa מ-80 ° C תרבות המניה לצלחת Trypticase סויה אגר (TSA) ולדגור על 37 מעלות צלזיוס למשך לילה.
- פיק מושבה אחת ולחסן לתוך 5 מיליליטר Trypticase סויה מרק (TSB) בצינור הכתיר הצמד 15 מיליליטר ולדגור על 37 מעלות צלזיוס למשך לילה בחממה רועדת בסל"ד 200.
2. הטבעת חיידקים בחרוזים אגר לזיהום כרוני (יום אחד לפני הזיהום)
- קח aliquot קטן של תרבות לילה חיידקים, לדלל 1:50 בופר פוספט (PBS) ולמדוד את הצפיפות האופטית (OD) ב600 ננומטר.
- לדלל את תרבות חיידקים בלילה על ידי הוספת 2 OD בצינור הכתיר הצמד חדש המכיל 20 מיליליטר של TSB הטרי.
- לדגור על 37 מעלות צלזיוס למשך כ - 34 שעות כדי להיכנס שלב בחממה רועדת בסל"ד 200, עד סכום כולל של 10-15 OD הוא הגיע.
- בינתיים, להכין את ה-TSA, עשויה TSB עם אגר 1.5%, החיטוי ולאזן על 50 מעלות צלזיוס באמבט מים. לאזן 150 מיליליטר של שמן מינרלים כבדים preautoclaved בבקבוק Erlenmeyer על 50 מעלות צלזיוס באמבט מים.
- ברגע שפ aeruginosa מגיע שלב היומן, לאסוף את תאי חיידקים על ידי צנטריפוגה ב2,700 XG במשך 15 דקות ב 4 ° C וזורקים supernatant.
- Resuspend את כדור החיידקים ב 1 מיליליטר של PBS סטרילי ומערבולת ביסודיות כדי resuspend את הכדור לחלוטין.
- השעיה חיידקי מערבבים 1 מיליליטר עם 9 מיליליטר של נוזל TSA מראש equilibrated ב50 ° C.
- הוסף את 10 מיליליטר TSA-פ תערובת aeruginosa לנפט כבד מינרלים (prewarmed על 50 מעלות צלזיוס) ומייד מערבבת במשך 6 דקות בטמפרטורת חדר. התסיסה חייבת לייצר מערבולת גלויה בנפט.
- מצנן את התערובת עד 4 ° C, תוך ערבוב בsp המינימוםeed ל35 דקות (איור 1).
- הנח את תערובת שמן אגר חרוזים בקרח במשך 20 דקות נוספות.
- העבר את אגר חרוזים ל50 צינורות מיליליטר פלקון ו צנטריפוגות ב 2,700 XG במשך 15 דקות ב 4 ° C.
- במדויק להסיר את שמן מינרלים ולשטוף עם PBS סטרילי שש פעמים, כמתואר בשלב 2.11. לאחר שלושה שוטף, ניתן pelleted חרוזים על ידי כוח משיכה במקום להשתמש בצנטריפוגות. לאחר השטיפה האחרונה, resuspend אגר חרוזים ב20-30 מיליליטר PBS.
- קח aliquot של חרוזים (כ 0.5 מיליליטר) וסביבה נקיה מחיידקי homogenize.
- קח את של חרוזים הומוגני 100 μl ולדלל ב900 μl של PBS סטרילית. סדרתי לדלל 1:10 עד 10 -6.
- דילול צלחת סידורי על צלחות ה-TSA, כוללים מדגם חי עד 10 -6 דגירה צלחות ב 37 ° C.
- מדוד את קוטר חרוז באמצעות מיקרוסקופ אור הפוכה במספר תחומים. קוטר חרוז חייב להיות בין 100-200 מיקרומטר ( איור 1).
- אחסנו את חרוזים לילה בשעה 4 ° C.
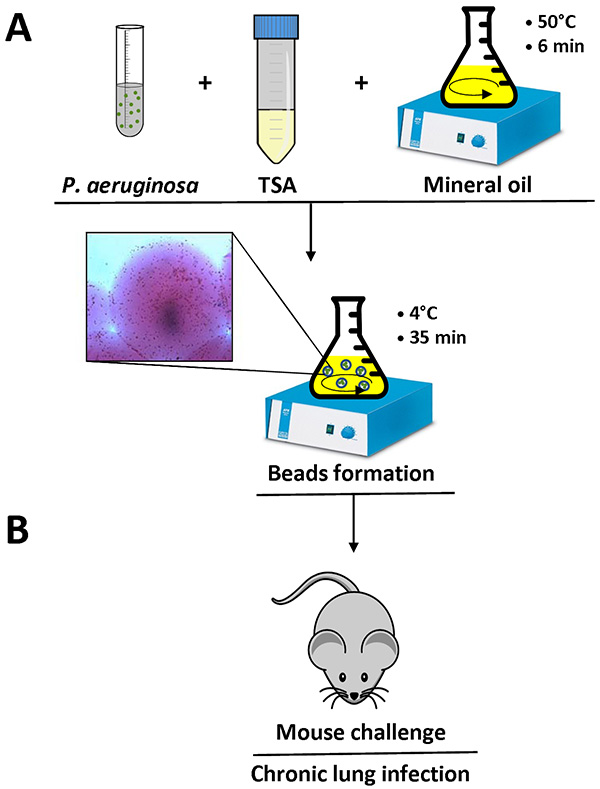
איור 1. סקירה של הזיהום בהכנת חרוזים ועכבר אגר. פ תאי aeruginosa הם resuspended ב 1 מיליליטר של PBS, והוסיפו ל9 מיליליטר של ה-TSA הנוזלי (50 מעלות צלזיוס). תערובת זו מתווספת ל150 מיליליטר שמן מינרלים כבד על 50 מעלות צלזיוס בבקבוק ובחש במהירות גבוהה במשך 6 דקות בטמפרטורה בחדר. כאשר הבקבוק הוא מקורר 4 ° C עם ערבוב איטי ל35 דקות, אגר מתמצק יצירת חרוזים, וחיידקים המצויים בתערובת מוטבעים בחרוזים אגר. פירוט של חרוז אגר המכיל תאים חיידקיים מוצג (א '). לאחר הסרת שמן מינרלים עם כמה שטיפות באמצעות PBS סטרילי, ההשעיה אגר חרוזים מוכנה fאו חיסון לריאות של עכברים על ידי הזרקת intratracheal (ב '). לחץ כאן לצפייה בתמונה גדולה יותר.
3. עכברי אתגר עם אגר-חרוזים
הצהרת אתיקה: פרוטוקול וניסוי זה פעלו בהתאם להנחיות מוועדת הטיפול בבעלי החיים ואתיקה של המכון המדעי סאן רפאלה.
- לספור את מספר יחידות המושבה להרכיב (CFU) על צלחות TSA כדי לקבוע את מספר CFU / מיליליטר בהשעיה אגר חרוזים. לדלל את אגר חרוזים עם PBS סטרילי ל2-4 x 10 7 CFU / מיליליטר כדי להגיע לבידוד אופטימלי של 1-2 x 10 6 ב50 μl.
- הרדימי C57Bl/6NCr (ז 20-22, 6-8 שבועות) עכברי זכרים עם קטמין (50 מ"ג / מיליליטר) ו xylazine (5 מ"ג / מיליליטר) ב0.9% NaCl מנוהל בהיקף של 0.002 מיליליטר / גרם משקל גוף על ידי זריקת intraperitoneal.
הערה: הרדמה נחשב adequate כאשר החיה נשארת עדיין בשקט, אינו מגיב לגירויים חיצוניים, ויש לו לב ונשימת שיעורים קבועים. - מניחים את העכבר במצב שכיבה. לחטא את המעיל של העכבר עם 70% אתנול.
- לחשוף את קנה הנשימה על ידי חתך אנכי של העור וצנרר קנה הנשימה עם קטטר סטרילי, גמיש 22 G 0.9 מ"מ x 25 IV מ"מ, שמירה על תשומת לב כדי להסיר את stylette תוך כדי התנועה לתוך קנה הנשימה. הכנס את הקטטר לא עמוק מדי לתוך קנה הנשימה. עצור לפני שהגיע לקארינה (הסתעפות).
- מייד לקחת נפח של 50 μl של השעיה חרוז אגר על ידי מזרק 1 מ"ל ולצרף אותו לקטטר. דחף בעדינות את הבוכנה של המזרק, המאפשר את חרוזים שמושתלים לתוך הריאות. סגירת החתך באמצעות קליפים תפר.
- מניחים את החיה על כרית חימום עד ער לחלוטין.
4. הערכת עכברים
- שימו לב לעכברים יומיים לסימנים קליניים כוללים באיכות מעיל, יציבה,ניידות, ומצב הידרציה. לפקח על משקל גוף ביום. עכברים שמאבדים ≥ 20% במשקל גוף חייבים להיות מורדמים.
- עקוב נקודה 5 לאוסף של נוזל שטיפה ברונכואלוואולרית (BAL) ונקודות 6 או 7 לאוסף של ריאות והניתוח של CFU סך הכל, ניתוח היסטולוגית, תגובה דלקתית במונחים של ספירת תאים מוחלטת והפרש בBAL, ניתוח ציטוקינים, ו myeloperoxidase פעילות (MPO).
5. אוסף נוזל BAL וניתוח
- להרדים את העכברים על ידי CO 2 שאיפה.
- מניחים את העכבר במצב שכיבה. לחטא את המעיל של העכבר עם 70% אתנול.
- לחשוף את קנה הנשימה ואת כלוב בית החזה על ידי חתך אנכי של העור. לחשוף את הריאות על ידי קיצוץ הסרעפת.
- הכנס חוט תפר מתחת לקנה הנשימה באמצעות פינצטה וצנרר קנה הנשימה עם קטטר סטרילי, גמיש 22 גרם 0.9 מ"מ x 25 מ"מ IV. משוך את שני קצוות של חוט התפירה כדי לאגד את catheter לקנה הנשימה ולקשור החוט סביב קנה הנשימה.
- קח את הנפח של 1 מיליליטר של RPMI 1640 באמצעות מזרק 1 מ"ל ולצרף אותו לקטטר. לדחוף את הבוכנה של המזרק כדי לשטוף את הריאות ומייד לשחזר את הנוזל, לאחסן אותו בצינור 15 מיליליטר.
שים לב: אם ציטוקינים הם להיות מנותחים, להוסיף מעכבי פרוטאז לRPMI 1640. - חזור על פעולה זו שלוש פעמים עם סכום כולל של 3 מיליליטר של RPMI. מעתה והלאה, לאחסן את נוזל BAL על קרח. עבור לשלב 6 לאיסוף והניתוח של ריאות.
הערה: אנא שים לב כי לא כל הנוזל להאסף (2.8 מרבי מיליליטר). - לכימות של חיידקים נמצאים בנוזל BAL, לטעום aliquot קטן (300 μl), סדרנו לדלל 1:10 ב PBS סטרילי, צלחת על צלחות TSA ולדגור על 37 מעלות צלזיוס למשך לילה.
- ספירת תאים הכולל שימוש במיקרוסקופ אופטי אור הפוך דילול aliquot של 1:02 נוזל BAL עם פתרון Tuerk בתא ספירת תאים 'שודד גופות.
- צנטריפוגה remaining נוזל BAL ב330 XG במשך 8 דקות ב 4 ° C. קח את supernatant לניתוח ציטוקינים ELISA, לאחסן אותו ב -80 ° C. בצע את פעולות 5.10-5.13 לספירת תאי ההפרש ידי cytospin.
- אם גלולה היא אדומה, lyse אריתרוציטים resuspending גלולה ב 250-300 μl של חיץ תמוגה RBC מדולל 1:10 ב מים מזוקקים אולטרה טהור במשך 3 דקות. לנטרל עם 2 מיליליטר PBS ו צנטריפוגות ב 330 XG במשך 8 דקות ב 4 ° C.
- בטל supernatant ו resuspend את הכדור ב 10% בסרום שור עוברי RPMI (FBS). השתמש בנפח שיספק 1 x 10 6 מיליליטר תאים /, המבוסס על סך ספירת תאים.
- הנח שקופיות מיקרוסקופ ומסננים לחריצים מתאימים בcytospin עם מסנני הקרטון מול מרכז cytospin. פיפטה 150 μl של כל דגימה לתוך הבארות המתאימות של cytospin ו צנטריפוגות בcytocentrifuge XG 300 למשך 5 דקות.
- כתם שקופיות על ידי Romanowsky מכתים באמצעות ערכה מסחרית, על פי maההוראות של nufacturer וכפי שתואר לעיל 12. בצע את פעולות 5.14-5.17 לניתוח פעילות MPO.
- צנטריפוגה הנפח הנותר של BAL ב380 XG במשך 5 דקות ב 4 ° C. בטל supernatant ו resuspend את הכדור ב 250 μl של כלוריד Hexadecyltrimethylammonium 0.5% במים מזוקקים אולטרה טהור לlyse התאים. ההשעיה יכולה להיות קפוא ב -20 מעלות צלזיוס במשך כמה ימים לפני ביצוע assay.
- צנטריפוגה ב XG 16,000 ל30 דקות ב 4 ° C ולהשתמש supernatant לבצע assay MPO בצלחות 96 היטב, ומוסיף את המדגם בשני עותקים לכל טוב ואם יש צורך, גם דילולים הנכונים של המדגם.
- הוסף לכל דגימה בבארות נפח שווה של 3,3 ', 5,5'-tetramethylbenzidine (TMB) כמצע לperoxidase. לאפשר התגובה לתתקיים בחושך במשך 5 דקות לפחות ועד שלא יהיה התפתחות נוספת בצבע.
- עצור את התגובה על ידי הוספת 2 MH 2 SO 4nd למדוד את OD ב 450 ננומטר. ערך OD יהיה ביחס ישר לפעילות peroxidase.
6. מדידה של עומס בקטריאלי בריאה וציטוקין ניתוח
- מייד לאחר איסוף נוזל BAL, ריאות בלו מהעכבר, יש לשטוף אותם בPBS סטרילי, אונות נפרדות, לשים אותם בצינור מסביב לתחתית עם 2 מיליליטר של PBS סטרילי ולאחסן על קרח.
שים לב: אם ציטוקינים הם להיות מנותחים, להוסיף מעכבי פרוטאז לPBS לצינורות. - הסביבה נקיה מהחיידקים homogenize ריאות, לקחת aliquot קטן (300 μl) מhomogenate, סדרנו לדלל 1:10 ב-PBS, צלחת על צלחות TSA ולדגור על 37 מעלות צלזיוס למשך לילה. שים לב שסך עומס החיידקים בדרכי האוויר יהיה הסכום של CFUs נמצא בנוזל BAL וריאות.
- צנטריפוגה homogenate שנותר בXG 16,000 ל30 דקות ב 4 ° C. קח את supernatant לניתוח ציטוקינים ELISA, ולאחסן ב -80 ° C.
7. בדיקה היסטולוגית
- לבצע ניתוח היסטולוגית רק על הריאות שבנוזל BAL לא נאסף, כדי לשמר את היבט ריאות ומאפיינים.
- להרדים את העכבר על ידי CO 2 שאיפה.
- לחשוף את כלוב בית החזה על ידי חתך אנכי של העור, לחשוף את הריאות על ידי חיתוך הסרעפת.
- ריאות והבלו, לשטוף אותם ב-PBS, להפריד בין האונות, לשים אותם בצינור המכיל פורמלין 5-10 מיליליטר 10% ניטראליים שנאגרו (פורמלין 4%) ולאחסן ב 4 ° C המוגנים מפני אור.
- ריאות להטביע בפרפין, באמצעות נהלים סטנדרטיים.
- לחתוך 5 מיקרומטר חלקים עבים באמצעות microtome.
- שקופיות כתם עם hematoxylin ו eosin ולכסות את השקופיות עם coverslip, על פי נהלים קבועים.
- בחן את השקופיות באמצעות מיקרוסקופ brightfield הפוך ולרכוש תמונות על ידי חיבור למיקרוסקופ למצלמה.
תוצאות
כאשר הפרוטוקול הוא נעשה בצורה נכונה, פ אגר חרוזים aeruginosa ימדדו בין 100-200 מיקרומטר וניתן להבחין במיקרוסקופ אור הפוכה על ידי pipetting נפח קטן של ההשעיה אגר חרוזים בשקופית. תאי חיידקים בודדים נראים בחרוזים אגר, כפי שמוצגים בפירוט באיור 1.
Discussion
השלבים הקריטיים בפ הכנת aeruginosa-חרוזים ואתגר עכבר מדווחים להלן.
זן פ aeruginosa משמש לאתגר עכברים הוא קריטי. תמותה, זיהום או פינוי כרוני עשוי להיות שונה באופן משמעותי בהתאם לזן החיידקים המשמש לאתגר. פ זן קליני aeruginosa...
Disclosures
החוקרים מצהירים כי אין להם אינטרסים כלכליים מתחרים.
Acknowledgements
מחקר במעבדתו של Bragonzi כבר מומן על ידי הקרן האיטלקית סיסטיק פיברוזיס (CFaCore) והאיחוד האירופי-F7-2009-223,670. חלק מהעבודה זו בוצע באביק, מעבדת מיקרוסקופיה מתקדמת, וhistopathology העכבר בוצע ביחידת הפתולוגי האנטומיה (מכון המדעי סאן רפאלה).
Materials
| Name | Company | Catalog Number | Comments |
| Bacto Tryptic Soy Broth | Becton Dickinson | 211823 | |
| Difco Agar, granulated | Becton Dickinson | 214510 | |
| Heavy mineral oil | Sigma-Aldrich | 330760-1L | |
| S-(+)-Ketamine hydrochloride | Sigma-Aldrich | K1884 | |
| Xylazine hydrochloride | Sigma-Aldrich | X1251 | |
| 1 ml Syringe 25 G 5/8 in 0.5 mm x 16 mm | PIC | 3071250300350 | |
| Catheter 22 G 0.9 mm x 25 mm | Becton Dickinson | 381223 | |
| Graefe Forceps - 0.5 mm Tips Curved | Fine Science Tools | 11152-10 | |
| Scissors, Iris, 11 cm, straight | World Precision Instruments | 501758 | |
| Suture clips | Fine Science Tools | 12040-01 | |
| Suture thread | Fine Science Tools | 18020-40 | |
| RPMI 1640 | Lonza | BE12-167F | |
| Complete protease inhibitor cocktail | Roche | 11836145001 | |
| Fast-Read 102 Burker disposable chamber | Biosigma | 390497 | |
| Tuerk solution | Fluka | 93770 | |
| RBC lysis buffer | Biolegend | 420301 | |
| Fetal bovine serum | Lonza | DE14-801F | |
| EZ cytofunnel | Thermo Scientific | A78710021 | |
| Superfrost ultra plus microscope slides | Thermo Scientific | J3800AMNZ | |
| Diff-Quik Romanowsky staining set | Medion Diagnostics | 130832 | |
| Hexadecyltrimethylammonium chloride | Sigma-Aldrich | 52366-10G | |
| 96-well EIA/RIA plate | Costar | 3590 | |
| 3,3’,5,5’- Tetramethylbenzidine | Sigma-Aldrich | T8665-1L | |
| Sulfuric acid | Sigma-Aldrich | 320501-1L | |
| 10% Neutral buffered formalin | Bio-Optica | 05-01005Q | |
| Harris hematoxylin non Papanicolau | Bio-Optica | 05-M06004 | |
| Eosin plus alcoholic solution | Bio-Optica | 05-M11007 | |
| Equipment | |||
| Shaking incubator | Amerex Instruments | Steady Shake 757 | |
| Water bath | Grant | SUB14 | |
| Homogenizer | Ystral | ||
| Precision balance | KERN | 440-47N | |
| Cytocentrifuge | Thermo Scientific | A78300003 | |
| Low Cost Heating Pad | 2biol | LCHP | |
| Homogenization probe | Ystral | 2366925(small) | |
| Inverted optical microscope | Zeiss | Axioplan2 | |
| Camera (microscope) | Zeiss | Axiocam MRc5 | |
| Rotary microtome | Leica | RM2255 | |
References
- Gibson, R., Burns, J. L., Ramsey, B. W. Pathophysiology and management of pulmonary infections in cystic fibrosis. Am. J. Respir. Crit. Care. 168, 918-951 (2003).
- Bragonzi, A. Murine models of acute and chronic lung infection with cystic fibrosis pathogens. IJMM. 300, 584-593 (2010).
- Cash, H. A., McCullough, B., Johanson, W. G., Bass, J. A. A rat model of chronic respiratory infection with Pseudomonas aeruginosa. Am. Rev. Respir. Dis. 119, 453-459 (1979).
- Starke, J. R., Langston, C., Baker, C. J. A mouse model of chronic pulmonary infection with Pseudomonas aeruginosa and Pseudomonas cepacia. Pediatr. Res. 22, 698-702 (1987).
- Pedersen, S. S., Hansen, B. L., Hansen, G. N. Induction of experimental chronic Pseudomonas aeruginosa lung infection with P. aeruginosa entrapped in alginate microspheres. APMIS. 98, 203-211 (1990).
- Bragonzi, A., et al. Nonmucoid Pseudomonas aeruginosa expresses alginate in the lungs of patients with cystic fibrosis and in a mouse model. J. Infect. Dis. 192, 410-419 (2005).
- van Heeckeren, A. M. Murine models of chronic Pseudomonas aeruginosa lung infection. Lab. Anim. 36, 291-312 (2002).
- Bragonzi, A., et al. Pseudomonas aeruginosa microevolution during cystic fibrosis lung infection establishes clones with adapted virulence AJRCCM. 180, 138-145 (2009).
- Kukavica-Ibrulj, I., Facchini, M., Cigana, C., Levesque, R. C., Bragonzi, A., Filloux, S., Ramos, J. L. Assessing Pseudomonas aeruginosa virulence and the host response using murine models of acute and chronic lung infection. Methods in Pseudomonas aeruginosa: Humana Press. , (2014).
- Moalli, F., et al. The Therapeutic Potential of the Humoral Pattern Recognition Molecule PTX3 in Chronic Lung Infection Caused by Pseudomonas aeruginosa. J. Immunol. 186, 5425-5534 .
- Paroni, M. Response of CFTR-deficient mice to long-term Pseudomonas aeruginosa chronic infection and PTX3 therapeutic treatment. J. Infect. Dis. In press, .
- Maxeiner, J., Karwot, R., Hausding, M., Sauer, K. A., Scholtes, P., Finotto, S. A method to enable the investigation of murine bronchial immune cells, their cytokines and mediators. Nat. Protoc. 2, 105-112 (2007).
- Bragonzi, A., et al. Pseudomonas aeruginosa microevolution during cystic fibrosis lung infection establishes clones with adapted virulence.. AJRCCM. In press, (2009).
- Pirone, L., et al. Burkholderia cenocepacia strains isolated from cystic fibrosis patients are apparently more invasive and more virulent than rhizosphere strains. Environ. Microbiol. 10, 2773-2784 (2008).
- Bragonzi, A., et al. Modelling co-infection of the cystic fibrosis lung by Pseudomonas aeruginosa and Burkholderia cenocepacia reveals influences on biofilm formation and host response. PLoS One. 7, .
- Bianconi, I., et al. Positive signature-tagged mutagenesis in Pseudomonas aeruginosa: tracking patho-adaptive mutations promoting long-term airways chronic infection. PLoS Pathog.. 7, (2011).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved