A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
4-כלי דגימה גישה ללימודים אינטגרטיביים של הפיזיולוגיה השליה האדם
In This Article
Summary
אנו מציגים שיטה מפורטת ללמוד פיזיולוגיה שליה אנושית ב vivo בטווח. השיטה משלבת דגימת דם מן הכלים הנכנסים והיוצאים על צדדי האם והעובר של השליה עם מדידות אולטראסאונד של זרימת הדם בנפח ודגימת רקמת השליה.
Abstract
השליה האנושית אינה נגישה במיוחד למחקר, בעוד שעדיין נמצא ברחם . ההבנה הנוכחית של הפיזיולוגיה השליה של האדם in vivo מבוססת אפוא במידה רבה על מחקרים בבעלי חיים, למרות המגוון הגבוה בין המינים באנטומיה שליה, המודינמיקה ומשך ההיריון. הרוב המכריע של מחקרים אנושיים השליה הם מחקרים vivo זלוף לשעבר או במבחנה מחקרים trophoblast. למרות במבחנה ומודלים של בעלי חיים חיוניים, אקסטרפולציה של תוצאות ממחקרים כאלה אל השליה האנושית in vivo אינו ברור. מטרתנו הייתה לחקור את הפיסיולוגיה של השליה האנושית ב- vivo , ולהציג פרוטוקול מפורט של השיטה. ניצול הגישה תוך intraabinal כדי הווריד הרחם ממש לפני החתך הרחם במהלך ניתוח קיסרי מתוכנן, אנו אוספים דגימות דם מן הכלים נכנסות ויוצאות על הצדדים האימהית והעובר של השליה. בעת שילוב conמידות מדידה מ דגימות דם עם נפח מדידות זרימת הדם, אנו יכולים לכמת שליה שליה ועובר ושחרור של כל המתחם. יתר על כן, דגימות רקמות שליה מן אותם זוגות העובר אותו יכול לספק מדידות של צפיפות טרנספורטר ופעילות היבטים אחרים של פונקציות השליה in vivo . באמצעות שימוש אינטגרטיבי זה בשיטת הדגימה של 4 כלי הדם אנו יכולים לבחון חלק מהמושגים הנוכחיים של העברת חומרים מזינים ושל חילוף החומרים ב vivo , הן בהריונות נורמליים ופתולוגיים. יתר על כן, שיטה זו מאפשרת זיהוי של חומרים מופרשים על ידי השליה כדי במחזור האם, אשר יכול להיות תרומה חשובה לחיפוש עבור סמנים ביולוגיים של תפקוד לקוי של השליה.
Introduction
על פי המכונים הלאומיים לבריאות, ארה"ב, השליה היא האיבר הכי פחות מובן בגוף האדם 1 , 2 , 3 . קשה לגשת וללמוד את השליה האנושית in vivo ללא הטלת סיכונים לא מוסריים על ההריון המתמשך. מחקרים על תפקוד שליה אצל האדם מבוססים אפוא במידה רבה על מודלים במבחנה ובבדיקות ex vivo . רוב מחקרים קודמים vivo של תחבורה השליה ומטבוליזם בוצעו בבעלי חיים 4 , 5 , 6 . עם זאת, כמו מבנה השליה פונקציות להשתנות במידה ניכרת בין המינים, אקסטרפולציה של תוצאות מבעלי חיים לבני אדם חייב להיעשות בזהירות. רק מספר קטן יותר של בני אדם במחקרי vivo חקר ספיגת שליה ועובר ותחבורה תחת פיזיולוגיה נורמליתאל, ואף אחד מהם לא חקר את ההעברה המשולבת של מספר תרכובות 7 , 8 , 9 , 10 , 11 , 12 , 13 . מחקרים בסיסיים אלה מראים כי במחקרים של vivo של השליה האנושית הם ריאליים, וכי הם עשויים לשרת מטרות אחדות. ראשית, מושגים עכשוויים של פונקציות השליה הנובעים בעיקר ממחקרים במבחנה , בחיות לשעבר ובבעלי חיים עשויים להיות נבדקים בסביבה אנושית ובכך לספק תובנה חדשה וספציפית יותר לשיליה האנושית. שנית, המאפיינים של השליה התפקודית הקשורה לצמיחה עוברית חריגה, רעלת הריון, סוכרת אימהית, תסמונת מטבולית והפרעות מטבוליות אימהיות אחרות יכולות להיות מאופיינות יותר. שלישית, האדם במחקרים vivo לספק הזדמנות לפתח אבחוניםטיק כלי ניבוי של תפקוד השליה.
על רקע זה התכוונו להקים אוסף מקיף של נתונים פיזיולוגיים כדי לחקור את תפקוד השליה האנושית in vivo. במהלך ניתוח קיסרי מתוכנן, אנו מנצלים את הגישה intraabdominal לוריד הרחם כדי לאסוף דגימות דם מן הכלים הנכנסים והיוצאים על צדדי האם והעובר של השליה (שיטת דגימת 4 כלי). דגימות אלה משמשים לחישוב ההפרשים ריכוז arteriovenous זוגיות של חומרים מזינים וחומרים אחרים 14 . בנוסף, אנו מודדים את זרימת הדם על שני צידי השליה על ידי אולטרסאונד. כתוצאה מכך, ספיגה שליה ועובר של כל מתחם ניתן לכמת. יתר על כן, ניתן לקבוע חומרים משוחררים על ידי השליה כדי מחזורי האם והעובר 15 , 16 , 17 . כאשר משלביםד עם פרמטרים קליניים של האם והילד, וכן ניתוחים של שליה ורקמות רלוונטיות אחרות, שיטה זו יש פוטנציאל מלהיב לשלב היבטים רבים של פונקציות השליה in vivo באותם זוגות העובר.
Protocol
המחקר אושר על ידי אנשי הגנת הנתונים בבית החולים האוניברסיטאי של אוסלו והוועדה האזורית לאתיקה למחקר רפואי ובריאותי, דרום נורבגיה 2419/2011. כל המשתתפים חתמו על הסכמה מדעת בכתב להכללה.
1. הכנות
הערה: ציר זמן עבור ההליכים מתואר באיור 1 .
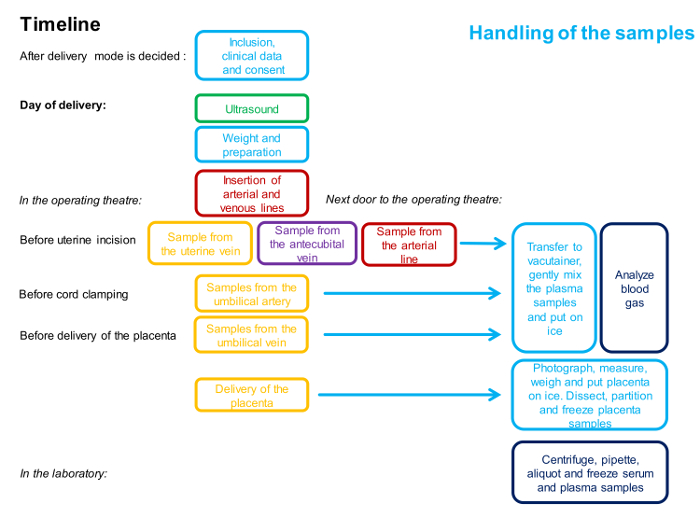
איור 1 : תרשים זרימה המתאר את התזמון ואת כוח האדם המעורב בהליך הדגימה של 4 כלי הדם.
צבע אחד מייצג אדם אחד. תיאור מפורט של השיטה ניתן בפרוטוקול. אנא לחץ כאן כדי להציג גרסה גדולה יותר של דמות זו.
- צוות
- ודא שכל אנשי הצוות הדרושים זמינים: מומחה לרפואת העובר בעל מיומנות גבוהה, שמנהל את מדידות האולטראסאונד, שני רופאים מיילדים המנתחים את הניתוח, אחד הרופאים ושתי האחיות אוספות את הדגימות, עוזר אחד המטפל בניתוחים של גז הדם ועוזר אחד המטפל דגימות אחרות ברצף ומיד לאחר האוסף.
הערה: במקרים של אוסף מתקדם יותר של רקמת השליה, נדרש אדם נוסף.
- ודא שכל אנשי הצוות הדרושים זמינים: מומחה לרפואת העובר בעל מיומנות גבוהה, שמנהל את מדידות האולטראסאונד, שני רופאים מיילדים המנתחים את הניתוח, אחד הרופאים ושתי האחיות אוספות את הדגימות, עוזר אחד המטפל בניתוחים של גז הדם ועוזר אחד המטפל דגימות אחרות ברצף ומיד לאחר האוסף.
- צִיוּד
- הכן את הציוד, 50 מ"ל של קרח קר 1 ז פוספט שנאגרו מלוחים (PBS), 25 מ"ל של פתרון ייצוב קר RNA ו 5 x 0.5 מ"ל של מתחם טמפרטורת חיתוך אופטימלי (אוקטובר). תווית את vacutainers וצינורות. ראה רשימה של ציוד זמני.
2. מאפיינים אימהיים
- רשום את המאפיינים הקליניים והאי-קליניים האימהיים בהכללה וחזור על השאלות הרלוונטיותלרבות משקל, בעת המשלוח. רשום את משך תקופת הצום לפני הניתוח קיסרי, וכל epotodes hypotensive המתרחשים במהלך הניתוח.
הערה: כלול את הנתונים הקליניים האימהיים המינימליים שדווחו בפרסום שפורסם לאחרונה מ- Global Pregnancy CoLaboratory (COLAB). מאמר זה כולל גם כמה היבטים חשובים מאוד בבחירת אוכלוסיות מחקר וצריך להתייחס בעת תכנון המחקר 18. - שקול להקליט מאפיינים אבהי, כולל אתני, גיל מדד מסת הגוף (BMI).
3. אולטרסאונד
- בצע את בדיקת אולטרסאונד דופלר ביום המסירה, עם הנשים במצב צום. בצע את הבדיקה במהלך תקופה של שלווה העובר, עם האשה במצב חצי שכיבה, מוטה מעט בכיוון רוחבי מול האזור של עניין על מנת למנוע דחיסה של אבי העורקים ו cava הווריד. צג את הפלט בעל ידי המדדים המכניים והתרמיים שבתצוגה.
- וריד טבורי
- דמיינו את הווריד הטבורי ב טרשת נפוצה סגיטלית או אלכסונית של הבטן העובר. למדוד את קוטר כלי פנימי בחלק ישר של הבטן הטבור תוך בטן, לפני כל הענפים נראים לעין. השתמש רגיל B- מצב לדמיין את כלי זווית זווית אנכית עבור מדידות בקוטר ולשמור כמה מסגרות אופטימלי עבור מדידות מאוחר יותר כדי למזער את ההשפעה של שינויים בקוטר pulsatile.
- חזור על המדידות חמש עד עשר פעמים 19 .
- באותו אתר, השתמשו באולטרסאונד של דופלר והתאימו את החללית כדי לקבל זווית חדירה נמוכה ככל האפשר (תמיד <30 °) כדי למדוד את המהירות המקסימלית בזמן (TAMX). השג את המהירות על פני תקופה של 3 - 5 שניות (זרימה לא פולטת).
- דמיינו את הווריד הטבורי ב טרשת נפוצה סגיטלית או אלכסונית של הבטן העובר. למדוד את קוטר כלי פנימי בחלק ישר של הבטן הטבור תוך בטן, לפני כל הענפים נראים לעין. השתמש רגיל B- מצב לדמיין את כלי זווית זווית אנכית עבור מדידות בקוטר ולשמור כמה מסגרות אופטימלי עבור מדידות מאוחר יותר כדי למזער את ההשפעה של שינויים בקוטר pulsatile.
- עורק הרחם
- השתמש דופלראולטרסאונד כדי להמחיש את עורק הרחם כפי שהוא חוצה את עורק השלפוחית החיצונית, מיד לאחר ענפים מן העורק iliac הפנימי. התאם את החללית באתר זה כדי לקבל זווית החדרה נמוכה (תמיד <30 °) ולמדוד TAMX. השג את מהירות המהירות הממוצעת של שלושה מחזורי לב.
- כפי שזה לא סביר לקבל זווית אנכית באותו אתר כמו TAMX נמדד, בצע את כלי דיסטלי כדי לקבל זווית נכונה למדידות קוטר קרוב ככל האתרים של מדידות קוטר כמו בר השגה. לא לכלול את מדידות קוטר אם כל כלי הנראה לעין מחוץ לאתר זה כפי שהוערך על ידי אולטרסאונד צבע דופלר.
- השתמש רגיל B- מצב לדמיין את כלי זווית זווית אנכית עבור מדידות בקוטר ולשמור כמה מסגרות אופטימלי עבור מדידות מאוחר יותר כדי למזער את ההשפעה של שינויים בקוטר pulsatile.
- חזור על המדידות חמש עד עשר פעמים 19 .
- הערה המיקום של השליה.
4. 4 כלי דם דגימה דם
הערה: ציר הזמן עבור ההליכים מתואר באיור 1 סקירה כללית של דגימות מתואר באיור 2 .
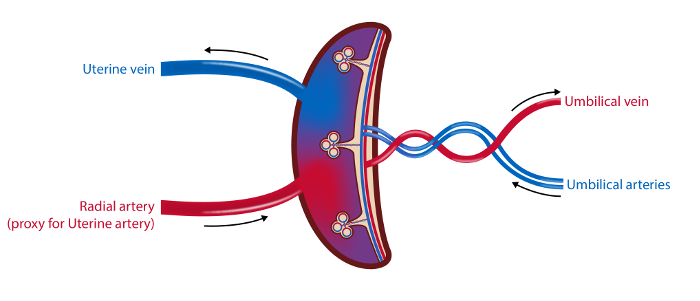
איור 2 : איור סכמטי של כלי הדם של השלד ואתרי הדגימה.
בשיטת הדגימה של 4 כלי הדם נלקחים דגימות דם מווריד הרחם, העורק הרדיאלי (כציר פרוקסי לעורק הרחם) ועורקי הטבור והווריד. זרימת הדם בעורק הרחם ואת הווריד הטבורי נמדדת על ידי אולטרסאונד. דגימות רקמות מן השליה נאספים. איור: Øystein H. Horgmo, אוניברסיטת אוסלו.5847fig2large.jpg "target =" _ blank "> אנא לחץ כאן כדי להציג גרסה גדולה יותר של דמות זו.
- נהלי בטיחות
- לספק את כל אנשי המבצע תיאטרון עם כפפות, חליפות שפשוף כירורגי, מסכות ו headwear.
- לספק את המנתחים ואנשי מחקר במגע עם שדה הפעולה עם חליפות שיחים כירורגי, מסכות, headwear, שמלות כפפות כפולות. משקפיים הם אופציונליים.
- לספק כוח אדם טיפול בדגימות דם עם כפפות.
- לספק אנשי טיפול דגימות שליה עם כפפות מסכה כירורגית. ההומוגניזציה דורשת שימוש ברדסים.
- הכנה בחדר הניתוח
- לתת תדרוך ולספק את הציוד לכל אנשי כי יסייע הדגימה לפני תחילת הניתוח.
- פנה אל רופא המרדים ואחות ההרדמה שיעזור עם הגישה העורקיית והפרידית היקפית, ולוודא כיאין נוזלים ניתנים תוך ורידי לפני הדגימה.
- תן שלושה מזרקים (10 מ"ל) ללא מחטים לאדם המסייע עם מדגם וריד antecubital ושני מזרקים (אחד 20 מ"ל ואחד 10 מ"ל) ו מזרק גז אחד (עם הפרין) לאדם המסייע עם העורק הרדיאלי.
- הכן שני מזרקים סטריליים (20 מ"ל), חמישה מזרקים סטריליים (10 מ"ל), שלושה "מחטים פרפר" ושני גז מזרקים עבור שדה הפעולה.
- גישה לכלי הדם.
- בצע את ההליך הסטנדרטי לפני הניתוח קיסרי כדי להבטיח גישה תוך ורידי תוך ורידי (iv).
הערה: וריד אנטיקוביטל עדיף כי קל יותר לצייר דוגמאות מאתר זה. - למקם את העורק הרדיאלי על פרק היד על ידי אולטרסאונד או על ידי מישוש. לאחר 0.5 מ"ל של שיכוך לידוקאין תת עורית, במקום קו עורק לתוך העורק הרדיאלי. ננטוש את הדגימה מאתר זה במקרה של שלוש כניסות כושלות, אואם האישה חווה כאב במהלך ההכנסה.
הערה: בצע את הניתוח של ניתוח קיסרי על פי הנוהל הסטנדרטי. רק ההתאמות הדרושות להליך הדגימה מפורטות להלן.
- בצע את ההליך הסטנדרטי לפני הניתוח קיסרי כדי להבטיח גישה תוך ורידי תוך ורידי (iv).
- דגימות דם אימהיות
הערה: השג את כל שלוש דגימות הדם האימהיות (וריד הרחם, העורק הרדיאלי והוריד האנטי-ווביטאלי) בו זמנית לפני חתך הרחם.- עבור הווריד הרחם, לאחר פתיחת חלל הבטן, להשתמש מפשק להרים את דופן הבטן לחשוף את הענפים העיקריים של הוורידים הרחם על הצדדים anterolateral של הרחם. השג דם בענפי וריד הרחם באותו צד כמו שליה ככל האפשר או להשתמש במקלדת הווריד הבולטת ביותר אם השיליה ממוקמת קו האמצע הרחם.
- הכנס מחט פרפר על מזרק גז דם בווריד הרחם בזווית של כ 30 מעלות ולאסוף דם באמצעות שאיפה עדינה, כדי להימנעהמוליזה. בעוד בזהירות לאבטח את המיקום הרביעי של מחט פרפר, להחליף את מזרק גז מלא דם על ידי 20 מ"ל ו מזרק 10 מ"ל ברציפות.
הערה: גישה אופטימלית מובטחת בצורה הטובה ביותר כאשר עומדים בצד הנגדי של הווריד הרחם הנבחר.
- הכנס מחט פרפר על מזרק גז דם בווריד הרחם בזווית של כ 30 מעלות ולאסוף דם באמצעות שאיפה עדינה, כדי להימנעהמוליזה. בעוד בזהירות לאבטח את המיקום הרביעי של מחט פרפר, להחליף את מזרק גז מלא דם על ידי 20 מ"ל ו מזרק 10 מ"ל ברציפות.
- עבור עורק הרדיאלי, לשאוב מן הקו הפנימי עורק. מחק את 5 מ"ל הראשון, ולאחר מכן לשאוב 3 מ"ל מזרק הפרין עבור ניתוחי גז, ואחריו 3 מ"ל בשני מזרקים (20 + 10 מ"ל).
- עבור הווריד האנטי-ווביטאלי, שואפים בעדינות מן הקטטר תוך ורידי. מחק את 5 מ"ל הראשון, ולאחר מכן לשאוב 30 מ"ל בשלושה מזרקים (10 מ"ל).
- בצע בדיקה סופית של אתר הדגימה על הווריד הרחם לפני שתתחיל לסגור את הבטן.
- עבור הווריד הרחם, לאחר פתיחת חלל הבטן, להשתמש מפשק להרים את דופן הבטן לחשוף את הענפים העיקריים של הוורידים הרחם על הצדדים anterolateral של הרחם. השג דם בענפי וריד הרחם באותו צד כמו שליה ככל האפשר או להשתמש במקלדת הווריד הבולטת ביותר אם השיליה ממוקמת קו האמצע הרחם.
- דגימות דם עובריות
- כאשר הילד נולד, מיד לשאוב דם מן העורק הטבורי, ללא clamping חבל הטבור או מתן השליה. התחל שנינותH מזרק לניתוח גז, ופעל עם שלוש מזרקים 10 מ"ל אם אפשר.
- כאשר הדגימות עורק מאובטח, מהדק את החבל ואת היד הילד למיילדת לפני הדגימה של וריד הטבור (גז דם 20 + 10 מ"ל מזרקים).
הערה: השג את כל דגימות הטבור בתוך שניות של לידה ועם השליה באתרה, אלא אם כן היא מנותקת באופן ספונטני. - בצע את ההמלצות הנורבגית על הידוק כבל מאוחר. במקרה של ילד במצוקה, מהדק וחותך את הכבל מיד ואת היד את הילד המיילדת ו neonatologist.
- טיפול בדגימות דם
- שים את גז מזרקים על הקרח תוך הכנת שאר דגימות הדם, ולנתח אותם מנתח גז בדם בתוך 5 דקות.
- מעבירים את דגימות הדם מיד vacutainers ומקום צינורות פלזמה על נדנדה עבור 1 - 2 דקות לפני לשים אותם על הקרח. השאירו את צינורות הסרום על העבודהספסל אטורי להתיישב במשך 30 דקות.
הערה: זהו שלב קריטי בהליך זה צריך תשומת לב נוספת, כי דגימות מכל חמשת האתרים צריך להיות מוכן בו זמנית כדי להבטיח איכות טובה. - צנטריפוגה דגימות פלזמה בהקדם האפשרי, תוך 30 דקות, ב 6 מעלות צלזיוס, 2,500 xG במשך 20 דקות.
- לאחר 30 דקות, צנטריפוגה דגימות בסרום בטמפרטורת החדר למשך 10 דקות ב 2,500 x גרם.
- Aliquot supernatants בזהירות 2 צינורות cryo מ"ל, משאיר 0.5 מ"ל של supernatant מעל גלולה כדי להבטיח טסיות פלסמה חינם.
- חנות דגימות ב -80 מעלות צלזיוס.
5. אוסף של רקמת השליה
- מניחים את השליה שטוח על מגש קרח לנתיחה צונן בהקדם האפשרי לאחר שהוא נמסר. צילום ולמדוד את הקוטר הארוך ביותר ואת הקוטר ב 90 מעלות.
- שקלו את השליה.
- רשום את המשקל, את שני הקטרים, כל gRoss פתולוגיה, מספר כלי החוט ואת מרווח הזמן בין משלוח כאשר השיליה הונחה על הקרח.
הערה: שלחו את השליה לבדיקה פתולוגית, אם צוין קלינית. - מניחים את השליה עם פני האם מול למעלה ולזהות 4 - 5 אתרי הדגימה ממוקמים באופן אקראי בכל רבע של השליה, הימנעות תחומים של הפתולוגיה כנה. הסר את decidua באמצעות מספריים לחתוך 3 - 5 מ"מ מן פני האם. איסוף 1 - 2 ס"מ 3 חתיכת רקמת וילות מכל אתר.
- לשטוף את הרקמה שנאספו בעדינות 50 מ"ל של 1M קר 1 PBS. מחלקים למספר חלקים מכל אתר דגימה ואליקוט.
הערה: גודל החלקים של השליה יהיה תלוי בניתוח המתוכנן. - הוסף aliquots של 0.1 - 0.5 ס"מ 3 דגימות רקמות 5 צינורות cryo ו הצמד להקפיא חנקן נוזלי.
- הוסף חתיכות קטנות של 0.1 - 0.2 ס"מ 3 לצינור עם 25 מ"ל של פתרון ייצוב RNA. חנות ב 46; C במשך 24 שעות, להשליך את הפתרון ייצוב ייצוב ולהחליף אותו. הַקפָּאָה.
- הוסף חתיכות של 0.5 ס"מ 3 כדי 5 cryo צינורות עם 0.5 מ"ל של אוקטובר, למעלה עם אוקטובר, לערבב להקפיא.
- חנות דגימות ב -80 מעלות צלזיוס עד הניתוח.
הערה: Burton et al. מספק סקירה מצוינת של היבטים מעשיים של דגימת השליה בהתאם לניתוחים מתוכננים. 20 שקול להכין את הרקמה הנותרת לבידוד של הממברנות microvillous והבזליים, וכדי לאסוף רקמה נשית על ידי טכניקה יניקה ואקום. 21 , 22
6. מאפיינים ילודים
- הקלט את המאפיינים הילודים, כולל אפגר-ניקוד (1, 5 ו -10 דקות), מין, משקל, אורך, גיל ההיריון וקבלה ליחידה לטיפול נמרץ בילודים (אורך ותוצאה של שהייה).
- שקול למדוד את הרכב הגוף הלידה על ידי מדידות אנתרופומטריות, האוויר לעקוףמנטלית או רנטגן כפול של רנטגן. 23 , 24
7. חישובים
- נניח הרכב דם דומה בעורק הרדיאלי והרחם ולחשב את ההבדל ריכוז arterilacental uteroplacental.
הפרשת ריכוז arteriovacental Uteroplacental = C A - C V
טבורי ורידי - ריכוז העורקים ההבדל = C V - C א
איפה C הוא ריכוז עם תחתי: א, עורק הרדיאלי; V, הווריד הרחם; V הווריד הטבורי ועורק הטבור. - חישוב נפח זרימת הדם, מ"ל / דקה (Q):
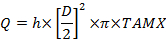
כאשר D הוא קוטר הספינה (ס"מ), TAMX היא מהירות הזמן המקסימלית בזמן ו - h הוא מקדם עבור פרופיל הדם המרחבי פרופיל. השתמש 0.5 כמו מקדם עבור וריד הטבור0.6 עבור עורק הרחם 25 , 26 . - חישוב ספיגת השלייה ושחרור על פי העיקרון של פיק:
ספיגה Uteroplacental = ( C A - C V ) x Qm
ספיגה העובר = (v C - C) X Q f
תחביבים: מ ', אמהית ו- f, עוברית.
תוצאות
שיטת הדגימה של 4 כלי הדם מיושמת בקליניקה הקלינית וקיבלנו בהצלחה דגימות דם מ -209 זוגות אם / תינוקות. ב 128 של אלה השגנו גם למדוד את נפח הדם. דגימה מלאה של 4 כלי דם ומדידות זרימה באיכות טובה של כלי הדם האימהיים והעובריים התקבלו ב -70 זוגות של האם-עובר (
Discussion
שיטת הדגימה של 4 כלי השיט היא רלוונטית לשלוש מטרות עיקריות. ראשית, ניתן להשתמש בו כדי ללמוד כיצד חומרים ספציפיים נלקחים על ידי השליה בצד האימהי ואולי מועברים למחזור הטבור ולעובר, כפי שמוצג על ידי גלוקוז שלנו ומחקרים חומצות אמיניות. שנית, השיטה רלוונטית מאוד לחקר חו...
Disclosures
למחברים אין מה לחשוף.
Acknowledgements
בראש ובראשונה, אנו מודים בכנות לאמהות שהשתתפו בפרויקט זה. לאחר מכן, אנו מכירים בכל הצוות אשר סייע ו להקל על הליך הדגימה, מרדים, אחות הרדמה אחיות כירורגית. הפרויקט לא היה אפשרי ללא מימון של דרום מזרח נורבגיה אזור הבריאות האזורי ואת היחידה המייעצת הנורבגית על בריאות האישה, אוניברסיטת אוסלו מימון מקומי המסופק על ידי בית החולים של אוניברסיטת אוסלו.
Materials
| Name | Company | Catalog Number | Comments |
| Maternal body composition | |||
| Impedance scale | Tanita | or similar | |
| Ultrasound measurements | |||
| Sequoia 512 ultrasound machine | Acuson | equipped with a curved transducer with colour and pulsewave Doppler (frequency bandwidth 2-6 MHz) | |
| Blood samples | |||
| Arerial cannula | BD Medical | 682245 | or similar |
| 20cc Eccentric Luer Tip Syringe without Needle | Termo | SS-20ES | or similar. 3 needed. |
| 10cc Eccentric Luer Tip Syringe without Needle | Termo | SS-10ES | or similar. 9 needed. |
| 5cc 6% Luer Syringe without Needle | Termo | SS-05S1 | or similar. 2 needed. |
| Arterial blood gas syringe | Radiometer Medical | or similar. 4 needed. | |
| Sterile winged needle connected to flexible tubing, 21 gauge | Greiner Bio-One | 450081 | (intended for single use).3 needed. |
| Vacutainer tube 6 mL EDTA | Greiner Bio-One | 456043 | or similar. Label with sample site. 10 needed. |
| Vacutainer tube 5 ml LH Lithium Heparin Separator | Greiner Bio-One | 456305 | or similar. Label with sample site. 5 needed. |
| Vacutainer tube 6 mL Serum Clot Activator | Greiner Bio-One | 456089 | or similar. Label with sample site. 5 needed. |
| Vacutainer tube 3 ml 9NC Coagulation sodium citrate 3,2% | Greiner Bio-One | 454334 | or similar. Label with sample site. 5 needed. |
| Cryogenic vials, 2.0 mL | Corning | 430488 | or similar. Label with sample site, serum/type of plasma and ID. 90 needed. |
| Marked trays to transport the syringes | to transport the blood samples in the operation theatre | ||
| Rocker | for gentle mixing of the samples | ||
| Ice | in styrofoam box | ||
| Liquid nitrogen | in appropriate container | ||
| Placenta samples | |||
| Metal tray | |||
| Ice | in styrofoam box | ||
| Calibrated scale | |||
| Metal ruler | |||
| 1 M Phosphate buffered saline | Sigma | D1408 | or similar. Dilute 10 M to 1M before use |
| RNA stabilization solution | Sigma | R0901-500ML | or similar |
| Optimal Cutting Temperature (O.C.T.) compound | vwr | 361603E | or similar |
| Cryogenic vials, 2.0 mL | Corning | 430488 | or similar. Label with sample site. content and ID. 10 needed. |
| Centrifuge tubes, conical bottom 50 mL | Greiner Bio-One | 227,285 | or similar. Label with "RNA later", sample site and ID. 2 needed. |
| Liquid nitrogen | in appropriate container | ||
| Fetal body composition | |||
| Calibrated scale | |||
| Measuring tape |
References
- Jansson, T., Powell, T. L. Role of the placenta in fetal programming: underlying mechanisms and potential interventional approaches. Clin Sci (Lond). 113 (1), 1-13 (2007).
- Hanson, M. A., Gluckman, P. D. Early developmental conditioning of later health and disease: physiology or pathophysiology. Physiol Rev. 94 (4), 1027-1076 (2014).
- Guttmacher, A. E., Spong, C. Y. The human placenta project: it's time for real time. Am J Obstet Gynecol. 213, 3-5 (2015).
- Battaglia, F. C., Regnault, T. R. Placental transport and metabolism of amino acids. Placenta. 22 (2-3), 145-161 (2001).
- Hay, W. W. Placental-fetal glucose exchange and fetal glucose metabolism. Trans Am Clin Climatol Assoc. 117, 321-339 (2006).
- Woollett, L. A. Review: Transport of maternal cholesterol to the fetal circulation. Placenta. 32, 218-221 (2011).
- Prenton, M. A., Young, M. Umbilical vein-artery and uterine arterio-venous plasma amino acid differences (in the human subject). J Obstet Gynaecol Br Commonw. 76 (5), 404-411 (1969).
- Cetin, I., et al. Plasma and erythrocyte amino acids in mother and fetus. Biol Neonate. 60 (2), 83-91 (1991).
- Filshie, G. M., Anstey, M. D. The distribution of arachidonic acid in plasma and tissues of patients near term undergoing elective or emergency Caesarean section. Br J Obstet Gynaecol. 85 (2), 119-123 (1978).
- Haberey, P. P., Schaefer, A., Nisand, I., Dellenbach, P. The fate and importance of fetal lactate in the human placenta -a new hypothesis. J Perinat Med. 10 (2), 127-129 (1982).
- Prendergast, C. H., et al. Glucose production by the human placenta in vivo. Placenta. 20 (7), 591-598 (1999).
- Metzger, B. E., Rodeck, C., Freinkel, N., Price, J., Young, M. Transplacental arteriovenous gradients for glucose, insulin, glucagon and placental lactogen during normoglycaemia in human pregnancy at term. Placenta. 6 (4), 347-354 (1985).
- Zamudio, S., et al. Hypoglycemia and the origin of hypoxia-induced reduction in human fetal growth. PLoS One. 5 (1), 8551 (2010).
- Holme, A. M., Roland, M. C., Lorentzen, B., Michelsen, T. M., Henriksen, T. Placental glucose transfer: a human in vivo study. PLoS One. 10 (2), 0117084 (2015).
- Holme, A. M., Roland, M. C., Henriksen, T., Michelsen, T. M. In vivo uteroplacental release of placental growth factor and soluble Fms-like tyrosine kinase-1 in normal and preeclamptic pregnancies. Am J Obstet Gynecol. 215 (6), 781-782 (2016).
- Paasche Roland, M. C., Lorentzen, B., Godang, K., Henriksen, T. Uteroplacental arterio-venous difference in soluble VEGFR-1 (sFlt-1), but not in soluble endoglin concentrations in preeclampsia. Placenta. 33 (3), 224-226 (2012).
- Brar, H. S., et al. Uteroplacental unit as a source of elevated circulating prorenin levels in normal pregnancy. Am J Obstet Gynecol. 155 (6), 1223-1226 (1986).
- Myatt, L., et al. Strategy for standardization of preeclampsia research study design. Hypertension. 63 (6), 1293-1301 (2014).
- Kiserud, T., Rasmussen, S. How repeat measurements affect the mean diameter of the umbilical vein and the ductus venosus. Ultrasound Obstet Gynecol. 11 (6), 419-425 (1998).
- Burton, G. J., et al. Optimising sample collection for placental research. Placenta. 35 (1), 9-22 (2014).
- Illsley, N. P., Wang, Z. Q., Gray, A., Sellers, M. C., Jacobs, M. M. Simultaneous preparation of paired, syncytial, microvillous and basal membranes from human placenta. Biochim Biophys Acta. 1029 (2), 218-226 (1990).
- Staff, A. C., Ranheim, T., Khoury, J., Henriksen, T. Increased contents of phospholipids, cholesterol, and lipid peroxides in decidua basalis in women with preeclampsia. Am J Obstet Gynecol. 180 (3), 587-592 (1999).
- Catalano, P. M., Thomas, A. J., Avallone, D. A., Amini, S. B. Anthropometric estimation of neonatal body composition. Am J Obstet Gynecol. 173 (4), 1176-1181 (1995).
- Ellis, K. J., et al. Body-composition assessment in infancy: air-displacement plethysmography compared with a reference 4-compartment model. Am J Clin Nutr. 85 (1), 90-95 (2007).
- Haugen, G., Kiserud, T., Godfrey, K., Crozier, S., Hanson, M. Portal and umbilical venous blood supply to the liver in the human fetus near term. Ultrasound Obstet Gynecol. 24 (6), 599-605 (2004).
- Acharya, G., et al. Experimental validation of uterine artery volume blood flow measurement by Doppler ultrasonography in pregnant sheep. Ultrasound Obstet Gynecol. 29 (4), 401-406 (2007).
- Wu, X., et al. Glutamate-glutamine cycle and exchange in the placenta-fetus unit during late pregnancy. Amino Acids. 47 (1), 45-53 (2015).
- Tuckey, R. C. Progesterone synthesis by the human placenta. Placenta. 26 (4), 273-281 (2005).
- Simmons, M. A., Meschia, G., Makowski, E. L., Battaglia, F. C. Fetal metabolic response to maternal starvation. Pediatr Res. 8 (10), 830-836 (1974).
- Simmons, M. A., Jones, M. D., Battaglia, F. C., Meschia, G. Insulin effect on fetal glucose utilization. Pediatr Res. 12 (2), 90-92 (1978).
- Bujold, E., et al. Evidence supporting that the excess of the sVEGFR-1 concentration in maternal plasma in preeclampsia has a uterine origin. J Matern Fetal Neonatal Med. 18 (1), 9-16 (2005).
- Jansson, T., Aye, I. L., Goberdhan, D. C. The emerging role of mTORC1 signaling in placental nutrient-sensing. Placenta. 33, 23-29 (2012).
- Cetin, I. Placental transport of amino acids in normal and growth-restricted pregnancies. Eur J Obstet Gynecol Reprod Biol. 110, 50-54 (2003).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved