Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
İnsan vücudunun fizyolojisini bütünleştiren 4 damarlı Örnekleme Yaklaşımı
Bu Makalede
Özet
Bu dönemde in vivo insan plasental fizyoloji çalışmak için ayrıntılı bir yöntem sunulmaktadır. Yöntem, plasentanın maternal ve fetal taraflarındaki gelen ve giden damarlardan alınan kan örneklerini, hacimsel kan akışı ve plasental doku örneklemesi ile ilgili ultrason ölçümleri ile birleştirir.
Özet
Insan plasenta rahimde iken hala araştırma için son derece erişilemez. Bu nedenle, plasental anatomi, hemodinamik ve gebeliğin süresindeki türler arasında yüksek çeşitliliğe rağmen, insan plasental fizyolojisinin in vivo olarak mevcut anlayışı büyük oranda hayvan çalışmalarına dayanmaktadır. İnsan plasenta çalışmalarının büyük çoğunluğu ex vivo perfüzyon çalışmaları veya in vitro trofoblast çalışmalardır. In vitro çalışmalar ve hayvan modelleri çok önemlidir, ancak bu tür çalışmaların sonuçlarının insan plasentasına in vivo ekstrapolasyonu kesin değildir. İnsana plasenta fizyolojisini venöz dönemde çalışmayı ve yöntemin ayrıntılı bir protokolünü sunmayı amaçladık. Planlanan sezaryen sırasında uterin vene uterin vene girişin uterus kesi öncesi istismar edilmesi, gelen ve giden damarlardan plasentanın maternal ve fetal taraflarındaki kan örneklerini toplarız. Konuyu birleştirirkenHacimsel kan akımı ölçümleri ile kan numunelerinden elde edilen santrasyon ölçümleri sayesinde, herhangi bir bileşiğin plasental ve fetal alımını ve salımını nicel olarak değerlendirebiliriz. Dahası, aynı anne-fetus çiftlerinden elde edilen plasental doku örnekleri, taşıyıcı yoğunluğunu, aktivitesini ve plasental fonksiyonların diğer yönlerini in vivo olarak ölçebilir . 4 damarlı örnekleme yönteminin bu entegre kullanımı sayesinde hem normal hem de patolojik gebeliklerde plasental besin transferinin ve metabolizmasının bazılarını in vivo olarak test edebiliyoruz. Ayrıca, bu yöntem, plasenta tarafından salgılanan maddelerin maternal dolaşımda tanımlanmasını sağlar ve bu da plasenta disfonksiyonunun biyolojik belirteçlerinin araştırılmasına önemli katkı sağlayabilir.
Giriş
Ulusal Sağlık Enstitüsüne (ABD) göre, plasenta insan vücudunda en az anlaşılmış organ 1 , 2 , 3'tür . Devam eden gebelikte etik olmayan riskler getirmeksizin insan plasentasını in vivo erişmek ve incelemek zordur. İnsandaki plasental fonksiyon çalışmaları büyük oranda in vitro ve ex vivo modellere dayanır. Plasental nakil ve metabolizma ile ilgili önceki in vivo çalışmaların çoğunluğu hayvanlar 4 , 5 , 6'da gerçekleştirilmiştir . Bununla birlikte, plasental yapı ve fonksiyonlar türler arasında önemli farklılık gösterdiğinden, hayvanlardan insanlara yapılan sonuçların dikkatle kullanılması gerekir. İn vivo çalışmaların sadece birkaç küçük insan plasental ve fetal alımını ve normal fizyolojikVe hiçbiri 7 , 8 , 9 , 10 , 11 , 12 , 13 numaralı bileşiklerin bir bütün olarak transferini araştırmamıştır. Bu temel çalışmalar insan plasentasının in vivo çalışmalarının uygulanabilir olduğunu ve çeşitli amaçlara hizmet edebileceğini göstermektedir. Birincisi, plasental fonksiyonların temelde in vitro , ex vivo ve hayvan çalışmalarından türetilen güncel kavramları insan ortamında test edilerek insan plasentasına yeni ve daha spesifik bir bakış açısı getirilebilir. İkincisi, anormal fetal büyüme, preeklampsi, maternal diyabet, metabolik sendrom ve diğer maternal metabolik bozukluklarla ilişkili disfonksiyonel plasentanın özellikleri daha iyi karakterize edilebilir. Üçüncü olarak, insan in vivo çalışmalar teşhis geliştirme fırsatı sağlarPlasental fonksiyonun tik ve prediktif araçları.
Bu arka planda insan plasental fonksiyonunu in vivo araştırmak için kapsamlı bir fizyolojik veri topluluğu oluşturmayı amaçladık . Planlı bir sezaryen sırasında, plasentanın maternal ve fetal taraflarındaki (4 damarlı örnekleme yöntemi) gelen ve giden damarlardan kan örnekleri toplamak için intraabdominal uterin ven girişini kullanırız. Bu numuneler besin maddeleri ve diğer maddelerin eşleştirilmiş arteriovenöz konsantrasyon farklılıklarını hesaplamak için kullanılır 14 . Buna ek olarak, ultrason ile plasentanın her iki tarafındaki hacimsel kan akışını ölçüyoruz. Sonuç olarak, herhangi bir bileşiğin plasental ve fetal alım miktarı belirlenebilir. Ayrıca plasenta tarafından maternal ve fetal dolaşımlara 15 , 16 , 17 serbest bırakılan maddelerin belirlenmesi mümkündür. BirleştirildiğindeD anne ve çocuğun klinik parametreleri ile birlikte, ve plasental ve diğer ilgili dokuların analizleri ile, bu yöntem, plasenta fonksiyonlarının birçok yönünü in vivo aynı anne-fetus çiftlerine entegre etmek için heyecan verici bir potansiyele sahiptir.
Protokol
Çalışma, Oslo Üniversitesi Hastanesi'ndeki veri koruma görevlileri ve Güney Norveç 2419/2011 Tıbbi ve Sağlık Araştırma Etikleri Bölgesel Komitesi tarafından onaylandı. Tüm katılımcılar, dahil edilme konusunda yazılı bir bilgilendirilmiş onam imzaladılar.
1. Preparatlar
NOT: İşlemler için bir zaman çizelgesi Şekil 1'de özetlenmiştir.
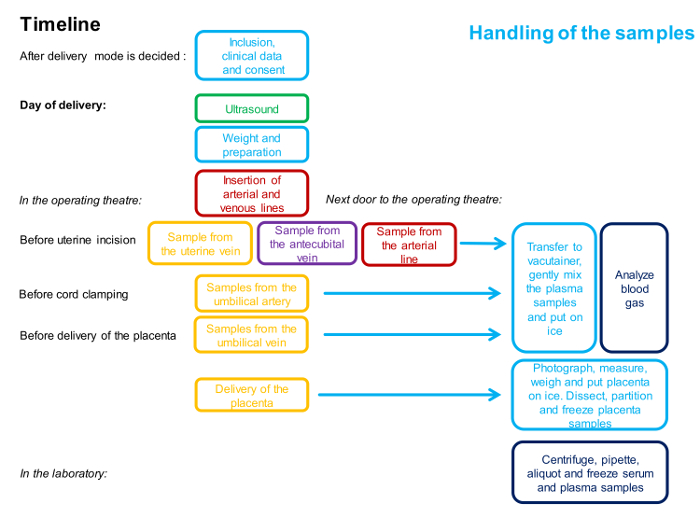
Şekil 1 : 4 damarlı Numune Alma İşleminde Zamanlamayı ve Personel İfadesini Tanımlayan Akış Şeması.
Tek renk bir kişiyi temsil eder. Yöntemin ayrıntılı açıklaması protokolde verilmiştir. Bu rakamın daha büyük bir versiyonunu görmek için lütfen tıklayınız.
- Personel
- Gerekli tüm personelin mevcut olduğundan emin olun: Ultrason ölçümlerini yapan oldukça yetenekli bir Fetal Tıp uzmanı, cerrahiyi yürüten iki doğum uzmanı, doğum uzmanlarından ve numuneleri toplayan iki hemşireden biri, kan gazı analizlerini yapan bir asistanı ve Diğer numuneler toplama işlemini ard arda ve derhal gerçekleştirdikten sonra.
NOT: Plasental dokunun daha gelişmiş toplanması durumunda ilave bir kişiye ihtiyaç vardır.
- Gerekli tüm personelin mevcut olduğundan emin olun: Ultrason ölçümlerini yapan oldukça yetenekli bir Fetal Tıp uzmanı, cerrahiyi yürüten iki doğum uzmanı, doğum uzmanlarından ve numuneleri toplayan iki hemşireden biri, kan gazı analizlerini yapan bir asistanı ve Diğer numuneler toplama işlemini ard arda ve derhal gerçekleştirdikten sonra.
- ekipman
- Ekipman, buz soğukluğunda 1 M fosfat tamponlu salin (PBS), 25 mL soğuk RNA stabilize edici çözelti ve 5 x 0.5 mL optimal kesme sıcaklığı bileşiği (OCT) hazırlayın. Vacutainers ve tüpleri etiketleyin. Deneysel ekipman listesini görün.
2. Anaokulleri
- Annelik klinik ve klinik dışı özelliklerini dahil ederek kaydedin ve ilgili soruları tekrarlayın veDoğumlar, doğum sırasında ağırlık dahil olmak üzere. Sezaryen öncesi oruç tutma süresini ve cerrahi sırasında meydana gelen herhangi bir hipotansif bölüme dikkat edin.
Not: Global pregnancy coLaboratory (COLAB) 'dan yeni yayınlanan en az maternal klinik veri kümesini ekleyin. Bu makale aynı zamanda çalışma popülasyonlarının seçiminde çok önemli bazı yönleri içermektedir ve çalışmayı planlarken ele alınmalıdır 18 . - Etnik köken, yaş ve beden kitle indeksi (BKİ) de dahil olmak üzere baba özelliklerini kaydetmeyi düşünün.
3. Ultrason
- Doppler ultrason muayenesini doğum gününde, kadınlar açlıkta gerçekleştirin. Muayene, aort ve vena kava basısından kaçınmak için, yarı-sırtüstü konumdaki kadının fetal durgunluk döneminde, ilgi bölgesinin biraz lateralinde eğildiğinde gerçekleştirilir. Içindeki çıktıyı izleyinYoğunluğu ekrandaki mekanik ve termik indekslerle belirtir.
- Umbilikal ven
- Göbek karını sagital veya oblik bir transeksiyonda göbekten damarı görselleştirin. Karın içi umbilikal venin düz bölümündeki iç büzgeci çapını, görülebilen dallardan önce ölçün. Normal B-modunu kullanın ve çap ölçümleri için tekneyi dik açılım açısı ile görselleştirin ve pulsatil çap değişikliklerinin etkisini en aza indirgemek için sonraki ölçümler için birkaç optimum kareyi tutun.
- Ölçümleri 5-10 kez tekrarlayın 19 .
- Aynı yerde, Doppler ultrasonu kullanın ve zaman ortalamalı maksimum hızı (TAMX) ölçmek için mümkün olduğunca düşük (30 ° 'lik) bir insonasyon açısı elde etmek için probu ayarlayın. Hızı 3 - 5 s'lik bir periyot boyunca elde edin (titreşimsiz akış).
- Göbek karını sagital veya oblik bir transeksiyonda göbekten damarı görselleştirin. Karın içi umbilikal venin düz bölümündeki iç büzgeci çapını, görülebilen dallardan önce ölçün. Normal B-modunu kullanın ve çap ölçümleri için tekneyi dik açılım açısı ile görselleştirin ve pulsatil çap değişikliklerinin etkisini en aza indirgemek için sonraki ölçümler için birkaç optimum kareyi tutun.
- Uterus arteri
- Doppler kullanUltrason, internal iliyak arterden dallandıktan hemen sonra, harici iliak arteri geçtiği için uterin arteri görselleştirir. Düşük insonasyon açısı (her zaman <30 °) elde etmek için probu bu bölgede ayarlayın ve TAMX'i ölçün. Hızı üç kalp çevriminin ortalama hızı olarak alın.
- TAMX ölçülene kadar aynı yerde dikey bir açı elde etmesi pek mümkün olmadığından, çap ölçümleri alanlarına yakın ulaşılabilen çap ölçümleri için doğru bir açı elde etmek için, distal olarak damarı takip edin. Renkli Doppler ultrasonografi ile değerlendirildiğinde görünür damarlar bu bölgeden önce kesilirse çap ölçümlerini hariç tutun.
- Normal B-modunu kullanın ve çap ölçümleri için tekneyi dik açılım açısı ile görselleştirin ve pulsatil çap değişikliklerinin etkisini en aza indirgemek için sonraki ölçümler için birkaç optimum kareyi tutun.
- Ölçümleri 5-10 kez tekrarlayın 19 .
- Plasentanın konumunu not edin.
4. 4 damarlı Kan Örneklemesi
NOT: İşlemler için zaman çizelgesi Şekil 1'de özetlenmiştir ve örneklerin genel görünümü Şekil 2'de gösterilmiştir.
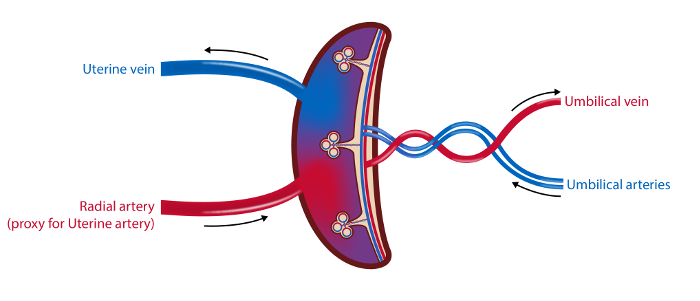
Şekil 2 : Plasental Vasküler Yapının Şematik Gösterimi ve Numune Alma Siteleri.
4 damarlı örnekleme yönteminde, uterin ven, radial arter (uterin arter için bir vekil olarak) ve göbek arterleri ve damardan kan örnekleri alınır. Uterin arter ve göbek bağı kan akımı ultrason ile ölçülür. Plasentanın doku örnekleri toplanır. Resim: Øystein H. Horgmo, Oslo Üniversitesi.5847fig2large.jpg "target =" _ blank "> Bu figürde daha büyük bir versiyonunu görmek için lütfen tıklayınız.
- Güvenlik prosedürleri
- Operasyon tiyatrosundaki tüm personele eldiven, cerrahi eldiven takımı, maskeler ve şapkalar takın.
- Operasyon alanıyla temas halindeki cerrahları ve araştırma personelini cerrahi kese elbiseleri, maskeler, şapkalar, önlüklar ve çift eldiven ile sağlayın. Gözlük isteğe bağlıdır.
- Kan numunelerini eldivenlerle tutan personel sağlayın.
- Plasenta numunelerine eldiven ve cerrahi maskeyle müdahale eden personel sağlayın. Homojenizasyon kaputların kullanılmasını gerektirir.
- Operasyon tiyatrosunda hazırlık
- Bir brifing verin ve ekipmanı ameliyat başlamadan önce numuneye yardımcı olacak tüm personele verin.
- Gerekli periferik arteryel ve venöz girişe yardımcı olacak anestezi uzmanı ve anestezi hemşiresinin adresini öğrenin veNumune almadan önce intravenöz olarak hiçbir sıvı verilmez.
- Antakübital ven örneğini ve iki şırıngayı (biri 20 mL ve bir tane de 10 mL) ve radial arteri destekleyen kişiye bir kan gazı şırıngasını (heparin ile) destekleyen kişiye iğneler olmadan üç şırınga (10 mL) verin.
- Ameliyat sahası için iki steril şırınga (20 mL), beş steril şırınga (10 mL), üç "kelebek iğne" ve iki kan gazı şırıngası hazırlayın.
- Kan damarlarına erişim.
- Periferik intravenöz (iv) erişimi sağlamak için sezaryen öncesi standart prosedür izleyin.
NOT: Antecubital ven tercih edilir, çünkü bu siteden örnek almak daha kolaydır. - Radial arteri ultrasonla veya palpasyonla bilekte lokalize edin. 0.5 mL subkutanöz lidokain analjeziyi takiben, radial artere bir arteriyel hat yerleştirin. Üç başarısız ekleme olması durumunda örneklemeyi bu siteden terk edin veyaEğer kadın yerleştirme sırasında acı çekerse.
NOT: Standart prosedüre göre sezaryonun cerrahi prosedürünü uygulayın. Yalnızca örnekleme prosedürü için gereken ayarlamalar aşağıda belirtilmiştir.
- Periferik intravenöz (iv) erişimi sağlamak için sezaryen öncesi standart prosedür izleyin.
- Anne kan örnekleri
NOT: Uterus insizyonundan önce aynı anda üç anne kan örneğini (uterin ven, radial arter ve antekübital ven) elde edin.- Uterin damar için, karın boşluğunu açtıktan sonra, karın duvarını kaldırmak ve uterusun anterolateral kenarlarındaki uterin venlerin ana dallarını ortaya çıkarmak için bir geri çekici kullanın. Mümkün olduğunca plasenta ile aynı yönde uterin damar dallarından kan alın veya plasenta rahim orta çizgisinde bulunduğu takdirde en belirgin damarı pleksus kullanın.
- Uterin damardaki bir kan gazı şırıngasına yaklaşık 30 derecelik bir açıda bir kelebek iğne takın ve önlemek için nazik bir aspirasyon ile kan toplamayınhemoliz. Kelebek iğnenin iv konumunu özenle sabitlerken dolu kan gazı şırıngasını 20 mL'lik ve 10 mL'lik şırıngayla ardışık olarak değiştirin.
NOT: Seçilen rahim damarının kontralateral tarafında durduğunuzda en iyi verimi sağlamak en iyisidir.
- Uterin damardaki bir kan gazı şırıngasına yaklaşık 30 derecelik bir açıda bir kelebek iğne takın ve önlemek için nazik bir aspirasyon ile kan toplamayınhemoliz. Kelebek iğnenin iv konumunu özenle sabitlerken dolu kan gazı şırıngasını 20 mL'lik ve 10 mL'lik şırıngayla ardışık olarak değiştirin.
- Radial arter için, intra-arteriyel hattan aspire edin. İlk 5 mL'yi atın ve daha sonra kan gazı analizleri için heparin enjektöründe 3 mL aspirat ve bunu takiben iki şırınga (20 + 10 mL) içinde 3 mL aspire edin.
- Antekübital ven için, intravenöz kateterden hafifçe aspire edin. İlk 5 mL'yi atın ve üç şırıngada (10 mL) 30 mL aspire edin.
- Karnı kapatmaya başlamadan önce uterin ven üzerindeki örnekleme alanının son muayenesini yapın.
- Uterin damar için, karın boşluğunu açtıktan sonra, karın duvarını kaldırmak ve uterusun anterolateral kenarlarındaki uterin venlerin ana dallarını ortaya çıkarmak için bir geri çekici kullanın. Mümkün olduğunca plasenta ile aynı yönde uterin damar dallarından kan alın veya plasenta rahim orta çizgisinde bulunduğu takdirde en belirgin damarı pleksus kullanın.
- Fetal kan örnekleri
- Çocuğunuz doğduğunda, umbilikal kordonu kelepçelemeden veya plasentayı göndermeden umblikal arterden hemen kan alın. Zekayı başlatH kan gazı analizi şırınga ve mümkünse üç 10 ml şırınga ile izleyin.
- Arteryel numuneler güvenceye alındığında, umblikal ven (kan gazı ve 20 + 10 mL şırınga) örneklemeden önce kordonu sıkıştırın ve çocuğu ebeye verin.
NOT: Teslimat saniye içinde ve kendiliğinden müstakil sürece yerinde plasenta ile tüm göbek örnekleri alın. - Geç kordon kelepçesi ile ilgili Norveç önerilerini izleyin. Bozulmuş bir çocuğun olması durumunda, kelepçeyi kelepçeleyin ve kesin derhal ve elini çocuğu ebe ve neonatologla görüşün.
- Kan örneklerinin taşınması
- Geri kalan kan numunelerini hazırlarken kan gaz şırıngalarını buz üzerine koyun ve 5 dakika içinde bir kan gazı analizöründe analiz edin.
- Kan numunelerini derhal vacutainers'a aktarın ve buz üzerine koymadan önce plazma tüplerini 1 - 2 dakika boyunca bir rocker üzerine koyun. Serum tüplerini emek üzerine bırakın.Atory tezgah 30 dakika yerleşmek için.
NOT: Prosedürdeki ekstra dikkat gerektiren kritik bir adımdır, çünkü beş bölgeden alınan numunelerin aynı kalitede olması için aynı anda hazırlanması gerekir. - Plazma örneklerini mümkün olan en kısa sürede santrifüj edin ve 30 dakika içinde, 6 ° C'de, 20 dakika süreyle 2,500 xg santrifüjleyin.
- 30 dakika sonra, serum örneklerini 10 dakika 2.500 x g'de oda sıcaklığında santrifüjleyin.
- Trombosit içermeyen plazma sağlamak için süpernatantları peletin üstünde 0,5 mL bırakarak, 2 mL cryo tüplerine dikkatle ayırın.
- Örnekleri -80 ° C'de saklayın.
5. Plasental Dokunun Toplanması
- Plasenta, buzağı soğutulmuş diseksiyon tepsisine mümkün olduğunca kısa sürede düz bir şekilde koyun. En uzun çapı ve çapı 90 derece fotoğraflayın ve ölçün.
- Plasentayı tartın.
- Ağırlığı, iki çapını, herhangi bir gRoss patolojisi, kordtaki damar sayısı ve doğumdan plasenta buza yerleştirilme zaman aralığı.
NOT: Plasenta, klinik olarak belirtilmişse, patolojik muayene için gönderilir. - Plasenta, maternal yüzeyi yukarı bakacak şekilde yerleştirin ve açık pozitif patolojilerin bulunduğu bölgeden kaçınarak, plasentanın her bir çeyreğinde tesadüfen bulunan 4-5 örnekleme bölgesini belirleyin. Anne yüzeyinden 3-5 mm kesmek için desiduyu makas kullanarak çıkartın. Her bir alandan 1 - 2 cm'lik 3 adet villous doku toplayın.
- Toplanan dokuyu yavaşça 50 mL soğuk 1M PBS içerisinde yıkayın. Her numune alanından birkaç parça halinde bölün.
Not: Plasenta parçalarının boyutu, planlanan analizlere bağlı olacaktır. - 5 kriyo boruları 0,5 cm3 doku örnekleri ve sıvı azot içinde dondurulması ek - 0.1 alikotları ekleyin.
- RNA, sabitleme çözeltisi 25 mL tüpe 0.2 cm 3-0,1 küçük parçalar ekleyin. 4'te saklama6 ° C'de 24 saat bekletin, RNA stabilizasyon solüsyonunu atın ve değiştirin. Donmak.
- Karıştırmak ve dondurularak, OKT ile OCT, yukarı 0.5 mL, 5 kriyo boruları 0,5 cm3 parçaları ekleyin.
- Analiz edilene kadar numuneleri -80 ° C'de saklayın.
NOT: Burton ve ark. Planlanan analizlere bağlı olarak plasental numunenin pratik yönlerine mükemmel bir genel bakış sağlar. 20 Kalan dokuyu, mikrovillus ve bazal zarları izole etmek için hazırlamayı ve vakum emme tekniği ile desidual dokuyu toplamayı düşünün. 21 , 22
6. Yenidoğan Özellikleri
- Apgar skoru (1, 5 ve 10 dakika), cinsiyet, kilo, uzunluk, gebelik haftası ve Yenidoğan Yoğun Bakım Ünitesine kabulün (kalışın uzunluğu ve sonucuna) dahil yenidoğanın özelliklerini kaydedin.
- Yenidoğan vücut kompozisyonunu antropometrik ölçümlerle, havayı yerinden değiştirerek ölçmeyi düşünün.Ment pletismograf veya çift X-ışını absorptiometrisi. 23 , 24
7. Hesaplamalar
- Radial ve uterin arterde benzer kan kompozisyonu varsayın ve uteroplasental arteriovenöz konsantrasyon farkını hesaplayın.
Uteroplasental arteriovenöz konsantrasyon farkı = C A - C V
Umbilikal venöz arteriyel konsantrasyon farkı = C v - C a
C, alt simgelerle konsantrasyon: A, radyal arter; V, rahim damarı; V göbek bağı ve a, göbek bağı. - Hacimdeki kan akışını, mL / dak (Q) hesaplayın:
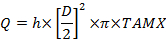
D, damar çapı (cm) olduğunda, TAMX, zaman ortalamalı maksimum hız ve h, uzaysal kan hızı profili için katsayıdır. Umblikal ven katsayısı olarak 0.5 kullanın veUterin arter 25, 26 için 0.6. - Plasental alımını hesaplayın ve Fick'in prensibine göre serbest bırakın:
Uteroplasental alım = ( C A - C V ) x Qm
Fetal alımı = (Cı-V - C) X Q f
Alt simgeler: m, maternal ve f, fetus.
Sonuçlar
4 damarlı örnekleme yöntemi klinik uygulamada uygulanabilir ve 209 ana / bebek çifti kan numunesini başarıyla elde ettik. Bunların 128'inde hacimsel kan akışını ölçmekteyiz. Hem ana hem de fetal damarların tam 4 damar örneklemesi ve kaliteli akış ölçümleri, 70 ana-fetus çiftinde elde edildi ( Şekil 3 ). Buna ek olarak, şimdiye kadar 30 preeklamptik hastadan alınan kan ve plasenta örneklerini aldık. Yöntemin 14...
Tartışmalar
Plasenta 4-gemi örnekleme yöntemi, üç ana amaç için uygundur. İlk olarak, spesifik maddelerin maternal tarafta plasenta tarafından nasıl alındığını ve glikoz ve amino asit çalışmalarımızla gösterildiği gibi muhtemelen umblikal dolaşıma ve fetusa transfer edildiğini incelemek için kullanılabilir. İkincisi, yöntem progesteron sonuçlarına göre plasenta tarafından üretilen ve maternal veya fetal dolaşıma bırakılan maddelerin incelenmesi ile oldukça yakından ilgilidir. Üçüncü ...
Açıklamalar
Yazarların açıklayacak bir şeyi yok.
Teşekkürler
Her şeyden önce, bu projeye katılan annelere içtenlikle teşekkür ederiz. Sonra, örnekleme prosedürüne yardımcı olan ve kolaylaştıran tüm personeli, Anestezi uzmanı, hemşire anestezisti ve cerrahi hemşirelerini kabul ediyoruz. Proje, Güneydoğu Norveç Bölgesel Sağlık Otoritesi ve Norveç Kadın Sağlığı Danışma Birimi, Oslo Üniversitesi ve Oslo Üniversitesi Hastanesi tarafından sağlanan yerel fonlardan sağlanan finansman olmaksızın mümkün olmazdı.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Maternal body composition | |||
| Impedance scale | Tanita | or similar | |
| Ultrasound measurements | |||
| Sequoia 512 ultrasound machine | Acuson | equipped with a curved transducer with colour and pulsewave Doppler (frequency bandwidth 2-6 MHz) | |
| Blood samples | |||
| Arerial cannula | BD Medical | 682245 | or similar |
| 20cc Eccentric Luer Tip Syringe without Needle | Termo | SS-20ES | or similar. 3 needed. |
| 10cc Eccentric Luer Tip Syringe without Needle | Termo | SS-10ES | or similar. 9 needed. |
| 5cc 6% Luer Syringe without Needle | Termo | SS-05S1 | or similar. 2 needed. |
| Arterial blood gas syringe | Radiometer Medical | or similar. 4 needed. | |
| Sterile winged needle connected to flexible tubing, 21 gauge | Greiner Bio-One | 450081 | (intended for single use).3 needed. |
| Vacutainer tube 6 mL EDTA | Greiner Bio-One | 456043 | or similar. Label with sample site. 10 needed. |
| Vacutainer tube 5 ml LH Lithium Heparin Separator | Greiner Bio-One | 456305 | or similar. Label with sample site. 5 needed. |
| Vacutainer tube 6 mL Serum Clot Activator | Greiner Bio-One | 456089 | or similar. Label with sample site. 5 needed. |
| Vacutainer tube 3 ml 9NC Coagulation sodium citrate 3,2% | Greiner Bio-One | 454334 | or similar. Label with sample site. 5 needed. |
| Cryogenic vials, 2.0 mL | Corning | 430488 | or similar. Label with sample site, serum/type of plasma and ID. 90 needed. |
| Marked trays to transport the syringes | to transport the blood samples in the operation theatre | ||
| Rocker | for gentle mixing of the samples | ||
| Ice | in styrofoam box | ||
| Liquid nitrogen | in appropriate container | ||
| Placenta samples | |||
| Metal tray | |||
| Ice | in styrofoam box | ||
| Calibrated scale | |||
| Metal ruler | |||
| 1 M Phosphate buffered saline | Sigma | D1408 | or similar. Dilute 10 M to 1M before use |
| RNA stabilization solution | Sigma | R0901-500ML | or similar |
| Optimal Cutting Temperature (O.C.T.) compound | vwr | 361603E | or similar |
| Cryogenic vials, 2.0 mL | Corning | 430488 | or similar. Label with sample site. content and ID. 10 needed. |
| Centrifuge tubes, conical bottom 50 mL | Greiner Bio-One | 227,285 | or similar. Label with "RNA later", sample site and ID. 2 needed. |
| Liquid nitrogen | in appropriate container | ||
| Fetal body composition | |||
| Calibrated scale | |||
| Measuring tape |
Referanslar
- Jansson, T., Powell, T. L. Role of the placenta in fetal programming: underlying mechanisms and potential interventional approaches. Clin Sci (Lond). 113 (1), 1-13 (2007).
- Hanson, M. A., Gluckman, P. D. Early developmental conditioning of later health and disease: physiology or pathophysiology. Physiol Rev. 94 (4), 1027-1076 (2014).
- Guttmacher, A. E., Spong, C. Y. The human placenta project: it's time for real time. Am J Obstet Gynecol. 213, 3-5 (2015).
- Battaglia, F. C., Regnault, T. R. Placental transport and metabolism of amino acids. Placenta. 22 (2-3), 145-161 (2001).
- Hay, W. W. Placental-fetal glucose exchange and fetal glucose metabolism. Trans Am Clin Climatol Assoc. 117, 321-339 (2006).
- Woollett, L. A. Review: Transport of maternal cholesterol to the fetal circulation. Placenta. 32, 218-221 (2011).
- Prenton, M. A., Young, M. Umbilical vein-artery and uterine arterio-venous plasma amino acid differences (in the human subject). J Obstet Gynaecol Br Commonw. 76 (5), 404-411 (1969).
- Cetin, I., et al. Plasma and erythrocyte amino acids in mother and fetus. Biol Neonate. 60 (2), 83-91 (1991).
- Filshie, G. M., Anstey, M. D. The distribution of arachidonic acid in plasma and tissues of patients near term undergoing elective or emergency Caesarean section. Br J Obstet Gynaecol. 85 (2), 119-123 (1978).
- Haberey, P. P., Schaefer, A., Nisand, I., Dellenbach, P. The fate and importance of fetal lactate in the human placenta -a new hypothesis. J Perinat Med. 10 (2), 127-129 (1982).
- Prendergast, C. H., et al. Glucose production by the human placenta in vivo. Placenta. 20 (7), 591-598 (1999).
- Metzger, B. E., Rodeck, C., Freinkel, N., Price, J., Young, M. Transplacental arteriovenous gradients for glucose, insulin, glucagon and placental lactogen during normoglycaemia in human pregnancy at term. Placenta. 6 (4), 347-354 (1985).
- Zamudio, S., et al. Hypoglycemia and the origin of hypoxia-induced reduction in human fetal growth. PLoS One. 5 (1), 8551 (2010).
- Holme, A. M., Roland, M. C., Lorentzen, B., Michelsen, T. M., Henriksen, T. Placental glucose transfer: a human in vivo study. PLoS One. 10 (2), 0117084 (2015).
- Holme, A. M., Roland, M. C., Henriksen, T., Michelsen, T. M. In vivo uteroplacental release of placental growth factor and soluble Fms-like tyrosine kinase-1 in normal and preeclamptic pregnancies. Am J Obstet Gynecol. 215 (6), 781-782 (2016).
- Paasche Roland, M. C., Lorentzen, B., Godang, K., Henriksen, T. Uteroplacental arterio-venous difference in soluble VEGFR-1 (sFlt-1), but not in soluble endoglin concentrations in preeclampsia. Placenta. 33 (3), 224-226 (2012).
- Brar, H. S., et al. Uteroplacental unit as a source of elevated circulating prorenin levels in normal pregnancy. Am J Obstet Gynecol. 155 (6), 1223-1226 (1986).
- Myatt, L., et al. Strategy for standardization of preeclampsia research study design. Hypertension. 63 (6), 1293-1301 (2014).
- Kiserud, T., Rasmussen, S. How repeat measurements affect the mean diameter of the umbilical vein and the ductus venosus. Ultrasound Obstet Gynecol. 11 (6), 419-425 (1998).
- Burton, G. J., et al. Optimising sample collection for placental research. Placenta. 35 (1), 9-22 (2014).
- Illsley, N. P., Wang, Z. Q., Gray, A., Sellers, M. C., Jacobs, M. M. Simultaneous preparation of paired, syncytial, microvillous and basal membranes from human placenta. Biochim Biophys Acta. 1029 (2), 218-226 (1990).
- Staff, A. C., Ranheim, T., Khoury, J., Henriksen, T. Increased contents of phospholipids, cholesterol, and lipid peroxides in decidua basalis in women with preeclampsia. Am J Obstet Gynecol. 180 (3), 587-592 (1999).
- Catalano, P. M., Thomas, A. J., Avallone, D. A., Amini, S. B. Anthropometric estimation of neonatal body composition. Am J Obstet Gynecol. 173 (4), 1176-1181 (1995).
- Ellis, K. J., et al. Body-composition assessment in infancy: air-displacement plethysmography compared with a reference 4-compartment model. Am J Clin Nutr. 85 (1), 90-95 (2007).
- Haugen, G., Kiserud, T., Godfrey, K., Crozier, S., Hanson, M. Portal and umbilical venous blood supply to the liver in the human fetus near term. Ultrasound Obstet Gynecol. 24 (6), 599-605 (2004).
- Acharya, G., et al. Experimental validation of uterine artery volume blood flow measurement by Doppler ultrasonography in pregnant sheep. Ultrasound Obstet Gynecol. 29 (4), 401-406 (2007).
- Wu, X., et al. Glutamate-glutamine cycle and exchange in the placenta-fetus unit during late pregnancy. Amino Acids. 47 (1), 45-53 (2015).
- Tuckey, R. C. Progesterone synthesis by the human placenta. Placenta. 26 (4), 273-281 (2005).
- Simmons, M. A., Meschia, G., Makowski, E. L., Battaglia, F. C. Fetal metabolic response to maternal starvation. Pediatr Res. 8 (10), 830-836 (1974).
- Simmons, M. A., Jones, M. D., Battaglia, F. C., Meschia, G. Insulin effect on fetal glucose utilization. Pediatr Res. 12 (2), 90-92 (1978).
- Bujold, E., et al. Evidence supporting that the excess of the sVEGFR-1 concentration in maternal plasma in preeclampsia has a uterine origin. J Matern Fetal Neonatal Med. 18 (1), 9-16 (2005).
- Jansson, T., Aye, I. L., Goberdhan, D. C. The emerging role of mTORC1 signaling in placental nutrient-sensing. Placenta. 33, 23-29 (2012).
- Cetin, I. Placental transport of amino acids in normal and growth-restricted pregnancies. Eur J Obstet Gynecol Reprod Biol. 110, 50-54 (2003).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır