È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Un β-glucuronidasi (GUS) Sulla base di analisi morte cellulare
In questo articolo
Riepilogo
Morte cellulare programmata test comunemente usati nei sistemi di mammiferi, come laddering DNA o saggi TUNEL, sono spesso difficili da riprodurre nelle piante. In combinazione con un sistema di giornalista GUS, proponiamo un rapido test basato impianti transitori per analizzare le proprietà morte potenziale di specifici geni.
Abstract
Abbiamo sviluppato un nuovo sistema di espressione transiente pianta che esprime allo stesso tempo il gene reporter β-glucuronidasi (GUS), con putativi regolatori positivi o negativi di morte cellulare. In questo sistema, N. lascia benthamiana sono co-infiltrati con una cassetta 35S espressione guidato contenente il gene da analizzare, e il GUS vettore pCAMBIA 2301 utilizzando LBA4404 ceppo Agrobacterium come veicolo. Poiché le cellule vive sono necessari per l'espressione GUS a verificarsi, perdita di attività GUS è previsto quando questo gene marcatore è co-espresso con regolatori positivi di morte cellulare. Allo stesso modo, un aumento dell'attività GUS si osserva quando i geni anti-apoptotici vengono utilizzati rispetto al controllo vettoriale. Come mostrato di seguito, abbiamo utilizzato con successo questo sistema nel nostro laboratorio per analizzare entrambi i giocatori pro-e anti-morte. Questi includono l'impianto anti-apoptotica Bcl-2 associati athanoGene (UFSP), la famiglia, così come, gli induttori conosciuti mammiferi di morte cellulare, come BAX. Inoltre, abbiamo utilizzato questo sistema per analizzare la funzione morte di troncamenti specifiche all'interno di proteine, che potrebbe fornire indizi sulla possibile modificazione post-traduzionale / attivazione di queste proteine. Qui, vi presentiamo un metodo rapido e sensibile impianto base, come un primo passo nello studio delle funzioni morte di specifici geni.
Protocollo
Nicotiana benthamiana piante sono coltivate in una temperatura controllata camera di crescita a 25 ° C. Completamente ampliato foglie sane di 3-6 piante settimana di vita sono utilizzati.
Suggerimento: I risultati migliori si ottengono utilizzando le foglie emergenti
1. Agrobacterium protocollo di infiltrazione transitoria:
Giorno 1
- LB Streak / rifampicina (25 mg / ml) / kanamicina (100 mg / ml) piastre di agar con gli stock di glicerolo di Agrobacterium tumefaciens (ceppo LBA4404) contenente i vettori appropriato con il gene (s) per essere analizzati per la morte cellulare e il vettore contenente la cassetta GUS sotto un promotore costitutivo. Sempre includere un controllo vettoriale vuoto come controllo negativo.
- Incubare a 28 ° C per 2 giorni.
3 ° giorno
- Inoculare 2 ml di LB contenente rifampicina (25 mg / ml) e kanamicina (100 mg / ml) con una singola colonia di ogni LB / Rifampicina / kanamicina piastra precedentemente striato.
- Incubare ogni cultura agitando a 28 ° C per 24 ore a 200 rpm fino a quando la densità massima crescita è stata raggiunta.
Suggerimento: Agglomerante a volte osservato, in cui le culture caso devono essere accuratamente risospesa (cioè pipettando su e giù) prima di procedere.
4 ° giorno
- Dopo l'incubazione, aumentare il volume totale di 10 ml di LB fresca (contenente gli antibiotici del caso) e acetosyringone (concentrazione finale 25 mM).
- Incubare ogni cultura agitando a 28 ° C per altre 16 ore.
5 ° giorno
- Il giorno seguente lavare ogni cultura due volte con l'aggiunta di 10 ml (non aggiungere acetosyringone) medio infiltrazione (10 mM MgSO 4 0,7 H 2 O, 9 mM MES, pH 5.6) e centrifugare a 4000 xg per 10 minuti a temperatura ambiente.
- Dopo la fase di centrifugazione finale, risospendere ogni cultura in 5 ml di mezzo di infiltrazione contenente acetosyringone (100 mM).
- Misurare il diametro esterno 600 nm, misura tra 0,1 e 0,9 sono accettabili.
Suggerimento: OD 600nm di fino a 0,1 sono stati utilizzati senza un problema, tuttavia, più elevati OD può produrre risultati più consistenti. - Incubare le culture per ulteriori 3 ore per preparare le culture Agrobacterium di infezione.
- Culture miscela contenente il gene (s) da analizzare e il controllo negativo (Agrobacterium contenente il vettore vuoto) in un rapporto 1:1 con la cultura che contiene la cassetta GUS.
- Infiltrarsi nel abaxial (sotto) lato di nuova lascia emergere con un 1 ml ago-meno siringa (Fig. 1).
Suggerimento: Infiltrati sia la miscela di controllo negativo (vuoto vettore + cassetta GUS) e la miscela contenente il gene da testare (gene x + cassetta GUS) su foglie opposte della stessa pianta. Utilizzare impianti triplice copia per ogni trattamento. - 3 giorni dopo l'infiltrazione delle accise infiltrato foglie e analisi per l'espressione delle proteine GUS.
2. Istochimiche GUS test
8 ° giorno
- Vuoto infiltrarsi nella X-Gluc medio substrato nelle foglie escisse.
- Incubare al buio a temperatura ambiente per una notte o fino distinte macchie blu.
Giorno 9
- Risciacquare con acqua distillata.
- Incubare in etanolo al 70% fino a clorofilla viene rimosso, poi il trasferimento di acqua distillata di nuovo. Visivamente valutare i livelli di espressione di GUS.
3. MUG saggio fluorimetrico:
8 ° giorno
- Isolare proteine totali dalla macinazione di dischi foglia infiltrato in un mortaio con azoto liquido. Aggiungere 100 uL di tampone GUS estrazione (50 mM Napi pH 7,0, 10 mM EDTA, 0.1% Triton X-100, 0,1% N-lauroylsarcosine sale di sodio, β-mercaptoetanolo (0,7 microlitri / ml) mantenendo il campione in ghiaccio.
- Centrifugare la sospensione a 14.000 g per 5 minuti a 4 ° C e prendere surnatante come totale delle proteine solubili.
- Misurare la concentrazione utilizzando un NanoDrop secondo le istruzioni del produttore.
- Regolare la concentrazione di proteine a 100 mg di proteina solubile totale per ogni campione mediante tampone di estrazione GUS.
- Aggiungere substrato MUG (4-metilumbelliferil-β-D-glucuronide triidrato), preparato in tampone di estrazione GUS ad una concentrazione finale di 2 mm. Un volume totale di 100 l per ogni campione (proteine + substrato MUG) dovrebbe essere sufficiente.
- Incubare le reazioni per 1 ora a 37 ° C.
- Fermare le reazioni con l'aggiunta di 800 ml di GUS fermare tampone (0,2 M Na 2 CO 3).
- Misurare la fluorescenza utilizzando un lettore di piastre a una lunghezza d'onda di eccitazione di 365 nm e lunghezza d'onda di emissione di 455 nm e confrontare i valori di una curva MU standard. Livelli di relazione sulle attività GUS come MU nmol / mg proteina solubile / min.
4. Azioni e soluzioni:
- Acetosyringone (1 M) stock (FW = 196,2 g) - 0,981 g in 5 ml di DMSO
- Kanamicina (100 mg / ml) magazzino - preparare nel dH 2 0 - Filtro sterilizzare
- Rifampicina (25 mg / ml) magazzino - la preparazione in DMSO
- Luria-Bertani (LB) liquido terreni di coltura: (1L)
1% (w / v) bacto-triptone, 10 g
0,5% (w / v) bacto-estratto di lievito, 5 g
170 mM di cloruro di sodio 10 g
pH - 7 - Acetosyringone (25 mM) = 25 ml di uno stock 1 M in un volume finale di 1 ml
- Infiltrazione Medio: (1L)
10 mM MgSO 4 0,7 dH 2 0 (FW = 246,48 g), 2,4648 g
9 mm MES (FW = 213,25 g), 1,91925 g
pH - 5.6 - Acetosyringone (100 mM) = 100 ml di uno stock 1M in un volume finale di 1 ml
- GUS Tampone di estrazione
Napi 50 mM pH 7,0, 10 mM EDTA, 0.1% Triton X-100, 0,1% N-lauroylsarcosine sale di sodio, β-mercaptoetanolo (0,7 microlitri / ml) - 2x Tampone fosfato
0,2 M NaH 2 PO 4 e 0,2 M Na 2 HPO 4 pH 7 - X-Gluc substrato
Sciogliere 1 mg di 5-bromo-4-cloro-3-indolil BD-glucuronide (X-Gluc) in 0,1 ml di metanolo. Aggiungere 1 ml di tampone fosfato 2x, 20 microlitri 0,1 M ferricianuro di potassio, 10μl Triton X-100 10% e 850 ml di acqua distillata.
5. Rappresentante dei risultati:
A seguito di questo protocollo, la perdita di espressione GUS è previsto quando si verifica la morte delle cellule. Abbiamo contemporaneamente espresso il gene reporter, β-glucuronidasi (GUS) con un membro del cito-protettiva Arabidopsis Bcl-2 associati athanoGene (UFSP) di famiglia. Siamo co-infiltrato N. benthamiana lascia con una cassetta 35S guidato espressione BORSA e il GUS vettore pCAMBIA 2301 utilizzando LBA4404 ceppo tumefaciens. Come mostrato nella figura 2, un aumento visibile nella colorazione GUS è stata osservata dopo questa infiltrazione. Al contrario, quando il noto pro-apoptotici membro della famiglia Bcl-2 BAX è stato utilizzato, una marcata riduzione della colorazione GUS è stata osservata (Fig. 2). In entrambi i casi, espressione di GUS era visibilmente diverso rispetto al controllo. Tuttavia, quando la differenza di espressione è meno evidente, saggi MUG fluorimetrico possono essere eseguite per quanitate espressione GUS.

Figura 1. Esempio di infiltrazione miscela Agrobacterium del lato abaxial di N. benthamiana lascia con un 1 ml ago-meno siringa.
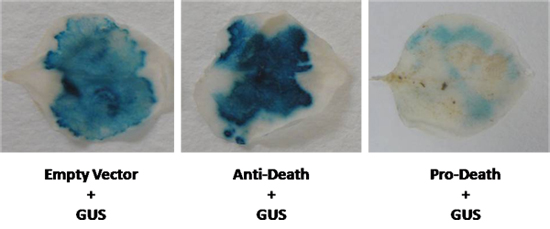
Figura 2. Un vettore GUS è stato co-espresso in N. benthamiana lascia con la morte anti-gene, e un noto induttore di morte cellulare. Livelli GUS sono stati confrontati con un controllo vettore vuoto (GUS controllo).
Discussione
E 'spesso difficile da usare tecniche di individuazione delle cellule morte in impianti che sono comuni nei sistemi di mammiferi. In combinazione con un sistema di giornalista GUS, presentiamo una base vegetale, metodo sensibile per la rilevazione e l'analisi di giocatori di morte cellulare. Questo metodo sfrutta il semplice fatto che le cellule vive sono necessari per l'espressione GUS a verificarsi. Per garantire risultati significativi e la ripetibilità, è fondamentale che le culture ospitare la cass...
Divulgazioni
Materiali
| Name | Company | Catalog Number | Comments |
| Nome del reagente | Azienda | Numero di catalogo | Commenti (opzionale) |
|---|---|---|---|
| Rifampicina | VWR | IC19549001 | Magazzino 25mg/ml in DMSO |
| 4'-idrossi-3 ', 5'-dimethoxyacetophenone (Acetosyringone) | VWR | TCD2666 | 0,981 g / mL in DMSO (1M stock) |
| 2 - (4-morfolino) etano monoidrato (MES) | VWR | EM-6110 | 1,92 g / L in acqua per fare 1 litro di media infiltrazione |
| Bacto-triptone | Pescatore | BP1421-2 | 10 g / L in acqua per fare 1 l di media LB |
| Bacto-estratto di lievito | VWR | EM1.03753.0500 | 5 g / L in acqua per fare 1 l di media LB |
| Cloruro di sodio | VWR | EM-7710 | 10 g / L in acqua per fare 1 l di media LB |
| Sodio fosfato monobasico monoidrato | VWR | MK-7868-12 | 2.5g / L in acqua per fare 50 mM di tampone Napi |
| Sodio fosfato bibasico eptaidrato | VWR | EMD-SX0715-1 | 5 g / L in acqua per fare 50 mM di tampone Napi |
| Solfato di magnesio eptaidrato | VWR | EM-MX0070-1 | 2,5 g / L in acqua per fare 1 litro di media infiltrazione |
| N-Lauroylsarcosine | VWR | TCL0151-500G | 0,1% v / v in tampone GUS |
| 5-Bromo-4-cloro-3-indossile-beta-D-glucuronide sale cyclohexylammonium (X-Gluc) | Oro Biotecnologie | G1281C | 1mg/100uL in metanolo 100% |
| 4-metilumbelliferil-μ-D-glucuronide idrato (MUG) | Sigma | M5664 | 2 mM in 100 uL di tampone di estrazione GUS |
| Ferrocianuro di potassio triidrato | VWR | EM-PX1460-1 | Magazzino 100mM per X-Gluc soluzione substrato |
| β-Methylumbelliferone (MU) | Sigma-Aldrich | M1381 | Per MU standard di utilizzo del buffer di estrazione curva GUS |
| Carbonato di sodio | VWR | EM-SX0395-11 | 0,2 M in acqua per fare GUS tampone arresto |
Riferimenti
- Jefferson, R. A. GUS fusions: , β-glucuronidase as a sensitive and versatile gene fusion marker in higher plants. EMBO J. 6, 3901-3901 (1987).
- Nishihara, M. Expression of the β-Glucuronidase Gene in Pollen of Lily (Lilium longiflorum), Tobacco (Nicotiana tabacum), Nicotiana rustica, and Peony (Paeonia lactiflora) by Particle Bombardment. Plant Physiol. 102, 357-357 (1993).
- Hodal, L. . Plant Science. 87, 115-115 (1992).
- Kabbage, M. The BAG proteins: a ubiquitous family of chaperone regulators. Cell Mol. Life Sci. . 65, 1390-1390 (2008).
- Kang, C. H. AtBAG6, a novel calmodulin-binding protein, induces programmed cell death in yeast and plants. Cell Death Differ. 13 (1), 84-84 (2006).
- Yan, J. . Plant Science. 165 (1), 1-1 (2006).
- Takayama, S., Reed, J. C. Molecular chaperone targeting and regulation by BAG family proteins. Nat Cell Biol. 3 (10), 237-237 (2001).
- Takayama, S. Cloning and functional analysis of BAG-1: a novel Bcl-2-binding protein with anti-cell death activity. Cell. 80 (2), 279-279 (1995).
- Vitha, S. Quantitative β-glucuronidase assay in transgenic plants. Biol. Plant. 35, 151-151 (1993).
- Otha, S. Construction and Expression in Tobacco of a β-Glucuronidase (GUS) Reporter Gene Containing an Intron Within the Coding Sequence. Plant Cell Physiol. 31, 805-805 (1990).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon