È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Determinazione del carbonile gruppi funzionali in Bio-oli da potenziometrica Titolazione: Il Metodo Faix
In questo articolo
Riepilogo
Here we present a potentiometric titration technique for accurately quantifying carbonyl compounds in pyrolysis bio-oils.
Abstract
composti carbonilici presenti in bio-oli sono noti per essere responsabile di proprietà cambia bio-olio su stoccaggio e durante l'aggiornamento. In particolare, carbonili provocano un aumento della viscosità (spesso indicato come 'invecchiamento') durante la conservazione di bio-oli. Come tale, il contenuto di carbonile stato precedentemente utilizzato come metodo di monitoraggio invecchiamento bio-olio e reazioni di condensazione con minore variabilità di misure di viscosità. Inoltre, carbonili sono anche responsabili della formazione di coke in processi di upgrading bio-olio. Data l'importanza dei carbonili in bio-oli, metodi analitici precisi per la loro quantificazione sono molto importanti per la comunità bio-olio. metodi di titolazione potenziometrica basati su carbonile oximation sono da tempo utilizzati per la determinazione del contenuto di carbonile a pirolisi bio-oli. Qui, presentiamo una modificazione delle tradizionali procedure carbonile oximation che si traduce in meno tempo di reazione, la dimensione del campione più piccolo, maggiore precisione, e più accdeterminazioni carbonile urato. Mentre i metodi tradizionali oximation carbonilici avvengono a temperatura ambiente, il metodo qui presentato Faix avviene ad una temperatura elevata di 80 ° C.
Introduzione
Mentre pirolisi bio-oli sono costituiti da una grande varietà di composti e gruppi funzionali chimici, quantificazione dei gruppi carbonilici è particolarmente importante. Carbonili sono noti per essere responsabile per l'instabilità del bio-olio durante sia stoccaggio 1 e elaborazione 2. Il metodo di titolazione qui presentata è una tecnica semplice che può misurare in modo affidabile il contenuto totale di carbonile di bio-oli. Solo i gruppi funzionali aldeidi e chetoni vengono quantificati utilizzando questo metodo; gruppi acidi e lattone carbossilici non sono quantificati.
Per l'analisi di bio-oli, la quantificazione dei gruppi carbonilici per titolazione è stata tradizionalmente realizzato con il metodo di Nicolaides 3. Questo metodo è stato comunemente utilizzato in letteratura bio-olio 4, 5, 6, 7. Questo è unprocedura in cui carbonili vengono convertiti al corrispondente ossima semplice (vedere Figura 1). La liberato HCl reagisce con piridina per forzare l'equilibrio al completamento. L'acido coniugato di piridina viene titolato con una quantità nota di NaOH (base titolante). Il numero di equivalenti di NaOH utilizzate è stechiometricamente equivalente alle moli di carbonilico presente nel bio-olio.
Il metodo Nicolaides, tuttavia, ha diversi limiti. Si può richiedere tempi di reazione più di 48 ore per raggiungere il completamento. Questo limita fortemente la produttività del campione. Utilizza piridina, che è tossico. sono necessari pesi campione di 1 a 2 g. peso del campione utilizzato dipende dalla quantità di idrossilammina HCl presente e il contenuto carbonilico del campione. Se le stime iniziali del peso del campione utilizzato non sono corrette, la titolazione deve essere ripetuto.
Faix et al. 8 ha sviluppato un metodo che è stato modificato here per affrontare i problemi del metodo Nicolaides. La reazione viene condotta a 80 ° C per 2 ore, aumentando così la produttività del campione. La piridina è stata sostituita con trietanolammina, che è una sostanza meno tossica. La dimensione del campione può essere ridotto a 100 a 150 mg. La trietanolammina consuma liberata HCl, guidando la reazione al completamento e la trietanolammina non consumato viene titolato direttamente. Una titolazione secondario del idrossilammina è inutile. Il confronto di questi metodi di titolazione ha dimostrato che il metodo Nicolaides sottostima significativamente il contenuto di carbonile di bio-oli 9.
Il metodo qui descritto è stato modificato dal metodo originale 8 essere più applicabile all'analisi di pirolisi bio-oli. Questo metodo è stato sviluppato per l'analisi di greggio pirolisi bio-oli, ma è stata applicata con successo ad altri tipi di oli derivati da biomassa e bioindicatori oli idrotrattati. Addizionale, questo metodo è stato utilizzato per monitorare i cambiamenti nel contenuto di carbonile sia durante l'invecchiamento e l'aggiornamento.
Protocollo
Attenzione: Si prega di rivedere tutte le schede di sicurezza materiale pertinente (MSDS) prima di iniziare. L'etanolo è infiammabile. Tutte le procedure di manipolazione di sostanze chimiche applicabili devono essere seguite, così come tutte le procedure e getta e trattamento dei rifiuti applicabili.
1. Soluzioni reagenti
- Preparare la soluzione di idrossilammina cloridrato (Soluzione A): Aggiungere 7,7 g di cloridrato di idrossilammina e 50 mL di acqua deionizzata in un pallone tarato da 250 mL. Quando tutti i solidi si sono dissolti, portare a segnare con etanolo. Ciò si traduce in una soluzione di cloridrato di idrossilammina 0,55 M a 80% (v / v) etanolo.
- Preparare la soluzione trietanolammina (soluzione B): Aggiungere 17.4 mL di trietanolammina in un pallone tarato da 250 ml. Aggiungere 10 ml di acqua, e poi diluito fino a volume con etanolo. 95% etanolo può essere utilizzato anche se l'aggiunta di acqua viene saltata. Ciò si traduce in una soluzione 0,48 M trietanolammina nel 96% (v / v) etanolo
- Preparare la acido cloridricosoluzione. In entrambi i casi l'acquisto di 0,1 N soluzione o preparare utilizzando 10 mL concentrato HCl e 1 L di acqua.
2. bio-olio di campionamento e trattare
- Assicurarsi che il campione di olio è a temperatura ambiente prima di prelevare un campione. Completamente omogeneizzare (mix agitando energicamente per almeno 1 minuto, e ispezionare visivamente il campione per assicurarsi che sia omogenea. Alcuni bio-oli possono richiedere tempi più lunghi agitando) bio-olio per ottenere un campione rappresentativo.
- Per il campione di bio-olio, utilizzare da 100 a 150 mg di bio-olio.
- Ridurre al minimo l'esposizione all'ossigeno e al calore per prevenire il degrado del campione prima dell'analisi.
3. Procedura analitica
- La standardizzazione della soluzione di base
- Lavaggio Na 2 CO 3 standard primario in stufa a 105 ° C durante la notte per garantire un campione secco. Consentire l'Na 2 CO 3 raffreddare a temperatura ambiente prima della pesatura.
- Pesare 100 a 150 mgdi carbonato di sodio in un recipiente di titolazione, registrare il peso effettivo, aggiungere un ancoretta e aggiungere acqua sufficiente a coprire il bulbo dell'elettrodo pH e di giunzione.
- Trasferire il campione in un recipiente di titolazione, lavando la fiala di reazione più volte separatamente con etanolo e acqua in proporzioni per ottenere una soluzione finale 80% di etanolo / acqua. Titolare con la soluzione acida utilizzando un titolatore automatico al punto finale. Registrare il punto finale. Il punto finale è definito come il punto di flesso della curva di titolazione.
- Ripetere la procedura due volte per ottenere i tre punti.
- Utilizzare il valore medio come la normalità della soluzione acida.
- Preparazione di Blanks titolazione
- Per Un Vuoto: aggiungere 0,5 mL dimetilsolfossido (DMSO) per un ml Fiala 5 con una palette di spin.
- Aggiungere 2 mL di soluzione di cloridrato di idrossilammina (soluzione A).
- Aggiungere 2 soluzione trietanolammina mL (soluzione B).
- Cap ermeticamente, posto a caldo (80 ° C) di caloreblocco ER o bagno di acqua e mescolare per 2 ore.
- Titolare con soluzione di acido utilizzando un titolatore automatico fino al punto finale, e registrare endpoint.
- Per il Bianco B: Se l'acido minerale è sospettato di essere presente nel campione, aggiungere 0,5 ml di DMSO a 5 ml flaconcino con una palette di spin.
- Aggiungere 2 soluzione trietanolammina mL (soluzione B).
- Cap ermeticamente e mescolare a 80 ° C per 2 ore.
- Trasferire il campione in un recipiente di titolazione, lavando la fiala di reazione più volte separatamente con etanolo e acqua in proporzioni per ottenere una soluzione finale 80% di etanolo / acqua. Titolare con la soluzione acida utilizzando un titolatore automatico al punto finale. Registrare il punto finale.
- Ripetere processo tre volte per ottenere i tre punti.
- La convalida del metodo su un carbonile Noto
- Pesare ~ 100 mg di 4- (benzilossi) benzaldeide (4-BBA) per un ml Fiala 5, registrare il peso effettivo, aggiungere una palette di spin.
- Aggiungere 0,5 mL di DMSO.
- Scioglierecampione in 2 mL di soluzione di idrossilammina cloridrato (soluzione A).
- Aggiungere 2 soluzione trietanolammina mL (soluzione B).
- Chiudere il coperchio ermeticamente e agitare a 80 ° C per 2 ore.
- Trasferire il campione in un recipiente di titolazione, lavando la fiala di reazione più volte separatamente con etanolo e acqua in proporzioni per ottenere una soluzione finale 80% di etanolo / acqua. Titolare con la soluzione acida utilizzando un titolatore automatico al punto finale. Registrare il punto finale.
- Ripetere il processo per tre volte, per ottenere tre punti.
- L'analisi di bio-olio con il metodo
- Pesare quasi 100 mg di bio-olio per flaconcino da 5 ml, registrare il peso effettivo e aggiungere una banderuola giro.
- Aggiungere 0,5 mL di DMSO.
- Sciogliere il campione in 2 soluzione idrossilammina cloridrato mL (soluzione A).
- Aggiungere 2 soluzione trietanolammina mL (soluzione B).
- Chiudere il coperchio ermeticamente e agitare a 80 ° C per 2 ore.
- esimo di trasferimentoe campione ad un recipiente di titolazione, lavando la fiala di reazione più volte separatamente con etanolo e acqua in proporzioni per ottenere una soluzione finale 80% di etanolo / acqua. Titolare con la soluzione acida utilizzando un titolatore automatico al punto finale. Registrare il punto finale.
- Ripetere il processo per tre volte, per ottenere tre punti.
- Blank C: Se l'acido minerale è sospettato di essere presente nel campione, pesare vicino a 100 mg di bio-olio in un mL flacone 5, registrare il peso e aggiungere una banderuola giro.
- Aggiungere 0,5 mL di DMSO.
- Aggiungere 2 soluzione trietanolammina mL (soluzione B).
- Cap ermeticamente e mescolare a 80 ° C per 2 ore.
- Trasferire il campione in un recipiente di titolazione, lavando la fiala di reazione più volte separatamente con etanolo e acqua in proporzioni per ottenere una soluzione finale 80% di etanolo / acqua. Titolare con la soluzione acida utilizzando un titolatore automatico al punto finale. Registrare il punto finale.
- Ripetere processo tre volte per ottenere i tre punti.
4. Calcoli
- La standardizzazione della soluzione di base
- Calcolare la concentrazione della soluzione di acido (mol / L) utilizzando la seguente equazione. Il peso del carbonato di sodio secco in grammi è w 1, la purezza è scritto come una frazione (ad esempio, il 99% è 0,99), ed il computer è in mL.
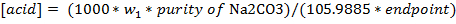
- Calcolare la concentrazione della soluzione di acido (mol / L) utilizzando la seguente equazione. Il peso del carbonato di sodio secco in grammi è w 1, la purezza è scritto come una frazione (ad esempio, il 99% è 0,99), ed il computer è in mL.
- La convalida del metodo su un carbonile Noto
- Calcolare la concentrazione di 4BBA (mol / L) nel campione usando la seguente equazione. Il peso del 4BBA in grammi è w 2, la purezza 4BBA è scritto come una frazione (ad esempio, il 99% è 0,99), la concentrazione della soluzione di acido (mol / L) è [acido], la trietanolammina / idrossilammina • HCl endpoint vuoto è EP BA (il valore medio di tre spazi vuoti, in mL), e il punto finale è EP (in mL).
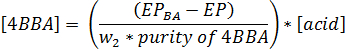
- Calcolare la concentrazione di 4BBA (mol / L) nel campione usando la seguente equazione. Il peso del 4BBA in grammi è w 2, la purezza 4BBA è scritto come una frazione (ad esempio, il 99% è 0,99), la concentrazione della soluzione di acido (mol / L) è [acido], la trietanolammina / idrossilammina • HCl endpoint vuoto è EP BA (il valore medio di tre spazi vuoti, in mL), e il punto finale è EP (in mL).
- Analisi di Bio-oil
- Calcolare la concentrazione di carbonili in bio-oli [CO] (mmol / g-bio olio) utilizzando la seguente equazione. Il peso del bio-olio in grammi è w 3, la concentrazione della soluzione di acido (mol / L) è [acido], la trietanolammina / idrossilammina • HCl endpoint vuoto è EP BA (il valore medio di tre sbozzati in mL) e il punto finale è EP (in mL).

- Calcolare la concentrazione di carbonili in bio-oli [CO] (mmol / g-bio olio) utilizzando la seguente equazione. Il peso del bio-olio in grammi è w 3, la concentrazione della soluzione di acido (mol / L) è [acido], la trietanolammina / idrossilammina • HCl endpoint vuoto è EP BA (il valore medio di tre sbozzati in mL) e il punto finale è EP (in mL).
- correzione acid
NOTA: La presenza di acidi minerali o acidi organici con pKa <2 può causare valori artificialmente bassi carbonilici causa della reazione dell'acido con trietanolammina.- Se questo si sospetta, eseguire gli spazi vuoti descritti nelle sezioni 3.2.6 e 3.4.8. Il peso del bio-olio nel campione in grammi èw 3, EP è il punto finale del campione e PE BA è la trietanolammina / vuoto idrossilammina. EP BB è il punto finale di vuoto B, EP BC è punto finale di vuoto C e il peso (g) di olio usato in bianco C è w BC:
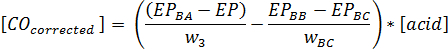
Per i campioni bio-olio che contengono acido acetico lo più, questo è un passo inutile.
- Se questo si sospetta, eseguire gli spazi vuoti descritti nelle sezioni 3.2.6 e 3.4.8. Il peso del bio-olio nel campione in grammi èw 3, EP è il punto finale del campione e PE BA è la trietanolammina / vuoto idrossilammina. EP BB è il punto finale di vuoto B, EP BC è punto finale di vuoto C e il peso (g) di olio usato in bianco C è w BC:
Risultati
Una tipica curva di titolazione è costituito da un singolo endpoint, come mostrato nella Figura 2. titolazioni tipici sia per un campione di bio-olio a crudo e una titolazione in bianco, sono mostrati. Come punto finale si trova nel punto di flesso della curva di titolazione; il punto finale può essere facilmente identificato tracciando la derivata prima della curva di titolazione (mostrata sull'asse destra, DPH / dV, nella Figura 2). Molti s...
Discussione
Curve di titolazione rappresentativi sono mostrati nella Figura 2. Una titolazione, nonché una titolazione di un campione di olio di pirolisi, sono mostrate. Inoltre, la prima derivata della curva di titolazione (DPH / dV) è mostrato, che permette un facile riconoscimento del punto finale della titolazione. La tabella inserto nella figura 2 mostra i dati triplicato per sia olio di pirolisi e titolazioni bianco, con valori medi e deviazioni standard. I valori indicati endpoint (in mL) ...
Divulgazioni
Gli autori non hanno nulla da rivelare.
Riconoscimenti
Questo lavoro è stato sostenuto dal Dipartimento dell'Energia degli Stati Uniti sotto contratto n DE-AC36-08GO28308 con il National Renewable Energy Laboratory. Il finanziamento fornito da US DOE Office of Energy Efficiency e le energie rinnovabili Ufficio Bioenergy Technologies. Il governo degli Stati Uniti mantiene e l'editore, accettando l'articolo per la pubblicazione, riconosce che il governo degli Stati Uniti mantiene il diritto non esclusivo, versato, irrevocabile, licenza mondiale di pubblicare o riprodurre il modulo pubblicato su quest'opera, o permettere ad altri di farlo, a fini di governo degli Stati Uniti.
Materiali
| Name | Company | Catalog Number | Comments |
| Analytical balance | accurate to 0.1 mg | ||
| dry block heater with magnetic stirrer, or hot water bath with magnetic stirrer | |||
| Automatic titrator | We used a Metrohm Titrando 809 automatic titrator, though other equivalent systems are acceptable | ||
| Deionized water | |||
| Ethanol (reagent grade) | CAS # 64-17-5 | ||
| Hydroxylamine hydrochloride | CAS # 5470-11-1 | ||
| Triethanolamine | CAS #102-71-6 | ||
| Hydrochloric acid (37%) | CAS # 7647-01-0 | ||
| Sodium Carbonate (primary standard) | SigmaAldrich | 223484 | |
| 4-(benzyloxy)benzaldehyde | CAS # 4397-53-9 | ||
| Dimethyl sulfoxide | CAS # 67-68-5 | ||
| 5 mL glass Reacti-vials with solid lid and teflon spinvane | Thermoscientific | TS-13223 | |
| 200 mL volumetric flask | |||
| Volumetric or mechanical pipettes |
Riferimenti
- Oasmaa, A., Kuoppala, E., Solantausta, Y. Fast pyrolysis of forestry residue. 2. physicochemical composition of product liquid. Energy Fuels. 17 (2), 433-443 (2003).
- Olarte, M., et al. Stabilization of Softwood-Derived Pyrolysis Oils for Continuous Bio-oil Hydroprocessing. Top. Catal. 59 (1), 55-64 (2016).
- Nicolaides, G. . The chemical characterization of pyrolytic oils. , (1984).
- Oasmaa, A., Korhonen, J., Kuoppala, E. An approach for stability measurement of wood-based fast pyrolysis bio-oils. Energy Fuels. 25 (7), 3307-3313 (2011).
- Chen, C. L., Lin, S. Y., Dence, C. W. . Methods in Lignin Chemistry. , 446-457 (1992).
- Scholze, B., Hanser, C., Meier, D. Characterization of the water-insoluble fraction from fast pyrolysis liquids (pyrolytic lignin) Part II. GPC, carbonyl groups, and 13C-NMR. J. Anal. Appl. Pyrolysis. 58-59, 387-400 (2001).
- Bayerbach, R., Meier, D. Characterization of the water-insoluble fraction from fast pyrolysis liquids (pyrolytic lignin). Part IV: Structure elucidation of oligomeric molecules. J. Anal. Appl. Pyrolysis. 85 (1-2), 98-107 (2009).
- Faix, O., Andersons, B., Zakis, G. Determination of Carbonyl Groups of Six Round Robin Lignins. Holzforschung. 52, 268-272 (1998).
- Black, S., Ferrell, J. Determination of Carbonyl Groups in Pyrolysis Bio-oils Using Potentiometric Titration: Review and Comparison of Methods. Energy Fuels. 30 (2), 1071-1077 (2016).
- Ferrell, J., et al. Standardization of Chemical Analytical Techniques for Pyrolysis Bio-oil: History, Challenges, and Current Status of Methods. Biofuels, Bioprod. Biorefin. 10, 496-507 (2016).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon