Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Определение карбонильных функциональных групп в биомасла потенциометрическим титрованием: The Faix метод
В этой статье
Резюме
Here we present a potentiometric titration technique for accurately quantifying carbonyl compounds in pyrolysis bio-oils.
Аннотация
Карбонильные соединения, присутствующие в биомасла, как известно, отвечает за изменения бионефть собственности при хранении и в процессе модернизации. В частности, карбонильные вызывают увеличение вязкости (часто называемый как "старение") при хранении биомасла. Таким образом, содержание карбонила ранее был использован в качестве метода отслеживания старения бионефть и реакции конденсации с меньшей изменчивостью, чем измерения вязкости. Кроме того, карбонилы также ответственны за формирование кокса в процессах модернизации био-нефти. Учитывая важность карбонилов в биомасла, точные аналитические методы их количественной оценки очень важны для сообщества био-масла. Потенциометрические методы титрования на основе карбонильного оксимирования уже давно используются для определения содержания карбонильной в пиролизных биомасла. Здесь мы представляем модификацию традиционных процедур карбонильного оксимирования, что приводит к уменьшению времени реакции, меньший размер выборки, более высокую точность и больше соглмочекислом определения карбонильных. В то время как методы оксимирования традиционные карбонильные происходить при комнатной температуре, метод Faix, представленные здесь происходит при повышенной температуре 80 ° С.
Введение
В то время как пиролизные биомасла состоят из большого разнообразия соединений и химических функциональных групп, определение количества карбонильных групп является особенно важным. Карбонилы , как известно, отвечают за нестабильность биомасло как во время хранения 1 и 2 обработки. Метод титрования, представленный здесь представляет собой простой метод, который позволяет надежно количественно определить общее содержание карбонильного био-масел. Только альдегидов и кетонов функциональные группы количественно с помощью этого метода; кислота и лактон карбоксильные группы не количественно.
Для анализа биомасла, определение количества карбонильных групп титрованием традиционно осуществляется с использованием метода Николаидес 3. Этот метод обычно используется в бионефть литературе 4, 5, 6, 7. Этопростая процедура , где карбонилов преобразуются в соответствующий оксим (см рисунок 1). Освобожденный HCl реагирует с пиридином, чтобы заставить равновесие к завершению. Конъюгат кислоты пиридина титруют с известным количеством NaOH (основание титранта). Число эквивалентов NaOH, используемых стехиометрически эквивалентно количеству молей карбонильного присутствующего в био-масла.
Метод Nicolaides, тем не менее, имеет несколько ограничений. Это может потребовать времени реакции свыше 48 часов, чтобы достичь завершения. Это серьезно ограничивает пропускную. Он использует пиридин, который является токсичным. Примеры веса от 1 до 2 г требуется. Вес образца используется зависит от количества гидроксиламина HCl настоящего и содержание карбонильного образца. Если первоначальные оценки веса образца, используемого являются неправильными, титрование должен быть повторен.
Faix и др. 8 был разработан метод , который был изменен часпрежде чем решать вопросы метода Nicolaides. Реакцию проводят при температуре 80 ° С в течение 2-х часов, тем самым увеличивая пропускную. Пиридин был заменен триэтаноламин, который является менее токсичных химических веществ. Размер выборки может быть уменьшен до 100 до 150 мг. Триэтаноламин потребляет освобожденную HCl, вождение реакции до завершения, и неизрасходованный триэтаноламин титруют непосредственно. Вторичный титрование гидроксиламина ненужно. Сравнение этих методов титрования показал , что метод Nicolaides значительно занижает содержание карбонила биомасла 9.
Описанный здесь метод был модифицирован с оригинального метода 8 , чтобы быть более применимо к анализу пиролизных биомасла. Этот метод был разработан для анализа сырой пиролизных биомасла, но он был успешно применен к другим типам биологической массы масел, в том числе гидроочищенных биомасла. Аддиционно, этот метод был использован для мониторинга изменений в содержание карбонильного в течение обоих старения и модернизации.
Access restricted. Please log in or start a trial to view this content.
протокол
Внимание: Пожалуйста, рассмотреть все соответствующие паспорта безопасности материала (MSDS) перед началом. Этанол легко воспламеняется. Все процедуры обработки применяются химические следует соблюдать, а также все одноразовые и процедуры обращения с отходами применимы.
1. Реагент Решения
- Готовят раствор гидрохлорида гидроксиламина (раствор А): Добавить 7,7 г гидрохлорида гидроксиламина и 50 мл деионизированной воды в 250-мл мерную колбу. Когда все твердые вещества растворились, разбавить, чтобы отметить с этанолом. Это приводит к тому раствора гидрохлорида 0,55 М гидроксиламина в 80% (об / об) этанола.
- Приготовьте раствор триэтаноламина (раствор В): Добавить 17,4 мл триэтаноламина в 250-мл мерную колбу. Добавляют 10 мл воды, а затем разбавить до метки с этанолом. 95% -ный этанол также может быть использован, если добавление воды пропускается. Это приводит к тому растворе 0,48 М триэтаноламин в 96% (об / об) этанола
- Приготовьте соляной кислотырешение. Либо приобрести 0,1 N раствора или готовят с использованием 10 мл концентрированной HCl и 1 л воды.
2. Био-масло Отбор проб и регулировать
- Убедитесь, что образец масла при комнатной температуре до снятия пробы. Тщательно гомогенизируют (смесь путем встряхивания энергично в течение не менее 1 минуты, и визуально осматривают образец, чтобы убедиться, что он является однородным. Некоторые био-масла может потребоваться более длительное время встряхивания) био-масла, чтобы получить репрезентативную выборку.
- Для образца био-масла, используют от 100 до 150 мг био-масла.
- Сведение к минимуму воздействие кислорода и тепла для предотвращения деградации образца перед анализом.
3. Аналитическая процедура
- Стандартизация базового решения
- Сухие Na 2 CO 3 первичный стандарт в печи при температуре 105 ° С в течение ночи , чтобы обеспечить сухого образца. Дайте Na 2 CO 3 , чтобы охладить до комнатной температуры перед взвешиванием.
- Взвесить 100 до 150 мгкарбоната натрия до сосуд для титрования, записать фактический вес, добавьте мешалку и добавить достаточное количество воды, чтобы покрыть электрод рН луковицу и стык.
- Передача пробы в сосуд для титрования, промывая реакционную колбу несколько раз отдельно с этанолом и водой в пропорции, чтобы сделать окончательный 80% -ного раствора этанола / воды. Титрование с кислотным раствором с использованием автоматического титратора в конечную точку. Запишите конечную точку. Конечная точка определяется как точка перегиба на кривой титрования.
- Повторите процесс дважды, чтобы получить три очка.
- Используйте среднее значение в качестве нормальность раствора кислоты.
- Приготовление титрование заготовок
- Для Blank A: добавить 0,5 мл диметилсульфоксида (ДМСО) в 5 мл флакон с перемещаемой лопастью.
- Добавьте 2 мл раствора гидрохлорида гидроксиламина (раствор А).
- Добавить 2 раствор триэтаноламина мл (раствор Б).
- Колпачок плотно, место в предварительно разогретой (80 ° C) теплаэр блок или водяная баня и перемешивают в течение 2-х часов.
- Титрование раствором кислоты с использованием автоматического титратора к конечной точке, а также записывать конечную точку.
- Для Blank B: Если минеральная кислота предположительно присутствует в образце, добавьте 0,5 мл ДМСО в 5 мл флакон с перемещаемой лопастью.
- Добавить 2 раствор триэтаноламина мл (раствор Б).
- Крышка плотно и перемешивают при 80 ° С в течение 2-х часов.
- Передача пробы в сосуд для титрования, промывая реакционную колбу несколько раз отдельно с этанолом и водой в пропорции, чтобы сделать окончательный 80% -ного раствора этанола / воды. Титрование с кислотным раствором с использованием автоматического титратора в конечную точку. Запишите конечную точку.
- Повторите процесс три раза, чтобы получить три очка.
- Проверка метода с использованием известного карбонильных
- Взвесить ~ 100 мг 4- (бензилокси) бензальдегида (4-BBA) в 5 мл флакон, записать фактический вес, добавить спиновый лопасть.
- Добавить 0,5 мл ДМСО.
- растворятьсяОбразец в 2 мл раствора гидрохлорида гидроксиламина (раствор А).
- Добавить 2 раствор триэтаноламина мл (раствор Б).
- Закрыть крышку плотно и перемешивают при 80 ° С в течение 2-х часов.
- Передача пробы в сосуд для титрования, промывая реакционную колбу несколько раз отдельно с этанолом и водой в пропорции, чтобы сделать окончательный 80% -ного раствора этанола / воды. Титрование с кислотным раствором с использованием автоматического титратора в конечную точку. Запишите конечную точку.
- Повторите этот процесс три раза, чтобы получить три очка.
- Анализ Био-масла Использование метода
- Взвесить близко к 100 мг био-масла в 5 мл флакон, записать фактический вес и добавить спиновую лопасть.
- Добавить 0,5 мл ДМСО.
- Растворение образца в растворе 2 мл гидрохлорида гидроксиламина (раствор А).
- Добавить 2 раствор триэтаноламина мл (раствор Б).
- Закрыть крышку плотно и перемешивают при 80 ° С в течение 2-х часов.
- Передача йе образец в сосуд для титрования, промывая реакционную колбу несколько раз отдельно с этанолом и водой в пропорции, чтобы сделать окончательный 80% -ного раствора этанола / воды. Титрование с кислотным раствором с использованием автоматического титратора в конечную точку. Запишите конечную точку.
- Повторите этот процесс три раза, чтобы получить три очка.
- Бланк C: Если минеральная кислота предположительно присутствует в образце, весят близко к 100 мг био-масла в 5 мл флакон, записать вес и добавить спиновую лопасть.
- Добавить 0,5 мл ДМСО.
- Добавить 2 раствор триэтаноламина мл (раствор Б).
- Крышка плотно и перемешивают при 80 ° С в течение 2-х часов.
- Передача пробы в сосуд для титрования, промывая реакционную колбу несколько раз отдельно с этанолом и водой в пропорции, чтобы сделать окончательный 80% -ного раствора этанола / воды. Титрование с кислотным раствором с использованием автоматического титратора в конечную точку. Запишите конечную точку.
- Повторите процесс три раза, чтобы получить три очка.
4. Расчеты
- Стандартизация базового решения
- Вычислить концентрацию кислотного раствора (моль / л) с помощью следующего уравнения. Масса сухого карбоната натрия в граммах W 1, чистота записывается в виде дроби (то есть, 99% составляет 0,99), а конечная точка находится в мл.
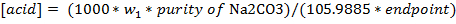
- Вычислить концентрацию кислотного раствора (моль / л) с помощью следующего уравнения. Масса сухого карбоната натрия в граммах W 1, чистота записывается в виде дроби (то есть, 99% составляет 0,99), а конечная точка находится в мл.
- Проверка метода с использованием известного карбонильных
- Вычислить концентрацию 4BBA (моль / л) в образце с использованием следующего уравнения. Вес 4BBA в граммах W 2, чистота 4BBA записывается в виде дроби (то есть, 99% составляет 0,99), концентрация раствора кислоты (моль / л) [кислота], триэтаноламин / гидроксиламин • HCl пустой конечной точкой является ЕР BA (среднее значение из трех заготовок, в мл), а конечная точка находится ЕР (в мл). <бр />
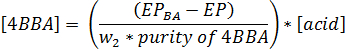
- Вычислить концентрацию 4BBA (моль / л) в образце с использованием следующего уравнения. Вес 4BBA в граммах W 2, чистота 4BBA записывается в виде дроби (то есть, 99% составляет 0,99), концентрация раствора кислоты (моль / л) [кислота], триэтаноламин / гидроксиламин • HCl пустой конечной точкой является ЕР BA (среднее значение из трех заготовок, в мл), а конечная точка находится ЕР (в мл). <бр />
- Анализ био-масла
- Вычислить концентрацию карбонилов в биомасла [СО] (ммоль / г-Биомасло) с использованием следующего уравнения. Вес био-масла в граммах W 3, концентрация раствора кислоты (моль / л) [кислота], триэтаноламин / гидроксиламин • HCl , пустой конечной точкой является ЕР BA (среднее значение из трех заготовок в мл) , а конечная точка находится ЕР (в мл).

- Вычислить концентрацию карбонилов в биомасла [СО] (ммоль / г-Биомасло) с использованием следующего уравнения. Вес био-масла в граммах W 3, концентрация раствора кислоты (моль / л) [кислота], триэтаноламин / гидроксиламин • HCl , пустой конечной точкой является ЕР BA (среднее значение из трех заготовок в мл) , а конечная точка находится ЕР (в мл).
- Кислотные коррекция
Примечание: Присутствие минеральных кислот или органических кислот с рКа <2 может привести к заниженным значения карбонильные вследствие реакции кислоты с триэтаноламина.- Если есть подозрение, выполняют заготовки, подробно описанные в разделах 3.2.6 и 3.4.8. Вес био-масла в образце в граммахW 3, EP является конечной точкой образца и ЕР BA является триэтаноламин / гидроксиламин пустым. EP BB является конечной точкой Blank B, BC EP является конечной точкой Blank C и вес (г) масла , используемого в Blank С, вес BC:
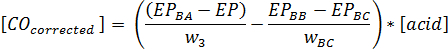
Для получения образцов бионефть, которые содержат в основном уксусную кислоту, это является ненужным шагом.
- Если есть подозрение, выполняют заготовки, подробно описанные в разделах 3.2.6 и 3.4.8. Вес био-масла в образце в граммахW 3, EP является конечной точкой образца и ЕР BA является триэтаноламин / гидроксиламин пустым. EP BB является конечной точкой Blank B, BC EP является конечной точкой Blank C и вес (г) масла , используемого в Blank С, вес BC:
Access restricted. Please log in or start a trial to view this content.
Результаты
Типичная кривая титрования состоит из одной конечной точки, как показано на рисунке 2. Типичные титрование как для исходного образца био-масла и чистого титрования, показаны. По мере того как конечная точка лежит в точке перегиба на кривой титрования; коне?...
Access restricted. Please log in or start a trial to view this content.
Обсуждение
Типичные кривые титрования показаны на рисунке 2. Пустое титрование, а также титрование для образца пиролизного масла, показаны. Кроме того, первая производная кривой титрования (DPH / Dv) показано, что позволяет легко признание титровании конечную точку. В следующей таблице заст?...
Access restricted. Please log in or start a trial to view this content.
Раскрытие информации
Авторы не имеют ничего раскрывать.
Благодарности
Эта работа была поддержана Департаментом энергетики США по контракту № DE-AC36-08GO28308 с Национальной лаборатории возобновляемых источников энергии. Финансирование предусмотрено DOE Управления США по энергоэффективности и возобновляемых источников энергии биоэнергетических технологий Office. Правительство США сохраняет и издатель, приняв статью для публикации, признает, что правительство США сохраняет за собой неисключительное, оплаченный, безотзывное, всемирную лицензию публиковать или воспроизводить опубликованную форму этой работы, или позволить другим делать это, для целей правительства США.
Access restricted. Please log in or start a trial to view this content.
Материалы
| Name | Company | Catalog Number | Comments |
| Analytical balance | accurate to 0.1 mg | ||
| dry block heater with magnetic stirrer, or hot water bath with magnetic stirrer | |||
| Automatic titrator | We used a Metrohm Titrando 809 automatic titrator, though other equivalent systems are acceptable | ||
| Deionized water | |||
| Ethanol (reagent grade) | CAS # 64-17-5 | ||
| Hydroxylamine hydrochloride | CAS # 5470-11-1 | ||
| Triethanolamine | CAS #102-71-6 | ||
| Hydrochloric acid (37%) | CAS # 7647-01-0 | ||
| Sodium Carbonate (primary standard) | SigmaAldrich | 223484 | |
| 4-(benzyloxy)benzaldehyde | CAS # 4397-53-9 | ||
| Dimethyl sulfoxide | CAS # 67-68-5 | ||
| 5 mL glass Reacti-vials with solid lid and teflon spinvane | Thermoscientific | TS-13223 | |
| 200 mL volumetric flask | |||
| Volumetric or mechanical pipettes |
Ссылки
- Oasmaa, A., Kuoppala, E., Solantausta, Y. Fast pyrolysis of forestry residue. 2. physicochemical composition of product liquid. Energy Fuels. 17 (2), 433-443 (2003).
- Olarte, M., et al. Stabilization of Softwood-Derived Pyrolysis Oils for Continuous Bio-oil Hydroprocessing. Top. Catal. 59 (1), 55-64 (2016).
- Nicolaides, G. The chemical characterization of pyrolytic oils. , Dept. of Chemical Engineering., University of Waterloo. Waterloo, Ontario, Canada. MASc Thesis (1984).
- Oasmaa, A., Korhonen, J., Kuoppala, E. An approach for stability measurement of wood-based fast pyrolysis bio-oils. Energy Fuels. 25 (7), 3307-3313 (2011).
- Chen, C. L. Methods in Lignin Chemistry. Lin, S. Y., Dence, C. W. , Springer-Verlag. Berlin, Heidelberg, New York. 446-457 (1992).
- Scholze, B., Hanser, C., Meier, D. Characterization of the water-insoluble fraction from fast pyrolysis liquids (pyrolytic lignin) Part II. GPC, carbonyl groups, and 13C-NMR. J. Anal. Appl. Pyrolysis. 58-59, 387-400 (2001).
- Bayerbach, R., Meier, D. Characterization of the water-insoluble fraction from fast pyrolysis liquids (pyrolytic lignin). Part IV: Structure elucidation of oligomeric molecules. J. Anal. Appl. Pyrolysis. 85 (1-2), 98-107 (2009).
- Faix, O., Andersons, B., Zakis, G. Determination of Carbonyl Groups of Six Round Robin Lignins. Holzforschung. 52, 268-272 (1998).
- Black, S., Ferrell, J. Determination of Carbonyl Groups in Pyrolysis Bio-oils Using Potentiometric Titration: Review and Comparison of Methods. Energy Fuels. 30 (2), 1071-1077 (2016).
- Ferrell, J., et al. Standardization of Chemical Analytical Techniques for Pyrolysis Bio-oil: History, Challenges, and Current Status of Methods. Biofuels, Bioprod. Biorefin. 10, 496-507 (2016).
Access restricted. Please log in or start a trial to view this content.
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены