Method Article
Analisi automatizzata dell'andatura per valutare il recupero funzionale nei roditori con lesione da contusione del nervo periferico o del midollo spinale
In questo articolo
Riepilogo
L'analisi automatizzata dell'andatura è uno strumento fattibile per valutare il recupero funzionale nei modelli di roditori di lesioni nervose periferiche e lesioni da contusione del midollo spinale. Mentre richiede una sola configurazione per valutare la funzione locomotoria in vari modelli sperimentali, è molto importante una meticolosa regolazione e formazione di prodotti duri e morbidi degli animali.
Abstract
Le lesioni nervose periferiche e centrali sono per lo più studiate nei roditori, in particolare nei ratti, dato che questi modelli animali sono sia economici che molti dati comparativi sono stati pubblicati in letteratura. Ciò include una moltitudine di metodi di valutazione per studiare il recupero funzionale dopo la lesione nervosa e la riparazione. Oltre alla valutazione della rigenerazione nervosa mediante istologia, elettrofisiologia e altre tecniche di valutazione in vivo e in vitro, il recupero funzionale è il criterio più importante per determinare il grado di rigenerazione neurale. L'analisi automatizzata dell'andatura consente la registrazione di una grande quantità di parametri correlati all'andatura come Paw Print Area e Paw Swing Speed, nonché misure di coordinazione tra gli arti. Inoltre, il metodo fornisce dati digitali delle zampe dei ratti dopo il danno neuronale e durante la rigenerazione nervosa, aggiungendo alla nostra comprensione di come le lesioni nervose periferiche e centrali influenzano il loro comportamento locomotore. Oltre al modello di lesione nervosa sciatica utilizzato prevalentemente, altri modelli di lesione nervosa periferica come il nervo femorale possono essere studiati con questo metodo. Oltre alle lesioni del sistema nervoso periferico, è possibile valutare le lesioni del sistema nervoso centrale, ad esempio la contusione del midollo spinale. Una valutazione dei dati valida e riproducibile dipende fortemente da una meticolosa regolazione delle impostazioni rigide e software prima dell'acquisizione dei dati. Inoltre, un'adeguata formazione degli animali da esperimento è di importanza cruciale. Questo lavoro ha lo scopo di illustrare l'uso dell'analisi automatizzata computerizzata dell'andatura per valutare il recupero funzionale in diversi modelli animali di lesione nervosa periferica e lesioni da contusione del midollo spinale. Sottolinea anche i limiti del metodo, ad esempio la valutazione della rigenerazione nervosa nei ratti con neurotmesi nervosa sciatica a causa del limitato recupero funzionale. Pertanto, si pensa che questo protocollo aiuti i ricercatori interessati alle lesioni nervose periferiche e centrali a valutare il recupero funzionale nei modelli di roditori.
Introduzione
Le lesioni del sistema nervoso periferico e centrale sono spesso studiate nei roditori, con conseguente grande quantità di dati comparativi riguardanti il decorso della lesione nervosa, della riparazione o della neuroprotezione per contrastare ulteriori lesionisecondarie e rigenerazione 1,2,3. Il risultato delle strategie di trattamento sperimentale nei modelli di roditori può essere valutato da una varietà di tecniche come istologia, immunoistochimica, elettrofisiologia e tecniche di imaging come le scansioni di microtomografia a raggi X (μCT), ma il criterio più importante per determinare il successo di un trattamento è - come nei pazienti umani - il grado di recupero funzionale4,5. I primi studi che studiano le prestazioni locomotorie nei roditori risalgono agli anni'40 6,7,8. Ratti e topi sono stati sottoposti a una grande quantità di studi che hanno studiato il loro comportamento locomotorenei decenni successivi 9,10,11. Al giorno d'oggi esiste una vasta gamma di tecniche di valutazione per modelli di roditori di lesioni nervose periferiche e centrali, che vanno dall'analisi dei percorsi pedonali con inchiostro e carta12,13,14 sulla cinematica della caviglia e dell'andatura15,16,17 ai metodi potenziati di machine learning, che consentono la complessa stima delle traiettorie di andatura, arto earticolazione 18,19.
L'analisi automatizzata computerizzata dell'andatura (AGA) viene utilizzata per valutare la funzione locomotoria a seguito di lesioni nervose periferiche e centrali e potenziale trattamento sperimentale di tali lesioni. Il dispositivo è costituito principalmente da una passerella di vetro e una fonte di luce che illumina le impronte delle zampe del roditore in correlazione con la pressione superata da loro. Questi dati vengono quindi computerizzati per calcolare un'ampia gamma di parametri statici e dinamici. Secondo Deumens, questi parametri possono essere ulteriormente suddivisi nelle categorie di parametri generali, parametri correlati al dolore e parametri correlati alla coordinazione dell'andatura20 (tabella 1). La fattibilità dell'AGA per rilevare cambiamenti nel comportamento dell'andatura è stata dimostrata in vari modelli animali di lesione nervosa periferica (PNI)21, come il nervo sciatico20, nervo femorale22e nervo mediano23,24. Viene anche usato regolarmente per valutare la funzione locomotoria nei ratti con lesioni nervose centrali, ad esempio ictus25 o contusione del midollo spinale26. I progressi del metodo risiedono nella grande quantità di dati comparabili e nella sua possibilità di registrare una pletora di parametri relativi all'andatura27. Questo documento mira a fornire ai ricercatori interessati ai modelli animali di PNI e lesioni del midollo spinale (SCI) una linea guida dettagliata e pratica per valutare la funzione locomotoria in tali modelli.
| Categoria | Parametro | Descrizione | |
| Parametri generali dell'andatura | Area di stampa (unità di distanza) | Area della stampa della zampa | |
| Lunghezza stampa (unità di distanza) | Lunghezza dell'impronta della zampa | ||
| Base di supporto (BoS) (unità di distanza) | Distanza tra le due zampe posteriori o anteriori | ||
| Lunghezza falcata (unità di distanza) | Distanza tra due posizionamenti consecutivi di una zampa | ||
| Parametri correlati al dolore dell'andatura | Tempo di oscillazione (s) | Durata della fase di oscillazione | |
| Tempo di stand (s) | Durata della fase di stance | ||
| Intensità media stampa zampa (unità arbitraria) | Media iIntensità della stampa della zampa durante la fase di posizione | ||
| Parametri relativi al coordinamento dell'andatura | Modelli di sequenza passo normale (NSSP) | Sequenze specifiche di posizionamenti delle zampe durante un ciclo a gradini | |
| Dispersioni di fase (%) | Differenze temporali tra i cicli dei gradini di due zampe specifiche | ||
| Indice di regolarità (RI) (%) | Quantificazione della coordinazione interlimb dividendo la quantità di NSSP impeccabile per 4 per il numero complessivo di posizionamento della zampa durante un ciclo a gradini | ||
Tabella 1: Parametri dell'andatura valutabili con l'analisi automatizzata dell'andatura. Le categorie in cui i parametri sono classificati sono scelte in base a Deumens etal.
Protocollo
Il protocollo sperimentale per tutti gli esperimenti è stato approvato in anticipo dall'Animal Protocol Review Board del governo della città di Vienna. Tutte le procedure sono state eseguite nel pieno rispetto della Dichiarazione di Helsinki sui diritti degli animali e della Guida per la cura e l'uso degli animali da laboratorio degli Istituti nazionali di sanità.
1. Alloggiamento per animali
- Ratti maschi della casa (Lewis o Sprague Dawley) del peso di 250-300 g sotto un ciclo chiaro/scuro di 12 ore con accesso ad libitum al cibo e all'acqua.
- Controllare sia la temperatura ambiente (mantenuta a 20-22 °C) che l'umidità (45%-65 %) per un adeguato alloggiamento degli animali. Per questo lavoro sono stati usati ratti maschi Lewis (PNI) e Sprague Dawley (SCI).
- Fornire una nuova gabbia pulita due volte a settimana. Ospita ratti in gruppi di due o tre e monitora attentamente il loro comportamento sociale e l'interazione. Lasciare ai ratti un periodo di acclimatazione di almeno 1 settimana prima di qualsiasi procedura chirurgica o test funzionale.
NOTA: I ratti richiedono almeno 5 giorni di allenamento giornaliero sull'apparato di analisi dell'andatura prima dell'intervento chirurgico, quindi calcola almeno 2 settimane tra l'arrivo dei ratti nella struttura e i dati programmati per la chirurgia sperimentale28.
2. Induzione di lesioni nervose
NOTA: Indossare dispositivi di protezione individuale come un abito chirurgico, guanti e una maschera. Nel caso in cui non sia disponibile un abito chirurgico sterile, è sufficiente anche un camice da laboratorio pulito e riciclato. A meno che non venga contaminato, l'abito o il mantello non deve essere cambiato tra gli animali ma tra le sessioni chirurgiche. Si raccomanda l'uso di guanti chirurgici sterili. Nel caso in cui tali guanti non siano disponibili, i guanti d'esame possono anche essere utilizzati ma devono essere lavati prima dell'intervento chirurgico utilizzando disinfettante chirurgico. I guanti dovrebbero essere cambiati tra gli animali.
- Il giorno dell'intervento chirurgico, cerca di ridurre al minimo qualsiasi quantità di stress per gli animali in quanto ciò potrebbe interferire con l'anestesia, ad esempio, gli animali richiederanno dosi più elevate di anestetici.
- Il giorno dell'intervento chirurgico, iniettare 0,05 mg di Buprenorfina/kg di peso corporeo in sospensione con 100-200 μL 0,9% di NaCl sottocutaneamente utilizzando una canula da 25 G 1 h prima dell'intervento chirurgico per fornire analgesia pre- e interoperativa. Se non indicato diversamente, il fianco del topo è il sito preferito per l'iniezione.
- Anestetizzare i ratti posizionandoli in una camera di induzione di anestesia collegata a un vaporizzatore di sevoflurane e un contenitore di gesso attivo per assorbire la CO2. Anestetizza il ratto inondando la scatola di anestesia con una miscela sevoflurane-ossigeno del 4-5% per circa 5 minuti utilizzando un flusso di ossigeno di 1,5 L/min (fase di iniziazione). Collegare una clip di ossimametria a una delle zampe per monitorare la saturazione di ossigeno nel sangue del roditore. Mantenere lo stato di anestesia generale con una miscela sieroflurane-ossigeno del 2,5-4,5%.
NOTA: Per la chirurgia sperimentale, l'anestesia generale è obbligatoria. Confermare l'anestesia generale controllando la mancanza di risposta per pizzicare lo stimolo della coda o delle zampe. - Quando il topo è entrato nell'anestesia generale, radersi il rispettivo areale che verrà utilizzato e disinfettare l'area scorrendola alternatamente con alcol e disinfettante per la pelle. Lo scorrimento finale deve essere eseguito con disinfettante per la pelle.
- Posizionarlo su un riscaldante regolabile nella posizione richiesta (supina per il modello del nervo femorale, incline al modello sciatico e SCI). Inserire una sonda termometrica flessibile nel retto del ratto per monitorare la temperatura dell'animale e mantenerla a circa 37 °C durante l'intervento chirurgico. Durante l'anestesia, proteggere gli occhi del topo dall'essiccazione usando unguento per gli occhi
3. Induzione chirurgica della lesione nervosa
- Quando si eseguono procedure chirurgiche, aderire rigorosamente ai sette principi di Halsted29 come segue:
- Maneggiare sempre delicatamente i tessuti quando si lavora con loro. Evitare di strappare o schiacciare i tessuti.
NOTA: I sistemi diretrattili self-made 30 o disponibili in commercio sono utili per tenere i muscoli e i vasi fuori dal campo operativo. - Mantenere con cura l'emostasi utilizzando un emostato elettrico per cauterizzare vasi o legature per garantire un'attenta emostasi.
- Mantenere sempre l'apporto di sangue ai tessuti sezionandoli con cura e maneggiandoli delicatamente.
- Mantieni un'asepsi rigorosa indossando una maschera, un abito e guanti sterili.
- Evitare la tensione sui tessuti applicando suture che non sono né troppo strette né troppo sciolte.
- Appose meticolosamente i tessuti riunendo i rispettivi bordi senza sovrapposizioni.
NOTA: Questo è particolarmente importante nel caso di neurorrofia epineuriale o perineuriale. Eseguire tutte le procedure microchirurgiche con ingrandimento 6x-16x utilizzando un microscopio operativo. Idealmente, il microscopio fornisce due coppie di oculari per consentire l'osservazione dell'operazione da parte di un assistente. - Evitare la creazione di spazi morti suturando attentamente i diversi strati tissutali.
- Maneggiare sempre delicatamente i tessuti quando si lavora con loro. Evitare di strappare o schiacciare i tessuti.
- Induzione della neurotmesi nervosa sciatica dell'arto posteriore destro
- Esporre il nervo sciatico destro a livello della metà della coscia eseguendo un'incisione lunga 5 cm sul lato dorsale dell'arto posteriore con una lama di bisturi #10 collegata a un manico #3 bisturi e sezionando la muscolatura sovrasquando e il tessuto molle. Posizionare un riavvolgitore all'interno della ferita per tenere la muscolatura sezionata e la pelle fuori dal situs. Esporre delicatamente il nervo rimuovendo il tessuto circostante utilizzando forbici microchirurgiche curve.
- Rimuovere un segmento nervoso lungo 8 mm del nervo sciatico 1-2 mm prossimale alla sua triforcazione con forbici microchirurgiche dritte.
- Ruotare il segmento nervoso di 180°, posizionarlo tra il ceppo prossimale e distale del nervo sciatico trasetto ed eseguire la neurorrofia epineuriale in ogni sito con due suture interrotte 10-0 e un supporto per ago microchirurgico.
- Induzione della neurotmesi nervosa femorale sull'arto posteriore destro
- Eseguire un'incisione longitudinale dell'inguine di 3-4 cm con una lama bisturi #10 collegata a un manico #3 bisturi al fine di esporre il fascio neurovascolare femorale destro. Utilizzare forbici chirurgiche per la dissezione smussata fino a quando non viene esposta la biforcazione del nervo femorale. Posizionare un riavvolgitore all'interno della ferita per tenere la muscolatura sezionata e la pelle fuori dal situs.
- Trascritti il motore esposto e i rami sensoriali distale alla biforcazione e accisa un segmento nervoso lungo 6 mm di ogni ramo, rispettivamente, utilizzando forbici microchirurgiche dritte.
- Ruotare entrambi i segmenti nervosi di 180°, posizionarli tra il ceppo prossimale e distale dei rami nervosi femorali trasgiunti ed eseguire la neurorrofia epineuriale in ogni sito con due suture interrotte 11-0 e un supporto per ago microchirurgico.
NOTA: Eseguire un innesto nervoso autologo omotopico innestando l'innesto motorio nel ramo motore originale e l'innesto sensoriale al ramo sensoriale originale. In alternativa, eseguire un innesto nervoso autologo eterotopico innestando l'innesto motorio nel ramo sensoriale originale e viceversa.
- Induzione della lesione da contusione del midollo spinale toracico
- Eseguire un'incisione cutanea attraverso la colonna vertebrale toracica con una lama bisturi #10 collegata a un manico di bisturi #3 seguito da due incisioni muscolari parallele ai processi spinosi per facilitare la retrazione muscolare. Posizionare un riavvolgitore all'interno della ferita per tenere la muscolatura sezionata e la pelle fuori dal situs.
- Identificare l'11a vertebra toracica (Th) ed esporre la lamina dell'arco vertebrale rimuovendo il tessuto sovrastante e il processo spinoso usando un rongeur.
- Eseguire una laminectomia utilizzando un micro trapano e una bava appropriata per praticare un piccolo foro nella lamina, leggermente più grande della punta del riflettore. Per evitare danni al midollo spinale, assottigliare la lamina solo durante l'apertura e l'allargamento del foro utilizzando un rongeur. Se il periostio è ancora intatto, rimuoverlo con cura utilizzando una sonda appuntita affilata senza danneggiare il dura mater.
- Dopo aver fatto in modo che venga fatto un foro abbastanza grande senza destabilizzare la lamina, tenere la colonna vertebrale dell'animale in posizione bloccandola rostralmente e caudally a Th11 con le pinze stabilizzanti del dispositivo di valutazione. Utilizzando le ruote a mano nella parte anteriore e laterale, posizionare l'asta di acciaio 3-5 mm sopra il foro della laminectomia. Infine, sottosogliere tutti gli animali ad un impatto con una forza definita di 150 kilodinina per indurre un grado da lieve a moderato di lesione da contusione al midollo spinale4.
- Eseguire la chiusura della ferita in strati anatomici utilizzando suture interrotte di poliglactina 4-0 o 5-0 e un portaaghi chirurgici. Pulire accuratamente la ferita pulerla delicatamente con un tampone di garza imbevuto di NaCl sterile allo 0,9%.
- Dopo l'intervento chirurgico, riportare gli animali nella gabbia di casa e ripararli dall'esposizione alla luce e al suono. Monitorare attentamente il comportamento degli animali fino al giorno postoperatorio (DPO) 7 e garantire un'assunzione sufficiente di cibo e acqua. Se necessario, fornire ulteriore fluido mediante iniezioni sottocutanee (ad esempio, 10 ml di NaCl 0,9%).
- Fornire analgesia post-operatoria per un minimo di 2 giorni per mezzo, ad esempio, di oppioidi (0,05 mg/kg di peso corporeo Buprenorfina per via sottocutanea (s.c.)) e/o antipiretici (4 mg/kg di peso corporeo Carprofen s.c.). Se necessario, e nel caso del modello SCI, fornire anche una terapia antibiotica postoperatoria (7,5 mg/kg di peso corporeo Enrofloxacina per os (p.o.)).
- In caso di lesione del midollo spinale, svuotare manualmente la vescica del topo fino a quando non ritorna la minzione spontanea.
4. Recupero dagli interventi chirurgici prima dell'analisi dell'andatura
NOTA: I ratti con lesione nervosa sciatica mostrano la tendenza a rosicchiare le zampe posteriori a causa dell'insorgenza di neuropatia dolorosa a seguito di lesioni nervose. Questa forma di automutilazione può causare l'autoamputazione delle dita dei piedi o di parti della rispettiva zampa posteriore. Preferire i ratti Lewis rispetto ad altri ceppi di ratto nel caso in cui si usi il modello di lesione nervosa sciatica, poiché questo ceppo di ratto mostra una tendenza minore all'autoutilizzazione31. I ratti con lesione nervosa sciatica mostrano anche la tendenza a sviluppare contratture dell'arto operato, che potrebbero comportare la loro esclusione dallo studio a causa di interferenze con l'acquisizione dei dati. Tali eventi avversi si verificano molto meno comuni nei ratti con lesioni femorali.
- Ispezionare gli animali operati quotidianamente dopo l'intervento chirurgico con particolare attenzione allo stato degli arti e delle zampe, rispettivamente.
NOTA: Nei ratti con SCI, all'altezza di Th11, il pene o la prolasse rettale possono verificarsi a causa della compromissione della capacità naturale degli animali di urinare e defecare. Questi eventi sono comunemente definiti come endpoint umani dello studio e implicano l'esclusione immediata dell'animale colpito dallo studio. - Continuare l'analgesia postoperatoria fino a quando i ratti non cessano di mostrare sintomi correlati al dolore.
- In caso di dolore persistente, somministrare gabapentin (30-120 mg/kg di peso corporeo) p.o. per trattare il dolore neuropatico.
5. Preparazione prima di eseguire l'analisi automatizzata dell'andatura
NOTA: La metodologia del sistema di analisi dell'andatura si basa sulla registrazione degli animali dal basso durante l'attraversamento di una lastra di vetro, che è illuminata da una luce LED verde. Quando le zampe degli animali contattano il pavimento, l'area della stampa della zampa viene illuminata e registrata da una videocamera ad alta velocità. Questi dati vengono quindi inviati tramite un cavo Ethernet a un computer che esegue il software di analisi dell'andatura. Mentre le impronte individuali possono essere classificate manualmente dallo sperimentatore, l'ultima versione del software presenta anche la classificazione automatica dell'impronta.
- Eseguire tutte le procedure di test al buio e in assenza di rumori fastidiosi. Poiché i ratti sono in grado di percepire le frequenze supersoniche, verificare anche che nessuna fonte emetta tali suoni.
NOTA: Eseguire analisi dell'andatura settimanalmente o ogni due settimane, ma non testare i ratti troppo frequentemente poiché soprattutto i ratti Lewis tendono a perdere interesse a partecipare alla procedura nel tempo quando sono esposti a un certo esercizio troppo frequentemente. Tuttavia, è necessario addestrare i ratti ogni giorno per 5 giorni prima dell'intervento chirurgico per abituarli all'ambiente di prova e alla procedura. - Durante le sessioni di allenamento e il giorno del test, preparare la sala prove comportamentale spegnendo tutte le sorgenti luminose, che altrimenti potrebbero interferire con la fotocamera del dispositivo di analisi dell'andatura automatizzata. Posizionare lo schermo del computer necessario per l'acquisizione dei dati lontano dalla fotocamera per evitare che la sua luce interferisca con la fotocamera.
- Assicurarsi che il dispositivo sia installato in una posizione stabile e in modo da prevenire qualsiasi forma di vibrazione, in quanto ciò interferirà seriamente con la procedura di acquisizione dei dati.
- Portare i ratti nella sala prove comportamentale e acclimatarli nella propria gabbia di casa per almeno 30 minuti prima del test.
NOTA: Quando si maneggiano gli animali, indossare dispositivi di protezione individuale come un abito chirurgico o un camice da laboratorio, guanti e una maschera.
6. Esecuzione di analisi automatizzate dell'andatura
- Sessioni di allenamento
NOTA: Durante l'allenamento, gli animali subiranno una curva di apprendimento, quindi si consiglia di regolare gradualmente il programma di allenamento. Usa le ricompense alimentari (ad esempio, 1-2 pezzi di cereali per la colazione) per premiare gli animali dopo aver completato con successo ogni sessione di allenamento.- Il primo giorno di allenamento, sollevare delicatamente l'animale tenendolo sotto il tronco e portarlo delicatamente all'ingresso della passerella.
- Posizionare l'animale nell'area di ingresso e lasciarlo esplorare l'apertura del corridoio senza alcuna interferenza da parte della persona che effettua la procedura di prova.
NOTA: Non urlare, fischiare, soffiare o colpire l'animale nel tentativo di motivarlo ad attraversare la passerella. Tutto questo comportamento stresserà gravemente l'animale e complicherà ulteriormente la procedura di acquisizione dei dati. - Aspetta che l'animale attraversi volontariamente la passerella per raggiungere la sua gabbia di casa. A volte, specialmente negli animali non addestrati, questo può richiedere fino a diversi minuti. Il primo giorno di allenamento, l'animale non è né previsto né richiesto per effettuare corse ininterrotte con velocità di camminata uniforme. Dovrebbe invece acclimatarsi all'apparato e alla procedura di prova.
- Il secondo giorno di allenamento, abituare gli animali ad entrare nella passerella senza esitazione e, anche a tornare alla loro gabbia di casa senza esitazione. Alcuni animali probabilmente avranno già imparato ad attraversare la passerella senza interruzioni, ma questo non è ancora necessario alla fine del secondo giorno.
- Il terzo giorno di allenamento, assicurati che gli animali imparino ad attraversare la passerella senza esitazione, annusare o altri movimenti esplorativi. Assicurati che camminino con velocità uniforme.
- Il quarto e il quinto giorno di allenamento, ripetere l'esercizio precedente per consolidare la procedura di prova.
NOTA: Nel caso in cui un animale non acquisisca l'abilità necessaria per attraversare correttamente la passerella entro la fine del periodo di allenamento di 5 giorni, aggiungi altri 2 giorni di allenamento (ad esempio, il fine settimana). Inoltre, prendi in considerazione l'esecuzione di un massimo di 3 sessioni di allenamento al giorno, separate da almeno 2 ore di riposo tra una sessione individuale e l'altra. Nel 95% dei casi, l'animale avrà acquisito l'esperienza di formazione richiesta entro la fine di questo lungo periodo di allenamento. Nel raro caso in cui un animale non abbia ancora acquisito questa abilità dopo 7 giorni di allenamento, si consiglia di posticipare la sessione di chirurgia sperimentale pianificata per almeno 1 settimana e di ripetere il suddetto regime di allenamento.
7. Acquisizione dei dati
NOTA: Il sistema di analisi dell'andatura visualizza ogni impronta della zampa mentre l'animale cammina e analizza automaticamente vari parametri dell'andatura come area di stampa paw, intensità di stampa della zampa, tempo di oscillazione della zampa e velocità di oscillazione della zampa(tabella 1). Poiché il sistema di analisi dell'andatura registra tutti i dati in base all'intensità generata dalle impronte delle zampe degli animali, assicurarsi che le impostazioni della fotocamera siano regolate in base al peso e alle dimensioni dei ratti. Inoltre, assicurarsi che la passerella sia asciutta e pulita prima della registrazione dei dati per evitare qualsiasi influenza sull'acquisizione dei dati.
- Prima di acquisizione di qualsiasi dato, pulire la passerella utilizzando un detergente commerciale per vetri e uno squeegee. Spruzzare la lastra di vetro più volte e quindi pulirla con lo squittio per rimuovere eventuali particelle dalla sua superficie. Inoltre, pulisci il sotto. Assicurarsi di rimuovere qualsiasi fluido dalle estremità della passerella poiché gli animali potrebbero altrimenti salirlo su di esso, il che influenzerebbe i dati registrati.
- Ripetere la procedura di pulizia ogni volta che è necessario, ad esempio la contaminazione della passerella e prima di registrare i dati di un topo da una gabbia diversa. Si pensa che questo impedisca all'animale di essere distratto dal profumo dei loro conspecifici.
- Prima della prima acquisizione dei dati, regolare le impostazioni della fotocamera adattando il peso degli animali. Confermalo mettendo l'animale più leggero e pesante sulla passerella e scegli un'impostazione della fotocamera che consenta una buona qualità dei dati in entrambi i casi. Regola il guadagno della fotocamera, la luce rossa del soffitto, la luce verde della passerella e la soglia di intensità verde (GIT) per garantire un rilevamento ottimale della stampa delle zampe.
NOTA: non modificare le impostazioni scelte dopo l'inizio dell'acquisizione dei dati in quanto ciò ostacolerà la comparabilità dei dati acquisiti. Come eccezione, il GIT può essere modificato durante la classificazione dei dati, ma questo deve essere fatto per tutte le prove in modo uniforme. - Definire e calibrare la passerella utilizzando la scheda di calibrazione fornita.
- Scegliere una fotocamera registrata elencata nella scheda Configurazione.
- Fare clic sul pulsante Apri acquisizione disponibile nella scheda Acquisisci.
- Scatta un'istantanea della passerella vuota e pulita, che verrà utilizzata come riferimento durante la seguente procedura di acquisizione dei dati.
- Si noti la modifica dello stato da In attesa di snapshot a Pronto per l'acquisizione.
- Fare clic sul pulsante Avvia acquisizione e notare la modifica dello stato da Pronto per l'acquisizione a In attesa di esecuzione per avviare.
- Posizionare un topo sulla passerella e seguire il movimento dell'animale sullo schermo del computer. Si noti la modifica dello stato da In attesa dell'esecuzione all'avvio dell'esecuzione della registrazione.
NOTA: il software classificherà automaticamente le esecuzioni che ritiene conformi in base alle caratteristiche di esecuzione preimpostate con un simbolo verde, mentre le esecuzioni non conformi verranno contrassegnate con un simbolo rosso. Il software interrompe automaticamente l'acquisizione dei dati quando sono state registrate tre esecuzioni conformi, ma l'acquisizione dei dati può essere continuata facendo di nuovo clic sul pulsante Avvia acquisizione.
8. Classificazione dei dati
NOTA: fare riferimento alla tabella 1 per un elenco dei parametri di risultato AGA. Sono necessarie almeno tre corse conformi in cui l'animale deve attraversare costantemente la passerella senza esitazione27. Inoltre, le velocità di corsa devono corrispondere all'interno delle stesse categorie definite nellaletteratura 30.
- Fare clic sul pulsante Classifica nella scheda Esplora sperimentale delle rispettive prove da classificare.
- Riproduci l'esecuzione acquisita con la velocità normale per avere l'impressione che i dati siano conformi ai requisiti elencati in precedenza.
- Nell'angolo sinistro-superiore, fare clic sul pulsante Classifica automaticamente per la classificazione automatica delle impronte dei pedoni da parte del software.
NOTA: Sebbene il software abbia un alto tasso di corretta classificazione delle zampe, a volte non riesce ad assegnare una zampa alle stampe o assegna la zampa sbagliata. Pertanto, ricontrolla sempre le impronte delle zampe classificate automaticamente in seguito. - Per il corretto calcolo dei normali pattern di sequenza di passo (NSP), assicurarsi che l'algoritmo di classificazione non sia confuso da impronte di zampe non visibili, portando a NSSP difettosi (Figura 1A). Pertanto, includere solo le impronte delle zampe rilevabili mentre la zampa contralaterale è visibile anche per i calcoli NSSP, ad esempio la zampa anteriore sinistra (LF) e la zampa posteriore destra (RH) (Figura 1B).

Figura 1: Dati AGA esemplari, che dimostrano la necessità di un doppio controllo manuale della corretta classificazione dei dati. Nel caso in cui un posizionamento rilevato di una zampa anteriore sia riuscito dal posizionamento rilevato di un'altra zampa anteriore (A) il software AGA potrebbe confondere questo con un modello di camminata non coordinato poiché non sono state rilevate zampe posteriori. Pertanto, si consiglia di ricontrollare sempre e selezionare una stampa iniziale della zampa, che viene rilevata quando è visibile anche la zampa contralaterale (B). Clicca qui per visualizzare una versione più grande di questa figura.
9. Calcolo delle statistiche
NOTA: Per regolare i dati di corsa per le modifiche correlate all'aumento di peso nel tempo, si consiglia vivamente di calcolare un rapporto della zampa sperimentale con una zampa non sperimentale (ad esempio, controllo). Inoltre, calcola il rapporto con i valori preoperatori di questo confronto zampa-zampa per considerare le differenze individuali nell'uso della zampa.
- Fare clic sul pulsante Visualizza statistiche di esecuzione per ottenere una panoramica completa sulle statistiche di esecuzione.
- Selezionare File ed esporta per esportare le statistiche di esecuzione o le statistiche di valutazione in un software per fogli di calcolo.
Risultati
12 ratti sono stati sottoposti a chirurgia sperimentale del nervo periferico. La resezione del nervo sciatico (Figura 2A) è stata eseguita in 7 ratti, mentre la neurotmesi nervosa femorale (Figura 2B) è stata indotta in 5 ratti. In tutti gli animali, il difetto nervoso è stato ricostruito per mezzo di un innesto nervoso autologo. La lesione da contusione del midollospinale (figura 2C)al livello Th11 è stata indotta in 6 ratti, per un totale di 18 ratti.
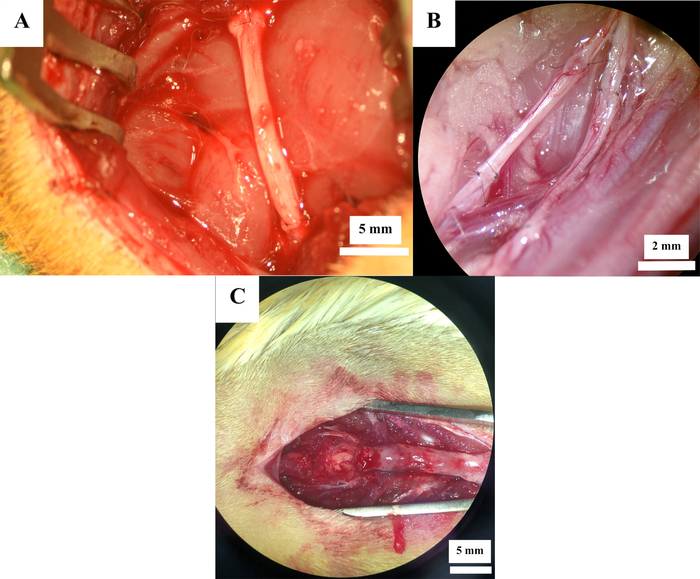
Figura 2: Siti operativi dopo la ricostruzione nervosa. Ricostruzione nervosa con autoinnesti nel nervo sciatico (A) e nervo femorale (B) così come dopo la lesione da contusione del midollo spinale (C). Clicca qui per visualizzare una versione più grande di questa figura.
Tutti gli animali si sono ripresi bene dall'intervento chirurgico e non si sono verificati casi di automutilazione. Un animale del gruppo delle lesioni nervose sciatiche ha sviluppato forti contratture della zampa posteriore destra durante il periodo di osservazione postoperatoria e ha dovuto essere escluso da ulteriori analisi dei dati.
Neurotmesi nervosa sciatica
Poiché il nervo sciatico fornisce innervazione muscolare e sensoriale alla maggior parte dell'arto posteriore, la sua resezione si traduce in una grave compromissione della funzione locomotoria. A seguito di lesioni, i ratti usano il tallone della zampa solo per il supporto delpeso (Figura 3B-E) e l'arto viene spostato in un movimento circonduttivo ampio. Pertanto, i cambiamenti locomotori valutati tramite AGA diventano evidenti attraverso un'area di stampasignificativamente ridotta (figura 4A)e un tempo di oscillazione significativamente aumentato (Figura 4B). Entrambi i parametri sono stati ancora significativamente modificati rispetto alle misurazioni Pre-OP alla fine del periodo di osservazione. Degno di nota, un animale ha sviluppato forti contratture della zampa posteriore destra a partire dalla settimana postoperatoria (WPO) 10. Ciò ha comportato un aumento dell'area di stampa della zampa posteriore destra a oltre il 150% rispetto alla zampa sinistra al WPO12 (Figura 5). Poiché si trattava di un estremo rispetto a tutti gli altri animali valutati in questo studio, abbiamo escluso questo animale dall'analisi dei dati relativi all'area di stampa.

Figura 3: Impronte rappresentative delle zampe prima e dopo la resezione delle dimensioni critiche del nervo sciatico destro e della riparazione dell'autoinnesto. Si noti la forte diminuzione dell'area di stampa a seguito dilesioni nervose( B ) rispetto a preoperatoriamente (A). Nonostante un leggero incremento nell'area di stampa durante il periodo di osservazione(C-E),le impronte delle zampe dell'arto posteriore destro rimasero notevolmente modificate rispetto alle registrazioni di base. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 4: Il corso del recupero funzionale dopo la resezione delle dimensioni critiche e la riparazione dell'autoinnesto del nervo sciatico. Il rapporto area di stampa (A) e lo swing time ratio (B) sono stati statisticamente modificati in modo significativo dai valori Pre-OP immediatamente dopo la resezione del nervo sciatico. Mentre l'area di stampa è rimasta significativamente diminuita rispetto alla linea di base fino a WPO10, Swing Time è stato ancora significativamente aumentato a valori Pre-OP a WPO12. *: p < 0,05 rispetto a Pre-OP, **: p < 0,01 rispetto al Pre-OP. Le barre di errore indicano ± errore standard della media (SEM). Clicca qui per visualizzare una versione più grande di questa figura.

Figura 5: Boxplot del corso dell'area di stampa a seguito di una lesione del nervo sciatico. Si noti l'estremo (ellisse rossa) al WPO12, che è spiegato dal fatto che un animale ha sviluppato forti contratture della zampa posteriore destra a partire da WPO10. L'animale è stato quindi escluso dall'analisi statistica mostrata nella figura 4. Clicca qui per visualizzare una versione più grande di questa figura.
Neurotmesi nervosa femorale
La resezione del nervo femorale provoca la denervazione del muscolo quadricipite della coscia33,34. Di conseguenza, l'estensione del ginocchio è compromessa, con conseguente iperflessione dell'articolazione della caviglia con sollevamento consecutivo del tallone della zampa. Pertanto, l'area di stampa della rispettiva zampa (Figura 6B), è fortemente ridotta dopo l'intervento chirurgico. L'area di stampa della zampa posteriore sinistra è aumentata a causa di uno spostamento compensativo del peso a sinistra. Questo dovrebbe essere tenuto a mente, poiché questo fenomeno influenza direttamente il rapporto calcolato tra la zampa "sperimentale" e "di controllo". A partire dalla reinnervazione WPO4 del quadricipite da parte del nervo femorale rigenerante porta all'inversione di questi cambiamenti con conseguente aumento dell'area di stampa delle zampe della zampa posteriore destra (Figura 7A). Poiché anche il muscolo quadricipite della coscia gioca un ruolo nella fase di oscillazione della rispettiva zampa, Swing Time (Figura 7B) è notevolmente prolungato nei ratti con lesione del nervo femorale. Rispecchiando il ritorno dell'area di stampa, Swing Time diminuisce man mano che il nervo femorale rigenerante raggiunge il muscolo quadricipite della coscia. Al WPO10, entrambi i parametri dell'andatura sono tornati alla linea di base, segnalando il pieno recupero funzionale.

Figura 6: Impronte rappresentative delle zampe. Impronte rappresentative della zampa prima della (A) e seguenti (B–E) resezione del nervo femorale destro e riparazione dell'autograft. L'area di stampa di RH è diminuita fortemente a WPO2 (B), mentre è diventato visibile un aumento dell'area di stampa della zampa posteriore sinistra (LH) a causa dell'aumento del carico di peso. L'area di stampa RH ha iniziato ad aumentare a partire dal WPO6 (C) accompagnato da una diminuzione dell'area di stampa di LH. A WPO8 (D) e WPO10 (E) L'area di stampa di RH è tornata vicino ai livelli preoperatori. (Adattato con il permesso di Heinzel et al.22, concesso in licenza sotto CC BY 4.0.) Clicca qui per visualizzare una versione più grande di questa figura.
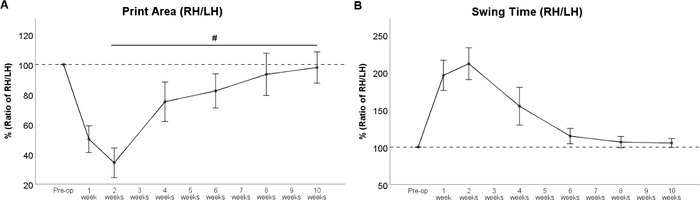
Figura 7: Il corso del recupero funzionale dopo la resezione di 7 mm e la riparazione dell'autoinnesto del nervo femorale. Il corso di Print Area Ratio (A) e Swing Time Ratio (B) ha rivelato un forte cambiamento immediatamente dopo la resezione del nervo femorale, ma i valori sono tornati ai valori preoperatori al WPO8. #: p < 0,05. Le barre di errore indicano ± SEM. (Adattato con il permesso di Heinzel et al.22, concesso in licenza sotto CC BY 4.0.) Clicca qui per visualizzare una versione più grande di questa figura.
Contusione del midollo spinale
L'analisi dell'andatura ha rivelato impronte di zampe marcatamente alterate dopo una lesione da contusione del midollo spinale toracico (Figura 8), il più degno di nota è un decremento nell'area di stampa e una marcata rotazione interna delle zampe posteriori al WPO2 (Figura 8B). Degno di nota, la rotazione della zampa è anche implementata come caratteristica valutabile nella BBB, sottosegnala l'applicabilità dell'analisi computerizzata dell'andatura per valutare i cambiamenti di andatura che sono stati originariamente valutati con i test Open Field. Per quanto riguarda il corso dei singoli parametri dell'andatura, la contusione del midollo spinale al livello di Th11 ha comportato una diminuzione del Rapporto area di stampa (Figura 9A) e un incremento del rapporto di tempo oscillante(Figura 9B). Entrambi i parametri tendevano verso i livelli di riferimento durante l'ulteriore corso del periodo di osservazione, ma non vi sono stati cambiamenti statisticamente significativi osservabili. Anche l'indice di regolarità dei parametri correlati al coordinamento (Figura 9C) è diminuito al WPO2, ma il grado variava notevolmente tra gli animali. Ha anche orientato verso valori preoperatori fino a WPO16. La base di supporto delle zampe posteriori (Figura 9D), un parametro generale dell'andatura secondo Deumens, ha mostrato un marcato aumento, che è stato statisticamente significativo da WPO10 a WPO14. Si è orientato verso i livelli di base a WPO16 e non è stato più modificato in modo significativo dal valore Pre-OP in questo momento.

Figura 8: Impronte rappresentative delle zampe posteriori. Paw stampa preoperatoriamente (A) e a seguito di una lesione alla contusione del midollo spinale toracico (B-F). Si noti la riduzione dell'area di stampa a partire dal WPO2 (B) accompagnata da una notevole rotazione interna delle zampe. Nel corso del periodo di osservazione (C-F) è osservabile un incremento dell'area di stampa e il gioco della rotazione interna. Clicca qui per visualizzare una versione più grande di questa figura.
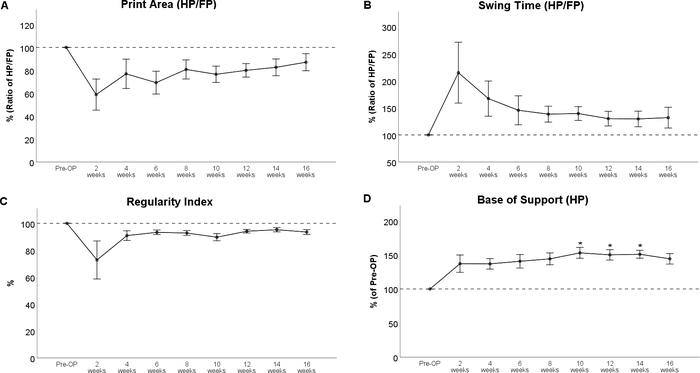
Figura 9: Contusione del midollo spinale al livello th 11. La contusione del midollo spinale all'11° th ha provocato alterazioni osservabili del Print Area Ratio (A) e swing time (B) e dell'indice di regolarità (C), ma questi cambiamenti non sono stati statisticamente significativi. A seguito di lesioni, la base di supporto delle zampe posteriori ha mostrato un marcato aumento rispetto al basale, ciò che era statisticamente significativo al WPO10 fino al WPO14. *: p < 0,05 rispetto al Pre-OP. Le barre di errore indicano ± SEM. Fare clic qui per visualizzare una versione più grande di questa figura.
File aggiuntivo 1: Dettagli sulla risoluzione dei problemi. Clicca qui per scaricare questo file.
Discussione
La valutazione del recupero funzionale nei modelli animali di PNI e SCI rimane impegnativa a causa della grande varietà di metodi di valutazione, ognuno con vantaggi e svantaggi individuali. Solo pochi approcci sono stati testati e convalidati in più modelli di lesioni nervose periferiche e centrali, anche se nuove promettenti tecniche che combinano il tracciamento del movimento e l'apprendimento automatico potrebbero potenzialmente spingere la ricerca neurocomportamentale al livello successivo di test funzionali. Siamo convinti che presto emergeranno metodi all'avanguardia ampiamente applicabili a un'ampia varietà di modelli di animali e lesioni. Alla luce di queste considerazioni, uno dei vantaggi dell'AGA è la possibilità di valutare il recupero funzionale in più modelli di lesione nervosa utilizzando un solo dispositivo. Fin dai primi anni 2000 questo approccio è stato utilizzato in modelli sperimentali di PNI come lo sciatico37,il peroneal38e la lesione nervosa femorale modello22, nonché dopo l'avulsione della radice sia del lombare39 che del plesso brachiale40. Con il metodo41 , 42sono state studiate anche varie lesioni nervose centrali, tra cui lesioni da contusione almidollo spinale. Con questo articolo, abbiamo presentato un protocollo dettagliato su come indurre tre lesioni nervose comunemente studiate e su come valutare il recupero funzionale in seguito. A nostro avviso, una linea guida pratica per i ricercatori interessati all'area della lesione nervosa sperimentale, della riparazione e della rigenerazione su come utilizzare al meglio le caratteristiche vantaggiose del metodo sarebbe di grande aiuto.
Diversi autori hanno affrontato il potenziale dell'AGA per valutare il recupero funzionale nei roditori, evidenziando il vantaggio del metodo di valutare contemporaneamente i parametri dell'andatura relativi alla reinnervazione motoria esensoriale 27,28. Inoltre, il confronto dei dati di una zampa sperimentale, ad esempio, la lesione nervosa ricostruita a una zampa non funzionante, come mostrato in entrambi i modelli presentati, consente l'inclusione di un controllo positivo intra-animale. Inversamente, una zampa operata senza ricostruzione chirurgica o trattamento aggiuntivo potrebbe servire come controllo negativo intra-animale. È stato anche dimostrato che è possibile combinare AGA con approcci di machine learning43. Nonostante i vantaggi del metodo, ha anche diversi limiti e svantaggi, come i lunghi sforzi di formazione, che sono obbligatori per abituare l'animale alla procedura diacquisizione 28,44. Un'altra limitazione dell'AGA è la dimensione massima degli animali ammissibili alla prova a causa delle dimensioni limitate dell'apparecchio. Pertanto, l'uso di AGA è attualmente limitato agli animali delle dimensioni di roditori e furetti45. Inoltre, gli approcci di valutazione neurocomportamentale recentemente emergenti nel campo del tracciamento del movimento in grado di apprendere automaticamente possono superare l'AGA sia nellacompletezza che nelle possibili applicazioni 18,19,46. La cosa più degna di nota, ma in accordo con altri metodi di valutazione, sembra che il recupero funzionale valutato dall'AGA sia fortemente limitato , se non addirittura presente, nei modelli di neurotmesi nervosa sciatica47,48. D'altra parte, L'AGA consente una valutazione completa del corso di recupero funzionale dopo la neurotmesi nervosa femorale come mostrato dai nostri dati. Con questo lavoro, abbiamo dimostrato che Paw Print Area è un parametro di andatura rappresentativo valutabile tramite AGA, che è esemplare per il corso del recupero funzionale nei due suddetti modelli di lesione nervosa periferica presentati da noi. Mentre il recupero funzionale ad integrum era osservabile dopo la riparazione autoinnesto del nervo femorale, i parametri AGA erano ancora significativamente cambiati dalla linea di base alla fine del periodo di osservazione dopo la riparazione dell'autoinnesto del nervo sciatico. È interessante notare in questo contesto che le contratture degli arti sono un fenomeno comune nei ratti con lesione nervosa sciatica e cautela è necessaria per non confondere questi segni di squilibrio muscolare e paralisi con il recupero funzionaleprocedente 32. Questo da un lato sottolinea l'incapacità del metodo AGA di rilevare un significativo recupero funzionale a seguito di lesioni da neurotmesi in questo modello. D'altra parte, solleva la questione se sia possibile valutare il modello di lesione nervosa sciatica del ratto, che è ancora il modello sperimentale di riparazione dei nervi più comunemente usato, attraverso l'analisi dell'andatura in generale nel caso in cui la lesione nervosa sia più grave dell'assonotmesi48. I dettagli sulla risoluzione dei problemi sono disponibili nel file complementare 1.
Abbiamo anche fornito dati esemplari sull'uso del metodo per valutare la funzione locomotoria nei ratti con lesione del midollo spinale, che è possibile senza alcuna modifica richiesta della procedura di configurazione o acquisizione hardware. Lo stesso principio si applica ad altri modelli di roditori di lesione nervosa centrale (CNI)26,49,50 e lesione da avulsione della radice. A differenza dei PNI isolati, le lesioni del midollo spinale sono molto più complesse nelle loro conseguenze fisiopatiche, poiché una moltitudine di strutture altamente importanti sono danneggiate, coinvolgendo vie efferente come i tratti corticospinale e rubrospinale e vie afferenti come le colonne dorsali e i tratti spinotalamici35. La sfida di valutare adeguatamente questi cambiamenti patologici si riflette nell'armamentario completo dei test comportamentali, come il Punteggio Basso, Beattie e Bresnahan (BBB)36. Il parametro dell'andatura Base of Support è stato segnalato per aumentare a seguito di lesioni nervose centrali, molto probabilmente per tenere conto di un'andatura instabile risultante. La base di supporto è stata significativamente cambiata dalla linea di base da WPO10 a WPO14 nel nostro modello, supportando la nostra presunzione che questo parametro consenta la valutazione del corso di recupero funzionale da parte dell'AGA a seguito di una lesione della contusione del midollo spinale toracico.
Siamo convinti che l'AGA sia uno strumento fattibile per valutare il recupero funzionale nei roditori con lesioni del sistema nervoso. Tuttavia, si consiglia di riflettere attentamente e accuratamente i cambiamenti osservati dell'andatura in ogni rispettiva configurazione sperimentale. Le alterazioni dei parametri dell'andatura, ad esempio un aumento dell'area di stampa a seguito di un decremento postoperatorio immediato o una diminuzione del tempo di oscillazione procedendo ad un'immediata elevazione postoperatoria di questo parametro, nel corso del periodo di osservazione non si riferiscono inevitabilmente al recupero funzionale. Invece questi cambiamenti possono anche essere correlati a un possibile adattamento funzionale per mantenere un'andatura poco appariscente, dato che i ratti sono una specie di preda e cercare di evitare di mostrare dolore o disabilità ai potenziali predatori51. Si raccomanda pertanto di utilizzare l'analisi automatizzata dell'andatura come strumento complementare per correlare i cambiamenti di andatura ad altre misure di risultato della lesione nervosa periferica e dellarigenerazione 21. Come accennato in precedenza, crediamo anche che dovrebbe essere attentamente riflesso se i roditori con neurotmesi nervosa sciatica dovrebbero essere studiati per mezzo dell'AGA poiché la nostra scoperta indica fortemente che il recupero funzionale è fortemente limitato in questo caso.
Come dimostrato nel nostro lavoro, l'asset principale di AGA è la possibilità di studiare la reinnervazione sia motoria che sensoriale in una moltitudine di modelli PNI sperimentali e CNI, richiedendo al contempo una sola configurazione. Pertanto, il metodo è, a nostro avviso, uno strumento altamente prezioso per test neurocomportamentali completi. Uno degli asset di AGA, che è la possibilità di studiare la reinnervazione motoria e sensoriale in vari modelli animali di PNI e CNI pur richiedendo una sola configurazione, è a nostro avviso il principale vantaggio del metodo rispetto ad altri metodi di valutazione per studiare il recupero funzionale, come l'analisi dei sentieri52,il test von Frey53o la cinematica dell'andatura16. La possibilità di valutare contemporaneamente i cambiamenti dell'andatura che sono correlati con i risultati di indagini elettrofisiologiche sul muscolo reinnervato22 o con metodi di valutazione per lafunzione sensoriale 54 è promettente per quanto riguarda le future applicazioni del metodo. Si consiglia pertanto di utilizzare l'AGA per studiare il recupero funzionale nei modelli di roditori del PNI dell'avaro, come il nervo ulnare, radiale o mediano, o i modelli sperimentalidi trasferimento nervoso 55, che rimangono ancora non studiato con questo metodo.
Con la presente forniamo un protocollo dettagliato su come utilizzare l'analisi automatizzata dell'andatura per studiare il recupero funzionale in tre modelli di roditori di lesione nervosa. Mentre il metodo richiede un'attenta considerazione di vari aspetti chiave come un allenamento adeguato e una meticolosa calibrazione dura e software, è uno strumento complementare fattibile e prezioso per valutare la rigenerazione nervosa nei modelli di roditori di lesione nervosa centrale e periferica.
Divulgazioni
Gli autori dichiarano che questo lavoro è stato supportato da Noldus Inc. Nessuno degli autori ha ricevuto alcun salario personale o alcun tipo di gratuità finanziaria. Gli autori non hanno altri interessi concorrenti da dichiarare.
Riconoscimenti
Gli autori ringraziano Karin Brenner per la sua appassionata cura degli animali. Gli autori ringraziano anche Claudia Keibl, James Ferguson, Gabriele Leinfellner e Susanne Drechsler per la loro assistenza durante gli interventi chirurgici sperimentali.
Materiali
| Name | Company | Catalog Number | Comments |
| 0.9% Saline | B. Braun Austria | 3570410 | Vehicle for drug delivery |
| 1 ml syringe | B. Braun Austria | 9161708V | Injecting device |
| 10 ml syringe | B. Braun Austria | 4606728 V | Injecting device |
| 1-Propanol, 2-Propanol, Hexetidin | Gebro Pharma | N/A | Alcoholic skin disinfection |
| 23-gauge (G) canula | B. Braun Austria | 4657667 | Canula for s.c. injection |
| 26-gauge (G) canula | B. Braun Austria | 4657683 | Canula for s.c. injection |
| 5 ml syringe | B. Braun Austria | 4606710 V | Injecting device |
| Buprenorphine hydrochloride | Sigma | B9275 | Analgetic agent |
| Burrs for Micro Drill | F.S.T | 19007-29 | Drilling of a hole inside the lamina |
| Caprofen | Zoetis Austria | N/A | Analgetic agent |
| Catwalk Automated gait analysis system | Noldus | N/A | Automatic analysis software of animal gait |
| Cauterizer Kit | F.S.T | 18010-00 | Cauterization of vessels during surgery |
| Enrofloxacin | Bayer Austria | N/A | Antibiotic |
| Ethilon (10-0) | ETHICON | 2810G | Suture material for neurrorhaphy |
| Ethilon (11-0) | ETHICON | EH7465G | Suture material for neurrorhaphy |
| Eye ointment | Fresenius Kabi Austria | 4302436 | Eye protection during anesthesia |
| Friedman-Pearson Rongeurs | F.S.T | 16221-14 | Surgical instrument |
| Gabapentin | Wedgewood Pharmacy | N/A | Analgetic agent |
| Goldstein retractor | F.S.T | 17003-03 | Retraction of tissues during surgery |
| Hair trimmer | Aescular | N/A | Hair trimmer for shaving of the operation site prior to surgery |
| Heating Pad for rodents | ALA Scientific Instruments | N/A | Regulation of body temperature |
| Impactor | Precision Systems and Instrumentation | N/A | Induction of spinal cord contusion |
Lewis rat ( ) ) | Janvier | N/A | Experimental animal |
| Magnetic Fixator Retraction System | F.S.T | 18200-50 | Retraction of tissues during surgery |
| Metzenbaum Baby Scissors | F.S.T | 14019-13 | Surgical instrument |
| Micro Drill | Word Precision Instruments | 503599 | Instrument for bone drilling |
| Micro Needle holder | F.S.T | 12076-12 | Surgical instrument |
| Micro-scissors (curved) | F.S.T | 15023-10 | Surgical instrument |
| Micro-scissors (straight) | F.S.T | 15007-08 | Surgical instrument |
| Mirror Finish Forceps | F.S.T | 11251-23 | Surgical instrument |
| Needle holder | F.S.T | 12002-12 | Surgical instrument |
| Operating microscope | Leica | M651 MSD | Magnification of the operative site |
| Povidone Iod | B. Braun Melsungen | N/A | Non-alcoholic skin disinfectant |
| Pulse Oximeter | STARR Life Sciences | N/A | Surveillance of heart rate and oxygen saturation |
| Rodent thermometer | BIOSEB | BIO-TK8851 | Surveillance of body temperature |
| Scalpel blade | F.S.T | 10010-00 (#10) | Surgical instrument to make an incision |
| Scalpel handle | F.S.T | 10003-12 (#3) | Surgical instrument to make an incision |
| Sevoflurane Inhalation Vapour, Liquid (100%) | Baxter | HDG9117A | Anesthetic |
| Spatula & Probe | F.S.T | 10090-13 | Surgical instrument |
Sprague Dawley rat ( ) ) | Janvier | N/A | Experimental animal |
| Sterila gauze 5x5cm | EVAC MEDICAL | E010.03.00215 | Sterile gauze compress |
| Tissue Forceps | F.S.T | 11021-12 | Surgical instrument |
| Vicryl (4-0) | ETHICON | V3040H | Suture material for subcutaneous sutures |
| Vicryl (5-0) | ETHICON | V303H | Suture material for subcutaneous sutures |
| Vicryl cutting needle (4-0) | ETHICON | V392ZH | Suture material for skin sutures |
| Vicryl cutting needle (5-0) | ETHICON | V391H | Suture material for skin sutures |
Riferimenti
- Mohanty, C. B., Bhat, D. I., Devi, B. I. Use of animal models in peripheral nerve surgery and research. Neurology India. 9, Supplement 100-105 (2019).
- Vela, F. J., et al. Animal models used to study direct peripheral nerve repair: a systematic review. Neural Regeneration Research. 15 (3), 491-502 (2020).
- Verma, R., Virdi, J. K., Singh, N., Jaggi, A. S. Animals models of spinal cord contusion injury. The Korean Journal of Pain. 32 (1), 12-21 (2019).
- de Medinaceli, L., Freed, W. J., Wyatt, R. J. An index of the functional condition of rat sciatic nerve based on measurements made from walking tracks. Experimental Neurology. 77 (3), 634-643 (1982).
- Navarro, X. Functional evaluation of peripheral nerve regeneration and target reinnervation in animal models: a critical overview. The European Journal of Neuroscience. 43 (3), 271-286 (2016).
- Sperry, R. W. The functional results of muscle transposition in the hind limb of the rat. The Journal of Comparative Neurology. 73 (3), 379-404 (1940).
- Sperry, R. W. The effect of crossing nerves to antagonistic muscles in the hind limb of the rat. The Journal of Comparative Neurology. 75 (1), 1-19 (1941).
- Sperry, R. W. Transplantation of motor nerves and muscles in the forelimb of the rat. The Journal of Comparative Neurology. 76 (2), 283-321 (1942).
- Zimmerman, E. A., Chambers, W. W., Liu, C. N. An experimental study of the anatomical organization of the Cortico-Bulbar System in the Albino Rat. The Journal of Comparative Neurology. 123, 301-323 (1964).
- Cohen, A. H., Gans, C. Muscle activity in rat locomotion: movement analysis and electromyography of the flexors and extensors of the elbow. Journal of Morphology. 146 (2), 177-196 (1975).
- Barnett, S. A. The Rat: A Study in Behaviour. , Aldine Publishing Company. (1963).
- Hare, G. M., et al. Walking track analysis: utilization of individual footprint parameters. Annals of Plastic Surgery. 30 (2), 147-153 (1993).
- Hare, G. M., et al. Walking track analysis: a long-term assessment of peripheral nerve recovery. Plastic and Reconstructive Surgery. 89 (2), 251-258 (1992).
- Bertelli, J. A., Mira, J. C. Behavioral evaluating methods in the objective clinical assessment of motor function after experimental brachial plexus reconstruction in the rat. Journa of Neuroscience Methods. 46 (3), 203-208 (1993).
- Varejao, A. S., Melo-Pinto, P., Meek, M. F., Filipe, V. M., Bulas-Cruz, J. Methods for the experimental functional assessment of rat sciatic nerve regeneration. Neurological Research. 26 (2), 186-194 (2004).
- Varejao, A. S., et al. Functional assessment of peripheral nerve recovery in the rat: gait kinematics. Microsurgery. 21 (8), 383-388 (2001).
- Varejao, A. S., et al. Ankle kinematics to evaluate functional recovery in crushed rat sciatic nerve. Muscle and Nerve. 27 (6), 706-714 (2003).
- Nath, T., et al. Using DeepLabCut for 3D markerless pose estimation across species and behaviors. Nature Protocols. 14 (7), 2152-2176 (2019).
- Mathis, A., et al. DeepLabCut: markerless pose estimation of user-defined body parts with deep learning. Nature Neuroscience. 21 (9), 1281-1289 (2018).
- Deumens, R., Jaken, R. J., Marcus, M. A., Joosten, E. A. The CatWalk gait analysis in assessment of both dynamic and static gait changes after adult rat sciatic nerve resection. Journal of Neuroscience Methods. 164 (1), 120-130 (2007).
- Heinzel, J., et al. Use of the CatWalk gait analysis system to assess functional recovery in rodent models of peripheral nerve injury - a systematic review. Journal of Neuroscience Methods. 345, 108889(2020).
- Heinzel, J. C., Hercher, D., Redl, H. The course of recovery of locomotor function over a 10-week observation period in a rat model of femoral nerve resection and autograft repair. Brain and Behavior. , 01580(2020).
- Chen, S. H., et al. Changes in GABA and GABA(B) receptor expressions are involved in neuropathy in the rat cuneate nucleus following median nerve transection. Synapse. 66 (6), 561-572 (2012).
- Chen, S. H., et al. Decreases of glycine receptor expression induced by median nerve injury in the rat cuneate nucleus contribute to NPY release and c-Fos expression. Life Sciences. 90 (7-8), 278-288 (2012).
- Hetze, S., Romer, C., Teufelhart, C., Meisel, A., Engel, O. Gait analysis as a method for assessing neurological outcome in a mouse model of stroke. Journal of Neuroscience Methods. 206 (1), 7-14 (2012).
- Sandner, B., et al. Systemic epothilone D improves hindlimb function after spinal cord contusion injury in rats. Experimental Neurology. 306, 250-259 (2018).
- Kappos, E. A., et al. Validity and reliability of the CatWalk system as a static and dynamic gait analysis tool for the assessment of functional nerve recovery in small animal models. Brain and Behavior. 7 (7), 00723(2017).
- Deumens, R., Marinangeli, C., Bozkurt, A., Brook, G. A. Assessing motor outcome and functional recovery following nerve injury. Methods in Molecular Biology. 1162, 179-188 (2014).
- Webster, G. V. Halstedian principles in the practice of plastic and reconstructive surgery. Stanford Medical Bulletin. 13 (3), 315-316 (1955).
- Bozkurt, A., et al. A flexible, sterile, and cost-effective retractor system for microsurgery. Microsurgery. 31 (8), 668-670 (2011).
- Carr, M. M., Best, T. J., Mackinnon, S. E., Evans, P. J. Strain differences in autotomy in rats undergoing sciatic nerve transection or repair. Annals of Plastic Surgery. 28 (6), 538-544 (1992).
- Dellon, A. L., Mackinnon, S. E. Sciatic nerve regeneration in the rat. Validity of walking track assessment in the presence of chronic contractures. Microsurgery. 10 (3), 220-225 (1989).
- Jackson, C. M. Anatomy of the rat. Transactions of the American Philosophical Society, Philadelphia, New Series, Volume XXVII, 1935. The Anatomical Record. 65 (1), By Eunice Chace Greene. With Foreword by Henry H Donaldson 127-129 (1936).
- Pena, M. C., Baron, J. Femoral nerve and rectus femoris muscle of the rat: a study in anatomy, histology, and histoenzymes. Annals of Plastic Surgery. 20 (6), 527-532 (1988).
- Kjell, J., Olson, L. Rat models of spinal cord injury: from pathology to potential therapies. Disease Models and Mechanisms. 9 (10), 1125-1137 (2016).
- Basso, D. M., Beattie, M. S., Bresnahan, J. C. A sensitive and reliable locomotor rating scale for open field testing in rats. Journal of Neurotrauma. 12 (1), 1-21 (1995).
- Bozkurt, A., et al. CatWalk gait analysis in assessment of functional recovery after sciatic nerve injury. Journal of Neuroscience Methods. 173 (1), 91-98 (2008).
- Godinho, M. J., et al. Immunohistochemical, ultrastructural and functional analysis of axonal regeneration through peripheral nerve grafts containing Schwann cells expressing BDNF, CNTF or NT3. PLoS One. 8 (8), 69987(2013).
- Pajenda, G., et al. Spatiotemporally limited BDNF and GDNF overexpression rescues motoneurons destined to die and induces elongative axon growth. Experimental Neurology. 261, 367-376 (2014).
- Matsuura, Y., et al. The effect of anti-NGF receptor (p75 Neurotrophin Receptor) antibodies on nociceptive behavior and activation of spinal microglia in the rat brachial plexus avulsion model. Spine (Phila Pa 1976). 38 (6), 332-338 (2013).
- Hamers, F. P., Lankhorst, A. J., van Laar, T. J., Veldhuis, W. B., Gispen, W. H. Automated quantitative gait analysis during overground locomotion in the rat: its application to spinal cord contusion and transection injuries. Journal of Neurotrauma. 18 (2), 187-201 (2001).
- Koopmans, G. C., et al. The assessment of locomotor function in spinal cord injured rats: the importance of objective analysis of coordination. Journal of Neurotrauma. 22 (2), 214-225 (2005).
- Frohlich, H., Claes, K., De Wolf, C., Van Damme, X., Michel, A. A machine learning approach to automated gait analysis for the Noldus Catwalk system. IEEE Transaction on Bio-medical Engineering. 65 (5), 1133-1139 (2018).
- Batka, R. J., et al. The need for speed in rodent locomotion analyses. Anatomical Record (Hoboken, N. J). 297 (10), 1839-1864 (2014).
- Wood, T., et al. A ferret model of encephalopathy of prematurity. Developmental Neuroscience. 40 (5-6), 475-489 (2018).
- Abbas, W., Masip Rodo, D. Computer methods for automatic locomotion and gesture tracking in mice and small animals for neuroscience applications: a survey. Sensors. 19 (15), Basel, Switzerland. (2019).
- Irintchev, A. Potentials and limitations of peripheral nerve injury models in rodents with particular reference to the femoral nerve. Annals of Anatomy. 193 (4), 276-285 (2011).
- Haastert-Talini, K. Modern Concepts of Peripheral Nerve Repair. Haastert-Talini, K., Assmus, H., Antoniadis, G. , Springer International Publishing. 127-138 (2017).
- Lu, L., et al. Growth differentiation factor 11 promotes neurovascular recovery after stroke in mice. Frontiers in Cellular Neuroscience. 12, (2018).
- Caballero-Garrido, E., Pena-Philippides, J. C., Galochkina, Z., Erhardt, E., Roitbak, T. Characterization of long-term gait deficits in mouse dMCAO, using the CatWalk system. Behavioral Brain Research. 331, 282-296 (2017).
- Graham, D. M., Hampshire, V. Methods for measuring pain in laboratory animals. Lab Animal. 45 (3), 99-101 (2016).
- Monte-Raso, V. V., Barbieri, C. H., Mazzer, N., Yamasita, A. C., Barbieri, G. Is the sciatic functional index always reliable and reproducible. Journal of Neuroscience Methods. 170 (2), 255-261 (2008).
- Stossel, M., et al. Comparative evaluation of chitosan nerve guides with regular or increased bendability for acute and delayed peripheral nerve repair: a comprehensive comparison with autologous nerve grafts and muscle-in-vein grafts. Anatomical Record (Hoboken). 301 (10), 1697-1713 (2018).
- Vrinten, D. H., Hamers, F. F. CatWalk' automated quantitative gait analysis as a novel method to assess mechanical allodynia in the rat; a comparison with von Frey testing. Pain. 102 (1-2), 203-209 (2003).
- Aman, M., Sporer, M., Bergmeister, K., Aszmann, O. Animal models for selective nerve transfers of the upper extremity. Handchirurgie Mikrochirurgie Plastische Chirurgie. 51 (4), 319-326 (2019).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon